PEMBUATAN DAN KARAKTERISASI
ELEKTRODA KERJA PLATINA TERMODIFIKASI FILM
POLIPIROL-ASAM GLUTAMAT (PPy-Asg)
Anceu Murniati A Buchari B Kelompok Keahlian Kimia Analitik
AJurusan Kimia Fakultas MIPA-UNJANI Jl.Terusan Sudirman PO.BOX 148 Cimahi
BProgram Studi Kimia FMIPA-ITB. Jl.Ganesha No.10 Bandung
Email : an_murniati@yahoo.co.id
Abstrak
Telah dilakukan penelitian pembuatan dan karakterisasi elektroda platina termodifikasi film polipirol-asam glutamat (PPy-Asg) dengan metode elektropolimerisasi secara voltammetri siklik (CV). Diperoleh optimasi kondisi elektropolimerisasi film PPy-Asg yaitu 0,05 M ; 0,01 M dan KClO4 0,1 M sebagai elektrolit
pendukung. Pelapisan film PPy-Asg digambarkan voltammogram sebanyak 10 siklus pada potensial 0-1000 mV dan laju selusur 100 mV/detik. Hasil rekaman FTIR film PPy-Asg memberikan pola spektrum khas dari pirol ditandai gugus fungsi N-H amina (3407 cm-1); C-H lingkar aromatik (3103 cm-1) ; C=C alkena (1680 cm-1), pada spektrum polipirol terdapat puncak yang lebih tajam dan terjadinya pergeseran bilangan gelombang menandai suatu polimerisasi dengan vibrasi melemah (pergeseran puncak N-H amina dari 3407 cm-1 menjadi 3398 cm-1 sedangkan pola spektrum PPy-Asg ditandai gugus fungsi O-H karboksilat (3123 cm-1) memungkinkan interaksi dari asam glutamat yang teramobilkan dalam jaringan polipirol. Hasil uji elektroda memberikan perilaku nerstian sebesar 59,82 mV/dekade pada konsentrasi larutan standar asam glutamat (Asg) 10-1-10-4 M dengan koefisien korelasi sebesar 0,99. Usia pemakaian elektroda terlapis film PPy-Asg adalah 14 hari ditandai dengan perubahan respon potensial (drift) sebesar 11,641 mV/hari. Nilai koefisien selektivitas menyatakan keberadaan glutamin dalam larutan uji cukup mengganggu terhadap asam glutamat (Kij > 1) sedangkan glisin dan leusin tidak mengganggu (Kij 1), sehingga elektroda termodifikasi film PPy-Asg cukup selektif terhadap asam glutamat (Asg).
Kata kunci: elekroda, film PPy-Asg.
elektropolimerisasi, voltammogram, potensial
Abstract
Condition of fabrication and characterization of platinum wire coated by polypyrrolle-glutamic acid film (PPy_Asg) electrode by electropolymerization methods in cyclic voltammetry (CV) has been studied. The optimum electropolymerization of PPy-Asg was between 0.05 M/0.01 M and 0.1 M of KClO4 as
supporting electrolyte. The potential scan was between 0 to 1000 mV and scan rate was carried out at 100 mV/s for 10 cycles. FTIR spectrum from pyrrolle by functional group of N-H amine ( 3407 cm-1); C-H aromatic ( 3103 cm-1) ; C=C alkene ( 1680 cm-1), spectrum of polypyrrolle there is sharper top and the happening of friction of polymerize is marked with weaken vibration ( friction of top N-H amine out of 3407 cm-1 becomes 3398 cm-1, the spectrum of PPg-Asg is marked by functional group O-H ( 3123 cm-1) what enables existence imobilized glutamic acid in polypirrolle network. The working electrode showed prepared nerntian behaviour which was 59.82 mV/decade at 10-2 to 10-4 M , with R2= 0.99 . The usage of PPy-Asg electrode was 14 days with change of potential response ( drift) 11,641 mV/days. Selectivity coefficient value express existence of glutamin in condensation of test enough bothering to glutamic acid ( Kij > 1) while glisin and leusin were not interference ( Kij < 1), so the film PPy-Asg electrode was enough selective to glutamic acid ( Asg).
Keywords : electrode, PPy-Asg film,
electropolymerization, voltammogram,
PENDAHULUAN
Saat ini, polipirol (PPy) merupakan salah satu polimer konduktif yang paling menjanjikan, dan telah diterima secara
komprehensif, karena memiliki
karakteristik yang sempurna, termasuk preparasi yang mudah, stabil, konduktivitas tinggi. PPy dapat memiliki penerapan yang luas dalam berbagai bidang, seperti sensor dan piranti-piranti elektrik. Contoh penerapan PPy untuk keperluan biosensor adalah penelitian Elkinci et al. (2007) dan Kiralp et a.l (2003). Film PPy diperoleh dengan cara elektropolimerisasi secara voltammetri siklik (CV) yaitu dengan mendepositkan monomernya dalam larutan elektrolit pada permukaan elektroda pada potensial anodik (oksidasi). Elektron pada konduksi polimer mampu merubah keadaan konduktif selama proses reduksi ataupun oksidasi. Dengan terbentuknya muatan positif pada polipirol maka anion tertentu dapat disisipkan dengan memanfaatkan
antaraksi perbedaan muatan untuk
mendapatkan polipirol termodifikasi
(Wang, 2000). NH NH NH NH N H n polipirol pirol elektroda e- e-+
Gambar 1. Pertumbuhan film PPy (Cheung
etal., 1990)
Menurut Wang, PPy yang bermuatan positif dapat bergabung secara reversibel dengan spesi anionik pada suatu larutan melalui proses oksidasi dan reduksi :
e A P A P _
dengan P adalah PPy dan A- sebagai dopan anion untuk menetralkan muatan. Adanya antaraksi perbedaan muatan dari PPy
melalui penyisipan anion dapat
menghasilkan PPy yang termodifikasi.
Proses reaksi redoks dari PPy selama CV terdiri dari tiga tahap. Pertama, selama
proses pertumbuhan polimer dengan
potensial dari -0,5 sampai +0,5 V dalam keadaan polimer netral. Kedua, setelah tercapai potensial oksidasi dari PPy, anion berdifusi memasuki polimer yang sedang tumbuh untuk menetralkan muatan polimer. Ketiga, ketika scan siklus kembali terjadi proses reduksi, anion lepas (Cheung et al, 1990). Dalam keadaan oksidasi, sistem
konjugasi elektron memperlihatkan
pelepasan elektron mendorong ke arah polimer konduktif. Muatan positif itu diimbangi oleh counter ion X-. Dalam keadaan reduksi, elektron bertambah, dan menghilangnya muatan positip dari rantai polimer. Secara serempak, counter ion itu
dipindahkan dari polimer untuk
menetralkan muatan. Jika mobilitas X -rendah, kation harus menyerap muatan negatip dari lingkungan sekitarnya. Dengan cara ini polimer dapat dengan mudah disetel sebagai anion dan penukar kation.
Pada polimerisasi secara elektrokimia, monomer dilarutkan dalam pelarut yang sesuai yang berisi larutan garam sebagai elektrolit pendukung. Monomer tersebut dioksidasi pada permukaan elektroda pada potensial anodik (oksidasi). Pada oksidasi awal, monomer membentuk radikal kation lalu bereaksi dengan monomer lain dalam
larutan membentuk oligomer dan
pertumbuhan rantai selanjutnya terbentuk
polimer. Perpanjangan polimer
terkonyugasi yang dihasilkan
mengakibatkan terjadinya penurunan
potensial oksidasi dibandingkan dengan oksidasi monomer.
elektroda polimer larutan
PPyo X
-elektroda polimer larutan
PPyo X
-elektroda polimer larutan
PPyo X
-elektroda polimer larutan
PPyo X -e -e -tahap-1 tahap-2 tahap-3 tahap-1
Gambar 2 Transfer anion selama proses redoks pada pertumbuhan polimer PPy
2
Elektroda termodifikasi polimer telah
dipertunjukkan sebagai sensor
potentiometrik untuk menentukan berbagai ion ataupun molekul serta aplikasi biologi (Alumaa et al., 2000; Cheung et al., 1990) telah meneliti bahwa asam glutamat dan dopamin dapat dijerap dan dilepaskan dari membran film polipirol dengan potensial yang terkontrol.
Asam glutamat dengan rumus molekul C5H9NO4 adalah suatu asam amino yang merupakan salah satu komponen penting protein yang dibutuhkan tubuh kita. Gugus R pada asam glutamat bermuatan negatif dan mempunyai tambahan gugus karboksil. Sifat gugus R pada asam glutamat menentukan polaritasnya. Asam glutamat dapat diproduksi dari senyawa lain , yaitu hidrolisis dari glutamin dengan enzim GLS dan GLS-2 (Lehninger, 1995 )
glutamin + H2O → asam glutamat + NH3 Asam glutamat yang merupakan suatu asam amino, apabila larut dalam air akan membentuk zwitter ion (ion amfoter dan memiliki titik isoelektrik sebesar 3,22.
Telah dilakukan penelitian tentang
pelapisan Ppy pada elektroda (Purwanto, 2004); amobilisasi suatu asam amino pada fim PPy (Suratman, 2003); Ernayati (2005). Optimasi kondisi elektropolimerisasi diperoleh dari variasi dua elektroda Pt pada kondisi komposisi berbeda dari larutan pirol dan KClO4 sebagai elektrolit pendukung. Uji kinerja elektroda tersebut dengan parameter faktor nerst dan batas deteksi. Dengan merujuk pada kajian penelitian sebelumnya tentang kondisi optimasi elektropolimerisasi film PPy-Asg penelitian sebelumnya, maka pada penelitian ini telah dibuat elektroda kerja kawat platina yang dimodifikasi dengan film polipirol-asam glutamat (Ppy-Asg). Karakterisasi elektroda termodifikasi Ppy-Asg yaitu perilaku nerstian, usia pemakaian elektroda dan koefisian selektivitas. Dengan demikian elektroda termodifiksai film Ppy-Asg diharapkan dapat menghasilkan suatu
elektroda kerja yang memenuhi
karakteristik elektroda membran selektif ion (ESI) sebagai sensor potensiometrik asam glutamat. Hasil rekaman FTIR memberikan informasi bahwa kehadiran ionofor asam glutamat damobilisasi dalam jaringan film polipirol.
METODOLOGI 1. Bahan Kimia
Bahan-bahan kimia yang digunakan
berkualitas pro analisis sebagian besar
produk Merck. Sebagai monomer
digunakan pirol 98 % (Sigma-Aldrich)
digunakan sebagai bahan pembuatan
polipirol, asam glutamat merupakan
ionofor. Sebagai elektrolit pendukung
digunakan KClO4. Digunakan juga larutan glutamin, glisin, leusin yang dipelajari pengaruhnya sebagai ion pengganggu. Semua senyawa tersebut dilarutkan dengan pelarut akuabides.
2. Peralatan
a. Peralatan pembuatan elektroda kerja
Digunakan kawat platina dengan diameter 0,4 mm dan panjangnya sekitar 2 cm. Untuk melengkapi panjang dari elektroda kerja tersebut digunakan batang tembaga dengan diameter 0,6 mm dengan panjang 7 cm. Sedangkan penggunaan soder dan timah untuk mematri antara tembaga dengan platina.
b. Peralatan pengukuran
Peralatan gelas yang biasa digunakan di laboratorium kimia. Untuk mempercepat pelarutan reagen dan sampel digunakan pengaduk magnetik dan batang magnetik, sedangkan untuk pengukuran pH digunakan pH-meter. Peralatan elektropolimerisasi PPy-Asg yaitu seperangkat sel elektrolisis terdiri dari elektroda kerja Pt, elektroda pembanding Ag/AgCl dan elektroda bantu dari kawat Pt (Gambar.3).
3
Gambar 3. Satu set mini sel elektrolisis Satu sel elektrolisis tersebut dihubungkan dengan potensiostat yang dilengkapi dengan satu set komputer dengan program
Basi-Epsilon dan pengolah data voltamogram
siklik dilakukan dengan program Origin7.
Digunakan FTIR untuk karakterisasi
lapisan film pirol, PPy dan Ppy-Asg.
c. Konstruksi elektroda kerja
Kawat Pt dengan diameter 0,4 mm dan panjangnya 2 cm dipatri dengan kawat tembaga yang panjangnya 5 cm. Elektroda tersebut dimasukkan ke dalam badan elektroda gelas sedemikian rupa sehingga kawat platina keluar dari badan elektroda dengan panjang sekitar 1 cm.
Gambar 4 Konstruksi elektroda kerja Pt
3. Pembuatan larutan
Dibuat larutan untuk keperluan
elektropolimerisasi pirol yaitu pirol 0,05 M, asam glutamat 0,01M dan kalium perklorat 0,1 M. Untuk keperluan pengukuran koefisien selektivitas dibuat beberapa larutan berikut: asam glutamat 0,25 M, glutamin 0,25 M larutan glisin 0,25 M; dan larutan leusin 0,25 M.
4. Pelapisan film PPy-Asg pada elektroda kerja Pt
Pelapisan elektroda kerja Pt dilakukan dalam sel elektrolisis yang terdiri dari elektroda kerja platina, elektroda pembantu dan elektroda pembanding Ag/AgCl. Sel elektrokimia tersebut dihubungkan dengan
potensiostat. Pemindaian potensial
dilakukan secara voltametri siklik
(Gambar.5).
Gambar 5. Sel elektropolimerisasi pirol secara voltametri siklik
5. Optimasi elektropolimerisasi pirol
(Murniati et al, 2007)
Optimasi elektropolimerisasi PPy-Asg meliputi pemilihan daerah potensial kerja, jumlah siklus, laju selusur dan komposisi larutan elektropolimerisasi. Optimasi
pengukuran diperoleh pada jendela
potensial 0-1000 mV dan laju selusur 100 mV/s sebanyak 10 siklus. Sedangkan untuk komposisi larutan elektropolimerisasi pirol terdiri dari Py-Asg 0,05 M dan 0,1 M dengan larutan KClO4 0,1 M.
6.Karakterisasi film dengan FTIR
Sejumlah pirol, polipirol dan PPy-Asg dilakukan uji FTIR untuk memperoleh informasi gugus fungsi dari masing-masing struktur tersebut.
7.Karakterisasi elektroda kerja terlapis polipirol-asam glutamat
Karakterisasi dilakukan secara
potensiometrik yaitu pengukuran potensial
yang meliputi penentuan trayek
pengukuran, faktor nernst, waktu respon, umur elektroda, dan selektivitas.
HASIL DAN PEMBAHASAN 1.Hasil pelapisan film PPy-Asg
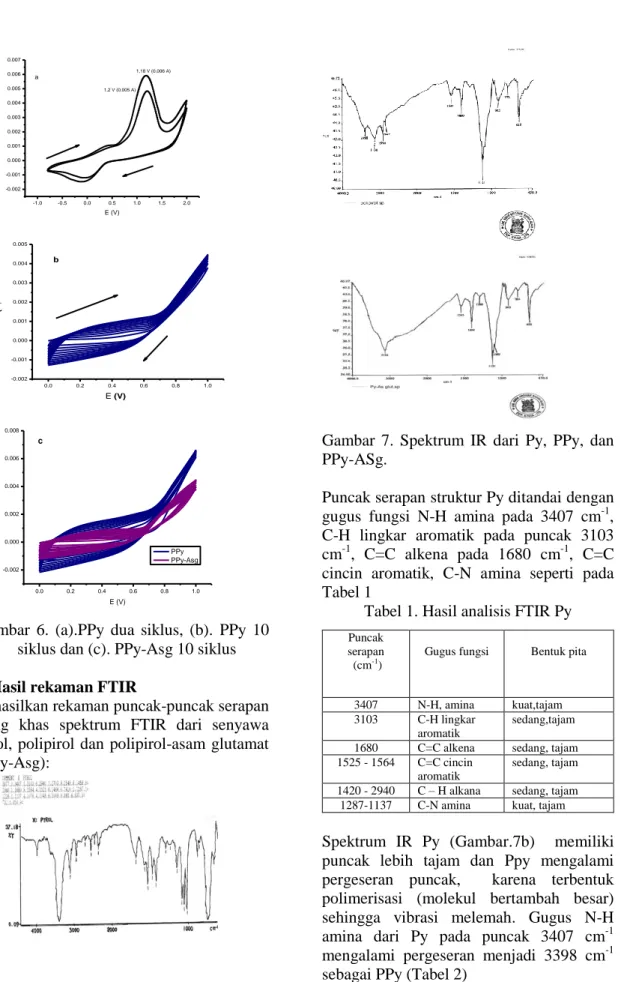
Optimasi kondisi eletropolimerisasi Ppy-Asg Optimasi pengukuran diperoleh pada jendela potensial 0-1000 Mv dan laju selusur 100 mV/s sebanyak 10 siklus.
Sedangkan untuk komposisi larutan
elektropolimerisasi pirol terdiri dari Py-Asg 0,05 M dan 0,1 M dengan larutan KClO4 0,1 M seperti pada Gambar . 6 berikut :
4
-1.0 -0.5 0.0 0.5 1.0 1.5 2.0 -0.002 -0.001 0.000 0.001 0.002 0.003 0.004 0.005 0.006 0.007 i (A) E (V) 1,2 V (0,005 A) 1,18 V (0,006 A) a 0.0 0.2 0.4 0.6 0.8 1.0 -0.002 -0.001 0.000 0.001 0.002 0.003 0.004 0.005 i (A ) E (V) b 0.0 0.2 0.4 0.6 0.8 1.0 -0.002 0.000 0.002 0.004 0.006 0.008 i (A) E (V) PPy PPy-Asg cGambar 6. (a).PPy dua siklus, (b). PPy 10 siklus dan (c). PPy-Asg 10 siklus
2.Hasil rekaman FTIR
Dihasilkan rekaman puncak-puncak serapan yang khas spektrum FTIR dari senyawa pirol, polipirol dan polipirol-asam glutamat (Ppy-Asg):
Gambar 7. Spektrum IR dari Py, PPy, dan PPy-ASg.
Puncak serapan struktur Py ditandai dengan gugus fungsi N-H amina pada 3407 cm-1, C-H lingkar aromatik pada puncak 3103 cm-1, C=C alkena pada 1680 cm-1, C=C cincin aromatik, C-N amina seperti pada Tabel 1
Tabel 1. Hasil analisis FTIR Py
Puncak serapan
(cm-1)
Gugus fungsi Bentuk pita
3407 N-H, amina kuat,tajam
3103 C-H lingkar
aromatik
sedang,tajam
1680 C=C alkena sedang, tajam
1525 - 1564 C=C cincin
aromatik
sedang, tajam
1420 - 2940 C – H alkana sedang, tajam
1287-1137 C-N amina kuat, tajam
Spektrum IR Py (Gambar.7b) memiliki puncak lebih tajam dan Ppy mengalami pergeseran puncak, karena terbentuk polimerisasi (molekul bertambah besar) sehingga vibrasi melemah. Gugus N-H amina dari Py pada puncak 3407 cm-1 mengalami pergeseran menjadi 3398 cm-1 sebagai PPy (Tabel 2)
5
Tabel 2. Hasil analisis FTIR polipirol
Puncak serapan
(cm-1)
Gugus fungsi Bentuk pita
3398 N-H, amina kuat, melebar
3134 C-H lingkar
aromatik
sedang,tajam
2920 C-H alkana sedang, tajam
1541 C=C cincin
aromatik
sedang, tajam
1400 C-N amina sedang, tajam
905 C=C alkena sedang, tajam
Struktur PPy-Asg) Gugus fungsi O-H karboksilat pada puncak 3123 cm-1, yaitu puncak melebar sampai sekitar 2000 cm-1. Puncak serapan sebelumnya terdapat pada puncak sekitar 2000 – 3500 cm-1. Hal ini memungkinkan adanya interaksi dari asam glutamat yang teramobilkan dalam jaringan PPy
Tabel 3. Hasil analisis FTIR PPy-Asg
Puncak serapan
(cm-1) Gugus fungsi Bentuk pita
3123 O-H dan C-H kuat, melebar
1541 C=C cincin
aromatik
sedang,tajam
1400-1464 C-H alkana sedang, tajam
1288-1089 C-O asam
karboksilat
kuat, tajam
1137-1287 C-N amina sedang, tajam
905 C=C alkena sedang, tajam
3. Perilaku nerstian
Untuk karakterisasi elektroda kerja kawat
Pt termodifikasi PPy-Asg dilakukan
pengukuran potensial terhadap larutan standar asam glutamat pada konsentrasi 10-1 sampai 10 -4 M
Tabel 4. Perilaku Nerstian elektroda
-log [asam
glutamat] Persamaan nernst
R2 10-1 – 10-5 Y = 45,488 x + 65,88 0,94 10-1 – 10-4 Y = 56,378 x + 44,10 0,99 10-2 – 10-5 Y = 41,764 x + 80,78 0,89 10-1 – 10-4 Y = 59,820 x + 32,63 0,99 4. Selektivitas
Dari kajian selektivitas diharapkan elektroda kerja hanya merespon asam glutamat saja tanpa merespon ion-ion
pengganggu senyawa lainnya. Untuk
melihat pengaruh ion pengganggu terhadap elektroda termodifikasi Ppy-Asg, telah dilakukan pengukuran potensial dari senyawa asam amino lainnya yaitu glisin, leusin, dan glutamin serta ion utama asam glutamat.
Tabel 5 Tetapan selektivitas dari asam amino ion pengganggu asam amino pot K ij Glutamin 2,40 Glisin 0,51 Leusin 0,14
Berdasarkan Tabel 4. keberadaan glutamin
dalam campuran cukup mengganggu
terhadap asam glutamat sedangkan glisin dan leusin tidak mengganggu karena Kij 1. Dengan demikian elektroda termodifikasi polipirol-asam glutamat cukup selektif terhadap asam glutamat terkecuali asam amino dengan gugus R yang mirip seperti glutamin dengan R dari rumus molekul glutamin adalah (CH2)2NH2 , karena asam glutamat diperoleh dari hidrolisis glutamin
(Lehninger, 1995) Pengaruh ion
pengganggu terhadap asam glutamat dapat dilihat di bawah ini
Gambar 8. Selektivitas 0 20 40 60 80 100 120 140 160 180 2 3 4 E ( m V )
- log [asam amino]
ASAM GLUTAMAT
GLISIN LEUSIN GLUTAMIN
6
5. Waktu respon
Waktu respon adalah waktu yang
dibutuhkan oleh elektroda yang tercelup dalam asam glutamat ketika diukur sampai mendapatkan potensialnya stabil. Dalam Tabel 5. dapat ditunjukkan bahwa secara umum makin rendah konsentrasi asam glutamat maka waktu responnya makin
besar. Pada konsentrasi rendah
perpindahan muatan ion asam glutamat dari larutan sangat lambat untuk mencapai permukaan elektroda kerja.
Tabel 6.Waktu respon konsentrasi asam glutamat terhadap potensial elektroda
-log
asam glutamat Waktu respon (detik)
7 115 6 180 5 150 4 130 3 120 2 64 1 15
Sedangkan pada konsentrasi yang tinggi
10-1–10-2 perpindahan anion asam glutamat ion asam lebih cepat. Hal ini bisa
dipengaruhi oleh komposisi asam glutamat dalam membran sebesar 10-2 M. Pada konsentrasi 10-7 waktu respon potensial sudah tidak stabil lagi . Pada konsentrasi asam glutamat antara 10-1- 10-4 M, waktu respon yang sesuai bagi analisis kuantitatif yang menggunakan kurva kalibrasi adalah 130 detik atau 2 menit.
0 50 100 150 200 7 6 5 4 3 2 1
- log (asam glutam at)
w a k tu r e s p o n ( d e ti k )
Gambar 9. Hubungan waktu respon konsentrasi asam glutamat terhadap potensial.
6. Umur Elektroda
Usia pemakaian elektroda PPy-Asg
diperoleh dengan cara mengukur potensial dari sejumlah larutan standar asam glutamat. Salah satu hasil yang diperoleh yaitu dengan perilaku nernstian. Cara tersebut dilakuan setiap hari sampai nilai dari faktor nenst stabil.
Ketika terjadi perubahan nilai potensial dan
faktor nernst maka usia pemakaian
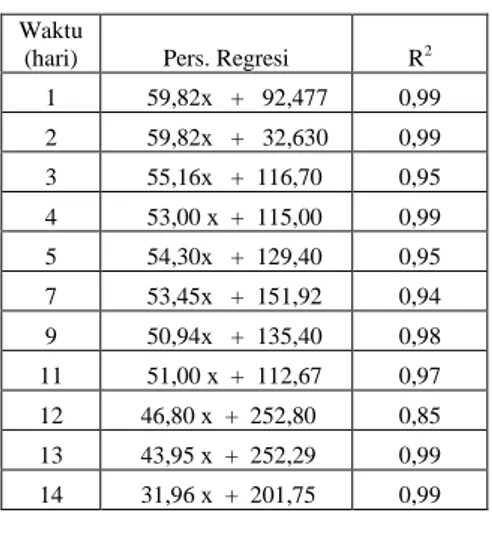
elektroda kerja tersebut sudah berakhir. Tabel 7. Usia pemakaian elektroda kerja
Waktu
(hari) Pers. Regresi R2
1 59,82x + 92,477 0,99 2 59,82x + 32,630 0,99 3 55,16x + 116,70 0,95 4 53,00 x + 115,00 0,99 5 54,30x + 129,40 0,95 7 53,45x + 151,92 0,94 9 50,94x + 135,40 0,98 11 51,00 x + 112,67 0,97 12 46,80 x + 252,80 0,85 13 43,95 x + 252,29 0,99 14 31,96 x + 201,75 0,99
Pada hari ke-14 slope (faktor nernst) telah berubah yang menandakan pemakaian elektroda terlapis polipirol asam glutamat masa pakainya adalah 14 hari.
0 10 20 30 40 50 60 70 1 2 3 4 5 7 9 11 12 13 14 w aktu (hari) S lo p e
Gambar 10. Usia pemakain elektroda Jika dibuat persamaan antara harga intersep sebagai fungsi waktu diperoleh persamaan K = 56,69 + 11,64 hari, dengan R2 = 0,66. Dari persamaan ini dapat disimpulkan bahwa elektroda mengalami perubahan respon potensial (drift) sebesar 11,641 mV/hari.
7
Gambar 11 Hubungan K terhadap waktu
KESIMPULAN
Hasil penelitian diperoleh optimasi kondisi elektropolimerisasi film PPy-Asg : 0,05 M ; 0,01 M dan KClO4 0,1 M sebagai elektrolit pendukung ; voltammogram siklik PPy-Asg dalam 10 siklus pada 0-1000 mV ; laju selusur 100 mV/detik. Rekaman FTIR memberikan pola spektrum khas dari Py,
PPy dan PPy-As. Kinerja elektroda
memberikan perilaku nerstian sebesar 59,82 mV/dekade pada konsentrasi asam glutamat 10-1-10-4 M.
Usia pemakaian elektroda terlapis film PPy-Asg adalah 14 hari yang ditandai dengan perubahan respon potensial (drift) sebesar 11,641 mV/hari. Elektroda termodifikasi film PPy-Asg cukup selektif terhadap asam glutamat (Asg).
UCAPAN TERIMAKASIH
1. Terimakasih Kemendiknas atas bantuan beasiswa BPPS Magister ITB 2004-2006
2. Terimakasih kepada Kepala
Laboratorium Penelitian Keahlian Kimia (KK) Analitik ITB yang memfasilitasi kegiatan penelitian ini.
DAFTAR PUSTAKA
Alumaa, A., A, Hallik., U, Macorg., V, Sammelsel., and J,Tamm (2000): Electrochimica Acta , 49, 1767-1774. Cheung, K.M., Bloor,D. dan Steven.G.C
(1990): The influence of unusual counterions on the electrochemistry and physical properties of polypyrrole,
Journal of Material Science, 25
Elkinci, Olcun., Boyukbayram, A.Elif., Kiralp, Semen., Toppare, Levent and Yagci, Yusuf (2007): Characterization
and Potential Applications of
Immobilized Glucose Oxidase and
Polyphenol Oxidase, Journal of
Macromolecular Science, Part A: Pure and Applied Chemistry, 44, 801–808. Ernayati,W (2005): Pembuatan Elektroda
Tipe Kawat Terlapis Film Polipirol-Lisin dan Penggunannya sebagai sensor Potensiometrik Lisin, Tesis, Departemen Kimia, ITB, Bandung. Kıralp Senem Toppare ., Yagci, and
Yusuf (2003): Immobilization of polyphenol oxidase in conducting copolymers and determination of phenolic compounds in wines with enzyme electrodes, International Journal of Biological Macromolecules,
33, 37–41.
Lehninger, 1995, Dasar-dasar Biokimia,
Jilid I, Penterjemah Maggy
Thenawidjaja, Erlangga, Jakarta.
Murniati,A and Buchari (2007):
Polypyrrolle glutamic acid coated wire
electrode, Proceeding in ICCS,
Yogyakarta: ANL/27-4.
Wang, J. (2000): Analytical
Electrochemistry, second edition, John Willey and sons, New York.
Purwanto, E(2004): Elektropolimerisasi Pirol dan Penggunannya Dalam Studi
Penghantaran Antibiotik melaui
membran, Tesis, Departemen Kimia, ITB, Bandung.
Suratman, A(2003): Pengaruh Asam Amino Pada Proses Elektropolimerisasi Pirol,
Tesis, Departemen Kimia, ITB,