III.
METODOLOGI PENELITIAN
A.
Bahan dan Alat
Bahan utama yang digunakan dalam penelitian ini adalah ubi jalar Cilembu dan ubi jalar ungu Ayamurasaki. Bahan-bahan kimia yang digunakan adalah akuades, K2SO4, HgO, H2SO4
pekat, H3BO3, indikator metil-merah biru, NaOH-Na2S2O3, HCl 0.02N, kapas, heksana, H2SO4
0.255N, NaOH 0.625N, K2SO4 10%, alkohol, HCl 25%, NaOH 25%, larutan Luff-Schrool, KI
20%, H2SO4 26.5%, Na2S2O3 0.1N, indikator pati, amilosa standar, NaOH 1 N, asam asetat 1N,
larutan iod, dan minyak.
Alat-alat yang digunakan untuk proses pembuatan pati antara lain pisau, pemarut, pengepres atau penyaring, cabinet drier, blender, ayakan 100 mesh. Alat-alat untuk penepungan
umbi antara lain pisau, penyawut, oven, disc mill, ayakan 100 mesh. Selanjutnya, alat-alat yang
digunakan untuk analisis antara lain neraca analitik, Whiteness Meter, Polarized Light Microscope,
oven, desikator, cawan aluminium, cawan porselen, labu Kjeldahl, Soxhlet, Spektrofotometer,
Rapid Visco Analyzer (RVA), Texturized Analyzer, sentrifuse, erlenmeyer, gelas ukur, gelas piala,
labu takar, sudip, gelas pengaduk, spatula, dan alat-alat gelas lainnya.
B.
Metode Penelitian
Penelitian ini terdiri dari 3 tahapan : 1) Pembuatan tepung dan pati ubi jalar Cilembu dan ubi jalar ungu Ayamurasaki; 2) Analisis fisikokimia dan fungsional; 3) Analisis statistika.
1.
Ekstraksi Pati Ubi Jalar
Pembuatan pati diawali dengan pembersihan ubi jalar dari kotoran dan tanah lalu dikupas dan diparut. Hasil parutan ditambah air dengan dengan perbandingan 1:5. Bubur ubi jalar kemudian disaring menggunakan mesin penyaring. Ampas dihancurkan, ditambah air, dan disaring lagi. Selanjutnya, seluruh cairan hasil penyaringan diendapkan. Setelah pati mengendap, air dibuang dan kemudian pati dicuci dengan air bersih 2-3 kali. Pati yang telah dipisahkan dari air kemudian dikeringkan menggunakan cabinet drier dengan suhu 60oC
selama 10 jam sampai kering (kadar air ≤ 14%), dihancurkan menggunakan blender, dan diayak menggunakan ayakan 100 mesh.
2.
Pembuatan Tepung Ubi Jalar
Tepung ubi jalar dibuat dengan mengeringkan sawutan ubi yang telah dikupas dan dicuci menggunakan cabinet drier pada suhu 60oC selama 5 jam sampai kering (kadar air
≤14%). Setelah kering, sawutan ini dihancurkan dan diayak sampai menjadi tepung dengan tingkat kehalusan 100 mesh.
3.
Analisis Fisikokimia dan Fungsional
i. Rendemen
Rendemen merupakan persen bobot sampel (pati atau tepung) terhadap ubi jalar segar yang telah dikupas.
% 100%
% 100 % 100%
ii. Karakteristik fisik
a) Densitas kamba (Bulk density) (Wirakartakusumah et al 1992)
Densitas kamba adalah masa partikel yang menempati suatu volume tertentu. Densitas kamba ditentukan dengan cara menimbang sejumlah tertentu sampel dalam gelas ukur sampai volume 20 ml.
/ b) Derajat putih
Pengukuran derajat putih hanya dilakukan pada pati ubi jalar. Pengukuran ini menggunakan alat Whiteness Meter (Kett Electric Laboratory (C-100-3)). Sebelumnya,
dilakukan kalibrasi menggunakan MgO dengan nilai derajat putih 100% (80.6). Sejumlah contoh dimasukkan ke dalam wadah khusus, lalu dimampatkan dan ditutup, kemudian dimasukkan ke dalam tempat pengukuran. Nilai derajat putih akan keluar pada layar (A).
%
80.6 100%
Keterangan :
A = Nilai yang terbaca pada alat
c) Warna (Pomeranz dan Meloan 1978)
Pengukuran warna dilakukan dengan Chromameter CR 300 Minolta. Sampel diletakkan di tempat yang telah disediakan kemudian tekan tombol start maka akan muncul nilai dalam berbagai skala. Skala yang dipilih untuk pengukuran adalah L*a*b* (CIE 1976). L menunjukkan kecerahan dengan nilai 0 (gelap/hitam)-100(terang/putih). Nilai a positif antara 100 (merah) dan negatif antara 80 (hijau). Nilai b positif antar 0-70 (kuning) dan negatif antara 0-0-70 (biru). Pengukuran dilakukan duplo dan dilakukan kalibrasi terlebih dahulu.
d) Bentuk dan ukuran granula pati
Alat yang digunakan untuk melihat bentuk dan intensitas birefrigence granula
pati adalah Polarized Light Microscope (Olympus Optical Co. Ltd, Japan). Suspensi pati
disiapkan dengan mencampurkan pati dan aquades (1%), kemudian dikocok. Suspensi diteteskan pada alat gelas objek dan ditutup dengan gelas penutup, preparat kemudian dipasang pada PLM. Pengamatan dilakukan dengan meneruskan cahaya terpolarisasi dengan perbesaran 400x. Polarized Light Microscope dapat mengamati ukuran granula
pati. Mikroskop ini dilengkapi dengan semacam alat pengukur pada lensa okulernya, dimana skala terkecil bernilai 10 μm.
Gambar 6. Diagram alir penelitian Analisis statistika
Ubi jalar
Pati
Analisis fisikokimia dan fungsional : • Rendemen • pH • Densitas kamba • Warna • Proksimat • Kadar pati • Kadar amilosa • Kadar amilopektin • Sifat gelatinisasi
• Absorbsi air dan minyak
Analisis fisikokimia dan fungsional : • Rendemen • pH • Densitas kamba • Derajat putih • Bentuk granula • Proksimat • Kadar pati • Kadar amilosa • Kadar amilopektin • Sifat gelatinisasi • Swelling power • Kelarutan • Kekuatan gel • Kejernihan pasta
Pembuatan tepung Ekstraksi pati
Gambar 7. Proses Ekstraksi Pati Ubi Jalar Pembersihan dan pengupasan Pemarutan Penambahan air (1:5) Penyaringan Pemisahan cairan dan endapan pati Pengendapan (8-12 jam) Ubi jalar Kulit Cairan Pengeringan ( 60oC, 10 jam) Penghancuran Pengayakan (100 mesh) Endapan Pati
Gambar 8. Proses Pembuatan Tepung Ubi Jalar
iii. Karakteristik kimia
a) Kadar air metode oven (AOAC 1995)
Cawan aluminium dikeringkan dalam oven pada suhu 105oC selama 15 menit, lalu
didinginkan dalam desikator selama 10 menit. Cawan ditimbang menggunakan neraca analitik. Sampel sebanyak 2-3 gram dimasukkan ke dalam cawan, kemudian cawan serta sampel ditimbang dengan neraca analitik. Cawan berisi sampel dikeringkan dalam oven pada suhu 105oC selama 1 malam (16 jam). Selanjutnya cawan berisi sampel didinginkan
dalam desikator, kemudian ditimbang.
Pengayakan (100 mesh) Pembersihan dan Pengupasan Penyawutan Pengeringan ( 600C, 5 jam ) Ubi jalar Kulit Sawut basah Sawut kering Penggilingan Tepung ubi
% 100%
% 100%
Keterangan :
a = bobot sampel awal (g)
b = bobot sampel dan cawan setelah dikeringkan (g) c = bobot cawan kosong (g)
b) Kadar abu (AOAC 1995)
Cawan pengabuan dibakar dalam tanur, kemudian didinginkan dalam desikator, dan ditimbang. Sampel sebanyak 3-5 gram ditimbang dalam cawan tersebut, kemudian cawan berisi sampel dibakar sampai didapatkan abu berwarna abu-abu atau sampai bobotnya konstan. Cawan yang berisi sampel didinginkan dalam desikator, kemudian ditimbang dengan neraca analitik.
Catatan : sebelum masuk tanur, sampel yang ada dalam cawan dibakar dulu menggunakan
hotplate sampai tidak mengeluarkan asap lagi.
% 100%
% %
100 100%
c) Kadar protein metode Mikro-Kjeldahl (AOAC 1995)
Sejumlah kecil sampel (kira-kira 100-250 mg) ditimbang, dipindahkan ke dalam labu Kjeldahl 30 ml. Setelah itu, ditambahkan 1.9 ± 0,1 gram K2SO4, 40 ± 10 mg HgO,
dan 2.0 ± 0.1 ml H2SO4 ke dalam labu Kjeldahl yang berisi sampel. Jika sampel lebih dari
150 mg, ditambahkan 0.1 ml H2SO4 untuk setiap 10 mg bahan organik di atas 15 mg.
Setelah itu, labu Kjeldahl yang berisi sampel didihkan selama 1-1.5 jam sampai cairan menjadi jernih. Setelah cairan jernih, labu Kjeldahl yang berisi sampel didinginkan dan ditambahkan sejumlah kecil air secara perlahan-lahan ke dalamnya, kemudian didinginkan kembali. Isi labu dipindahkan ke dalam alat destilasi dicuci dan dibilas 5-6 kali dengan 1-2 ml air, air cucian dipindahkan ke dalam alat destilasi.
Erlenmeyer 125 ml yang berisi 5 ml larutan H3BO3 dan 2-4 tetes indikator
(campuran dua bagian metil merah 0.2% dalam alkohol dan satu bagian metil blue 0.2%
dalam alkohol) diletakkan di bawah kondensor. Ujung tabung kondensor harus terendam di bawah larutan H3BO3 kemudian ditambahkan 8-10 ml larutan NaOH-Na2S2O3 dan
dilakukan destilasi sampai tertampung kira-kira 15 ml destilat di erlenmeyer. Setelah itu, tabung kondensor dibilas dengan air dan bilasannya ditampung dalam erlenmeyer yang sama. Selanjutnya, isi erlenmeyer diencerkan sampai kira-kira 50 ml dan kemudian dititrasi dengan HCl 0.02 N yang sudah distandardisasi sampai terjadi perubahan warna menjadi abu-abu. Penentuan protein juga dilakukan untuk blanko.
% 14,007 100%
% % 6,25
% %
100 100%
d) Kadar lemak metode soxhlet (AOAC 1995)
Sampel yang akan dianalisis ditimbang sebanyak 1-2 gram lalu dimasukkan ke dalam selongsong kertas lalu dikeringkan dalam oven pada suhu tidak lebih dari 80oC
selama lebih kurang satu jam. Selongsong kemudian dimasukkan ke dalam alat Soxhlet yang telah dihubungkan dengan labu lemak yang berisi batu didih yang telah dikeringkan dan telah diketahui bobotnya. Sampel diekstrak dengan heksana atau pelarut lemak lainnya selama lebih kurang 6 jam. Pelarut kemudian disuling kembali dan hasil ekstraksi lemak dikeringkan dalam oven pengering pada suhu 105oC. Labu berisi lemak sampel
kemudian didinginkan dalam desikator lalu ditimbang bobotnya. Pengeringan diulangi hingga didapat bobot yang tetap.
% 100%
% %
100 100%
Keterangan :
a = Bobot labu lemak setelah diekstraksi (g) b = Bobot labu lemak sebelum diekstraksi (g) c = Bobot sampel (g)
e) Kadar karbohidrat (by difference)
Kadar karbohidrat dihitung sebagai sisa dari kadar air, kadar abu, lemak, dan protein. Kadar karbohidrat dapat ditentukan sebagai berikut:
Kadar karbohidrat (%bb) = 100% - (kadar air + kadar abu + kadar lemak + kadar protein) (%bb)
% %
100 100%
f) Nilai pH (Apriyantono et al. 1989)
Timbang sebanyak 1 gram sampel, kemudian tambahkan 20 ml air dan diaduk sampai larut. Selanjutnya, sebanyak 50 ml air ditambahkan lagi dan dihomogenisasi.
Larutan ini diendapkan selam 1 jam. Supernatan diambil untuk diukur pHnya menggunakan pHmeter terkalibrasi.
g) Kadar pati metode Luff-Schroorl (AOAC 1997) •Pembuatan larutan Luff-Schoorl
Sebanyak 25 g CuSO4.5H2O sejauh mungkin bebas besi, dilarutkan dalam 100 ml
air, 50 g asam sitrat dilarutkan dalam 50 ml air dan 388 g soda murni (Na2CO3.10H2O)
dilarutkan dalam 300-400 ml air mendidih. Larutan asam sitrat dituangkan dalam larutan soda sambil dikocok hati-hati. Selanjutnya, ditambahkan larutan CuSO4. Sesudah
dingin ditambahkan air sampai 1L. Bila terjadi kekeruhan, didiamkan kemudian disaring.
•Persiapan contoh
Sampel sebanyak 0.1 g ditimbang dalam erlenmeyer 300 ml, dan ditambah 50 ml akuades dan 5 ml HCl 25 %, kemudian dipanaskan pada suhu 100oC selama 3 jam.
Setelah didinginkan, suspensi dinetralkan dengan NaOH 25 % sampai pH 7. Pindahkan secara kuantitatif dalam labu takar 100 ml, kemudian tepatkan sampai tanda tera dengan air destilata. Larutan ini kemudian disaring kembali dengan kertas saring.
•Analisis contoh
Sebanyak 25 ml filtrat dari persiapan contoh ditambah 25 ml larutan Luff-Schoorl
dalam erlenmeyer. Dibuat pula perlakuan blanko yaitu 25 ml larutan Luff Schoorl
dengan 25 ml akuades. Erlenmeyer dihubungkan dengan pendingin balik, kemudian dididihkan. Pendidihan larutan dipertahankan selama 10 menit. Selanjutnya, didinginkan secepatnya dan ditambah 15 ml KI 20 % dan dengan hati-hati ditambah 25 ml H2SO4 26.5%. Yodium yang dibebaskan dititrasi dengan larutan Na2SO3 0.1N
memakai indikator pati sebanyak 2-3 ml. Untuk memperjelas perubahan warna pada akhir titrasi maka sebaiknya pati diberikan pada saat titrasi hampir berakhir.
•Perhitungan kadar pati
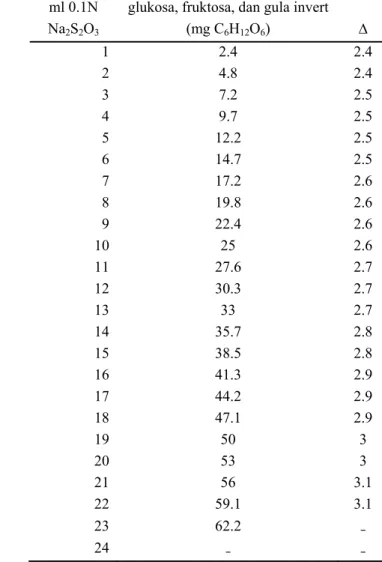
Dengan mengetahui selisih antara titrasi blanko dan titrasi contoh, kadar gula reduksi setelah inversi (setelah dihidrolisa dengan HCl 25 %) dalam bahan dapat dicari dengan menggunakan tabel 7 selisih kadar gula inverse dengan sebelum inverse dikalikan 0.9 merupakan kadar pati dalam bahan.
% 100% 0.9
% %
Tabel 7. Penentuan glukosa, fruktosa, dan gula invert dalam suatu bahan pangan dengan metode Luff-Schoorl
ml 0.1N Na2S2O3
glukosa, fruktosa, dan gula invert
(mg C6H12O6) ∆ 1 2.4 2.4 2 4.8 2.4 3 7.2 2.5 4 9.7 2.5 5 12.2 2.5 6 14.7 2.5 7 17.2 2.6 8 19.8 2.6 9 22.4 2.6 10 25 2.6 11 27.6 2.7 12 30.3 2.7 13 33 2.7 14 35.7 2.8 15 38.5 2.8 16 41.3 2.9 17 44.2 2.9 18 47.1 2.9 19 50 3 20 53 3 21 56 3.1 22 59.1 3.1 23 62.2 ₋ 24 ₋ ₋
h) Kadar amilosa metode IRRI (Apriyantono et al. 1989 ) •Pembuatan kurva standar
Sebanyak 40 mg amilosa murni dimasukkan ke dalam tabung reaksi. Kemudian ke dalam tabung reaksi tersebut ditambah 1ml etanol 95 % dan 9 ml NaOH 1 N. Tabung reaksi dipanaskan dalam air mendidih sekitar 10 menit sampai semua amilosa membentuk gel. Setelah didinginkan, campuran tersebut dipindahkan secara kuantitatif ke dalam labu takar 100 ml dan tepatkan air sampai tanda tera. Sebanyak 1, 2, 3, 4, dan 5 ml larutan tersebut dipipet ke dalam labu takar 100 ml. Masing-masing labu takar ditambahkan dengan asam asetat 1 N sebanyak 0.2, 0.4, 0.6, 0.8, 1 ml, kemudian masing-masing ditambah 2 ml larutan iod dan tepatkan dengan air sampai tanda tera. Setelah didiamkan selama 20 menit, ukur absorbansi dari intensitas warna biru yang terbentuk dengan spektrofotometer pada panjang gelombang 625 nm. Buat kurva standar sebagai hubungan antara kadar amilosa (sumbu x) dengan absorbansi (sumbu y).
•Analisis contoh
Sebanyak 100 mg contoh dimasukkan ke dalam tabung reaksi. Kemudian ke dalam tabung reaksi tersebut ditambah 1 ml etanol 95% dan 9 ml NaOH 1N. Tabung reaksi dipanaskan dalam air mendidih sekitar 10 menit untuk mengelatinisasi pati. Setelah didinginkan, campuran tersebut dipindahkan secara kuantitaif ke dalam labu takar 100 ml dan tepatkan sampai tanda tera. Sebanyak 5 ml larutan tersebut dipipet dan dipindahkan ke dalam labu takar. Ke dalam labu takar tersebut ditambahkan 1 ml asam asetat 1N, kemudian ditambah 2 ml larutan iod dan tepatkan dengan air sampai tanda tera. Setelah didiamkan selama 20 menit, ukur absorbansi dari intensitas warna biru yang terbentuk menggunakan spektrofotometer pada panjang gelombang 625 nm.
% 100
% %
100 100%
Keterangan :
C = Konsentrasi amilosa contoh dari kurva standar (mg/ml) V = Volume akhir contoh (ml)
FP = Faktor pengenceran W = Berat contoh (mg)
i) Kadar amilopektin metode IRRI (Apriyantono et al. 1989)
Pati terdiri dari amilosa dan amilopektin. Oleh karena itu, kadar amilopektin dapat dihitung dari selisih kadar pati dengan kadar amilosa.
% % %
iv. Karakteristik fungsional
a) Pasting property dengan Rapid Visco Analyzer (RVA) (AACC 2000 dengan
modifikasi)
Profil amilograf diukur menggunakan Rapid Visco Analyzer (RVA, Model
Tecmaster, Newsport Scientific, Australia). Sebanyak ± 3.00 g sampel dilarutkan secara langsung pada akuades sebanyak ±25 ml pada carnister. Pada pengukurannya digunakan
standar dua dimana akan diatur suhu awalnya 50oC dalam satu menit pertama kemudian
dipanaskan sampai suhu 95oC dalam waktu 7.5 menit dan ditahan pada suhu tersebut
selama 5 menit. Setelah itu, suhu sampel didinginkan kembali sampai suhu 50oC dalam
waktu 7.5 menit dan ditahan selama 2 menit. Kecepatan rotasi diatur pada 160 rpm selama proses. Parameter yang dapat diukur antara lain viskositas puncak (VP), viskositas pada akhir waktu ditahan 95oC atau viskositas pasta panas (VPP), viskositas akhir (VA) pada
akhir pendinginan, viskositas breakdown (VBD = VP-VPP), viskositas balik (VB =
b) Daya kembang (Swelling power) dan kelarutan (Solubility index) (Li dan Yeh 2001
dengan modifikasi)
Pati dengan konsentrasi 1% dipanaskan menggunakan waterbath dengan kisaran
suhu 60oC, 70oC, 80oC, 90oC, dan 95oC masing-masing selama 30 menit kemudian
disentrifuse dengan kecepatan 3000 rpm selama 30 menit. Supernatan hasil sentrifuse dipisahkan dari endapannya untuk mengukur kelarutan. Swelling power dihitung dengan
cara membagi endapan hasil sentrifuse dengan bobot pati kering sebelum dipanaskan.
/
Keterangan :
X = bobot tabung dan endapan (g) Y = bobot tabung kosong (g) W= bobot sampel (g)
Supernatan yang didapatkan dari hasil sentrifuse kemudian dikeringkan dan dinyatakan sebagai kelarutan. Nilai kelarutan dapat dihitung sebagai presentase bobot pati hasil pengeringan supernatan dengan bobot sampel.
%
Keterangan :
X = bobot cawan dan endapan (g) Y = bobot cawan kosong (g)
W = bobot sampel (g)
c) Kekuatan gel (Wattanacjant et al. 2002 dengan modifikasi)
Karakteristik tekstur gel diukur dengan menggunakan alat Texturized Analyzer
(TA-XT2). Pati dengan konsentrasi 20% dipanaskan dari suhu 30oC sampai suhu 95oC dan
dipertahankan selama suhu 30 menit, kemudian didinginkan sampai suhu 50oC. Pasta ini
dituangkan ke dalam tabung dengan diameter 4 cm dan tinggi 5 cm, lalu disimpan pada suhu -4 oC selama 24 jam. Sel ditekan dengan kecepatan penetrasi 2 mm/s dan jarak 15
mm.
d) Kejernihan pasta (Wattanachant et al. 2002)
Pasta pati (1%) dibuat dengan cara melarutkan 50 mg sampel dengan 5 ml air di dalam tabung berulir. Selanjutnya, tabung ini dimasukkan ke dalam air mendidih selama 30 menit dimana setiap 5 menit dilakukan pengadukan. Setelah didinginkan selama beberapa menit, sampel siap diukur absorbansinya dengan panjang gelombang 650 nm. Blanko untuk pengukuran ini menggunakan aquades.
e) Absorbsi air dan minyak (Sathe dan Salunke 1981)
Sebanyak 1 gram sampel dilarutkan ke dalam 10 ml minyak kemudian diaduk selama 30 detik. Setelah itu, larutan ini didiamkan selama 30 menit lalu disentrifuse selama 40 menit dengan kecepatan 3500 rpm. Supernatan dipisahkan untuk ditimbang.
/ / Keterangan : a = bobot cairan (g) b = bobot supernatan (g) c = bobot sampel (g)