KANDUNGAN LOGAM BERAT Cu, Zn, DAN Pb DALAM AIR,
IKAN NILA (Oreochromis niloticus) DAN IKAN MAS
(Cyprinus carpio) DALAM KERAMBA JARING APUNG,
WADUK SAGULING
SHITA FEMALA SHINDU
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR 2005
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa Skripsi yang berjudul:
Kandungan Logam Berat Cu, Zn dan Pb dalam Air,
Ikan Nila (Oreochromis niloticus ) dan Ikan Mas (Cyprinus carpio) dalam Keramba Jaring Apung, Waduk Saguling
Adalah benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Skripsi ini
Bogor, Desember 2005
SHITA FEMALA SHINDU C24101004
ABSTRAK
SHITA FEMALA SHINDU. Kandungan Logam Berat Cu, Zn, dan Pb dalam Air, Ikan Nilai (Oreochromis niloticus ) dan Ikan Mas (Cyprinus carpio) dalam Keramba Jaringa Apung, Waduk Saguling. Dibimbing oleh ISDRADJAD STYOBUDIANDI dan IDIL ARDI
Waduk Saguling merupakan salah satu lingkungan perairan yang sangat mungkin tercemar oleh logam berat. Proses perpindahan logam berat dari air ke dalam tubuh ikan sangat mungkin terjadi, yang pada akhirnya akan berdampak buruk bagi ikan ter sebut dan manusia yang mengkonsumsinya. Penelitian ini bertujuan untuk mengetahui kandungan logam berat Pb, Cu, dan Zn dalam air, dalam tubuh ikan nila, dan ikan mas yang dibudidayakan dalam keramba jaring apung di Waduk Saguling. Selain itu juga mengeta hui kisaran nilai dari parameter suhu, pH, alkalinitas, dan oksigen terlarut pada bulan Juni dan Juli.
Penelitian ini dilakukan pada bulan Juni-Juli 2005. Penentuan stasiun pengambilan contoh didasarkan atas daerah masukan air (inlet), keberadaan lokasi jaring apung, dan daerah outlet. Kandungan logam berat yang terukur dilakukan secara deskriptif, yaitu dengan membandingkan data yang diperoleh dengan literatur penunjang.
Hasil penelitian menunjukan bahwa secara umum kandungan logam Cu dan Zn di perairan Waduk Saguling pada bulan Juni berada di atas baku mutu air tawar sedangkan logam Pb pada bulan Juni dan Juli masih berada di bawah baku mutu air tawar menurut PP. RI No. 82 tahun 2001. Keberadaan logam berat di perairan sangat dipengaruhi kondisi alam yang terjadi, yaitu hujan lebih sering terjadi pada bulan Juni. Kandungan logam Cu dan Zn pada ikan nila dan ikan mas cenderung berada di bawah nilai maksimum yang diperbolehkan. Sedangkan kandungan logam Pb pada ikan nila dan mas berada di atas nilai maksimum yang diperbolehkan (SK Dirjen POM No. 037/25/B/SKVII/1989). Nilai parameter suhu, pH, alkalinitas, dan DO pada kedalaman tertentu masih berada dalam kisaran nilai yang dianjurkan untuk kegiatan budidaya menurut literatur yang ada, kecuali pada stasiun 2. Kandungan oksigen terlarut di stasiun 2 pada kedalaman 4 meter sudah tidak layak untuk keberlangsungan budidaya ikan.
Kondisi perairan yang sudah tercemar oleh logam berat telah mengakibatkan ikan-ikan yang dibudidaya mengandung logam berat dalam tubuhnya. Apabila ikan tersebut dikonsumsi oleh manusia, akan terjadi perpindahan logam berat dari tubuh ikan ke dalam tubuh manusia yang mengkonsumsinya.
Hak cipta milik Shita Femala Shindu, tahun 2005
Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari Institut Pertanian Bogor, sebagian atau seluruhnya dalam bentuk apa pun, baik cetak, fotokopi, mikrofilm, dan sebagainya
KANDUNGAN LOGAM BERAT Cu, Zn, DAN Pb DALAM AIR,
IKAN NILA (Oreochromis niloticus) DAN IKAN MAS
(Cyprinus carpio) DALAM KERAMBA JARING APUNG,
WADUK SAGULING
SHITA FEMALA SHINDU
SKRIPSI
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Manajemen Sumberdaya Perairan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR 2005
SKRIPSI
Judul : Kandungan Logam Berat Pb, Cu, dan Zn dalam Badan Air,
Ikan Nila (Oreochromis niloticus ) dan Ikan Mas (Cyprinus carpio) dalam Keramba Jaring Apung, Waduk Saguling.
Mahasiswa : SHITA FEMALA SHINDU
NRP : C24101004
Disetujui,
Pembimbing I Pembimbing II
Dr. Ir. Isdradjad S, MSc Idil Ardi, M.Si NIP. 131 471 378 NIP. 950 000 797
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
PRAKATA
Alhamdulillah, puji syukur penulis panjatkan ke hadirat Allah SWT yang telah melimpahkan rahmat serta hidayah-Nya yang telah diberika n kepada penulis sehingga dapat menyelesaikan skripsi dengan judul Kandungan Logam Berat
Cu, Zn, dan Pb dalam Air, Ikan Nila (Oreoc hromis niloticus) dan Ikan Mas (Cyprinus carpio) dalam Keramba Jaring Apung, Waduk Saguling.
Penulis mengucapkan terima kasih kepada :
1. Dr. Ir. Isdradjad S, M.Sc dan Idil Ardi, M.Si selaku komisi pembimbing skripsi yang telah banyak memberikan bimbingan dan pengarahan sehingga penulis dapat menyelesaikan skripsi ini.
2. Dr. Ir. Tri Heru Prihadi, M.Sc yang telah memberikan kesempatan kepada penulis untuk ikut melakukan penelitian di Pusat Riset Perikanan Budidaya Departemen Kelautan dan Perikanan.
3. Ir. Agustinus M. Samosir, M.Phil selaku penguji tamu dan Dr. Ir. M. Mukhlis Kamal, M.Sc dari Program Studi S1 Departemen Manajemen Sumberdaya Perairan yang telah memberikan saran dan masukan dalam penyempurnaan penulisan skripsi ini.
4. Bu Ati, Pak Usman, Mba Tita, Mba Tami, Kak Andria, Kak Bowo, Kak Wendi, Kak Nizar, yang telah membantu di lapang selama penelitian. MSP ’36, ’37, ’38, ’39, ’40, ’41, saudaraku di FKM-C, Sanggar Ahad, IKADA, dan Forces atas segala dukungannya.
5. Abah, ’Mi, Yayu, Aa, beserta seluruh keponakanku yang telah memberikan do’a, cinta dan kasih sayang serta semangat yang tak pernah putus kepada penulis.
6. Seluruh keluarga di Bandung, Lampung dan di Subang atas perhatian dan kasih sayangnya selama ini.
Penulis berharap skripsi ini dapat memberikan informasi yang berguna dan bermanfaat kepada semua pihak yang memerlukannya.
Bogor, Desember 2005
DAFTAR ISI
Halaman
DAFTAR ISI ... viii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... ... xi
DAFTAR LAMPIRAN ... xii
I. PENDAHULUAN 1.1. Latar Belakang ... ... 1
1.2. Perumusan Masalah ... 2
1.3. Tujuan ... 3
1.4. Manfaat ... ... 3
II. TINJAUAN PUSTAKA 2.1. Logam Berat ... 4
2.2. Kandungan Logam Berat dalam Air ... 4
Tembaga (Cu) ... 5
Seng (Zn) ... 6
Timbal (Pb) ... 7
2.3. Akumulasi Logam Berat dalam Tubuh Ikan ... ... 8
2.4. Klasifikasi dan Morfologi Ikan Ikan Nila (Oreochromis niloticus) ... 9
Ikan Mas (Cyprinus carpio) ...…. 10
2.5. Waduk Saguling ... ... 11
2.6. Kualitas Air ... 12
Suhu... 12
pH... 13
Alkalinitas ... 13
Oksigen terlarut (DO) ... ... 14
III. BAHAN DAN METODE 3.1. Waktu dan Lokasi Penelitian... 15
3.2. Alat, Bahan, dan Kegunaan... 15
3.3. Metode Kerja Penentuan Stasiun Pengambilan Contoh... 15
Pengambilan Contoh Air ... 16
Pengambilan Contoh I kan... ... 16
Pengambilan Organ Tubuh Ikan... 16
Perlakuan Contoh Analisa... ... 18
3.4. Analisa Data Analisa Kandungan Logam Berat... ... 18
Faktor Konsentrasi ... 18
IV. HASIL DAN PEMBAHASAN
4.1. Logam Berat dalam Air ... 20
Kandungan Cu dalam Air... 20
Kandungan Zn dalam Air ... 22
Kandungan Pb dalam Air ... 23
4.2. Logam Berat pada Ikan Nila dan Ikan Mas... ... 24
Kandungan Cu pada Ikan Nila dan Ikan Mas ... ... 25
Kandungan Zn pada Ikan Nila dan Ikan Mas... 27
Kandungan Pb pada Ikan Nila dan Ikan Mas ... 29
4.3. Kualitas Perairan... ... 31
Suhu... ... 31
pH... 32
Alkalinitas ... 34
Oksigen terlarut (DO) ... 35
4.4. Usulan Upaya Pengelolaan Waduk Saguling ... ... 36
V. KESIMPULAN ... ... 38
DAFTAR PUSTAKA ... ... 39
DAFTAR TABEL
Halaman
1 Nilai baku mutu logam berat dalam air dan tubuh ikan ... ... 18 2 Nilai baku mutu suhu, pH, DO, dan alkalinitas ... 19
DAFTAR GAMBAR
Halaman
1 Bagan alir pendekatan masalah ... 3
2 Ikan nila (Oreochromis niloticus ) ... 10
3 Ikan mas (Cyprinus carpio) ... 11
4 Peta lokasi Waduk saguling ... 17
5 Denah lokasi stasiun pengamatan ... 17
6 Grafik kandungan logam Cu dalam air ... 20
7 Grafik kandungan logam Zn dalam air ... 22
8 Grafik kandungan logam Pb dalam air ... 23
9 Grafik kandungan logam Cu pada organ ikan ... 25
10 Grafik faktor konsentrasi logam Cu ... ... 26
11 Grafik kandungan logam Zn pada organ ikan ... 27
12 Grafik faktor konsentrasi logam Zn ... ... 28
13 Grafik kandungan logam Pb pada organ ika n ... 29
14 Grafik faktor konsentrasi logam Pb ... ... 29
15 Grafik suhu air ... ... 31
16 Grafik pH ... ... 33
17 Grafik alkalinitas ... ... 34
DAFTAR LAMPIRAN
Halaman
1 Data curah hujan ... ... 42
2 Prosedur analisa kandungan logam berat pada organ tubuh ikan ... 43
3 Kandungan logam berat pada organ ikan nila dan ikan mas... 44
4 Kandungan logam berat dalam air disetiap stasiun ... 45
5 Kandungan logam berat dalam air pada kedalaman berbeda ... ... 46
6 Parameter fisika dan kimia disetiap stasiun ... 47
I. PENDAHULUAN
1.1. Latar Belakang
Waduk Saguling merupakan salah satu waduk di Propinsi Jawa Barat yang memiliki banyak fungsi. Waduk ini digunakan sebagai Pembangkit Listrik Tenaga Air (PLTA) sejak tahun 1985, juga be rfungsi sebagai pengendali banjir, penampung air sementara dari sungai Citarum, dan dimanfaatkan sebagai kegiatan budidaya, seperti ikan mas dan ikan nila dengan menggunakan sistem keramba jaring apung. Akibat dari fungsi Waduk Saguling tersebut, memungkinkan masuknya berbagai jenis limbah dan zat pencemar yang berpotensi menurunkan kualitas air di waduk tersebut. Hasil penelitian Surachman (2003), menunjukan bahwa penurunan kualitas air Waduk Saguling salah satunya disebabkan oleh pencemaran perairan karena logam berat yang merupakan hasil limbah industri yang ada di DAS Citarum Hulu. Umumnya air limbah industri mengandung logam berat tertentu, karena dalam proses produksinya banyak melibatkan bahan kimia, seperti industri kimia, industri cat, industri pupuk (Darmono,1995).
Keberadaan zat pencemar dalam perairan akan mempengaruhi makhluk hidup yang ada di dalamnya. Masuknya zat pencemar ke dalam tubuh biota air dapat melalui saluran pernapasan dan saluran pencernaan (Saeni, 1989). Melalui proses rantai makanan, memungkinkan perpindahan zat pencemar dalam hal ini logam berat, dari suatu makhluk hidup ke makhluk hidup lain yang mengkonsumsinya. Keadaan ini bila dibiarkan terus menerus tentunya dapat menimbulkan kasus pencemaran logam berat.
Oleh karena itu, penelitian ini dilakukan untuk mengetahui kadar logam berat tertentu yang ada di perairan dan di dalam tubuh ikan. Logam berat jenis Pb, Cu, dan Zn, yang merupakan jenis logam berat berbahaya bila terakumulasi dalam jumlah yang tinggi dan menjadi limbah yang berbahaya bagi biota yang hidup di air.
1.2. Perumusan Masalah
Kandungan logam berat dalam perairan secara alamiah berada dalam jumlah yang relatif sedikit. Aktifitas manusia di DAS Citarum Hulu seperti kegiatan industri, domestik, pertanian, dan lainnya dapat menjadi faktor penyebab terjadinya peningkatan kandungan logam berat dan dapat menimbulkan pencemaran logam berat pada perairan waduk. Hasil penelitian Surachman (2003), beberapa kandungan logam berat pada Waduk Saguling sudah melebihi baku mutu air sehingga dikatakan tidak layak bagi kondisi perikanan, seperti timbal (Pb), tembaga (Cu), dan seng (Zn).
Keberadaan ikan-ikan budidaya yang ada di dalam Waduk Saguling, tentunya akan terpengaruh oleh kondisi perairan yang sudah tercemar. Ikan yang hidup di kawasan perairan yang tercemar oleh logam berat sangat memungkinkan di dalam tubuhnya mengandung logam berat. Pada konsentrasi tertentu akan mengakibatkan terganggunya fungsi organ, yang pada akhirnya dapat menyebabkan kematian. Apabila ikan-ikan tersebut dikonsumsi oleh manusia dalam waktu yang lama akan menyebabkan gangguan kesehatan, seperti kerusakan jaringan organ tubuh, kemandulan, bahkan kematian.
Berdasarkan pertimbangan tersebut, diperlukan suatu kajian yang dapat memberikan informasi terkini mengenai kandungan logam berat di Waduk Saguling, khususnya kandungan timbal (Pb), tembaga (Cu), dan seng (Zn). Kandungan logam di Waduk Saguling apabila telah melebihi baku mutu air, diharapkan dapat segera diambil tindakan perbaikan untuk mengemba likan kondisi Waduk Saguling seperti semula, serta konsumsi terhadap ikan hasil budidaya dan ikan hasil tangkap dapat dipertimbangkan dalam sisi kesehatan manusia yang mengkonsumsinya.
Gambar 1 Bagan alir pendekatan masalah
1.3. Tujuan
Penelitian ini bertujuan untuk mengetahui kandungan logam berat timbal (Pb), tembaga (Cu), dan seng (Zn) dalam air, dalam organ tubuh ikan nila dan ikan mas yang dibudidayakan dalam keramba jaring apung di Waduk Saguling. Organ ikan nila dan ikan mas yang dijadikan objek dalam penelitian ini yaitu, hati, ginjal, dan daging. Selain itu mengetahui kisaran nilai dari parameter suhu, pH, alkalinitas dan oksigen terlarut pada bulan Juni dan bulan Juli.
1.4. Manfaat
Penelitian ini bermanfaat untuk memberikan informasi tentang kandungan logam berat dalam air, dalam tubuh ikan nila dan ikan mas yang dibudidaya. Informasi ini diharapkan dapat digunakan oleh pemerintah, dan pengelola pabrik sebagai bahan kajian dalam pengelolaan Waduk Saguling, sehingga pemanfaatan sumberdaya yang ada dapat dilakukan secara berkelanjutan. Serta sebagai informasi kepada masyarakat apakah ikan nila dan ikan mas hasil budidaya aman untuk dikonsumsi. Limbah (Logam berat) Perairan Kegiatan Budidaya Fitoplankton Zooplankton Ikan Besar Ikan Kecil Faktor alam
Hujan, Gunung meletus, Erosi, Aktivitas manusia
II. TINJAUAN PUSTAKA
2.1. Logam Berat
Logam berat adalah logam yang massa atom relatifnya besar (Sunardi 2004). Menurut Vouk (1986) diacu dalam Martaningtyas (2004), terdapat 80 jenis dari sejumlah 109 unsur kimia yang telah teridentifikasi di muka bumi ini termasuk ke dalam jenis logam berat.
Keberadaan logam berat di muka bumi sangat berperan bagi makhluk hidup. Beberapa logam dibutuhkan dalam tubuh makhluk hidup yang turut mempengaruhi kerja enzim, seperti logam Zn pada enzim karboksipeptidase yang berfungsi dalam pencernaan protein, Cu yang berikatan dengan protein juga mempunyai fungsi dalam pembentukan hemoglobin, kolagen, pembuluh darah pada manusia (Palar 2004). Selain bermanfaat bagi manusia, juga bermanfaat bagi biota air, beberapa logam yang bersifat essensial antara lain Ca, P, Mg, merupakan logam yang berguna untuk pembentukan kutikula atau sisik pada ikan, dan logam Cu, Zn, Mn, dalam jumlah tertentu merupakan logam yang sangat bermanfaat dalam pembentukkan hemosianin dalam sistem darah dan enzimatik pada hewan air (Darmono 1995). Logam berat selain berperan dalam tubuh makhluk hidup juga bermanfaat dalam aktivitas manusia, yang dapat dimanfaatkan sebagai bahan baku maupun sebagai bahan tambahan dalam kegiatan industri (http://www.dnet.net.id 2005).
Pemanfaatan logam dalam aktivitas manusia, dapat membahayakan kehidupan manusia itu sendiri dan lingkungan sekitarnya apabila dalam memanfaatkannya tidak memperhatikan keseimbangan lingkungan, karena kandungan logam berat yang ada di lingkungan dapat terakumulasi dalam tubuh makhluk hidup (Martaningtyas 2004).
2.2. Kandungan Logam Berat dalam Air
Air merupakan senyawa penting dalam kehidupan makhluk hidup. Keberadaan logam berat sebagai zat pencemar dalam perairan akan berpengar uh
terhadap kehidupan yang ada di dalam dan sekitar lingkungan perairan tersebut, karena makhluk hidup tidak akan pernah lepas dalam memanfaatkan air.
Logam-logam dalam perairan keberadaannya berasal dari sumber alamiah dan dari aktivitas yang dilakukan oleh manusia, sumber logam alamiah yang masuk dalam badan perairan bisa berupa pengikisan batu mineral yang banyak bersumber dari perairan, partikel-partikel yang ada di udara yang masuk keperairan dikarenakan terbawa oleh air hujan. Adapun logam yang berasal dari aktivitas manusia berasal dari limbah industri dan limbah rumah tangga (Palar 2004). Pada air tawar yang mengalir (sungai), logam yang terkandung umumnya berasal dari buangan air limbah, erosi, dan dari udara secara langsung (Darmono 1995).
Penyebab utama logam berat menjadi bahan pencemar berbahaya adalah karena sifatnya yang tidak dapat dihancurkan (non degradable) oleh organisme hidup yang ada di lingkungan. Akibatnya, logam-logam tersebut terakumulasi ke lingkungan, terutama mengendap di dasar perairan membentuk senyawa kompleks bersama bahan organik dan anorganik (http://www.dnet.net.id 2005).
Logam berat tembaga (Cu), Seng (Zn), dan timbal (Pb), merupakan beberapa logam yang ada di perairan dan dapat terakumulasi dalam tubuh makhluk hidup.
Tembaga (Cu)
Tembaga dengan nama kimia cuprum dilambangkan dengan Cu. Dalam tabel periodik unsur -unsur kimia, tembaga menempati posisi dengan nomor atom (NA) 29 dan mempunyai bobot atau berat atom (BA) 63,546 (Palar 2004).
Logam Cu digolongkan kedalam kelompok logam penghantar listrik yang terbaik setelah perak, karena itu logam Cu banyak digunakan dalam bidang elektronika dan perlistrikan. Dalam bidang industri lainnya, senyawa Cu juga digunakan pada industri cat, insektisida, dan fungisida (Palar 2004).
Secara alamiah, logam Cu masuk kedalam perairan sebagai akibat peristiwa erosi dan dari udara yang terbawa oleh air hujan. Sedangkan dari aktivitas manusia berasal dari limbah industri.
Logam Cu merupakan logam esensial yang bermafaat dalam pembentukan hae mosianin sistem darah dan enzimatik bagi hewan air (Darmono 1995). Namun,
keberadaanya yang tinggi pada perairan dapat berakibat buruk bagi ikan, seperti menghambat oksidasi asam laktat dalam insang. Konsentrasi Cu dalam badan air bila berada dalam kisaran 2,5-3,0 ppm akan membunuh ikan yang ada di dalamnya (Jackins et al 1970; bryan 1976; dan Reisch et.al 1979 diacu dalam Palar 2004). Apabila ikan yang tercemar logam Cu dikonsumsi oleh manusia akan mengakibatkan pengaruh buruk bagi kesehatan manusia itu se ndiri. Gejala yang timbul pada manusia akibat keracunan akut adalah mual, muntah, sakit perut, hemolisis, metrifisis, kejang dan akhirnya mati. Pada keracunan kronis, logam Cu tertimbun di dalam hati dan menyebabkan hemolisis. Hemolisis terjadi karena tertimbunnya H2O2 dalam sel darah merah sehingga terjadi oksidasi dari lapisan sel, akibatnya sel menjadi pecah (Darmono 1995)
Seng (Zn)
Seng dengan nama kimia zinc dilambangkan dengan Zn. Dalam tabel periodik unsur-unsur kimia, seng menempati posisi dengan nomor atom (NA) 30 dan mempunyai bobot atau berat atom (BA) 65,37.
Banyak aktivitas manusia yang mengakibatkan konsentrasi Zn dalam alam meningkat, seperti industri biji besi dan logam serta industri lain, karena logam Zn dimanfaatkan dalam produksi cat, bahan keramik, gelas, lampu dan pestisida (Darmono 1995). Limbah industri yang mengandung logam Zn di buang ke perairan dalam jumlah banyak, maka akan mencemari perairan tersebut. Bahkan secara biologis logam Zn berasal dari ekskresi manusia dan binatang (Syahminan 1996). Senyawa Zn mempunyai kemampuan melarut yang relatif tinggi, maka logam tersebut tersebar luas di perairan (Llyod 1992 diacu dalam Damaiyanti 1997).
Logam Zn berperan dalam kerja enzim dalam tubuh, tetapi pada konsentrasi tertentu dapat bersifat racun. Pada ikan, saat senyawa Zn masuk ke dalam tubuh melalui insang melebihi kebutuhan, kelebihannya akan dibuang melalui ekskresi yang dikenal dengan purifikasi (Llyod 1992 diacu dalam Damaiyanti 1997), namun jika konsentrasi yang tinggi pada perairan berlangsung lama maka kemungkinan besar logam Zn dapat terakumulasi dalam tubuh ikan tersebut dan proses pengeluaran tidak sebanding dengan konsumsi terhadap logam Zn tersebut. Apabila ikan tersebut dikonsumsi oleh manusia akan terjadi proses
biomagnifikasi melalui rantai makann. Pada manusia, menurut peneliti Child Health di London mengingatkan bahwa seng memiliki efek samping dimungkinkan dapat merusak perkembangan mental anak-anak (http://www. kompas.com 2004).
Timbal (Pb)
Timbal dalam keseharian lebih dikenal timah hitam, dalam bahasa ilmiahnya dinamankan plumbum, dan logam ini disimbolkan dengan Pb. Logam ini termasuk dalam kelompok logam golongan IV-A pada tabel periodik unsur kimia mempunyai nomor atom (NA) 82 dengan bobot atau berat atom (BA) 207,2 (Palar 2004).
Darmono (1995) dan Palar (2004) menjelaskan sifat-sifat timbal sebagai berikut: 1) Merupakan logam yang lunak; 2) Mempunyai titik lebur yang rendah; 3) Merupakan logam yang tahan terhadap peristiwa korosi; 4) bila dicampur dengan logam yang lain membentuk logam campuran yang lebih bagus dari pada logam murninya; 5) Merupakan penghantar listrik yang tidak baik.
Logam Pb dalam perairan berasal dari debu yang mengandung logam Pb yaitu dari hasil pembakaran bensin yang mengandung Pb tetra etil, erosi dan limbah industri (Saeni 1989). Darmono (1995) juga menjelaskan bahwa limbah industri yang mengandung logam Pb, seperti industri kimia, industri percetakan, dan industri yang memproduksi logam, dan cat akan menambah kandungan logam Pb dalam perairan apabila limbah tersebut di buang ke perairan.
Kandungan logam Pb yang tinggi pada perairan juga dapat berakibat buruk pada biota yang ada di dalamnya. Konsentrasi Pb yang mencapai 188 mg/l, dapat membunuh ikan (Palar 2004). Logam Pb yang terdapat pada perairan akan menyebabkan proses bioakumulasi dalam tubuh biota yang ada diperairan, misalnya ikan. Kandungan logam Pb dalam tubuh akan mengganggu aktivitas enzim, seperti asam ä amino levulinat dehidrase (ALAD), Hem sintetase, dan enzim lain yang terlibat dalam sistem hemotopoietik. Ikan yang mengandung Pb apabila dikonsumsi oleh manusia akan berdampak buruk bagi manusi tersebut karena logam Pb yang bersifat akumulatif. Menurut Sunardi (2004), keberadaannya didalam tubuh tidak dapat dikeluarkan lagi sehingga makin lama jumlahnya semakin meningkat dan menumpuk di otak, saraf, jantung, hati, dan
ginjal yang pada akhirnya dapat menimbulkan kerusakan jaringan yang ditempatinya. Dijelaskan pula oleh Wirarni (1997) diacu dalam Novianty (1997), bahwa keracunan logam Pb pada manusia dapat menimbulkan kemandulan, keguguran dan kematian pada bayi. Batas maksimal logam Pb yang boleh masuk pada orang dewasa adalah 2 mg/hari.
2.3. Akumulasi Logam Berat dalam Tubuh Ikan
Simkis (1984) diacu dalam Darmono (1995) mengelompokan logam dalam tubuh sebagai berikut: logam-logam ringan seperti Na, K, Ca, dan Mg merupakan logam berat dalam kelompok A yang keterlibatan ion logamnya dalam makhluk hidup menyangkut proses fisiologis. Logam berat yang dimasukan dalam kelompok B merupakan logam-logam yang terlibat dalam proses-proses enzimatik dan menimbulkan polusi, misalnya Cu, Zn, Cd, Hg, dan Pb. Aktivitas dari logam kelas A masuk ke dalam tubuh hewan biasanya dengan cara difusi membran sel, sedangkan kelas B terikat dengan protein.
Absorpsi logam, selain masuk melalui insang dapat masuk melalui kulit (kutikula) dan lapisan mukosa (Darmono 1995). Faktor yang mempengaruhi toksisitas logam berat dalam perairan terhadap makhluk hidup antara lain, perubahan dalam siklus hidup, umur dan ukuran tubuh, jenis kelamin, pengaruh lapar dan aktivitas, serta kemampuan adaptasi terhadap logam itu sendiri (Bryan 1976 diacu dalam Connell and Miller 1995).
Menurut Simkiss and Mason (1983) diacu dalam Akbar (2002), logam masuk ke dalam jaringan tubuh biota secara umum melalui tiga cara, yaitu:
1. Endositosis dimana pengambilan partikel dari permukaan sel
dengan membentuk wahana perpindahan oleh membran plasma. Proses ini sepertinya berperan dalam pengambilan logam berat dalam bentuk tidak terlarut.
2. Diserap dari air. Sembilan puluh persen kandungan logam
dalam jaringan berasal dari penyerapan oleh sel epitel insang. Insang diduga sebagai organ yang menyerap logam berat dari air.
3. Diserap dari makanan dan sedimen. Penyerapan logam berat dari makanan dan sedimen oleh biota bergantung pada strategi mendapatkan makanan.
Hubungan antara jumlah absorpsi logam dan kandungan logam dalam air biasanya secara proporsional, dimana kenaikan kandungan logam dalam jaringan sesuai dengan kenaikan kandungan logam dalam air. Pada logam-logam esensial kandungannya dalam jaringan biasanya melalui regulasi (diatur pada batas-batas konsentrasi tertentu kandungan logam konstan), tetapi pada logam-logam non esensial kandungan logam tersebut dalam jaringan naik terus sesuai dengan kenaikan konsentrasi logam dalam air lingkungannya (non regulasi) (Darmono 1995).
2.4. Klasifikasi dan Morfologi Ikan Ikan Nila (Oreochromis niloticus)
Ikan nila hidup di perairan yang dalam dan luas maupun di kolam yang sempit dan dangkal, seperti sungai, waduk, rawa, tambak air payau. Ikan nila hidup pada nilai pH berkisar antara 6–8,5 namun pertumbuhannya akan optimal pada pH 7–8 dan pada suhu 25–30 0C (Suyanto 2003).
Ikan nila tergolong ikan pemakan segala (omnivora), seperti : plankton,
alga, crustacea, insecta, dan organisme benthos. Ikan nila memiliki sifat– sifat
unggul, antara lain: efesien dalam pemanfaatan pakan, pertumbuhannya cepat, bergizi tinggi dan dagingnya mirip dengan kakap merah (Suyanto 2003). Klasifikasi ikan nila (Trewavas 1982 diacu dalam Suyanto 2003) :
Filum : Chordata Subfilum : Vertebrata Klass : Osteichthyes Subklass : Acanthoptherygii Ordo : Percomophi Subordo : Percoidea Famili : Cichlidae Genus : Oreochromis
25 cm
Gambar 2 Ikan Nila (Oreochromis niloticus)
Ikan nila (Oreochromis niloticus ) memiliki ciri garis vertikal berwarna gelap pada sirip-sirip ekor, punggung, dan dubur. Bentuk tubuh pipih ke arah vertikal (kompres), mata sedikit menonjol dan cukup besar dengan bagian tepi tubuh berwarna putih, bibir tebal dan biasa disembulkan. Ikan ini memiliki sirip yang lengkap. Posisi sirip ventral terhadap pektoral adalah torasik. Garis linear terputus menjadi dua yaitu atas dan bawah (Suyanto 2003).
Ikan Mas (Cyprinus carpio)
Ikan mas hidup di tempat-tempat dangkal dengan arus yang tidak deras, baik di sungai, danau maupun genangan air lainnya, serta tumbuh optimal pada suhu 20-25 0C dan pH berkisar 7-8. Ikan mas dikenal sebagai pemakan segala, antara lain memakan serangga kecil, siput, cacing, sampah dapur, potongan ikan dan lain-lain (Asmawi 1986).
Ikan mas yang dibudidayakan dengan sistem keramba jaring apung, biasanya hidup pada kedalaman yang lebih dangkal dari pada ikan nila. Pada 1 unit KJA dipasang 2 jaring pada kedalaman yang berbeda pada bagian permukaan ditebar benih ikan mas, dan di bawah jaring ikan mas dipasng jaring untuk penebaran benih ikan nila. Sisa pakan atau pun feses ikan mas dapat dimanfaatkan oleh ikan nila sebagai bahan makanannya.
Klasifikasi ikan mas menurut Weber dan De Beaufort (Saanin 1980) adalah : Filum : Chordate Subfilum : Vertebrata Klass : Pisces Ordo : Ostariophysi Subordo : Cyprinoidea Famili : Cyprinidae Subfamili : Cyprinoinae Genus : Cyprinus
Spesies : Cyprinus carpio
21 cm
Gambar 3 Ikan Mas (Cyprinus carpio)
Ikan Mas (Cyprinus carpio ) mempunyai ciri-ciri badan memanjang dan agak pipih, lipatan mulut dengan bibir yang halus, dua pasang kumis kadang-kadang yang satu diantaranya rudimenter, ukuran dan warna badan sangat beragam (Sumantadinata 1984).
2.5. Waduk Saguling
Waduk Saguling merupakan salah satu dari tiga waduk cascade di Jawa Barat, yang memiliki luas sebesar 5600 Ha (pada elevasi ± 643 m) dengan volume ± 875 juta m3 (http://www.dnet.net.id 2005).
Waduk saguling dibangun pada tahun 1985 sebagai pembangkit listrik. Secara ekologis, Waduk Saguling memiliki fungsi sebagai pengendali banjir dan pengendapan berbagai senyawa dari Sungai Citarum. Senyawa– senyawa dari Sungai Citarum yang masuk ke perairan merupakan limbah yang berasal dari kegiatan manusia, seperti limbah industri, limbah domestik, limbah pertanian dan lainnya.
Waduk Saguling juga dimanfaatkan oleh masyarakat sekitar untuk kegiatan perikanan, seperti penangkapan, pemancingan, dan budidaya dengan sistem Keramba Jaring Apung (KJA). Menurut Darsono (2005) jumlah keramba jaring apung yang terdapat di Waduk Saguling saat ini berjumlah 4000 keramba jaring apung.
2.6. Kualitas Air
Dalam lingkungan perairan bentuk logam antara lain berupa ion-ion bebas, pasangan ion organik, dan ion komplek. Kelarutan logam dalam air dikontrol oleh beberapa parameter fisika dan kimia seperti: suhu, pH, oksigen terlarut dan alkalinitas (Darmono 1995). Se makin tinggi nilai alkalinitas dapat menurunkan toksisitas logam berat seperti tembaga (Cu) sedangkan pada pH yang asam dapat meningkatan pelarutan seng (Zn) dalam air dan toksisitas Zn juga akan meningkat dengan meningkatnya suhu dan menurunnya oksigen terlarut. Begitu juga dengan tembaga (Pb), toksisitas tembaga akan meningkat dengan menurunnya oksigen terlarut (Effendi 2003).
Suhu
Suhu suatu badan air dipengaruhi oleh musim, lintang (latitude), ketinggian dari permukaan laut (altitude), waktu dalam hari, sirkulasi udara, penutupan awan, dan aliran serta kedalaman badan air (Effendi 2003).
Haslam (1995) diacu dalam Effendi (2003) menyatakan bahwa peningkatan suhu menyebabkan penurunan kelarutan gas dalam air, misalnya gas O2, CO2, N2, CH4, dan sebagainya. Selain itu peningkatan suhu juga menyebabkan peningkatan kecepatan metabolisme dan respirasi organisme air yang selanjutnya mengakibatkan peningkatan konsumsi oksigen. Pada peningkatan suhu perairan sebesar 10 0C menyebabkan peningkatan konsumsi
oksigen oleh organisme akuatik sekitar 2-3 kali lipat. Namun, peningkatan suhu ini disertai dengan penurunan kadar oksigen terlarut sehingga keberadaan oksigen seringkali tidak mampu memenuhi kebutuhan oksigen bagi organisme akuatik untuk melakukan proses metabolisme dan respirasi (Effendi 2003). Apabila perairan tercemar oleh logam berat, maka sifat toksisitas dari logam berat terhadap biota air akan semakin meningkat seiring meningkatnya suhu.
pH
Derajat Keasaman (PH) menunjukkan kekuatan antara asam dan basa dalam air, juga dapat diartikan dengan kadar konsenstrasi ion hodrogen dalam larutan (Priyono 1994).
Pescod (1973) menyatakan pH perairan dipengaruhi oleh suhu, fotosintesis, respirasi, oksigen terlarut, dan keberadaan ion-ion dalam perairan tersebut. (Mackereth (1989) diacu dalam Effendi (2003), berpendapat bahwa pH berkaitan erat dengan karbondioksida dan alkalinitas. Semakin tinggi nilai pH semakin tinggi pula alkalinitas dan semakin rendah karbondioksida bebas, bahkan pada pH<5, alkalinitas dapat mencapai nol.
Kelarutan logam dalam air juga dikontrol oleh pH air. Kenaikan pH air akan menurunkan kelarutan logam dalam air, karena kenaikan pH mengubah kestabilkan dari bentuk karbonat menjadi hidroksida yang membentuk ikatan dengan partikel pada badan air sehingga akan mengendap membentuk lumpur. pH juga mempengaruhi toksisitas suatu senyawa kimia, seperti logam berat. Menurut Novotny and Olem (1994) diacu dalam Effendi (2003) menyatakan bahwa toksisitas logam memperlihatkan peningkatan pada pH yang rendah.
Alkalinitas
Alkalinitas atau kebasaan adalah suatu pengukuran terhadap kapasitas suatu badan air untuk menetralkan suatu asam (Priyono 1994).
Penyusun utama alkalinitas dalam perairan tawar terdiri dari kalsium dan magnesium sebagai kation sedangkan anion terdiri dari bikarbonat dan karbonat. Alkalinitas dihasilkan dari karbon dioksida dan air yang dapat melarutkan sedimen batuan karbonat manjadi bikarbonat (Effendi 2003).
Nilai alkalinitas diperairan alami jarang melampaui nilai 500 mg/l CaCO3. Konsenstrasi alkalinitas yang tinggi dalam perairan biasanya berhubungan dalam pembuangan limbah yang masuk ke perairan (Priyono 1994).
Oksigen terlarut (DO)
Oksigen merupakan salah satu gas yang terlarut dalam perairan. Kadar oksigen yang terlarut diperairan dapat berfluktuasi secara harian dan musiman, tergantung pada percampuran (mixing), pergerakan masa air, aktivitas fotosintesis, respirasi dan limbah yang masuk ke badan air (Effendi 2003).
Kebutuhan organisme akuatik terhadap oksigen terlarut sangat tinggi, sehingga kandungan oksigen terlarut yang cukup sangat berarti bagi kehidupan organisme akuatik. Proses dekomposisi bahan organik dan oksidasi bahan anorganik oleh dekomposer dapat mengurangi kadar oksigen terlarut sehingga mencapai nol (anaerob) (Tebbut 1992, diacu dalam Effendi 2003). Konsentrasi oksigen yang aman bagi kehidupan harus berada diatas titik kritis dan tidak terdapat bahan lain yang bersifat racun (Pescod 1973). Proses metabolisme dalam tubuh juga membutuhkan oksigen dalam jumlah banyak dengan meningkatnya suhu perairan.
III. METODE PENELITIAN
3.1. Waktu dan Lokasi Penelitian
Penelitian dilakukan pada bulan Juni-Juli 2005 di Waduk Saguling, Jawa Barat. Analisa kandungan logam berat di dalam organ tubuh ikan dan air dilakukan di Laboratorium Kimia Pusat Penelitian Tanah, Bogor. Analisa kualitas perairan seperti suhu, pH, alkalinitas, dan oksigen terlarut (DO) dilakukan secara insitu.
3.2. Alat, Bahan, dan Kegunaan
Alat yang digunakan dalam penelitian adalah kotak pendingin (cool box) sebagai tempat ikan contoh, botol polietilen sebagai tempat contoh air, alat mengambil air contoh menggunakan Van dorn bottle Sampler, termometer air raksa, pH universal, alat bedah, alat untuk titrasi dalam pengukuran DO dan alkalinitas (pipet, erlenmeyer, gelas ukur), dan alat analisis logam berat yaitu Atomic Absorption Spectrophotometer.
Adapun bahan-bahan yang digunakan dalam penelitian, yaitu bahan untuk titrasi DO dan alkalinitas (MnSO4, H2SO4, KI Alkalis, Na-Thiosulfat, HCl) organ tubuh ikan (daging, hati, dan ginjal), air contoh yang diambil dari lokasi penelitian untuk analisis kandungan logam berat, HNO3 sebagai bahan pengawet contoh air untuk analisa kandungan logam berat.
3.3. Metode Kerja
Penentuan Stasiun Pengambilan Contoh
Stasiun yang dipilih diharapkan dapat mewakili kondisi perairan Waduk Saguling, sehingga pengambilan contoh dilakukan pada empat wilayah, yaitu: DAM, daerah yang terletak lebih dekat ke arah outlet (lokasi air keluar dari waduk) sebagai stasiun 1. Bongas, daerah yang padat kegiatan budidaya dengan sistem keramba jaring apung (stasiun 2). Stasiun 3 yaitu Suka Tengah, daerah ini dimanfaatkan sebagai daerah budidaya meskipun tidak sepadat di Bongas dan
letaknya lebih berdekatan dengan stasiun 4, yaitu Maroko. Maroko. Maroko terletak lebih dekat ke arah inlet (air masuk ke dalam waduk) .
Penentuan stasiun pengambilan contoh ikan dilakukan pada dua stasiun yang merupakan wilayah kegiatan budidaya jaring apung yaitu: Suka Tengah dan Bongas. Masing-masing wilayah dipilih keramba dengan pertimbangan ikan-ikan yang ada di keramba berukuran besar (siap dikonsumsi).
Pengambilan Contoh Air
Pengambilan contoh air dilakukan pada tanggal 13 juni 2005 dan 17 Juli 2005. Contoh air diambil pada kedalaman yang berbeda di tiap stasiunnya, yaitu pada permukaan, kedalaman 4 meter, dan 8 meter. Pada masing-masing
kedalaman dilakukan pengambilan contoh air dengan dua kali ulangan. Contoh air diambil dengan menggunakan Van Dorn bottle sampler. Contoh air dimasukan ke dalam botol polietilen dan diawetkan dengan penambahan HNO3 sampai pH < 2, selanjutnya dianalisa di laboratorium.
Pengambilan Contoh Ikan
Pengambilan contoh ikan dilakukan pada tanggal 13 juni 2005. Pengambilan contoh ikan dilakukan pada dua stasiun (stasiun 2 dan 3), pada masing-masing stasiun dipilih 1 keramba. Di stasiun 2 ikan yang diambil adalah ikan mas dan ikan nila, sedangkan di stasiun 3 hanya ikan nila. Hal ini dikarenakan pada stasiun 3 tidak ditemukan ikan mas berukuran besar. Ikan mas yang diambil berumur kira-kira tiga bulan, sedangkan ikan nila 1-2 minggu lebih tua. Ikan nila dan ikan mas yang dibudidaya, berasal dari benih ikan yang ditebar pada ukuran 5 cm dan pembenihan tidak dilakukan di dalam waduk, melainkan dari kolam pembenihan yang berada dari daerah sekitar waduk. Pengambilan ikan dengan menggunakan serok yang dilakukan oleh nelayan setempat.
Pengambilan Organ Tubuh Ikan
Ikan-ikan yang diambil dari keramba tersebut dibedah dan diambil daging, hati, dan ginjalnya. Organ contoh yang dibutuhkan untuk analisis logam berat seperti daging, hati, dan ginjal diperoleh dari beberapa ikan yang dikumpulkan untuk memenuhi berat minimal yang dibutuhkan untuk analisa (3-5 gram berat basah/organ). Organ contoh tersebut masing-masing dimasukan ke dalam botol film, kemudian dapat diawetkan dengan pembekuan sampai siap dianalisa.
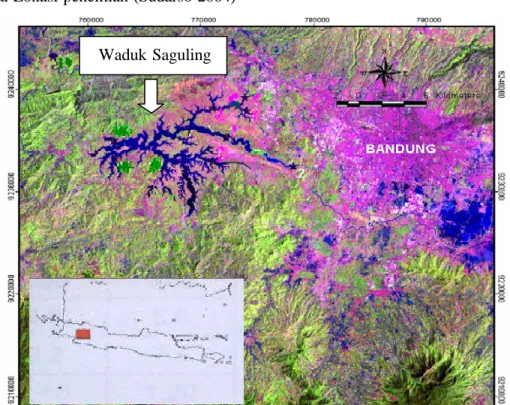
Peta Lokasi penelitian (Sudarso 2004)
Gambar 4 Peta lokasi Waguk Saguling
Denah lokasi stasiun pengamatan di Waduk Saguling (Nuryanto 2001)
Keterangan:
1. DAM 3. Suka tengah 2. Bongas 4. Maroko
Gambar 5 Denah lokasi stasiun pengamatan Waduk Saguling
4
1 3
Perlakuan Contoh Analisa
Pengukuran logam berat pada contoh organ tubuh ikan dan air menggunakan metode AAS (Atomic Absorption Spectrophotometrik ) yang dilakukan di laboratorium. Prinsip dari metode ini berdasarkan pada penguapan larutan sampel, kemudian logam yang terkandung di dalamnya diubah menjadi atom bebas (Darmono 1995) . Prosedur analisa logam berat pada organ ikan ditampilkan pada lampiran 2.
3.4. Analisa Data
Analisa Kandungan Logam Berat
Kandungan logam berat yang terukur dilakukan secara deskriptif, yaitu dengan membandingkan kandungan logam berat dalam air dengan baku mutu air menurut PP. RI No. 82 tahun 2001 tentang pengelolaan kualitas air dan pengendalian pencemaran air kelas III, yaitu air yang peruntukannya dapat digunakan untuk kegiatan budidaya perikanan. Sedangkan kandungan logam berat pada organ tubuh ikan (daging, hati dan ginjal) dibandingkan dengan kandungan maksimum logam berat dalam tubuh ikan pada SK Dirjen POM No. 037/25/B/SKVII/1989 mengenai batas maksimum cemaran logam dalam produk pangan. Nilai baku mutu dari masing-masing logam berat dapat dilihat pada tabel berikut:
Tabel 1 Nilai baku mutu logam berat dalam air dan tubuh ikan Jenis logam
berat
Kandungan Maksimum pada Air
Kandungan maksimum dalam tubuh ikan Tembaga (Cu) 0.02 ppm 20 ppm Seng (Zn) 0.05 ppm 100 ppm Timbal (Pb) 0.03 ppm 0.2 ppm Faktor Konsentrasi
Perbedaan kandungan logam berat pada ikan dan dalam air serta untuk mengetahui tingkat akumulatif logam berat pada organ tubuh ikan, didekati
dengan mencari indeks Faktor Konsentrasi (FK) (Van Esch 1977, diacu dalam Jumariyah 2001):
FK = Kadar logam berat pada ikan (ppm)
Kadar logam berat dalam air (ppm)
Analisa Kualitas Air
Nilai parameter fisika dan kimia yang diukur dibandingkan dengan baku mutu air menurut PP. RI No. 82 tahun 2001 dan hasil studi pustaka dari beberapa sumber. Nilai baku mutu dari parameter yang diukur dan sumbernya dapat dilihat pada tabel berikut:
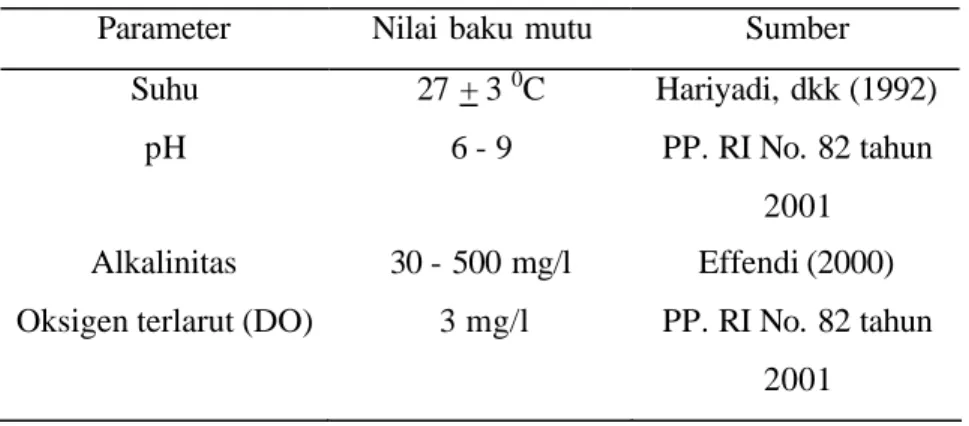
Tabel 2 Nilai baku mutu suhu, pH, DO, dan alkalinitas.
Parameter Nilai baku mutu Sumber
Suhu 27 + 3 0C Hariyadi, dkk (1992)
pH 6 - 9 PP. RI No. 82 tahun
2001
Alkalinitas 30 - 500 mg/l Effendi (2000)
Oksigen terlarut (DO) 3 mg/l PP. RI No. 82 tahun
IV. HASIL DAN PEMBAHASAN
3.1. Logam Berat dalam Air
Kandungan logam berat Cu, Zn, dan Pb pada perairan selain keberadaannya secara alamiah di perairan tersebut, juga tidak terlepas dari aktivitas manusia yang ada di sekitar perairan tersebut. Fluktuasi konsentrasi logam berat dapat dipengaruhi oleh masuknya buangan yang mengandung logam berat, seperti limbah industri, limbah domestik, dan pertanian yang masuk ke perairan, debu yang masuk ke perairan dengan bantuan air hujan, aliran sungai dan angin. Rendahnya kandungan logam berat di perairan dibandingkan dalam tubuh makhluk hidup, dikarenakan kecenderungan dari logam tersebut membentuk senyawa dengan protein jaringan makhluk hidup (Darmono 1995).
Kandungan logam berat Cu, Zn, dan Pb berdasarkan hasil penelitian yang dilakukan pada bulan Juni dan Juli di perairan Waduk Saguling dapat dijelaskan sebagai berikut:
Kandungan Cu dalam Air
Logam Cu merupakan logam yang keberadaannya di perairan dapat secara alami dan dikarenakan adanya aktifitas manusia. Dalam waktu tertentu, kandungan logam Cu dalam perairan akan berfluktuasi, tergantung dari kondisi alam dan buangan dari aktivitas manusia yang mengandung logam Cu yang masuk ke perairan.
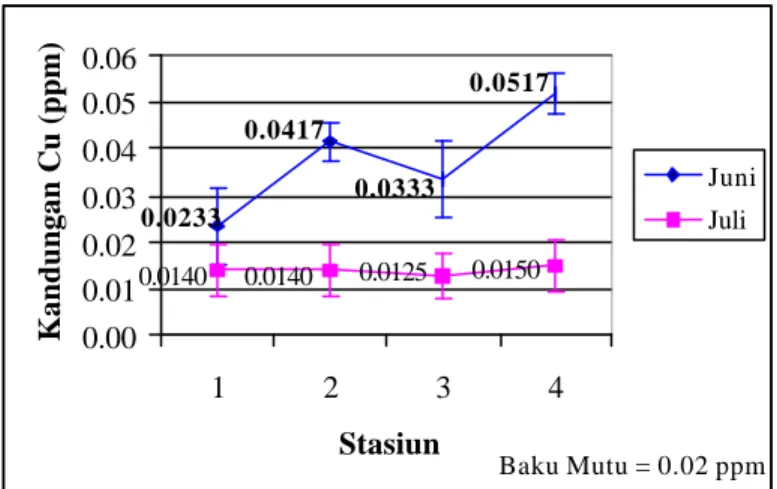
Gambar 6 Grafik kandungan Cu dalam air
0.0233 0.0417 0.0333 0.0517 0.0140 0.0140 0.0125 0.0150 0.00 0.01 0.02 0.03 0.04 0.05 0.06 1 2 3 4 Stasiun Kandungan Cu (ppm) Juni Juli Baku Mutu = 0.02 ppm
Gambar 6 menerangkan sebaran nilai rata-rata kandungan logam berat Cu pada masing-masing stasiun. Kandungan logam berat Cu pada bulan Juni berkisar antara 0,01-0,03 ppm dengan rata-rata 0,023+0,0082 ppm pada stasiun 1, 0,04-0,05 ppm dengan rata -rata 0,0417+0,0041 ppm pada stasiun 2, 0,025-0,03 ppm dengan rata 0,0333+0,0082 ppm pada stasiun 3, 0,05-0,06 ppm dengan rata-rata 0,0517+0,0041 ppm pada stasiun 4. Sedangkan pada bulan Juli berkisar tidak terukur-0,02 ppm dengan rata-rata 0,014+0,0055 ppm pada stasiun 1, tidak terukur-0,02 ppm dengan rata-rata 0,014+0,0055 ppm pada stasiun 2, tidak terukur-0,02 ppm dengan rata-rata 0,0167+0,0050 ppm pada stasiun 3, 0,01-0,02 ppm dengan rata-rata 0,015+0,0055 ppm pada stasiun 4.
Hasil pengamatan kandungan logam berat Cu pada keempat stasiun pengamatan di perairan Waduk Saguling mengalami penurunan pada bulan Juli. Rendahnya kandungan logam berat Cu pada bulan Juli dapat dikarenakan kondisi alam yang berbeda pada saat pengambilan contoh air, yaitu pada bulan Juli curah hujan lebih tinggi dari pada bulan Juni (Lampiran 1). Pada bulan Juli kandungan logam Cu menunjukan sebaran nilai yang tidak berbeda antar stasiun, pengambilan contoh air pada keempat stasiun dilakukan pada hari yang sama dalam cuaca yang cerah.
Pada bulan Juni, di daerah Waduk Saguling sering turun hujan, sehingga tingginya kandungan logam Cu pada bulan Juni diduga adanya pergerakan air. massa air lebih dalam yang lebih banyak mengandung logam Cu naik ke permukaan karena adanya pembalikan massa air. Kandungan Cu juga secara alamiah dapat berasal dari pengikisan dari batu mineral yang banyak di sekitar perairan, partikel-partikel logam yang ada di udara yang masuk ke perairan karena air hujan (Palar 2002).
Tingginya kandungan Cu pada stasiun 4 dikarenakan lokasinya yang lebih dekat dengan aliran Sungai Citarum, yang diduga membawa limbah yang mengandung logam Cu. Selain itu, pengambilan contoh air dilakukan pada hari yang sama dengan stasiun 2, yaitu sore hari sebelum pengambilan contoh air terjadi hujan deras. Sehingga pada stasiun 2 kandungan Cu lebih banyak di bandingkan stasiun 1 dan 3.
Sesuai dengan ketentuan baku mutu yang ditetapkan oleh PP. RI. No. 82 tahun 2001 tentang pengelolaan kualitas air dan pengendalian pencemaran air bahwa baku mutu Cu pada perairan yang diperuntukan pembudidayaan ikan air tawar sebesar 0,02 ppm, maka kandungan Cu pada bulan Juni di masing-masing stasiun sudah melewati baku mutu, pada bulan Juli kondisinya lebih baik. Namun bukan berarti, kondisi kandungan logam berat Cu pada perairan tersebut aman, karena ada kemungkinan peningkatan kandungan Cu secara tiba-tiba.
Kandungan Zn dalam Air
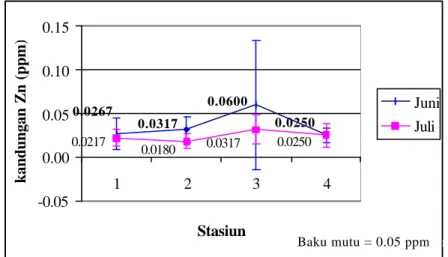
Logam Zn merupakan logam yang ditemukan dalam kerak bumi dalam jumlah lebih banyak dibandingkan logam Cu dan Pb (Stoker and Seager 1979 in Darmono, 1995). 0.0267 0.0317 0.0600 0.0250 0.0217 0.0180 0.0317 0.0250 -0.05 0.00 0.05 0.10 0.15 1 2 3 4 Stasiun kandungan Zn (ppm) Juni Juli
Gambar 7 Grafik kandungan Zn dalam air
Pada gambar 7, kandungan logam Zn pada masing-masing stasiun menunjukan nilai yang tidak berbeda nyata. Kandungan logam berat Zn di masing-masing stasiun pada bulan Juni berkisar 0,01-0,06 ppm dengan rata-rata 0,0267+0,0175 ppm pada stasiun 1, 0,01-0,05 ppm dengan rata-rata 0,0317+0,0147 ppm pada stasiun 2, 0,01-0,08 ppm dengan rata-rata 0,06+0,0735 ppm pada stasiun 3, dan 0,01-0,03 ppm dengan rata-rata 0,025+0,0084 ppm pada stasiun 4. Sedangkan pada bulan Juli berkisar 0,01-0,04 ppm dengan rata -rata 0,0217+0,0098 ppm pada stasiun 1, tidak terukur -0,03 ppm dengan rata-rata 0,018+0,0084 ppm pada stasiun 2, 0,01-0,06 ppm dengan rata-rata 0,0317+0,0160
ppm pada stasiun 3, 0,01-0,05 ppm dengan rata -rata 0,025+0,0138 ppm pada stasiun 4.
Kandungan Zn pun sama dengan kandungan Cu dimana secara umum cenderung mengalami penurunan pada bulan Juli. Keberadaan logam Zn pada stasiun 3 dapat did uga kandungan Zn secara alami di stasiun 3 lebih banyak dibandingkan stasiun lainnya. Hal ini terlihat kandungan Zn pada stasiun 3 cenderung lebih tinggi pada bulan Juni dan Juli. Nilai deviasi yang tinggi pada stasiun 3 diduga karakteristik dari stasiun 3 yang dekat dengan daerah inlet dan pemanfaatannya sebagai daerah budidaya. Keberadaan logam Zn juga sangat dipengaruhi oleh sifat logam Zn yang mudah melarut dalam perairan daripada logam Cu dan Pb.
Sesuai dengan ketentuan baku mutu yang ditetapkan oleh PP. RI No. 82 tahun 2001 tentang pengelolaan kualitas air dan pengendalian pencemaran air bahwa baku mutu Zn pada perairan yang diperuntukan bagi pembudidayaan ikan air tawar sebesar 0,05 ppm, maka kandungan Zn pada masing-masing stasiun belum melewati baku mutu, kecuali pada bulan juni di stasiun 3.
Kandungan Pb dalam Air
Logam Pb merupakan logam yang keberadaannya di bumi sangat sedikit. Pb yang ditemukan dalam kerak bumi berjumlah 12,5 mg/kg (Stoker and Seager 1979, diacu dalam Darmono 1995). Seperti logam Cu dan Zn, logam Pb juga berada dalam perairan dapat terjadi secara alamiah dan juga sebagai dampak dari aktivitas manusia.
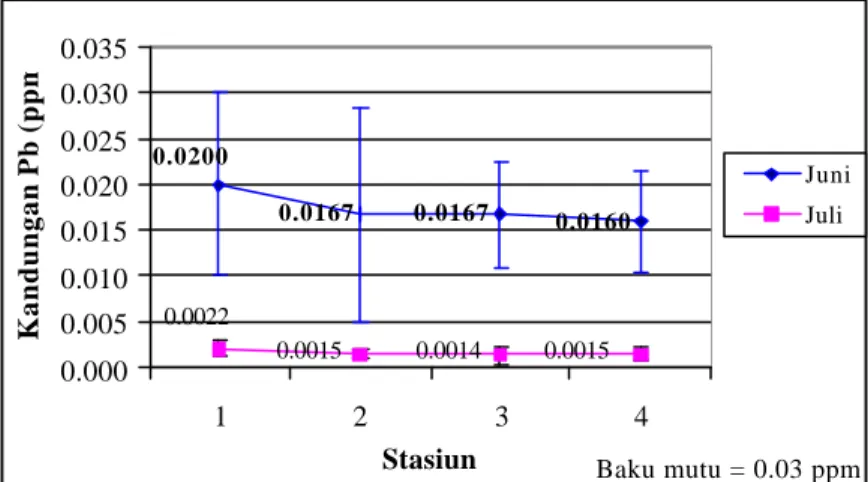
Gambar 8 Grafik kandungan Pb dalam air 0.0200 0.0167 0.0167 0.0160 0.0022 0.0015 0.0014 0.0015 0.000 0.005 0.010 0.015 0.020 0.025 0.030 0.035 1 2 3 4 Stasiun Kandungan Pb (ppm) Juni Juli Baku mutu = 0.03 ppm
Hasil pengukuran kandungan logam Pb, menunjukan perbedaan antara bulan Juni dan Juli. Pada bulan Juli, kandungan logam Pb mengalami penurunan di masing-masing stasiun. Kandungan logam Pb di masing-masing stasiun pada bulan Juni berkisar antara tidak terukur-0,03 ppm dengan rata-rata 0,02+0,01 ppm pada stasiun 1, tidak terukur-0,03 ppm dengan rata -rata 0,0167+0,0115 ppm pada stasiun 2, tidak terukur-0,02 ppm dengan rata-rata 0,0167+0,0058 ppm pada stasiun 3, dan tidak terukur-0,02 ppm dengan rata -rata 0,016+0,0055 ppm pada stasiun 4. Sedangkan pada bulan Juli berkisar 0,001-0,003 ppm dengan rata-rata 0,0022+0,001 ppm pada stasiun 1, 0,001-0,002 ppm dengan rata -rata 0,0015+0,0005 ppm pada stasiun 2, tidak terukur-0,003 ppm dengan rata-rata 0,0014+0,0009 ppm pada stasiun 3, tidak terukur-0,002 ppm dengan rata-rata 0,0015+0,0007 ppm pada stasiun 4.
Kandungan Pb yang terdapat di perairan selain keberadaanya secara alamiah di perairan tersebut, juga dapat berasal dari limbah industri yang mengandung Pb dan dari buangan bahan bakar kendaraan bermotor. Pada stasiun 1 terlihat kandungan Pb yang cenderung lebih besar dari stasiun lainnya, hal ini dapat dikarenakan lokasi stasiun 1 yang paling dekat dengan jalan yang sering dilalui kendaraan bermotor, logam Pb yang berasal dari asap kendaraan bermotor dapat secara alami masuk ke perairan karena adanya angin dan hujan. Namun, secara umum sebaran kandungan logam Pb menunjukan nilai yang tidak berbeda antar stasiun
Kandungan Pb pada masing-masing stasiun tersebut belum melebihi baku mutu yang ditetapkan oleh PP. RI No. 82 tahun 2001 tentang pengelolaan kualitas air dan pengendalian pencemaran air, dimana baku mutu Pb yang ditetapkan pada perairan yang diperuntukan untuk pembudidayaan ikan air tawar sebesar 0,03 ppm.
3.2. Logam Berat pada Ikan Nila dan Ikan Mas
Ikan nila dan ikan mas merupakan jenis ikan pemakan segala (omnivora), artinya selain memakan pelet yang diberikan, ikan nila dan ikan mas juga memakan organisme yang ada seperti fitoplankton, zooplankton, atau ikan kecil yang ada.
Keberadaan logam berat di air menimbulkan terjadinya proses akumulasi di tubuh organisme air. Akumulasi biologis dapat terjadi melalui absorpsi langsung terhadap logam berat yang terdapat dalam air dan melalui rantai makanan. Akumulasi terjadi karena kecenderungan logam berat untuk membentuk senyawa kompleks de ngan zat-zat organik yang terdapat dalam tubuh organisme (Sanusi dkk 1985). Hal ini mengakibatkan kandungan logam berat dalam tubuh organisme akan lebih tinggi dibandingkan dengan logam berat dalam lingkungannya.
Ikan nila dan ikan mas yang menjadi objek penelitian merupakan ikan yang dibudidayakan dalam keramba jaring apung. Masa panen kedua ikan ini sekitar 4-4,5 bulan. Namun, ikan yang diambil untuk penelitian ini adalah ikan yang berusia sekitar 3-3,5 bulan.
Kandungan Cu pada Ikan Nila dan Ikan Mas
Logam Cu merupakan salah satu logam berat yang dibutuhkan dalam tubuh makhluk hidup (logam esensial). Logam berat Cu dan Zn masuk dalam tubuh hewan air dalam bentuk ion. Penyerapan melalui insang dan saluran pencernaan, dan kemudian diangkut oleh darah serta didistribusikan keseluruh tubuh yang memerlukannya (Darmono 1995)
1.3 1.1 4.4 6.2 16.4 13.6 1.6 4.4 11.9
0
5
10
15
20
2
3
Stasiun
Kandungan Cu (ppm)
Daging Nila Hati Nila Ginjal Nila Daging Mas Hati Mas Ginjal MasGambar 9 Grafik kandungan Cu pada organ ikan Baku mutu = 20 ppm
Gambar 10 Grafik faktor konsentrasi Cu
Pada gambar 9, kandungan logam berat Cu bervariasi pada masing-masing organ ikan yang diamati. Ikan dengan jenis yang sama atau pun berbeda yang diambil pada stasiun 2 dan 3, menunjukan perbedaan yang tidak terlalu jauh. Kandungan logam berat Cu paling tinggi terdapat pada ginjal kemudian hati dan dalam jumlah yang paling sedikit terdapat pada daging. Pada gambar 9 menunjukan kandungan logam Cu pada ginjal ikan nila lebih tinggi daripada ginjal ikan mas, sedangkan pada hati dan daging menunjukan nilai yang hampir sama pada stasiun yang sama. Tingginya kandungan logam Cu dalam ginjal, berkaitan dengan fungsi ginjal sebagai penyaring sisa metabolisme dalam tubuh. Logam Cu yang berlebih akan dikeluarkan dari tubuhnya oleh ginjal, selama fungsi ginjal tidak mengalami gangguan akibat dari pengaruh buruk logam berat yang terakumulasi dalam tubuhnya.
Keberadaan logam Cu dalam tubuh ikan nila dan mas belum melebihi nilai maksimum yang diperbolehkan, terlebih lagi kandungan logam Cu dalam daging yang masih rendah. Namun, mengkonsumsi ikan yang sudah tercemar oleh logam berat perlu diwaspadai mengingat sifat dari logam yang dapat terakumulasi dalam organ tubuh jika dikonsumsi dalam jumlah banyak dan relatif lama.
Kemampuan organ tubuh dalam mengakumulasi logam berat ditentukan oleh nilai Faktor Konsentrasi (FK). Semakin tinggi nila i FK pada suatu organ, menunjukan semakin tinggi organ tersebut mengakumulasi logam tersebut. Berdasarkan nilai FK, Van Esch (1977) diacu dalam Sanusi (1985)
31.18 105.6 393.6 38.4 105.6 285.6 33 186 408 0 50 100 150 200 250 300 350 400 450 Daging Nila Hati Nila Ginjal Nila Daging Mas
Hati Mas Ginjal Mas
Daging Nila Hati Nila
Ginjal Nila
St. 2 St. 3
mengelompokan sifat pollutan ke dalam tiga urutan yaitu: sangat akumulatif (FK>1000), akumulatif sedang (FK 100– 1000), dan akumulatif rendah (FK<100).
Pada gambar 8 menunjukan bahwa logam Cu bersifat akumulatif sedang pada hati dan ginjal baik pada ikan nila maupun ikan mas, dan bersifat akumulatif rendah pada daging ikan nila dan ikan mas. Sifat logam yang dapat terakumulasi ini, dapat mengakibatkan biomagnifikasi pada tingkat trofik yang lebih tinggi.
Kandungan Zn pada Ikan Nila dan Ikan Mas
Logam Zn merupakan logam esensial bagi makhluk hidup. Logam Zn seringkali dibutuhkan dalam aktivitas kerja enzim. Kandungan Zn yang tinggi dalam tubuh dapat mengurangi pengaruh buruk dari keberadaan timbal dalam tubuh (Fergusson 1989), tetapi jika keberadaannya melebihi dari kebutuhan dalam tubuhnya akan mempengaruhi fungsi organ yang di tempatinya.
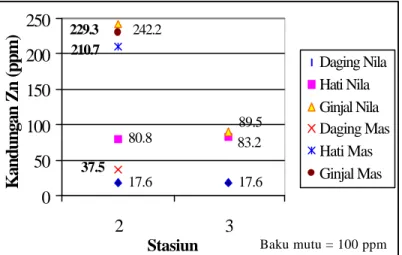
17.6 17.6 80.8 83.2 89.5 242.2 37.5 210.7 229.3
0
50
100
150
200
250
2
3
StasiunKandungan Zn (ppm)
Daging Nila Hati Nila Ginjal Nila Daging Mas Hati Mas Ginjal MasGambar 11 Grafik kandungan Zn pada organ ikan Baku mutu = 100 ppm
Gambar 12 Grafik faktor konsentrasi Zn
Gambar 12 Grafik faktor konsentrasi Zn
Kandungan Zn dalam jaringan tubuh ikan yang dianalisa adalah jauh lebih tinggi daripada logam Cu. Tingginya konsentrasi logam Zn yang terukur dalam organ tubuh diduga sifat logam Zn yang mudah melarut dalam air, sehingga mudah terserap dalam organ tubuh. Kandungan Logam berat Zn sama dengan kandungan logam berat Cu, yaitu kandungan logam berat pada ginjal jauh lebih banyak dari pada kandungan logam berat pada daging dan hati. Hal ini terlihat pada ikan nila dan ikan mas. Tingginya kandungan Zn pada ginjal dikarenakan ginjal merupakan organ yang berfungsi menyaring sisa metabolisme yang pada akhirnya sisa metabolisme tersebut akan dikeluarkan dari dalam tubuhnya.
Pada gambar 10, nilai FK untuk logam Zn menunjukan bahwa logam Zn bersifat sangat akumulatif hampir pada semua organ tubuh ikan yang diamati, kecuali pada daging ikan nila yang bersifat akumulatif sedang. Pada hati ikan mas, logam Zn lebih tinggi nilai faktor konsentrasinya dibandingkan pada hati ikan nila, hal ini diduga kemampuan ikan mas dalam mengeliminir logam Zn lebih rendah dari pada ikan nila. Selain itu pengaruh pakan juga mempengaruhi, pakan ikan mas seluruhnya berasal dari pellet, yang diduga pellet tersebut mengandung logam Zn yang tinggi. Perbedaan tingkat akumulasi pada organ yang berbeda dan pada spesies yang berbeda antara logam Cu dan Zn dipengaruhi oleh beberapa hal, yaitu: spesies, jenis organ, jenis polutan, dan besarnya kadar pollutan dalam air (Gipps and Collee 1980, diacu dalam Sanusi 1985).
555.21 2551.58 7648.42 1184.21 6653.687241.05 293.33 1491.67 1386.67 0 1000 2000 3000 4000 5000 6000 7000 8000 9000 Daging Nila Hati Nila Ginjal Nila Daging Mas
Hati Mas Ginjal Mas
Daging Nila Hati Nila
Ginjal Nila
St. 2 St. 3
Kandungan Pb pada Ikan Nila dan Ikan Mas
Berbeda dengan Zn dan Cu, logam Pb merupakan logam nonesensial yang keberadaanya dalam tubuh makhluk hidup dapat dikatakan tidak diharapkan. Keberadaan logam Pb dalam tubuh seringkali menggantikan logam esensial dalam aktivitas kerja enzim dan bersifat menghambat kerja enzim (Palar 2004). Sebagaimana yang dinyatakan oleh Fergusson (1989) ba hwa kandungan Pb yang tinggi dapat menurunkan kandungan Cu dalam tubuh.
0.48 0.86 0.88 0.91 0.86 0.95 0.48 1.97 0.48 0 0.5 1 1.5 2 2.5 2 3 Stasiun Kandungan Pb (ppm) Daging Nila Hati Nila Ginjal Nila Daging Mas Hati Mas Ginjal Mas
Gambar 13 Grafik kandungan Pb pada organ ikan
Gambar 14 Grafik faktor konsentrasi Pb
Pada pengukuran kandungan Pb, nilai kandungan Pb jauh lebih rendah dari pada Cu dan Zn baik yang ada dalam air maupun pada organ ikan yang
Baku mutu = 0.2 ppm 52.69 56.89 28.74 117.96 28.74 28.74 54.49 51.50 51.50 0 20 40 60 80 100 120 140 Daging Nila Hati Nila Ginjal Nila Daging Mas
Hati Mas Ginjal Mas
Daging Nila Hati Nila
Ginjal Nila
St. 2 St. 3
diamati. Berbeda dengan pengukuran kandungan Cu dan Zn, pada pengukuran kandungan Pb terlihat kandungan Pb pada hati ikan mas terlihat paling tinggi dari pada organ lainnya, sedangkan ginjal dan daging ikan mas memiliki konsentrasi yang sama. Tingginya konsentrasi Pb dihati berkaitan dengan peran hati yang terlibat dalam metabolisme zat makanan serta sebagian besar toksikan, dihati ini toksikan akan mengalami detoksifikasi. Apabila logam Pb terkandung pada organ hati dalam waktu lama dapat menyebabkan kerusakan hati seperti kematian sel hati (nekrosis). Pada ikan nila, kandungan Pb pada ginjal lebih tinggi dari pada hati dan terendah terkandung pada daging. Hal ini menunjukan perbedaan kemampuan organ tubuh dan jenis ikan dalam mengakumulasi logam berat Pb.
Berdasarkan nilai FK pada gambar 12, logam Pb bersifat akumulatif rendah pada hampir semua organ ikan, kecuali pada organ hati ikan mas bersifat akumulatif sedang. Tinggin ya logam Pb yang terakumulasi pada hati ikan mas di duga keberadaan ikan mas yang hidup pada kedalaman yang lebih dangkal dari ikan nila. Buangan bahan bakar yang mengandung logam Pb dari perahu yang menjadi alat transportasi dalam waduk dapat meningkatkan logam Pb terakumulasi dalam organ ikan mas. Sifat Pb yang sulit untuk diekskresikan, mengakibatkan organ ini terakumulasi pada organ hati. Tingkat akumulatif yang lebih tinggi pada hati ikan mas juga terlihat secara morfologi. Pada ukuran yang sama, ukuran hati ikan mas lebih besar dari ikan nila, ada kemungkinan besarnya ukuran tersebut dikarenakan hati ikan mas lebih banyak berkontraksi sebagai upaya untuk mengeliminir logam Pb yang terkandung di dalamnya. Upaya mengeluarkan logam Pb dari tubuhnya, karena logam ini bersifar racun bagi makhluk hidup (Darmono 1995).
Hasil pengukuran menunjukan bahwa kandungan logam berat pada organ ikan dengan jenis ikan yang berbeda, terlihat perbedaan kemampuan mengakumulasi logam berat yang ada di perairan. Pada ikan nila, untuk logam berat Cu, Zn, dan Pb lebih banyak terakumulasi pada ginjal. Sedangkan ikan mas, untuk logam berat Cu dan Zn pada ginjal namun untuk Pb pada hati.
3.3. Kualitas Perairan
Aktivitas manusia dan pengaruh alam akan mempengaruhi kondisi kua litas perairan. Pengukuran beberapa parameter kualitas air dilakukan untuk mengetahui kondisi perairan pada masing-masing stasiun dan pengaruhnya terhadap toksisitas logam berat. Beberapa parameter yang berpengaruh pada kandungan dan toksisitas logam berat antara lain suhu, pH, alkalinitas dan Oksigen terlarut.
Suhu
Suhu merupakan faktor penting dalam lingkungan perairan. Suhu yang tinggi dapat berpengaruh terhadap beberapa proses kimia yang terjadi di perairan, misalnya respirasi dan fotosintesa. Dengan suhu yang semakin tinggi sampai batas-batas tertentu proses fotosintesa akan semakin aktif. Suhu mempunyai pengaruh yang penting terhadap proses kehidupan ikan seperti nafsu makan, pernafasan, reproduksi dan pertumbuhan. Cahaya matahari yang masuk ke perairan mengalami penyerapan dan berubah menjadi energi panas, proses penyerapan cahaya ini berlangsung lebih intensif pada lapisan bagian atas perairan sehingga lapisan ini akan lebih panas dan mempunyai densitas yang lebih kecil dari lapisan bawahnya. Kondisi ini mengakibatkan terjadinya stratifikasi panas pada kolom air. Selain itu peningkatan suhu juga menyebabkan penurunan kelarutan gas dalam air, salah satunya gas O2 (Effendi 2000).
27.5 27 28 28 25.63 25.83 26.75 26.33
24
25
26
27
28
29
30
1
2
3
4
Stasiun
Suhu (
oC)
Juni JuliGambar 15 Grafik suhu air
Hasil pengukuran suhu pada masing-masing stasiun pada bulan Juni berkisar antara 26,5-28 0C dengan rata-rata 27,5+0,6325 0C pada stasiun 1, 26-28
0C dengan rata -rata 27+0,8944 0C pada stasiun 2, 27-29 0C dengan rata -rata
28+0,8944 0C pada stasiun 3 dan stasiun 4. Sedangkan pada bulan Juli suhu lebih rendah dibanding pada bulan Juni, dimana pada stasiun 1 berkisar 24,5-27,4 0C dengan rata-rata 25,63+1,3866 0C, 25-26 0C dengan rata-rata 25,8333 + 0,4082 0C pada stasiun 2, 26-28 0C dengan rata-rata 26,75+0,9874 0C pada stasiun 3 dan 25,5– 27,5 0C dengan rata-rata 26,3333 + 0,9309 0C pada stasiun 4.
Kisaran suhu pada masing-masing stasiun cukup baik untuk pertumbuhan ikan, yaitu pada stasiun 2 dan stasiun 3 wilayah tersebut banyak dimanfaatkan sebagai daerah budidaya ikan. Sebaran suhu selama penelitian tidak menunjukan perbedaan yang terlalu jauh antara stasiun yang ada kegiatan budidaya dan stasiun yang tidak ada kegiatan budidaya, artinya jumlah cahaya yang masuk ke perairan menyebar merata pada masing-masing stasiun. Namun, jika dilihat dari kedalaman 0, 4 m, dan 8 m (lampiran 7) memperlihatkan nilai yang semakin menurun pada perairan yang lebih dalam. Hal ini dikarenakan cahaya yang masuk ke perairan lebih rendah. Sebaran suhu pada masing-masing stasiun maupun pada kedalaman yang berbe da, memperlihatkan nilai suhu yang layak untuk kegiatan perikanan. Nilai suhu yang masih baik untuk kegiatan perikanan dapat mengurangi pengaruh negatif dari sifat logam terhadap biota air yang ada dalam perairan tersebut, khususnya ikan. Hal ini dikarenakan proses metabolisme tidak mengalami gangguan.
pH
pH merupakan parameter yang menyatakan kandungan hidrogen yang larut dalam air. pH dapat mempengaruhi kandungan unsur ataupun senyawa kimia yang terdapat di perairan, diantaranya mempengaruhi kandungan logam berat yang ada di perairan. Menurut Palar (2004), toksisitas logam berat juga dipengaruhi oleh perubahan pH, toksisitas dari logam berat akan meningkat bila terjadi penurunan pH.
7.67 7.67 7.50 6.83 8.00 7.50 7.50 8.42
6
7
8
9
10
1
2
3
4
Stasiun
pH
Juni Juli Gambar 16 Grafik pHPada bulan Juni pH berkisar antara 7-8 dengan rata-rata 7,5+0,4472 pada stasiun 1, 6,5-7 dengan rata 6,83+0,2582 pada stasiun 2, 7– 8,5 dengan rata-rata 7,6667+0,6831 pada stasiun 3, 7-8,5 dengan rata-rata -rata-rata 7,6667+0,6831 pada stasiun 4. Sedangkan pada bulan Juli nilai pH rata -rata 7,5+0 pada stasiun 1 dan stasiun 2, pada stasiun 3 berkisar antara 7,5-9 dengan rata -rata 8,4167+0,7360 dan 7,5-8,5 dengan rata-rata 8+0,4472 pada stasiun 4.
Hasil pengkuran pH pada masing-masing stasiun tidak terlihat perbedaan yang terla lu besar antara pengukuran pada bulan Juni dan bulan Juli. Pada stasiun 2 memiliki pH yang lebih rendah dibandingkan stasiun lainnya. Kegiatan budidaya yang padat pada stasiun 2 diduga mempengaruhi keasaman perairan yang diakibatkan adanya proses dekomposisi bahan-bahan organik yang berasal dari sisa pelet dan sisa metabolisme yang dapat meningkatkan keasaman perairan. Pada kedalaman yang berbeda, nilai pH menunjukan penurunan pada perairan yang lebih dalam, kondisi ini terdapat pada masing-masing stasiun. Penurunan nilai pH pada perairan yang lebih dalam diakibatkan pada perairan yang lebih dalam kandungan oksigen semakin rendah sehingga menurunkan nilai pH.
Kondisi pH pada masing-masing stasiun masih berada dalam kisaran normal 6-9 untuk kehidupan biota dan budidaya ikan menurut PP. RI no. 82 tahun 2001, nilai pH yang masih berada dalam kisaran tersebut diduga tidak mempengaruhi sifat toksisitas dari logam berat.
Alkalinitas
Alkalinitas adalah gambaran kapasitas air untuk menetralkan asam dikenal dengan sebutan acid-neutralizing capacity (ANC), alkalinitas juga diartikan sebagai kapasitas penyangga (buffer capacity ) terhadap perubahan pH perairan (Effendi 2000). 88.69 98.5433 119.8567 126.6933 92.2063 101.3565 111.2106 115.4338 60 80 100 120 140 160 1 2 3 4 Stasiun Alkalinitas (mg/l CaCO 3 ) Juni Juli
Gambar 17 Grafik Alkalinitas
Hasil pengukuran alkalinitas pada masing-masing stasiun diperoleh nilai dengan hasil pengukuran pada bulan Juni cenderung lebih tinggi dibanding pada bulan Juli. Pada bulan Juni nilai alkalinitas rata -rata 88,69 mg/l CaCO3 pada stasiun 1, pada stasiun 2 berkisar antara 80,24-122,92 mg/l CaCO3 dengan rata-rata 98,5433+19,3816 mg/l CaCO3, pada stasiun 3 berkisar antara 97,73-152,04 mg/l CaCO3 dengan rata -rata 119,8567+25,5068 mg/l CaCO3, dan pada stasiun 4 berkisar antara 105,58-160,48 mg/l CaCO3 dengan rata-rata 126,6933+26,4418 mg/l CaCO3. Sedangkan pada bulan Juli berkisar antara 76,02-118,25 mg/l dengan rata-rata 92,2068+14,4866 mg/l CaCO3 pada stasiun 1, 80,24-114,03 mg/l CaCO3 dengan rata-rata 101,3565+12,5280 mg/l CaCO3 pada stasiun 2, 84,46-152,03 mg/l CaCO3 dengan rata-rata 111,2106+30,9956 mg/l CaCO3 pada stasiun 3, dan 92,91-135,14 mg/l CaCO3 dengan rata-rata 115,4338+20,6318 mg/l CaCO3 pada stasiun 4.
Pada gambar 17, alkalinitas pada masing-masing stasiun menunjukan nilai yang tidak berbeda pada bulan Juni maupun Juli. Namun, dari grafik tersebut menunjukan adanya kecenderungan bahwa semakin mendekati inlet maka
alkalinitas semakin tinggi. Hal ini dikarenakan alkalinitas dipengaruhi oleh buangan yang masuk ke perairan sebagai akibat dari aktivitas manusia maupun faktor alam.
Jika dilihat berdasarkan kedalaman, pada masing-masing stasiun secara umum menunjukan bahwa semakin dalam nilai alkalinitas semakin tinggi, dikarenakan adanya kecenderungan partikel-partikel zat untuk bergerak ke bagian lebih bawah.
Nilai alkalinitas pada tiap stasiun dan pada kedalaman yang berbeda dengan nilai standar devisiasi yang tinggi menunjukan nilai yang beragam. Meskipun demikian, perbedaan nilai alkalinitas masih mencerminkan kondisi perairan yang masih layak untuk kegiatan perikanan. Sebaga imana Effendi (2000) menyatakan bahwa nilai alkalinitas di perairan berkisar antara 5 hingga ratusan mg/l CaCO3, dan nilai alkalinitas yang baik berkisar antara 30-500 mg/l CaCO3.
Kandungan oksigen terlarut
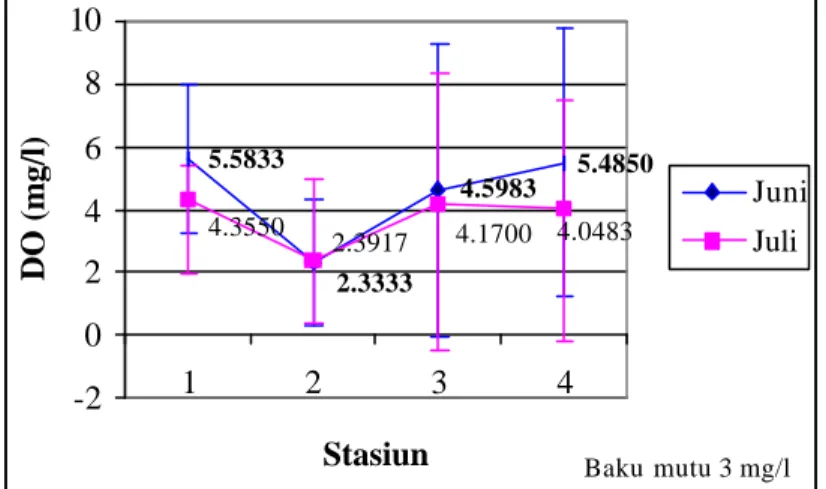
Oksigen terlarut berasal dari difusi oksigen yang terdapat di udara dan hasil fotosintesis oleh tumbuhan air dan fitoplankton. Kelarutan oksigen juga di pengaruhi oleh suhu, yaitu akan mengalami penurunan pada suhu yang meningkat. Oksigen terlarut sangat dibutuhkan oleh semua biota air, yaitu untuk respirasi, aktifitas biota air, dan penguraian bahan organik oleh bakteri dekomposer. 5.5833 4.5983 2.3333 5.4850 4.0483 4.1700 2.3917 4.3550 -2 0 2 4 6 8 10 1 2 3 4 Stasiun DO (mg/l) Juni Juli
Gambar 18 Grafik oksigen terlarut (DO)
Dari hasil pengukuran pada bulan Juni cenderung lebih tinggi dibanding pada bulan Juli. Dimana pada bulan Juni nilai oksigen terlarut berkisar antara 2,58-7,73 mg/l dengan rata-rata 5,5833+2,3995 mg/l pada stasiun 1, 0-4,42 mg/l dengan rata-rata 2,3333+1,9859 mg/l pada stasiun 2, 0-10,3 mg/l dengan rata-rata 4,5987+4,6864 mg/l pada stasiun 3, dan 0,74-10,3 mg/l dengan rata-rata 5,485+4,2762 mg/l pada stasiun 4. Sedangkan pada bulan Juli berkisar antara 2,94-5,89 mg/l dengan rata -rata 4,355+1,0529 mg/l pada stasiun 1, 0-6,62 mg/l dengan rata-rata 2,3917+2,5565 mg/l pada stasiun 2, 0-9,57 mg/l dengan rata-rata 4,17+4,1745 mg/l pada stasiun 3, dan 0-7,73 mg/l dengan rata-rata 4,0483+3,4051 mg/l pada stasiun 4.
Kandungan oksigen masing-masing stasiun menunjukan sebaran nilai rata–rata yang tidak begitu berbeda antarstasiun baik pada bulan Juni maupun Juli. Nilai standar deviasi yang tinggi pada stasiun 2, 3, dan 4, menjelaskan kondisi yang rawan bagi ikan. Pada lampiran 7 terlihat bahwa pada kedalaman 8 meter sudah tidak terdapat kandungan oksigen terlarut, artinya pada kedalaman 8 meter sudah tidak layak bagi kehidupan ikan budidaya.
Berdasarkan nilai rata -ratanya, umumnya kandungan oksigen terlarut masih memenuhi batas minimum yang ditetapkan dalam PP. RI No. 82 tahun 2001 yaitu 3 mg/l, kecuali pada stasiun 2. Pada stasiun 2 kandungan oksigen terlarut baik pada bulan Juni maupun pa da bulan Juli berada dibawah 3 mg/l. Hal ini dikarenakan pada stasiun 2 merupakan daerah budidaya dengan jumlah keramba lebih banyak dibanding pada stasiun 3, yang menunjukan pemanfaatan oksigen oleh ikan jauh lebih banyak, sehingga oksigen terlarut yang terukur jumlahnya lebih sedikit. Nilai yang relatif rendah ini dapat mempengaruhi toksisitas logam berat terhadap ikan yang bermula dari terganggunga proses metabolisme dan respirasi ikan tersebut.
4.4. Usulan Upaya Pengelolaan Waduk Saguling
Kondisi Waduk Saguling yang rentan akan masuknya zat pencemar, akan mengakibatkan dampak yang merugikan bagi pihak terkait. Salah satu usaha pengelolaan Waduk Saguling yang dapat dilakukan adalah pengendalian pencemaran. Upaya pengendalian pencemaran yang dilakukan bertujuan agar