Halaman 1 dari 12
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS ANDALAS
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA
RENCANA PROGRAM DAN KEGIATAN PEMBELAJARAN SEMESTER (RPKPS) Mata
Kuliah : KIMIA ANORGANIK I Dosen : 1. Dra. Rahmayeni, MS 2. Dr. Syukri 3. Prof. Dr. Syukri Arief 4. Prof. Dr. Novesar Jamarun 5. Dr. Zulhadjri 6. Dr. Upita Septiani 7. Dr. Yetria Rilda 8. Admi, MSi
Kode/sks : PAK 251/3 SKS Status : Wajib
Prasyarat : Telah mengikuti mata kuliah Kimia Dasar I dan II
Universitas : Andalas Jurusan : Kimia
Fakultas : FMIPA Prodi : Kimia
Semester : Kimia
KOMPETENSI:
1. Mahasiswa memiliki kemampuan pengetahuan, pemahaman dan penerapan tentang struktur atom, mekanika gelombang, energi orbital, sistim periodik, sifat keperiodikan, term simbol, ikatan kimia (konsep Lewis, teori VSEPR, ikatan kovalen, energi ikatan, hibridisasi, teori orbital molekul,) dan struktur molekul
2. Mahasiswa memiliki kemampuan pengetahuan, pemahaman dan penerapan tentang simetri molekul (operasi simetri dan unsur-unsur simetri), struktur dan ikatan senyawa kompleks koordinasi dan struktur zat padat ionik.
POKOK BAHASAN 1. Struktur Atom
2. Sistim Periodik dan sifat Keperiodikan 3. Ikatan Kimia dan Struktur Molekul 4. Simetri Molekul
Halaman 2 dari 12 (1) (2) (3) (4) (5) (6) MING GU KE KEMAMPUAN AKHIR YANG DIHARAPKAN (KOMPETENSI) BAHAN KAJIAN BENTUK PEMBELAJA RAN KRITERIA PENILAIA N (INDIKAT OR) BOBO T NILAI (%) 1. 1. Mengetahui rencana pembelajaran dan pembagian tugas 2x50 menit
2. Mampu menjelaskan latar belakang dan
perkembangan teori atom yang telah dipelajari pada mata kuliah prasyarat 3. Mampu menjelaskan teori
atom Borh dan menurunkan perumusannya 1x50 menit
4. Mampu menjelaskan dualisme sifat partikel dan gelombang
5. Mampu menjelaskan kenapa posisi dan momentum partikel tak dapat ditentukan secara tepat (Prinsip ketidak pastian Heisenberg)
Rencana Pembelajaran
Perkembangan teori atom
Teori atom Borh
Mekanika gelombang, Penjelasan rencana pembelajaran dan materi pokok Pendahuluan dan umpan balik Presentasi Dosen, diskusi dan umpan balik Pekerjaan rumah dan kuiz 2% 2. 2x50 menit 1. Mampu menjelaskan penggunaan persamaan Schrodinger untuk sistim atom dengan satu
elektron
2. Mampu menjelaskan Penggunaan fungsi gelombang radial dan sudut untuk orbital atom
Persamaan Schrodinger
Fungsi gelombang radial dan sudut serta orbital
Presentasi Dosen dan umpan balik
Halaman 3 dari 12
serta dapat
menggambarkan orbital-orbital atom
3. Mampu menentukan energi orbital untuk sistim dengan satu elektron 1x50 menit
4. Mampu menjelaskan penggunaan persamaan Schrodinger untuk sistim atom dengan elektron lebih dari satu
molekul Energi Orbital Untuk Sistem Satu elektron Sistem atom dengan banyak elektron 3. 2x50 menit 1. Mampu menjelaskan tingkat energi orbital-orbital atom
2. Dapat membuat
konfigurasi elektron dari atom-atom dengan benar 1x50 menit
3. Dapat menentukan term simbol untuk elektron yang berada pada orbital tertentu Tingkat energi orbital Konfigurasi Elektron Term Simbol Presentasi Dosen, diskusi dan umpan balik Pekerjaan rumah dan kuiz 2% 4. 2x50 menit 1. Mampu menjelaskan penggolongan unsur dan kegunaan sistim periodik 2. Mampu menjelaskan
kecendrungan energi ionisasi , Afinitas elektron dan keelektronegatifan dalam sistim periodik dan penyimpangan-penyimpangan dari keteraturan Penggolongan unsur Sifat-sifat keperiodikan Presentasi Dosen, diskusi dan umpan balik Pekerjaan rumah atau kuiz 1% 5. 2x50 menit
Halaman 4 dari 12
kecendrungan jari-jari atom dalam sistim
periodik, penentuan efek shielding terhadap jari-jari atom dan muatan formal 1x50 menit
2. Mampu menjelaskan kecendrungan sifat magnit dari unsur-unsur dalam sistim periodik
dan efek shielding Sifat magnit Dosen dan umpan balik rumah dan kuiz 6. 2x50 menit 1. Mampu menjelaskan bagaimana zat padat ionik terbentuk melalui Ikatan ion
2. Mampu menjelaskan konsep Lewis dalam menentukan struktur molekul ion dan kovalen 3. Mampu membuat
struktur molekul berdasarkan konsep Lewis dan yang melanggar atruran ketentuan
4. Mampu menjelaskan pembentukan ikatan rangkap dan energi ikatan 1x50 menit
5. Mampu menentukan muatan formal atom-atom dalam molekul dan
struktur yang stabil berdasarkan muatan formal dan resonansi
Ikatan Ion Konsep dan aturan Lewis Struktur molekul Ikatan rangkap dan energi ikatan Muatan formal dan resonansi Presentasi Dosen dan umpan balik Pekerjaan rumah dan kuiz 2% 7. 2x50 menit 1. Mampu menggambarkan
ikatan dalam molekul- Teori Ikatan valensi,
Presentasi Dosen dan
Pekerjaan rumah
Halaman 5 dari 12
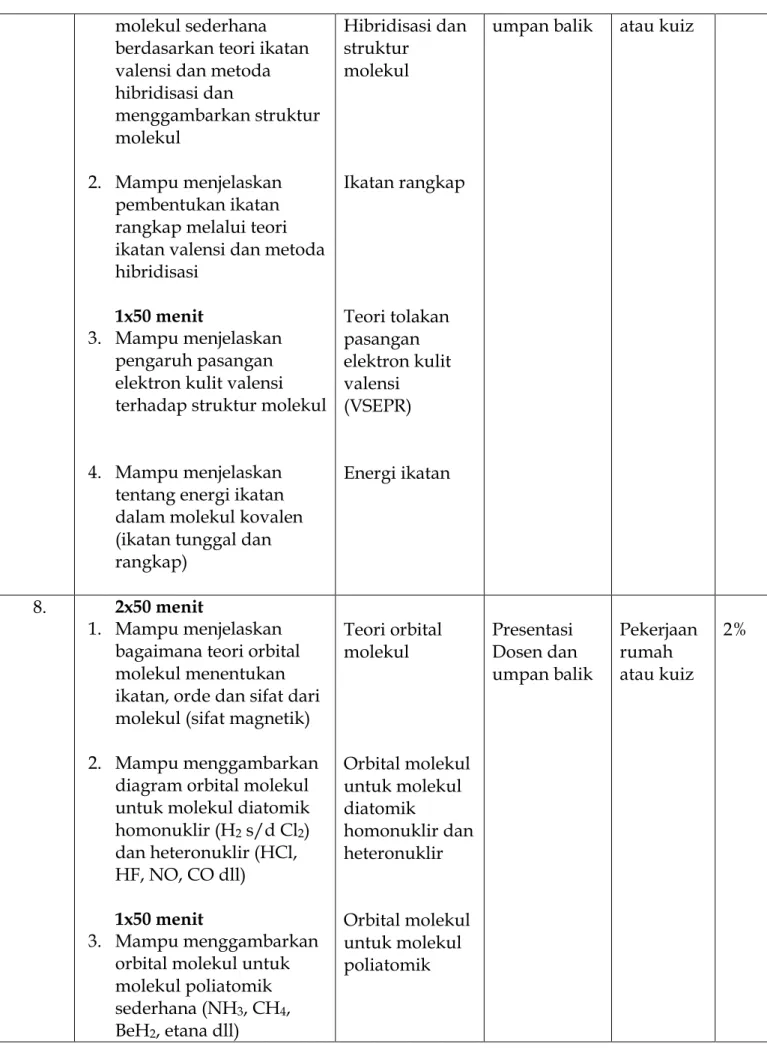
molekul sederhana berdasarkan teori ikatan valensi dan metoda hibridisasi dan
menggambarkan struktur molekul
2. Mampu menjelaskan pembentukan ikatan rangkap melalui teori ikatan valensi dan metoda hibridisasi
1x50 menit
3. Mampu menjelaskan pengaruh pasangan elektron kulit valensi terhadap struktur molekul 4. Mampu menjelaskan
tentang energi ikatan dalam molekul kovalen (ikatan tunggal dan rangkap) Hibridisasi dan struktur molekul Ikatan rangkap Teori tolakan pasangan elektron kulit valensi (VSEPR) Energi ikatan
umpan balik atau kuiz
8. 2x50 menit
1. Mampu menjelaskan bagaimana teori orbital molekul menentukan ikatan, orde dan sifat dari molekul (sifat magnetik) 2. Mampu menggambarkan
diagram orbital molekul untuk molekul diatomik homonuklir (H2 s/d Cl2) dan heteronuklir (HCl, HF, NO, CO dll)
1x50 menit
Halaman 6 dari 12 9.
U J I A N M I D S E M E S T E R
10. 2x50 menit
1. Mampu menjelaskan tentang simetri molekul 2. Mampu menjelaskan
tentang operasi simetri dan unsur-unsur simetri molekul (rotasi, refleksi, inversi, rotasi-refleksi, identitas)
1x50 menit
3. Mampu menentukan Point group dari molekul-molekul dan tabel
karakter
4. Mampu menjelaskan hubungan simetri molekul dengan sifat kepolarannya
Operasi simetri dan unsur unsur simetri
Point group dan tabel karakter Kepolaran molekul Presentasi Dosen, peragaan dan umpan balik Pekerjaan rumah atau kuiz 2% 11. 2x50 menit
1. Mampu menjelaskan apa itu senyawa komplek dan penemuannya
2. Mampu menjelaskan teori rantai
Blomstram-Jorgensen dalam meramalkan struktur CoCl3.6NH3
3. Mampu menjelaskan teori koordinasi Werner dalam meramalkan struktur CoCl3.6NH3
1x 50 menit
Halaman 7 dari 12
12. 2x50 menit
1. Mampu menjelaskan bagaimana teori ikatan valensi (cara Pauling) dalam menerangkan struktur dan ikatan senyawa koordinasi (kompleks oktahedral, dan tetrahedral)
1x50 menit
2. Mampu menjelaskan bagaimana teori ikatan valensi (cara Pauling) dalam menerangkan struktur dan ikatan senyawa koordinasi (segiempat datar, segitiga bipiramid) Teori ikatan valensi untuk senyawa koordinasi Presentasi Dosen, diskusi dan umpan balik 2% 13. 2x 50 menit 1. Mampu menjelaskan bagaimana teori medan kristal dalam
menerangkan struktur dan ikatan senyawa koordinasi (Oktahedral, tetrahedral, segiempat datar dan tetra hedral) 2. Mampu menjelaskan
perubahan medan oktahedral menjadi segiempat datar (untuk kompleks Cu(NH3)4+2 ) dan efek Janh Teller 3. Mampu menentukan
energi kestabilan medan kristal untuk kompleks oktahedral, tetrahedral (medan kuat dan lemah) 1x50 menit
4. Mampu menjelaskan
Teori medan kristal
Efek Jahn Teller
Halaman 8 dari 12
faktor-faktor yang mempengaruhi energi pembelahan medan kristal (sifat ligan, muatan atom pusat, jenis orbital d, jenis ligan)
5. Mampu menjelaskan kelebihan teori medan kristal dalam menjelaskan warna2 senyawa
koordinasi keterbatasan dari teori tersebut
yang mem- pengaruhi pembelahan medan kristal Kelemahan teori medan kristal 14. 2x50 menit 3. Mampu menjelaskan bagaimana teori orbital molekul menerangkan struktur dan ikatan senyawa kompleks koordinasi melalui overlap orbital-orbital atom
4. Mampu membuat diagram orbital molekul kompleks Oktahedral, bujur sangkar dan tetrahedral) dan menentukan sifat-sifat kompleks
1x 50 menit
5. Mampu menjelaskan Ikatan ( asam dan basa Lewis) dalam kompleks koordinasi (back bonding) dan pengaruhnya
terhadap kekuatan ikatan dan frekuensi serapan senyawa kompleks Teori orbital molekul untuk senyawa kompleks koordinasi Diagram orbital molekul Ikatan dalam kompleks koordinasi Presentasi Dosen diskusi dan umpan balik Pekerjaan rumah atau kuiz 2% 15. 2x50 menit
Halaman 9 dari 12 2. Mampu mengklasifikasi ligan 3. Mampu menerangkan streokimia senyawa kompleks (bilangan koordinasi 2,3,4,5,6 dst) 1x50 menit 4. Mampu menjelaskan Isomer senyawa koordinasi (isomer
geometri, enansiomer dan optik) Klasifikasi ligan Streokimia senyawa kompleks Isomer senyawa koordinasi 16. 2x 50 menit 6. Mampu menjelaskan pembentukan ikatan ion dalam zat padat ionik 7. Menjelaskan sifat-sifat
senyawa ionik
8. Mampu menentukan energi pembentukan zat padat ionik dan Energi Kisi kristal
9. Mampu menentukan konstanta modelung 1x50 menit
10. Mampu menghitung energi kisi kristal menggunakan siklus Born-Haber Ikatan ion Sifat-sifat senyawa ionik Energi kisi Konstanta modelung Siklus Born-Haber Presentasi Dosen, diskusi dan umpan balik Pekerjaan rumah atau kuiz 2% 17. 2x50 menit 11. Mampu menjelaskan pengaruh kovalensi dalam kristal ionik
12. Mampu menjelaskan cara penentuan jari-jari ion dalam zat padat ionik
Halaman 10 dari 12
13. Mampu menjelaskan pengaruh perbandingan jari-jari ion terhadap struktur dalam zat padat ionik
1x50 menit
14. Menjelaskan jenis kisi kristal dalam struktur zat padat ionik
15. Sistim kristal zat padat dengan struktur dengan geometri MX, MX2, AmBnXp
Geometri kisi kristal
Kisi dan Sistim kristal
U J I A N A K H I R S E M E S T E R
NORMA AKADEMIK:
1. Kegiatan pembelajaran sesuai jadwal resmi, toleransi keterlambatan 10 menit 2. Selama proses pembelajaran berlangsung HP dimatikan
3. Selama proses pembelajaran tidak dibenarkan keluar masuk kelas
4. Pengumpulan tugas sesuai jadwal, bagi yang terlambat persentase nilai tuga dikurangi 5. Untuk mengikuti ujian harus tatap muka 75% kehadiran
NILAI AKHIR: Tugas 10% Kuis 20 % UTS 35 % UAS 35% REFERENSI:
1. Bowser J.R, Inorganic Chemistry, Cole Publishing, California, 1993 2. Cotton, Wilkinson, and Gaus, Basic Inorganic Chemistry, Wiley, 1995
3. Catherine E Housecroft and Alan G. Sharpe, Inorganic Chemistry, 2nd Ed, Pearson Education Limited, England, 2005
4. Huheey, Keiter, and Keiter, Inorganic Chemistry, 4th Ed. HaperCollins, 1993
5. Edward Lisic, Introduction to Coordination Chemistry, Infinity Publishing Com, 2005 6. Miessler G.L., Donald A. Tarr, Inorganic Chemistry, Prentice Hall, Englewood, New
Jersey, 1991
7. Petrucci, Harwood, Herring, Madura, General Chemistry, 9th ed, Pearson Int. ed. 2007 TUGAS TERSTRUKTUR:
Pekerjaan Rumah :
Halaman 11 dari 12
1. Menurut Borh elektron yang bergerak pada orbit tertentu akan mempunyai harga momentum sudut yang tertentu. Tentukan harga momentum sudut tersebut dan dapatkan juga harganya dari dualisme sifat partikel menurut de Brouglie.
2. Menggambarkan orbital-orbital atom hidrogen yang terletak pada sumbu koordinat x,y dan z!
3. Menyebutkan batasan-batasan (postulat) yang harus diperhatikan dalam menggunakan persamaan Schrodinger untuk menentukan struktur atom!
Bab II. Menyelesaikan soal-soal yang berkaitan dengan sistim periodik Contoh:
1. Menjelaskan kenapa afinitas elektron silikon dan sulfur lebih besar dari pada fosfor. 2. Menjelaskan kenapa jari-jari Na+ < jari-jari Na, jari-jari Cu > jari-jari Cu+ >jari-jari Cu2+ 3. Menentukan urutan jari-jari atom dari yang paling besar untuk atom-atom Ni (28), Cu
(29), Zn(30)
Bab III. Menyelesaikan soal-soal yang berkaitan dengan ikatan kimia dan struktur molekul Contoh:
1. Menuliskan struktur Lewis yang mungkin untuk molekul-molekul berikut yang hanya mempunyai ikatan kovalen tunggal
a. ICl b. Br2 c. NI3 d. H2Se
2. Menggambarkan struktur lewis dan hitung muatan formal atom-atom yang terdapat pada
a. metil sianat, CH3OCN b. Metil isosianat, CH3NCO
3. Menentukan langkah yang harus dilakukan dalam menulis struktur dan ikatan senyawa jika melanggar ketentuan oktet.
Menerapkan cara tersebut dalam penentuan struktur dan ikatan senyawa IBr3 dan SF4 4. Membuat bentuk diagram orbital molekul dari NO dan NH3 berapa orde ikatannya dan
tentukan sifat magnit
Bab IV. Menyelesaikan soal-soal yang tekait dengan simetri molekul Contoh :
1. Menjelaskan diantara senyawa-senyawa yang mempunyai cincin enam benzen, borazin, piridin dan S6 kenapa hanya benzen yang mempunyai 6 kali sumbu rotasi utama!
2. Menjelaskan diantara senyawa-senyawa berikut CF4, SF4, [BF4]- dan XeF4 kenapa hanya XeF4 yang mempunyai 4 kali sumbu rotasi utama
3. Menunjukkan bahwa N2O4 adalah planar dan molekul ini mempunyai tiga bidang simetri!
Bab V. Menyelesaikan soal-soal yang terkait dengan senyawa kompleks koordinasi Contoh :
1. Menjelaskan bagaimana teori ikatan valensi menjelaskan tentang keberadaan senyawa kompleks dari Ni(Cl)42- dan Ni(CN)42-!
2. Menjelaskan apa saja kelemahan dari teori ikatan valensi dan medan kristal masing-masingnya dalam menjelaskan tentang senyawa kompleks koordinasi?
Halaman 12 dari 12
4. Menghitungenergi pembelahan medan kristal (CFSE) dalam Dq untuk kompleks oktahedaral dari ion logam berikut.
(a) V+2 (b) Mn+3 (c) Mo+3 (d) Au+3
Bab VI : Menyelesaikan soal-soal yang terkait dengan dengan zat padat ionik Contoh :
1. Menjelaskan apa yang dimaksud dengan konstanta Modelung?
2. Menjelaskan apa yang dimaksud dengan bilangan koordinasi kation dalam kisi kristal?
3. Diketahui jarak antar inti iodium dalam kristal LiI adalah 427 pm sedangkan jarak antar inti litium dan iodium adalah 302, 5 pm. Jika dianggap antara kation dan anion berinteraksi tentukanlah jari-jari ion I- dan Li+ dan buat gambarnya!
Dibuat Diperiksa Disetujui
Tanggal Tanggal Tanggal
Oleh Oleh Oleh
Jabatan Dosen MK Jabatan Tim Evaluasi