BAB II
TINJAUAN PUSTAKA
2.1 Penyakit Kulit Karena Infeksi Jamur (Dermatomikosis)
Dermatomikosis adalah penyakit pada kulit, kuku, rambut dan mukosa yang disebabkan infeksi jamur (Marwali, 2000). Dermatomikosis mempunyai arti umum, yaitu semua penyakit jamur yang menyerang kulit (Djuanda, 2005). Faktor yang mempengaruhi terjadinya penyakit kulit antara lain iklim yang panas, tingkat pengetahuan, pendidikan dan personal hygiene masyarakat yang rendah. Oleh karena itu, infeksi jamur pada umumnya terjadi di negara-negara tropis dan diperparah oleh mengenakan pakaian yang tidak menyerap keringat (Havlickova dan Friedrich, 2008).
Kondisi dengan kelembaban tinggi merupakan lingkungan yang baik untuk pertumbuhan jamur penyebab penyakit kulit (Sarudji, 2010). Jamur penyebab penyakit kulit bertahan pada temperatur 25-280C dan dapat menginfeksi kulit manusia didukung oleh kondisi hangat dan lembab (Havlickova dan Friedrich, 2008). Ruangan tertutup yang kurang ventilasi serta terdapat banyak manusia di dalamnya akan memiliki kelembaban lebih tinggi dibanding di luar ruangan (Sarudji, 2010).
2.1.1 Macam-macam dermatomikosis a. Dermatofitosis
sebagai sumber nutrisi, dengan menyerang jaringan berkeratin, seperti stratum korneum pada epidermis, rambut, dan kuku (Verma, 2008).
Dermatofita merupakan kelompok taksonomi jamur kulit superfisial yang terdiri dari 3 genus, yaitu Microsporum, Trichophyton, dan Epidermophyton. Kemampuannya untuk membentuk ikatan molekuler terhadap keratin dan menggunakannya sebagai sumber makanan menyebabkan mereka mampu berkolonisasi pada jaringan keratin. Jamur ini hanya menginfeksi jaringan keratin superfisial seperti kulit, rambut dan kuku sehingga dermatofita disebut sebagai jamur keratinofilik (Djuanda, 2007).
Penamaan kelainan akibat jamur memiliki aturan tertentu. Kata pertama biasanya diawali ”tinea” dan diikuti oleh kata kedua yang menyatakan lokasi tubuh yang terinfeksi. Gambaran klinik jamur dermatofita menyebabkan beberapa bentuk klinis yang khas, satu jenis dermatofita menghasilkan klinis yang berbeda tergantung lokasi anatominya (Djuanda, 2005).
Bentuk-bentuk gejala klinis dermatofitosis: 1. Tinea korporis
Tinea korporis adalah infeksi jamur dermatofita pada kulit halus (globurus
skin) di daerah muka, badan, lengan dan glutea. Penyakit ini lebih sering
Tinea korporis disebabkan oleh jamur golongan dermatofita yang
mempunyai sifat mencernakan keratin. Penyebab tersering adalah Trichophyton rubrum dan Trichophyton mentagropytes. Gambaran klinis yaitu keluhan gatal terutama bila berkeringat. Oleh karena gatal dan digaruk, lesi semakin meluas, terutama di daerah kulit yang lembab. Kelainan yang terlihat dalam klinis merupakan lesi bulat atau lonjong, berbatas tegas terdiri atas eritema, skuama, kadang-kadang dengan vesikel dan papul di tepi. Daerah tengahnya biasanya lebih tenang. Kadang-kadang terlihat erosi dan krusta akibat garukan. Lesi-lesi pada umumnya merupakan bercak-bercak terpisah satu dengan yang lain. Kelainan kulit dapat pula terlihat sebagai lesi-lesi dengan pinggir polisiklik, karena beberapa lesi kulit yang menjadi satu. Khas dari infeksi ini ada central healing (Djuanda, 2007).
Gambar 2.1 Gambaran klinis dari tinea korporis 2. Tinea kruris
Tinea Kruris adalah penyakit jamur dermatofita didaerah lipat paha,
infeksi ini adalah Epidermophyton floccosum lalu diikuti oleh Trichophyton mentagrophytes dan Trichophyton rubrum. Ketiga spesies ini merupakan dermatofit yang menyukai daerah yang hangat dan lembab pada intertriginosa dan kulit yang mengalamin oklusi seperti disela paha (Djuanda, 2007).
Tinea kruris sering terdapat di daerah dengan iklim hangat, lembab, dan
faktor predisposisi meliputi sepatu tertutup dan sering terpapar. Tinea kruris adalah invasi folikel rambut, ini paling sering terjadi pada musim panas, pada pria muda, dan orang dengan pakaian ketat (Budimulja, 2009).
Kelainan kulit yang tampak pada sela paha merupakan lesi berbatas tegas. Peradangan pada tepi lebih nyata daripada bagian tengahnya. Bila penyakit ini menjadi menahun, dapat berupa bercak hitam disertai sedikit sisik. Erosi dan keluarnya cairan biasanya akibat garukan (Djuanda, 2007).
Gambaran klinisnya merupakan lesi bulat atau lonjong, berbatas tegas terdiri atas eritema, skuama, kadang-kadang dengan vesikel dan papul di tepi lesi. Daerah tengahnya biasa lebih tenang, sementara di tepi lebih aktif yang sering disebut dengan central healing. Kadang-kadang terlihat erosi dan krusta akibat garukan. Kelainan kulit juga dapat dilihat secara polisiklik, karena beberapa lesi kulit yang menjadi satu. Lesi dapat meluas dan memberikan gambaran yang tidak khas terutama pada pasien imunodefisiensi (Djuanda,2007).
3. Tinea pedis
Tinea pedis atau sering juga disebut Athelete foot yaitu merupakan penyakit
yang disebabkan oleh infeksi jamur dermatofita di daerah kulit telapak tangan dan kaki, punggung kaki, serta daerah interdigital. Penyakit ini disebabkan oleh jamur yang tumbuh dengan subur dalam keadaan lembab. Penyakit ini sering terjadi pada orang dewasa yang setiap hari harus memakai sepatu tertutup dan pada orang yang sering bekerja ditempat basah, mencuci, disawah dan sebagainya. Keluhan penderita bervariasi mulai dari tanda keluhan sampai mengeluh sangat gatal dan nyeri karena terjadinya infeksi sekunder dan peradangan (Madani, 2000).
Tinea pedis merupakan kelainan dermatofitosis terbanyak di dunia.
Dilaporkan 70% dari populasi menderita tinea pedis yang paling banyak menyerang pada laki-laki dibandingkan dengan wanita. Serta tidak ditentukan dan dipengaruhi oleh etnik atau ras tertentu. Pada tinea pedis tidak ditemukan hubungan sebagai penyebab kematian (Cortney dan Robbins, 2015).
Tinea pedis disebabkan oleh jamur Trichophyton mentagrophytes.
Karakteristik Trichophyton mentagrophytes menghasilkan jenis yang relatif tidak ada peradangan dari dermatofitosis dengan eritema kusam dan sisik keperakan yang melibatkan seluruh telapak kaki dan sisi kaki menampilkan moccasin (Chamlin, et al., 2008).
Ada 3 bentuk gambaran klinis yang sering dijumpai pada tinea pedis yaitu: - Bentuk intertriginosa
- Bentuk vesikuler akut
Dijumpai vesikel dan bula di bawah kulit terutama pada telapak kaki bagian tengah kemudian meluas. Sering disertai infeksi sekunder, keluhan penderita di sini berupa perasaan gatal dan sakit.
- Bentuk hiperkeratotik
Tampak pengelupasan kulit terus-menerus disertai eritama dan hiperkeratosis. Bila hiperkeratosis hebat dapat timbul fisura yang dalam. Daerah yang paling sering dikenai adalah telapak tangan dan kaki.
Gambar 2.3 Gambaran klinis dari tinea pedis 2.2 Antijamur
Menurut Ganiswara (1995), berdasarkan cara kerjanya, obat antijamur dibedakan menjadi 4 yaitu :
1) Berikatan kuat dengan sterol yang terdapat pada membran sel jamur. Ikatan ini mengakibatkan kebocoran membran sel, sehingga terjadi kehilangan beberapa bahan intrasel dan menyebabkan kerusakan yang tetap pada sel jamur.
Contoh: nistatin dan amfoterisin.
2) Masuk kedalam sel jamur dengan bantuan sitosin deaminasi dan dalam sitoplasma akan bergabung dengan RNA setelah mengalami deaminase menjadi 5-fluorourasil. Sintesis protein sel jamur terganggu akibat penghambatan langsung sintetis DNA oleh metabolit fluorourasil.
Contoh : flusitosin.
3) Menghambat mitosis jamur dengan mengikat protein mikrotubuler dalam sel. Contoh : griseofulvin.
4) Menimbulkan gangguan terhadap sintesis asam nukleat atau penimbunan peroksida dalam sel jamur sehingga terjadi kerusakan dinding sel yang mengakibatkan permeabilitas terhadap berbagai zat intrasel meningkat.
Contoh : imidazol (mikonazol, klotrimazol). 2.2.1 Mikonazol nitrat
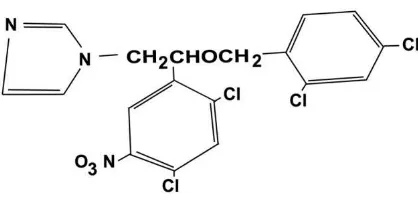
2.2.1.1 Struktur kimia mikonazol nitrat (Reynold, 1989)
2.2.1.2 Sifat-sifat mikonazol nitrat
Nama kimia mikonazol nitrat adalah 1-(2,4-dikloro-beta-(2,4-diklorobenzil) oksi)-fenetil) imidazol mononitrat. Merupakan serbuk hablur, putih atau praktis putih, berbau lemah. Sangat sukar larut dalam air dan isopropanol, sukar larut dalam etanol, kloroform, dan propilen glikol, agak sukar larut dalam metanol, larut dalam dimetilformamid, mudah larut dalam dimetilsulfoksida (Depkes RI, 1995).
2.2.1.3 Mekanisme kerja mikonazol nitrat
Mikonazol nitrat adalah antijamur spektrum luas dari kelompok imidazol. Mikonazol nitrat biasanya dioleskan pada kulit atau selaput lendir untuk menyembuhkan infeksi jamur. Obat ini bekerja dengan menghambat biosintesis ergosterol pada membran sel jamur yang menyebabkan terjadinya kerusakan pada dinding sel jamur, sehingga terjadi peningkatan permeabilitas membran, dan pada akhirnya menyebabkan sel jamur kehilangan nutrisi selulernya. Obat ini terutama digunakan untuk pengobatan penyakit kulit mikosis (Wyatt, 2001).
2.2.1.4 Farmakodinamika
Mikonazol memiliki aktivitas antifungi terhadap dermatofita dan ragi, serta memiliki aktivitas antibakteri terhadap basil dan kokus gram positif. Aktivitas ini menghambat biosintesa ergosterol di dalam jamur dan mengubah komposisi komponen-komponen lemak di dalam membran, yang menyebabkan nekrosis sel jamur (Gubbins, 2009).
2.2.1.5 Farmakokinetika
g/hari. Lebih dari 90% dilaporkan terikat pada protein plasma. Mikonazol dimetabolisme di hati membentuk metabolit inaktif. Pada pemberian secara oral, sekitar 10-20% diekskresikan melalui urin dalam bentuk metabolit, dan sekitar 50% diekskresikan dalam bentuk utuh pada faeces setelah 6 hari. Hanya sedikit yang diabsorbsi bila diberikan secara topikal. Obat ini tersedia dalam bentuk krim 2% dan bedak tabur, dipakai dua kali sehari, dioleskan secukupnya, merata, pada kulit yang terinfeksi (Reynold, 1989).
2.2.1.6 Penggunaan Klinik
Mikonazol nitrat diindikasikan untuk infeksi kulit yang disebabkan oleh dermatofit atau khamir dan fungi lainnya seperti:
1. Pitriasis versikolor (panu)
2. Tinea korporis (kurap di leher/badan) 3. Tinea kruris (kurap di selangkangan) 4. Tinea pedis (kutu air di telapak kaki)
Mikonazol nitrat juga memiliki khasiat antibakteri terhadap bakteri gram positif, maka dapat juga digunakan untuk mengobati penyakit fungi yang mengalami infeksi sekunder bakteri (Dismukes, 2000).
2.3Nanopartikel
fleksibilitasnya untuk dikombinasi dengan berbagai teknologi lain sehingga membuka potensi yang luas untuk dikembangkan pada berbagai keperluan dan target. Kelebihan lain dari nanopartikel adalah adanya peningkatan afinitas dari sistem karena peningkatan luas permukaan kontak pada jumlah yang sama. Pembentukan nanopartikel dapat dicapai dengan berbagai teknik yang sederhana. Nanopartikel pada sediaan farmasi dapat berupa sistem obat dalam matriks seperti nanosfer, nanokapsul, nanoliposom dan nanoemulsi (Kawashima, et al., 2000). 2.4Nanoemulsi
Emulsi merupakan sediaan yang mengandung dua fase yang tidak tercampur, yaitu air dan minyak, dimana cairan yang satu terdispersi menjadi tetesan kecil (droplet) dalam cairan lainnya yang dstabilkan dengan zat pengemulsi atau surfaktan yang cocok (Anief, 2000). Tipe emulsi dapat dibuat berdasarkan perbandingan antara fase minyak dan airnya. Apabila fase minyak didispersikan ke fase air dalam jumlah yang banyak, maka emulsi merupakan tipe minyak dalam air dan sebaliknya. Tipe emulsi minyak dalam air lebih disukai dalam formulasi karena tidak memberikan kesan lengket pada kulit dan lebih mudah tercucikan (Young, 1972).
Homogenisasi dapat dilakukan dengan magnetic stirrer atau homogenizer dengan kecepatan yang minimal dimana fase minyak harus diteteskan secara perlahan kedalam fase air (Young, 1972).
Nanoemulsi merupakan sistem emulsi yang transparan, tembus cahaya dan merupakan dispersi minyak air yang dstabilkan oleh surfaktan, memiliki ukuran droplet 2-500 nm (Shakeel, et al., 2008). Nanoemulsi telah diterapkan dalam berbagai industri farmasi, seperti untuk sistem penghantar transdermal, produk perawatan tubuh dan pembawa yang baik pada obat sehingga dapat meningkatkan bioavalabilitas dalam tubuh (Gutierrez, et al., 2008).
Tampilan visual nanoemulsi lebih jernih dibandingkan mikroemulsi karena mengandung droplet dalam ukuran lebih kecil dari panjang gelombang pada spektrum tampak (Rajalakshmi, et al., 2011).
Droplet berukuran kecil menyebabkan penurunan gaya gravitasi dan gerak Brown sehingga mencegah sedimentasi atau creaming dari sediaan selama penyimpanan (Tadros, 2005). Nanoemulsi memiliki stabilitas dalam jangka panjang, meningkatkan stabilitas kinetik dan tidak menunjukkan pemisahan atau pengkeruhan (Kwon, et al., 2014).
2.4.1 Keuntungan nanoemulsi
Nanoemulsi memiliki beberapa keuntungan sebagai berikut :
2) Ukuran tetesan yang kecil mencegah terjadinya flokulasi dan memungkinkan sistem untuk tetap tersebar tanpa adanya pemisahan, serta dapat mencegah koalesens.
3) Nanoemulsi cocok untuk penghantaran bahan aktif melewati kulit. Luas permukaan yang besar dari sistem emulsi memungkinkan penetrasi yang cepat dari bahan aktif.
4) Karena ukuran yang kecil, nanoemulsi dapat melewati permukaan kulit yang kasar dan dapat meningkatkan penetrasi obat.
5) Karena sifatnya yang transparan dan fluiditasnya (pada konsentrasi minyak yang sesuai) dapat memberikan estetika yang menarik dan menyenangkan saat digunakan.
6) Ukuran tetesan yang kecil memudahkan penyebarannya dan penetrasi mungkin dapat ditingkatkan karena tegangan permukaan dan tegangan antarmuka yang rendah (Swarbrick, 2007).
Nanoemulsi sama seperti mikroemulsi, tipe nanoemulsi dibagi menjadi minyak dalam air (m/a), air dalam minyak (a/m), dan bicontinuous yang merupakan bentuk transisi dari tipe m/a dan a/m dengan mengubah volume minyak dan air, dimana ketiga tipe tersebut bergantung pada konsentrasi dan sifat kimia surfaktan, minyak, dan bahan yang terlarut didalamnya. Transisi antara berbagai tipe tersebut dapat terjadi dan disebabkan oleh perubahan suhu atau modifikasi perbandingan surfaktan dan kosurfaktan (Swarbrick, 2007).
minyak dan air berada dalam kesetimbangan dan menunjukkan tegangan antarmuka yang rendah antara dua fase (Ansel dan Propovich, 1999).
Solans (2003) mengatakan bahwa pembentukan nanoemulsi memerlukan pemasukan energi. Energi tersebut diperoleh dari peralatan mekanik ataupun potensi kimiawi yang terdapat dalam komponen. Meskipun demikian, jumlah energi yang diperlukan bervariasi. Menurut Fast dan Mecozzi (2009), emulsi akan terbentuk secara spontan pada penambahan minyak dan surfaktan ke dalam air karena tegangan antarmuka yang rendah akibat jumlah surfaktan yang besar. Sistem yang terbentuk secara spontan merupakan sistem yang stabil secara termodinamika.
2.4.2 Pembuatan nanoemulsi
Nanoemulsi dapat dibuat melalui 3 cara, yaitu: a. Penggunaan homogenizer bertekanan tinggi
Metode ini menggunakan tekanan tinggi untuk menghasilkan emulsi dalam ukuran sangat kecil yaitu sekitar 1 nm. Dispersi kedua fase (minyak dan air) diperoleh dengan melewatkan campuran melalui lubang-lubang kecil pada tekanan yang sangat tinggi (500-5000 psi), menghasilkan ukuran partikel emulsi yang sangat halus. Teknik ini sangat efisien namun menghabiskan banyak energi dan metode ini tidak dapat digunakan untuk zat aktif yang tidak tahan pada pemanasan karena emulsi dapat mengalami kenaikan suhu selama homogenisasi. b. Metode emulsifikasi energi rendah
kedalam fase pendispersi. Metode ini pada umumnya menghasilkan emulsi dengan ukuran sekitar 50-500 nm.
c. Prinsip PIT (Phase Inversion Temperature)
Metode ini dilakukan dengan mengubah faktor yang mempengaruhi HLB, seperti suhu dan/atau konsentrasi surfaktan. Ketika emulsi minyak dalam air yang menggunakan surfaktan non ionik dipanaskan hingga mencapai suhu kritis (PIT), maka emulsi akan berbalik menjadi fase air dalam minyak. Pada suhu ini ukuran droplet mencapai ukuran minimum dan tegangan antar permukaan juga mencapai titik minimum, namun droplet kecil ini sangat tidak stabil dan cepat menggumpal. Apabila didinginkan secara cepat, maka dapat diperoleh droplet berukuran kecil dan stabil (Rajalakshmi, et al., 2011).
2.4.3 Surfaktan
Surfaktan atau zat aktif permukaan adalah molekul dan ion yang diadsorpsi pada antar muka. Secara kimia, molekul surfaktan terdiri atas gugus polar dan non polar. Apabila surfaktan dimasukkan dalam sistem yang terdiri dari air dan minyak, maka gugus polar akan mengarah ke fase air sedangkan gugus non polar akan mengarah ke fase minyak. Surfaktan yang memiliki gugus polar lebih kuat cenderung membentuk tipe minyak dalam air (m/a), sedangkan apabila gugus non polar yang lebih kuat cenderung membentuk tipe air dalam minyak (a/m) (Martin, et al., 1993).
Surfaktan yang dipilih harus:
2. Menghasilkan film yang fleksibel yang dapat merusak bentuk tetesan pada kedua fase sehingga dapat bercampur.
3. Memiliki sifat hidrofil-lipofil untuk memberikan lengkungan yang tepat pada daerah antarmuka agar dapat terlihat tipe sistem yang diinginkan, m/a, a/m atau biocontinuous (Swarbrick, 2007).
Molekul surfaktan dapat dikelompokkan berdasarkan sifat alami gugus hidrofiliknya. Ada empat klasifikasi dari surfaktan, yaitu (Swarbrick, 2007):
1. Surfaktan anionik
Surfaktan ini gugus hidrofiliknya bermuatan negatif. Contoh: Sodium lauril sulfat, potassium laurat. 2. Surfaktan kationik
Surfaktan ini gugus hidrofiliknya bermuatan positif. Contoh: Cetrimid, benzalkonium klorida
3. Surfaktan amfolitik (zwitterionik)
Surfaktan ini gugus hidrofiliknya dapat bermuatan negatif dan positif. Contoh: Lesitin
4. Surfaktan nonionik
Surfaktan ini gugus hidrofiliknya tidak bermuatan. Contoh: Sotbitan ester (span), polisorbat (tween). 2.4.4 Kosurfaktan
meningkatkan mobilitas ekor hidrokarbon sehingga penetrasi minyak pada bagian ekor menjadi lebih besar (Swarbrick, 2007).
Kosurfaktan umumnya molekul kecil, khususnya alkohol rantai pendek hingga sedang (C3-C8) yang dapat berdifusi cepat diantara fase minyak dan air. Alkohol rantai sedang, seperti pentanol dan heksanol adalah kosurfaktan yang efektif tetapi sangat berpotensi menimbulkan iritasi. Beberapa peneliti telah meneliti kemungkinan penggunaan surfaktan nonionink sebagai kosurfaktan karena iritasinya rendah (Swarbrick, 2007).
2.4.5 Penentuan ukuran nanopartikel
Metode yang paling umum digunakan adalah analisa gambar (mikrografi). Metode ini meliputi metode mikroskopi dan metode holografi. Alat yang sering digunakan biasanya SEM, TEM dan AFM. Namun seiring dengan berkembangnya ilmu pengetahuan yang lebih mengarah ke era nanoteknologi, para peneliti mulai menggunakan Laser Diffraction dan Dynamic Light Scattering (DLS). Metode ini dinilai lebih akurat bila dibandingkan dengan metode analisa gambar maupun metode ayakan (sieve analyses), terutama untuk sample-sampel dalam ukuran nanometer. Alat yang sering digunakan untuk mengukur partikel beserta distribusinya adalah particle size analyzer (PSA). Salah satu metode yang digunakan alat ini adalah prinsip dynamic light scattering (DLS). Metode ini juga dikenal sebagai quasi-elastic light scattering (QELS). Alat ini berbasis Photon Correlation Spectroscopy (PCS). DLS cocok digunakan untuk sampel-sampel
dalam orde nanometer (Soppimath, et al., 2001).
dengan metode kering ataupun pengukuran partikel dengan metode ayakan dan analisa gambar untuk sampel berukuran kecil. Terutama untuk sampel-sampel ukuran nanometer dan submicron yang biasanya memliki kecenderungan aglomerasi yang tinggi. Hal ini dikarenakan partikel didispersikan ke dalam media sehingga partikel tidak saling beraglomerasi (menggumpal). Dengan demikian ukuran partikel yang terukur adalah ukuran dari single particle. Selain itu hasil pengukuran dalam bentuk distribusi, sehingga hasil pengukuran dapat diasumsikan sudah menggambarkan keseluruhan kondisi sampel (Soppimath, et al., 2001). 2.4.6 Stabilitas fisik nanoemulsi
Stabilitas merupakan kemampuan suatu produk obat atau kosmetik untuk bertahan dalam batas spesifikasi yang ditetapkan sepanjang periode penyimpanan dan penggunaan untuk menjamin identitas, kekuatan, kualitas dan kemurnian produk. Sediaan yang stabil adalah sediaan yang masih berada dalam batas yang dapat diterima selama periode penyimpanan dan penggunaan. Kestabilan suatu emulsi ditandai dengan tidak terjadinya creaming atau tetap jernih, tidak mengalami perubahan pada bau, warna, dan sifat-sifat fisik lainnya (Martin, et al., 1993).
Beberapa parameter stabilitas fisik nanoemulsi adalah: a. Organoleptis atau pemisahan fisik
Pemeriksaan ini bertujuan untuk mengamati adanya perubahan atau pemisahan fase, timbulnya bau dan perubahan warna.
b. Viskositas
c. Ukuran partikel
Perubahan ukuran partikel rerata atau distribusi ukuran partkel merupakan hal yang penting, karena diameter partikel nanoemulsi harus berkisar antara 2-500 nm (paling baik dibawah 100 nm).
d. Pemeriksaan pH
Sediaan topikal sebaiknya memiliki pH yang sesuai dengan pH kulit, yaitu 4,5-6,5. Apabila pH terlalu basa akan menyebabkan kulit menjadi kering, sedangkan pH yang terlalu asam akan menimbulkan iritasi pada kulit.
e. Pemeriksaan tipe nanoemulsi
Pengujian ini dilakukan untuk mengetahui tipe nanoemulsi yang terbentuk adalah berupa tipe minyak dalam air (m/a) atau air dalam minyak (a/m).
f. Pemeriksaan tegangan permukaan
Uji ini dilakukan untuk memeriksa tegangan permukaan nanoemulsi yang terbentuk.
g. Uji mekanik (uji sentrifugasi)
Uji mekanik ini dilakukan untuk mengetahui terjadinya pemisahan fase. Sediaan disentrifugasi pada kecepatan 3800 rpm selam 5 jam atau 5000-10000 rpm selam 30 menit. Hal ini dilakukan karena perlakuan tersebut sama besarnya dengan pengaruh gaya gravitasi terhadap penyimpanan selama setahun (Abdulkarim, et al., 2010).
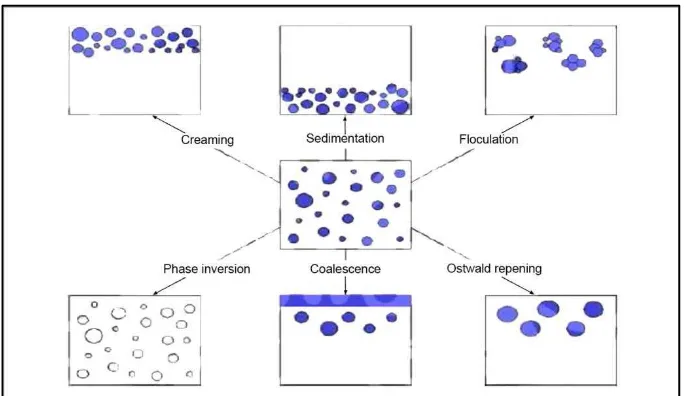
Beberapa ketidakstabilan yang sering timbul dalam sediaan nanoemulsi, yaitu:
1. Creaming
Creaming adalah pemisahan fase emulsi atau terbentuknya dua lapisan
emulsi akibat perbedaan densitas antara fase terdispersi dan medium pandispersi karena agregat mempunyai kecendrungan yang lebih besar untuk naik kepermukaan emulsi. Ketidakstabilan ini bersifat reversibel sehingga dapat didispersi kembali dengan pengocokan. Untuk mencegah terjadinya creaming, densitas fase terdispersi dan medium pendispersi harus berkisar sedekat mungkin (Abdulkarim, et al., 2010).
2. Sedimentasi
Sedimentasi adalah pemisahan antara padatan dan cairan karena pengaruh gaya gravitasi, akibatnya partikel berukuran besar turun dan mengendap di bagian bawah emulsi (Abdulkarim, et al., 2010).
3. Flokulasi
Flokulasi adalah penggabungan partikel bergantung pada gaya tolak-menolak elektrostatis (zeta potensial). Ketidakstabilan ini masih dapat diperbaiki dengan pengocokan karena film antar permukaan masih ada (Martin, et al., 1993).
4. Inversi
5. Koalesens
Koalesens adalah proses ketika tetesan fase dalam mendekat dan berkombinasi membentuk partikel lebih besar dan menjadi suatu lapisan. Hal ini terjadi bukan hanya karena energi bebas permukaan tetapi juga karena tidak semua permukaan partikel terlapisi oleh surfaktan (Martin, et al., 1993). Ketidakstabilan ini merupakan kerusakan yang lebih besar dari pada creaming. Usaha untuk menstabilkan kembali keadaan ini tidak dapat dilakukan dengan pengocokan, namun membutuhkan pengemulsi tambahan dan pemrosesan kembali (Ansel, 1989).
6. Ostwald Ripening
Ostwald Ripening adalah proses ketika tetesan yang kecil berubah menjadi besar dan membentuk tetesan yang baru. Fenomena ini berhubungan dengan sistem yang memiliki ukuran tetesan yang bervariasi. Fenomena koalesens dan ostwald ripening menyebabkan pemisahan sistem menjadi tiga fase, yaitu fase internal, eksternal dan emulgator (Abdulkarim, et al., 2010).
Skema kerusakan pada emulsi dapat dilihat pada Gambar 2.5.
2.5 Sediaan Krim
Krim adalah sediaan setengan pada berupa emulsi mengandung air tidak kurang dari 60% dan dimaksudkan untuk pemakaian luar (Depkes RI, 1979). Menurut Farmakope Indonesia Edisi IV, krim adalah bentuk sediaan setengah padat mengandung satu atau lebih bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai (Depkes RI, 1995).
Krim dapat diformulasikan dalam dua tipe yaitu tipe minyak dalam air (m/a) dan tipe air dalam minyak (a/m). Kedua fase yang berbeda dalam krim distabilkan dengan penambahan surfaktan (Ansel, 1989). Krim tipe minyak dalam air lebih disukai konsumen karena tidak memberikan kesan lengket dan berminyak serta lebih mudah dibersihkan dibandingkan krim tipe air dalam minyak (Mishra, et al., 2014).
2.6 Permeabilitas dan Penetrasi Kulit
Penyampaian obat melalui kulit menjadi alternatif yang lebih diinginkan dari pada penyampaian obat secara oral. Penyampaian obat oral sering menyebabkan gangguan lambung dan inaktivasi sebagian obat karena first paa metabolism di hati. Absorbsi obat melalui kulit menghasilkan level dalam darah
yang lebih lama dan lebih disukai daripada obat oral (Kumar, et al., 2010).
Penetrasi melalui stratum korneum terjadi secara difusi pasif. Setiap bahan mempunyai kemampuan tertentu untuk berdifusi, namun bahan-bahan yang larut dalam lemak lebih mudah berdifusi daripada bahan-bahan yang larut dalam air (Putro, 1997). Beberapa faktor yang mempengaruhi penetrasi di kulit adalah usia, jenis kelamin, lokasi kulit, kelembapan kulit, keadaan kulit seperti kulit normal atau mengalami perubahan, kulit dengan atau tanpa rambut serta kecepatan metabolisme bahan dalam kulit (Tranggono dan Latifah, 2007).
Faktor-faktor yang berpengaruh pada bahan yang diaplikasikan pada kulit antara lain:
a. Besar atau kecilnya molekul dari bahan tersebut b. Daya larut bahan itu dalam lemak atau air c. Berbasis lemak atau garam
d. Tingkat keasaman (pH) dari bahan
e. Kecepatan pemberian bahan pada kulit (Tranggono dan Latifah, 2007). 2.7 Uji Penetrasi in vitro
Studi penetrasi in vitro dilakukan untuk mengukur kecepatan dan jumlah senyawa yang melewati kulit, dimana hal tersebut bergantung pada obat, bentuk sediaan, bahan eksipien, bahan peningkat penetrasi dan variabel formulasi lainnya (Witt dan Bucks, 2003).
hewan. Membran diletakkan diantara kedua kompartemen yang dilengkapi 0-ring untuk menjaga letak membran. Selanjutnya kompartemen reseptor diisi dengan larutan penerima. Suhu pada sel dijaga dengan air menggunakan water jacket di sekeliling kompartemen reseptor. Sediaan yang akan diuji diaplikasikan pada membran kulit. Kemudian pada interval waktu tertentu cairan dari kompartemen reseptor diambil beberapa mL dan segera digantikan dengan cairan yang sama sejumlah cairan yang diambil. Selanjutnya jumlah obat yang terpenetrasi melalui kulit dapat dianalisis dengan metode yang sesuai (Fan, et al., 2007).
2.8 Pengujian Aktivitas Antijamur
Pengujian aktivitas antijamur sama artinya dengan menentukan kerentanan jamur terhadap suatu zat antijamur. Beberapa faktor yang mempengaruhi aktivitas antijamur in vitro antara lain adalah pH lingkungan, komponen media, stabilitas zat antijamur, ukuran inokulum, masa inkubasi dan aktivitas metabolisme mikroorganisme (Asmaedy, 1991).
Menurut Ganiswara (1995), metode pengujian aktivitas antijamur in vitro berdasarkan prinsipnya dibagi menjadi :
a) Metode Difusi
Metode ini dapat dilakukan dengan dua cara yaitu: - Cara cakram (disc)
Pada cara ini dipergunakan cakram kertas saring yang mengandung suatu zat antijamur dengan kekuatan tertentu yang diletakkan pada lempeng agar yang telah diinokulasi dengan jamur uji, selanjutnya diinkubasi pada suhu 250C selama 7-14 hari. Pengamatan dilakukan terhadap daerah bening yang terbentuk di sekeliling kertas cakram yang menunjukkan zona hambatan pertumbuhan jamur.
- Cara sumur
Pada lempeng agar yang telah diinokulasi oleh jamur uji dibuat sebidang sumur. Sumur kemudian diisi dengan zat uji, diinkubasi 25ºC selama 7-14 hari. Pengamatan dilakukan dengan melihat ada atau tidaknya zona hambatan di sekeliling sumur.
b) Metode Dilusi
Pada metode ini zat antijamur dicampur dengan media agar yang kemudian diinokulasi dengan jamur uji. Pengamatan dilakukan dengan melihat tumbuh atau tidaknya jamur dalam media. Aktivitas zat antijamur ditentukan dengan melihat konsentrasi hambat minimum (KHM), yaitu konsentrasi hambatan terkecil dari zat antijamur yang dapat menghambat pertumbuhan jamur uji.
Metode ini dapat dilakukan dengan dua cara : - Cara penipisan lempeng agar
Pada cara ini, zat uji diencerkan sehingga diperoleh suatu larutan uji yang
mengandung 100μg/mL, larutan ini sebagai larutan sediaan. Dari larutan sediaan
Jamur uji diinokulasikan setelah agar membeku dan kering. Zat diinkubasi pada suhu 250C selama 7-14 hari. Aktivitas zat uji ditentukan sebagai KHM.
- Cara pengenceran tabung
Prinsip dari cara ini adalah penghambatan pertumbuhan jamur dalam pembenihan cair oleh suatu zat antijamur yang dicampur ke dalam pembenihan. Zat uji diencerkan secara serial dengan metode pengenceran kelipatan dua dalam media cair, kemudian diinokulasi dengan jamur uji dan diinkubasi pada suhu 370C selama 7-14 hari. Aktivitas zat uji ditentukan sebagai KHM.
2.8.1 Parameter aktifitas antijamur 1. Zona Hambat
Menurut Gaman dan Sherrington (1994), metode difusi agar dari prosedur Kirby-Bauer, sering digunakan untuk mengetahui sensitivitas mikroba. Prinsip
dari metode ini adalah penghambatan terhadap pertumbuhan mikroba, yaitu zona hambat akan terlihat sebagai daerah jernih di sekitar sumuran yang mengandung zat antimikrobia. Luas zona hambat pertumbuhan mikrobia menunjukkan sensitifitasnya terhadap zat antimikrobia yang digunakan. Selanjutnya, dikatakan bahwa semakin besar luas zona hambat yang terbentuk berarti mikrobia tersebut semakin sensitif. Zona hambat merupakan tempat mikrobia terhambat pertumbuhannya akibat senyawa antimikrobia.
2. Konsentrasi Hambat Minimal (KHM)
dari metode tube dilution. KHM ditentukan dengan mengamati tingkat kekeruhan pada tabung yang telah dibuat seri pengenceran. Penentuan KHM mula-mula dilakukan dengan membuat pengenceran ekstrak antijamur pada medium cair yang ditambahkan dengan jamur uji pada beberapa konsentrasi berbeda dalam persen (%). Larutan ekstrak antijamur pada kadar terkecil yang terlihat jernih tanpa adanya pertumbuhan jamur uji ditetapkan sebagai KHM.
3. Konsentrasi Bunuh Minimal (KBM)
Bahan antimikrobia bersifat menghambat bila digunakan dalam konsentrasi kecil, namun bila ditingkatkan dapat mematikan mikroorganisme. Berdasarkan hal tersebut, perlu diketahui KBM (Konsentrasi Bunuh Minimum) bahan antimikrobia terhadap mikroorganisme. KBM adalah konsentrasi terendah bahan antimikrobia yang mematikan. Pada penentuan KBM, uji tidak menggunakan medium perbenihan sehingga jamur tidak diberi nutrisi untuk tumbuh sehingga yang dibunuh adalah jamur yang tidak mengalami pertumbuhan (Lay, 1994).
2.8.2 Tricophyton mentagrophytes Klasifikasi Tricophyton mentagrophytes: Kingdom : Fungi
Phylum : Ascomycota Class : Euascomycetes Order : Onygenales
Family : Arthrodermataceae Genus : Trichophyton
Bentuk makroskopis Trichophyton mentagrophytes adalah merupakan tenunan lilin, berwarna putih sampai putih kekuningan yang agak terang atau berwarna violet merah. Kadang bahkan berwarna pucat kekuningan dan coklat. Jamur ini merupakan jamur filamentous yang menyerang kulit yang menggunakan keratin sebagai nutrisinya. Keratin adalah protein utama dalam kulit, rambut dan kuku. Jamur Trichophyton mentagrophytes tumbuh dengan subur di area yang hangat dan lembab. Hal tersebut menjadi lazim apabila kita memakai sepatu berbahan plastik atau berkeringat banyak (Anonim, 2007).
2.8.3 Microsporum canis Klasifikasi Microsporum canis : Kingdom : Fungi
Phylum : Ascomycota Class : Eurotiomycota Order : Onygenales
Family : Arthrodermataceae Genus : Microsporum Spesies : Microsporum canis
Microsporum canis memiliki konidia yang besar, berdinding kasar,
Jamur ini menyebabkan tinea kapitis pada anak-anak. Cendawan ini menyebar secara radial pada lapisan kulit berkeratin dengan pembentukan cabang hifa dan kadang-kadang artrospora. Peradangan jaringan hidup di bawahnya sangat ringan dan hanya terlihat sedikit bagian yang bersisik kering. Biasanya terjadi iritasi, eritema (merah dan menyebar pada kulit), edema (akumulasi berlebihan zat alir serum di dalam jaringan), dan terbentuk gelembung pada bagian tepi yang menjalar, lingkaran berwarna merah jambu ini menimbulkan nama ringworm (kadas).
2.8.4 Candida albicans
Klasifikasi Candida albicans menurut Waluyo (2004) adalah: Kingdom : Fungi
Phylum : Thallophyta Class : Deuteromycetes Order : Moniliales Family : Cryptococcaceae Genus : Candida
Species : Candida albicans
Candida albicans dapat hidup sebagai saprofit tanpa menyebabkan