BAB II Deskripsi Proses 13 BAB II
DESKRIPSI PROSES
2.1. Spesifikasi Bahan Baku dan Produk 2.1.1. Spesifikasi Bahan Baku
1. Acrylonitrile
Fase : cair
Warna : tidak berwarna
Aroma : seperti bawang merah dan bawang
putih Specific gravity : 0,8060 Titik didih : 77-79 ˚C Titik leleh : -84 ~ -83 ˚C
Kelarutan : 0,0073 kg/1 kg air (20 ˚C),
sangat larut dalam etanol dan eter Komposisi bahan : 99,99% Acrylonitrile
(Asumsi 100% Acrylonitrile) (Tongsuh Petrochemical Corp., Ltd., 1997)
2. Air
Berat molekul : 18,015 kg/kmol Densitas (25 °C) : 998 kg/m3 Fase : cair Specific gravity : 1,00 Titik beku : 0 °C Titik didih : 100 °C Viskositas : 0,8949 cP (Kirk Othmer, 1991)
BAB II Deskripsi Proses 14 Standar air bersih
Bau : tidak berbau
Jumlah zat padat terlarut : 0,0015 kg/L
Rasa : tidak berasa
Suhu : 30 °C
pH : 6,5 – 9,0
(Depkes RI, 1990)
3. Katalis
Jenis : Raney Copper
Luas permukaan : 9.500 m2/kg Volume pori total : 0,0003 m3/kg Berat jenis ( bulk ) : 1.200 kg/m3
Kadar : 48% Cu , 21% Al Diameter : 0,0032 m (BASF, 2009) 2.1.2 Spesifikasi Produk Acrylamide 50% solution Bentuk : cair Warna : bening pH : 5 – 6,5
Titik didih (1 atm) : 104 °C
Densitas : 1,038
Specific gravity (25 °C) : 1,0412 Viskositas (25 °C) : 2,71 cP
Flammibilty : nonflammable
BAB II Deskripsi Proses 15 2.2. Konsep Proses
2.2.1. Dasar Reaksi
Reaksi pembuatan acrylamide dari acrylonitrile dan air merupakan reaksi eksotermis. Reaksi berlangsung pada suhu 70–120 °C dan tekanan 3,03 bar. Konversi reaksi sebesar 97%. Reaksi berjalan baik pada reaktor fixed bed (Onuoha & Wainwright, 1984). Reaksi berlangsung pada kondisi adiabatis dan non-isotermal.
Reaksi yang terjadi adalah :
H H H H H C = C – C ≡ N + H2O
𝑅𝑎𝑛𝑒𝑦 𝐶𝑜𝑝𝑝𝑒𝑟
→ C = C – C – N
H H O H acrylonitrile air acrylamide
2.2.2. Pemakaian Katalis
Reaksi hidrolisis acrylonitrile menjadi acrylamide merupakan reaksi cair-cair dengan katalis padat yang berlangsung dalam reaktor fixed bed. Katalis yang digunakan adalah raney copper. Katalis raney copper terdiri dari 2%-45% berat aluminium dengan kisaran diameter 0,002–0,5 inchi (US Patent No. 3.920.740, 1975). Katalis raney copper memiliki umur aktif hingga 2 tahun (Onuoha & Wainwright, 1984).
2.2.3. Mekanisme Reaksi
Reaksi pembentukan acrylamide dengan proses hidrolisis acrylonitrile adalah termasuk reaksi heterogen yang melibatkan dua fase yaitu reaktan dalam fase cair dan katalis dalam fase padat.
Mekanisme reaksi yang terjadi adalah sebagai berikut:
1. Transfer massa reaktan dari badan utama fluida ke permukaan luar katalis (external diffusion)
2. Transfer massa reaktan dari permukaan luar ke permukaan dalam pori – pori katalis (internal diffusion).
BAB II Deskripsi Proses 16 4. Reaksi pada permukaan katalis.
5. Desorbsi produk reaksi dari permukaan dalam katalis.
6. Transfer massa produk dari permukaan dalam ke permukaan luar katalis. 7. Transfer massa produk dari permukaan luar ke badan utama fluida.
(Fogler, 1999) Pada mekanisme reaksi katalitis ini, tahap difusi dan adsorpsi berlangsung sangat cepat, sedangkan reaksi pada permukaan katalis berlangsung paling lambat. Sehingga kecepatan reaksi katalitis secara keseluruhan dikontrol oleh reaksi permukaan (Onouha & Wainwright, 1984). Mekanisme reaksi :
A + S AS (Adsorpsi acrylonitrile)
B + S BS (Adsorbsi air)
AS + BS CS + S (Reaksi di permukaan katalis)
CS C + S (Desorpsi acrylamide)
1. Adsorbsi
Adsorbsi A di permukaan katalis
A + S AS 𝑟𝐴 = 𝑘𝐴𝐶𝐴𝜃𝑣− 𝑘−𝐴𝜃𝐴 ………..(1) dimana KA = A A k k
, dan karena adsorpsi A di permukaan katalis cepat
maka 𝑟𝐴 𝑘𝐴≈ 0 𝜃𝐴 = 𝐾𝐴𝐶𝐴𝜃𝑣 ... (2) kA k-A kA k-A KB k-B k-C kC ks
BAB II Deskripsi Proses 17 Adsorbsi B di permukaan katalis
B + S BS 𝑟𝐵 = 𝑘𝐵𝐶𝐵𝜃𝑣− 𝑘−𝐵𝜃𝐵…....(3)
dimana KB = kB
k−B, dan karena adsorpsi B di permukaan katalis cepat maka 𝑟𝐵
𝑘𝐵 ≈ 0
𝜃𝐵 = 𝐾𝐵𝐶𝐵𝜃𝑣 ... (4)
2. Reaksi permukaan katalis
AS + BS CS + S 𝑟𝑆 = 𝑘𝑆𝜃𝐴𝜃𝐵 ...(5)
3. Desorpsi
Desorpsi produk utama
CS C + S 𝑟𝐶 = 𝑘−𝐶𝜃𝐶− 𝑘𝐶𝐶𝐶𝜃𝑣 ….(6)
dimana 𝐾𝐶 = 𝑘𝐶
𝑘−𝐶, dan karena desorpsi C di permukaan katalis cepat maka 𝑟𝐶 𝑘−𝐶 ≈ 0 𝜃𝐶 = 𝐾𝐶𝐶𝐶𝜃𝑣 ...(7) Neraca permukaan 𝜃𝐴+ 𝜃𝐵+ 𝜃𝐶+ 𝜃𝑣 = 1 𝐾𝐴𝐶𝐴𝜃𝑣+ 𝐾𝐵𝐶𝐵𝜃𝑣+ 𝐾𝐶𝐶𝐶𝜃𝑣+ 𝜃𝑣 = 1 (𝐾𝐴𝐶𝐴+ 𝐾𝐵𝐶𝐵+ 𝐾𝐶𝐶𝐶+ 1)𝜃𝑣 = 1 𝜃𝑣 = 1 1+𝐾𝐴𝐶𝐴+𝐾𝐵𝐶𝐵+𝐾𝐶𝐶𝐶 ………(8) ks k-C kC KB k-B
BAB II Deskripsi Proses 18 Subtitusi persamaan (8) ke persamaan (2) dan (4)
𝜃𝐴 = 𝐾𝐴𝐶𝐴
1+𝐾𝐴𝐶𝐴+𝐾𝐵𝐶𝐵+𝐾𝐶𝐶𝐶 ………(9) 𝜃𝐵 = 𝐾𝐵𝐶𝐵
1+𝐾𝐴𝐶𝐴+𝐾𝐵𝐶𝐵+𝐾𝐶𝐶𝐶 ………(10)
Subtitusi persamaan (9) dan (10) ke persamaan (5) 𝑟𝑆 = 𝑘𝑠𝐾𝐴𝐾𝐵𝐶𝐴𝐶𝐵
(1+𝐾𝐴𝐶𝐴+𝐾𝐵𝐶𝐵+𝐾𝐶𝐶𝐶)2 ………(11)
Dengan ksKB = k, maka persamaan (11) menjadi :
𝑟𝑆 =
𝑘𝐾𝐴𝐶𝐴𝐶𝐵
(1+𝐾𝐴𝐶𝐴+𝐾𝐵𝐶𝐵+𝐾𝐶𝐶𝐶)2……… (12)
2.2.4. Tinjauan Kinetika
Reaksi hidrolisis acrylonitrile menjadi acrylamide dikontrol oleh reaksi pada permukaan aktif katalis, sehingga persamaan kecepatan reaksinya :
𝑟 = 𝑘𝐾𝐴𝐶𝐴𝐶𝐵
(1+𝐾𝐴𝐶𝐴+𝐾𝐵𝐶𝐵+𝐾𝐶𝐶𝐶)2 (13) dengan r : kecepatan reaksi hidrolisis (kmol/s.kg)
CA : konsentrasi acrylonitrile (kmol/m3)
CB : konsentrasi air (kmol/m3)
CC : konsentrasi acrylamide (kmol/m3)
(Onuoha & Wainwright, 1984) Data kecepatan reaksi yang terkoreksi, konsentrasi acrylonitrile, air dan acrylamide yang sesuai digunakan untuk menyusun rumus kecepatan yang berdasarkan konsentrasi.
r =3.39×10
-8C
A0.66C
B1.27C
C-0.46dengan :
k = 3.39 x 10
-8E
A= 49.2 kJ/mol
BAB II Deskripsi Proses 19
Persamaan konstanta kecepatan reaksi
𝑘 = 𝐴𝑒
−𝐸𝐴𝑅𝑇dengan :
R = 8.314 J/mol.K
T = 362 K
maka harga konstanta Arrhenius
𝐴 =
𝑘 𝑒−𝐸𝐴𝑅𝑇𝐴 =
3.39 𝑥 10−8 𝑒− 49200 𝐽 𝑚𝑜𝑙⁄ 8.314 𝐽 𝑚𝑜𝑙.𝐾⁄ 𝑥 362 𝐾= 1.0465
Sehingga persamaan konstanta kecepatan reaksi:
𝑘 = 1.0465 𝑒
(−49200 𝑅𝑇 )
2.2.5. Tinjauan Termodinamika
Pada reaksi dipermukaan katalis, terjadi reaksi hidrolisis antara acrylonitrile dengan air menghasilkan acrylamide. Dengan tinjauan termodinamika, penentuan sifat reaksi berjalan secara eksotermis atau endotermis dapat diketahui dari perhitungan ΔH298.
Reaksi hidrolisis:
CH2=CHCN(l) + H2O(l) CH2=CHCONH2(l)
Tabel 2.1 Harga ΔHfº Masing-masing Komponen
Komponen Harga ΔHfº (kJ/mol)
C3H3N 180,6 H2O -285,8 C3H5ON -170 ΔHRº = ΔHfº produk − ΔHfº reaktan = n.ΔHfº C3H5ON− (n.ΔHfº C3H3N + n. ΔHfº H2O) = [-170− (180,6 − 285,8)] kJ/mol = -64,8 kJ/mol = -64.800 J/mol Raney Copper
BAB II Deskripsi Proses 20 Karena harga ΔH yang dihasilkan negatif, maka reaksi bersifat eksotermis.
Dalam tinjauan termodinamika, hubungan antar panas reaksi, suhu dan konstanta kesetimbangan adalah sebagai berikut:
2 ln RT H dT K d o (Smith-VanNess, 1975) Bila persamaan tersebut diturunkan menjadi:
0 1 1' ' ln T T R H K K (Smith-Van Ness, 1975) Sifat reaksi yang reversible atau irreversible dapat diketahui dari harga konstanta kesetimbangan.
Tabel 2.2 Harga ΔGfº Masing-masing Komponen Komponen Harga ΔGfº (kJ/mol)
C3H3N 191,1
H2O -237,1
C3H5ON -97,9
Bila ditinjau dari energi bebas Gibbs diperoleh :
ΔGfº298 = ΔGfº produk − ΔGfº reaktan
= ΔGfº C3H5ON− (ΔGfº C3H3N + ΔGfº H2O)
= [-97,9− (191,1– 237,1)] kJ/mol = -51,9 kJ/mol = -51.900 J/mol Harga konstanta kesetimbangan pada keadaan standar
ΔGfº298 = -R.T ln K(298)
-51.900 = -8,314 × 298 ln K(298)
K(298) = 1,252×109
Harga konstanta kesetimbangan pada keadaan 362 K
ln(K(343)/ 1,252×109) = - ((-64.800/8,314) × (1/362-1/298))
K(343) = 4,049×107
Dari perhitungan di atas dapat disimpulkan bahwa reaksi yang terjadi adalah reaksi searah ke produk (irreversible).
BAB II Deskripsi Proses 21 2.2.6. Kondisi Operasi
Reaksi pembentukan acrylamide dari acrylonitrile dan air merupakan reaksi hidrolisis, dijalankan dalam reaktor fixed bed, yang beroperasi pada tekanan 3,03 bar dan kisaran suhu 70–120 °C (Onuoha & Wainwright, 1984).
Kondisi operasi sebagai berikut :
a. Komposisi acrylonitrile masuk reaktor
Kisaran komposisi reaktan masuk reaktor adalah 5%-50% berat acrylonitrile (Kirk Othmer,1991). Komposisi reaktan masuk reaktor adalah 13% berat acrylonitrile (Onuoha & Wainwright, 1984).
b. Temperatur
Kisaran temperatur reaksi adalah 70–120 °C, agar reaksi tetap berada fase cair. Dipilih suhu masuk reaktor 89 °C.
c. Tekanan
Tekanan tidak terlalu berpengaruh pada reaksi. Tekanan masuk reaktor sebesar 3,03 bar agar reaksi tetap berjalan dalam fase cair.
2.3. Diagram Alir Proses
2.3.1. Diagram Alir Kualitatif (lihat gambar 2.1 halaman 22) 2.3.2. Diagram Alir Kuantitatif
(lihat gambar 2.2 halaman 23) 2.3.3. Diagram Alir Proses
BAB II Deskripsi Proses 22 Keterangan: C3H3N : Acrylonitrile H2O : Air C3H5ON : Acrylamide MIXER REAKTOR
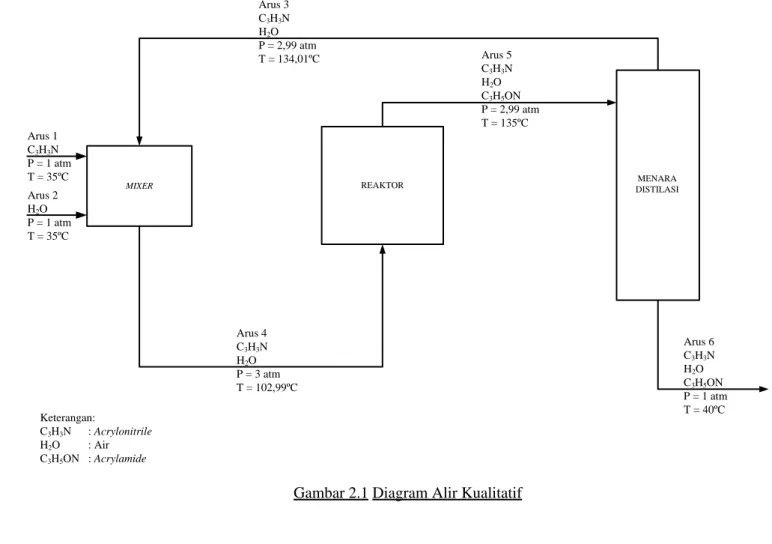
Gambar 2.1 Diagram Alir Kualitatif
Arus 2 H2O P = 1 atm T = 35ºC Arus 1 C3H3N P = 1 atm T = 35ºC Arus 4 C3H3N H2O P = 3 atm T = 102,99ºC Arus 3 C3H3N H2O P = 2,99 atm T = 134,01ºC Arus 5 C3H3N H2O C3H5ON P = 2,99 atm T = 135ºC MENARA DISTILASI Arus 6 C3H3N H2O C3H5ON P = 1 atm T = 40ºC
BAB II Deskripsi Proses 23 Keterangan: C3H3N : Acrylonitrile H2O : Air C3H5ON : Acrylamide MIXER REAKTOR
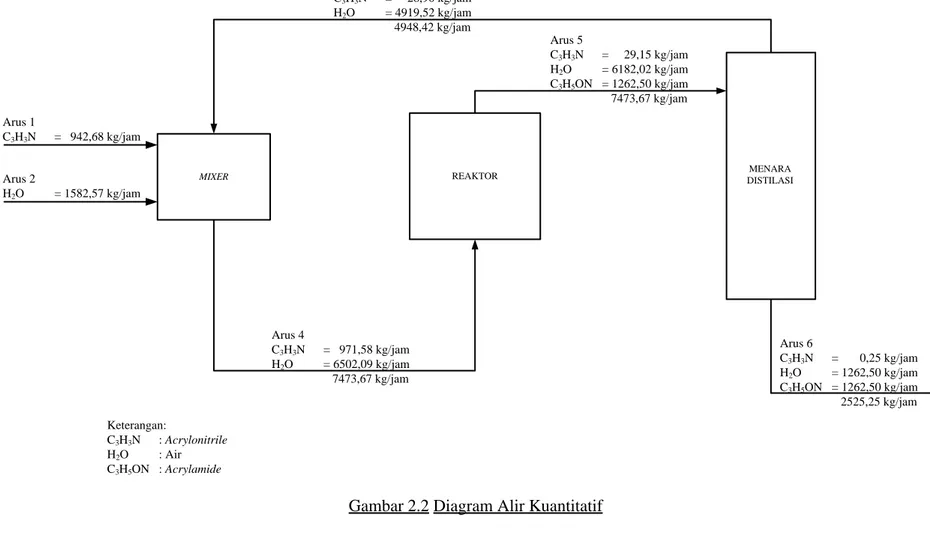
Gambar 2.2 Diagram Alir Kuantitatif
Arus 2 H2O = 1582,57 kg/jam Arus 1 C3H3N = 942,68 kg/jam Arus 4 C3H3N = 971,58 kg/jam H2O = 6502,09 kg/jam 7473,67 kg/jam Arus 3 C3H3N = 28,90 kg/jam H2O = 4919,52 kg/jam 4948,42 kg/jam Arus 5 C3H3N = 29,15 kg/jam H2O = 6182,02 kg/jam C3H5ON = 1262,50 kg/jam 7473,67 kg/jam MENARA DISTILASI Arus 6 C3H3N = 0,25 kg/jam H2O = 1262,50 kg/jam C3H5ON = 1262,50 kg/jam 2525,25 kg/jam
BAB II Deskripsi Proses 24
BAB II Deskripsi Proses 25 2.3.4. Langkah Proses
a. Tahap Persiapan Bahan Baku
Mula–mula bahan baku acrylonitrile dan air yang berasal dari tangki penyimpanan (35°C, 1,01 bar), dipompa menuju mixer. Mixer ini juga menerima arus recycle (acrylonitrile dan air) dari menara distilasi. Komposisi umpan masuk reaktor adalah 13% berat acrylonitrile. Dari mixer diperoleh campuran acrylonitrile dan air dengan komposisi 13% acrylonitrile yang kemudian dipompa menuju reaktor.
b. Tahap Pembentukan Acrylamide
Campuran acrylonitrile dan air dengan komposisi 13% acrylonitrile masuk ke dalam reaktor yang merupakan reaktor fixed bed. Reaktor bekerja secara adiabatis dan non isotermal, dengan suhu masuk reaktor 89 °C dan tekanan 3,03 bar, agar reaksi tetap berjalan pada fase cair. Di dalam reaktor terjadi proses hidrolisis acrylonitrile menjadi acrylamide dengan adanya katalis raney copper dalam bed reaktor. Produk reaktor terdiri atas acrylamide, sisa acrylonitrile dan air.
c. Tahap Pemurnian Produk
Produk keluaran reaktor (acrylamide, sisa acrylonitrile dan air) diumpankan ke dalam menara distilasi untuk menguapkan acrylonitrile dan air, sehingga diperoleh hasil bawah larutan acrylamide 50%. Tekanan operasi kolom dijaga 3,03 bar. Selanjutnya hasil atas menara distilasi dialirkan kembali ke mixer. Sedangkan produk bottom sebagai hasil bawah distilasi dialirkan dan sebagian dipanaskan menggunakan reboiler. Hasil keluaran dari reboiler sebagian dialirkan kembali ke dalam menara distilasi dan sebagian lagi diturunkan suhunya hingga 40 °C menuju tangki penyimpanan acrylamide.
BAB II Deskripsi Proses 26 2.4. Neraca Massa dan Neraca Panas
Produk : Acrylamide 50% solution
Kapasitas : 20.000 ton/tahun
Satu tahun produksi : 330 hari Waktu operasi selama 1 hari : 24 jam
2.4.1. Neraca Massa
Neraca massa prarancangan pabrik acrylamide sesuai dengan Gambar 2.2
Tabel 2.3 Neraca Massa Mixer
Komponen
Input Output
Arus 1 Arus 2 Arus 3
(recycle) Arus 4
kg/jam kg/jam kg/jam kg/jam
C3H3N 942,6821 - 28,8948 971,5769
H2O - 1.582,5704 4.919,5210 6.502,0915 Total 7.473,6683 7.473,6683
Tabel 2.4 Neraca Massa Reaktor
Komponen Input Output Arus 4 Arus 5 kg/jam kg/jam C3H3N 971,5769 29,1473 H2O 6.502,0915 6.182,0210 C3H5ON - 1.262,5000 Total 7.473,6683 7.473,6683
Tabel 2.5 Neraca Massa Menara Distilasi
Komponen
Input Output
Arus 5 Arus 3 Arus 6
kg/jam kg/jam kg/jam
C3H3N 29,1473 28,8948 0,2525
H2O 6.182,0210 6.502,0915 1.262,5000
C3H5ON 1.262,5000 - 1.262,5000
BAB II Deskripsi Proses 27 Tabel 2.6 Neraca Massa Total
Komponen
Input Output
Arus 1 Arus 2 Arus 6
kg/jam kg/jam kg/jam
C3H3N 942,6821 - 0,2525
H2O - 1.582,5704 1.262,5000
C3H5ON - - 1.262,5000
Total 7.473,6683 7.473,6683
2.4.2. Neraca Panas
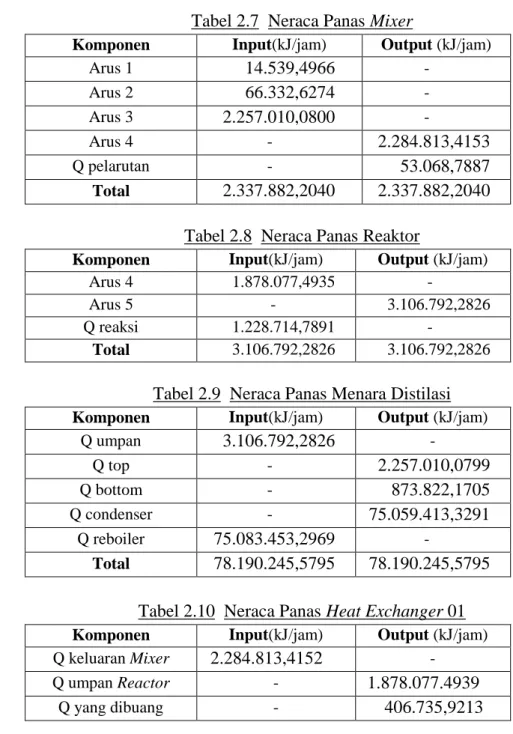
Tabel 2.7 Neraca Panas Mixer
Komponen Input(kJ/jam) Output (kJ/jam)
Arus 1 14.539,4966 - Arus 2 66.332,6274 - Arus 3 2.257.010,0800 - Arus 4 - 2.284.813,4153 Q pelarutan - 53.068,7887 Total 2.337.882,2040 2.337.882,2040
Tabel 2.8 Neraca Panas Reaktor
Komponen Input(kJ/jam) Output (kJ/jam)
Arus 4 1.878.077,4935 -
Arus 5 - 3.106.792,2826
Q reaksi 1.228.714,7891 -
Total 3.106.792,2826 3.106.792,2826
Tabel 2.9 Neraca Panas Menara Distilasi Komponen Input(kJ/jam) Output (kJ/jam)
Q umpan 3.106.792,2826 - Q top - 2.257.010,0799 Q bottom - 873.822,1705 Q condenser - 75.059.413,3291 Q reboiler 75.083.453,2969 - Total 78.190.245,5795 78.190.245,5795
Tabel 2.10 Neraca Panas Heat Exchanger 01 Komponen Input(kJ/jam) Output (kJ/jam)
Q keluaran Mixer 2.284.813,4152 -
Q umpan Reactor - 1.878.077.4939
BAB II Deskripsi Proses 28 Tabel 2.11 Neraca Panas Heat Exchanger 02
Komponen Input(kJ/jam) Output (kJ/jam)
Q keluaran EV 873.822,1705 -
Q produk - 109.913,8413
Q yang dibuang - 763.908,3292
Tabel 2.12 Neraca Panas Total
Komponen Input (kJ/jam) Output (kJ/jam)
Arus 1 14.539,4966 - Arus 2 66.332,6274 - Q reboiler 75.083.453,2969 - Q reaksi 1.228.714,7887 - Arus 6 - 109.913,8413 HE-01 - 406.735,9213 Q condenser - 75.059.413,3291 HE-02 - 763.908,3292 Q pelarutan - 53.068,7887 Total 76.393.040,2096 76.393.040,2096
2.5. Tata Letak Pabrik dan Peralatan Proses
Tata letak pabrik adalah tempat kedudukan dari seluruh bagian pabrik, meliputi tempat kerja alat, tempat kerja karyawan, tempat penyimpanan barang, tempat penyediaan sarana utilitas, dan sarana lain bagi pabrik. Beberapa faktor perlu diperhatikan dalam penentuan tata letak pabrik, antara lain adalah pertimbangan ekonomis (biaya konstruksi dan operasi), kebutuhan proses, pemeliharaan keselamatan, dan perluasan dimasa mendatang.
Bangunan pabrik meliputi area proses, area tempat penyimpanan bahan baku dan produk, area utilitas, bengkel mekanik untuk pemeliharaan, gudang untuk pemeliharaan dan plant supplies, ruang kontrol, laboratorium untuk pengendalian mutu dan pengembangan, unit pemadam kebakaran, kantor administrasi, kantin, poliklinik, tempat ibadah, area parkir, dan taman bagi para pegawai.
Pengaturan letak peralatan proses pabrik harus dirancang seefisien mungkin. Beberapa pertimbangan perlu diperhatikan yaitu ekonomi, kebutuhan proses, operasi, perawatan, keamanan, perluasan dan pengembangan pabrik. Peletakan alat-alat proses harus sebaik mungkin sehingga memberikan biaya konstruksi
BAB II Deskripsi Proses 29 dengan operasi minimal. Biaya konstruksi dapat diminimalkan dengan mengatur letak alat sehingga menghasilkan pemipaan terpendek dan membutuhkan bahan konstruksi paling sedikit. Peletakan alat harus memberikan ruangan cukup bagi masing-masing alat agar dapat beroperasi dengan baik, dengan distribusi utilitas mudah. Peralatan membutuhkan perhatian lebih dari operator harus diletakkan dengan ruang kontrol. Valve, tempat pengambilan sampel, dan instrumen harus diletakkan pada ketinggian tertentu sehingga mudah dijangkau oleh operator. Peletakan alat harus memperhatikan ruangan untuk perawatan. Misal, pada heat exchanger memerlukan cukup ruang untuk pembersihan pipa. Peletakan alat-alat proses harus sebaik mungkin, agar jika terjadi kebakaran tidak ada pekerja terperangkap di dalamnya serta mudah dijangkau kendaraan atau alat pemadam kebakaran.
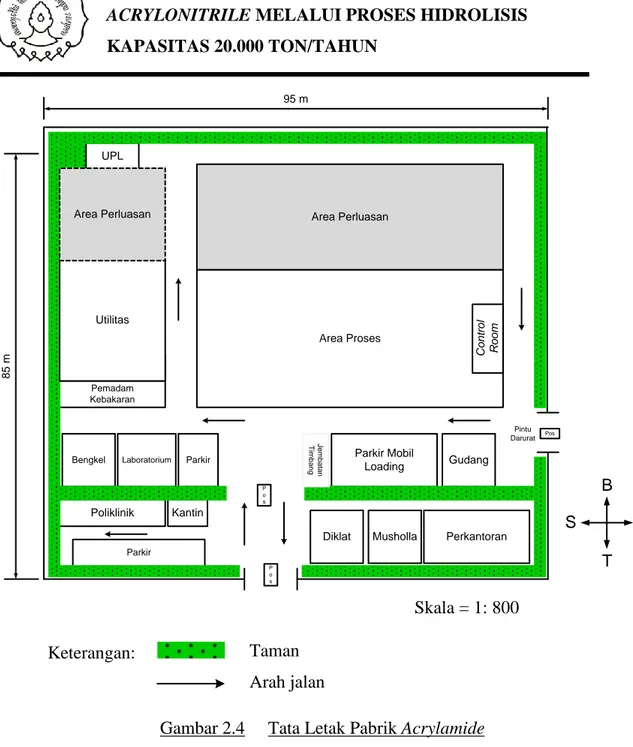
Susunan tata letak pabrik harus sangat diperhatikan sehingga memungkinkan adanya distribusi bahan-bahan dengan baik, cepat dan efisien. Hal tersebut akan sangat mendukung kelancaran di dalam proses produksi pabrik yang dirancang. Sketsa tata letak pabrik dapat dilihat pada Gambar 2.4 dan gambar tata letak peralatan proses dapat dilihat pada Gambar 2.5.
BAB II Deskripsi Proses 30 UPL Ruang Genera tor Laboratorium Poliklinik Kantin Pemadam Kebakaran Parkir Mobil Loading Bengkel Perkantoran Gudang P o s Parkir P o s Parkir Pintu Darurat 8 5 m 95 m J e m b a ta n T im b a n g Musholla Diklat Pos Area Perluasan C o n tr o l R o o m Area Proses Utilitas Area Perluasan B T U S
Gambar 2.4 Tata Letak Pabrik Acrylamide Taman
Arah jalan
Skala = 1: 800
BAB II Deskripsi Proses 31 60 m 40 m C o n tr o l R o o m T-03 T-01 HE-02 ACC CD RB M R MD HE-01 T-02 Keterangan Gambar : T-01 = Tangki Acrylonitrile T-02 = Tangki Air T-03 = Tangki Acrylamide M = Mixer R = Reaktor MD = Menara Distilasi HE-01 = Cooler 1 HE-02 = Cooler 2 CD = Condenser RB = Reboiler ACC = Accumulator
Gambar 2.5 Tata Letak Peralatan Proses