KERANGKA PEMIKIRAN
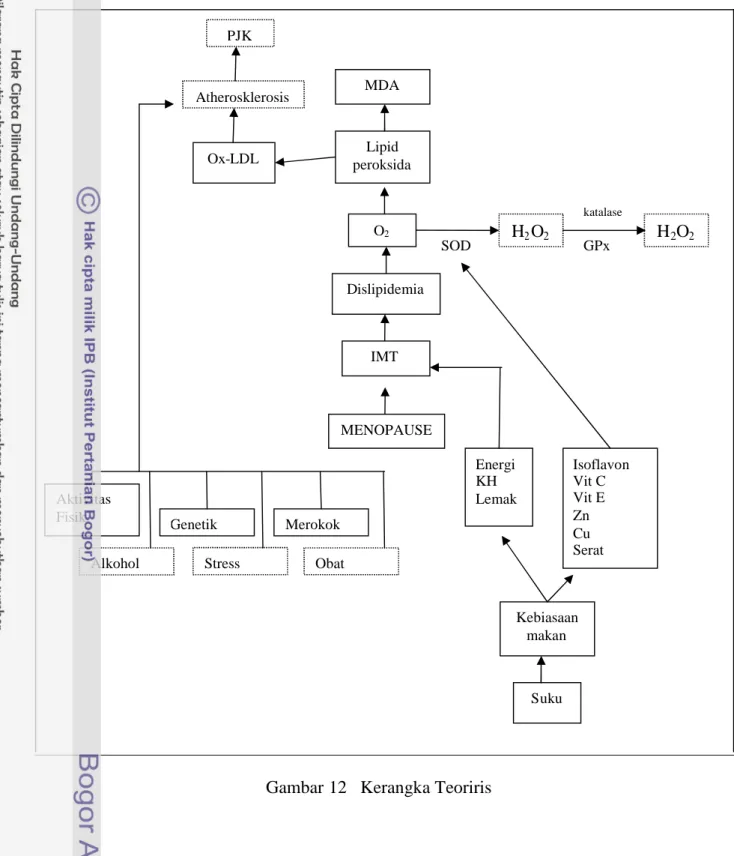
Menopause adalah kondisi fisiologis pada wanita dimana terjadi penurunan fungsi ovarium yang mengakibatkan penurunan produksi hormon estrogen. Hal tersebut dapat mengakibatkan gangguan metabolisme lemak sehingga meningkatkan risiko terjadinya peroksidasi lipid yang dapat mengakibatkan risiko terjadinya PJK. Konsumsi antioksidan dapat mengurangi kemungkinan terjadinya lipid peroksida. Antioksidan yang dimaksud dapat diperoleh dari luar tubuh (eksogen) seperti dari makanan (vit C, vit E, selenium, Zn, dan Cu) maupun antioksigen endogen atau yang terbentuk dari dalam tubuh (SOD, katalase dan glutation peroksidase). Antioksidan dari luar akan berpengaruh pada kerja antioksidan endogen.
Penyakit jantung koroner (PJK) secara umum dapat disebabkan karena adanya faktor risiko lipid yang terdiri dari meningkatnya kolesterol, LDL kolesterol, trigliserida dan turunnya HDL kolesterol. Faktor risiko yang kedua adalah faktor risiko non lipid yang terdiri dari merokok, hipertensi, aktifitas fisik, obesitas, diabetes mellitus, konsumsi lemak (SAFA, MUFA, PUFA), alkohol, stress dan konsumsi obat tertentu. Faktor risiko yang tidak bisa dihindari terdiri dari jenis kelamin, usia, keturunan, riwayat keluarga.
Tahap awal perjalanan menuju PJK adalah konsumsi yang tidak seimbang (khususnya tinggi karbohidrat, lemak dan protein) yang mengakibatkan kegemukan ditandai dengan peningkatan IMT. Kegemukan akan menyebabkan penumpukan lemak visceral yang selanjutnya mengakibatkan disregulasi pengeluaran adipocytokin. Hal ini akan berisiko pada hipertensi, diabetes mellitus dan dislipidemia sehingga akan mempermudah terjadinya atherosklerosis dan PJK.
Gambar 12 Kerangka Teoriris Diteliti Tidak diteliti PJK Atherosklerosis IMT Dislipidemia Lipid peroksida Kebiasaan makan Suku Isoflavon Vit C Vit E Zn Cu Serat Energi KH Lemak Merokok Aktivitas Fisik Stress Genetik Obat MENOPAUSE Alkohol O2 H2O2 H2O2 SOD katalase GPx MDA Ox-LDL
METODE PENELITIAN
Desain Penelitian
Desain penelitian adalah 2x4 minggu cross-over paralel group, RCT (randomized control triall) dengan washout. Cross-over merupakan suatu cara untuk membandingkan beberapa perlakuan pada sampel yang sama di waktu yang berbeda, sehingga akan diperoleh hasil yang lebih tepat dengan jumlah sampel yang lebih sedikit dibandingkan dengan metode paralell group trials (Hills & Armitage 1979; Garcia et al. 2004). Untuk mengurangi carryover effect maka diterapkan satu periode washout selama 4 minggu. Dalam pelaksanaan penelitian, peneliti tidak mengetahui jenis perlakuan yang diterima oleh setiap sampel, hanya petugas lapangan dan sampel yang mengetahui perlakuan apa yang diberikan.
Protokol pelaksanaan penelitian sudah mendapatkan Persetujuan Etik dari Badan Penelitian dan Pengembangan Kesehatan Departemen Kesehatan Republik Indonesia No: LB.03.04/KE/6693/2009.
Tempat dan Waktu Penelitian
Lokasi penelitian berada di Kota Bogor. Sampel yang diambil berasal dari beberapa posbindu yang menjadi binaan Dinkes Kota Bogor. Dasar pemilihan lokasi adalah keaktifan posbindu sehingga mempermudah operasional penelitian di lapangan. Lokasi penelitian terpilih berasal dari Kelurahan Tanah Sareal, Pondok Rumput, Ciwaringin, Ciomas dan Sindang Sari.
Penapisan sampel mulai dilakukan sejak bulan Maret hingga April 2009, sedangkan intervensi dilakukan mulai Mei hingga Agustus 2009. Penelitian ini dibagi menjadi 2 fase, dimana fase I pengambilan darah dilakukan pada 26 Mei 2009 (sebelum intervensi) dan 24 Juni 2009 (setelah intervensi), sedangkan fase II dilakukan pada 22 Juli 2009 (sebelum intervesi) dan 20 Agustus 2009 (setelah intervensi). Selanjutnya analisis serum darah dilakukan sejak April 2009 hingga Januari 2010.
Populasi dan Sampel Penelitian
1. Populasi Target
Target populasi pada penelitian ini adalah wanita yang telah menopause antara 1 hingga 5 tahun dan tinggal di wilayah Kota Bogor. Populasi studi adalah wanita menopause antara 1 hingga 5 tahun yang menjadi binaan posbindu terpilih. Selanjutnya populasi tersebut harus memenuhi kriteria inklusi dan eksklusi yang telah ditetapkan.
2. Sampel
Sampel harus memenuhi kriteria penerimaan melalui anamnesis, pemeriksaan fisik, antropometri, dan hasil penapisan pemeriksaan darah. Berdasar hasil penapisan terpilih sampel yang selanjutnya akan dijelaskan tujuan penelitian, perlakuan penelitian yang akan dilakukan, manfaat dan kerugian menjadi sampel penelitian. Jika sampel bersedia, maka akan menandatangani formulir persetujuan tertulis terhadap tindakan media yang dilakukan.
3. Penentuan Jumlah Sampel
Penelitian ini menggunakan rumus sampel desain cross over Sd
N = 10.5 ---2 D 10.5 = 90%, P 0,05
Sd = standar deviasi kolesterol total = 34.6 mm/dL (Alrasyid 2007) D = perbedaan atau efek yang diharapkan =19.6 mm/dL (Alrasyid
2007)
N = 33
Banyaknya sampel yang diperlukan dengan power 90% dan p 0,05 berdasar hasil penelitian yang pernah dilakukan oleh Alrasyid (2007 ) minimal dibutuhkan 33 sampel. Mengingat waktu penelitian yang relatif lama (3.5 bulan) dan untuk mengantisipasi drop out selama penelitian, maka jumlah minimal sampel ditambah 100%, sehingga jumlah sampel di awal penelitian diambil sebanyak 67 sampel.
Sampel terpilih akan dibagi secara random untuk menentukan kelompok perlakuan. Random dilakukan menggunakan tabel acak. Proporsi jumlah sampel terbagi rata pada 2 kelompok perlakuan. Pengacakan dilakukan oleh personil yang tidak turut dalam kegiatan penelitian dan tidak disaksikan sampel dan peneliti (peneliti tidak mengetahui sampel terpilih untuk masing-masing perlakuan).
Kriteria Inklusi, Eksklusi dan Pengeluaran
Adapun kriteria inklusi dan eksklusi sampel adalah. Kriteria Inklusi
- Wanita menopause, masa menopause antara 1 tahun hingga 5 tahun - Menopause terjadi secara alami
- Bersedia menjadi responden dan mematuhi peraturan yang dibuat selama penelitian dengan mengisi surat pernyataan
- Salah satu profil lipid darah tidak normal (kolesterol > 200 mg/dL, kolesterol-LDL > 130 mg/dL trigliserida > 150 mg/dL, kolesterol-HDL < 40 mg/dL) atau mengalami hipertensi (sistolik > 140 mmHg dan atau diastolik > 90 mmHg)
Kriteria eksklusi
- Mempunyai riwayat atau sedang mengalami penyakit hati, ginjal, gangguan tiroid, kanker, PJK, stroke, diabetes mellitus dan penyakit lainnya
- Rutin mengkonsumsi suplemen
- Rutin mengkonsumsi obat hipoglikemi, fitofarmaka, hipolipid. - Penganut vegetarian
- Menggunakan terapi estrogen Kriteria Pengeluaran
- Pada saat masuk dalam fase perlakuan, sampel tidak mengonsumsi tempe selama 3 hari berturut-turut
- Indikasi kriteria eksklusi ditemukan pada sampel sewaktu penelitian berlangsung
Alur Penelitian
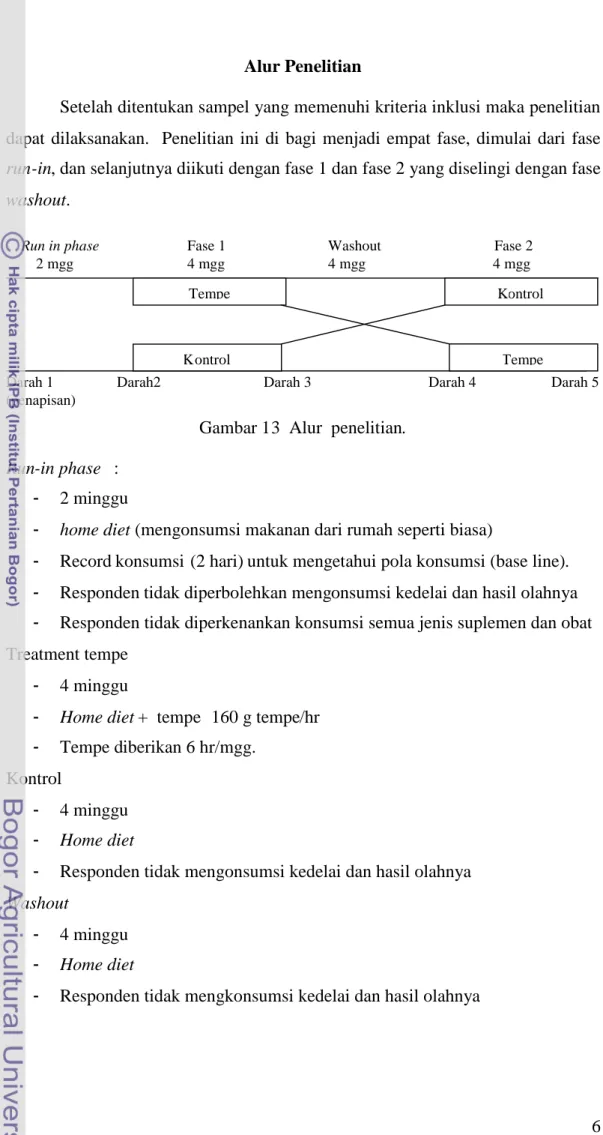
Setelah ditentukan sampel yang memenuhi kriteria inklusi maka penelitian dapat dilaksanakan. Penelitian ini di bagi menjadi empat fase, dimulai dari fase
run-in, dan selanjutnya diikuti dengan fase 1 dan fase 2 yang diselingi dengan fase washout.
Run in phase Fase 1 Washout Fase 2
2 mgg 4 mgg 4 mgg 4 mgg
Darah 1 Darah2 Darah 3 Darah 4 Darah 5
(penapisan)
Gambar 13 Alur penelitian.
Run-in phase :
- 2 minggu
- home diet (mengonsumsi makanan dari rumah seperti biasa)
- Record konsumsi (2 hari) untuk mengetahui pola konsumsi (base line). - Responden tidak diperbolehkan mengonsumsi kedelai dan hasil olahnya - Responden tidak diperkenankan konsumsi semua jenis suplemen dan obat Treatment tempe
- 4 minggu
- Home diet + tempe 160 g tempe/hr
- Tempe diberikan 6 hr/mgg. Kontrol
- 4 minggu - Home diet
- Responden tidak mengonsumsi kedelai dan hasil olahnya
Washout
- 4 minggu - Home diet
- Responden tidak mengkonsumsi kedelai dan hasil olahnya
Tempe Kontrol
Responden mempersiapkan seluruh kebutuhan makannya sendiri kecuali tempe yang disiapkan oleh peneliti.
Tahap pertama penapisan adalah mendaftar semua ibu menopause dengan masa menopause 12 bln – 59 bln. Calon sampel diundang untuk mendapat penjelasan tentang penelitian meliputi tahapan penelitian serta kerugian dan keuntungan menjadi sampel. Calon sampel yang bersedia mengikuti tahapan penelitian diwajibnya mengisi form persetujuan. Form persetujuan merupakan dasar untuk dimulainya penelitian yaitu tahap run in.
Sebelum run in, dilakukan pemeriksaan spesimen darah dan antropometri sebagai pengukuran dasar (base line) untuk penapisan sampel. Calon sampel wajib puasa sekitar 10-12 jam sebelum dilakukan pengambilan darah. Pengambilan darah serentak dilakukan pada hari yang sama dimulai jam 6.30 WIB hingga jam 9.00 WIB, selanjutnya darah di bawa ke laboratorium untuk dipisahkan serum nya dan serum disimpan dalam suhu -200C sebelum dilakukan pemeriksaan laboratorium. Parameter yang diukur pada tahap tersebut meliputi: kolesterol total, K-LDL, K-HDL, trigliserida dan tekanan darah. Individu yang memenuhi kriteria inklusi akan dimasukkan sebagai sampel penelitian.
Sampel terpilih akan menjalani run in phase, dimana mereka mulai menghindari konsumsi tempe, produk kedelai, maupun suplement yang biasa dikonsumsi selama minimal 2 minggu. Fase run in dilakukan selama 2 minggu untuk membersihkan kadar isoflavon dalam darah sampel dan merupakan tahap sosialisasi sebelum masuk pada tahap intervensi.
Setelah run in selesai atau sebelum fase 1 dimulai, maka dilakukan pengambilan darah ke 2. Selanjutnya secara random, sampel dibagi menjadi 2 kelompok yaitu kelompok perlakuan (intervensi tempe) dan kelompok kontrol. Diakhir fase 1 dilakukan kembali pengambilan darah (yang ke 3), diikuti dengan
washout selama 4 minggu. Selesai washout kemudian dilakukan pengambilan
darah ke 4, setelah itu masuk fase 2 yaitu fase cross over, dimana sampel yang pada fase 1 masuk pada kelompok intervensi, maka pada fase ke 2 masuk ke kelompok plasebo, begitu juga sebaliknya. Fase 2 juga dilakukan selama 4 minggu. Setelah 4 minggu fase 2 berakhir, maka dilakukan pengambilan darah terakhir (ke 5).
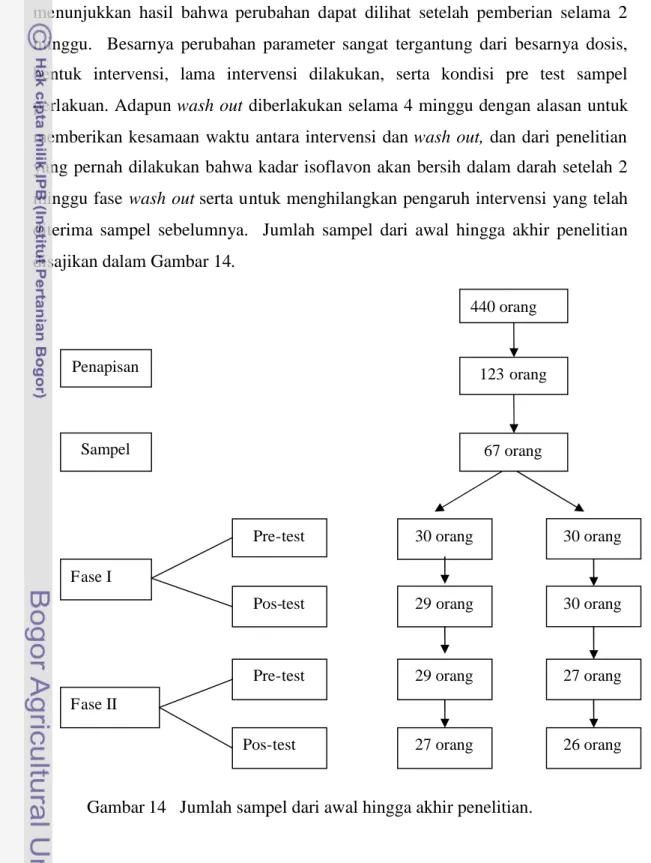
Fase Intervensi diberikan selama 4 minggu berdasar hasil berbagai penelitian terdahulu yang menyatakan bahwa minimal intervensi protein kedelai maupun isoflavon dilakukan selama 2 minggu, dan dalam selang waktu tersebut dapat dilihat perubahan pada parameter yang diukur. Penelitian terdahulu yang memberikan protein kedelai maupun isoflavon terhadap profil lipid juga menunjukkan hasil bahwa perubahan dapat dilihat setelah pemberian selama 2 minggu. Besarnya perubahan parameter sangat tergantung dari besarnya dosis, bentuk intervensi, lama intervensi dilakukan, serta kondisi pre test sampel perlakuan. Adapun wash out diberlakukan selama 4 minggu dengan alasan untuk memberikan kesamaan waktu antara intervensi dan wash out, dan dari penelitian yang pernah dilakukan bahwa kadar isoflavon akan bersih dalam darah setelah 2 minggu fase wash out serta untuk menghilangkan pengaruh intervensi yang telah diterima sampel sebelumnya. Jumlah sampel dari awal hingga akhir penelitian disajikan dalam Gambar 14.
Gambar 14 Jumlah sampel dari awal hingga akhir penelitian.
123 orang Penapisan Sampel Fase I 67 orang 30 orang 30 orang
Pos-test 29 orang 30 orang
29 orang 27 orang 27 orang 26 orang Pos-test Pre-test Pre-test Fase II 440 orang
Sampel total terpilih sebanyak 67 orang, namun yang hadir pada saat pengambilan darah pre-test hanya 60 orang. Sebanyak 7 orang tidak hadir karena bekerja di tempat yang jauh sehingga tidak memungkinkan untuk diberi intervensi. Dari 60 orang yang mengikuti awal intervensi, terdapat 53 orang yang mengikuti semua prosedur penelitian secara lengkap. Terjadi drop out sebanyak 7 orang disebabkan karena 1 orang sakit (tetanus), 1 orang tidak hadir saat pengambilan darah terakhir, dan 5 orang tidak bersedia melanjutkan intervensi dengan alasan non medis.
Untuk setiap pengambilan darah ke 1 hingga ke 5 dilakukan prosedur yang sama, diawali dengan puasa selama 10-12 jam sebelumnya dan pengambilan darah dilakukan serentak pada hari yang sama dimulai pukul 6.30 hingga selesai. Darah selanjutnya dibawa ke laboratorium dan dipisahkan serumnya, dibagi ke dalam beberapa cuvet kecil dengan volume sesuai dengan jenis pemeriksaan. Serum disimpan pada suhu -200C sebelum didistribusikan ke laboratorium yang akan melakukan analisis lebih lanjut.
Intervensi
Tempe yang digunakan sebagai bahan intervensi berasal dari satu produsen tempe yang ada di Kota Bogor, hal tersebut untuk menjamin keseimbangan kandungan isoflavon yang dihasilkan karena menggunakan prosedur yang selalu sama saat pembuatannya. Kedelai sebagai bahan dasar pembuatan tempe adalah merek Americana, sedangkan ragi yang digunakan diproduksi oleh PT. Aneka Fermentasi Industri, Bandung (BPOM RI. MD 262628001051).
Teori yang ada menunjukkan bahwa kandungan isoflavon tempe akan lebih tinggi pada tempe yang mengalami 2 kali perebusan. Berdasar hal tersebut, peneliti menunjuk satu produsen dengan proses pembuatan melalui perebusan 2 kali. Sebelum ditentukan produsen tempe yang akan diambil sebagai pemasok, dilakukan analisa isoflavon pada 2 tempat pembuatan tempe, dimana kedua tempat tersebut mengerjakan pembuatan tempe dengan proses yang berbeda.
Hasil analisis yang dilakukan sebanyak 3 kali uji isoflavon menunjukkan bahwa 160 g tempe mentah basah mengandung rata-rata 49.3 mg isoflavon.
Kandungan protein dalam 160 gr tempe mentah 26.4 g yang masih dianggap aman untuk diberikan setiap harinya.
Intervensi tempe yang diberikan sebanyak 160 g per hari, 6 hari dalam seminggu selama 4 minggu. Selama fase intervensi, setiap hari jam 06.00 WIB produsen tempe mengantar tempe mentah ke peneliti. Proses pemasakan membutuhkan waktu sekitar 1 jam dan proses pengemasan membutuhkan waktu sekitar 30 menit. Sekitar jam 09.00 WIB tempe matang yang telah dikemas siap didistribusikan ke sampel, dan tiba dirumah sampel sekitar pukul 09.30 WIB hingga 11.00 WIB. Tempe tidak harus dihabiskan pada satu saat tertentu, namun diminta untuk dihabiskan dalam satu hari. Untuk mengontrol kepatuhan konsumsi tempe, maka setiap hari petugas pengantar tempe menanyakan konsumsi tempe sehari sebelumnya.
Tempe diberikan sebanyak 160 g atau setara dengan 4 potong tempe ukuran sedang. Menu tempe yang diberikan diganti setiap hari dengan ragam jenis masakan : 1. Panggang rempah 2. Oseng 3. Bumbu kencur 4. Panggang opor 5. Sukiyaki 6. Semur 7. Bumbu kacang 8. Kari kemangi 9. Bacem 10. Sambal kencur 11. Botok Instrumen Penelitian
Formulir yang digunakan dalam penelitian ini terdiri dari:
1. Formulir karakteristik sampel (usia, pendidikan, pekerjaan, pengeluaran, suku, lama menopause, kebiasaan Olah Raga dan merokok)
2. Formulir pengetahuan gizi 3. Formulir pemeriksaan darah
4. Formulir IMT
5. Formulir antropometri (BB, TB)
6. Formulir kesehatan (tekanan darah, status kesehatan saat pemeriksaan) 7. Formulir konsumsi : Food Frequency Quesioner (FFQ) dan food record.
Peralatan dan Bahan
Peralatan dan bahan yang digunakan meliputi
1. Timbangan BB merek seca dengan ketelitian 0,1 kilogram 2. Pengukur TB microtoise dengan ketelitian 0,1 centimeter
3. Pengukur tekanan darah sphygmomanometer dengan ketelitian 1,0 mmHg 4. Peralatan pengambil darah: syringe 10cc, kapas, alkohol, plester, tabung 5. Peralatan laboratorium: tube, sentrifuse, freezer, lemari es, shaker, printer,
spectrophotometer UV-1601 dengan panjang gelombang 200-800 nm (untuk pemeriksaan MDA) , ELISA reader (untuk pemeriksaan SOD dan OxLDL), Hitachi 902 analyzer (enzymatic colorimetric test untuk pemeriksaan profil lipid), AAS (untuk pemeriksaan Zn).
Jenis dan Cara Pengumpulan Data
Data yang dikumpulkan selama penelitian meliputi karakterisik responden yang terdiri dari: nama, tanggal lahir, menstruasi terakhir, lama menopause, suku bangsa, status pernikahan, frekuensi kehamilan, jumlah anak, keikutsertaan KB, jenis KB yang digunakan. Identitas responden dikumpulkan di awal tahap penelitian. Data sosial ekonomi meliputi : pendidikan, pekerjaan, pendapatan, pengeluaran, jumlah anggota keluarga dalam satu rumah. Data aktivitas fisik meliputi aktivitas di rumah dan olah raga (lama, jenis, dan frekuensi).
Data status kesehatan yang dikumpulkan meliputi riwayat penyakit, konsumsi obat, kebiasaan konsumsi suplement. Pemeriksaan kesehatan dilakukan oleh dokter yang meliputi pemeriksaan fisik, anamnesa, keluhan dan riwayat penyakit. Pemeriksaan kesehatan dilakukan setiap kali akan dilakukan pengambilan darah.
kali dilakukan pengambilan darah. Pengukuran TB menggunakan Microtoise dengan ketelitian 0.1 cm, pengukuran BB menggunakan timbangan injak merek seca ketelitian 0.1 kg, dan pengukuran tekanan darah menggunakan alat ukur tekanan darah tensimeter raksa.
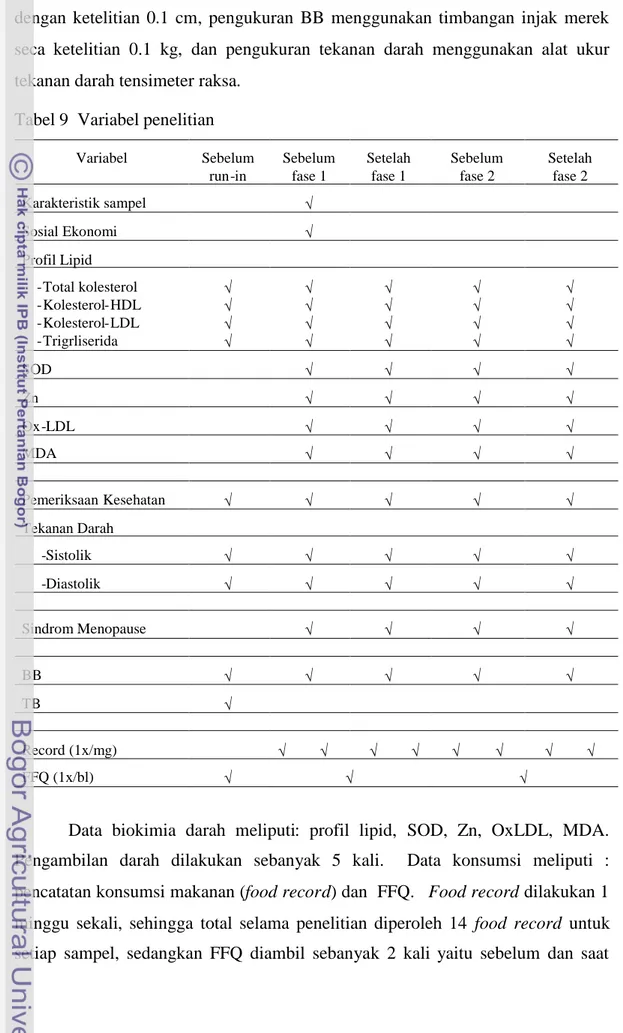
Tabel 9 Variabel penelitian
Variabel Sebelum run-in Sebelum fase 1 Setelah fase 1 Sebelum fase 2 Setelah fase 2 Karakteristik sampel Sosial Ekonomi Profil Lipid -Total kolesterol -Kolesterol-HDL -Kolesterol-LDL -Trigrliserida SOD Zn Ox-LDL MDA Pemeriksaan Kesehatan Tekanan Darah -Sistolik -Diastolik Sindrom Menopause BB TB Record (1x/mg) FFQ (1x/bl)
Data biokimia darah meliputi: profil lipid, SOD, Zn, OxLDL, MDA. Pengambilan darah dilakukan sebanyak 5 kali. Data konsumsi meliputi : pencatatan konsumsi makanan (food record) dan FFQ. Food record dilakukan 1 minggu sekali, sehingga total selama penelitian diperoleh 14 food record untuk setiap sampel, sedangkan FFQ diambil sebanyak 2 kali yaitu sebelum dan saat
penelitian untuk melihat perubahan frekuensi konsumsi. Dari hasil food record dianalisis konsumsi energi, karbohidrat, lemak, kolesterol, PUFA, MUFA, SAFA, protein, vitamin E, Se, Zn, Cu dan Fe serta serat. Kepatuhan konsumsi tempe ditanyakan setiap hari (pada keesokan harinya, bersamaan dengan pemberian tempe pada sampel).
Tabel 10 Indikator dan metode pengumpulan data
Variabel Indikator Kunci Metode
Karakteristik responden
Umur, lama menopause, frekuensi kehamilan, alat KB yang pernah digunakan
Wawancara berdasar kuesioner
Sosial ekonomi Pengeluaran per kapita/bulan Pekerjaan
Pendidikan
Wawancara berdasar kuesioner
Status kesehatan Pernah/tidak pernah sakit, kebiasaan minum obat, pemeriksaan fisik kesehatan
Pemeriksaan dan Wawancara
Riwayat penyakit Jenis penyakit yang pernah diderita Wawancara berdasar kuesioner Konsumsi
Food record FFQ
Konsumsi per hari
Frekuensi dalam 1 bulan terakhir
Pengisian formulir food record Wawancara berdasar kuesioner
Antropometri BB, TB Pengukuran BB dan TB
Biokimia darah Kolesterol total K-LDL K-HDL Trigliserida SOD MDA Ox-LDL Zn Analisis laboratorium
Zat gizi dan non gizi pada tempe
Protein dan Asam amino Lemak dan asam lemak Zn, Fe, Cu
Isoflavon
Analisis laboratorium
Pengambilan sampel darah dilakukan 5 kali (1 kali penapisan dan 4 kali saat perlakuan). Sampel darah diambil sebanyak 8 ml dimasukkan dalam tabung tanpa koagulan dan kemudian diputar dengan sentrifuse untuk diambil serumnya. Serum di bagi menjadi 7 (5 untuk variabel dan 2 cadangan). Serum disimpan dalam freezer -200C sebelum dilakukan analisis. Kandungan gizi dan non gizi tempe yang dianalisis adalah : protein, asam amino, lemak, asam lemak, Zn, Cu, dan isoflavon total.
Pengendalian Kualitas Data
Tim peneliti direkruit dengan seleksi sehingga memenuhi kriteria tertentu dengan tujuan agar penelitian menghasilkan data yang berkualitas. Kriteria petugas lapangan adalah sebagai berikut:
- perempuan - lulusan S-1 gizi
- mempunyai pengalaman dalam mewawancarai responden - mempunyai pengalaman di lapangan
- dapat berkomunikasi dengan baik - tertarik dengan penelitian ini - disiplin
- mempunyai komitmen untuk menyelesaikan pekerjaan
- mempunyai kapasitas untuk membuat laporan kegiatan lapangan - mampu bekerja sendiri maupun sebagai tim
Semua calon petugas lapangan/pewawancara dilatih selama 1 hari di dalam ruangan dan 1 hari di lapangan. Materi yang diberikan selama pelatihan adalah latar belakang dan tujuan penelitian survei, desain penelitian, metode pemilihan sampel, bagaimana menghadapi responden, penguasaan kuesioner, proses wawancara, teknik wawancara (pendekatan, pelaksanaan, probing), penyelesaian masalah dan simulasi (praktek di kelas). Hari kedua akan dilakukan ujicoba wawancara di lapangan dengan kriteria responden mirip dengan responden penelitian. Setelah pelatihan maka modifikasi/perbaikan manual dilakukan sesuai dengan pengalaman saat uji coba di lapangan.
Uji coba kuesioner dilaksanakan untuk mencatat berapa lama waktu dibutuhkan untuk wawancara, menilai alur pertanyaan dan format kuesioner serta
jawaban yang kemungkinan belum tercantum sebagai pilihan di kuesioner. Selain itu juga untuk memastikan bahwa kuesioner telah dipahami dengan baik oleh pewawancara dan menghindari aspek sensitif.
Reliabilitas pertanyaan dikendalikan untuk menjaga konsistensi pertanyaan yang diberikan oleh pewawancara. Hal ini dilakukan terhadap sub sampel dari setiap pewawancara dengan cara wawancara ulang yang dilakukan oleh peneliti dan dibandingkan dengan jawaban responden sebelumnya.
Pertemuan rutin petugas dilakukan untuk memastikan data telah terkumpul dengan baik dan untuk mengetahui masalah serta penyelesaiannya di lapangan. Petugas lapangan secara rutin dikumpulkan bersama-sama setiap hari untuk mendiskusikan hal tersebut. Hasil wawancara akan diperiksa oleh pewawancara lain dan di periksa kembali oleh peneliti, hal tersebut untuk memastikan semua kuesioner sudah dijawab dengan lengkap oleh sampel.
Pemilihan tempat analisis serum berdasarkan kemampuan peralatan dan tenaga laboratorium yang berpengalaman mengalanisis parameter tertentu. Hal tersebut menyebabkan analisis tidak dapat dilakukan di satu laboratorium namun menyebar menjadi beberapa tempat. Tabel berikut berisi tempat analisis serum dilakukan,.
Tabel 11 Laboratorium analisis biokimia darah
No. Jenis pemeriksaan Tempat pemeriksaan
1. Profil lipid Lab. Patologi Klinik FK – UI
2. SOD Lab. Biokimia FMIPA Universitas Brawijaya
3. MDA Lab. Biokimia FMIPA Universitas Brawijaya
4. Ox-LDL Lab. Biokimia FMIPA Universitas Brawijaya
5. Zn Lab. Biokimia Puslibang Gizi dan Makanan
Kemenkes RI
6. Isoflavon tempe Lab. Bioprospeksi Bidang Mikrobiologi LIPI 7. Protein & asam amino tempe Lab. Terpadu IPB
8. Lemak & asam lemak tempe Lab. Terpadu IPB 9. Zn, Cu dan Fe tempe Lab. Terpadu IPB
Penilaian terhadap proses pengumpulan data dilakukan di lapangan oleh supervisor untuk memeriksa apakah pewawancara mengumpulkan data dengan tepat. Selain itu juga untuk mengetahui masalah yang ditemukan di lapangan. Penilaian kualitas data entry dilakukan minimal 10% dari total data. Entry ulang akan dilakukan jika terdapat inkonsistensi. Pengukuran antropometri dilakukan oleh tenaga terlatih dan alat ukur yang digunakan (timbangan, microtoise) telah dikalibrasi sebelum digunakan.
Pengambilan darah dilakukan oleh tenaga ahli sedangkan analisis sampel darah dilakukan di beberapa laboratorium yang sudah terstandarisasi. Pengambilan darah selalu dilakukan serentak mulai jam 6.30 WIB hingga 9.00 WIB. Hal tersebut dilakukan untuk meminimalkan variasi hari dan cuaca serta kondisi lain yang dikhawatir mempengaruhi spesimen darah.
Metode Pemeriksaan Laboratorium
Secara rinci prosedur kerja analisis spesimen darah dimuat dalam lampiran. Berikut secara ringkas adalah reagent yang digunakan dalam analisis tersebut.
1. Profil lipid
- Kolesterol total: diperiksa dengan metode enzymatic colorimetric test “cholesterol CHOD-PAP (Roche, 2007). No Katalog 11489232-216 - Trigliserida: diperiksa dengan metode enzymatic colorimetric test
“triglycerides GPO-PAP (Roche, 2007). No Katalog 11488872-216 - Kolesterol-LDL: diperiksa dengan metode enzymatic colorimetric test
“LDL-cholesterol CHOD-PAP (Roche, 2007).
- Kolesterol-HDL diperiksa dengan metode enzymatic colorimetric test “HDL-cholesterol CHOD-PAP (Roche, 2007). No Katalog 04713184-190 2. Aktifitas SOD diperiksa dengan metode activity assay menggunakan reagent
merk Northwest (NWK-SOD02)
3. OxLDL diperiksa dengan metode enzyme immunoassay menggunakan reagent merk Mercodia, Swedia
4. MDA diperiksa dengan spektrofotometer, bahan yang digunakan antara lain TCA, Na Thio, dan HCl
Pengolahan dan Analisis Data
Pengolahan data dilakukan secara bertahap, dimulai dari data yang terkumpul di lapangan hingga data siap dianalisis. Data yang terkumpul di lapangan akan diperiksa oleh peneliti, jika terdapat kekurangan data pewawancara akan melengkapi dengan wawancara ulang kepada sampel. Jawaban pertanyaan dikoding oleh pewawancara sehingga mempermudah proses input data. Selanjutnya data diinput ke komputer. Jika proses input data telah selesai, dilakukan proses pembersihan data dengan cara melihat sebaran data setiap variabel. Data ekstrim akan dicek kembali ke kuesioner. Data yang telah dibersihkan selanjutnya dianalisis secara diskriptif dan statistik menggunakan soft
ware statistik. Sebelum dilakukan uji statistik lanjut semua data disajikan dalam
bentuk statistik elementer (minimal, maksimal, rata-rata dan standar deviasi). Data kuantitatif konsumsi pangan (food record) yang diambil 1x/mgg direkapitulasi untuk mengetahui berbagai jenis pangan dan ukuran (gram) yang dikonsumsi sampel. Untuk bahan makanan khususnya jajanan yang tidak lazim, peneliti membeli bahan makanan tersebut di warung sekitar tempat tinggal responden. Terindikasi ada sekitar 20 jenis jajanan yang dibeli dan digunakan untuk mengetahui bahan asal dan berat makanan. Daftar ini digunakan sebagai panduan dalam memasukkan jenis makanan ke dalam soft ware. Semua jenis makanan dan berat makanan kemudian dimasukkan dalam soft ware Nutrisurvey untuk dihitung energi, karbohidrat, protein, lemak, kolesterol, MUFA, SAFA, PUFA, serat, vitamin E, Seng dan Cu. Hasil tersebut kemudian dibandingkan dengan AKG (WKNPG 2004) untuk mengetahui kecukupan zat gizi setiap sampel. Data kualitatif konsumsi pangan (FFQ) merupakan data pendukung kuantitatif di ambil 1x/bln direkapitulasi dan dikonversi dalam hari atau minggu untuk menggambarkan frekuensi konsumsi responden.
Analisis data yang pertama dilakukan adalah pengukuran diskriptif terhadap beberapa parameter seperti karakteristik individu dan sosial ekonomi. Beberapa ukuran yang dianalisis antara lain: mean (rata-rata), median, standar deviasi, nilai minimum, dan nilai maksimal. Uji statistik parameter biokimia darah dilakukan melalui beberapa tahap. Tahap pertama adalah menguji distribusi sebaran normalitas data dengan menggunakan Uji
Kosmogorov-Smirnov dan Uji homogenitas varian menggunakan Lavena test. Jika p>0.05 maka sebaran data tergolong terdistribusi normal dan varians data tergolong homogen. Untuk mengetahui perubahan kadar parameter biokimia darah sebelum dan setelah intervensi serta membandingkan antara kelompok perlakuan dan kontrol (K-T, K-LDL, K-HDL, trigliserida, SOD, Zn, Ox-LDL dan MDA) digunakan Anova design repeated measurement atau GLMRM (general linier
model repeated measurement).
Untuk mengetahui hubungan masing-masing konsumsi zat gizi terhadap perubahan kadar setiap parameter biokimia darah dilakukan uji bivariat dengan uji pearson jika data terdistribusi normal dan uji sperman jika data tidak terdistribusi normal. Selanjutnya analisis regresi linier multivariat digunakan untuk mengetahui faktor (konsumsi zat gizi) yang paling mempengaruhi perubahan parameter darah setelah perlakuan.
Definisi Operasional
Definisi operasional berisi definisi dari setiap parameter atau variabel yang diukur disertai dengan alat ukur yang digunakan, cara mengukur dan hasil ukurnya. Selengkapnya disajikan pada Tabel 12 berikut.
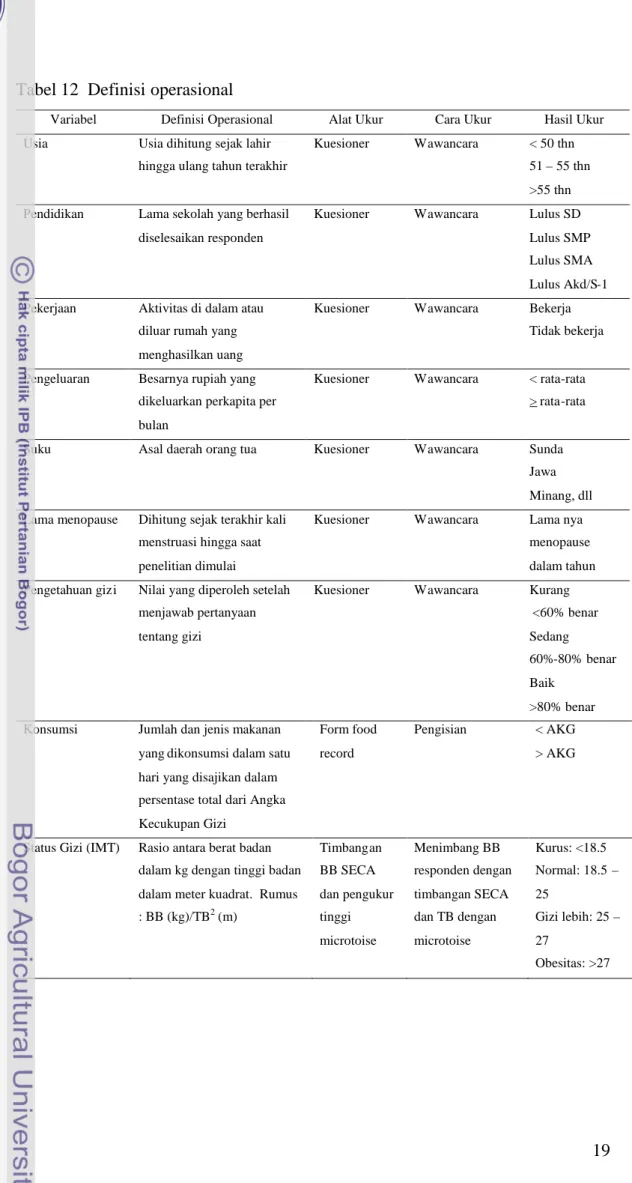
Tabel 12 Definisi operasional
Variabel Definisi Operasional Alat Ukur Cara Ukur Hasil Ukur
Usia Usia dihitung sejak lahir
hingga ulang tahun terakhir
Kuesioner Wawancara < 50 thn
51 – 55 thn >55 thn Pendidikan Lama sekolah yang berhasil
diselesaikan responden
Kuesioner Wawancara Lulus SD
Lulus SMP Lulus SMA Lulus Akd/S-1 Pekerjaan Aktivitas di dalam atau
diluar rumah yang menghasilkan uang
Kuesioner Wawancara Bekerja
Tidak bekerja
Pengeluaran Besarnya rupiah yang dikeluarkan perkapita per bulan
Kuesioner Wawancara < rata-rata
> rata-rata
Suku Asal daerah orang tua Kuesioner Wawancara Sunda
Jawa Minang, dll Lama menopause Dihitung sejak terakhir kali
menstruasi hingga saat penelitian dimulai
Kuesioner Wawancara Lama nya
menopause dalam tahun Pengetahuan gizi Nilai yang diperoleh setelah
menjawab pertanyaan tentang gizi
Kuesioner Wawancara Kurang
<60% benar Sedang 60%-80% benar Baik
>80% benar
Konsumsi Jumlah dan jenis makanan
yang dikonsumsi dalam satu hari yang disajikan dalam persentase total dari Angka Kecukupan Gizi
Form food record
Pengisian < AKG
> AKG
Status Gizi (IMT) Rasio antara berat badan dalam kg dengan tinggi badan dalam meter kuadrat. Rumus : BB (kg)/TB2(m) Timbangan BB SECA dan pengukur tinggi microtoise Menimbang BB responden dengan timbangan SECA dan TB dengan microtoise Kurus: <18.5 Normal: 18.5 – 25 Gizi lebih: 25 – 27 Obesitas: >27
Variabel Definisi Operasional Alat Ukur Cara Ukur Hasil Ukur Tekanan darah Hasil pengukuran sistolik dan
diastolic yang dilakukan pada posisi duduk setelah
beristirahat minimal 10 menit
Tensi meter Mengukur tekanan darah pada lengan bagian atas Hipertensi: sistolik >140 mmHg dan atau diastolik <90 mmHg Non hipertensi: sistolik <140 mmHg dan diastolik < 90 mmHg
Genetik Penyakit yang diturunkan dari salah satu orang tua atau saudara yang lebih tua
Kuesioner Wawancara Ada: jika salah satu keluarga yang lebih tua mengalami salah satu jenis pyk degeneratif Tidak ada: jika tidak ada anggota keluarga yang terkena pyk degeneratif
Merokok Kebiasaan merokok yang
dilakukan sehari-hari
Kuesioner Wawancara Ya: jika saat
penelitian sampel terbiasa merokok Tidak: jika saat penelitian sampel tidak merokok Aktivitas fisik Kegiatan olah raga yang
dilakukan secara rutin dalam satu minggu
kuesioner Wawancara Jarang (<3x/mg) Sering (>3x/mg)
K-Total Kadar kolesterol dalam serum
darah Analisis laboratorium Pengambilan darah lewat vena dan dianalisis di Lab Rasio K-LDL Kadar LDL dalam serum darah Analisis laboratorium Pengambilan darah lewat vena dan dianalisis di Lab Rasio K-HDL Kadar HDL dalam serum darah Analisis laboratorium Pengambilan darah lewat vena dan dianalisis di Lab Rasio
Variabel Definisi Operasional Alat Ukur Cara Ukur Hasil Ukur Trigliserida Kadar trigliserida dalam
serum darah
Analisis laboratorium
Pengambilan darah lewat vena dan dianalisis di Lab
Rasio
SOD Kadar enzim superoksida
dismutase dalam serum darah
Analisis laboratorium
Pengambilan darah lewat vena dan dianalisis di Lab
Rasio
Zinc Kadar Zn dalam serum darah Analisis
laboratorium
Pengambilan darah lewat vena dan dianalisis di Lab
Rasio
MDA Kadar MDA dalam
serum darah
Analisis laboratorium
Pengambilan darah lewat vena dan dianalisis di Lab
Rasio
Oksidasi LDL Kadar oksidasi LDL dalam serum darah
Analisis laboratorium
Pengambilan darah lewat vena dan dianalisis di Lab