Universitas Negeri Gorontalo Page 73 PERSETUJUAN PEMBIMBING
Jurnal yang berjudul:
PHARMACOPHORE MODELING DAN STUDI MOLECULAR DOCKING
SENYAWA DERIVATIF Δ9-TETRAHYDROCANNABINOL TERHADAP RESEPTOR CANNABINOID CB1 DAN CB2
Oleh :
ARIANI HUTUBA NIM. 821411047
Telahdiperiksadandisetujui
Pembimbing I Pembimbing II
Dr. Teti S. Tuloli, S.Farm.,M.Si.,Apt La Ode Aman, S.Pd.,M.Si NIP. 19800220 200801 2 007 NIP. 19770421 200604 1 002
Mengetahui KetuaJurusanFarmasi
Dr. Widysusanti Abdulkadir, M.Si., Apt NIP. 19711217 200012 2 001
Universitas Negeri Gorontalo Page 74
Pharmacophore Modeling Dan Studi Molecular Docking Senyawa Derivatif
Δ9-Tetrahydrocannabinol Terhadap Reseptor Cannabinoid CB1 Dan CB2 Ariani Hutuba, Teti S. Tuloli, La Ode Aman *)
Jurusan Farmasi, Fakultas Ilmu-Ilmu Kesehatan dan Keolahragaan Universitas Negeri Gorontalo
Email: [email protected] ABSTRAK
Penelitian ini merupakan penelitian teoritis eksploratif dimana derivatif senyawa Δ9-Tetrahydrocannabinol dikembangkan terhadap reseptor cannabinoid CB1 dan CB2. Penelitian ini menggunakan metode Molecular docking dan mengembangkan pharmacophore modeling untuk target aktif. Hasil molecular docking melibatkan studi mode ikatan yang berbeda dari satu ligan dengan sisi aktif target reseptor CB1 dan CB2 dengan bantuan AUTODOCK-VINA. Dari hasil docking terdapat 13 senyawa yang memiliki pharmacophore model dengan sisi aktif pengikatan yang sama terhadap asam amino reseptor CB1 yaitu ILE37, PHE384, TYR248, ARG348. Interaksi yang terlihat menunjukkan Gugus –O dari ligan dengan gugus asam amino pada reseptor cannabinoid 1. Untuk reseptor cannabinoid 2 terdapat 21 senyawa yang memiliki pharmacophor model dengan sisi aktif pengikatan yang sama terhadap asam amino reseptor CB2 yaitu VAL513 dan LEU291 dengan ikatan hidrofobik antara ligan dan reseptor.
Kata Kunci: Δ9-Tetrahydrocannabinol, pharmacophore modeling, Molecular docking.
PENDAHULUAN
Salah satu tumbuhan yang terus dikembangkan untuk penemuan obat baru adalah ganja. Cannabinoids adalah istilah yang digunakan untuk kelompok khas senyawa C21 dan termasuk analog yang hadir dalam Cannabis sativa (Rao and Alexandros, 1987). Tanaman yang termasuk dalam family (cannabaceae) yang hanya memiliki satu genus (cannabis) dengan hanya satu spesies (sativa) telah digunakan selama berabad-abad sebagai obat rekreasi serta berbagai efek farmakologisnya.
Efek farmakologis dari cannabinoid dimediasi melalui setidaknya dari dua G-protein coupled, reseptor transmembran. Reseptor CB1, salah satu reseptor yang ditemukan pada otak manusia dengan kepadatan tertinggi
dibagian sistem saraf seperti hipokampus, hipotalamus, cereblum, basal ganglia, batang otak, tulang belakang, dan amygdala (Pavlopoulos et al., 2006). Reseptor CB2, awalnya diidentifikasi dari makrofag hadir dalam limpa, dan dinyatakan terutama di peripheral (John, 2005).
Berdasarkan senyawa aktif utama derivatif Δ9-Tetrahydrocannabinol, beberapa kelompok penelitian mengembangkan dan mensintesis senyawa yang poten terhadap Cannabinoid receptor CB1 dan CB2. Pada Protein Data Bank
(www.pdb.org), struktur Cannabinoid
receptor 1 diperoleh dengan (PDB ID : 2KOE) dan Cannabinoid receptor 2 (PDB ID : 2KI9) yang di identifikasi
Universitas Negeri Gorontalo Page 75 dengan metode difraksi NMR dengan
resolusi tertentu.
Cannabinoids non-tradisional yang sangat poten dikembangkan oleh Pfizer pada tahun 80an yaitu CP-55940 (2, DMH=1,1 –dimethylheptyl). Beberapa tahun kemudian dalam pengembangan obat anti-inflamasi non steroid, Sterling-Winthrop melaporkan 3, Pravadoline dan senyawa yang terkait juga menghambat adenilat siklase, adalah antinosiseptif dan berinteraksi dengan G-Protein coupled di otak. Aminoalkylindoles yang dikembangkan oleh Sterling-Winthrop menunjukkan farmakologi khas dari cannabinoid secara in vivo dan memiliki afinitas tinggi untuk kedua CB1 cannabinoid dan reseptor CB2 yaitu 4, WIN-55,212-2 (Huffman, WIN-55,212-2005).
Biologi komputasi dan bioinformatika berpotensi tinggi dalam ilmu kimia medisinal, tidak hanya mempercepat proses penemuan obat tetapi juga mengubah cara penemuan dan perancangan obat. Rational Drug Design (RDD) memfasilitasi dan mempercepat proses rancangan obat, yang melibatkan berbagai metode untuk mengidentifikasi senyawa baru. Salah satu contoh metode yang digunakan adalah penambatan molekul obat dengan reseptor yang sering disebut molecular docking. Reseptor disini merupakan sisi aktif dari kerja obat yang berperan terhadap efek farmakologi. Penambatan (Docking) adalah proses dimana dua molekul dicocokkan melalui penambatan dalam ruang 3D (Ramya et al., 2011).
METODE PENELITIAN Lokasi dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Biokimia Medik Farmasi Fakultas Ilmu Ilmu Kesehatan dan
Keolahragaaan, Universitas Negeri Gorontalo selama 4 (empat) minggu. Alat
Perangkat keras berupa Personal Computer (PC) dengan prosesor intel (R) Atom (TM) CPU N550 @1,50 GHz (3CPUs) yang mampu melakukan perhitungan kimia komputasi. Perangkat lunak berupa Operating System (OS) Microsoft® Windows 7 Ultimate 32-bit (6.1, Build 7601), Marvin Sketch, Open Babel GUI, Pymol, Open3Dalign, Autodock Tools 1.5.6, dan VINA.
Bahan
Bahan penelitian berupa data set derivatif Δ9-tetrahydrocannabinol dengan binding affinity reseptor CB1 dan CB2. Struktur reseptor Cannabinoid reseptors (CBRs) diperoleh dari Protein Data Bank
(www.pdb.org), dengan kode (PDB ID :
2KOE) untuk Cannabinoid reseptor 1 dan (PDB ID : 2KI9) untuk Cannabinoid receptor 2.
Preparasi ligan
Tujuannya mendapatkan struktur molekul yang stabil dan aktif untuk mengembangkan pharmacophore modelling dengan menggunakan Marvin Sketch.
Preparasi reseptor
Untuk keperluan molecular docking, reseptor cannabinoid CB1 dan CB2 yang telah dimuat dilakukan preparasi dengan menggunakan UCSF Chimera. Hal ini bertujuan untuk mendapatkan satu protein target, penghilangan molekul air, dan penambahan hydrogen. Seluruh protein target disimpan dalam format *.pdb
Universitas Negeri Gorontalo Page 76
Molecular Docking
Untuk memprediksikan konformasi terikat dan energi pengikatan dari ligan dengan makromolekul target menggunakan AutoDock. Salah satu keuntungan AutoDock dapat memprediksikan antara pengikatan ligan-reseptor dengan efektif, cepat dan akurat. AutoDock secara otomatis menghitung Gasteiger charges, merges nonpolar hydrogens, assigns AutoDock type to each atom, dan torsion). Ligan-reseptor disimpan dalam format *.pdbqt. AutoDock menggunakan metode berdasarkan Grid untuk mengevaluasi dengan cepat pengikatan energi dari konformasi. Dalam metode ini, protein target tertanam dalam kotak. Preparasi parameter Grid dan pengaturan properti Grid dengan menggunakan perintah Grid Box. Disimpan dalam bentuk *.txt
Validasi dan analisis dari docking Reseptor-Ligan
Program VINA yang dapat kembali pose di bawah terpilih Root Mean Square Deviasi (RMSD) nilai dari konformasi dikenal (biasanya 1 Å atau 2 Å tergantung pada ukuran ligan) dianggap telah berhasil dilakukan. Pose seleksi kemudian diikuti oleh scoring dan peringkat untuk mempelajari mana dari fungsi scoring tersedia sebagian akurat peringkat pose sehubungan dengan nilai-nilai rmsd mereka.
HASIL DAN PEMBAHASAN
Dari hasil docking didapatkan 13
senyawa derivatif
Δ9-tetrahydrocannabinol memiliki best mode yang memiliki binding affinity bertanda negatif (-). Hal ini berarti bahwa senyawa-senyawa tersebut memiliki kemampuan berikatan dan bereaksi secara spontan terhadap reseptor cannabinod 1 yang ditunjukkan pada tabel 1.
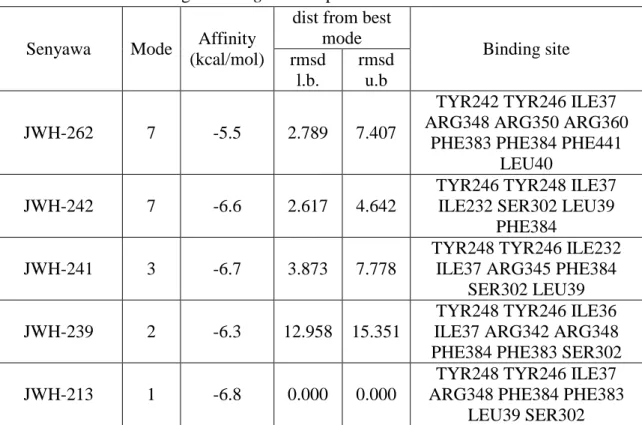
Tabel 1. Hasil docking senyawa derivatif Δ9-tetrahydrocannabinol dan berbagai residu asam amino sebagai binding site reseptor Cannbinoid 1
Senyawa Mode Affinity (kcal/mol)
dist from best mode Binding site rmsd l.b. rmsd u.b JWH-262 7 -5.5 2.789 7.407
TYR242 TYR246 ILE37 ARG348 ARG350 ARG360
PHE383 PHE384 PHE441 LEU40
JWH-242 7 -6.6 2.617 4.642
TYR246 TYR248 ILE37 ILE232 SER302 LEU39
PHE384
JWH-241 3 -6.7 3.873 7.778
TYR248 TYR246 ILE232 ILE37 ARG345 PHE384
SER302 LEU39 JWH-239 2 -6.3 12.958 15.351
TYR248 TYR246 ILE36 ILE37 ARG342 ARG348 PHE384 PHE383 SER302
JWH-213 1 -6.8 0.000 0.000
TYR248 TYR246 ILE37 ARG348 PHE384 PHE383
Universitas Negeri Gorontalo Page 77
JWH-212 1 -6.5 0.000 0.000
TYR248 TYR246 ILE37 ARG348 PHE384 PHE383
LEU40 SER302 JWH-211 3 -6.5 12.852 15.180
TYR248 TYR246 ILE36 ILE37 PHE384 PHE383
LEU39 SER302 JWH-210 3 -6.5 13.315 14.142
TYR248 TYR246 ILE37 ARG348 PHE384 PHE383
PHE440 LEU39 SER302
JWH-182 2 -6.3 1.900 8.049
TYR246 TYR242 ILE37 ARG344 PHE384 PHE440
PHE 441 LEU39 LEU40 SER302
JWH-181 2 -6.9 11.272 14.063
TYR248 TYR246 ILE37 ILE232 PHE384 PHE383 PHE440 LEU39 LEU40
SER302
JWH-180 1 -6.6 0.000 0.000
TYR248 TYR246 ILE37 ILE36 ARG342 PHE384 PHE383 LEU39 LEU40
SER302
JWH-149 2 -5.5 1.782 7.012
TYR248 TYR246 ILE37 ARG348 PHE383 PHE440
LEU39 LEU40 SER302
JWH-122 1 -6.6 0.000 0.000
TYR248 TYR246 ILE37 ARG342 ARG348 PHE384
PHE383 LEU40 SER302 Untuk JWH-262 Ikatan hidrogen yang
terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 4.4 Ǻ. JWH-242 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom O pada asam amino SER (reseptor) dengan panjang ikatan 6.1 Ǻ. JWH-241 ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 4.3 Ǻ. JWH-239 ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 4.1 Ǻ. JWH-213 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 3.1 Ǻ. JWH-212 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor)
dengan panjang ikatan 3.1 Ǻ. JWH-211 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom O pada asam amino SER (reseptor) dengan panjang ikatan 5.9 Ǻ. JWH-210 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 3.1 Ǻ. JWH-182 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 3.5 Ǻ. JWH-181 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom O pada asam amino ARG (reseptor) dengan panjang ikatan 6.0 Ǻ. JWH-180 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 3.2 Ǻ. JWH-149 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam
Universitas Negeri Gorontalo Page 78 amino ARG (reseptor) dengan panjang
ikatan 3.0 Ǻ. JWH-122 Ikatan hidrogen yang terlihat antara atom O (ligan) dan atom N pada asam amino ARG (reseptor) dengan panjang ikatan 3.1 Ǻ. Selanjutnya dari hasil docking menggunakan program Autodock-Vina
diperoleh 21 senyawa derivatif Δ9-Tetrahydrocannabinol dengan Pharmacophore modeling dan binding site yang sama terhadap reseptor cannabinoid 2 (CB2) yang ditunjukkan
pada tabel 2
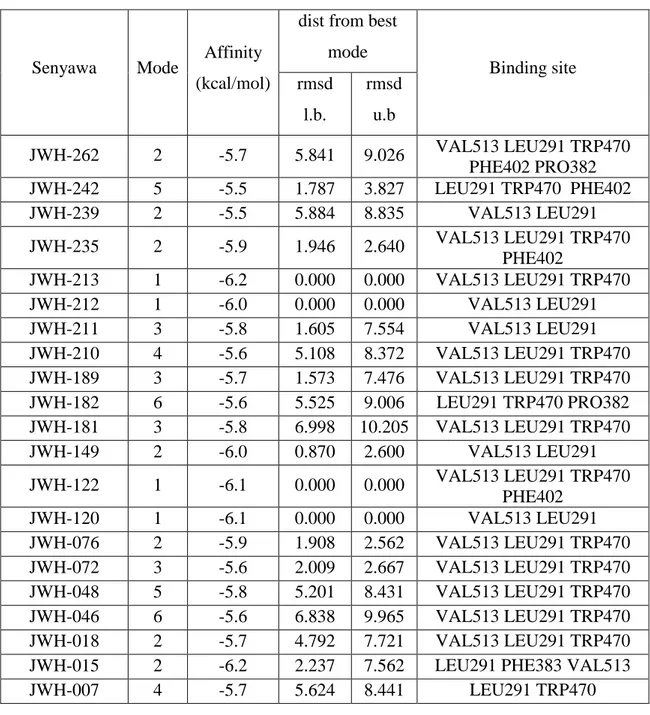
Tabel 2. Hasil docking senyawa derivatif Δ9-tetrahydrocannabinol dan berbagai residu asam amino sebagai binding site reseptor Cannbinoid 2
Senyawa Mode Affinity (kcal/mol)
dist from best mode Binding site rmsd l.b. rmsd u.b JWH-262 2 -5.7 5.841 9.026 VAL513 LEU291 TRP470 PHE402 PRO382 JWH-242 5 -5.5 1.787 3.827 LEU291 TRP470 PHE402 JWH-239 2 -5.5 5.884 8.835 VAL513 LEU291 JWH-235 2 -5.9 1.946 2.640 VAL513 LEU291 TRP470 PHE402 JWH-213 1 -6.2 0.000 0.000 VAL513 LEU291 TRP470 JWH-212 1 -6.0 0.000 0.000 VAL513 LEU291 JWH-211 3 -5.8 1.605 7.554 VAL513 LEU291 JWH-210 4 -5.6 5.108 8.372 VAL513 LEU291 TRP470 JWH-189 3 -5.7 1.573 7.476 VAL513 LEU291 TRP470 JWH-182 6 -5.6 5.525 9.006 LEU291 TRP470 PRO382 JWH-181 3 -5.8 6.998 10.205 VAL513 LEU291 TRP470 JWH-149 2 -6.0 0.870 2.600 VAL513 LEU291 JWH-122 1 -6.1 0.000 0.000 VAL513 LEU291 TRP470 PHE402 JWH-120 1 -6.1 0.000 0.000 VAL513 LEU291 JWH-076 2 -5.9 1.908 2.562 VAL513 LEU291 TRP470 JWH-072 3 -5.6 2.009 2.667 VAL513 LEU291 TRP470 JWH-048 5 -5.8 5.201 8.431 VAL513 LEU291 TRP470 JWH-046 6 -5.6 6.838 9.965 VAL513 LEU291 TRP470 JWH-018 2 -5.7 4.792 7.721 VAL513 LEU291 TRP470 JWH-015 2 -6.2 2.237 7.562 LEU291 PHE383 VAL513
Universitas Negeri Gorontalo Page 79 Penelitian ini menggunakan dua
pendekatan berdasarkan desain struktur obat yaitu molecular docking dan pemodelan farmakofor untuk mengukur potensi senyawa derivatif Δ9-Tetrahydrocannabinol terhadap reseptor cannabinoid. Dari hasil docking ditemukan bahwa model pharmacophor yang telah divalidasi memprediksi bahwa asam amino yang berikatan
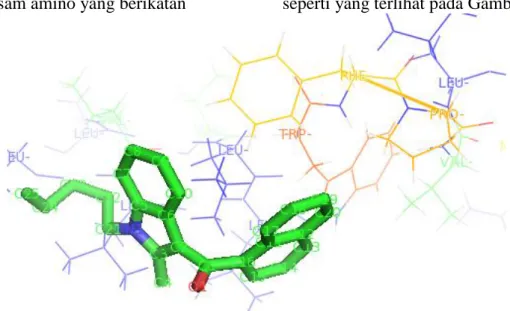
dengan ligan memiliki rantai samping alifatik (asam amino non polar) seperti LEU dan VAL sehingga dapat membentuk interaksi ikatan hidrofobik antara ligan dan reseptor (Robert, 2002). Ikatan hidrofobik, adalah ikatan yang cukup lemah, tetapi sangat penting dalam interaksi obat yang sangat larut lemak dengan lemak dari sel membran seperti yang terlihat pada Gambar 1.
Gambar 1. Pharmacophore model senyawa derivatif Δ9-Tetrahydrocannabinol terhadap cannabinoid reseptor 2
PENUTUP Kesimpulan
Dari hasil penelitian dan pembahasan diatas, dapat disimpulkan beberapa hal sebagai berikut :
1. Pharmacophore model senyawa derivatif Δ9-Tetrahydrocannabinol terhadap cannabinoid reseptor 1 yaitu JWH-262, JWH,-242, JWH-241, JWH-239, JWH-213, JWH-212, JWH-211, JWH-210, JWH-182, JWH-181, JWH-180, JWH-149, JWH-122 dengan sisi aktif pengikatan yang sama terhadap asam amino reseptor CB1 yaitu ILE37, PHE384, TYR248, ARG348. Sedangkan untuk reseptor cannabinoid 2 yaitu JWH-262, JWH,-242, JWH-239, JWH-213, JWH-212, JWH-211, JWH-210, JWH-189, JWH-182, JWH-181, JWH-149, JWH-122, JWH-120, JWH-076, JWH-072, JWH-048, JWH-046, JWH-018, JWH-015, JWH-007 dengan sisi aktif pengikatan yang sama terhadap asam amino reseptor CB2 yaitu VAL513 dan LEU291.
2. Interaksi senyawa derivatif Δ9-tetrahydrocannabinol dengan reseptor CB1 dan CB2 menunjukkan nilai binding affinity (-). Hal ini berarti semakin negatif nilai energi bebas suatu senyawam semakin tinggi pula terjadi kespontanan interaksi antara senyawa dengan
Universitas Negeri Gorontalo Page 80 reseptor. Dari hasil penelitian
senyawa derivatif Δ9-tetrahydrocannabinol memiliki interaksi ikatan hidrogen dan ikatan hidrofobik. Gugus –O dari ligan menunjukkan ikatan terjadi antara ligan dengan gugus asam amino pada reseptor cannabinoid 1. Sedangkan Cannabinoid reseptor 2 menunjukkan ikatan hidrofobik antara ligan dan reseptor.
Saran
Sebaiknya perlu dilakukan in-silico screening lebih lanjut menggunakan
senyawa derivatif
Δ9-tetrahydrocannabinol dengan model pendekatan modifikasi senyawa dengan aktivitas yang lebih baik. Perlu dilakukan uji lebih lanjut tentang aktivitas senyawa derivatif Δ9-tetrahydrocannabinol terhadap cannabinoid reseptor CB1 dan CB2. DAFTAR PUSTAKA
A. C. Howlett, F. Barth, T. I. Bonner, G. Cabral, P. Casellas, W. A. Devane, C. C. Felder, M. Herkenham, K. Mackie, B. R. Martin, R. Mechoulam, and R. G. Pertwee. 2002. International Union of Pharmacology. XXVII. Classification of cannabinoid receptors. Pharmacol Rev: 161‐202.
Arooj M, Sakkiah S, Kim S, Arulalapperumal V, Lee KW. 2013. A combination of receptor-based pharmacophore modeling & QM techniques for identification of human chymase inhibitors. PLoS ONE
8(4):e63030 DOI
10.1371/journal.pone.0063030.
Christian, Rӓtsch. 2001. Marijuana medicine: a world tour of the healing and visionary power of cannabis. Rochester : Inner Traditions/Bear & company De Petrocellis, L., Melck, D., Palmisano, A., et al. 1998. The endogenous cannabinoid anandamide inhibits human breast cancer cell proliferation. proc. natl. acad. Sci. USA : 8375– 8380.
Derkinderen, P., Toutant, M., Burgaya, F., et al. 1996. Regulation of a neuronal form of focal adhesion kinase by anandamide. Science 273: 1719–1722.
Deshmukh, L., Vinogradova, O., Makriyannis, A., Tiburu, E., Tyukhtenko, S., Janero, D. 2009. NMR solution structure of human cannabinoid receptor-1 helix 7/8 peptide: candidate electrostatic interactions and microdomain formation. Biochem. Biophys. Res.Commun : 441-446
Deshmukh, L., Vinogradova, O., Tiburu, E.K., Tyukhtenko, S., Janero, D.R., Makriyannis, A. 2009. Structural biology of human cannabinoid receptor-2 helix 6 in membrane-mimetic environments.
Biochem.Biophys.Res.Commun : 243-248
Dimitrios Vlachakis; Paraskevas Fakourelis; Vasileios Megalooikonomou; Christos Makris; and Sophia Kossida.
2015. DrugOn: a fully integrated pharmacophore
Universitas Negeri Gorontalo Page 81
modeling and structure optimization toolkit. PeerJ 3: 725; DOI 10.7717/peerj.725 Foloppe, N., & Chen, I.-J. (2009).
Conformational Sampling and Energetics of Drug-like Molecules. Current Medicinal Chemistry, 16, 3381-3413.
Galiegue, S., Mary, S., Marchand, J., et al. 1995. Expression of central and peripheral cannabinoid receptors in human immune tissues and leukocyte subpopulations. Eur. J. Biochem: 54–61.
Gardner, E. L. (2002) Addictive potential of cannabinoids: the underlying neurobiology. Chem. Phys. Lipids : 267–290.
Herkenham, M., Lynn, A. B., Johnson, M. R., Melvin, L. S., De Costa, B. R., and Rice, K. C. 1991. Characterization and localization of cannabinoid receptors in rat brain: a quantitative in vitro autoradiographic study. J. Neurosci : 563–583.
Istyastono, E.P. 2007. Peran Komputer dalam Penemuan Obat. Online (http://www.chem-is-try.com, diakses 31 Mei 2015) John W. Huffman. 2005. Structure–
activity relationships for 1-alkyl-3-(1 naphthoyl)indoles at the cannabinoid CB1 and CB2 receptors: steric and electronic effects of naphthoyl substituents. New highly selective CB2 receptor agonists. Bioorg. Med. Chem : 89–112 Klein, T. W., Newton, C., and
Friedman, H. 1998. Cannabinoid receptors and immunity. Immunol : 373–381.
Mahmoud A. Elsohly. 2007. Marijuana and the cannabinoid.
New Jersey : Humana Press
Mechoulam R, Gaoni Y. 1964. Isolation, structure, and partial synthesis of an active constituent of hashish. J Am Chem Soc : 86 -1646
Motiejunas, D., & Wade, R. (2006). Structural, Energetics, and Dynamic Aspects of Ligand-Receptor Interactions. In J. B. Taylor & D. J. Triggle (Eds.), Comprehensive Medicinal Chemistry II Volume 4: Computer Assisted Drug Design (Vol. 4, pp. 193-214). Elsevier.
Oleg Trott, 2009. AutoDock Vina: Improving the speed and accuracy of docking with a new scoring function, efficient
optimization, and
multithreading. Article first
published online:
DOI: 10.1002/jcc.21334
Patrick J. Sinko. 2006. Farmasi fisika dan ilmu farmasetika. Jakarta : Buku kedokteran EGC
Pires DE, Ascher DB, Blundell TL. 2014. mCSM: predicting the effects of mutations in proteins using graph-based signatures. Bioinformatics 30:335–342 DOI 10.1093/bioinformatics/btt691.
Universitas Negeri Gorontalo Page 82 Presley BC, Jansen-Varnum SA
, Logan BK. 2013. Analysis of synthetic cannabinoids in botanical material: A review of analytical methods and fi ndings; Forensic Sci Rev : 28-46 Ramya T. Sri, V. Sathyanathan, Kumar
D. P., Chowdhari M. 2011. Docking Studies on Synthesizwd Quinazoline Compounds Against Androgen Receptor. Int. J. Pharm & Ind. Res : 266 – 269
Rao S. Rapaka., Alexandros Makriyannis. 1987. Structure-Activity Relationships of the Cannabinoids. Rockville, Maryland : U.S. Department of Health and human services
S, pavlopoulos., GA, Thakur., SP, Nikas., A, Makriyannis. 2006. Cannabinoid receptors as therapeutic targets. Curr Pharm : 1751-1769
Schlicker, E. and Kathmann, M. 2001. Modulation of transmitter release via presynaptic cannabinoid receptors. Trends Pharmacol Sci : 565–572.
Schneider, G., & Baringhaus, K.-H. (2008). Molecular Design: Concepts and Applications. WILEY-VCH.
Sellasie, 2003. History Of Quantitative
Structure-Activity Relationships
Chemistry Department Pomona College Claremont, California,
Burger Burgeros Medicinal Chemistry And Drug Discovery Siswandono dan Soekardjo, B. 2000.
Kimia Medisinal. Surabaya : Airlangga University Press.
Thomsen R., Christensen M. H. 2006. MolDock: A New Technique for High-Accuracy Molecular Docking. J. Med. Chem : 3315 – 3321
Vlachakis D, Kossida S. 2013. Molecular modeling and pharmacophore elucidation study of the Classical Swine Fever virus helicase as a promising pharmacological target. PeerJ 1:e85 DOI 10.7717/peerj.85.
Wartmann, M., Campbell, D., Subramanian, A., Burstein, S. H., and Davis, R. J. 1995. The MAP kinase signal transduction pathway is activated by the endogenous cannabinoid anandamide. FEBS Lett : 133– 136.
Wermuth CG. 1998. Glossary of terms used in medicinal chemistry (IUPAC recommendations 1997). Annual Reports in Medicinal Chemistry 33:385–395. Zhang M,White RA,Wang L, Goldman R, Kavraki L, Hassett B. 2005. Improving conformational searches by geometric screening. Bioinformatics 21(5):624–630 DOI 10.1093/bioinformatics/bti055.