BAB II
TINJAUAN PUSTAKA
II.1. STROKE II.1.1. DEFINISI
Stroke adalah suatu episode disfungsi neurologi akut disebabkan oleh iskemik atau perdarahan berlangsung 24 jam atau meninggal, tapi tidak memiliki bukti yang cukup untuk diklasifikasikan (Sacco dkk, 2013).
Stroke iskemik adalah episode disfungsi neurologis disebabkan infark fokal serebral,spinal dan infark retinal. Dimana infark SSP (Sistem Saraf Pusat) adalah kematian sel pada otak, medulla spinalis, atau sel retina akibat iskemia, berdasarkan :
• Patologi, imaging atau bukti objektif dari injury fokal iskemik pada
serebral, medula spinalis atau retina pada suatu distribusi vaskular tertentu.
• Atau bukti klinis dari injury fokal iskemik pada serebral, medulla
Stroke hemoragik adalah disfungsi neurologis yang berkembang cepat yang disebabkan oleh kumpulan darah setempat pada parenkim otak atau sistem ventrikular yang tidak disebabkan oleh trauma (Sacco dkk,2013)
II.1.2 Epidemiologi
WHO memperkirakan insidensi stroke ini akan meningkat dari 1,1 juta di tahun 2000 menjadi 1,5 juta jiwa pada 2025, berdasarkan proyeksii populasi penduduk. Di Indonesia insiden stroke sebesar 51,6/100.000 penduduk. Penderita laki-laki lebih banyak daripada perempuan dan profil usia dibawah 45 tahun : 11,8%, usia 45-64 tahun : 54,2% dan usia lebih dari 65 tahun 33,5%. (Truelsen, 2006)
Meskipun dapat mengenai semua usia, insiden stroke meningkat dengan bertambahnya usia. Perbandingan insidens pria dan wanita pada umur 55-64 tahun adalah 1,25; pada umur 65-74 tahun adalah 1,50; 75-84 tahun adalah 1,07; dan pada umur > 85 tahun adalah 0,76. (Lloyd dkk,2009)
II.1.3 Faktor Resiko
Faktor- faktor resiko untuk terjadinya stroke dapat diklasifikasikan sebagai berikut : (Sjahrir, 2003).
1. Non modifiable risk factors : a. Usia
c. Keturunan / genetik
2. Modifiable risk factors
a. Behavioral risk factors
1. Merokok
2. Unhealthy diet : lemak, garam berlebihan, asam urat, kolesterol, low
fruit diet.
3. Alkoholik
4. Obat – obatan: narkoba (kokain), antikoagulansia, antiplatelet, obat kontrasepsi.
b. Physiological risk factors
1. Penyakit hipertensi 2. Penyakit jantung 3. Diabetes mellitus
4. Infeksi/lues, arthritis, traumatic , AIDS, lupus 5. Gangguan ginjal
6. Kegemukan (obesitas)
7. Polisitemia, viskositas darah meninggi dan penyakit perdarahan 8. Kelainan anatomi pembuluh darah
II.1.4 Klasifikasi
Dasar klasifikasi yang berbeda – beda diperlukan, sebab setiap jenis stroke mempunyai cara pengobatan, pencegahan dan prognosa yang berbeda, walaupun patogenesisnya sama (Misbach,2011)
I. Berdasarkan patologi anatomi dan penyebabnya : 1. Stroke iskemik
a. Transient Ischemic Attack (TIA) b. Thrombosis serebri
c. Emboli serebri 2. Stroke Hemoragik
a. Perdarahan intraserebral b. Perdarahan subarachnoid
II. Berdasarkan stadium / pertimbangan waktu 1. Transient Ischemic Attack (TIA) 2. Stroke in evolution
3. Completed stroke
III. Berdasarkan sistem pembuluh darah 1. Sistem karotis
2. Sistem vertebrobasiler
3. Lacunar Infarct (LACI)
4. Posterior Circulation Infarct (POCI)
V. Klasifikasi Stroke Iskemik berdasarkan kriteria kelompok peneliti TOAST (Sjahrir, 2003)
1. Aterosklerosis Arteri Besar 2. Kardioembolisme
3. Oklusi Arteri Kecil
4. Stroke Akibat dari Penyebab Lain yang Menentukan a. Non-aterosklerosis Vaskulopati
• Non inflamasi
• Inflamasi non infeksi • Infeksi
b. Kelainan Hematologi atau Koagulasi
5. Stroke Akibat dari Penyebab Lain yang Tidak Dapat Ditentukan
II.1.5 Patofisiologi
II.1.5.1 Patofisiologi Stroke Iskemik
Iskemik otak mengakibatkan perubahan dari sel neuron otak secara bertahap, yaitu (Sjahrir, 2003):
Tahap 1 :
c. Kegagalan energi.
d. Terminal depolarisasi dan kegagalan homeostasis ion. Tahap 2 :
a. Eksitoksisitas dan kegagalan homeostasis ion.
b. Spreading depression.
Tahap 3 : Inflamasi
Respon inflamatorik pada stroke iskemik akut mempunyai pengaruh buruk yang memperberat bagi perkembangan infark serebri. Berbagai penelitian menunjukkan adanya perubahan kadar sitokin pada penderita stroke iskemik akut. Sitokin adalah mediator peptida molekuler, merupakan protein atau glikoprotein yang dikeluarkan oleh suatu sel dan mempengaruhi sel lain dalam suatu proses inflamasi, contohnya limfokin dan interleukin (IL-1 beta, IL-6, IL-8, TNF-α) yang merupakan sitokin pro inflamatorik. Adanya IL-8 tersebut merupakan diskriminator terkuat yang membedakan kasus stroke dengan non stroke. Produksi sitokin yang berlebihan mengakibatkan plugging mikrovaskuler serebral dan pelepasan mediator vasokonstriktif endotel sehingga memperberat penurunan aliran darah, juga mengakibatkan eksaserbasi kerusakan Blood Brain Barrier (BBB) dan parenkim melalui pelepasan enzim hidrolitik, proteolitik dan produksi radikal bebas yang akan menambah neuron yang mati (Sjahrir, 2003)
II.1.5.2 Patofisiologi Stroke Hemoragik
Perdarahan intraserebral biasanya timbul karena pecahnya mikroaneurisma (Berry aneurysm) akibat hipertensi maligna. Hal ini paling sering terjadi di daerah subkortikal, serebelum, dan batang otak. Hipertensi kronik menyebabkan pembuluh arteriol berdiameter 100 – 400 mikrometer mengalami perubahan patologi pada dinding pembuluh darah tersebut berupa lipohialinosis, nekrosis fibrinoid serta timbulnya aneurisma tipe
Bouchard. (Caplan, 2000).
Perdarahan intraserebral sekunder (sekitar 12 sampai 22% dari seluruh kejadian perdarahan intraserebral) disebabkan oleh penyebab lain selain pecahnya pembuluh darah kecil, misalnya, aneurisma, malformasi arteri-vena, transformasi hemoragik stroke iskemik, dan neoplasma (Brouwers dkk, 2012).
II.2 TUMOR OTAK II.2.1 Pendahuluan
Tumor otak dapat berupa tumor jinak atau ganas, atau primer atau metastase. Tumor otak primer yaitu tumor yang langsung berasal dari sel-sel di otak. (Hill dkk, 2002)
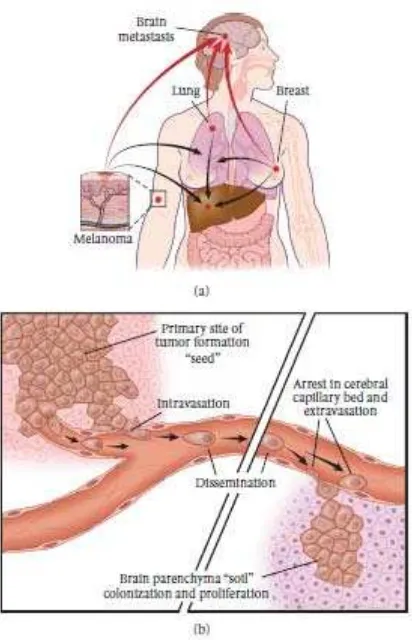
Brain metastase mayoritas berasal dari kanker paru, payudara, dan
proses metastasis: ia dapat berperan sebagai pelindung sistem saraf pusat yang kuat dari masuknya sel-sel kanker, namun ia juga dapat berperan aktif dalam melindungi sel-sel metastase pada saat ekstravasasi dan proliferasi di otak. Mekanisme interaksi antara sel-sel kanker dan sel-sel endotel serebral belum diketahui secara pasti. (Wilhelm dkk, 2013)
Proses metastasis sangat kompleks, namun secara garis besar dibagi atas dua tahap utama. Pertama, migrasi sel-sel tumor dari tumor primer ke berbagai jaringan, dan kedua proses kolonisasi dari sel-sel tumor di lokasi barunya. (Rahmathulla dkk, 2011)
II.2.2 Epidemiologi
Tumor otak dapat mengenai setiap jenis usia, namun insidens nya meningkat sesuai dengan usia. Tumor pada susunan saraf pusat didapatkan sekitar 6% dari seluruh neoplasma pada individu usia 15-29 tahun, dengan laki-laki memiliki insidens lebih tinggi dibandingkan dengan wanita. (Hill dkk 2002)
Insidens rata-rata tumor otak sekitar 2.6 juta pertahun pada usia 15-29 tahun. Tingkat insidens tumor otak tertinggi didapatkan pada usia 35 - >39 tahun. Diikuti usia 20-24 tahun dan kemudian usia 15-29 tahun. (Bendel dkk, 2006)
Brain metastase merupakan salah satu jenis tumor intrakranial yang
dimana tumor otak primer dijumpai sekitar 17.000 kasus baru/tahun. Mayoritas brain metastase berasal dari kanker paru (40% 50%), kanker payudara (15%- 25%) dan melanoma malignan (5%-20%). (Wilhelm dkk, 2013)
Gambar 1. Skema Proses Metastasis. (a) Pembentukan sel tumor metastasi pada asal tumor primer (b) Sel tumor metastase lepas dari tumor primer kemudian masuk ke pembuluh darah.
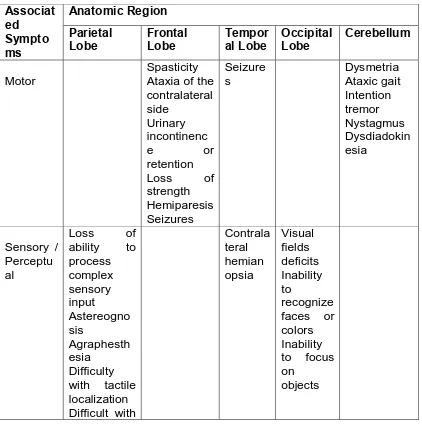
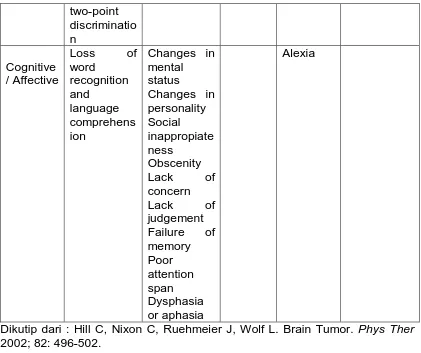
II.2.3 Gejala Klinik
Tumor otak dapat memiliki gejala dan tanda yang bervariasi, tergantung pada lokasi, tipe, dan tingkat pertumbuhan dari tumor tersebut. (Hill dkk,2002)
two-point
Dikutip dari : Hill C, Nixon C, Ruehmeier J, Wolf L. Brain Tumor. Phys Ther 2002; 82: 496-502.
II.2.4 Klasifikasi
Klasifikasi menurut WHO merupakan standard klasifikasi yang digunakan secara luas di seluruh dunia. (Louis dkk 2007)
Tabel 2. Klasifikasi Tumor Sistem Saraf Pusat berdasarkan WHO TUMOURS OF
NEUROEPITHELIAL TISSUE Astrocytic Tumours
Pilocytic astrocytoma Pilomyxoid astrocytoma
Subependymal giant cell astrocytoma
Pleomorphic xanthoastrocytoma Diffuse astrocytoma
Giant cell glioblastoma Choroid plexus tumours Choroid plexus papilloma
Atypical choroid plexus papilloma Choroid plexus carcinoma
Other neuroepithelial tumours Astroblastoma
Choroid glioma of the third ventricle
Angiocentric glioma
Neuronal and mixed neuronal-glial tumours
Dysplastic gangliocytoma of cerebellum (Lhermitte-Duclos)
Desmoplastic infantile astrocytoma/ gangliocytoma Papillary glioneuronal tumour
Rosette-forming glioneuronal tumour of the fourth ventrice
Paraganglioma
Tumour of the pineal region Pineocytoma
Pineal parenchyma tumour of intermediate differentiation
Pineoblastoma
Papillary tumour of the pineal region
Embryonal tumours Medulloblastoma Desmoplastic/nodular medulloblastoma
Medulloblastoma with extensive nodularity
Anaplastic medulloblastoma Large cell medulloblastoma
CNS primitive neuroectodermal tumour
CNS neuroblastoma
CNS Ganglioneuroblastoma Medullo epithelioma
Ependymoblastoma
Perineurioma, NOS Malignant Perineurioma Malignant peripheral
Nerve sheath tumour (MPNST) Epithelioid MPNST
MPNST with mesenchimal differentiation
Melanotic MPNST
MPNST with glandular differentiation
TUMOURS OF THE MENINGES Tumours of the meningothelial cells
Meningioma Meningothelial Fibrous (fibroblastic) Transitional (mixed) Psammomatous Angiomatous Microcystic Secretory
Lymphoplasmacyte-rich Metaplastic
Anaplastic (malignant) Mesenchymal tumours Lipoma
Angiolipoma Hibernoma Liposarcoma
Solitary fibrous tumour Fibrosarcoma
Malignant fibrous histiocytoma Leiomyoma
Ewing sarcoma – PNET
Primary melanocytic lesions Diffuse melanocytosis
Melanocytoma Malignant melanoma Meningeal melanomatosis
Other neoplasms related to the meninges GERM CELL TUMOURS Germinoma
Embryonal carcinoma Yolk sac tumour Choriocarcinoma Teratoma
Mature Immature
Teratoma with malignant transformation
TUMOUR OF THE SELLAR REGION Craniopharyngioma
Adamntinomatous Papillary
Granular cell tumour Pituicytoma
Spindel cell ococytoma of the adenohypophysis METASTATIC TUMOUR
Dikutip dari : Louis dkk. The 2007 WHO Classification of Tumours of the Central Nervous System. Acta Neuropathol 2007;114:97-109.
II.2.5 Diagnosis
Pemeriksaan neurologis dapat membantu memberikan diagnosa banding dari tumor otak. Alat diagnostik dapat memberikan informasi spesifik dan akurat dari lokasi, ukuran, dan karakteristik dari suatu tumor. Teknik imaging seperti Computed Tomography (CT), Magnetic Resonance Imaging (MRI), dan angiografi sering digunakan untuk membantu menegakkan diagnosa. (Hill dkk 2002)
II.3 LIPOPROTEIN
II.3.1 Pengenalan Lipoprotein
Lipoprotein merupakan alat pengangkut utama dari kolestrol dan lipid lainnya. Dua jenis lipoprotein utama yang bertanggung jawab dalam transport kolestrol yaitu LDL dan HDL. (Cobbold dkk, 2002)
vertebra dan juga pada serangga. Lipoprotein di sintesa terutama di liver dan intestinal. (Jonas, 2002)
Kolestrol adalah substansi lemak yang terdapat di dalam sel-sel tubuh, yang mengalir dalam darah pada partikel yang disebut dengan lipoprotein. Tiga lipoprotein utama yaitu LDL, HDL, dan VLDL. (Birtcher, 2004)
Pada plasma puasa dari individu hanya terdiri dari partikel VLDL, LDL dan HDL, dan tidak mengandung chylomicrons. (Crook, 2012)
Plasma puasa merupakan pemeriksaan penting dalam menilai trigliserida karena kadar trigliserida meningkat beberapa jam setelah makan. Kadar trigliserida tidak puasa bervariasi tergantung pada berapa jam post-prandial, dimana kadar tertinggi didapatkan pada 4-5 jam stetelah makan. Kadar trigliserida didapatkan dari formula Friedwald, dimana untuk formula ini memakai plasma puasa. (Nigam, 2011)
Kadar total kolestrol, kolestrol LDL, kolestrol HDL menurun 3-5 jam setelah makan terakhir, jika dibandingkan dengan kadar pada plasma puasa. Kadar trigliserida meningkat pada 6 jam setelah makan, jika dibandingkan dengan kadar pada plasma puasa. Perubahan maksimal kadar plasma puasa dan non puasa untuk :( Langsted dkk, 2008)
II.3.2 Struktur Lipoprotein
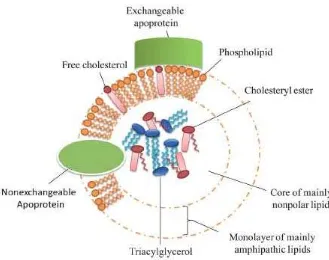
Lipoprotein adalah partikel yang terdiri dari lipid dan protein. Pada inti berupa lipid nonpolar berupa ester koliesteryl dan triasilgliserol, dan pada lapisan luar berupa posfolipid, kolestrol non esterifikasi dan protein. (Ahmadraji dkk, 2013)
Gambar 2. Struktur Umum Lipoprotein
Dikutip dari : Ahmadraji, T., Killard, A. 2013. The Evolution of Selective Analyses of HDL and LDL cholestrol in clinical and point of care testing.
Analytical Method; 5(15): 3612-25
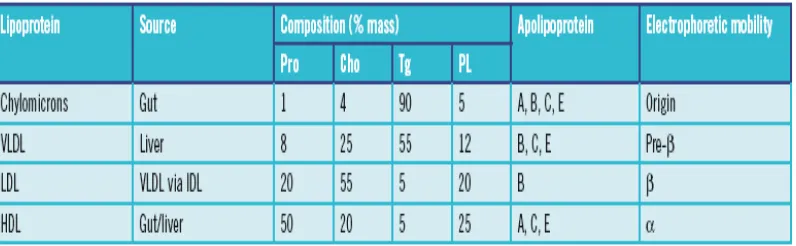
II.3.3 Klasifikasi Lipoprotein
Tabel 3 . Karakteristik dari Lipoprotein
Dikutip dari : Crook, M.A. 2012. Lipoproteins. In: Arnold, H., editors. Clinical Biochemistry and Metabolic Medicine. Hodder Education
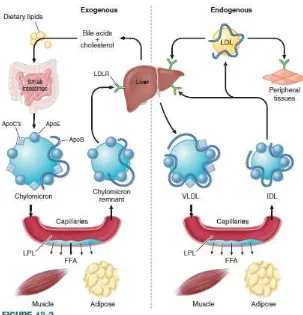
II.3.4 Metabolisme Lipoprotein
Metabolisme lipoprotein dapat dibagi atas tiga jalur yaitu metabolisme eksogen, jalur metabolisme endogen, dan jalur reverse cholestrol transport. Kedua jalur pertama berhubungan dengan metabolisme kolestrol LDL dan trigliserid, sedangkan jalur reverse cholestrol transport khusus mengenai metabolisme kolestrol HDL. (Crook, 2012)
II.3.4.1 Jalur Metabolisme Eksogen
Kolestrol dan asam lemak berasal dari makanan berlemak yang di makan, kemudian bersama dengan empedu di absorbsi di sel mukosa intestinal dan kemudian mengalami re-esterifikasi dari bentuk ester kolestrol dan trigliserida.
II.3.4.2 Jalur Metabolisme Endogen
Jalur metabolisme endogen berasal dari trigliserida dan kolestrol yang di sintesis di hati dan di sekresi ke dalam sirkulasi sebagai lipoprotein VLDL. Dalam sirkulasi, trigliserida dalam VLDL akan mengalami hidrolisis oleh enzim lipoprotein lipase (LPL), dan VLDL berubah menjadi IDL yang juga akan mengalami hidrolisis dan berubah menjadi LDL. Sebagian VLDL, IDL, dan LDL akan mengangkut kolestrol ester kembali ke hati. LDL adalah lipoprotein yang paling banyak mengandung kolestrol. Sekitar 70% dari LDL melalui reseptor LDL mengalami endositosis di hepar.Sebagian dari kolestrol dalam LDL akan dibawa ke hati dan jaringan lainnya, seperti kelenjar adrenal, testis, dan ovarium yang mempunyai reseptor untuk kolestrol LDL.
II.3.4.3 Jalur reverse cholestrol transport
Gambar 3. Metabolisme Lipoprotein jalur endogen dan eksogen
Dikutip dari : Rader, D.J., Hobbs, H.H. Disorder of Lipoprotein Metabolism. In: Jameson, J.L., editors. Endocrinology. McGraw Hill Professional Publishing
II.3.5 Fungsi Lipoprotein
kemudian di ekskresikan dalam bentuk asam empedu (‘reverse cholestrol
transport’). (Jonas, 2002)
II.3.6 Patofisiologi Lipoprotein pada Stroke
Atrosklerosis dapat terjadi akibat inflamasi kronik dari interaksi antara lipoprotein, monosit yang berasal dari makrofag, komponen dari imunitas alami dan adaptif, elemen selluer normal dari dinding arteri. Proses tersebut menyebabkan pembentukan lesi kompleks atau plaque yang dapat menembus hingga ke dalam lumen arteri, sehingga mengganggu aliran darah. Plaque yang terbentuk dapat ruptur, menyebabkan trombosis intravaskular yang akhirnya menyebabkan komplikasi klinik akut yaitu infark miokard dan stroke. (Brunzell dkk, 2008)
Diantara beberapa faktor yang berkontribusi dalam aterosklerosis, kadar kolestrol merupakan salah satu faktor dominan yang berperan dalam inisiasi dan progresifitas atersklerosis. (Brunzell dkk, 2008)
Tahap awal aterosklerosis terjadi pada ruang diantara sel endotel dan sel otot polos, di lapisan subendotel atau intima. Pada daerah tersebut terdapat deposit kolestrol, yang kemudian terbentuk “sel foam”. Bila akumulasi lipid berlanjut, terbentuk ateroma atau plaq fibrous, yang menyebabkan peningkatan jumlah dari proliferasi sel otot polos dan lipid ekstraselluler, sehingga merusak dinding pembuluh darah dan menggangggu aliran darah serta merangsang pembentukan plaq lebih lanjut. (Cobbold dkk, 2002)
Pembawa utama kolestrol dan lipid lainnya dalam tubuh yaitu lipoprotein. Dua jenis lipoprotein utama yang bertanggung jawab dalam transport kolestrol yaitu LDL dan HDL. Kedua jenis liportein tersebut dapat masuk ke dalam aliran darah sampai ke lapisan intima. Bila lipoprotein menempati lapisan intima yang rapuh maka oksidasi lebih mudah terjadi. Oksidasi terjadi bila sel melepaskan radikal bebas seperti radikal peroksil dan reaksi kimia. Sel tersebut merusak lipoprotein, dan bila pertahanan partikell antioksidan terganggu, maka dapat menyebabkan peroksidasi dari inti lipid. Pada stadium yang lanjut, proses tersebut dapat menyebabkan modifikasi dari permukaan protein, sehingga memungkinkan terjadinya oksidasi lipoprotein menjadi scavenger reseptor. (Cobbold dkk, 2002)
Reverse transport cholestrol diduga sebagai mekanisme HDL dalam
efektif sebagai perlindungan terhadap serangan radikal bebas. (Cobbold dkk, 2002)
Resiko stroke menurun diduga oleh karena kolestrol HDL memiliki efek antiaterosklerotik secara langsung, yaitu meliputi kemampuannya dalam transportasi kolestrol dalam kembali dari sel perifer menuju ke hepar. Selain itu juga kolestrol HDL diduga dapat mencegah aterosklerosis melalui inhibisi oksidasi LDL pada dinding arteri, yang dapat berpengaruh secara langsung pada pelepasan faktor relaksing dari endotelium. (Soyama dkk, 2013)
Mekanisme yang menjelaskan hubungan antara kolestrol LDL dan perdarahan intreserebral masih belum jelas. Salah satu teori yang dapat menjelaskan hubungan antara kolestrol LDL dan perdarahan intreserebral yaitu peranan dari level serum kolestrol dalam menjaga integritas dari pembuluh darah vaskular. Rendahnya kadar kolestrol berhubungan dengan nekrosis dari sel otot polos medial, sehingga menyebabkan rendahnya resistensi dan akhirnya menyebabkan ruptur dinding vaskular. Lebih lanjut disebutkan bahwa level kolestrol dapat memodifikasi kemampuan agregasi platelet melalui faktor aktivasi platelet, sehingga rendahnya kadar kolestrol dapat menurunkan agregasi platelet, yang dapat menjadi predisposisi dari kejadian perdarahan intraserebral. (Rodriguez dkk, 2011)
II.3.7 Patofisiologi Lipoprotein pada Tumor Otak
peningkatan kolestrol LDL serta kadar total kolestrol diduga berhubungan dengan level sitokin proinflamasi, termasuk didalamnya yaitu nekrosis faktor-α dan interleukin-6. (Hu dkk 2011)
Sistem saraf pusat mempunyai mekanisme dalam transport dan suplai kolestrol, yang diduga memiliki hubungan dengan hemostasis kolestrol dari tubuh. Sel-sel otak menggunakan manfaat kolestrol dari serum, setelah kolestrol tersebut didistribusikan melewati BBB, atau berasal dari sintesis endogen di dalam otak. Lipoprotein memegang peranan penting dalam redistribusi kolestrol di dalam SSP. Beberapa lipoprotein berinteraksi dengan reseptor khusus dari sel penerima, sehingga menyebabkan uptake selluler dan pemecahan partikel lipoprotein. (Gatchev dkk, 1994)
Lipoprotein β (LDL) berpartispasi dalam transport kolestrol dalam
melewati BBB, dimana dalam jalur ini mempengaruhi suplai kolestrol ke SSP. (Gatchev dkk, 1994)
Proses lanjutan dari pertumbuhan selluler ditandai dengan peningkatan gangguan sintesa kolestrol dengan adanya akumulasi kolestrol pada jaringan yang tumbuh dan reduksi dari kolestrol HDL pada plasma. Stress oksidatif dapat membentuk beberapa tipe lipid yang dapat merusak jaringan. (Hasan, dkk 2009)
Fungsi utama dari HDL yaitu menjaga homeostasis normal kolestrol. Pada saat jaringan tumor berkembang, terjadi peningkatan pembuangan sisa kolestrol dari intraselluler, sehingga diduga bahwa rendahnya kadar kolestrol HDL berhubungan dengan peningkatan metabolisme kolestrol pada jaringan yang mengalami proliferasi. (Hasan, dkk 2009)
malondialdehyde (MDA). Malondialdehyde mempunyai efek sitotoksik yang
tinggi dan menginhibisi kerja enzim protektif, yang dapat bertindak sebagai perangsang terjadinya tumor dan agen karsinogenik. (Hasan, dkk 2009)
II.4 Kerangka Teori Remodelling VLDL
↑HDL berhubungan dengan ↓ insidens dari kolestrol dan lipid lainnya (Cobbold, 2002)
IDL
Lipoprotein di klasifikasikan dalam 5 kelompok utama, yaitu chylomicrons, VLDL, IDL , LDL, dan HDL. ( Crook, 2012)
Lipid Peroksidasi Plasma puasa hanya terdiri dari
partikel VLDL, LDL dan HDL,tidak mengandung
chylomicrons. (Crook, 2012)
Pada jalur metabolisme endogen, VLDL remnants hidrolisa IDL remodelling oleh Hepatic Lipase LDL (Rader,2010)
LDL plasma native LDL masuk ke endotel LDL oksidasi efek proaterogenik aterosklerosis (Cobbold,2002)
HDL mempunyai efek mencegah lipid peroksidasi
Anti carcinogen dan AntI oksidan (Dabrowa 2011)
LDL↑, VLDL↑, (<40mg/dL) Stroke Iskemik (Curb, 2003)
LDL & VLDL ↑, HDL↓
LDL↑ (>106 mg%), VLDL↑(>30 mg%) Stroke Iskemik(Sredhar, 2010)
LDL & VLDL ↑, HDL↓
Stroke Iskemik (Mahmood, 2009)
LDL↑,VLDL↑,HDL↓
II.5 Kerangka Konsep
LIPOPROTEIN
LDL HDL
TUMOR OTAK STROKE