PENGARUH JENIS LARUTAN PERENDAM SERTA METODE PENGERINGAN TERHADAP
SIFAT FISIK, KIMIA, DAN FUNGSIONAL GELATIN DARI KULIT CUCUT
[The Influence of Solvent Variety and Drying Method on Physical,
Chemical and Functional Characteristic of Shark Skin Gelatin]
Made Astawan
1), dan Tita Aviana
2)1)Staf Pengajar Jurusan Teknologi Pangan dan Gizi, FATETA, Institut Pertanian Bogor, Kampus IPB Darmaga Bogor 16002
2) Alumni Jurusan Teknologi Pangan dan Gizi,FATETA, Institut Pertanian Bogor, Kampus IPB Darmaga Bogor 16002
Diterima 23 September 2002/Disetujui 16 April 2003
ABSTRACT
Gelatin is a denaturation product of collagen and has been widely utilized for foods, photography uses, medical materials, and culture materials for microorganisms. Recently, gelatin’s uses has expanded to new applications such as health foods. Gelatin of land animal origin such as bovine and porcine has been mainly used. However, gelatin with new properties is desired to develop expanded applications. In this research gelatin was made from shark skin. The shark skin collagen was distended by acetic acid solution (acid process) and sodium hydroxide solution (alkali process), and gelatin was then extracted at 80oC of water. The extracted gelatin was dried by vacuum drying and freeze drying to obtain powder product. Shark gelatin produced by the combination of alkali and vacuum drying process (OVB gelatin) had better qualities on yield, water content, gel strength, melting point, and emulsion stability as compared to the others. Sensory evaluation indicated that shark gelatin had lower values in color, odor, and performance as compared to the commercial gelatin of fish, pig and bovine (SKW Biosystem). However, as compared to the commercial gelatins, OVB gelatin had a similar values on gel strength (202 bloom) and emulsion stability (100%), but higher values on viscosity (8 cP) and pH (9.3). Those values indicated that ray skin gelatin can be used to substitute the commercial gelatin in some food industries
Key words: Gelatin, shark, melting point, and emulsion stability
PENDAHULUAN
Gelatin adalah protein dari kolagen kulit, membran, tulang dan bagian tubuh berkolagen lainnya. Gelatin jika direndam dalam air akan mengembang dan menjadi lunak, berangsur-angsur menyerap air 5-10 kali bobot semula. Gelatin larut dalam air panas dan jika didinginkan membentuk gel (Anonim, 1978).
Dalam industri pangan, gelatin ikan digunakan antara lain sebagai perekat, coating terutama pada produk beku (refrigerated or frozen product)(BioFX, 2000), gelling agent, binding agent, pembentuk film dan penstabil (Croda, 2000).
Bahan baku gelatin komersial sebagian besar berasal dari sapi dan babi. Penggunaan gelatin babi merupakan penghambat utama bagi pengembangan produk-produk pangan di negara-negara yang penduduknya mayoritas beragama Islam, seperti halnya di Indonesia. Sumber utama lain yang sangat potensial sebagai bahan baku gelatin adalah kolagen yang berasal dari ikan. Menurut Surono et al., (1994) tulang dan kulit ikan sangat potensial sebagai sumber gelatin karena mencakup 10-20 % dari total berat tubuh ikan.
Pada penelitian ini dilakukan proses ekstraksi dan analisis sifat fisik, kimia dan fungsional gelatin dengan bahan baku kulit ikan cucut. Beberapa sifat gelatin hasil penelitian dibandingkan dengan gelatin komersial asal sapi, babi dan ikan (SKW Biosystem).
METODOLOGI
Bahan dan alat
Bahan baku yang digunakan pada penelitian ini adalah kulit ikan cucut yang diperoleh dari TPI Pelabuhan Ratu Sukabumi. Bahan lain yang digunakan adalah akuades, etanol 98 %, asam asetat, dan NaOH. Alat yang digunakan adalah alat-alat gelas, penyaring Buchner, pH meter, rotavapor, heater, waterbath, pengering vakum, desikator, blender/mortar, loyang alumunium, baskom atau wadah plastik, pisau dan kain saring.
Metode
Prinsip pembuatan gelatin adalah hidrolisis kolagen kulit cucut dengan menggunakan pelarut asam atau basa. Gelatin yang dihasilkan (tipe A untuk asam dan tipe B untuk basa) selanjutnya diekstraksi dengan air panas,
dikeringkan dan ditepungkan. Penelitian ini dilakukan dengan menggunakan dua jenis larutan perendam (untuk hidrolisis), yaitu asam asetat dan NaOH, serta dua jenis metode pengeringan yaitu pengering vakum dan pengering beku (freeze dryer). Terhadap gelatin yang dihasilkan selanjutnya dilakukan analisis sifat fisik, kimia dan fungsional (warna, penampakan umum, bau, aw. kadar air,
abu, lemak, protein, logam berat, NaCl, komposisi asam amino, nitrogen non protein, kekentalan, pH, titik leleh, titik isoelektrik, suhu dan waktu pembentukan gel, kekuatan gel, densitas kamba, kapasitas emulsi dan stabilitas emulsi) serta dibandingkan dengan gelatin komersial.
HASIL DAN PEMBAHASAN
Pada penelitian ini dihasilkan empat jenis gelatin, yaitu : OVA (perlakuan asam asetat dengan metode pengering vakum), FDA (perlakuan asam asetat dengan metode freeze dryer), OVB (perlakuan basa NaOH dengan metode pengering vakum), FDB (perlakuan basa NaOH dengan metode freeze dryer). Analisis sifat fisik, kimia dan fungsional gelatin kulit cucut dapat dilihat pada Tabel 1.
Rendemen
Analisis varian menunjukkan bahwa metode pengeringan, serta interaksi antara metode pengeringan dan jenis larutan perendam berpengaruh sangat nyata (p<0.01) terhadap rendemen. Rendemen gelatin tertinggi diperoleh dari gelatin dengan perlakuan OVB yaitu 17.2 %
sedangkan yang terendah didapat dari perlakuan FDB yaitu 4.1 % (Tabel 1). Pada perendaman menggunakan larutan perendam NaOH, kemungkinan kolagen terkonversi secara maksimal menjadi gelatin sedangkan pada perendaman menggunakan asam asetat, masih ada kolagen yang belum terkonversi menjadi gelatin atau telah terjadi degradasi lanjutan pada gelatin yang telah terbentuk. Selain itu terdapat kecenderungan bahwa perlakuan dengan pengering vakum menghasilkan rendemen lebih banyak daripada freeze dryer. Pada pengering vakum, gelatin hanya sedikit sekali tertinggal di dalam loyang sehingga dapat dikatakan tidak mempengaruhi rendemen yang dihasilkan. Sebaliknya pada freeze dryer, pengambilan gelatin yang telah kering dari botol pengering sangat sulit karena gelatin menempel kuat sehingga masih ada gelatin yang tertinggal dalam botol pengering.
Derajat putih
Sesungguhnya warna bukanlah parameter penting yang dinilai pada pemilihan gelatin, tetapi cukup berpengaruh terhadap subyektivitas seseorang. Analisis varian menunjukkan bahwa perlakuan jenis larutan perendam, metode pengeringan dan interaksinya berpengaruh sangat nyata terhadap derajat putih gelatin. Secara keseluruhan, warna yang dihasilkan adalah kuning kecoklatan. Gelatin FDA memiliki nilai derajat putih tertinggi (Tabel 1) yaitu 50.5. Nilai derajat putih ini jauh lebih rendah dibandingkan gelatin yang diperoleh dengan metode spray dryer, yaitu 100 (Astawan et al., 2001).
Tabel 1. Sifat fisik, kimia dan fungsional gelatin kulit cucut berdasarkan jenis larutan perendam dan metode pengeringan
Parameter OVA FDA OVB FDB
Rendemen (%) 8.9a 6.9 a 17.2 b 4.1 a Derajat putih 49.9 a 50.5 b 46.5 c 44.9 d Nilai aw 0.70 a 0.74 b 0.76 b 0.76 b Kadar air (%) 12.4 a 9.3 a 4.3 a 9.3 a Kadar abu (%) 4.3 a 2.9 a 3.9 a 3.7 a Kadar NNP (%) 1.6 a 1.4 a 1.7 a 1.4 a Kadar protein (%) 80.9 a 85.4 a 81.1 a 86.6 a Kadar lemak (%) 0.5 a 0.4 a 1.7 a 0.7 a Nilai pH 5.1a 5.3 a 9.2 c 7.8b Kadar NaCl (%) 0.1 a 0.03 a 0.02 a 0.09 a
Kekuatan gel (bloom) 100.4b 111.7c 112.1c 43.1a
Viskositas (cP) 5.3 a 8.57c 8c 6.9b Titik leleh (oC) 24 a 24 a 26 a 20 b Titik isoelektrik 7 8 4 5 Densitas kamba (gr/ml) 0.6 a 0.3 a 0.3 a 0.4 a Kapasitas emulsi (%) 52.5 a 35 b 46.5 a 51 a Stabilitas emulsi (%) 86 a 85.3 a 100 a 97 a
Keterangan : Nilai yang diikuti oleh huruf yang berbeda pada baris yang sama menunjukkan adanya perbedaan yang nyata (p<0.05).
OVA : perlakuan asam asetat dan pengering vakum; FDA : perlakuan asam asetat dan freeze dryer; OVB : perlakuan basa NaOH dan pengering vakum; FDB: perlakuan basa NaOH dan freeze dryer
Dengan demikian jelaslah bahwa warna kecoklatan yang timbul lebih disebabkan oleh metode pengeringan dibandingkan faktor lainnya.
Nilai a
wAktivitas air (aw) merupakan jumlah air bebas yang
dapat digunakan oleh mikroba untuk pertumbuhannya. Pengukuran nilai aw dilakukan pada suhu yang sama yaitu
27.30C. Nilai aw berkisar antara 0.70 – 0.76 (Tabel 1).
Analisis varian menunjukkan bahwa perlakuan OVA menghasilkan gelatin dengan nilai aw terendah, serta
berbeda nyata dengan perlakuan lainnya.
Kadar air
Kadar air dalam bahan pangan merupakan salah satu faktor yang mempengaruhi aktivitas enzim, mikroba, kimia, serta reaksi-reaksi non enzimatis, sehingga menimbulkan perubahan pada sifat-sifat organoleptik, penampakan, tekstur, citarasa dan nilai gizi. Analisis varian menunjukkan bahwa kedua jenis perlakuan dan interaksinya tidak berpengaruh nyata terhadap kadar air gelatin yang dihasilkan. Nilai kadar air gelatin dari keempat kombinasi perlakuan (Tabel 1) berkisar antara 4.3 – 12.4%, sehingga masih memenuhi standar mutu SNI tentang gelatin(1995) yaitu kadar air maksimal 16%.
Kadar abu
Kadar abu produk berkisar antara 2.9 – 4.3 % (Tabel 1). Kombinasi kedua perlakuan tidak berpengaruh nyata terhadap kadar abu produk. Dari ke-empat jenis gelatin, hanya gelatin FDA yang memiliki kadar abu yang sesuai dengan standar mutu SNI (1995) yaitu maksimal 3.25. Tingginya kadar abu pada gelatin hasil penelitian kemungkinan disebabkan oleh masih adanya komponen mineral yang terikat pada kolagen, yang belum terlepas saat proses pencucian sehingga ikut terekstraksi dan terbawa pada gelatin yang dihasilkan.
Kadar protein dan nitrogen non protein (NNP)
Ikan bertulang rawan (seperti cucut) mempunyai kandungan NNP berkisar 33-38.6% dari seluruh nitrogen tubuh, yaitu jauh lebih tinggi dibandingkan ikan bertulang keras (9.2-18.3%) (Simidu, 1961). Tabel 1 menunjukkan kadar NNP gelatin berkisar antara 1.4 – 1.7 % . Kadar protein ditentukan dengan metode Kjeldahl, dimana kadar N total dikurangi dengan kadarNNP, kemudian dikalikan dengan faktor konversi yaitu 5.46 (proses asam) dan 5.51 (proses basa) (Eastoe dan Leach, 1977).Kadar protein gelatin kulit cucut berkisar antara 80.9 % (gelatin OVA) sampai 86.6% (gelatin FDB). Kadar protein dipengaruhi oleh proses perendaman kulit dimana reaksi pemutusan ikatan hidrogen dan pembukaan struktur
koil kolagen terjadi secara optimal sehingga protein terekstrak dan terlepas dari gelatin, akibatnya menurunkan kadar protein gelatin. Analisis varian menunjukkan bahwa kombinasi perlakuan tidak berpengaruh nyata terhadap kadar protein gelatin.
Kadar lemak
Kadar lemak tertinggi terdapat pada gelatin OVB (1.7%) sedangkan yang terendah terdapat pada gelatin FDA (0.4%) (Tabel 1). Kisaran nilai tersebut cukup baik karena tidak melebihi 5 % yang merupakan batasan nilai maksimal untuk persyaratan mutu gelatin (Jobling dan Jobling, 1983 yang dikutip oleh Pelu et al., 1998).
Nilai pH
Nilai pH akan berpengaruh terhadap aplikasi gelatin. Gelatin dengan pH netral sangat baik untuk produk daging, farmasi, fotografi, cat dan sebagainya. Sedangkan gelatin dengan pH rendah akan sangat baik untuk digunakan dalam produk juice, jelly, sirop dan sebagainya. Nilai pH gelatin sangat dipengaruhi oleh jenis larutan perendam. Kisaran pH untuk gelatin OVA (5.1)dan FDA (5.3) sesuai dengan kisaran pH gelatin dengan proses asam menurut Tourtellote (1980), yaitu 3.8 - 6 dan menurut Wainewright (1977) yaitu 4 - 7. Sedangkan untuk gelatin OVB dan FDB, nilai pH-nya lebih tinggi dari kisaran pH yang berlaku untuk gelatin dengan proses basa menurut Tourtellote (1980), yaitu 5 - 7.1. Tingginya pH pada gelatin OVB (9.2) dan FDB (7.8) (Tabel 1) kemungkinan disebabkan oleh adanya larutan perendam (NaOH) yang terperangkap pada saat proses swelling. Larutan perendam yang terperangkap ini sulit untuk dicuci atau dihilangkan secara sempurna sehingga mempengaruhi pH akhir produk.
Kadar NaCl
Kadar NaCl gelatin hasil penelitian berkisar antara 0.02 – 0.1 % (Tabel 1), terjadi penurunan dibandingkan kadar garam bahan bakunya yang berkisar antara 0.6 – 1.8 % (Kreuzer dan Ahmad, 1978). Kadar NaCl pada gelatin hasil penelitian ini tidak berbeda jauh dengan kadar NaCl pada gelatin komersial Leiner Davis, yaitu 0.06% (Astawan et al, 2001).
Kekuatan gel
Kekuatan gel pada gelatin dipengaruhi oleh asam, alkali dan panas yang akan merusak struktur gelatin sehingga gel tidak akan terbentuk (Glicksmann, 1969). Jenis larutan perendam yang digunakan berpengaruh pada panjang rantai peptida gelatin. Menurut Stainsby (1977) kekuatan gel gelatin berkaitan dengan panjang rantai asam
amino dimana rantai asam amino yang panjang akan menghasilkan kekuatan gel yang besar pula.
Gelatin FDA dan OVB memiliki kekuatan gel yang lebih baik dibandingkan gelatin lainnya, yaitu masing 111 dan 112 bloom (Tabel 1). Pada proses hidrolisis yang optimal, rantai asam amino yang terbentuk pada saat konversi kolagen menjadi gelatin adalah panjang sehingga kekuatan gel yang dihasilkan juga tinggi.
Viskositas
Pengukuran viskositas dilakukan pada suhu 60oC.
Nilai viskositas terbesar didapat pada gelatin FDA (8.57 cP) sedangkan nilai terendah didapat pada gelatin OVA (5.3 cP) (Tabel 1). Viskositas dipengaruhi oleh BM (berat molekul) dan distribusi molekul gelatin. Ada kecenderungan bahwa perlakuan perendam basa menghasilkan viskositas lebih besar daripada perlakuan asam (Tabel 1). Hal ini kemungkinan disebabkan pada proses perendaman, perendam basa menghasilkan gelatin secara optimal dengan rantai-rantai peptida panjang sehingga BM menjadi lebih besar dan viskositas yang terukur pun lebih besar.
Titik leleh
Pada Tabel 1 terlihat bahwa gelatin OVA, FDA dan OVB memiliki titik leleh yang tidak berbeda nyata (24-26oC), tetapi lebih tinggi dibandingkan titik leleh gelatin
FDB (20oC). Nilai-nilai tersebut sesuai dengan titik leleh
gelatin menurut Shelby (1955), yaitu antara 24 – 33oC.
Titik leleh dipengaruhi oleh keadaan awal pembentukan gel. Apabila gel terbentuk dengan cepat, maka gel yang dihasilkan kurang stabil dan lebih cepat meleleh. Selain itu gelatin yang mengalami pengeringan dengan suhu lebih tinggi umumnya menunjukkan titik leleh yang lebih tinggi pula.
Titik isoelektrik
Pengetahuan tentang titik isoelektrik gelatin sangat berhubungan dengan aplikasinya dalam berbagai produk, terutama berkaitan dengan kelarutan protein. Pada titik isoelektriknya, kelarutan protein sangat rendah shingga terjadi penggumpalan atau pengendapan protein.Untuk aplikasi yang menginginkan kelarutan gelatin, kisaran pH yang dapat digunakan adalah kisaran selain pH titik isoelektrik. Menurut Eastoe (1967) titik isoelektrik gelatin dapat bervariasi antara 4.8 – 9.4. Gelatin dengan proses asam memiliki titik isoleketrik lebih tinggi dibandingkan gelatin dengan proses basa. Berdasarkan pengamatan (Tabel 1), titik isoelektrik gelatin OVA dan FDA masing-masing adalah 7 dan 8, sedangkan untuk gelatin OVB dan FDB masing-masing adalah 4 dan 5.
Densitas kamba
Densitas kamba berhubungan dengan ukuran atau luas permukaan bahan yang diukur. Densitas kamba sangat berguna dalam penyimpanan. Bila densitas kambanya besar, maka dalam wadah yang sama dapat disimpan lebih banyak bahan. Pengukuran densitas kamba terhadap keempat perlakuan menunjukkan bahwa gelatin hasil penelitian memiliki densitas kamba antara 0.3 – 0.6 (Tabel 1). Analisis varian menunjukkan bahwa kedua perlakuan dan interaksinya tidak berpengaruh nyata terhadap densitas kamba.
Kapasitas emulsi
Berdasarkan pengamatan pada gelatin hasil penelitian (Tabel 1), kapasitas emulsi tertinggi diperoleh dari gelatin OVA (52.5%) sedangkan kapasitas emulsi terendah didapat dari gelatin FDA (35%).
Stabilitas emulsi
Gelatin sebagai koloid yang bersifat hidrofilik dapat digunakan untuk menstabilkan koloid yang bersifat hidrofobik, sehingga efektif digunakan sebagai pengemulsi dan penstabil dalam sistem emulsi (Glicksman, 1969). Pembentukan emulsi pada gelatin dipengaruhi oleh gugus polar bebas yang larut dalam air dan rantai hidrokarbon yang larut pada fase minyak. Berdasarkan pengamatan yang dilakukan, stabilitas emulsi terbesar diperoleh dari gelatin OVB yaitu 100 % diikuti gelatin FDB, OVA dan FDA (Tabel 1). Stabilitas emulsi yang tidak mencapai 100% kemungkinan dikarenakan protein tidak cukup besar untuk menyelimuti seluruh globula lemak sehingga globula lebih bebas bergerak dan membentuk agregat satu sama lain sehingga emulsi menjadi kurang stabil.
Suhu dan waktu pembentukan gel
Analisis ini dilakukan pada tiga macam suhu yaitu 70C, 170C dan 27oC (Tabel 2). Pada suhu ruang (sekitar
270C) semua larutan gelatin tetap cair dan tidak dapat
membentuk gel. Gel dapat terbentuk pada suhu 17 dan 70C, dimana makin rendah suhu maka makin cepat waktu
yang diperlukan untuk membentuk gel. Menurut Glicksman (1969) pembentukan gel pada gelatin terjadi akibat ikatan hidrogen antar molekul gelatin sehingga dihasilkan gel semi padat yang terikat dalam komponen air.
Komposisi asam amino
Analisis komposisi asam amino ditentukan dengan teknik High Performance Lyquid Chromatography (HPLC). Tabel 3 menunjukkan komposisi asam amino yang terkandung pada gelatin kulit cucut. Kandungan glisin pada gelatin OVA (24.8%) dan OVB (24.7%) hampir mencakup sepertiga bagian dari kandungan total asam amino. Hal ini
sesuai dengan pendapat Charley (1982) yang menyatakan bahwa glisin merupakan asam amino utama dan merupakan sepertiga dari seluruh asam amino yang menyusun gelatin.
Logam berat
Analisis logam berat sangat penting bagi gelatin antara lain untuk menentukan apakah gelatin tersebut
aman digunakan, terutama dikonsumsi dalam produk pangan atau obat-obatan. Pada Tabel 4 terlihat bahwa kandungan logam berat pada gelatin tergolong rendah dan sesuai dengan SNI 1995, bahkan beberapa logam berat dinyatakan tidak terdeteksi. Hal ini menunjukkan bahwa gelatin hasil penelitian bersifat aman dan dapat digunakan di industri pangan.
Tabel 2. Suhu dan waktu pembentukan gel pada gelatin kulit cucut OVA dan OVB Jenis
Perlakuan Suhu (
oC) Waktu
(menit) perlakuan Jenis Suhu (
oC) Waktu
(menit)
OVA 7 26 OVB 7 24
17 120 17 120
27 Tak terbentuk gel 27 Tak terbentuk gel
FDA 7 26 FDB 7 26
17 90 17 80
27 Tak terbentuk gel 27 Tak terbentuk gel
Tabel 3. Komposisi asam amino gelatin ikan cucut OVA dan OVB (%, b/b)
Asam amino OVA OVB Referensi*
Aspartat 5.9 5.5 6 - 7 Glutamat 12.2 11.6 - Serin 4.1 3.3 2.9 - 4.2 Histidin 1.2 1.0 0.7 - 1 Glisin 24.8 24.7 26 - 31 Threonin 3.3 3.3 2.2 - 2.4 Arginin 9.3 9.0 8 - 9 Alanin 10.8 10.4 8 - 11 Tirosin 0.5 0.3 0.2 - 1 Methionin 2.4 2.1 0.7 - 1 Valin 2.9 2.9 2.6 - 3.4 Fenilalanin 2.5 2.2 2 - 3 l-leusin 2.76 2.36 - Leusin 3.25 3.13 3 - 3.5 Lisin 3.82 3.71 4 - 5 Jumlah Total 89.73 85.5
*) : Kandungan asam amino gelatin menurut Poppe (1992)
Tabel 4. Kandungan logam berat gelatin ikan cucut OVA dan OVB
Llogam OVA (mg/kg) OVB (mg/kg) SNI 1995 Raksa (Hg) Ttd Ttd - Timbal (Pb) Ttd Ttd Maks. 50 mg/kg
Tembaga (Cu) 7.75 4.85 Maks. 30 mg/kg
Arsen (As) Ttd Ttd Maks. 2 mg/kg
Seng (Zn) 11.87 35.03 Maks. 1000 mg/kg
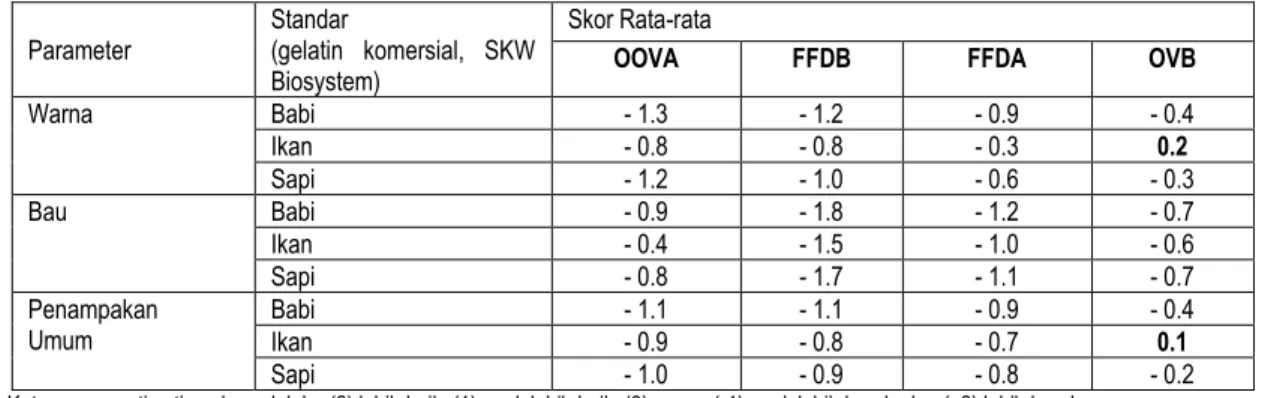
Tabel 5. Uji organoleptik gelatin cucut menggunakan uji pembandingan jamak terhadap gelatin babi, sapi dan ikan komersial
Parameter Standar (gelatin komersial, SKW
Biosystem)
Skor Rata-rata
OOVA FFDB FFDA OVB
Warna Babi - 1.3 - 1.2 - 0.9 - 0.4 Ikan - 0.8 - 0.8 - 0.3 0.2 Sapi - 1.2 - 1.0 - 0.6 - 0.3 Bau Babi - 0.9 - 1.8 - 1.2 - 0.7 Ikan - 0.4 - 1.5 - 1.0 - 0.6 Sapi - 0.8 - 1.7 - 1.1 - 0.7 Penampakan Umum Babi - 1.1 - 1.1 - 0.9 - 0.4 Ikan - 0.9 - 0.8 - 0.7 0.1 Sapi - 1.0 - 0.9 - 0.8 - 0.2
Keterangan: arti setiap skor adalah : (2) lebih baik, (1) agak lebih baik, (0) sama, (-1) agak lebih buruk, dan (–2) lebih buruk.
Perbandingan antara gelatin hasil penelitian dan
gelatin komersial
Sebagai pembanding digunakan gelatin babi, ikan dan sapi komersial yaitu gelatin SKW Biosystem. Namun karena keterbatasan jumlah produk, maka tidak semua analisis dilakukan terhadap gelatin komersial.
Berdasarkan data pada Tabel 6, terlihat bahwa gelatin hasil penelitian memiliki derajat putih lebih rendah daripada gelatin komersial, terutama gelatin babi dan sapi. Pengukuran viskositas dilakukan pada suhu 60oC, dimana
hasil pengukuran menunjukkan bahwa gelatin komersial memiliki viskositas yang lebih rendah. Densitas kamba pada gelatin komersial tidak terlalu jauh berbeda dengan gelatin hasil penelitian, demikian juga dengan stabilitas emulsi.
Nilai pH gelatin hasil penelitian menunjukkan nilai yang agak tinggi pada perlakuan basa, kemungkinan disebabkan adanya sisa larutan perendam yang masih terikat pada saat proses swelling. Kapasitas emulsi gelatin hasil penelitian tidak setinggi pada gelatin komersial, terutama pada gelatin ikan komersial tetapi sedikit menyamai gelatin babi dan sapi. Walaupun kapasitas emulsi gelatin hasil penelitian kurang baik, namun bila dilihat dari stabilitas emulsi cukup baik.
KESIMPULAN DAN SARAN
Analisis sifat fisik, kimia dan fungsional gelatin menunjukkan gelatin dengan proses asam umumnya memiliki sifat yang hampir sama dengan gelatin dengan proses basa, kecuali pada rendemen dan pH larutan. Pembuatan gelatin dengan penggunaan pengering vakum lebih menguntungkan dari segi ekonomis dan waktu dibandingkan freeze dryer.
Perbandingan beberapa sifat fisik, kimia dan fungsional gelatin hasil penelitian dengan gelatin komersial (SKW Biosystem) menunjukkan perbedaan nilai yang beragam. Berdasarkan data-data tersebut, dapat dikatakan bahwa aplikasi gelatin hasil penelitian lebih terbatas dibandingkan gelatin komersial dari sapi dan babi.
Untuk penelitian lebih lanjut, perlu diadakan usaha penghilangan bau amis pada gelatin cucut. Berdasarkan informasi tentang sifat fisik, kimia dan fungsionalnya, perlu dilakukan penelitian mengenai aplikasi gelatin kulit cucut pada berbagai produk pangan.
Tabel 6. Perbandingan beberapa sifat gelatin hasil penelitian dengan gelatin komersial. Jenis gelatin Derajat putih
Viskositas (cP) Kekuatan gel (bloom) Densitas kamba (gr/ml) pH Kapasitas emulsi (%) Stabilitas emulsi (%) OVA 49.9 5.3 117.2 0.6 5.1 52.5 86 FDA 50.5 8.6 111.7 0.3 5.3 35 85.3 OVB 46.5 8 202.2 0.3 9.3 46.5 100 FDB 44.9 6.9 43.1 0.4 7.8 51 97 Gelatin babi* 78.7 3 200 0.6 5.2 50 100 Gelatin ikan* 58.1 3.6 200 0.1 5.7 70 100 Gelatin sapi* 65.2 2.9 200 0.6 5.3 50 100
UCAPAN TERIMA KASIH
Peneliti mengucapkan terima kasih kepada Kantor Menteri Negara Riset dan Teknologi – Lembaga Ilmu Pengetahuan Indonesia, yang telah membiayai penelitian ini melalui Proyek Riset Unggulan Terpadu (RUT) VIII dengan Surat Perjanjian Kerjasama Nomor: 011.09/SK/RUT/2001 tanggal 26 Januari 2001.
DAFTAR PUSTAKA
Anonim. 1978. Mutu dan Cara Uji Gelatin. Departemen
Perindustrian. Jakarta
Astawan, M., P. Hariyadi, R. Peranginangin. 2001.
Teknik Ekstraksi Gelatin dari Kulit dan Tulang Ikan serta Aplikasinya pada Produk Pangan. Laporan RUT.
BioFX. 2000. Fish Gelatin and Buffered Fish Gelatin
Blocks, Diluents and Coating Solutions. www.biofx.com/fish.html
Charley, H. 1982. Food Science. 2nd edition. John Wiley
and Sons, New York
Croda. 2000. Fish Gelatin. http://www.croda.co.uk/pharma/
nutritional.html.
Eastoe, J.E. 1967. Treatise on Collagen. Di dalam Ward,
A.G and A. Courts (Ed.). The Science and Technology of Gelatin. Academic Press, New York.
Eastoe, J.E and A.A. Leach. 1977. The Chemical
Examination of Gelatin. Di dalam Ward, A.G dan A. Courts (ed.). The Science and Technology of Gelatin. Academic Press, New York.
Edi. W.C.K. 1998. Pengaruh konsentrasi asam asetat
(CH3COOH) dan lama perendaman kulit ikan cucut
botol (squalus acanthias) pada pembuatan gelatin. Skripsi. Fakultas Perikanan dan Ilmu Kelautan, IPB, Bogor.
Glicksman, M. 1969. Gum Technology in The Food
Industry. Academic Press, New York.
Grossman, S. and M. Bergman. 1991. Process for The
Production of Gelatin from Fish Skins. European Patent Application 043266 A1.
Kreuzer, R. and R. Ahmed. 1978. Shark Utilization and
Marketing. Food and Agriculture Organization of The United Nations, Rome.
Pelu, H., S. Harwati, E. Chasanah. 1998. Ekstraksi Gelatin
dari Kulit Ikan Tuna melalui Proses Asam. Jurnal Penelitian Perikanan Indonesia Vol. IV (2) : 66-74. BPTP, Jakarta
.
Poppe, J. 1992. Gelatin. Di dalam A. Imeson (ed.).
Thickening and Gelling Agents for Food. Blakcie Academic and Professional, London.
Setyorini, D. 1994. Kajian Proses Demineralisasi dan
Liming dalam Ekstraksi Gelatin dari Kolagen Tulang Sapi. Skripsi. IPB, Bogor.
Shelby,J.W. 1955. Brit.Fd.Mfg.Inds.Res.Ass. Res. Reports,
no.65
Simidu,W. 1961. Nonprotein Nitrogenous Compounds. Di
dalam Borgstrom (Ed.). Fish as Food, Vol. 1. Academic Press, New York.
SNI. 063735. 1995. Mutu dan Cara Uji Gelatin. Dewan
Standarisasi Mutu Pangan., Jakarta
Stainsby, G. 1977. The Gelatin and The Sol-Gel
Transformation. Di dalam Ward, A.G dan A.G Courts (Ed.). The Science and Technology of Gelatin. Academic Press, New York
Surono, N. Djazuli, D. Budiyanto, Widarto, Ratnawati, Aji U.S., Suyini A.M., Sugiran. 1994. Penerapan
Paket Teknologi Pengolahan Gelatin dari Kulit Cucut. Laporan BBPMHP, Jakarta.
Tourtellote, P. 1980. Gelatin. Di dalam Encyclopedia of
Science and Technology. McGraw Hill Book Company, New York.
Wainewright, F.W. 1977. Physical Test for Gelatin and
Gelatin Products. Di dalam Ward, A.G. dan A.G. Courts (Ed.). The Science and Technology of Gelatin. Academic Press, New York.