TINJAUAN PUSTAKA
Penyakit Infeksi Koi Herpesvirus (KHV)
Ikan mas (Cyprinus carpio) adalah ikan yang dibudidayakan secara luas sebagai bahan makanan. Sebanyak 1.5 juta metrik ton diproduksi terutama di Asia maupun Eropa (www.fao.org). Budidaya ikan mas memberikan sumbangan protein untuk penduduk yang berdiam di Asia, Eropa dan Timur Tengah (Aoki et al. 2007).
Koi herpesvirus diidentifikasi pertama kali tahun 1998 yang menyebabkan kematian massal pada ikan mas budidaya di Israel (Gilad et al. 2002) dan Amerika Serikat (Gray et al. 2002). Carp nephritis and gill necrosis virus (CNGV) adalah nama awal virus yang berasal dari virus DNA yang morfologinya mirip dengan anggota kelompok Herpesviridae yang nama lainnya adalah koi herpesvirus dan Cyprinid herpesvirus (Dishon et al. 2005). Nama lain dari virus KHV adalah Cyprinid Herpesvirus 3 atau CyHV-3 (Aoki et al. 2007). Virus ini masuk ke Indonesia pada tahun 2002 melalui perdagangan ikan koi (Sunarto et al. 2004).
Dari percobaan kohabitasi antara ikan sehat dan ikan terinfeksi KHV yang dilakukan oleh Hutoran et al. (2005) diperoleh hasil bahwa ikan yang sakit mengalami ganggunan berupa gerakan yang tidak terkoordinasi dan berenang tidak beraturan yang merupakan tanda-tanda adanya gangguan saraf (neurological disorder). Gangguan ini diperjelas dengan berkurangnya frekuensi gerakan ekor dan kehilangan keseimbangan pada beberapa ikan. Penyebaran penyakit ini melalui air dan bersifat sangat menular.
Menilik dari nama gejala penyakit yang ditimbulkan, virus ini memang menginfeksi terutama pada bagian insang dan ginjal ikan. Dari kajian histopatologi pada insang, tampak jelas bahwa virus ini mengakibatkan inflamasi pada renal tubul ginjal dan mengakibatkan sel-sel yang terinfeksi mengalami pembentukan badan inklusi pada inti selnya. Kajian histopatologi insang ikan yang sakit menunjukkan bahwa terdapat sel-sel inflamasi di insang dan epitel insang mengalami hiperplasia. Kajian dengan menggunakan indirect immunofluorescen microscopy terhadap insang, ginjal, otak dan hati menunjukkan bahwa virus KHV terakumulasi pada insang dan ginjal (Pikarsky et al. 2005).
Keberadaan virus pada ikan dapat dideteksi secara cepat dengan menggunakan metode PCR ( Gray et al. 2002; Gilad et al. 2002) dan menggunakan metode LAMP (loop- mediated isothermal amplification)(Soliman & El-Matbouli 2005).
Metode LAMP tidak memerlukan mesin PCR dalam mengamplifikasi DNA, akan tetapi memerlukan Bst DNA polymerase, dua primer inner, dua primer outer dan dua primer loop untuk mengamplifikasi DNA. Reaksi dilakukan pada suhu 65 oC selama 60 menit. Dari 50 ekor ikan sampel yang diperiksa dengan PCR, 37 ekor dinyatakan positif KHV sedang 13 ekor negatif. Melalui metode LAMP semua sampel dinyatakan positif.
Virus KHV (Koi Herpesvirus)
Nama herpes berasal dari bahasa Yunani yaitu herpein yang berarti kronis / laten / infeksi yang selalu terjadi. Sebanyak 100 macam herpesvirus telah diisolasi. Virus ini memiliki ukuran DNA genom yang besar mencapai 235 kbp dan tersusun dari 35 polipeptida. Secara umum kelompok herpesvirus ini berukuran 180-200 nm, memiliki amplop yang tersusun dari glikoprotein. Pada bagian antara amplop dan kapsid terdapat tegument yang tersusun dari protein. Kapsid berbentuk ikosahedral dengan diameter 95-105 nm. Pada bagian pusat terdapat DNA yang dikelilingi oleh nukleokapsid. Bentuk DNA genom kelompok herpesvirus adalah berutas ganda yang berukuran 130-230 kbp (www.herpes.org).
Struktur virus herpes dapat dilihat pada gambar berikut ini:
Gambar 1. Penampang melintang kelompok herpesvirus (pathmicro.med.sc.edu/virol/herpes)
Koi herpesvirus merupakan virus DNA utas ganda yang memiliki 31 polipeptida dan delapan protein glikosilat dimana 12 polipeptidanya memiliki berat molekul yang sama dengan CHV (cyprinid herpesvirus) dan 10 polipeptidanya sama dengan CCV
(channel catfish virus). KHV memiliki kapsid simetri ikosahedral dengan diameter 100-110 nm, sedangkan virion matang memiliki amplop yang longgar sehingga ukuran diameternya menjadi 170-230 nm. Selain itu juga terdapat benang-benang penyangga seperti struktur tegument pada permukaan inti yang mirip dengan kelompok Herpesvirus (Pokorova et al. 2005).
Hutoran et al. (2005) melaporkan bahwa virus yang diisolasi dari ikan mas yang mengalami kematian massal di Israel memiliki ukuran DNA genom besar yaitu 277 kbp, lebih besar dari ukuran DNA genom kelompok Herpesviridae. Penemuan yang lain adalah hanya sebagian kecil fragmen yaitu 16-45 bp yang mirip dengan beberapa DNA genom virus yang lain. Karakter koi herpesvirus yang dilaporakan dari penelitian Hutoran adalah:
1. Virus sangat menular 2. Transmisi melalui air
3. Terinduksi menjadi penyakit apabila temperatur tertekan sehingga berada pada level 18-24 oC, baik pada skala penelitian di laboratorium (indoor) maupun di kolam (outdoor)
4. Memiliki inang yang terbatas yaitu ikan mas dan koi
5. Tidak dapat dipropagasi pada epitelioma pappilosum cell (EPC), tetapi dapat dipropagasi pada koi fin cell (KFC)
6. Morfologi dan diameter konsisten sesuai dengan herpesvirus meskipun kadang-kadang pada bagian inti virus (core) berisi massa non-simetri berukuran kecil
7. Analisis terhadap sekuen fragmen DNA tidak menunjukkan adanya kesamaan dengan genom virus yang sudah diketahui
8. Virus memiliki molekul DNA utas ganda yang sangat besar yaitu 277 kbp, lebih besar dibanding dengan genom herpesvirus yang sudah ada.
Penyebaran KHV sejak awal ditemukan dan penyebarannya di empat benua di dunia seperti dilaporkan oleh Crane et al. (2004) dapat dilihat pada tabel berikut.
Tabel 1. Penyebaran virus KHV di empat benua di dunia
Sumber: Crane et al. (2004)
Adapun gambar virus KHV yang diambil dari koi fin cell dan diamati dengan mikroskop elektron ditunjukkan oleh Gambar 2.
Gambar 2. Koi herpesvirus yang diambil dari koi fin cell, diamati dengan
mikroskop electron yang memperlihatkan adanya kapsid berbentuk simetri ikosahedral (tanda panah pada gambar A) dan beramplop (tanda panah pada gambar B), diwarnai dengan pewarnaan negative phosphotungstat 2 % (Hutoran et al. 2005)
Crane et al. (2004) melaporkan bahwa virus KHV memiliki sensitifitas terhadap kondisi fisika-kimia. Namun penelitian berikutnya secara detil masih perlu dilakukan untuk mengungkap kondisi fisika-kimia yang berpengaruh terhadap sensitifitas virus.
Tabel 2. Sensitivitas KHV terhadap kondisi fisika dan kimia
Sensitifitas/Kerentanan Terhadap Kondisi Fisika-Kimia
Temperatur Infektifitas virus hilang setelah berada pada suhu 35 oC selama dua hari atau pada suhu 60 oC selama 30 menit
pH Infektifitas hilang pada pH <3 atau pH>11
Bahan kimia Sensitif terhadap kloroform (diasumsikan sensitive juga terhadap bahan pelarut lemak yang lain) Desinfektan Desinfektan yang dianjurkan merujuk pada
ketetapan Office International des Epizooties, OIE (2003), perlu diteliti lebijh lanjut
Kelangsungan hidup Virus dapat bertahan hidup di air selama 20 jam dan lebih lama pada kolam dengan kondisi buruk, ada yang menyebutkan juga bahwa virus hanya mampu bertahan paling lama empat jam.
Sumber: Crane et al. (2004)
KHV merupakan virus yang baru dikenal keberadaannya ketika menyebabkan kematian massal pada budidaya ikan mas dan Koi di Israel tahun 1998. Sebelum disekuensing, KHV masih diberi nama CNGV (carp nephritis and gill necrosis virus) (Dishon et al. 2005) dan masih diduga merupakan anggota family Herpesviridae karena kemiripannya dengan family Herpesviridae yaitu berupa DNA berutas ganda yang dibungkus oleh kapsid ikosahedral , lapisan protein tegument dan amplop virus yang tersusun oleh glikoprotein. Berdasarkan data yang ada di GeneBank, dari seluruh KHV yang ada sekarang baru terdapat tiga genom virus yang sudah disekuensing secara lengkap (genom). Tiga genom KHV tersebut berasal dari Jepang, Israel dan Amerika Serikat (Aoki et al. 2007). Genom KHV memiliki ukuran sekitar 295 kbp dengan perincian sebesar 295.271 bp untuk KHV dari Jepang, 295.146 bp untuk KHV dari Amerika Serikat dan 295.138 bp untuk KHV yang berasal dari Israel. Dari ukuran tersebut tampak ada perbedaan jumlah basa nitrogen dan bervariasi untuk masing-masing strain/serotype virus dimana KHV dari Jepang memiliki ukuran genom yang paling besar diikuti Amerika Serikat dan Israel.
Namun demikian KHV masih meragukan apabila digolongkan ke dalam family Herpesviridae karena memiliki ukuran molekul yang cukup besar yang waktu itu
diduga sebesar 277 kb ketika diketahui pertama kali, lebih besar dari ukuran molekul anggota family Herpesviridae yang sudah ada yaitu 125-245 kb. Di samping itu kegagalan dalam membuktikan adanya hubungan kekerabatan (secara genetik) antara KHV dengan family Herpesviridae juga menyebabkan keraguan uuntuk memasukkan KHV ke dalam family ini. Setelah disekuensing oleh Aoki et al. (2007) baru dapat dipastikan bahwa KHV memang bagian dari family Herpesviridae. KHV memiliki hubungan erat dengan Cyprinid Herpesvirus 1 dan 2 (CyHV-1 dan CyHV-2) yang menyebabkan penyakit carp pox dan hematopoietic necrosis pada ikan mas koki (gold fish). Selain itu KHV juga memiliki kekerabatan dengan Ictalurid herpesviridae (IcHV-1) dan ranid HV-1 (penyebab tumor pada katak). Selanjutnya KHV telah diusulkan secara formal ke dalam anggota Alloherpesviridae dengan nama spesies Cyprinid Herpesvirus 3 atau disingkat menjadi CyHV-3 (Aoki et al. 2007).
Vaksin DNA pada Ikan
Ikan adalah organisme yang mudah terifeksi penyakit yang diakibatkan oleh parasit, bakteri, cendawan dan virus apabila dibudidayakan dalam sistem terkontrol. Penanggulangan penyakit dengan menggunakan bahan kimia termasuk antibiotik memberikan dampak yang tidak baik bagi lingkungan maupun manusia yang mengonsumsinya. Penyakit yang disebabkan oleh virus relatif lebih ditangani karena tidak ada treatmen komersial maupun kemoterapetan yang ekonomis yang bermanfaat dalam penanggulangan penyakit infeksi KHV. Oleh karena itu langkah-langkah yang perlu dilakukan adalah langkah-langkah yang bersifat profilaksis misalnya vaksinasi dan diagnosis penyakit dalam rangka pencegahan terjadinya wabah penyakit (Leong et al. dalam www.nps.ars.usda.gov).
Vaksinasi mampu meningkatkan produktifitas ikan salmon secara signifikan di Norwegia. Produksi ikan salmon pada tahun 1987 sebesar 65,000 metrik ton dan meningkat menjadi 700,000 metrik ton pada tahun 2007. Penggunaan vaksin juga mereduksi penggunaan antibiotik dari 48,500 kg menjadi 649 kg (Gravningen & Berntsen 2008).
Vaksin yang pertama kali dikembangkan pada budidaya ikan adalah vaksin terhadap penyakit bakterial pada tahun 1970. Vaksin mulai diintroduksikan ke lingkungan akuakultur pada awal tahun 1980. Adanya vaksin ini ikut meningkatkan secara signifikan dalam pertumbuhan industri budidaya serta penerimaan konsumen terhadap ikan yang dibudidayakan. Hal ini disebabkan karena berkurangnya dampak
terhadap lingkungan serta peningkatan mutu bahan pangan dari ikan karena adanya minimalisasi dalam penggunaan antibotik (Lorenzen & LaPatra 2005).
Vaksin virus untuk ikan jarang dijual secara komersial. Di Amerika Serikat sendiri agak sulit untuk mendapatkan lisensi peredaran karena prosesnya panjang dan biayanya mahal serta efikasi vaksin yang tidak konsisten. Kendala yang lain adalah masalah keamanan vaksin virus yang diatenuasi masih dipertanyakan karena memiliki potensi untuk bangkit kembali dan menginfeksi inang yang divaksinasi (Leong et al. dalam www.nps.ars.usda.gov). Berkembangnya penyediaan vaksin untuk menanggulangi penyakit yang diakibatkan oleh viral haemorrhagic septicaemia virus (VHSV), infectious haematopoietic necrosis virus (IHNV), infectious pancreatic necrosis virus (IPNV) dan infectious salmon anemia virus (ISAV) cukup memberikan perlindungan bagi budidaya ikan salmon. Di sisi lain, penumbuhan virus bakal vaksin di sel kultur ikan memerlukan biaya yang tidak sedikit. Untuk efisiensi biaya budidaya maka vaksin DNA perlu dikembangkan lebih lanjut. Pada level eksperimen vaksin ini dapat melawan virus dengan tingkat paling efisien. Vaksin ini berbasis pada plasmid DNA yang membawa sisipan gen misalnya glikoprotein dan disertai dengan promoter dan terminator/polyA untuk keperluan ekspresi di ikan (Lorenzen & LaPatra 2005).
Hirono (2005) mengelompokkan perkembangan vaksin pada ikan menjadi tiga generasi. Generasi pertama adalah vaksin konvensional yang dibagi menjadi dua kelompok yaitu vaksin yang diinaktivasi/dimatikan (inactivated vaccine) dan vaksin hidup yang dilemahkan (live attenuated vaccine). Vaksin generasi kedua adalah vaksin protein rekombinan (recombinant protein vaccine) dan vaksin generasi ketiga adalah vaksin DNA (DNA vaccine).
Vaksin yang diinaktivasi memiliki keuntungan tidak ada resiko infeksi sedangkan kelemahannya adalah biaya produksi mahal, pada beberapa kasus tidak ada respon kekebalan yang ditimbulkan, serta daya tahan yang ditimbulkan relatif singkat. Vaksin yang dilemahkan memiliki keuntungan yaitu mampu menginduksi tanggap kebal humoral dan seluler serta memiliki daya proteksi dalam waktu relatif lama. Kelemahan vaksin yang dilemahkan adalah memungkinkan terjadinya infeksi. Keuntungan vaksin protein rekombinan adalah biaya produksi tidak mahal serta dapat diproduksi secara massal, sedangkan kelemahannya adalah tidak mampu mengaktivasi kekebalan seluler. Vaksin DNA memiliki keuntungan yaitu tidak menimbulkan resiko infeksi, mudah dikembangkan dan diproduksi, bersifat stabil dan
mampu mengaktivasi sistem kekebalan baik humoral maupun seluler, sedang kelemahannya adalah terbatasnya protein yang bersifat imunogenik.
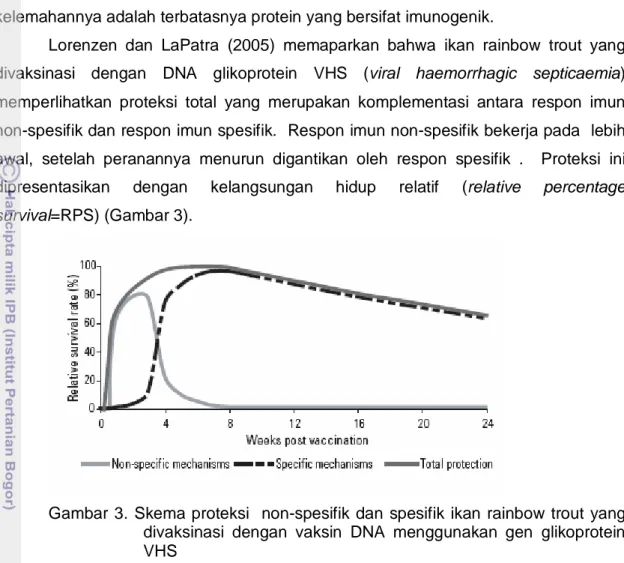
Lorenzen dan LaPatra (2005) memaparkan bahwa ikan rainbow trout yang divaksinasi dengan DNA glikoprotein VHS (viral haemorrhagic septicaemia) memperlihatkan proteksi total yang merupakan komplementasi antara respon imun non-spesifik dan respon imun spesifik. Respon imun non-spesifik bekerja pada lebih awal, setelah peranannya menurun digantikan oleh respon spesifik . Proteksi ini dipresentasikan dengan kelangsungan hidup relatif (relative percentage survival=RPS) (Gambar 3).
Gambar 3. Skema proteksi non-spesifik dan spesifik ikan rainbow trout yang divaksinasi dengan vaksin DNA menggunakan gen glikoprotein VHS
Vaksin DNA Penyandi Glikoprotein
Vaksin DNA untuk menanggulangi IHNV (Infectious Hematopoietic Necrosis Virus) adalah vaksin DNA pertama yang dikembangkan pada ikan salmon. Dari uji gen nucleoprotein (N), phosphoprotein (P), matriks protein (M) , non-virion protein (NV protein dan glikoprotein (G) yang disisipkan ke dalam vaksin plasmid maka glikoprotein (G) saja yang bersifat imunogenik sehingga mampu menginduksi respon imun pada ikan rainbow trout Onchorhyncus mykiss. Proteksi yang sama ditunjukkan juga oleh gen G yang disisipkan pada vaksin plasmid dan divaksinasikan pada ikan salmon Atlantik Salmo salar. Ikan divaksinasi dengan dosis 0.1, 1.0 dan 2.5 µg. Satu bulan kemudian ikan diuji tantang dengan virus IHHNV. Dari percobaan tersebut didapatkann hasil bahwa netralisasi dan pembentukan antibodi yang protekstif dapat diinduksi oleh glikoprotein. Namun demikian produksi antibodi dapat dibuktikan pada percobaan ikan dengan ukuran yang lebih besar ( Lapatra et al. 2001). .
Aplikasi vaksin DNA yang mengandung sisipan gen glikoprotein dapat menginduksi terbentuknya alpha/beta interferon pada ikan rainbow trout yang diuji tantang setelah 30 atau 70 hari setelah vaksinasi. Proteksi yang diberikan cukup lama karena respon imun yang terbentuk bersifat spesifik yaitu terhadap gen G. Vaksin DNA menginduksi perlindungan antiviral yang bersifat non-spesifik pada mulanya yang dimediasi oleh alpha/beta interferon, berikutnya baru terbentuk respon imun yang bersifat spesifik. Vaksin DNA dengan menggunakan gen glikoprotein untuk mencegah penyakit IHHNV pada ikan rainbow tout mampu memberikan proteksi secara signifikan empat hari setelah vaksinasi. Uji tantang setelah 28 hari vaksinasi memberikan rentang yang paling tinggi antara kematian ikan kontrol dan ikan perlakuan, dibandingkan dengan uji tantang pada 1, 7, 14 dan 21 hari (Kim et al. 2000).
Vaksin DNA untuk penyakit infeksi SVCV (spring viremia carp virus) yang mengandung gen glikoprotein lengkap (full length) menghasilkan nilai relative percent survival (RPS) sebesar 48% (primer tidak disebutkan). Perlakuan vaksinasi 10 µg pada penelitian ini dapat menginduksi respon kekebalan berperantara sel (CMI=cell mediated immunity), namun antibody tidak terdeteksi. Penelitian tentang vaksin DNA untuk SVCV pada ikan mas merupakan penelitian yang pertama kali dilakukan (Kanellos et al. 2006).
Vaksin DNA untuk penyakit SVCV asal Amerika Utara pada ikan koi menggunakan gen glikoprotein menghasilkan nilai RPS sebesar 50-88%. Penelitian ini merupakan penelitian pertama yang dilaporkan berhasil dilakukan pada ikan koi. Penelitian ini membuktikan bahwa vaksin DNA untuk penyakit SVCV (pSGnc) dapat menginduksi terbentuknya proteksi yang bersifat spesifik. Hasil penelitian tersebut sekaligus memvalidasi potensi pSGnc yang dapat digunanakan dalam pencegahan penyakit SVCV (Emmenegger & Kurath 2008).
Konstruksi Vaksin
Tahap pertama dalam memproduksi vaksin DNA adalah mengidentifikasi dan mengklon antigen protektif yang berasal dari patogen. Plasmid yang menjadi agen dalam vaksinasi diproduksi dalam kultur bakteri dan dimurnikan. Vaksin diberikan ke sel yang menjadi mesin untuk memproduksi protein G, sesuai dengan gen yang diklon. Setelah glikoprotein diproduksi maka tubuh akan mengenali adanya protein / antigen asing yang masuk ke dalam tubuh. Setelah dideteksi oleh sistem imun ikan
maka tubuh memberikan reaksi dengan terbentuknya antibodi yang homolog. Skema tentang konstruksi singkat plasmid untuk vaksin dapat dilihat dalam ilustrasi yang diwakili oleh vaksin DNA dari kelompok Rhabdovirus berikut ini (Lorenzen & LaPatra 2005).
Gambar. 4. Skema gambaran partikel Rhabdovirus (a), vaksin plasmid (b) dan protein G virus
Kontruksi plasmid dilakukan dengan menyisipkan gen ke dalam plasmid yang mengandung promoter tertentu. Beberapa jenis promoter yang sudah diisolasi dan sudah dicoba pada beberapa spesies ikan oleh beberapa peneliti adalah promoter cytomegalovirus (CMV) dari virus manusia, elongation factor-1α (EF-1α) dari ikan medaka, β-actin dari ikan medaka dan myosin light chain-2 (Mylz-2) dari ikan zebra (Alimuddin 2003). Berdasarkan penelitian pada ikan zebra, promoter β-actin dan Mylz-2 menunjukan aktivitas lebih kuat dibandingkan EF-1α. Sedangkan CMV menunjukan aktivitas lebih rendah. Hal ini dikarenakan promoter CMV berasal dari virus manusia dimana ada kemungkinan bahwa tidak semua elemen cis-acting-nya dikenali oleh faktor trans-acting dari ikan zebra. Sedangkan promoter lainnya yang berasal dari ikan menunjukan aktivitas yang tinggi. Promoter β-actin merupakan
promoter yang bersifat house-keeping yaitu akan selalu aktif dalam siklus hidupnya. Selain bersifat house-keeping, β-actin juga mempunyai sifat ubiquitous (Hacket 1993), dimana promoter ini akan aktif dimana-mana dan constitutive (Volckaert et al. 1994) yang berarti bahwa promoter ini bisa aktif tanpa diberikan rangsangan dari luar seperti suhu dan hormon.
Promoter β-actin dari ikan medaka dilaporkan dapat aktif pada spesies yang sama, sekerabat atau berbeda jenis dengan asal promoter, seperti pada ikan rainbow trout (Yoshizaki 2001), ikan zebra (Alimuddin et al. 2005), ikan nila (Kobayashi et al. 2007), ikan lele (Ath-thar 2007), dan ikan mas (Purwanti 2007). Penggunaan promoter β-actin pada konstruksi vaksin DNA KHV memiliki peluang besar untuk mengaktivasi gen glikoprotein pada ikan mas.
Metode transfer vaksin DNA adalah hal yang penting ketika dikaitkan dengan aplikasi di lapangan (Leong et al. dalam www.nps.ars.usda.gov). Transfer vaksin pada mamalia menggunakan strategi injeksi intramuscular (IM) dengan gene-gun. Teknik ini sebenarnya efektif dalam menginduksi terbentuknya respon imun pada ikan, akan tetapi teknologi ini terlalu mahal apabila diaplikasikan pada budidaya ikan. Injeksi intramuscular (IM) sederhana plasmid DNA yang telah dimurnikan dalam buffer netral lebih efisien diterapkan di ikan daripada di hewan tipe yang lain (Lorenzen & LaPatra 2005). Meskipun aplikasi melalui injeksi IM merupakan metode yang dapat dipertimbangkan dalam vaksinasi, akan tetapi pengembangan aplikasi dengan metode yang lain perlu terus dikembangkan misalnya melalui perendaman atau melalui pencampuran dengan pakan (edible vaccine) dengan mempertimbangkan keamanan bagi lingkungan (Leong et al. dalam www.nps.ars.usda.gov.)
Kajian yang dilakukan terhadap distribusi dan ekspresi vaksin DNA terhadap lymphocystis disease virus (LCDV) pada ikan sebelah menunjukkan hasil bahwa plasmid yang mengandung vaksin terdistribusi pada otot bekas penyuntikan, otot yang berseberangan dengan lokasi penyuntikan, usus, insang, limpa, ginjal depan, hati dan gonad setelah vaksinasi selama tujuh hari. Hasil tersebut diperoleh melalui kajian PCR maupun RT-PCR. Konstruksi vaksin tersebut membawa gen gfp (gene fluorescent protein) dimana fluoresensi dapat diamati pada otot bekas penyuntikan, otot yang berseberangan dengan bekas penyuntikan, usus, insang, limpa, ginjal depan dan hati pada jam ke-36 setelah vaksinasi. Pada hari ke-60 fluoresensi menjadi lebih lemah, namun demikian tetap terdeteksi 90 hari setelah vaksinasi.
Terdistribusinya vaksin DNA pada beberapa organ yang lain dapat memproduksi antigen yang dapat menginduksi kekebalan spesifik ikan (Zheng et al. 2006).
Respons Imun pada Ikan
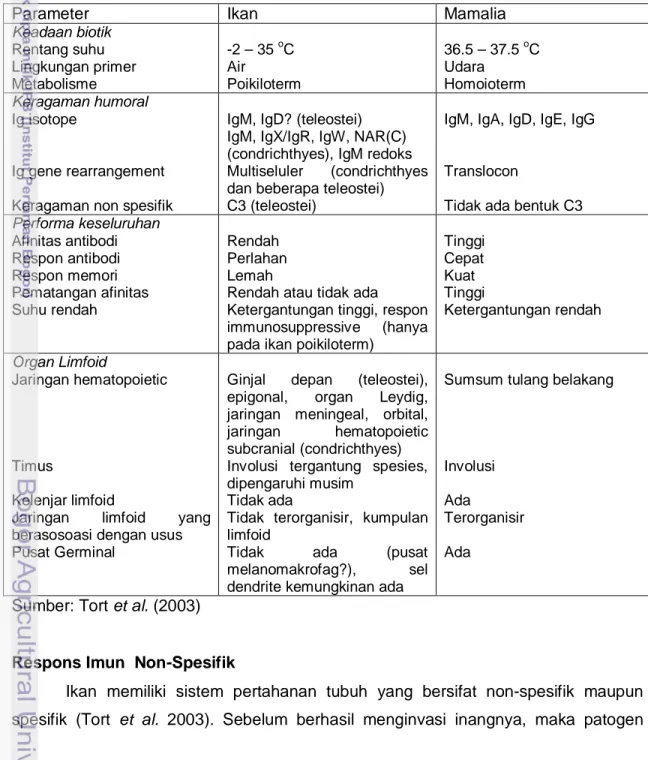
Ikan memiliki respon imun humoral maupun seluler sebagaimana vertebrata yang lain. Ikan dan mamalia memiliki kesamaan dan perbedaan imunitas (Tabel 3).
Tabel 3. Perbedaan antara imunitas ikan dan mamalia
Parameter Ikan Mamalia
Keadaan biotik Rentang suhu Lingkungan primer Metabolisme -2 – 35 oC Air Poikiloterm 36.5 – 37.5 oC Udara Homoioterm Keragaman humoral Ig isotope Ig gene rearrangement Keragaman non spesifik
IgM, IgD? (teleostei) IgM, IgX/IgR, IgW, NAR(C) (condrichthyes), IgM redoks Multiseluler (condrichthyes dan beberapa teleostei) C3 (teleostei)
IgM, IgA, IgD, IgE, IgG
Translocon
Tidak ada bentuk C3 Performa keseluruhan Afinitas antibodi Respon antibodi Respon memori Pematangan afinitas Suhu rendah Rendah Perlahan Lemah
Rendah atau tidak ada Ketergantungan tinggi, respon immunosuppressive (hanya pada ikan poikiloterm)
Tinggi Cepat Kuat Tinggi Ketergantungan rendah Organ Limfoid Jaringan hematopoietic Timus Kelenjar limfoid
Jaringan limfoid yang berasosoasi dengan usus Pusat Germinal
Ginjal depan (teleostei), epigonal, organ Leydig, jaringan meningeal, orbital, jaringan hematopoietic subcranial (condrichthyes) Involusi tergantung spesies, dipengaruhi musim
Tidak ada
Tidak terorganisir, kumpulan limfoid
Tidak ada (pusat melanomakrofag?), sel dendrite kemungkinan ada
Sumsum tulang belakang
Involusi Ada
Terorganisir Ada
Sumber: Tort et al. (2003)
Respons Imun Non-Spesifik
Ikan memiliki sistem pertahanan tubuh yang bersifat non-spesifik maupun spesifik (Tort et al. 2003). Sebelum berhasil menginvasi inangnya, maka patogen
harus berhadapan terlebih dahulu dengan barier pertahanan tubuh yang bersifat fisik dan kimiawi. Patogen harus menembus barikade lendir/mucus yang ada di bagian tubuh paling luar. Lendir ini memiliki kemampuan untuk menggumpalkan antigen secara kimiawi. Setelah itu patogen harus mampu menerobos kulit maupun melewati sisik terlebih dahulu untuk ikan yang bersisik. Setelah bagian ini lolos maka pathogen harus berhadapan dengan sistem pertahanan non-spesifik lainnya dalam tubuh (Tort et al. 2003).
Sistem pertahanan yang bersifat non-spesifik terdiri atas pertahanan seluler dan humoral. Pertahanan non spesifik seluler melibatkan makrofag, granulosit, non-specific cytotoxic cells (NCC).dan cell-line. Makrofag dan granulosit merupakan sel fagositik yang bersifat motil yaitu dapat bergerak ke seluruh bagian-bagian tubuh. Makrofag dan granulosit dapat ditemukan atau diisolasi dari darah, organ limfoid yaitu ginjal depan dan rongga peritoneal (peritoneal cavity) Granulosit terdiri atas neutrofil dan eosinofil, sedangkan basofil jarang ditemukan. Non-specific cytotoxic cells (NCC) pada ikan identik dengan natural killer (NK) cells pada mamalia. Sel ini bertugas untuk melisis sel kanker pada mamalia, sedangkan di ikan berfungsi untuk menghadapi parasit. Sel ini dapat ditemukan di darah, jaringan limfoid, usus dan ginjal depan. Cell line leukosit ini jarang ditemukan. Cell line ini berperanan dalam melakukan fagositosis. Pertahanan non spesifik humoral diperankan oleh lisozim, komplemen, interferon, protein C-reaktif, transferin dan lektin (Iwama & Nakanishi 1996).
Lisozim dapat ditemukan di lendir/mucus, serum dan telur. Zat ini berfungsi untuk membantu mendegradasi lapisan peptidoglikan pada dinding sel bakteri baik gram positif maupun gram negatif. Lisozim juga mendorong aktifitas fagositosis yaitu sebagai opsonin atau secara langsung mengaktifkan leukosit polimorfonuklear (neutrofil) dan makrofag. Neutrofil juga berisi sebagian besar myeloperoksidase yang terlibat dalam aktifitas bakterisidal (Mohanty et al. 2007). Lisozim merupakan salah satu respon alamiah (innate) yang dapat terinduksi dengan cepat (Tort et al. 2003).
Komplemen adalah sebutan yang diberikan untuk rangkaian 20 protein yang bersama dengan pembentuk bekuan darah, fibrinolisin dan pembentukan kinin, membentuk salah satu sistem-sistem pemacu enzim yang ditemukan dalam plasma. Sistem-sistem ini secara karakteristik menghasilkan suatu reaksi cepat, berkekuatan tinggi terhadap suatu fenomena berjenjang di mana hasil satu reaksi akan menjadi pemecah substansi berikutnya secara enzimatik (Roitt 2003). Komplemen pada
mamalia berbeda dengan ikan. Mamalia hanya punya satu isoform molekul C3 yang dikode oleh satu loci, sementara ikan mengekspresikan beberapa isoform C3 aktif. Ikan trout (Onchoryncus mykiss) dan medaka (Oryzias latipes) mengekspresikan tiga isoform C3, ikan seabrem (Sparus aurata) dan mas (Cyprinus carpio) mengekspresikan lima isoform C3 serta ikan zebra (Danio rerio) memiliki tiga loci yang mengkode tiga isoform C3 (Tort et al. 2003).
Interferon adalah protein atau glikoprotein yang dapat menghambat replikasi virus. Pada mamalia terdapat tiga tipe interferon yaitu interferon α, β, dan Ә. Interferon α dan β terdapat pada ikan bertulang sejati dan tidak terdapat pada kelompok lainnya. Interferon Ә disekresikan oleh leukosit yang berasal dari ginjal depan ikan. Protein C-reaktif adalah protein pertama yang tampak pada plasma manusia dan hampir semua hewan (termasuk invertebrata dan moluska) ketika terjadi kerusakan jaringan, infeksi atau inflamasi. Protein ini berperanan dalam melakukan presipitasi polisakarida C (CPS=C-polysaccharides) yang terdapat pada dinding sel bakteri (Iwama & Nakanishi 1996). Protein C-reaktif berukuran 118 kDa dengan koefisien sediimentasi 6.5 S dan memperlihatkan mobilitas tipe β pada medan elektroforesis (Ingram 1980). Faktor ini akan meningkat jumlahnya pada fase akut suatu penyakit infeksi mikrobial dan akan mengikat fosforil-kolin dari glikopeptida dinding sel bakteri, cendawan dan parasit (Rijkers 1982).
Transferin adalah glikoprotein pengikat besi (Fe) yang berperanan dalam transport Fe mulai dari absorbsi, penyimpanan, dan pemanfaatannya pada semua vertebrata (Iwama & Nakanishi 1996). Berat molekul transferin tergantung spesies ikan. Berat molekul transferin pada ikan mas 58-70 kDa, sedang pada ikan dogfish 75-80 kDa. Transferin mempunyai aktifitas antimikrobial yang menghambat pemanfaatan metal oleh bakteri, mengangkut Fe dari situs penyerapannya di usus dan perombakan Hb ke berbagai lokasi penyimpanan (Ingram 1980).
Lektin adalah perantara respon imun yang penting pada vertebrata tingkat tinggi. Protein ini memiliki kemampuan untuk mengikat karbohidrat yang terlibat dalam perlekatan ke dinding sel. Lektin memblokir perlekatan patogen ke dinding sel sehingga invasi dapat digagalkan. Lektin juga terlibat dalam menginduksi mekanisme respon imun yang lain misalnya mengaktifasi komplemen (Tort et al. 2003). Lektin pernah ditemukan terdapat dalam serum darah ikan salmon yang berperan dalam melakukan opsonisasi terhadap bakteri Aeromonas salmonicida. Lektin
meningkatkan aktifitas bakterisidal dan aktifitas makrofag dalam memfagositosis bakteri A.salmonicida (Ewart et al. 2001).
Respons Imun Spesifik
Sistem pertahanan spesifik dibedakan menjadi dua macam yaitu yang bersifat seluler dan humoral. Sistem pertahanan spesifik seluler diperankan oleh kekebalan berperantara sel (cell mediated immunity/CMI) dalam hal ini limfosit Tc, sedangkan pertahanan spesifik humoral diperankan oleh antibodi (Tort et al. 2003).
Kekebalan berperantara sel pada mamalia diperankan oleh sel Tcytotoxic (CTL=cytotoxic lymphocyte). Sel T ini memiliki molekul CD8 pada permukaannya untuk berinteraksi dengan molekul major histocompatibility complex kelas I (MHC I) pada permukaan sel APC (antigen presenting cell) yang menyajikan antigen (Hirono 2005). Sel Tc ini akan mencari sel-sel yang mengalami kelainan fisiologis untuk dihancurkan. Tujuan pembungihangusan ini adalah untuk menghindari penyebaran penyakit (Kuby 1997).
Roitt (2003) memaparkan bahwa kekebalan berperantara sel (seluler) melibatkan limfosit Tc yang dihasilkan di kelenjar timus yang bekerjasama dengan NK (natural killer= non specific cytitoxic cells/NCC) dalam menghancurkan sel yang mengalami kelainan. Ruang lingkup sel NK ini terbatas sehingga perlu bantuan antibodi untuk mengahancurkan sel yang terinfeksi parasit intraseluler yaitu virus. Antibodi menyelimuti sel yang terinfeksi virus sementara NK yang memiliki reseptor khusus terhadap antibodi berikatan dengan antibodi. Antibodi akan membawa sel NK mendekat ke sel sasaran dengan membentuk suatu jembatan. Sel NK yang diaktifkan oleh kompleks antigen-antibodi mampu membunuh sel terinfeksi melalui mekanisme ekstraseluler. Pembunuhan sel ini bersifat non-spesifik. Pembunuhan sel terinfeksi virus yang bersifat spesifik dilakukan oleh sel Tc. Sel ini berhubungan dengan sel target dengan bantuan molekul major histocompatibility complex (MHC) kelas I. Melalui pengenalan terhadap antigen permukaan ini maka sel-sel sitotoksik datang untuk membuat kontak yang lebih intim dengan sel target. Sel sitotoksik juga melepaskan Ә-interferon yang membantu memperkecil peluang penyebaran virus ke sel-sel yang lainnya yang berdekatan. Sel sitotoksik melakukan pembumihangusan sel target sehingga penyebaran virus dapat dihentikan.
Kekebalan spesifik humoral dilakukan oleh antibodi. Pembentukan antibodi diawali dengan terjadinya interaksi antara antigen dengan makrofag. Interaksi ini
terdeteksi oleh sel Thelper dan sel T ini memberikan sinyal melalui sitokin/interleukin kepada sel B untuk melakukan prolifareasi. Sel B yang telah mengalami proliferasi menghasilkan antibodi yang sesuai dengan antibodi yang menginduksinya (Roitt 2003).
Mamalia memiliki beberapa kelas antibodi/immunoglobulin (Ig yaitu IgA, IgD, IgE IgG dan IgM. Ikan bertulang sejati memiliki kelas Ig yang terbatas yaitu IgM. IgM ini berukuran 800 kD (Tort et al. 2003), dengan koefisien sedimentasi 16 S dan berbentuk monomer, tetramer dan pentamer (Walczak 1985). Semua kelas Ig mengandung karbohidrat yang terikat pada atom C dari rantai H. Dalam proses pengikatan karbohidrat seperti manosa, galaktosa, fukosa pada situs asparagin, serin atau treonin diperlukan enzim N-asetil-glukosamin-asparagin transglikosilase. Ikatan karbohidrat ini diperlukan untuk meningkatkan kelarutan Ig, mencegah degradasi katabolik dan mempermudah sekresi antibodi dari sel pembentuknya. Ig M merupakan makroglobulin dimana kestabilan struktur molekulnya dilakukan oleh rantai J. Klasifikasi Ig tersebut didasarkan atas sifat fisiko-kimia, kandungan karbohidrat dan komposisi asam amino molekul Ig (Rosenshein et al. 1985).
Antibodi berfungsi sebagai adaptor yang secara intrinsik mampu mengaktifkan sel komplemen dan merangsang sel-sel fagosit, serta mengikat mikroba penyerang. Adaptor mempunyai tiga bagian utama, dua bagian berkaitan dengan komplemen dan fagosit (fungsi biologis) dan satu bagian khusus untuk mengikat mikroorganisme (fungsi pengenalan eksternal) (Roitt 2003). Mekanisme kerja antibodi dilakukan melalui netralisasi, presipitasi dan aglutinasi, opsonisasi dan fungsi berperantara komplemen. Netralisasi dilakukan dengan cara memblokir pada bagian reseptor antigen atau bagian yang aktif secara enzimatik. Netralisasi dilakukan dengan interaksi antara antibodi dengan antigen sehingga menghasilkan kompleks antigen-antibodi. Terjadinya kompleks ini memudahkan terjadinya fagositosis. Dalam peranannya sebagai penetral antigen, maka antibodi berfungsi sebagai presipitin yang mengendapkan antigen, agglutinin yang menggumpalkan antigen dan opsonin yang berguna untuk melapisi antigen sehingga mudah difagositosis. Proses terjadinya ikatan antara antibodi dengan antigen mengawali kerjasama antara antibodi dengan komplemen. Komplemen berperan dalam rangkaian reaksi yang berjenjang dengan melibatkan komplemen lain dan menimbulkan reaksi peradangan (Iwama & Nakanishi 1996).