Isolasi Bakteri Endofit Dari Sea Grass Yang Tumbuh Di Kawasan Pantai Pulau Lombok Dan Potensinya Sebagai Sumber Antimokroba
Terhadap Bakteri Patogen
1)Lalu Zulkifli, Dwi Soelistya Diah Jekti, Mahrus, Nur Lestari dan an Dewa Ayu Citra Rasmi Program Studi Pendidikan Biologi FKIP Universitas Mataram
Email: [email protected] ABSTRAK
Telah dilakukan isolasi bakteri endofit dari seagrass jenis Enhalus acoroides (Linneaus f.) Royle, yang tumbuh di perairan pantai Kuta Lombok Tengah. Media yang digunakan adalah 1$ %+, 76$ GDQ 0DF &RQNH\¶ $JDU GHQJDQ PHQJJXQDNDQ EDJLDQ DNDU EDWDQJ GDQ GDXQ sebagai sumber isolat. Dilakukan subkultur berulang hingga diperoleh isolat endofit yang membentuk koloni tunggal.Terhadap koloni tunggal ini dilakukan identifikasi morfologi dan uji biokimia. Selanjutnya dilakukan uji aktivitas antibakteri dengan metode Difusi Agar (Disk diffusion test) dengan teknik sumuran menggunakan lima bakteri uji klinis yaitu :
Escherichia coli, Pseudomonas aeruginosa, Klebsiella pneumonia, Shygella dysentriae, dan
Staphylococcus. aureus. Kategori sensitivitas bakteri uji klinis terhadap ekstrak bakteri endofit mengacu kepada Mukherjee (1989). Identifikasi morfologi, uji biokimia dan uji aktifitas antibakteri dilakukan terhadap 11 isolat dari 28 isolat awal yang diperoleh diperoleh, Hasil menunjukkan bahwa semua isolat bakteri endofit tergolong dalam bentuk batang, 8 diantaranya termasuk Gram Positif. Hasil uji antibakteri menggunakan metode Difusi agar dengan teknik sumuran menunjukkan bahwa hampir semua isolat memiliki aktivitas antibakteri terhadap bakteri uji dengan daya hambat yang bervariasi. Diperoleh satu isolat yang palingkuat efeknya dan paling luas spektrumnya yaitu isolate 1 yang mampu menghambat pertumbuhan 4 jenis bakteri uji (E. coli, P. aeruginosa, K. pneumonia, S. dysentriae, dan S. aureus) hingga sampai pada kategori sensitif (dimeter zona hambat lebih dari 12 mm). Dapat disimpulkan bahwa isolat bakteri endofit yang berasal dari seagrass sukup potensial untuk dikembangkan sebagai salah satu alternatif sumber antibakteri untuk mengatasi penyakit yang disebabkan oleh bakteri pathogen.
Kata Kunci: Antimikroba, bakteri endofit, lamun (sea grass), aktivitas antibakteri. ABSTRACT
Have done the isolation of endophytic bacteria on seagrass kind Enhalus acoroides (Linnaeus f.) Royle, who grew up in the coastal waters of Kuta Lombok. The medium used is NA, BHI, TSA and Mac Conkey 'Agar, using the roots stems and leaves as a source of isolates. Subcultures performed repeatedly to obtain isolates endophytic form colonies tunggal.Terhadap single colony is to identify morphological and biochemical tests. Furthermore, the antibacterial activity test by the method Diffusion Agar (Disk diffusion test) with wells technique uses five clinical trials that bacteria: Escherichia coli, Pseudomonas aeruginosa, Klebsiella pneumonia, Shygella dysentriae, and Staphylococcus. aureus. Categories sensitivity of bacteria clinical trials of endophytic bacteria extract refers to Mukherjee (1989). Identification of morphological, biochemical tests and antibacterial activity test conducted on 11 isolates of 28 isolates obtained initial obtained results showed that all isolates of endophytic bacteria belong in the form of rods, 8 of which include Gram Positive. Antibacterial test results using the diffusion method in order to pitting technique showed that almost all isolates possess antibacterial activity against bacteria inhibition test with varied. Retrieved palingkuat one isolate its effects and the most extensive spectrum that isolate one capable of inhibiting the growth of four kinds of test bacteria (E. coli, P. aeruginosa, K. pneumoniae, S. dysentriae, and S. aureus) to arrive at a sensitive category (dimeter inhibitory zone more than 12 mm). It can be concluded that endophytic bacteria isolates originating from sukup seagrass potential to be developed as an alternative source of antibacterial to treat diseases caused by pathogenic bacteria.
I. Pendahuluan
Dewasa ini resistensi antiobiotik telah menjadi masalah mendasar dalam klinik dan pengobatan. Peningkatan jumlah antibiotic untuk melawan meningkatnya sifat resistensi ini, bakteri patogin telah mampu meresponnya dengan menghasilkan progeninya yang tidak lagi sensitive terhadap antibiotic tertentu. Bahkan terhadap berbagai kelompok patogin, termasuk fungi dan bakteri telah mampu resisten terhadap beberapa antibiotik (multidrug resistance) (Levy, 2002). Hal ini menunjukkan semakin pentingnya penelitian untuk menemukan sumber antibiotik baru yang mampu mengatasi infeksi bakteri maupun jamur dimana sumber antibiotik tersebut dapat berasal dari beraneka ragam sumber daya alam di dunia.
Kecedrungan baru dalam penemuan obat baru menekankan investigasi terhadap ekosistem laut untuk mengeksplorasi berbagai macam senyawa antimikroba, yang dapat menjadi sumber untuk mengatasi berbagai macam penyakit termasuk kanker, AIDS, malaria, dan berbagai macam penyakit yang disebabkan oleh virus, bakteri dan fungi (Nazar et al., 2009). Sebagian besar komponen kimia yang berasal dari tanaman yang digunakan sebagai obat atau bahan obat adalah merupakan metabolit sekunder (Radji, 2005). Menurut Strobel & Daisy (2003), senyawa metabolit sekunder yang dihasilkan dari jaringan tumbuhan memiliki aktivitas biologi yang tinggi.Penggunaan produk herbal sebagai terapi alternatif beberapa
penyakit semakin berkembang luas dan popular. Hal ini disebabkan karena obat bahan alam memiliki efek samping yang rendah dan aman untuk pengobatan jangka panjang (Ebadi, 2007).
Metabolit sekunder termasuk dapat diproduksi oleh mikroorganisme endofit yang dalam habitat aslinya dapat membentuk koloni dalam jaringan tanaman. Mikroorganisme endofit dapat ditemukan pada berbagai jaringan tanaman diantaranya biji, ovula, buah, batang, akar, umbi akardan dauntetapi tidak menyebabkan penyakit
pada tanaman tersebut..
Mikroorganisme endofit telah berhasil diisolasi dari berbagai tanaman.
Pada ekosistem darat maupun yang tersebar di daerah pantai dan laut. Mikroorganisme endofit mempunyai arti ekonomis karena mampu menghasilkan senyawa bioaktif yang sangat potensial untuk dikembangkan menjadi obat. Hal ini karena mikroorganisme merupakan organisme yang mudah ditumbuhkan, memiliki siklus hidup yang pendek daripada tanaman dan dapat menghasilkan senyawa bioaktif dalam jumlah besar. Oleh karena itu, isolasi mikroorganisme endofit yang dapat memproduksi metabolit sekunder dari tanaman inangnya merupakan sebuah peluang besar dimasa mendatang (Radji, 2005).
Tumbuhan laut diketahui menghasilkan sejumlah besar metabolit sekunder diversitasnya sangat tinggi (Blunt et al., 2004).Sea grass (lamun)merupakan tumbuhan berbunga
berkembangbaik pada lingkungan perairan laut dangkal, daerah yang selalu mendapat genangan air laut. Lamun termasuk dalam familii
Hydrocharitaceae and
Potamogetonaceae, dimana tersebar dalam 13 genus dan 58 spesies di permukaan bumi. Berbagai macam obat dan bahan kimia penting telah diisolasi dari sea grass tersebut (Ravikumar et al., 2005).
Indonesia merupakan Negara yang terkenal dengan keanekaragaman hayati, termasuk tumbuhan lamun. Sepanjang perairan pantai Pulau Lombok banyak ditumbuhi berbagai
macam spesies lamun.
Penelitianmengenaipotensiantibakteriba kteri endofitdan pengujian potensi
antibakteri simbion
tersebutbelumpernahdilakukan
daribeberapajenislamun masih kurangdilakukan,khususnyadiPulau Lombok. Berdasarkan hal tersebut, perlu dilakukan penelitian mengenai.potensi antibakteridaribakteri endofit lamun(Seagrass) yang tumbuh di Pulau Lombok. Hal ini dapat dilakukan melalui Isolasibakteri endofit dari berapajenis lamun dan dan uji aktivitas antimikrobanya terhadap bakteri uji klinik. Tujuan dari penelitian ini adalah untuk mengetahui jenis bakteri endofit yang berhasil diisolasi dari sea grass yang tumbuh di perairan pantai pulau Lombok dan menguji potensinya sebagai sumber antibakteri pathogen.
II.Bahan Dan Metode
2.1. Alat dan Bahan Penelitian _
Alat-alat yang digunakan dalam penelitian ini adalah laminar air flow, autoklaf, cawan petri-(perti dish), jarum ose, bunsen, kompor listrik, pengaduk kaca, pinset, inkubator, aluminium foil,
bunsen, gelas ukur, tabung reaksi, erlenmeyer, jangka sarong, inkubator, centrifuge, timbangan analitik, silet,
blue tipe, kaca objek, mikroskop,
vortex, shaker. Bahan-bahan yang digunakan dalam penelitian ini adalah beberapa spesies tumbuhan lamun (seagrass), media Nutrien agar (NA), media nutrient broth (NB), media agar darah (NBA), muller hinton agar (MHA), larutan Natrium Hipoklorit (Na0C1) 4%, aquades steril, kertas suing, spiritus, kapas, biakan bakteri, alkohol 70%, alkohol 96%, NaC1 0,9% steril, bakteri uji klinik Streptococcus mutans, Staphylococcus aureus sp, E.
coli, antibiotik Cyprfloxasin.
2.2. Isolasi Bakteri Endofit dari Seagrass
Sampel lamundiambil dari Perairan Teluk Awang dan di daerah sekitar Pantai Keruak Lombok Timur pada kedalaman 0,5 - 1 meter dengan menggunakan pisau kemudian dimasukkan dalam kantong plastik dan disimpan sementara dalam cool box.
Sampel dibersihkan dengan
menggunakkan air laut steril untuk menghilangkan kotoran, maupun oganisme epifit yang menempel pada permukaannya dan diambil sebanyak ± 1gram sampel lamun bagian akar, stem dan buahnya. Selanjutnya dilakukan pengenceran hingga 105. Kemudian diambil sebanyak 100 µl dari pengenceran setiap pengenceran tersebut yang selanjutnya disebar pada permukaan media NA dengan
menggunakkan spreader dan diinkubasi selama 3 hari pada suhu 30 0C. Selanjutnya dilakukan pengamatan setiap hari untuk melihat adanya koloni yang tumbuh (Radjasa et al., 2003). Disiapkan empat jenis media steril yaitu media Nutrient agar, Trypticase Soy agar, Mac Conkey's agar, dan media Brain heart infusion. Isolat bakteri endofit yang tumbuh ditransfer ke nutrient agar slant tube dan disubkultur secara regular setiap minggu serta disimpan pada suhu 4°C sebelum digunakan (Suryakanti, S et al., 2014 ) 2.3. Uji Antibakteri
Pengkondisian kultur
Kultur isolat bakteri endofit diambil 2 lop/ose dimasukkan pada medium cair 10 ml NB steril lalu di vortex.Diinkubasi selama 24 jam pada suhu 32 °C, digoyang selama 24 jam dalam 150 putaran/jam. Selanjutnya disentrifugasi pada 5000 g selama 30 menit sehingga dihasilkan supernatant. UJi Penghambatan Pertumbuhan bakteri
Uji antibakteri menggunakan metode Difusi agar (Disk diffusion test) dengan teknik sumuran dengan mengacu pada ICMR (2009).
Bakteri patogen yang sudah disegarkan dibuat pengenceran dengan mencampurkan 1 ose suspensi bakteri patogen ke dalam tabung reaksi . yang
telah berisi NaCl 0,9%.
Dihomogenkan menggunakan vortex dan kekeruhannya distandarisasi dengan ketentuan turbiditas Mc Farland 0,5. Kemudian suspensi bakteri yang telah distandarisasi tadi, dioleskan ke media MHA dengan rata.Membuat lubang pada media MHA dengan diameter 6 mm. Kemudian masukkan supernatant ± 50
ul ke dalam setiap lubang media MHA yang telah diinokulasi bakteri patogen
dan Cyprofloxasin sebagai control
positif dan DMSO sebagai control negatif, dilakukan 3 kali ulangan.Diinkubasi selama 2 x 24 jam, diameter daya hambat diukur dan isolat bakteri endofit yang positif menunjukkan daya hambat dikatakan sebagai isolat potensial
2.4. Identifikasi Isolat dan analisis hasil uji aktifitas antimikroba
Pengecatan Gram terhadap isolat akan dilakukan sesuai prosedur (Pratita dan Putra, 2012), Uji biokimia/fisiologi mengacu pada Cappuccino dan Sherman (2001). Data diperoleh melalui pengamatan morfologi, pewarnaan gram. Data hasil uji aktivitas antimikroba bakteri endofit dari seagrass diperoleh melalui pengamatan terhadap ada tidaknya daya hambat dan juga pengukuran zona hambat terhadap pertumbuhan bakteri uji klinik. Data pengamatan visual juga akan direcord dengan kamera.Penentuan potensi aktifitas endofit berdasarkan adanya zona hambat mengacu pada Mukherjee (Tania, 2011).
III. Hasil Dan Pembahasan 3.1. Isolasi Bakteri Endofit Dari Sea Grass
Isolasi mikroba endofit dari seagrass dari perairan pantai Kuta Lombok Tengah telah dilakukan dan diperoleh 20 isolat mikroba. Isolat tersebut diperoleh dari tanaman lamun sebagai mana yang ditunjukkan pada gambar (4.1). Bagian tanaman lamun yang digunakan sebagai sumber adalah akar, batang, dan daun. Media yang digunakan adalah NA, BHI, TSA dan
0DF &RQNH\¶ $JDU 3HQJJXQDDQ berbagai jenis media tersebut dimaksudkan untuk meningkatkan peluang tumbuhnya berbagai jenis mikroba.
Proses isolasi dilakukan dimulai dengan mencuci sampel dengan air mengalir hingga bersih dari kotoran yang menempel. Sampel dipotong setiap bagian daun, batang, bunga, dan akar. Secara terpisah setiap bagian seagrass selanjutnya direndam di dalam larutan natrium hipoklorit 4% selama 5 menit, kemudian direndam dalam etanol 70% selama 1 menit. Semua sampel dibilas dengan air laut steril beberapa kali sampai bau natrium hipoklorit dan etanolnya hilang. Secara terpisah, masing-masing sampel, kecuali bagian batang seagrass, dihaluskan, diambil cairannya dan diencerkan hingga 105.
Setiap pengenceran dikultur dengan metode tuang ke media NA, BHI, TSA, MCA dalam wadah cawan petri dengan pelarut menggunakan air laut. Khusus bagian batang, dilakukan pengirisan di permukaannya untuk menghilangkan mikroba epifit dan diletakkan di atas media tumbuh. Semua kultur diinkubasi pada suhu 300 C selama 24-48 jam. Dilakukan subkultur berulang hingga diperoleh isolat endofit yang membentuk koloni tunggal kemudian diinokulasi di media NA Slant (NAS). 3.2. Identifikasi morfologi dan struktur selendofit
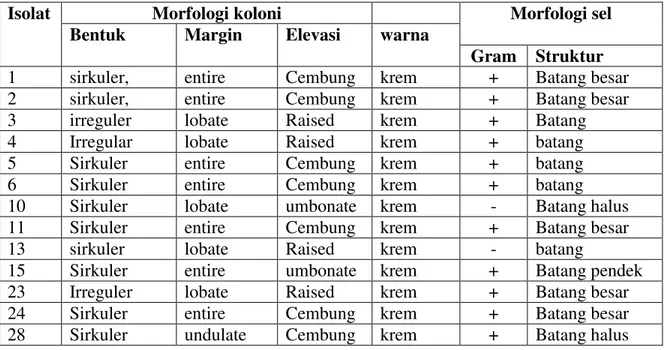
Morfologi koloni semua isolat dapat dilihat pada Table 1, dan hanya ditemukan morfologi sel berbentuk batang.
Table 1. Ciri Morfologi Koloni Dan Struktur Sel Endofit
Isolat Morfologi koloni Morfologi sel
Bentuk Margin Elevasi warna
Gram Struktur
1 sirkuler, entire Cembung krem + Batang besar
2 sirkuler, entire Cembung krem + Batang besar
3 irreguler lobate Raised krem + Batang
4 Irregular lobate Raised krem + batang
5 Sirkuler entire Cembung krem + batang
6 Sirkuler entire Cembung krem + batang
10 Sirkuler lobate umbonate krem - Batang halus
11 Sirkuler entire Cembung krem + Batang besar
13 sirkuler lobate Raised krem - batang
15 Sirkuler entire umbonate krem + Batang pendek
23 Irreguler lobate Raised krem + Batang besar
24 Sirkuler entire Cembung krem + Batang besar
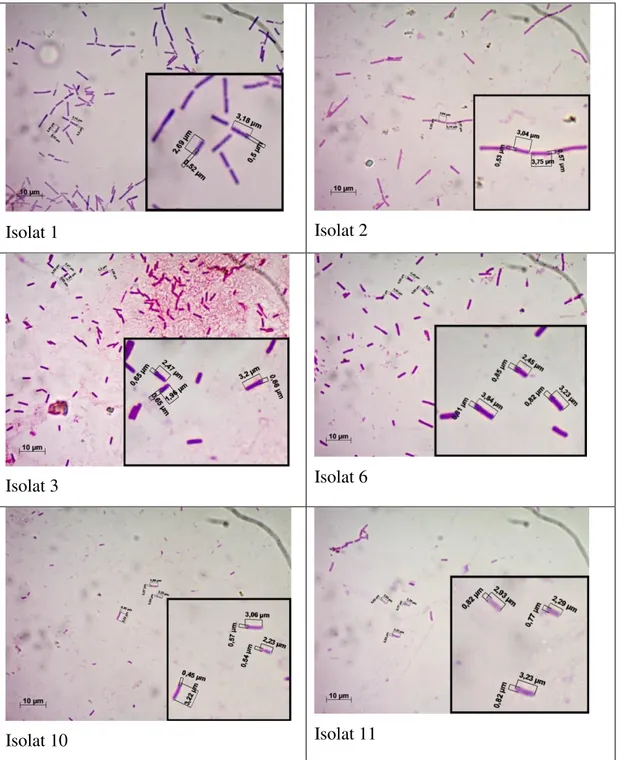
Isolat 1 Isolat 2
Isolat 3 Isolat 6
Isolat 10 Isolat 11
Gambar 1. Morfologi sel Isolat endofit yang diperoleh dari lamundari seagrass spesies
I
solat 13 Isolat 15
Isolat 23 Isolat 24
Isolat 28
Gambar 2. Morfologi sel Isolat endofit yang diperoleh dari seagrass spesies Enhalus
acoroides (Linneaus f.) Royle.
Mikroba endofit hasil isolasi seagrass ditemukan terutama hampir di seluruh bagian tanaman: akar, batang,
dan daun.Menurut Purwanto
dkk.(2014), bakteri endofit dapat masuk ke dalam jaringan tanaman umumnya melalui akar, namun bagian tanaman
yang terpapar udara langsung seperti bunga, batang, daun (melalui stomata) dan kotiledon, juga dapat menjadi jalur masuk bakteri endofit. Bakteri endofit yang telah masuk ke dalam tanaman dapat tumbuh hanya di satu titik tertentu atau menyebar ke seluruh
tanaman. Desrian dkk. (2014) berhasil mengisolasi mikroba endofit dari bagian akar, batang dan daun tanaman Binahong. Bagian tanaman yang digunakan adalah akar (ujung bawah, tengah, atas), batang (ujung, tengah, bawah), daun (bawah, tengah, pucuk), rizoma akar dan rizoma batang. Purwanto dkk.(2014) menemukan isolat endofit tanaman sirih paling banyak di daun dan El-Deeb dkk. (2012) yang meneliti endofit pada tanaman
Plectranthus tenuiflorus menemukan
jumlah mikroba endofit paling banyak juga pada daun.
Mikroba endofit dari seagrass mulai menunjukkan pertumbuhan pada 24 jam setelah inokulasi dan paling
lama 48 jam. Sedikit berbeda dibanding penemuan bakteri endofit dari sirih hijau yang mulai tumbuh pada 48 jam dalam penelitian Purwanto dkk. (2014) dan Bahgat dkk. (2014). Morfologi koloni menunjukkan keragaman diantara isolat tersebut, didominasi oleh sel berbentuk batang dan termasuk gram positif, kecuali isolat 13 termasuk gram negative. Selengkapnya dapat dilihat pada Tabel 1.
3.3. Karakterisasi Biokimia dan fisiologi isolat endofit.
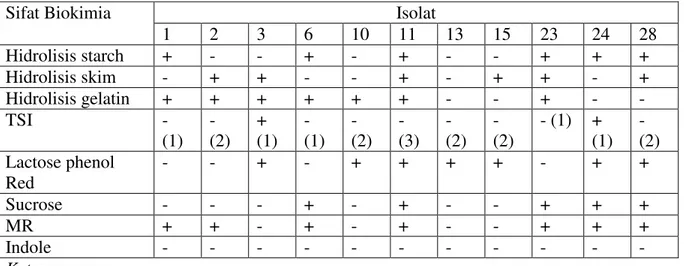
Uji biokimia bakteri endofit meliputi Hidrolisis starch, Hidrolisis skim, Hidrolisis TSI gelatin, Lactose phenol Red, Sucrose, MR dan Indole, sebagai mana yang disajikan pada Tabel 2.
Tabel 2. Aktivitas Enzimatis Ekstra Seluler (Biokimia) Bakteri Endofit Lamun
Sifat Biokimia Isolat
1 2 3 6 10 11 13 15 23 24 28 Hidrolisis starch + - - + - + - - + + + Hidrolisis skim - + + - - + - + + - + Hidrolisis gelatin + + + + + + - - + - - TSI - (1) - (2) + (1) - (1) - (2) - (3) - (2) - (2) - (1) + (1) - (2) Lactose phenol Red - - + - + + + + - + + Sucrose - - - + - + - - + + + MR + + - + - + - - + + + Indole - - - - Keterangan:
Tanda negative (-): reaksi negative Tanda positif (+): reaksi positif
(1) bersifat basa; (2) bersifat asam; (3) bersifat basa di permukaan media dan asam di dasar tabung
Sifat biokimia endofit dilakukan dengan melihat aktivitas enzimatis ekstra selulernya pada beberapa substrat yaitu: starch, gelatin, skim, TSI, Kaldu Lactose Phenol Red, Sukrose, Indol, dan Methyl Red. Jika memiliki enzim
amylase maka akan mampu
menghidrolisis amilum (starch), demikian juga gelatin dan skim. TSI adalah media yang mengandung lactose, glukosa, sodium tiosulfat, digunakan untuk menguji sifat sel yang mampu memproduksi H2S dan menggunakan sumber gula lactose dan glukosa saja serta dapat menghasilkan asam jika menjadi kuning dan basa jika
merah dengan indicator phenol red. Uji indol menggunakan media SIM dengan
UHDJHQ NRYDF¶V +DVLO XML DNWLYLWDV
biokimia endofit dapat dilihat pada Table 2. Belum bisa ditentukan jenis isolat endofit karena masih membutuhkan beberapa uji, misalnya: INVIC tidak lengkap, ammonium sulphate broth, selulosa agar, xiloheximate, dan tributirit agar.
Selanjutnya diuji aktivitasnya terhadap pertumbuhan bakteri isolat klinis. Luas zona hambat dibandingkan dengan standar menurut Mukherjee (1989) dalamTania (2011).
Diameter Kategori
> 12 mm Sensitive
” V G PP Intermediate
< 6 mm (= diameter sumuran) Resisten
Produksi antibakteri oleh bakteri
endofit dilakukan dengan
menginokulasi isolat endofit murni pada medium NB dan diinkubasi pada suhu 300 C selama 48 jam.Kultur kemudian disentrifugasi dengan
kecepatan 150 rpm pada suhu kamar selama 48 jam. Sel dipisahkan dengan
sentrifuge kultur dengan kecepatan
5000 rpm selama 15 menit. Supernatan dan pellet kemudian dipisahkan.
1 .Aktivitas isolat 1 pada
bakteri Pseudomonas aeruginosa
2. Aktivitas isolat 1 pada bakteri
3. Aktivitas isolat 1 pada bakteri
Staphylococcus aureus
4 .Aktivitas isolat 1 pada bakteri
Salmonella Thypi
5 .Aktivitas isolat 1(MBt 1) pada bakteri Klebsiella pneumoniae
6. Aktivitas isolat 2 (MBt) pada bakteri
Escherichia coli
Gambar3.Foto Zona hambat oleh extract dari isolat endofit terhadap beberapa bakteri uji klinis.
gambar7. Aktivitas isolat 3 (TB2)
pada bakteri Escherichia coli Gambar 8. Aktivitas isolat 3 pada
gambar 9. Aktivitas isolat 3 pada bakteri Staphylococcus aureus
Gambar 10. Aktivitas isolat 3 pada bakteri Pseudomonas aeruginosa
11. Aktivitas isolat 3 pada bakteri
Staphylococcus aureus
Gambar 12. Aktivitas isolat 4 (TB) pada bakteri Escherichia coli
Gambar 4.. Beberapa foto sampling Zona hambat oleh ekstrak dari isolat endofit terhadap beberapa bakteri uji klinis. (Lanjutan)
Hail uji diperoleh 10 isolat yang memiliki kemampuan menghambat
pertumbuhan bakteri klinis, yang didominasi dari bagian batang dan daun. Purwanto dkk. (2014) berhasil mengisolasi mikroba endofit dari tanaman sirih hijau (Piper betle L.) paling banyak dari bagian daun.
Table 3. Aktivitas Bakteri Endofit Lamun Terhadap Pertumbuhan Bakteri Klinis Bakteri Klinis Diameter Zona Hambat Isolat endofit (mm)
1 2 3 6 10 11 13 23 24 28 Escherichia coli 21 10 11 36 12 14 0 23* 0 0 Katagori S K K S S S R S R R Klebsiella pneumoniae 19 0 0 0 0 0 0 0 0 0 Katagori S R R R R R R R R R Pseudomonas aeruginosa 31 37 0 0 20 40 10 22* 16 33 Katagori S S R R S S I S S S
Staphylococcus aureus 20 23 19 * 17 11 0 0 0 0 Katagori S S S T S I R R R R Salmonella typhy 0 25** 0 0 0 0 0 0 0 0 Katagori R S R R R R R R R R Keterangan:
No.1,2,3,6, dst : nomor isolat
*: ada batas antara koloni endofit dan bakteri klinis **:diameter koloni bakteri endofit
Katagori aktivitas antibakteri menurut Mukherjee (1989) dalam Tania (2011). S: sensitive
I: Intermediate
Hasil uji aktivitas bakteri endofit terhadap pertumbuhan bakteri klinis menunjukkan sifat yang bevariasi, dan pada bakteri klinis yang berbeda yang selengkapnya dapat dilihat pada Table 3. Luas zona hambat dibandingkan dengan standar menurut Mukherjee (1989) dalamTania (2011). Diperoleh 10 isolat yang memiliki aktivitas menghambat pertumbuhan bakteri klinis, namun yang paling potensial adalah isolat 1. Isolat ini mampu menghambat pertumbuhan bakteri klinis (Escherichia coli, Pseudomonas
aeruginosa, Klebsiella pneumonia,
Shygella dysentriae, dan
Staphylococcus. aureus) hingga
katagori sensitive kecuali pada bakteri
Salmonella thypi yang tidak terhambat
pertumbuhannya.. Isolat ini diisolasi dari batang seagrass pada media Mac
&RQNH\µV $JDU Isolat 1 adalah bakteri
berbentuk batang, gram positif, sifat-sifat biokimianya dapat dilihat pada Table 2.
IV. KESIMPULAN
Analisis morfologi dan biokimia menunjukkan bahwa semua bakteri termasuk dalam kelompok Bacillus dan
sebagian besar merupakan kelompok Gram Positif. Hasil uji antibakteri terhadap pertumbuhan bakteri klinis dari isolat yang diperoleh menunjukkan bahwa hampir semua memiliki aktivitas antimikroba menghambat, namun yang paling potensial adalah isolat 1. Isolat ini mampu menghambat pertumbuhan bakteri klinis (Escherichia
coli, Pseudomonas aeruginosa,
Klebsiella pneumonia, Shygella
dysentriae, dan Staphylococcus. aureus)
hingga katagori sensitif.
DAFTAR PUSTAKA
AliM.S,Ravikumar,S.,andBeula.J.M,20 12.Bioactivity of seagrass
against the dengue
fevermosquito Aedesaegypti larvae .Asian Pacific Journal
of Tropical
Biomedicine(2012)1-5.
Azkab, M. H., 1999, Pedoman Inventarisasi Lamun, Oseana, Volume XXIV, Nomor 1, : 1-
16 ISSN 0216-1877 Bahgat, MM, El Bous, MM, Kawashty,
SA, Mohammed E, NA. 2014. Characterization of Endophytic Bacteria Isolatd from the Medicinal Plant
CapparissinaicaVeill. and Analyze its Bioactive Flavonoid. Botany.Indian Journal Of Applied Research Volume : 4 | Issue : 11 | November 2014 | ISSN - 2249-555X
Blunt, J.W., B.R. Copp, M.H.G.
Munro, P.T. Northcote and M.R. Prinsep: Marine natural
products. Nat. Prod. Rep., 21, 1-49 (2004).
Cappuccino, James G., dan Natalie Sherman, 2001, Microbiology : A Laboratory Manual, sixth edition, Benjamin Cummings, San Fransisco.
Desriani, UM Safira P, M Bintang, M Rivai, L Lisdiyanti. 2014. Isolasi danKarakterisasi Bakteri Endofit dari Tanaman Binahong dan Katepeng China.Jurnal Kesehatan Andalas. 2014; 3(2).
http://jurnal.fk.unand.ac.id Ebadi, M. 2007. Pharmacodynamic
Basis of Herbal Medicine. 2nd Ed. CRC Press. Boca Raton.
El-Deeb, B., Fayez, K, Gherbawy, Y. 2013. Isolation and characterization of endophytic bacteria from Plectranthus tenuiflorus medicinal plant in Saudi Arabia desert and their antimicrobial activities. Journal of Plant Interactions, Vol. 8, No. 1, 56- 64,
http://dx.doi.org/10.1080/17 429145.2012.680077
Kiswara, W. 1997. Struktur komunitas padang lamun perairan indonesia. Inventarisasi dan Evaluasi Potensi Laut-Pesisir II, Jakarta: P3O LIPI : 54-61. Levy, S.B., Factors impacting on the
problem of antibiotic resistance,
J. Antimicrob. Chemother.
(2002) 49 (1): 25-30.
Nazar, S. S. Ravi kumar, G. Prakash Wi l l i ams, M. Sy ed Al i and P. Suganthi: Screening of Indian coastal plant extracts for larvicidal acti vity of Cul ex quinquefaciat us. Ind. J. Sci. Technol ., 2, 24-27 (2009). Pratita, MY., Putra, SR., Isolasi Dan
Identifikasi Bakteri Termofilik Dari Sumber Mata Air Panas Di Songgoriti Setelah Dua Hari Inkubasi, Jurnal Teknik Pomits Vol. 1, No. 1, (2012) 1-5. Purwanto, UMS, FH Pasaribu, M
Bintang. 2014. Isolasi Bakteri Endofit dari
Tanaman Sirih Hijau (Piper betle L.) dan Potensinya sebagai Penghasil Senyawa Antibakteri. Current Biochemistry. Volume 1 (1): 51 ± 57.e-ISSN: 2355-7877.Journal Homepage: http://biokimia.ipb.ac.id/Jour nal Email: current.biochemistry@gmail .com
Radji, M. Peran Bioteknologi dan mikroba endofit Dalam pengembangan obat herbal. Ravikumar, S., S. Nazar, A. Nural Shiefa and S. Abideen : Antibacterial activity of traditional therapeutic coastal medicinal plants against some pathogens. J. Environ. Biol., 26, 383-386 (2005).
Ravikumar,S.,ThajuddinN.,SuganthiP., JacobSandVinodkumarT. 2010. Bioactive Potential of seagrass bacteria against Human
bacterial Pathogens.Journal
ofEnvironmental Biology.
387-389.
Tania. 2011. Parameter Analisis Data. www.media unpad.ac.id. Diakses pada tanggal 26 Oktober 2013 Tomascik T, A.J. Mah, A. Nontji and
of the Indonesia Sea. Part One. The Ecology of Indonesian Series Vol. VII. Hong Kong: Periplus Edition (HK) Ltd.
Watermann,B. 1999.Alternative antifoulant techniques present andfuture. Limno Mar: 1-6.