PENETAPAN KADAR ETANOL DAN PROFIL SENYAWA YANG TERDAPAT DALAM HASIL PRODUKSI “CIU” RUMAHAN DUSUN
SENTUL DESA BEKONANG KABUPATEN SUKOHARJO DENGAN METODE KROMATOGRAFI GAS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh: Fajar Dwi Riyanto
NIM: 088114043
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENETAPAN KADAR ETANOL DAN PROFIL SENYAWA YANG TERDAPAT DALAM HASIL PRODUKSI “CIU” RUMAHAN DUSUN
SENTUL DESA BEKONANG KABUPATEN SUKOHARJO DENGAN METODE KROMATOGRAFI GAS
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh: Fajar Dwi Riyanto
NIM: 088114043
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
PENETAPAN KADAR ETANOL DAN PROFIL SENYAWA YANG TERDAPAT DALAM HASIL PRODUKSI “CIU” RUMAHAN DUSUN
SENTUL DESA BEKONANG KABUPATEN SUKOHARJO DENGAN METODE KROMATOGRAFI GAS
Skripsi yang diajukan oleh:
Fajar Dwi Riyanto
NIM : 088114043
telah disetujui oleh
Pembimbing
iii
Pengesahan Skripsi Berjudul
PENETAPAN KADAR ETANOL DAN PROFIL SENYAWA YANG TERDAPAT DALAM HASIL PRODUKSI “CIU” RUMAHAN DUSUN
SENTUL DESA BEKONANG KABUPATEN SUKOHARJO DENGAN METODE KROMATOGRAFI GAS
Oleh :
Fajar Dwi Riyanto
NIM : 088114043
Dipertahankan di hadapan Panitia Penguji Skripsi
Fakultas Farmasi
Universitas Sanata Dharma
pada tanggal: 2 Juli 2013
Mengetahui
Fakultas Farmasi
Universitas Sanata Dharma
Dekan
Ipang Djunarko, M.Sc., Apt
Panitia Penguji Tanda tangan
1. Jeffry Julianus, M.Si. ………..
2. Lucia Wiwid Wijayanti, M.Si. ………..
iv
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah
ini, maka saya bersedia menanggung segala sanksi sesuai peraturan
perundang-undangan yang berlaku.
Yogyakarta, 12 Juli 2013
Penulis,
v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertandatangan dibawah ini, saya mahasiswa Universitas Sanata
Dharma:
Nama : Fajar Dwi Riyanto
No Mahasiswa : 088114043
Demi pengembangan ilmu pengetahuan, saya memberikan kepada perpustakaan
Universitas Sanata Dharma karya ilmiah saya yang berjudul:
PENETAPAN KADAR ETANOL DAN PROFIL SENYAWA YANG TERDAPAT DALAM HASIL PRODUKSI “CIU” RUMAHAN DUSUN SENTUL DESA BEKONANG KABUPATEN SUKOHARJO DENGAN METODE KROMATOGRAFI GAS
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan
kepada perpustakaan Universitas Sanata Dharma hak untuk menyimpan,
mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan
data, mendistribusikan secara terbatas, dan mempublikasikan di Internet atau
media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya
maupun memberikan royalty kepada saya selama tetap mencantumkan nama saya
sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 12 Juli 2013
Yang menyatakan
vi
Karya Sederhana Ini Saya Persembahkan Untuk:
Bapak (Mulyana) dan Ibu (Murwani) Tercinta
Kakak ku (Tatang Ony) yang tersayang
vii
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Kuasa atas segala
limpahan berkat dan kasih-Nya sehingga penelitian dan penyusunan skripsi yang
berjudul “penetapan kadar etanol dan profil senyawa yang terdapat dalam hasil
produksi “ciu” rumahan dusun sentul desa bekonang kabupaten sukoharjo dengan
metode kromatografi gas” dapat diselesaikan dengan baik. Skripsi ini disusun
sebagai salah satu syarat untuk meraih gelar Sarjana Farmasi (S.Farm) di Fakultas
Farmasi, Universitas Sanata Dharma, Yogyakarta.
Dalam pelaksanaan penelitian hingga selesainya penyusunan skripsi ini,
penulis mendapat banyak dukungan dan bantuan dari berbagai pihak. Oleh karena
itu, penulis mengucapkan terima kasih kepada:
1. Bapak Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta.
2. Bapak Jeffry Julianus, M.Si. selaku dosen pembimbing yang dengan sabar
memberikan pengarahan, masukan, kritik dan saran baik selama penelitian
maupun penyusunan skripsi ini.
3. Ibu Lucia Wiwid Wijayanti, M.Si. selaku dosen penguji yang telah
memberikan saran dan kritik yang membangun dalam penyusunan skripsi.
4. Ibu Dra. Maria Margaretha Yetty Tjandrawati M.Si. selaku dosen penguji
yang telah memberikan saran dan kritik yang membangun dalam penyusunan
viii
5. Ibu dr. Fenty, M. Kes., Sp.PK, selaku dosen pembimbing akademik atas
bimbingan dan semangat yang telah diberikan selama ini.
6. Ibu Rini Dwi Astuti, M.Sc, Apt. selaku Kepala Laboratorium Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta.
7. Seluruh Dosen Fakultas Farmasi Universitas Sanata Dharma yang telah
memberikan ilmu yang bermanfaat demi kemajuan mahasiswa dalam bidang
farmasi.
8. Seluruh staff laboratorium kimia Fakultas Farmasi Universitas Sanata
Dharma: Mas Bimo, Mas Bima, yang telah banyak membantu selama
penelitian di laboratorium.
9. Albert, Curut, Wawan, Efa, Widi, Cyntia dan teman-teman lainnya yang selalu
membantu.
10.PKS saya Koh Robby yang selalu mendukung dalam doa dan supportnya.
11.Semua pihak yang tidak dapat disebutkan satu per satu yang telah membantu
penulis dalam mewujudkan skripsi ini.
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan
skripsi ini, sehingga segala kritik dan saran yang membangun sangat penulis
harapkan. Semoga skripsi ini membantu dan bermanfaat bagi pembaca pada
khususnya dan ilmu pengetahuan pada umumnya.
ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ……… i
HALAMAN PERSETUJUAN PEMBIMBING ………. ii
HALAMAN PENGESAHAN ………. iii
PERNYATAAN KEASLIAN KARYA ………. iv
x
A. Jenis dan Rancangan Penelitian ………. 19
B. Variabel ………. 19
1. Variabel bebas ………. 19
2. Variabel tergantung ………. 19
3. Variabel pengacau terkendali ……….. 19
C. Definisi Operasional ………. 20
D. Bahan Penelitian ……… 20
E. Alat Penelitian ……… 20
xi
1. Pemilihan sampel ………. 21
2. Preparasi sampel ………. 21
3. Analisi kualitatif ……….. 21
4. Pembuatan seri baku ……….. 22
B. Optimasi dan Pemilihan Standar Internal ... 24
C. Uji Kualitatif Sampel ………. 26
1. Analisis kualitatif berdasarkan waktu retensi (tR) etanol …… 26
2. Analisis kualitatif menggunakan GC-MS ……… 27
D. Pembuatan Kurva Baku Etanol ……….. 31
E. Preparasi Sampel ………. 32
xii
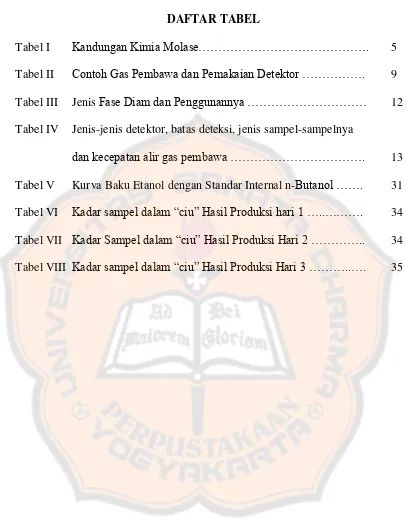
DAFTAR TABEL
Tabel I Kandungan Kimia Molase………. 5
Tabel II Contoh Gas Pembawa dan Pemakaian Detektor ………. 9
Tabel III Jenis Fase Diam dan Penggunannya ……… 12
Tabel IV Jenis-jenis detektor, batas deteksi, jenis sampel-sampelnya
dan kecepatan alir gas pembawa ………. 13
Tabel V Kurva Baku Etanol dengan Standar Internal n-Butanol ……. 31
Tabel VI Kadar sampel dalam “ciu” Hasil Produksi hari 1 …..………. 34
Tabel VII Kadar Sampel dalam “ciu” Hasil Produksi Hari 2 ………….. 34
xiii
DAFTAR GAMBAR
Gambar 1. Gambar Lintasan Embden-Meyerhof-Parnas ………. 7
Gambar 2 Gambar skematis kromatografi gas ……… 9
Gambar 3 Gambar sistem injeksi ………. 10
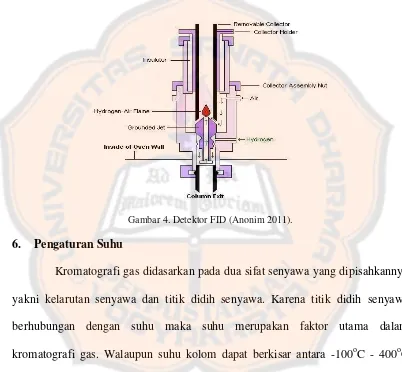
Gambar 4 Detektor FID ……….. 14
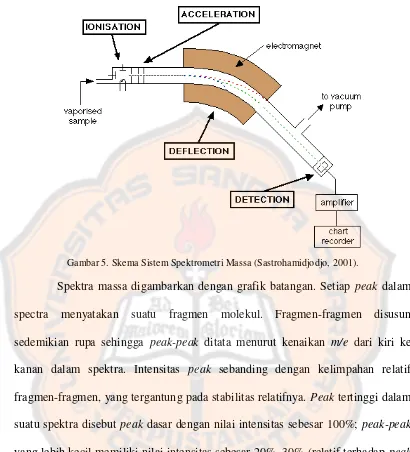
Gambar 5 Skema Sistem Spektrometri Massa……….. 17
Gambar 6 Kromatogram etanol dengan standar internal methanol... 25
Gambar 7 Kromatogram etanol dengan standar internal n-butanol.... 25
Gambar 8 Kromatogram baku etanol (8%v/v) ……… 26
Gambar 9 Kromatogram sampel (2%v/v) ………... 26
Gambar 10 Kromatogram sampel 1 ……….……….. 28
Gambar 11 Spektra Massa Senyawa Pada Waktu Retensi 2.233 min.. 28
Gambar 12 Kromatogram sampel 2 ………..……….. 29
Gambar 13 Spektra Massa Senyawa Pada Waktu Retensi 2.217 min.. 29
Gambar 14 Kromatogram sampel 3 ……….……… 30
Gambar 15 Spektra Massa Senyawa Pada Waktu Retensi 2.083 min.. 30
Gambar 16 Spektra Massa Senyawa Pada Waktu Retensi 2.308 min.. 30
Gambar 17 Kurva hubungan antara kadar etanol (%v/v) vs Rasio AUC etanol/butanol ……… 32
xiv
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis etanol ………. 40
Lampiran 2 Sertifikat analisis N-Butanol ………. 42
Lampiran 3 Kromatogram GC-MS Sampel 1 ………... 44
Lampiran 4 Kromatogram GC-MS Sampel 2 ………... 44
Lampiran 5 Hasil Analisi Spektra Massa Sampel 1 dan 2…………. 45
Lampiran 6 Kondisi Kromatografi Gas-Spektrofotometri Massa .... 46
Lampiran 7 Kromatogram GC-MS Sampel 3 ………... 47
Lampiran 8 Hasil Analisi Spektra Massa Sampel 3 ……….. 48
Lampiran 9 Hasil Analisi Spektra Massa Sampel 3………... 49
Lampiran 10 Hasil Validasi Metode Analisis... 50
Lampiran 11 Perhitungan Kurva Baku ………. 54
Lampiran 12 Kromatogram Baku Etanol ………. 56
Lampiran 13 Kromatogram Sampel ………. 61
Lampiran 14 Kondisi Kromatogram Gas ………. 77
Lampiran 15 Perhitungan Sampel Alkohol ………. 78
xv
INTISARI
Kabupaten Sukoharjo, dusun Bekonang merupakan daerah penghasil etanol yang digunakan untuk tujuan medis. Pembuatannya menggunakan ampas tetes tebu yang disebut molase yang difermentasikan sehingga menghasilkan kadar etanol yang kemudian di destilasi secara sederhana. Selain etanol, fermentasi tetes tebu menghasilkan senyawa lain, sehingga perlu diketahui kadar etanol dan mengetahui senyawa lain yang terdapat dari hasil fermentasi.
Penetapan kadar etanol dan untuk mengetahui kandungan senyawa yang terdapat dalam hasil produksi menggunakan instrumen kromatografi gas dan gas chromatography-mass spectra dengan hasil optimasi yaitu suhu awal 70oC, dengan initial time: 2 menit dan peningkatan suhu sebanyak: 30oC/min, dan temperatur final: 220oC, dengan waktu final: 2 menit, suhu injektor B yang digunakan 200oC; dengan suhu detektor A 250oC, serta range:3. Dan parameter validasi yaitu akurasi: 101.8%, presisi: 1.26, linearitas: r:0.9996, batas kuantifikasi: 6.363, dan batas deteksi: 1.909, SD:0.077. Senyawa n-butanol digunakan sebagai standar internal dalam penetapan kadar etanol.
Hasil penetapan kadar etanol dari sampling sejumlah 14 rumah produksi diketahui yaitu hari 1 29.779%v/v±1.725; hari 2: 29.762%v/v ±2.237; dan hari 3: 30.316%v/v±2.085. di setiap harinya diambil 600,0 ml sampel Berdasarkan data diatas dengan dilakukan uji statistik dengan uji ANOVA satu arah bahwa kadar etanol dari setiap hari produksi dan setiap tempat produksi tidak berbeda bermakna. Senyawa lain hasil produksi diketahui adalah yaitu asam asetat, aseton.
xvi
ABSTARCT
Sukoharjo district, Bekonang producing ethanol used for medical purposes. Raw material is molasses residue, which is in the making fermented to produce ethanol and then in a simple distillation. Besides ethanol, molasses fermentation produce other compounds that need to know the levels of ethanol and other compounds contained content of the fermentation.
Determination of ethanol content and to determine the content of compounds contained in the instruments of production using gas chromatography and gas chromatography-mass spectra. optimization results that the initial temperature of 70°C, initial time: 2 minutes; rate: 30°C/min; final temperature: 220°C; final time: 2 minutes; injector B: 200°C; detector A: 250°C; range: 3. As well as the accuracy parameter validation: 101.8%, precision: 1.26, linearity: r: 0.9996, LOQ: 6.363, and LOD: 1.909, SD: 0077. N-Butanol is used as an internal standard in the determination of levels of ethanol because there is variation in the measurement tool and as a correction factor.
Assay results are known the day 1 29.779%v/v±1.725; day 2: 29.762%v/v ±2.237; and day 3: 30.316%v/v±2.085, with one-way ANOVA test is known that the production of each days did not differ significantly. Other compounds that are known to yield acetic acid, acetone.
1 BAB I PENDAHULUAN
A. Latar Belakang Penelitian
Kabupaten Sukoharjo merupakan salah satu kabupaten di Jawa Tengah,
dan di wilayah kabupaten Sukoharjo terdapat desa yang memiliki sentra produksi
etanol yang dikenal dengan nama Bekonang, dan hasil produksinya yang banyak
dikenal masyarakat dengan nama “Ciu Bekonang”. Mayoritas warga di Desa
Bekonang merupakan pengrajin industri rumah tangga pembuatan etanol dan hal
ini sudah dilakukan oleh warga setempat sejak dahulu kala.
Ciu produksi Bekonang dibuat dari bahan dasar tetes tebu yang
difermentasikan dan mengalami proses destilasi sehingga diperoleh etanol
(Widodo, 2004). Senyawa yang dihasilkan mempunyai kandungan utama etanol,
sedangkan senyawa lain yang dihasilkan berupa asam sitrat dengan kadar rata-rata
6,82% (Widyanti, 2010). Hasil produksi biasanya digunakan untuk etanol medis
sehingga perlu diketahui kadar yang dihasilkan agar diketahui seberapa efektif
hasil fermentasi, serta perlu diketahui senyawa lain yang terdapat dalam hasil
fermentasi agar diketahui keberadaan senyawa yang berbahaya untuk medis.
Penelitian ini bertujuan untuk penetapan kadar Etanol hasil produksi Ciu industri
rumahan di daerah bekonang dan juga ingin mengetahui kandungan senyawa
Kromatografi gas merupakan metode untuk melakukan pengukuran
secara kualitatif dan kuantitatif untuk bahan-bahan yang mudah menguap, serta
stabil pada pemanasan tinggi. Prinsip pemisahan dalam kromatografi gas yaitu
dengan cara partisi dari komponen-komponen senyawanya dengan menggunakan
fase gas sebagai fase gerak, dan fase cair sebagai fase diam. Prinsip penetapan
kadar dengan kromatografi gas adalah sampel diinjeksikan pada instrumen dan
oleh gas yang mempunyai tekanan tertentu sampel dibawa menuju kolom kapiler
untuk dipisahkan berdasarkan komponen penyusun dan diteruskan menuju
detektor. Dari detektor dihasilkan sinyal pembacaan untuk dicatat oleh rekorder
sehingga menghasilkan kromatogram. Kadar senyawa diketahui dengan
menghitung luas area kromatogram. Etanol dapat dianalisis menggunakan
kromatografi gas karena merupakan senyawa volatil yaitu senyawa yang mudah
menguap pada suhu kamar, sehingga memenuhi syarat untuk dapat ditetapkan
kadarnya melalui kromatografi gas (Dean, 1995).
Penelitian penetapan kadar etanol dari Ciu hasil produksi industri
rumahan di daerah sukoharjo menggunakan metode Kromatografi Gas yang telah
dilakukan optimasi dan validasi metode. Hasil optimasi yang didapatkan yaitu
suhu awal 70oC, initial time: 2 menit; rate: 30 oC /min; temperatur final: 220 oC;
waktu final: 2 menit; injektor B :200 oC; detektor A: 250 oC; range :3 (Waskito,
2013). Sedangkan validasi dilakukan untuk memberikan jaminan bahwa metode
analisis dengan sistem kromatografi gas memenuhi parameter-parameter validasi
sehingga dapat memberikan hasil analisis yang valid dengan memenuhi parameter
kuantifikasi: 1.729%v/v, dan batas deteksi: 0.5%v/v, disini SD: 0.077, sehingga
metode telah valid (Rombang, 2013).
1. Perumusan Masalah
Berdasarkan latar belakang permasalahan di atas, timbul permasalahan
sebagai berikut:
a. Apa saja kandungan senyawa yang terdapat pada hasil Ciu produksi industri
rumahan hasil fermentasi tetes tebu di daerah sukoharjo?
b. Berapakah kadar etanol hasil Ciu produksi industri rumahan hasil fermentasi
tetes tebu di daerah sukoharjo?
2. Keaslian Penelitian
Sejauh yang diketahui penulis dan studi pustaka yang telah dilakukan
penulis, penelitian mengenai penetapan kadar dan profil kandungan hasil produksi
industri rumahan di daerah sukoharjo secara kromatografi gas belum dilakukan,
tetapi penulis menggunakan acuan kerja berdasarkan penelitian yang berjudul
Perbandingan Metode Kromatografi Gas dan Berat Jenis Pada Penetapan Kadar
Etanol Dalam Minuman Anggur (Mardoni, 2002).
3. Manfaat penelitian
a. Manfaat metodologis.
Dengan penelitian ini diharapkan dapat memberikan sumbangan
ilmiah mengenai metode kromatografi yang dipilih untuk menetapkan kadar
b. Manfaat praktis.
Dengan penelitian ini diharapkan dapat memberikan informasi
mengenai kadar etanol dalam hasil produksi Ciu dan kandungan yg terdapat
di dalamnya dengan metode Kromatografi Gas.
B. Tujuan Penelitian
Tujuan dilakukan penelitian ini adalah untuk mengetahui :
a. Kandungan dari senyawa yang terdapat pada hasil fermentasi tetes tebu yang
diproduksi di daerah sukoharjo.
b. Mengetahui kadar etanol dari hasil fermentasi tetes tebu yang di produksi di
5 BAB II
PENELAAHAN PUSTAKA A. Tetes Tebu (Molase)
Molase adalah hasil samping yang berasal dari pembuatan gula tebu
(Saccharum officinarum L). Tetes tebu berupa cairan kental dan diperoleh dari
tahap pemisahan kristal gula. (Juwita, 2012).
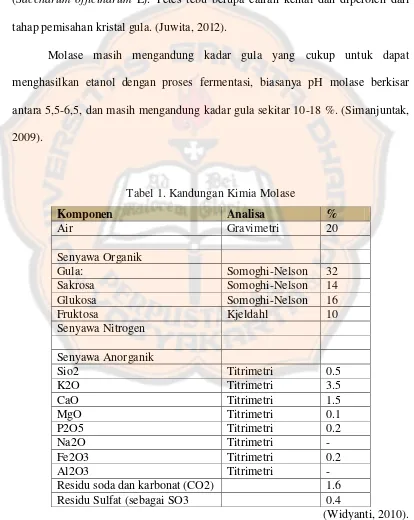
Molase masih mengandung kadar gula yang cukup untuk dapat
menghasilkan etanol dengan proses fermentasi, biasanya pH molase berkisar
antara 5,5-6,5, dan masih mengandung kadar gula sekitar 10-18 %. (Simanjuntak,
2009).
Tabel 1. Kandungan Kimia Molase
Komponen Analisa %
Air Gravimetri 20
Senyawa Organik
Gula: Somoghi-Nelson 32 Sakrosa Somoghi-Nelson 14 Glukosa Somoghi-Nelson 16 Fruktosa Kjeldahl 10 Senyawa Nitrogen Residu Sulfat (sebagai SO3 0.4
B. Ciu Bekonang
Di desa bekonang kabupaten Sukoharjo terdapat pengrajin industri kecil
skala rumah tangga yang menghasilkan Etanol untuk keperluan bahan baku kimia
industri dan juga keperluan pengobatan. Etanol yang dihasilkan berasal dari
fermentasi tetes tebu. Tetes tebu tersebut diberikan enzim yang berasal dari jamur
lalu didiamkan beberapa hari, hasil fermentasi di destilasi dengan alat buatan
sendiri yang berasal dari drum, lalu hasil destilasi tersebut disaring sehingga
menghasilkan cairan yang jernih. (Widodo, 2004).
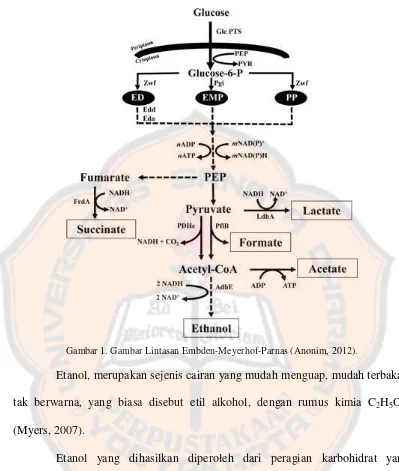
Dalam fermentasi ini glukosa didegradasi menjadi etanol dan CO2 melalui
suatu jalur metabolisme yang disebut glikolisis yang biasa jalurnya disebut jalur
Gambar 1. Gambar Lintasan Embden-Meyerhof-Parnas (Anonim, 2012).
Etanol, merupakan sejenis cairan yang mudah menguap, mudah terbakar,
tak berwarna, yang biasa disebut etil alkohol, dengan rumus kimia C2H5OH
(Myers, 2007).
Etanol yang dihasilkan diperoleh dari peragian karbohidrat yang
berkataliskan enzim. Enzim tersebut mengubah karbohidrat ke glukosa kemudian
ke etanol. Reaksi ini terjadi tanpa adanya oksigen dan menghasilkan CO2.
Etanol adalah pelarut yang umum, etanol dapat larut di air dan larut di
pelarut organik, termasuk asam asetat, aseton, benzena, karbon tetraklorida,
kloroform, dietil eter, gliserol, piridin, dan toluene (Lide, 2000).
C. Kromatografi Gas
Kegunaan umum dari kromatografi gas adalah untuk pemisahan dinamis
dan identifikasi semua jenis senyawa organik yang mudah menguap dan juga
untuk melakukan analisis kualitatif dan kuantitatif senyawa dalam suatu campuran
(Gandjar, 2007).
Kromatografi gas terdapat dua tipe yang sering digunakan, tipe pertama
yaitu gas-solid (adsorption) chromatography dan gas-liquid (partition)
chromatography. Pada tipe kedua yaitu kromatografi gas-cair lebih banyak
digunakan dan menggunakan kolom kapiler sebagai fase diamnya (Christian,
2004).
Bagian dasar yang ada di kromatografi gas:
a. Sumber gas dengan regulator tekanan serta pengatur aliran gas
b. tempat injeksi
c. Kolom kapiler
d. Detektor
e. Oven pengatur suhu kolom agar sampel tetap dalam kondisi gas
Gambar 2. Gambar skematis kromatografi gas (Anonim, 2011).
1. Gas Pembawa
Gas pembawa atau dengan kata lain fase gerak karena tujuan utamanya
yaitu membawa sampel (solute) menuju kolom dan tidak berpengaruh pada
selektifitas. Syarat gas pembawa yaitu murni dan tidak reaktif, gas pembawa
keadaan murni agar tidak berpengaruh pada detektor dan disimpan dalam tangki
bertekanan tinggi (Gandjar, 2007).
Tabel 2. Contoh Gas Pembawa dan Pemakaian Detektor.
Gas pembawa Detektor
Hidrogen Hantar panas
Helium Hantar panas
Ionisasi nyala
Fotometri nyala
Termoionik
Nitrogen Ionisasi nyala
Tangkap electron
Fotometri nyala
Termoionik
Argon Ionisasi nyala
Argon + metana 5% Tangkap electron
Karbon dioksida Hantar panas
2. Sistem Injeksi Sampel
Komponen utama selanjutnya adalah ruang suntik atau inlet. Fungsinya
adalah untuk menghantarkan sampel ke aliran gas pembawa menuju kolom.
(Gandjar, 2007). Pada kromatografi gas biasanya yang digunakan yaitu sampel
berupa cairan, dan di injekkan ke dalam kotak panas yang berfungsi untuk
mengubah sampel cair menjadi fase gas (flash vaporization) tanpa terfraksinasi
dan terdekomposisi. Pada kolom kapiler biasanya digunakan sampel yang sedikit
yaitu 0,1nL (nanoliter) yang membutuhkan gas pembawa, sehingga hanya dalam
jumlah kecil sampel yang masuk ke dalam kolom (Dean, 1995).
Dikarenakannya sampel yang diperlukan sangat kecil, dalam
pengukurannya akan sulit maka akan digunakan teknik pemecah suntikan (split
injection) sehingga aliran gas akan dibagi 2 setelah sampel di ijeksikan, satu aliran
akan dimasukkan kedalam kolom, dan aliran lainnya akan dibuang (Gandjar,
2007).
3. Kolom
Kolom merupakan tempat terjadinya proses pemisahan karena di
dalamnya terdapat fase diam, sehingga merupakan komponen yang sentral
(Gandjar, 2007). Kolom yang berfungsi sebagai pemisah mengandung fase diam
yang bias berupa adsorben (kromatografi gas, padat) atau cairan. Kolom tersebut
terbuat dari logam, gelas, atau silika (Dean, 1995).
a. Kolom kemas.
Kolom dapat berbentuk apapun selama masih dapat mengisi tempat
pemanas, kolom yang ada biasanya berbentuk melingkar, berbentuk U,
dan berbentuk W, tetapi yang paling sering digunakan adalah yang
berbentuk melingkar (Cristian, 2004).
b. Kolom kapiler.
Jenis kolom kapiler berbeda dengan kolom kemas, dan kolom
kapiler lebih sering digunakan dikarenakan kemampuan kolom kapiler
memberikan harga jumlah plat teori yang sangat besar (> 300.000 Pelat)
(Gandjar, 2007).
4. Fase Diam
Fase diam yang dipilih berdasarkan polaritas dari sampel yang akan
diujikan, dengan prinsip “ like dissolve like ”, oleh karena itu fase diam yang polar
akan lebih berinteraksi dengan senyawa yang lebih polar, dan begitulah
sebaliknya fase diam yang non polar akan lebih berinteraksi dengan senyawa yang
Tabel 3. Jenis fase diam dan penggunannya.
Fase diam Polaritas Golongan sampel Suhu maksimum oC Squalen Non polar Hidrokarbon 125 oC Apiezon L Non polar Hidrokarbon, ester,
eter
300 oC
Metil silikon Non polar Steroid, pestisida, alkaloida, ester
300 oC
Dionil ptalat Semi polar Semua jenis 170 oC Dietilenglikosuksinat Polar Ester 200 oC
Carbowax 20M Polar Alkohol, amina aromatik, keton
250 oC
(Gandjar, 2007).
5. Detektor
Komponen yang terpenting selanjutnya yaitu detektor. Detektor
merupakan perangkat yang berada di ujung kolom tempat keluarnya fase gerak
yang membawa sampel yang telah di pisahkan menjadi komponennya (Gandjar,
2007).
Detektor harus mempunyai karakteristik sebagai berikut:
a. Sensitivitas yang tinggi.
b. Stabil.
c. Waktu respon terhadap senyawa yang cepat.
d. Respon yang baik pada semua komponen organik.
e. Kemudahan penggunaan.
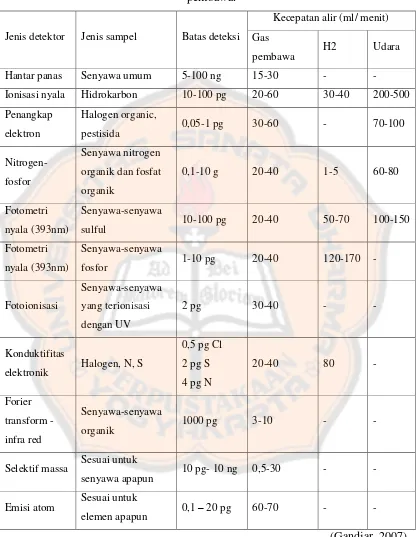
Tabel 4. Jenis detektor, batas deteksi, jenis sampel dan kecepatan alir gas
pembawa.
Jenis detektor Jenis sampel Batas deteksi
Kecepatan alir (ml/ menit)
Gas
pembawa H2 Udara
Hantar panas Senyawa umum 5-100 ng 15-30 - -
Ionisasi nyala Hidrokarbon 10-100 pg 20-60 30-40 200-500
Penangkap
elektronik Halogen, N, S
0,5 pg Cl
Selektif massa Sesuai untuk
senyawa apapun 10 pg- 10 ng 0,5-30 - -
Emisi atom Sesuai untuk
elemen apapun 0,1 – 20 pg 60-70 - -
Flame-ionization detector (FID) adalah detektor yang paling popular
dikarenakan memiliki sesitivitas yang tinggi 0,02 coloumb per gram dari
hidrokarbon (Dean, 1995). Detektor ini tidak sensitif terhadap kebanyakan bahan
anorganik dan termasuk air, sehingga pelarut dapat diinjeksikan dan tidak
mengganggu hasil kromatogram (Christian, 2004).
Gambar 4. Detektor FID (Anonim 2011).
6. Pengaturan Suhu
Kromatografi gas didasarkan pada dua sifat senyawa yang dipisahkannya
yakni kelarutan senyawa dan titik didih senyawa. Karena titik didih senyawa
berhubungan dengan suhu maka suhu merupakan faktor utama dalam
kromatografi gas. Walaupun suhu kolom dapat berkisar antara -100oC - 400oC
tetapi tetap harus dikendalikan karena pada suhu tertentu fase diam berada dalam
a. Pemisahan isothermal.
Pemisahan dengan suhu ini dilakukan untuk analisis rutin dan suhu
yang digunakan yaitu beberapa derajat dibawah titik didih komponen
campuran utama. Pemisahan jenis ini perlu diperhatikan, dikarenakan jika
suhu terlalu tinggi maka komponen akan terelusi tanpa terpisah, tetapi jika
suhu terlalu rendah maka sampel akan terlalu lama di kolom sehingga
semakin lebar puncaknya (Gandjar, 2007).
b. Pemisahan suhu terprogram.
Pemisahan ini dilakukan dengan suhu terendah dari titik didih
campuran, lalu diatur penambahan suhunya secar berkala dengan
kecepatan kira-kira 3 – 5 oC/menit sehingga didapatkan pemisahan yang
optimum (Dean, 1995).
7. Analisis kuantitatif
Analisis kuantitatif secara kromatografi gas menggunakan metode
standar internal. Metode standar internal digunakan karena terdapat
ketidakpastian yang disebabkan injeksi sampel, kecepatan aliran gas, dan
variasi keadaan kolom dapat diminimalisasi. Dalam prosedur ini, standar
internal yang telah diukur dengan seksama dimasukkan ke dalam setiap
larutan baku dan sampel, dan rasio luas puncak analit terhadap luas puncak
standar internal adalah parameter analisisnya. Puncak standar internal dan
puncak lainnya harus terpisah dengan baik sebagai syarat keberhasilan
D. Kromatografi Gas - Spektro Massa
Kromatografi Gas – Spektro Massa merupakan kombinasi pemisahan
antara kromatografi gas menggunakan detektor spektrometri massa. Kombinasi
ini merupakan salah satu teknik untuk memisahkan, mengukur dan
mengidentifikasi senyawa organik yang bersifat volatil dan semivolatil dalam
campuran kompleks (Anonim, 2009).
Kelebihan dari metode ini yaitu dapat memisahkan senyawa dengan baik
dan dapat langsung di deteksi struktur senyawanya, serta kelemahan ini yang
hanya dapat memisahkan senyawa volatil dan semivolatil (Anonim, 2009).
Spektrometri massa merupakan suatu instrumen yang dapat menyeleksi
molekul-molekul gas bermuatan berdasarkan massa atau beratnya. Spektra massa
dapat diperoleh dengan mengubah senyawa suatu sampel menjadi ion-ion yang
bergerak cepat yang dipisahkan berdasarkan perbandingan massa terhadap muatan
(m/e) (Khopkar, 1990).
Metode ini merupakan teknik analisis yang menyediakan informasi
secara kualitatif dan kuantitatif mengenai komposisi atom dan molekul dari
senyawa organik dan anorganik dan struktur kimianya, sehingga dapat diperoleh
bobot molekulnya (Pradyot, 1995).
Prinsip dasar dari spektrometri massa adalah pembentukan ion baik dari
senyawa organic maupun anorganik dengan metode tertentu dan terjadi pemisahan
ion tersebut berdasarkan massanya dalam satuan (m/z) sehingga dapat terdeteksi
Gambar 5. Skema Sistem Spektrometri Massa (Sastrohamidjodjo, 2001).
Spektra massa digambarkan dengan grafik batangan. Setiap peak dalam
spectra menyatakan suatu fragmen molekul. Fragmen-fragmen disusun
sedemikian rupa sehingga peak-peak ditata menurut kenaikan m/e dari kiri ke
kanan dalam spektra. Intensitas peak sebanding dengan kelimpahan relatif
fragmen-fragmen, yang tergantung pada stabilitas relatifnya. Peak tertinggi dalam
suatu spektra disebut peak dasar dengan nilai intensitas sebesar 100%; peak-peak
yang lebih kecil memiliki nilai intensitas sebesar 20%, 30% (relatif terhadap peak
dasar). Kadang-kadang peak dasar ini disebabkan oleh ion molekul, tetapi sering
E. Keterangan Empiris
Berdasarkan keterangan empiris etanol dibuat dari tetes tebu yang disebut
molase yang merupakan hasil samping yang berasal dari pembuatan gula tebu
yang difermentasikan oleh suatu mikroba selama seminggu sehingga kadar yang
diperoleh berkisar 20-30%. Komponen yang dihasilkan dari hasil fermentasi yaitu
19
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian non eksperimental dengan
rancangan penelitian deskriptif dikarenakan hanya mendeskripsikan keadaan yang
ada tanpa ada manipulasi subjek uji.
B. Variabel 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah ciu hasil produksi industri
rumahan daerah Sukoharjo
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah kadar etanol hasil
produksi
3. Variabel pengacau terkendali
Variabel pengacau terkendali yang terdapat dalam penelitian ini adalah:
a. Pelarut, untuk mengatasinya digunakan pelarut pro analisis dengan kemurnian
tinggi.
b. Suhu kolom, suhu injektor dari kromatografi gas
c. Kondisi lingkungan, dikarenakan etanol mudah menguap, oleh karena itu
C. Definisi Operasional
1. Sampel yang digunakan adalah ciu hasil produksi industri rumahan daerah
Sukoharjo.
2. Penetapan kadar digunakan sistem kromatografi gas dengan fase gerak
berdasarkan hasil optimasi yaitu suhu awal 70oC, initial time: 2 menit; rate: 30
o
C /min; temperatur final: 220 oC; waktu final: 2 menit; injektor B :200 oC;
detektor A : 250 oC; range :3.
3. Analisis kualitatif untuk mengetahui kandungan senyawa dan profil senyawa
lain yang terdapat dalam sampel ciu.
4. Kadar etanol dinyatakan dalam satuan %v/v.
D. Bahan-bahan Penelitian
Bahan yang digunakan dalam penelitian adalah hasil pengolahan
fermentasi tetes tebu baku etanol p.a.(E. Merck), , n-butanol p.a (E. Merck),
akuabides (Fakultas Farmasi Universitas Sanata Dharma), gas hydrogen HP
99,995% (CV. Perkasa), udara tekan (Laboratorium Analisis Pusat Universitas
Sanata Dharma), gas nitrogen HP 99,9995% (CV. Perkasa).
E. Alat-alat Penelitian
Alat yang digunakan dalam penelitian ini meliputi seperangkat alat
Kromatografi Gas (HP 5890) dengan Flame Ionization Detector (FID), kolom
kapiler DB-Wax (30 m, i.d. 0,25 mm), alat-alat gelas yang lazim digunakan untuk
F. Prosedur Kerja 1. Pemilihan sampel
Penelitian ini menggunakan sampel yang berasal dari Desa Bekonang
yang merupakan hasil industri rumahan produksi alkohol. Sampel diambil Kurang
lebih 600,0 ml setiap produksi dan diambil sebanyak 3 kali produksi yang
dilakukan di 14 rumah produksi dari 70 rumah produksi, pemilihan tempat
produksi dengan cara random yaitu dengan mengambil undian.
2. Preparasi sampel
Sampel yang didapat dihomogenkan terlebih dahulu dengan cara digojog
pada setiap botol, kemudian disaring dengan kertas whatman no 1 agar lebih
jernih. Kemudian disimpan dalam botol tertutup untuk menghindari penguapan
sampel.
3. Analisi Kualitatif
Uji Waktu Retensi. Etanol p.a kurang lebih 800 μl diambil dengan mikro pipet kemudian ditambahkan n-butanol kurang lebih 600 μl kedalam labu takar 10 ml, kemudian di encerkan dengan aquabidest hingga tanda dan digojog. Sampel
kurang lebih 2,0 ml diambil kemudian ditambahkan n-butanol kurang lebih 0,6 ml
kedalam labu takar 10 ml, kemudian di encerkan dengan aquabidest hingga tanda
dan digojog. Masing-masing diambil 1,0 µl disuntikkan kedalam kolom melalui
tempat injeksi ke alat kromatografi gas kemudian dibandingkan waktu retensinya.
Analisis GC-MS. Sampel kurang lebih 600,0 ml diambil untuk dilakukan
Kemudian sampel dituang kedalam LAB, lalu alat dijalankan pada suhu 70oC
selama 1 jam, kemudian hasil penguapan disimpan sebagai sampel 1. Penguapan
dilanjutkan lagi dengan suhu 100oC selama 1 jam, kemudian hasil penguapan
disimpan sebagai sampel 2. Sampel yang tidak menguap ditampung sebagai
sampel 3. Ketiga sampel yang didapat dilakukan analisi kualitatif menggunakan
GC-MS untuk mengetahui kandungan dalam sampel yang ada selain kandungan
etanol.
4. Pembuatan seri baku
Seri baku yang digunakan pada sampel ini yaitu etanol dengan
penambahan standar internal yaitu n-butanol.
Etanol p.a kurang lebih 200; 400; 600; 800; 1000 μl diambil menggunakan mikro pipet kemudian ditambahkan standar internal n-butanol
kurang lebih 600 μl kemasing-masing labu takar 10 ml, kemudian di encerkan dengan aquabidest hingga tanda dan gojog homogen.
5. Pembuatan kurva baku
Larutan baku sebanyak 1µl dari masing-masing konsentrasi seri larutan
baku disuntikkan kedalam kolom melalui tempat injeksi ke alat kromatografi gas.
Setelah didapat kromatogram dihitung luas area dari etanol, dan n-butanol.
Dilakukan replikasi 3 kali.
6. Penetapan kadar sampel
Sampel yang telah dipreparasi sebanyak 42 digojog hingga homogen dan
kurang lebih 2,0 ml diambil menggunakan mikropipet kedalam labu takar 10 ml
aquabidest hingga 10 ml. Sampel sebanyak 1µl diinjeksikan kedalam kolom
kromatografi gas dengan sistem yang sudah di optimasi. Nilai AUC yang
didapatkan kemudian dimasukkan kedalam persamaan kurva baku etanol, maka
akan didapat kadar etanol dalam sampel
G. Analisis Hasil
Analisis kualitatif dilakukan dengan membandingkan waktu retensi (tR)
senyawa sampel dengan senyawa baku dan juga digunakan kromatografi
gas-spektrofotometri massa (GC-MS). Analisis kuantitatif yang dilakukan adalah
penetapan kadar etanol berdasarkan data AUC sampel serta AUC kurva baku etanol.
24
BAB IV
PEMBAHASAN
A. Pemilihan Sampel
Penelitian ini menggunakan sampel Ciu hasil produksi rumahan yang
berasal dari dusun Sentul desa Bekonang, Kabupaten Sukoharjo, Jawa Tengah.
Sampel diambil di 14 rumah produksi dari total 70 rumah produksi.
Masing-masing sampel diambil sebanyak 600,0 ml selama 3 kali masa produksi.
Pengambilan sampel ini termasuk pengambilan secara acak karena dari 70 rumah
produksi diundi untuk diambil sebanyak 20%, sehingga setiap sampel memiliki
kesempatan yang sama untuk terambil. Kriteria representatif pengambilan sampel
dikendalikan dengan pengadukan sampel hingga homogen dan pemipetan sampel
dari berbagai sisi wadah sampel.
B. Optimasi dan Pemilihan Standar Internal
Optimasi yang dilakukan Waskito, 2013 ditujukan agar terjadi pemisahan
sempurna antar peak sampel, sehingga pengukuran kadar setiap senyawa tidak
dipengaruhi oleh senyawa lain. Serta selain itu optimasi juga digunakan agar peak
sampel tidak bertumpuk juga dengan standar internal. Senyawa yang digunakan
Gambar 6 .Kromatogram etanol dengan standar internal methanol
Gambar 7 .Kromatogram etanol dengan standar internal n-butanol
Melalui hasil kromatogram diatas diketahui bahwa jika menggunakan
standar internal metanol diketahui waktu retensinya (tR) terlalu dekat dan
dikhawatirkan mengganggu peak sampel, dan pada kromatogram dengan standar
internal n-butanol memeliki resolusi yang baik sehingga dapat digunakan sebagai
C. Uji Kualitatif Sampel
1. Analisis kualitatif berdasarkan waktu retensi (tR) etanol
Analisis kualitatif dilakukan dengan membandingkan waktu retensi (tR)
sampel dengan waktu retensi (tR) etanol dengan menggunakan standar internal
n-butanol. Analisis kualitatif ini dilakukan untuk membuktikan bahwa di dalam
sampel yang diuji terdapat etanol. Hal tersebut ditunjukkan dengan adanya (tR)
sampel dengan (tR) baku pembanding yang sama. Hasil kromatogram yang
diperoleh dari baku etanol dan sampel adalah sebagai berikut:
Gambar 8 .Kromatogram baku etanol (8%v/v)
Dari kromatogram yang dihasilkan, antara baku etanol memiliki waktu
retensi yang tidak jauh berbeda dengan sampel. Waktu retensi baku etanol adalah
253.5 detik. Waktu retensi senyawa pada sampel adalah 254 detik, dengan demikian
dapat dikatakan bahwa senyawa yang terdapat pada sampel yaitu etanol.
2. Analisis kualitatif dengan GC-MS
Untuk mengetahui kandungan yang terdapat di dalam sampel dan juga
untuk membuktikan keberadaan kandungan etanol maka dilakukan analisis
kualitatif menggunakan kromatografi gas dengan detektor spektrometri massa.
Digunakan kromatografi gas dengan detektor spektrometri massa yaitu agar dapat
diketahui berbagai kandungan senyawa yang terdapat dalam ciu hasil produksi.
Sampel diuapkan dengan menggunakan vaccum evaporator dengan 2
suhu berbeda yaitu pada suhu 70oC dan 100oC menggunakan destilasi berulang
yaitu menggunakan suhu 70oC selama 1 jam kemudian dilanjutkan pada suhu
100oC dan hasil penguapan ditampung sehingga didapatkan 3 sampel yang akan
diuji, tujuan diuapkan dengan 2 suhu yang berbeda yaitu agar terjadi pemisahan
senyawa-senyawa yang mempunyai titik didih berbeda dan untuk lebih dipekatkan
kadarnya, sehingga dapat lebih mudah diketahui senyawa yang terdapat pada
Gambar 10. Kromatogram sampel 1
Dapat dilihat dari hasil kromatogram gambar 8 bahwa pada penguapan di
suhu 70oC hanya terdapat satu senyawa yang mempunyai tR 2.233 menit,
sehingga bisa dipastikan hanya ada satu senyawa. Dan hasil spektra massa
senyawa tersebut sebagai berikut:
Gambar 11. Spektra massa senyawa pada waktu retensi 2.233 menit
Berdasarkan hasil spektra massa pada gambar 9 diketahui bahwa
senyawa yang terdapat pada sampel 1 mempunyai nilai m/z =45, dengan
similarity index 99 berdasarkan hasil tersebut dibandingkan dengan data yang ada
pada database, sehingga dapat diketahui bahwa senyawa yang mempunyai nilai
Gambar 12. Kromatogram sampel 2
Dapat dilihat dari hasil kromatogram gambar 10 bahwa pada penguapan
di suhu 100oC hanya terdapat satu senyawa yang berada pada tR 2.217 menit,
sehingga bisa dipastikan hanya ada satu senyawa. Dan hasil spektra massa
senyawa tersebut sebagai berikut:
Gambar 13. Spektra massa senyawa pada waktu retensi 2.217 menit
Berdasarkan hasil spektra massa pada gambar 11 diketahui bahwa
senyawa yang terdapat pada sampel 1 mempunyai nilai m/z =45, dengan
similarity index 99 berdasarkan hasil tersebut dibandingkan dengan data yang ada
pada database, sehingga dapat diketahui bahwa senyawa yang mempunyai nilai
Gambar 14. Kromatogram sampel 3 (hasil penguapan)
Dapat dilihat dari hasil kromatogram gambar 12. bahwa sampel yang
tidak menguap pada suhu 100oC terdapat tiga senyawa yang terukur yaitu
senyawa pertama berada pada tR 2.083 menit, senyawa kedua berada pada tR
2.308 menit, dan senyawa ketiga berada pada tR 2.675 menit. Dan hasil spektra
massa senyawa tersebut sebagai berikut:
Gambar 15. Spektra massa senyawa pada waktu retensi 2.308 menit
Berdasarkan hasil spektra massa pada gambar 13 diketahui bahwa
senyawa pertama yang terdapat pada sampel 3 mempunyai berat molekul sebesar
394g/mol dengan similarity index 77. Senyawa kedua yang terdapat pada sampel
3 mempunyai berat molekul sebesar 58g/mol dengan similarity index 99 pada
gambar 15 senyawa ketiga yang terdapat pada sampel 3 mempunyai berat molekul
sebesar 60g/mol dengan similarity index 99 pada gambar 17 dan kemudian
berdasarkan hasil tersebut dibandingkan dengan data yang ada pada database yang
terdapat di alat diketahui bahwa senyawa kedua yang mempunyai berat molekul
58g/mol yaitu Aseton, senyawa ketiga yang mempunyai berat molekul 60 g/mol
yaitu asam asetat.
D. Pembuatan Kurva Baku Etanol
Larutan baku etanol dibuat dengan cara melarutkan sejumlah etanol p.a
dengan pelarut aquabidest dan digunakan standar internal n-butanol. Dalam
pembuatannya dibuat dengan kadar etanol 2%; 4%; 6%; 8%; dan 10% v/v, dengan
menambahkan standar internal berupa n-butanol sebanyak 0.6 ml ke
masing-masing larutan baku.
Tabel 5. Kurva Baku Etanol dengan Standar Internal n-Butanol
Replikasi 1 Replikasi 2 Replikasi 3
Konsentrasi (%v/v)
Rasio AUC Konsentrasi (%v/v)
Berdasarkan hasil perhitungan tabel diatas dapat dilihat bahwa nilai
korelasi (r) untuk replikasi 1 (0.9999), untuk replikasi 2 (0.9993), dan untuk
replikasi 3 (0.9994), yang mempunyai nilai terbaik yaitu replikasi 1 (0.9999),
sehingga dalam penggunaan untuk perhitungan kadar etanol menggunakan
persamaan regresi linier replikasi 1.
Gambar 17. Kurva hubungan antara Kadar Etanol (%v/v) vs Rasio AUC etanol/butanol
Dari kurva baku etanol di atas menunjukkan hubungan linear antara
jumlah analit dengan respon AUC. Kurva tersebut menggambarkan terjadinya
peningkatan respon AUC proporsional sesuai dengan meningkatnya jumlah analit
di dalam sampel.
E. Preparasi Sampel
Sampel yang digunakan berupa CIU hasil produksi di dusun Sentul desa
Bekonang. Sampel yang sejumlah 42 dengan jumlah 600 ml dari masing-masing
tempat produksi digojog hingga homogen, hal ini dilakukan agar sampel
tercampur sempurna, sehingga dalam pengambilan cuplikan di wadah akan
0,000
mempunyai kadar yang sama. Untuk menghindari partikel kotoran yang
kemungkinan dapat menyumbat kolom maka perlu dilakukan penyaringan.
Setelah disaring lalu lalu diambil sejumlah 2,0 ml larutan sampel dan 0.6 ml
n-butanol, dimasukkan kedalam labu ukur 10 ml, lalu di add dengan aquabides
hingga tanda, n-butanol digunakan sebagai standar internal yang berfungsi untuk
faktor koreksi ketika penetapan kadar.
F. Penetapan Kadar Sampel
Sampel yang telah di preparasi sebelumnya masing-masing diambil 1 µl
untuk disiapkan diinjekkan ke kolom kromatografi gas, penggambilan
menggunakan syring khusus untuk kromatografi gas. Alat kromatografi gas
sebelumnya sudah di sesuaikan kondisinya dengan hasil optimasi sebelumnya,
kondisi alat kromatografi gas adalah sebagai berikut:
Gas : Nitrogen, Hidrogen, Udara
Kolom : Cp-Wax 52 CB, 25m x 032mm
Fase Diam : Polietilen glikol
Jenis Detektor : FID (flame ionization detector)
Tekanan Kolom : 10 psi
Kecepatan Aliran Gas Udara : 394 ml/min
Kecepatan Aliran Gas Hidrogen : 36.2 ml/min
Kecepatan Aliran Gas Pembawa Nitrogen : 0.9 ml/min; Nitrogen make up:
27.5 ml/min
Tabel 6. Kadar Sampel Hari ke 1.
Tabel 7. Kadar Sampel Hari ke 2.
Tabel 8. Kadar Sampel Hari ke 3.
No Sampel Kadar %(v/v) No Sampel Kadar %(v/v)
semua rumah produksi menghasilkan kadar etanol yang selalu berubah, atau tidak
tetap. Rentang kadar etanol pada setiap harinya yaitu hari 1 29.779%v/v±1.725;
Berdasarkan data diatas dengan dilakukan uji statistik dengan uji
ANOVA satu arah bahwa kadar etanol dari setiap hari produksi tidak berbeda
bermakna.
37
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Senyawa yang terdapat pada CIU hasil produksi yaitu etanol, asam asetat,
aseton.
2. Kadar etanol yang diproduksi cukup bervariasi, rata-rata yaitu hari 1
29.779%v/v±1.725; hari 2: 29.762%v/v±2.237; dan hari 3:
30.316%v/v±2.085. Dengan uji ANOVA satu arah diketahui hasil
produksi tidak berbeda bermakna setiap harinya.
B. Saran
Perlu dilakukan penetapan kadar senyawa lain yang berada pada hasil
DAFTAR PUSTAKA
Anonim, 2008, http://www.cdc.gov/NIOSH/ershdb/EmergencyResponseCard_ 29750029 .html, diakses tanggal 28 Oktober 2011.
Anonim, 2009, Gas Chromatography-Mass Spectrometry, MiPlaza Materials Analysis, Jerman.
Anonim, 2011, http://chemwiki.ucdavis.edu/Analytical_Chemistry/Instrumental_ Analysis/Gas_Chromatography, diakses tanggal 31 oktober 2011.
Anonim, 2012, http://aem.asm.org/content/77/2/706/F2.expansion.html, diakses tanggal 10 desember 2012
Christian, G.D., 2004, Analytical Chemistry, Sixth Edition, Jhon Wiley & Sons, Inc., United States of America, , 65, 66, 555 – 565, 574.
Day, R.A. and Underwood, A.L., 1986, Analisis Kimia Kuantitatif, Airlangga, Jakarta 404.
Dean, J. A., 1995, Analytical Chemistry Handbook, Mc Graw-Hill, Inc., United States of America, 4.1 – 4.63.
Fessenden, R. J. dan Fessenden, J. S., 1986. Kimia Organik, Edisi Ketiga, diterjemahkan oleh Aloysius Hadyana Pudjaatmaka, Penerbit Erlangga, Jakarta, 267.
Fessenden, R.J. and Fessenden, J.S., 1994, Kimia Organik, Jilid 2, Penerbit Erlangga, Jakarta, pp. 181-183, 455.
Gandjar, G.I., 2007, Kimia Farmasi Analisis, Pustaka Pelajar, Yogyakarta, 419 – 437.
Gross, J.H., 2004, Mass Spectrometry A textbook, Springer Berli Heidelberg, Germany.
Juwita, R., 2012, Studi Produksi Alkohol Dari Tetes Tebu (Saccharum Officinarum L) Selama Proses Fermentasi, Skripsi, Universitas Hasanudin, Makasar, 3.
Khopkar, 1990, Konsep Dasar Kimia Analitik, UI Press, Jakarta, pp. 166, 231, 232, 389.
Lide, DR, 2000, CRC Handbook of Chemistry and Physics, 81st edition.
Mardoni, 2006, Perbandingan Metode Kromatografi Gas dan Berat Jenis Pada Penetapan Kadar Etanol dalam Minuman Anggur, Skripsi, Universitas Sanata Dharma, Yogyakarta, 29-37.
Myers, Richard L., Myers, Rusty L., 2007, The 100 most important chemical compounds: a reference guide, Westport, Conn. Greenwood Press, 122.
Pradyot, P., 1995, Dean’s Analytical Chemistry Handbook, McGrawHill, New York, pp. 10.2 , 10.26.
Rombang, A. D., 2013, Validasi Metode Penetapan Kadar Etanol Dan Profil Senyawa Yang Terdapat Dalam Hasil Produksi “Ciu” Rumahan Desa Sentul Kabupaten Sukoharjo Dengan Metode Kromatografi Gas, Skripsi (In Progress), Universitas Sanata Dharma.
Sastrohamidjodjo, H., 2001, Spektroskopi, Liberty, Yogyakarta, 168.
Sebayang, F., 2006, Pembuatan Etanol dari Molase Secara Fermentasi Menggunakan Sel Saccharomyces cerevisiae yang Termobilisasi pada Kalsium Alginat, Jurnal Teknologi Proses USU, Sumatera Utara, 7.
Simanjuntak, R., 2009, Studi Pembuatan Etanol Dari Limbah Gula (Molase), Skripsi, Universitas Sumatera Utara, Sumatra Utara, 4.
Skoog, D. A., West, D. M., and Holler, F. J., 1994, Analytical Chemistry An Introduction. Sixth Edition, Saunders College Publishing, USA, 507.
Waskito, A. A. P., 2013, Optimasi Metode Penetapan Kadar Etanol Dan Profil Senyawa Yang Terdapat Dalam Hasil Produksi “Ciu” Rumahan Desa Sentul Kabupaten Sukoharjo Dengan Metode Kromatografi Gas, Skripsi (In Progress), Universitas Sanata Dharma.
Widyanti, E.M., 2010, Produksi Asam Sitrat Dari Substrat Molase Pada Pengaruh Penambahan Vco (Virgin Coconut Oil) Terhadap Produktivitas Aspergillus Niger Itbcc L74 Terimobilisasi, Tesis, UNDIP, Semarang.
LAMPIRAN
Lampiran 3: Kromatogram GC-MS Sampel 1
Lampiran 10. Hasil Validasi Metode Analisis
Tabel Data replikasi kurva baku etanol
Baku etanol
Replikasi I Replikasi II Replikasi III Replikasi IV Replikasi V Seri
meliputi selektivitas, linearitas, akurasi, presisi, rentang, limit of detection, limit of
quantitation. Konsentrasi yang digunakan merupakan kosentrasi rendah, sedang,
dan tinggi dari konsentrasi seri baku yang dibuat yaitu 0,2 ml, 0,6 ml dan 1,0 ml.
1. Selektivitas
Tabel Perbandingan Retention Time baku etanol dan standar internal n-butanol
Konsentrasi seri larutan baku
etanol
TR etanol TR n-butanol Resolusi
2%v/v 254 324 15,7
6%v/v 254 324 12,9
10%v/v 254 324 14,0
Berdasarkan tabel di atas dapat dilihat bahwa resolusi antar peak analit
(etanol) dengan peak terdekat telah memenuhi persyaratan resolusi yang baik
Peak Start TR Max TR End TR
1 252 254 256
2 321 324 326
Kromatogram pengukuran sampel pada kondisi optimal
Peak Start TR Max TR End TR
1 254 256 260
2 324 327 329
Kromatogram baku etanol konsentras 600µL
Berdasarkan kedua gambar, dapat dilihat kromatogram hasil pengukuran
baku dan kromatogram hasil pengukuran sampel pada kondisi optimasi
menunjukkan waktu retensi yang tidak jauh berbeda.
2. Linearitas
Linearitas ditunjukkan oleh nilai koefisien korelasi (r). Dari pengukuran
kurva baku didapatkan nilai untuk replikasi I = 0,9981 ; replikasi II = 0,9993 ;
replikasi III = 0,9981, replikasi IV = 0,9971; dan replikasi V = 0,9996. Nilai r
untuk kelima replikasi tersebut sudah memenuhi persyaratan dan dipilih nilai r
yang paling mendekati 1 yaitu nilai r pada replikasi V.
3. Akurasi
Akurasi dinyatakan sebagai % recovery. Penetapan % recovery dilakukan
dengan mengukur 3 seri konsentrasi baku dari lima seri konsentrasi baku yang
digunakan
Tabel Data % recovery Kadar
dan konsentrasi level tinggi (1000 µl). Pada konsentrasi level rendah (200 µl) nilai
yang diperoleh tidak memenuhi persyaratan akurasi yang baik.
4. Presisi
Presisi dinyatakan dengan Coefficient of Variation (CV).
Tabel Coefficient of Variations (CV) etanol
∑ 44,8 x 10-4
Nilai batas kuantifikasi (LOQ) yang diperoleh adalah 1,729%v/v.
Berdasarkan nilai tersebut kadar sampel yang digunakan pada tidak boleh lebih
rendah dari kadar 1,729%v/v, sehingga pada penelitian ini penggunaan kadar
terkecil 2%v/v masih memenuhi persyaratan akurasi dan presisi.
Nilai batas deteksi (LOD) yang diperoleh adalah 0,518%v/v.
Berdasarkan nilai tersebut dapat diketahui jika metode kromatografi gas yang
digunakan masih dapat mengukur etanol sampai batas kadar terkecil 0,518%v/v
Lampiran 11: Perhitungan Kurva Baku
Baku Etanol dan Butanol
0.2 0.4 0.6 0.8 1
TR Etanol 245.5 243.6 247.3 246.1 246.2
AUC Etanol 0.175 0.576 0.628 0.906 1.01
TR Butanol 314.8 313.9 317.3 316.1 315.9
AUC Butanol 0.854 1.259 0.895 0.965 0.858
Baku Etanol dan Butanol
0.2 0.4 0.6 0.8 1
TR Etanol 255.5 255.3 256.1 255.7 256.1
AUC Etanol 0.187 0.434 0.601 0.755 1.096
TR Butanol 326.2 325.8 327.1 326.2 326.6
AUC Butanol 0.739 0.829 0.73 0.73 0.588
Baku Etanol dan Butanol
0.2 0.4 0.6 0.8 1
TR Etanol 252.7 251.3 251.7 253.1 251.3
AUC Etanol 0.178 0.41 0.61 0.943 1.107
TR Butanol 323.6 321.9 322.2 324 322.2
AUC Butanol 0.94 0.929 0.93 1.034 0.991
1. Seri Baku 1 Etanol dengan Standar Internal N-Butanol
Perhitungan Rasio AUC Etanol dengan AUC N-Butanol
2. Seri Baku 2 Etanol dengan Standar Internal N-Butanol
Perhitungan Rasio AUC Etanol dengan AUC N-Butanol
Rasio = 𝐴𝑈𝐶𝐸𝑡𝑎𝑛𝑜𝑙
3. Seri Baku 3 Etanol dengan Standar Internal N-Butanol
Perhitungan Rasio AUC Etanol dengan AUC N-Butanol
Lampiran 12: Kromatogram Baku Etanol a. Kurva baku 2%
Replikasi 1
Replikasi 2
b. Kurva baku 4%
Replikasi 1
Replikasi 2
c. Kurva baku 6%
Replikasi 1
Replikasi 2
d. Kurva baku 8%
Replikasi 1
Replikasi 2
e. Kurva baku 10%
Replikasi 1
Replikasi 2
Lampiran 13: Kromatogram Sampel
Keterangan
A: peak etanol
B: peak n-butanol
Lampiran 14: Kondisi Kromatogram Gas Kondisi Alat Kromatografi Gas
Mulai 10.30 -
Gas Nitrogen, Hidrogen, Udara
Column Cp-Wax 52 CB, 25m x 032mm
Column Head Presure 10 psi
Press. Udara 4 bar
Press. Nitrogen 1.5 bar
Flow Nitrogen Carier 0.9 ml/min
Init temp 70
Lampiran 15: Perhitungan Sampel Alkohol
1. AUC Sampel Alkohol
Sampel hari 1 replikasi 1
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
Sampel hari 1 replikasi 2
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
1 2 3 4 5
TR Etanol 252.5 252.3 253.4 253.3 253.4
TR Butanol 323.6 323.1 324.3 324.4 324.4
Sampel hari 1 replikasi 3
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
Sampel hari 2 replikasi 1
TR Butanol 321.1 322 320.5 321.9
AUC Butanol 1.167 1.346 1.112 1.179
Sampel hari 2 replikasi 2
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
Sampel hari 2 replikasi 3
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
Sampel hari 3 replikasi 1
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
1 2 3 4 5
TR Etanol 253.7 254.3 254.2 255.2 253.8
AUC Etanol 0.837 0.709 0.833 0.916 0.919
AUC Butanol 1.259 1.025 1.221 1.207 1.206
Sampel hari 3 replikasi 2
I.Temp = 70, I.Time = 2 , 200 & 250, range 3
Sampel hari 3 replikasi 3
2. Contoh Perhitungan Sampel hari 1
a. Rasio AUC Etanol dengan N-Butanol
Sampel (Rasio) = 𝐴𝑈𝐶𝐸𝑡𝑎𝑛𝑜𝑙
b. Perhitungan regresi linier
No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
Tabel Kadar Sampel Hari ke 1.
3. Perhitungan Sampel Hari 2
a. Rasio AUC Etanol dengan N-Butanol
Sampel (Rasio) = 𝐴𝑈𝐶𝐸𝑡𝑎𝑛𝑜𝑙
b. Perhitungan menggunakan kurva baku
No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
Tabel Kadar Sampel Hari ke 2.
4. Perhitungan Sampel Alkohol Hari 3
a. Rasio AUC etanol vs butanol
Sampel (Rasio) 1 = 0.837
b. Perhitungan menggunakan kurva baku
No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
etanol/butanol Kadar No
Rasio AUC
Tabel Kadar Sampel Hari ke 3.
BIOGRAFI PENULIS
Penulis skripsi berjudul “Penetapan kadar etanol dalam hasil
produksi “ciu” rumahan desa sentul kabupaten sukoharjo
dengan metode kromatografi gas” memiliki nama lengkap Fajar
Dwi Riyanto. Penulis lahir di Pangkalan Bun Provinsi
Kalimantan Tengah pada tanggal 31 Oktober 1990 sebagai anak kedua pasangan
Mulyana dan Murwani. Pendidikan formal yang pernah diikuti penulis yaitu TK
Cahaya Mulia Pangkalan Bun (1995-1996), SD Katolik Santa Maria Pangkalan
Bun (1996-2002), SMP Negeri 1 Pangkalan Bun (2002-2005), SMA Negeri 1
Pangkalan Bun (2005-2008), kemudian tahun 2008 melanjutkan kuliah di
Fakultas Farmasi Universitas Sanata Dharma. Selama menempuh kuliah penulis
aktif dalam berbagai kegiatan dan organisasi beberapa diantaranya, Panitia PPnEC
Farmasi (2008,2009), Pengurus BEMF Farmasi (2009, 2010), Panitia INSADHA
(2010), dan yang terakhir Tim Humas dan Promosi Universitas Sanata Dharma