PEMBUATAN DAN EVALUASI SEDIAAN TOPIKAL GEL ANTIOKSIDAN EKSTRAK DAUN JAMBU BIJI (Psidium guajava L.)
DENGAN GLISERIN SEBAGAI HUMECTANT
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh
Juliana
NIM: 108114064
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
i
PEMBUATAN DAN EVALUASI SEDIAAN TOPIKAL GEL ANTIOKSIDAN EKSTRAK DAUN JAMBU BIJI (Psidium guajava L.)
DENGAN GLISERIN SEBAGAI HUMECTANT
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh
Juliana
NIM: 108114064
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Skripsi ini kupersembahkan untuk :
The Lord, Jesus Christy and Holy Spirit
Papa, Mama, Mami, Papi, Kakak dan Adek
Sahabat-sahabatku dan teman-temanku terkasih
vii
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas
berkat dan penyertaan-Nya sehingga penulis dapat menyelesaikan skripsi berjudul
“Pembuatan dan Evaluasi Sediaan Topikal Gel Antioksidan Ekstrak Daun Jambu
Biji (Psidium guajava L.) dengan Gliserin sebagai Humectant” sebagai salah satu
syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm.) Universitas Sanata
Dharma Yogyakarta.
Penulis menyadari bahwa dalam penelitian dan penyusunan skripsi ini
tidak terlepas dari bantuan dan dukungan dari berbagai pihak, baik secara
langsung maupun tidak langsung. Oleh karena itu, penulis mengucapkan terima
kasih kepada:
1. Orang tua penulis atas doa, kasih sayang, nasihat, dan dukungan yang
diberikan baik secara moril maupun materiil sehingga skripsi ini dapat
diselesaikan.
2. Ibu Aris Widayati, M.Si., Apt., Ph.D. selaku Dekan Fakultas Farmasi
Universitas Sanata Dharma dan semua dosen Fakultas Farmasi yang telah
memberikan ilmu serta bimbingan kepada penulis.
3. Ibu Dr. Sri Hartati Yuliani, M.Si., Apt. selaku dosen pembimbing dan dosen
penguji pada skripsi ini yang telah menyediakan waktu bimbingan,
mendampingi penulis dengan sabar, memberikan motivasi dan saran kepada
viii
4. Ibu C.M. Ratna Rini Nastiti, M.Pharm., Apt. selaku dosen penguji yang telah
memberikan dukungan, kritik, dan saran yang membangun selama proses
pembuatan skripsi.
5. Ibu Melania Perwitasari, M.Sc., Apt. selaku dosen penguji yang telah
memberikan dukungan, kritik, dan saran yang membangun selama proses
pembuatan skripsi.
6. Kakak dan adik atas doa, kasih sayang, nasihat, dan dukungan yang diberikan
baik secara moril maupun materiil sehingga skripsi ini dapat diselesaikan.
7. Ibu Phebe Hendra, M.Si., Ph.D., Apt. selaku dosen pembimbing akademik
yang telah mendampingi dan memberikan perhatian hingga penulis
menyelesaikan perkuliahan dengan baik.
8. Sahabat-sahabatku Agnes, Elvira, Giovanna, Priscilla, Sita, Olivia, dan Liana
yang selalu memberikan dukungan, semangat, doa, canda tawa, dan menjadi
sukacita tersendiri bagi penulis dalam proses penelitian dan penyusunan
skripsi.
9. Teman- teman Kost Palem tercinta, Ayu, Budi, Erna, Titin, Tari, dan Lena,
teman-teman Greeter Youth, serta teman-teman komsel Ester dan G.O.F yang
selalu memberikan dukungan kepada penulis dalam menyelesaikan skripsi
ini.
10. Vivian, Rosi, Lilin, Bakti, Naomi, Kezia, Sisca, Agi, Sita, Hans, Lulu,
Sammy, Nia, Nafta, dan Tiffany terima kasih untuk diskusi, kebersamaan,
dukungan, bantuan, canda dan tawa selama penelitian dan penyusunan
ix
11. Segenap laboran dan karyawan, Mas Bimo, Pak Parlan, Pak Mus, Pak
Wagiran, Pak Ketul, Mas Agung, Pak Heru atas bantuan dan kerjasama di
laboratorium selama ini.
12. Teman-teman angkatan 2010 Fakultas Farmasi Universitas Sanata Dharma
untuk kebersamaan dan pengalaman yang tidak terlupakan selama menjalani
proses belajar dan semua pihak yang telah mendukung dan tidak dapat
penulis sebutkan satu per satu.
Penulis menyadari bahwa skripsi ini banyak kekurangan dan masih jauh
dari sempurna. Penulis mengharapkan kritik dan saran yang membangun dari
semua pihak sehingga dapat menjadi pembelajaran bagi penulis untuk menjadi
lebih baik. Harapan penulis semoga skripsi ini dapat bermanfaat bagi
perkembangan ilmu kefarmasian, pembaca, dan seluruh pihak.
x
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
LEMBAR PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
xi
E. Bahan-Bahan yang Digunakan dalam Formulasi Gel ... 12
1. Carbopol ... 12
BAB III METODE PENELITIAN... 20
A. Jenis Penelitian ... 20
xii
C. Definisi Operasional ... 20
C. Bahan Penelitian ... 21
D. Alat Penelitian ... 22
E. Tata Cara Penelitian ... 22
1. Identifikasi Ekstrak Daun Jambu Biji (Psidium guajava L.) ... 22
2. Identifikasi Tanin dalam Ekstrak Daun Jambu Biji (Psidium guajava L.) Secara Kualitatif... 22
3. Pembuatan Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.) ... 23
4. Uji Sifat Fisis Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.) ... 24
5. Uji Iritasi Primer Draize Test ... 25
6. Penetapan Kadar Tanin dalam Ekstrak dan dalam Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.) Secara Spektrofotometri Ultraviolet-Visibel ... 25
G. Analisis Hasil ... 29
BAB IV HASIL DAN PEMBAHASAN ... 31
A. Identifikasi Ekstrak Daun Jambu Biji (Psidium guajava L.) ... 31
B. Identifikasi Tanin dalam Ekstrak Daun Jambu Biji (Psidium guajava L.) Secara Kualitatif ... 31
xiii
D. Uji Sifat Fisis Gel Antioksidan Ekstrak Daun Jambu Biji
(Psidium guajava L.) ... 34
1. Uji organoleptis dan pH ... 34
2. Uji viskositas ... 35
3. Uji daya sebar ... 37
E. Uji Iritasi Primer Draize Test ... 38
F. Penetapan Kadar Tanin dalam Ekstrak dan dalam Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.) Secara Spektrofotometri Ultraviolet-Visibel ... 40
1. Penetapan operating time (OT) ... 40
2. Penetapan panjang gelombang maksimum ... 41
3. Pembuatan kurva baku asam tanat ... 42
4. Penetapan kadar tanin ekstrak dan gel antioksidan ekstrak daun jambu biji (Psidium guajava L.) ... 44
xiv
LAMPIRAN ... 56
xv
DAFTAR TABEL
Halaman
Tabel I. Formula yang diacu ... 23
Tabel II. Formula yang digunakan ... 23
Tabel III. Sistem klasifikasi untuk reaksi kulit ... 30
Tabel IV. Interpretasi nilai Primary Irritation Index (PPI) ... 30
Tabel V. Hasil uji kualitatif tanin ... 31
Tabel VI. Hasil uji organoleptis dan pH ... 34
Tabel VII. Sifat fisis dan stabilitas gel antioksidan ekstrak daun jambu biji (Psidium guajava L.) ... 35
Tabel VIII. Hasil scanning panjang gelombang maksimum asam tanat ... 42
Tabel IX. Kurva baku asam tanat ... 43
Tabel X. Hasil %CV kurva baku asam tanat ... 44
Tabel XI. Kadar tanin dalam ekstrak daun jambu biji ... 44
Tabel XII. Kadar tanin dalam gel antioksidan ekstrak daun jambu biji (Psidium guajava L.) ... 45
xvi
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kulit ... 7
Gambar 2. Daun jambu biji (Psidium guajava L.) ... 10
Gambar 3. Unit monomer asam akrilat dalam polimer carbopol ... 12
Gambar 4. Struktur gliserin ... 13
Gambar 5. Struktur propilen glikol ... 13
Gambar 6. Struktur trietanolamin ... 14
Gambar 7. Struktur metil paraben ... 14
xvii
Lampiran 4. Pengujian Sifat Fisis dan Stabilitas Gel Antioksidan
Ekstrak Daun Jambu Biji (Psidium guajava L.) ... 61
Lampiran 5. Pengaruh Konsentrasi Gliserin Terhadap Viskositas Gel
Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava
L.) ... 64
Lampiran 6. Pengaruh Konsentrasi Gliserin Terhadap Pergeseran
Viskositas Gel Antioksidan Ekstrak Daun Jambu Biji
(Psidium guajava L.) ... 76
Lampiran 7. Pengaruh Konsentrasi Gliserin Terhadap Daya Sebar Gel
Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava
L.) ... 78
Lampiran 8. Uji Iritasi Primer Gel Antioksidan Ekstrak Daun Jambu Biji
(Psidium guajava L.) ... 84
Lampiran 9. Optimasi Penetapan Kadar Tanin dalam Ekstrak dan
dalam Gel Ekstrak Daun Jambu Biji (Psidium guajava L.) ... 85
Lampiran 10. Kadar Tanin dalam Ekstrak Daun Jambu Biji (Psidium
xviii
Lampiran 11. Kadar Tanin dalam Ekstrak Cair Daun Jambu Biji (Psidium
guajava L.) ... 92
Lampiran 12. Pengaruh Konsentrasi Gliserin Terhadap Kadar Tanin
dalam Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium
guajava L.) ... 93
Lampiran 13. Pengaruh Konsentrasi Gliserin Terhadap Perubahan Kadar
Tanin dalam Gel Antioksidan Ekstrak Daun Jambu Biji
(Psidium guajava L.) ... 105
xix
INTISARI
Penuaan dini merupakan permasalahan yang sering dihadapi wanita, terutama pada kalangan manusia usia produktif dan penyebab terjadinya penuaan dini adalah radikal bebas. Antioksidan digunakan untuk menangkap radikal bebas. Salah satu tanaman yang mempunyai aktivitas antioksidan yaitu daun jambu biji yang akan diformulasikan dalam bentuk gel. Penelitian ini bertujuan untuk mengetahui pengaruh peningkatan gliserin sebagai humectant terhadap sifat fisis dan stabilitas gel antioksidan ekstrak daun jambu biji (Psidium guajava L.).
Penelitian ini merupakan rancangan eksperimental murni. Gel antioksidan ekstrak daun jambu biji dibuat sebanyak 4 formula dengan konsentrasi gliserin 0%, 7,5%, 15%, dan 30%. Sifat fisis dilihat berdasarkan viskositas dan daya sebar. Stabilitas sediaan dilihat dari pergeseran viskositas dan perubahan kadar tanin. Analisis data menggunakan software R.3.1.0 untuk melihat signifikansi perbedaan dari data yang diperoleh.
Hasil penelitian menunjukkan peningkatan konsentrasi gliserin memberikan pengaruh terhadap viskositas dan daya sebar, serta tidak memberikan pengaruh terhadap stabilitas gel antioksidan ekstrak daun jambu biji (Psidium
guajava L.) selama empat minggu penyimpanan.
xx
ABSTRACT
Premature aging is a problem often faced by women, especially in their productive age. Premature aging is caused by free radical. Antioxidants are used to free radicals scavenging. One of the plants that has antioxidant activity is guava leaves, that will be formulated in gel form. The aim of this study was to determine the effect of the increase of glycerin concentration as humectant to physical properties and the stability of antioxidant gel guava leaves (Psidium guajava L.) extract.
The design of this study was purely experimental. Antioxidant gel guava leaves extract gel was made in 4 formulas with the glycerin concentration of 0%, 7,5%, 15%, and 30%. Physical properties of gel could be determined by its viscosity and spreadibility. The gel stability could be determined by the viscosity shift and the changes of tanin level. The data were analyzed by using R.3.1.0 software to determine the significance of the difference of the obtained data.
The result of this study showed the increase of glycerin concentration affect on the viscosity and spreadibility, but it didn’t affect on the stability of antioxidant gel guava leaves (Psidium guajava L.) extract.
1
BAB I PENGANTAR
A. Latar Belakang
Penuaan dini merupakan proses penuaan pada kulit yang lebih cepat dari
seharusnya, di mana penuaan dini menjadi permasalahan yang sering dihadapi
wanita, terutama pada kalangan wanita usia produktif. Penuaan dini ditandai
dengan kondisi kulit yang kering, kasar, bersisik disertai dengan keriput dan noda
hitam atau flek. Salah satu faktor penyebab terjadinya penuaan dini adalah adanya
radikal bebas (Swastika, Mufrod, dan Purwanto, 2013). Makanan instan, asap
rokok, pejanan UV, sinar elektromagnetik, radiasi rendah, polusi udara dari asap
kendaraan bermotor, dan obat-obat tertentu merupakan sumber pembentuk radikal
bebas (Jain, Kataria, dan Guruprasad, 2004).
Antioksidan digunakan untuk menangkap radikal bebas (Taurino,
Daneida, Anna, Sonia, Vanessa, Montserrat, et al, 2008). Antioksidan mampu
menghambat reaksi berantai radikal bebas dalam tubuh dengan cara
mendonasikan satu atau lebih elektronnya kepada senyawa oksidan untuk diubah
menjadi senyawa yang stabil (Kikuzaki, Hisamoto, Hirose, Akiyama, dan
Taniguchi, 2002). Sediaan kosmetik yang memiliki aktivitas antioksidan dapat
digunakan untuk mencegah dan memperbaiki dampak penuaan dini pada kulit
(Ardhie, 2011).
Daun jambu biji mengandung beberapa metabolit sekunder hasil dari
skrining fitokimia, salah satunya tanin. Tanin merupakan komponen utama dalam
astringen, antibakteri, antidiare, dan antioksidan (Desmiaty, Ratih, Dewi, dan
Agustin, 2008; Yuliani, Udarno, dan Hayani, 2003). Menurut Qian dan
Nihorimberre (2004) daun jambu biji menunjukkan potensi sebagai antioksidan
dengan menghambat dan mencegah terjadinya oksidasi, sedangkan pada
penelitian yang dilakukan Rusdiana, Boesro, dan Ade (2007), ekstrak daun jambu
biji (Psidium guajava L.) memiliki aktivitas antioksidan tergolong kuat dengan
IC50 sebesar 7,2 mg/100 mL. Berdasarkan hal tersebut, maka dalam upaya
pemanfaatan daun jambu biji (Psidium guajava L.) yang memiliki aktivitas
antioksidan akan diformulasikan dalam bentuk sediaan topikal semisolid.
Gel merupakan sediaan semisolid yang tersusun dari suatu suspensi
partikel organik dan partikel anorganik yang terpenetrasi oleh cairan (Ansel,
2005). Sediaan gel sering digunakan untuk berbagai macam sistem penghantaran
sediaan farmasi serta mengakomodasikan zat aktif yang digunakan. Sediaan gel
juga memiliki beberapa keuntungan seperti mudah mengering, memberi sensasi
dingin pada kulit karena mengandung banyak air, residu yang tidak meninggalkan
rasa lengket setelah pengaplikasian, absorpsi pada kulit lebih baik daripada krim
(Garg, Aggarwal, Garg, dan Singla, 2002; Voigt, 1994; Yahendri, 2012). Sediaan
gel dipilih karena memiliki daya penetrasi yang tinggi ke dalam kulit sehingga
dapat mencegah penuaan dini pada kulit (Allen, 2002).
Humectant merupakan salah satu faktor yang sangat berpengaruh
terhadap sifat fisis dan stabilitas sediaan gel. Humectant berfungsi menjaga
kestabilan sediaan gel dengan menarik air dari lingkungan dan menjaga
humectant, di mana berasal dari lemak tumbuhan, sehingga aman digunakan pada
sediaan topikal. Gliserin digunakan sebagai humectantdengan konsentrasi ≤ 30%,
gliserin memiliki sifat higroskopis dan kental sehingga dapat mempengaruhi sifat
fisis dari sediaan (Rawling, Harding, Watkinson, Chandar dan Scott, 2002), maka
pada penelitian ini dilakukan variasi konsentrasi gliserin untuk melihat pengaruh
gliserin sebagai humectant terhadap sifat fisis dan stabilitas gel antioksidan
ekstrak daun jambu biji (Psidium guajava L.).
1. Perumusan masalah
Apakah peningkatan konsentrasi gliserin sebagai humectant berpengaruh
terhadap sifat fisis dan stabilitas gel antioksidan ekstrak daun jambu biji (Psidium
guajava L.) selama 4 minggu penyimpanan ?
2. Keaslian penelitian
Sejauh penelusuran pustaka penulis, penelitian tentang “Pembuatan dan
Evaluasi Sediaan Topikal Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.) dengan Gliserin sebagai Humectant” belum pernah dilakukan. Adapun penelitian yang terkait adalah “Formulasi Gel Antioksidan dari Ekstrak Daun Jambu Biji (Psidium guajava L.) dengan Menggunakan Aquapec HV-505” yang dilakukan oleh Rusdiana dkk., (2007) dengan melakukan variasi ekstrak daun jambu biji dan propilen glikol sebagai enchancer.
Selain itu pada penelitian yang dilakukan Sukmawati, Arisanti, dan Wijayanti
PVA, HPMC, dan gliserin secara signifikan mempengaruhi sifat fisika seperti
viskositas dan daya sebar, sedangkan variasi konsentrasi gliserin secara signifikan
mempengaruhi waktu mengering dari sediaan.
Penelitian yang dilakukan oleh Fachry, Arief, dan Guntur (2012)
:“Kondisi Optimal Proses Ekstraksi Tanin dari Daun Jambu Biji
Menggunakan Pelarut Etanol”, hasil penelitian diperoleh kondisi optimal proses ekstraksi tanin dari daun jambu biji dengan menggunakan etanol 96% pada
temperatur 50 0C selama waktu ekstraksi 150 menit.
3. Manfaat penelitian
a. Manfaat teoritis
Memberikan wawasan pengetahuan mengenai penggunaan gliserin
sebagai humectant dalam gel antioksidan ekstrak daun jambu biji
(Psidium guajava L.).
b. Manfaat praktis
Memberikan gambaran mengenai pengaruh peningkatan konsentrasi
gliserin sebagai humectant terhadap sifat fisis dan stabilitas gel
antioksidan ekstrak daun jambu biji (Psidium guajava L.). Penelitian ini
B. Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui pengaruh peningkatan
konsentrasi gliserin sebagai humectant terhadap sifat fisis (viskositas dan daya
sebar) dan stabilitas (pergeseran viskositas dan perubahan kadar tanin) gel
6
BAB II
PENELAAHAN PUSTAKA
A. Antioksidan
Antioksidan merupakan senyawa yang melengkapi kekurangan elektron
yang dimiliki radikal bebas, sehingga reaksi berantai dari pembentukan radikal
bebas dapat dihambat (Winarsi, 2007). Selain itu, antioksidan juga dapat
memperlambat atau mencegah proses oksidasi di dalam tubuh (Quezada, Asencio,
Valle, dan Aguilera, 2004). Antioksidan diperlukan tubuh untuk menetralisir
radikal bebas sehingga mampu melindungi tubuh dari kerusakan stres oksidatif
dan menghambat terjadinya penyakit degeneratif. Secara alami, antioksidan
terdapat dalam tubuh dan dapat mengatasi efek radikal bebas. Tetapi jika jumlah
radikal bebas dalam tubuh terlalu banyak, maka diperlukan antioksidan yang
berasal dari luar tubuh (eksogen) untuk mengatasi kekurangan antioksidan
endogen tersebut (Kikuzaki et al., 2002; Sibuea, 2003).
Antioksidan berdasarkan sumber dibagi menjadi dua jenis, yaitu
antioksidan alami dan antioksidan sintetik. Antioksidan alami (vitamin C,
flavonoid, polifenol, dan lain-lain) biasanya dapat diperoleh dari tumbuhan level
tinggi seperti buah-buahan, sayuran, dan teh (Sing, 2007). Antioksidan alami
tersebar di beberapa bagian tanaman seperti pada bagian kayu, kulit kayu, akar,
daun, bunga, biji, buah, dan serbuk sari (Sarastani, Suwarna, Apriyanto, 2002).
Sedangkan antioksidan sintetik (BHT, BHA, propil galat, butil-hidroksitoluen)
Uguz, Oktay, Beydemir, dan Kufrevioglu, 2004). Antioksidan alami menjadi
alternatif yang sangat dibutuhkan karena adanya kekhawatiran antioksidan sintetik
dapat menimbulkan toksisitas pada tubuh (Sunarni, 2005).
Antioksidan topikal digunakan untuk mencegah penuaan dan mediasi
kerusakan kulit oleh sinar UV. Antioksidan topikal harus dapat diabsorpsi ke
dalam kulit dan dihantarkan ke tempat aksi dalam bentuk aktif. Absorpsi dapat
dipengaruhi oleh beberapa faktor, yaitu kelarutan dalam air atau lemak, bentuk
molekul dalam komponen sediaan, pH, dan pembawa yang digunakan dalam
sediaan (Weisberg, 2002).
B. Kulit
Gambar 1. Struktur kulit (Brown dan Tony, 2002)
Kulit merupakan organ terluas yang terletak paling luar dan menutupi
seluruh permukaan tubuh, di mana di setiap bagian yang berbeda dari kulit
memiliki kekakuan yang bervariasi. Telapak kaki dan telapak tangan serta
sela-sela jari merupakan daerah yang paling kaku dan tebal. Struktur sel-sel pada kulit
wajah bersifat sangat tipis, sehingga memungkinkan sediaan kosmetik dapat
Kulit memiliki beberapa fungsi, dan fungsi utama kulit adalah sebagai
pengatur suhu tubuh dan sirkulasi kelembaban, serta sintesis vitamin B dan D
(Allen, 2002). Fungsi lain dari kulit sebagai pelindung tubuh dari pengaruh luar
baik secara fisik maupun imunologik. Selain itu kulit juga berperan penting dalam
interaksi antar individu dengan lingkungan, di mana kulit merupakan indera yang
sensitif terhadap sentuhan dan terkadang membuat perasaan emosional (Rawling
et al., 2002).
Kulit terdiri dari tiga lapisan utama, yaitu :
1. Epidermis
Epidermis merupakan lapisan dari kulit yang paling luar yang terdiri dari
banyak lapisan sel keratinosit yang aktif melakukan regenerasi dan menarik untuk
diperhatikan dalam perawatan kulit (Dwikarya, 2006). Lapisan epidermis tersusun
atas stratum corneum, stratum lucidum, stratum granulosum, stratum spinosum,
dan stratum germinativum. Lapisan epidermis berfungsi sebagai proteksi barier,
sintesis vitamin D dan sitokin, pigmentasi, pembelahan dan mobilisasi sel
(Baumann dan Saghari, 2009).
2. Dermis
Lapisan dermis merupakan lapisan yang terletak di bawah lapisan
epidermis dan jauh lebih tebal daripada lapisan epidermis (Djuanda, Hamzah, dan
Aisah, 2003). Tersusun atas serabut kolagen dan elastin yang menentukan
elastisitas kulit (Dwikarya, 2006). Di dalam lapisan dermis terdapat
keringat, saluran keringat, ujung pembuluh darah dan ujung saraf (Tranggono dan
Fatma, 2007).
3. Hipodermis
Terdiri dari jaringan ikat longgar yang berisi sel-sel lemak di dalamnya
berfungsi sebagai cadangan makanan (Djuanda dkk., 2003). Lapisan hipodermis
sendiri berfungsi menunjang suplai darah ke lapisan dermis untuk regenerasi,
sebagai bantalan atau penyangga benturan bagi organ-organ tubuh bagian dalam.
Lapisan ini terdapat ujung-ujung saraf tepi, pembuluh darah, dan getah bening
(Baumann et al., 2002).
C. Daun Jambu Biji
1. Klasifikasi tanaman
Klasifikasi tanaman jambu biji adalah sebagai berikut :
Kingdom : Plantae
Sub Kingdom : Tracheobionta
Divisi : Spermatophyta
Sub Divisi : Magnoliophyta
2. Morfologi tanaman
Morfologi dari daun jambu biji seperti berikut berbentuk bundar telur
agak menjorong atau agak bundar sampai meruncing, pangkal membulat, tepi
rata, berhadapan, bertulang menyirip, berbintik, mempunyai warna daun hijau
kekuningan ataupun hijau, panjang helai daun 6 cm sampai 14 cm, dan lebar daun
3 cm sampai 6 cm, panjang tangkai 3 mm sampai 7 mm, daun yang muda berbulu
sedangkan daun yang tua permukaan atasnya menjadi licin (Syamsuhidayat dan
Hutapea, 1991).
Gambar 2. Daun jambu biji (Psidium guajava L.) (Rahman, 2009).
3. Kandungan kimia
Daun jambu biji mengandung beberapa metabolit sekunder hasil dari
skrining fitokimia seperti tanin, polifenolat, flavanoid, monoterpenoid
siskuiterpen, alkaloid, kuinon, sapoin, kuarsetin, guayaverin, minyak atsiri, asam
malat, asam ursolat, dan asam oksalat (Sudarsono, Wahyuono, Donatus, dan
Purnomo, 2002 ; Rusdiana, dkk., 2007). Komponen utama dari daun jambu biji
yaitu tanin, di mana besarnya mencapai 9-12% (Yuliani dkk., 2003). Tanin
memiliki beberapa aktivitas seperti astringen, antibakteri, antidiare dan
4. Kajian farmakologis
Menurut beberapa penelitian yang telah dilakukan, daun jambu biji telah
terbukti memiliki beberapa efek farmakologis, seperti antiinflamasi (Ojewole,
2006), antibakteri (Arima dan Danno, 2002; Rattanachaikunsopon dan
Phumkhachorn, 2007; Kamal, Rahul, Kumar, dan Lakshmi, 2008; Qadan,
Thewaini, Ali, Afifi, Elkhawad, dan Matalka, 2005), antidiabetes (Kamal et al.,
2008), antihipertensi (Ojewole, 2005), antioksidan (Qian dan Nihorimbere, 2004;
Chen dan Yen, 2007; Kamal et al., 2008), hepatoprotektif (Kamal et al., 2008).
Ekstrak daun jambu biji memiliki aktivitas antioksidan dengan nilai IC50 sebesar
7,2 mg/100mL (Rusdiana dkk, 2007).
D. Gel
Gel merupakan sediaan semisolid yang tersusun dari suatu suspensi
partikel organik dan anorganik yang saling berikatan dan terpenetrasi oleh cairan
(Ansel, 2005). Untuk membuat sediaan gel, biasanya diperlukan beberapa
komponen seperti bahan pengembang, pelarut, penahan lembab, dan pengawet
(Barel, Paye, dan Maibach, 2001). Gel dikelompokkan dalam dua fase yaitu fase
tunggal dan fase ganda. Gel fase tunggal terdiri dari partikel organik yang tersebar
dalam suatu cairan sehingga tidak terlihat adanya ikatan antara molekul besar
yang terdispersi dan cairan, sedangkan gel fase ganda terdiri dari jaringan partikel
yang terpisah (Yanhendri, 2012).
Syarat sediaan gel dalam penggunaan dermatologi sebagai berikut
tiksotropik, mempunyai daya sebar yang baik, mudah dibersihkan, kompatibel
(Mohamed, 2004; Meenakshi, 2013). Bentuk sediaan gel memiliki beberapa
keuntungan di antaranya residu yang tidak meninggalkan rasa lengket setelah
diaplikasikan, gel akan segera mencair jika terjadi kontak dengan kulit dan
membentuk lapisan film yang mudah dicuci, bening, mudah mengering, absorpsi
pada kulit lebih baik daripada krim (Garg et al., 2002; Voigt, 1994; Yanhendri,
2012).
E. Bahan- Bahan yang Digunakan dalam Formulasi Gel
1. Carbopol
Pemerian dari carbopol adalah serbuk putih, higroskopis, asam, dan
sedikit berbau khas. Carbopol dalam formulasi sediaan semisolid digunakan
sebagai rheology modifier, serta dapat digunakan sebagai material bioadhesive,
controlled release agent, emulsifying agent, agen stabilitas, agen pensuspensi
(Rowe, Sheskey, dan Quinn, 2009).
Gambar 3. Unit monomer asam akrilat dalam polimer carbopol (Rowe et al., 2009)
Carbopol merupakan polimer sintesis dari asam akrilat (CH=COOH)
memiliki berat molekul tinggi dari ikatan silang asam akrilat dengan alil sukrosa
atau alil eter pentaerythritol. Carbopol mengandung 56-68% gugus asam
karboksilat, berat molekul secara teoritis diperkirakan antara 7x105 sampai 4x109,
memiliki kekentalan 40.000-60.000 cP, kejernihan sangat baik, serta efisiensi
2. Gliserin
Gliserin merupakan cairan jernih, kental, tidak berbau, tidak berwarna,
berasa manis, dan bersifat higroskopis. Gliserin memiliki bobot molekul 92,09
dan rumus empirik C3H8O3. Beberapa fungsi dari gliserin yaitu pengawet,
co-solvent, humectant, pelarut, emolien, penetration enhancer, dan bahan
pengisotonis. Gliserin stabil pada tekanan dan suhu yang normal. Campuran
gliserin dengan air, etanol 95%, dan propilen glikol secara kimiawi stabil. Gliserin
dalam sediaan topikal digunakan sebagai humectant yang dapat melembabkan
kulit dengan konsentrasi penggunaan gliserin kurang dari 30% (Vikas, Saini,
Singh, Rana dan Joshi, 2011; Rowe, et al., 2009).
Gambar 4. Struktur gliserin (Rowe et al., 2009)
3. Propilen glikol
Gambar 5. Struktur propilen glikol (Rowe et al., 2009)
Propilen glikol memiliki sifat jernih, tidak berwarna, manis, rasa khas,
praktis tidak berbau, kental, menyerap air pada udara lembab. Propilen glikol
dapat digunakan antara lain sebagai humectant, pelarut, kosolven larut air,
penstabil vitamin, pengawet dalam sediaan parenteral dan non parenteral (Rowe et
4. Trietanolamin
Trietanolamin memiliki sifat cairan kental jernih, memiliki sedikit bau
amonia, tidak berwarna sampai berwarna kuning pucat, sangat higroskopis,
memiliki pH 10,5 dalam 0,1 N larutan. Trietanolamin digunakan sebagai agen
pembasa terutama dalam sediaan topikal (Rowe et al., 2009). Trietanolamin
bersifat basa maka dapat digunakan untuk menetralisasi carbopol, di mana tidak
menimbulkan ancaman netralisasi berlebihan hingga berujung hilangnya
viskositas (Osborne dan Amann, 1990).
Gambar 6. Struktur trietanolamin (Rowe et al., 2009)
5. Metil paraben
Nama kimia dari metil paraben adalah methyl-4-hydroxybenzoate. Metil
paraben berbentuk kristal, tidak berbau, memiliki rasa sedikit terbakar, dan
berwarna putih. Konsentrasi penggunaan yang umum digunakan dalam sediaan
topikal yaitu 0,02 - 0,3%. Metil paraben larut dalam air panas 800C (1:30), eter
(1:10), metanol, dan etanol 95%. Metil paraben digunakan sebagai antimikroba
dalam kosmetik, formulasi farmasetika, dan produk makanan (Rowe et al, 2009).
Metil paraben merupakan paraben paling kecil aktivitasnya, memiliki
aktivitas antimikroba pada pH 4-8, di mana aktivitas antimikroba dari metil
paraben akan meningkat dengan peningkatan panjang rantai alkil. Selain itu
dengan menggunakan kombinasi paraben dapat meningkatkan aktivitas
antimikroba dari metil paraben (Rowe et al., 2009).
6. Aquadest
Aquadest merupakan cairan jernih, tidak berbau, tidak berwarna, tidak
mempunyai rasa dan memiliki pH 5-7. Rumus kimia dari aquadest adalah H2O
dengan berat molekul sebesar 18.02. Aquadest dibuat dengan menyuling air yang
memenuhi persyaratan dan tidak mengandung zat tambahan lain. Fungsi dari
aquadest sebagai pelarut (Direktorat Jendral Pengawasan Obat dan Makanan RI,
1995).
F. Sifat Fisis dan Stabilitas Gel
1. Viskositas
Viskositas adalah suatu ukuran tahanan suatu cairan untuk mengalir, di
mana semakin tinggi viskositas, semakin besar pula tahanannya, sehingga
semakin besar energi yang dibutuhkan untuk membuat cairan tersebut mengalir
pada kecepatan tertentu (Sinko, 2006). Peningkatan viskositas akan menurunkan
daya sebar dan menaikkan waktu retensi pada tempat aksi. Viskositas merupakan
salah satu parameter penting pada sediaan semisolid, karena menentukan lama
tinggal sediaan di kulit, sehingga obat dapat dihantarkan dengan baik. Pengukuran
viskositas menjadi tahap penting yang harus dilakukan untuk mengetahui sifat alir
diaplikasikan dengan baik. Pengujian viskositas dapat diukur dengan
menggunakan berbagai jenis viskometer berdasarkan kebutuhan formulator (Garg
et al., 2002 ; Herh, Tkachul, Wu, Bernzen dan Rudolph, 1998).
2. Daya sebar
Daya sebar adalah kemampuan dari suatu sediaan untuk menyebar di
tempat aplikasi di mana sediaan tersebut diaplikasikan pada daerah tertentu. Daya
sebar merupakan aspek yang bertanggung jawab terhadap penerimaan konsumen
dalam penggunaan suatu sediaan, untuk menghantarkan dosis obat yang tepat
pada tempat target, serta kemudahan untuk pengaplikasian dan dikeluarkan dari
kemasan. Faktor-faktor yang mempengaruhi daya sebar dari suatu sediaan antara
lain : rigiditas, suhu pada tempat aksi, viskositas, laju penguapan pelarut, dan
lama tekanan. Daya sebar dan viskositas memiliki hubungan yang bertolak
belakang, di mana viskositas meningkat akan menurunkan daya sebar dan
begitupun sebaliknya (Garg, et al., 2002).
Metode pelat sejajar (parallel-plate method) merupakan metode yang
sering digunakan dalam penentuan dan pengukuran daya sebar pada sediaan
semisolid. Keuntungan dari metode ini adalah sederhana, tidak memerlukan
banyak biaya, mudah untuk dilakukan. Namun di sisi lain, metode ini juga
memiliki kerugian seperti kurang presisi, sensitif dan data yang didapat harus
3. Pergeseran viskositas
Perubahan viskositas selama penyimpanan menjadi perhatian utama,
karena viskositas mempengaruhi stabilitas dan karakteristik dari suatu sediaan.
Beberapa faktor yang mempengaruhi perubahan viskositas antara lain agregasi
partikel yang tidak tergantung pada kandungan polimer, meskipun polimer dapat
mengurangi kecepatan perubahan ukuran partikel, dan bahan-bahan yang dapat
meningkatkan viskositas atau interaksi bahan tersebut dengan sistem dispersi
(Zatz dan Kushla, 1996).
G. Landasan Teori
Penuaan dini dapat disebabkan oleh radikal bebas yang berasal baik dari
luar maupun dalam tubuh. Antioksidan digunakan untuk menangkap radikal
bebas. Salah satu tanaman yang mempunyai aktivitas antioksidan yaitu daun
jambu biji. Menurut Qian dan Nihorimberre (2004) daun jambu biji menunjukkan
potensi aktivitas sebagai antioksidan dengan menghambat dan mencegah terjadi
oksidasi, sedangkan pada penelitian Rusdiana dkk., (2007) ekstrak daun jambu
biji (Psidium guajava L.) memiliki aktivitas antioksidan tergolong kuat dengan
IC50 sebesar 7.2 mg/100 mL.
Gel merupakan sediaan semisolid yang tersusun dari suatu suspensi
partikel organik dan partikel anorganik yang terpenetrasi dalam cairan. Sediaan
gel memiliki beberapa keuntungan seperti mudah mengering, memberi sensasi
dingin pada kulit karena mengandung banyak air, residu yang tidak meninggalkan
rasa lengket setelah pengaplikasian, absorpsi pada kulit lebih baik daripada krim,
memiliki daya penetrasi tinggi ke dalam kulit sehingga dapat mencegah penuaan
dini.
Formulasi sediaan gel terdapat humectant sebagai salah satu komponen
penyusun dari sediaan gel, selain bahan pengembang, pengawet, dan pelarut.
Humectant merupakan salah satu faktor yang berpengaruh terhadap sifat fisis dan
stabilitas sediaan gel. Humectant berfungsi menjaga kestabilan dari sediaan
dengan menarik air dari lingkungan. Gliserin dapat digunakan sebagai humectant
dengan konsentrasi ≤ 30%. Selain sebagai humectant, gliserin juga dapat
digunakan sebagai emolien, penetration enchancer, co-solvent, dan bahan
pengisotonis. Pada penelitian ini digunakan gliserin sebagai humectant dengan
variasi konsentrasi untuk mengetahui pengaruhnya terhadap sifat fisis dan
stabilitas gel antioksidan ekstrak daun jambu biji (Psidium guajava L.) selama 4
minggu penyimpanan.
Pengaruh peningkatan konsentrasi gliserin terhadap sifat fisis dan
stabilitas gel antioksidan ekstrak daun jambu biji (Psidium guajava L.) dianalisis
statistik menggunakan software R 3.1.0. Sifat fisis dilihat dari daya sebar dan
viskositas. Sedangkan stabilitas dilihat dari pergeseran viskositas dan perubahan
H. Hipotesis
Peningkatan konsentrasi gliserin sebagai humectant memberikan
pengaruh terhadap sifat fisis dan stabilitas gel antioksidan ekstrak daun jambu biji
20
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Penelitian yang dilakukan termasuk jenis penelitian eksperimental murni.
B. Variabel Penelitian
1. Variabel bebas pada penelitian ini adalah penggunaan gliserin sebagai
humectant dalam formula gel antioksidan ekstrak daun jambu biji (Psidium
guajava L.) dengan konsentrasi 0%, 7,5%, 15%, dan 30%.
2. Variabel tergantung pada penelitian ini adalah sifat fisis (organoleptis, pH,
daya sebar dan viskositas) dan stabilitas (pergeseran viskositas dan perubahan
kadar tanin) gel antioksidan ekstrak daun jambu biji (Psidium guajava L.)
setelah 4 minggu penyimpanan, dan uji iritasi.
3. Variabel pengacau terkendali pada penelitian ini adalah alat dan bahan yang
digunakan, lama pengadukan, kecepatan pengadukan, prosedur pembuatan
dan pengujian, lama penyimpanan, kondisi penyimpanan.
4. Variabel pengacau tak terkendali pada penelitian ini adalah suhu dan
kelembaban udara ruangan selama pembuatan dan pengujian, suhu
penyimpanan gel antioksidan ekstrak daun jambu biji (Psidium guajava L.),
serta subyektifitas penulis dalam pengamatan reaksi iritasi hewan uji.
C. Definisi Operasional
1. Gel antioksidan ekstrak daun jambu biji (Psidium guajava L.) adalah sediaan
humectant yang sesuai dengan formula dan prosedur pembuatan penelitian
ini.
2. Ekstrak daun jambu biji adalah ekstrak kering hasil dari daun jambu biji yang
diperoleh dari PT. Industri Jamu Borobudur Semarang.
3. Ekstrak cair adalah ekstrak yang digunakan pada penelitian ini didapat dari 20
gram ekstrak daun jambu biji yang didispersikan dalam 100 mL etanol yang
dipanaskan selama 150 menit pada suhu 500C, kemudian disaring
menggunakan corong Buchner dengan bantuan pompa vakum.
4. Humectant adalah salah satu faktor yang mempengaruhi sifat fisis dan
stabilitas dari sediaan gel antioksidan ekstrak daun jambu biji (Psidium
guajava L.). Humectant yang digunakan pada penelitian ini adalah gliserin.
5. Sifat fisis adalah parameter yang digunakan untuk mengetahui kualitas dari
gel antioksidan ekstrak daun jambu bijimeliputi daya sebar dan viskositas.
6. Stabilitas gel ditentukan dari besarnya nilai pergeseran viskositas dari 48 jam
setelah pembuatan dan 4 minggu penyimpanan yaitu kurang dari 10%, serta
perubahan kadar tanin selama 4 minggu penyimpanan.
7. Kadar tanin adalah presentase kadar dalam ekstrak dan gel antioksidan
ekstrak daun jambu biji (Psidium guajava L.).
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah ekstrak daun jambu
biji yang diperoleh dari PT. Industri Jamu Borobudur Semarang (Lampiran 1),
carbopol 940 (kualitas farmasetis), propilen glikol (kualitas farmasetis), gliserin
(Farmasi Sanata Dharma), etil asetat (kualitas teknis), natrium karbonat (Merck),
asam tanat (Merck), asam fosfomolibdat (Merck), natrium wolframat (Merck),
asam fosfat (Merck), gelatin (Merck), asam klorida (kualitas teknis), natrium
klorida (Merck), reagen FeCl3, dan kelinci.
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah alat-alat gelas
(Pyrex-Germany), timbangan analitik (Mettler Toledo), spektrofotometer UV-Vis
OPTIMA SP-3000 plus, sonikator, waterbath (Tamson Zoetermeer- Holand 1985
0023), viskometer seri VT 04 (Rion-Japan), alat pengukur daya sebar, hot plate
magnetic stirer, mixer (Miyako), pH universalstick,, corong pisah, pipet volume,
glassfirn, pompa vakum, corong Buchner, dan alat pengukur bulu kelinci.
F. Tata Cara Penelitian
1. Identifikasi Ekstrak Daun Jambu Biji (Psidium guajava L.)
Ekstrak daun jambu biji diperoleh dari PT. Industri Jamu Borobudur
Semarang dan telah diuji identitasnya, dibuktikan dengan Certificate of
Analysis.
2. Identifikasi Tanin dalam Ekstrak Daun Jambu Biji (Psidium guajava L.)
Secara Kualitatif
Ekstrak daun jambu biji ditambah dengan gelatin dan FeCl3.
Penambahan gelatin jika positif tanin terdapat endapan putih, sedangkan
penambahan FeCl3 jika positif tanin terbentuk kompleks berwarna hitam
3. Pembuatan Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.)
a. Formula
Formula yang digunakan mengacu pada International Journals
of Pharmaceutical Compounding dengan judul Gel Compounding dalam
Maheswara (2010). Formula yang digunakan adalah sebagai berikut :
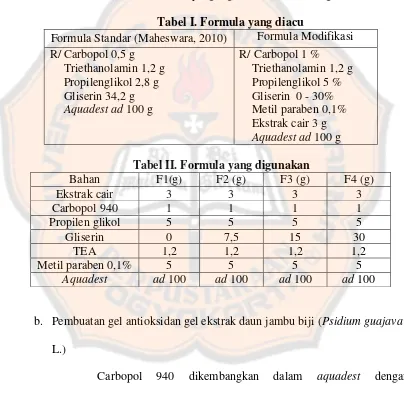
Tabel I. Formula yang diacu
Formula Standar (Maheswara, 2010) Formula Modifikasi R/ Carbopol 0,5 g
Tabel II. Formula yang digunakan
Bahan F1(g) F2 (g) F3 (g) F4 (g)
b. Pembuatan gel antioksidan gel ekstrak daun jambu biji (Psidium guajava
L.)
Carbopol 940 dikembangkan dalam aquadest dengan
menaburkan carbopol di atas aquadest (campuran 1). Pengembangan
dilakukan selama 24 jam. Dilarutkan ekstrak dengan propilen glikol,
kemudian diaduk dengan mixer sebentar baru ditambahkan gliserin
Setelah itu ditambahkan campuran (1) dan TEA ke dalam campuran (2)
diaduk dengan mixer selama 3 menit.
4. Uji Sifat Fisis Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava
L.)
a. Uji organoleptis dan pH
Uji organoleptis dilakukan dengan cara mengamati warna, bau
dan bentuk setelah 48 jam gel selesai dibuat. Pengujian pH dilakukan
dengan pH universal stick dengan cara memasukkan ke dalam gel dan
membandingkan warna dengan standar. Nilai pH yang diinginkan adalah
rentang pH 5-6, yaitu pH yang tidak mengiritasi kulit.
b. Uji daya sebar
Gel sebanyak 1 gram ditimbang, diletakkan di bagian tengah
kaca bulat berskala. Di atas gel diletakkan kaca bulat lainnya ditambahkan
dengan pemberat sehingga total berat di atas gel 125 gram, didiamkan
selama 1 menit dan dicatat diameter penyebarannya dari empat bagian
sisi. Pengujian daya sebar dilakukan setelah 48 jam gel selesai dibuat dan
dilakukan sebanyak 3 kali replikasi.
c. Uji viskositas
Uji viskositas dilakukan 48 jam setelah pembuatan dan 4
minggu penyimpanan, serta dilakukan sebanyak 3 kali replikasi.
Masing-masing formula gel ditentukan viskositasnya dengan menggunakan alat
gerakan jarum penunjuk viskositas, dan ukuran rotor yang digunakan
adalah skala dua.
5. Uji Iritasi Primer Draize Test
Uji iritasi primer yang dilakukan menggunakan metode Draize Test
dengan dua ekor kelinci. Cara : sejumlah 0,5 gram gel ekstrak daun jambu
biji dioleskan pada kulit punggung kelinci seluas 2,5 cm x 2,5 cm yang telah
dicukur, kemudian olesan tersebut ditutup dengan kasa steril. Pengamatan
dilakukan pada interval waktu 24 jam, 48 jam, dan 72 jam dengan
mengamati apakah terdapat eritema dan edema yang timbul setelah
pemaparan (Deveda, Jain, Vyas, Khambete, dan Jain, 2010).
6. Penetapan Kadar Tanin dalam Ekstrak dan dalam Gel Antioksidan Ekstrak
Daun Jambu Biji (Psidium guajava L.) Secara Spektrofotometri
Ultraviolet-Visibel
a. Larutan standar asam tanat
Sebanyak lebih kurang 5 mg asam tanat ditimbang dan
dilarutkan dengan aquabidestillata dalam labu ukur 50,0 mL sehingga
didapatkan konsentrasi sebesar 100 µg/mL. Larutan standar ini harus
selalu dibuat baru setiap kali akan melakukan pengujian.
b. Penetapan operating time (OT)
Tiga seri larutan baku asam tanat dibuat dari larutan standar
asam tanat 100 µg/mL dengan mengambil masing-masing sebanyak 5,0;
7,0; 9,0 mL dimasukkan ke dalam labu ukur 10,0 mL kemudian
didapatkan konsentrasi sebesar 50, 70, dan 90 µg/mL. Sebanyak 1,0 mL
dari masing-masing konsentrasi 50, 70, dan 90 µg/mL dimasukkan dalam
labu ukur 10,0 mL ditambahkan 1,0 mL larutan Na2CO3 jenuh dan 0,5 mL
pereaksi Folin denis, kemudian diencerkan dengan aquabidestillata
hingga tanda. Larutan dihomogenkan dan diukur serapannya
menggunakan spektrofotometer UV-Vis pada panjang gelombang 760 nm
selama 30 menit setiap 5 menit.
c. Penetapan panjang gelombang maksimum
Tiga seri larutan baku asam tanat dibuat dari larutan standar
asam tanat 100 µg/mL dengan mengambil masing-masing sebanyak 5,0;
7,0; 9,0 mL dimasukkan ke dalam labu ukur 10,0 mL kemudian
diencerkan dengan aquabidestillata hingga tanda batas sehingga
didapatkan konsentrasi sebesar 50, 70, dan 90 µg/mL. Sebanyak 1,0 mL
dari masing-masing konsentrasi 50, 70, dan 90 µg/mL, dimasukkan dalam
labu ukur 10,0 mL ditambahkan 1,0 mL larutan Na2CO3 jenuh dan 0,5 mL
pereaksi Folin denis, kemudian diencerkan dengan aquabidestillata
hingga tanda. Larutan dihomogenkan dan diukur serapan dengan
spektrofotometer UV-Vis pada panjang gelombang 600-800 nm setelah
operating time tercapai.
d. Pembuatan kurva baku asam tanat
Enam seri larutan baku asam tanat dibuat dari larutan standar
asam tanat 100 µg/mL dengan mengambil masing-masing sebanyak 4,0;
kemudian diencerkan dengan aquabidestillata hingga tanda batas
sehingga didapatkan konsentrasi sebesar 40, 50, 60, 70, 80, dan 90
µg/mL. Sebanyak 1,0 mL dari masing-masing seri larutan baku asam
tanat diambil dan dimasukkan dalam labu ukur 10,0 mL ditambahkan 1,0
mL larutan Na2CO3 jenuh dan 0,5 mL pereaksi Folin denis, kemudian
diencerkan dengan aquabidestillata hingga tanda. Larutan dihomogenkan
dan diukur serapannya pada panjang gelombang maksimum dan setelah
operating time tercapai.
e. Penetapan kadar tanin ekstrak daun jambu biji
Sebanyak lebih kurang 10 mg ekstrak daun jambu biji ditimbang
dan dilarutkan dengan aquabidestillata kemudian dimasukkan dalam labu
ukur 50,0 mL, diencerkan hingga tanda sehingga didapat konsentrasi 200
µg/mL. Larutan diultrasonikasi selama 15 menit. Sebanyak 1,0 mL
larutan ekstrak daun jambu biji dimasukkan dalam labu ukur 10,0 mL
ditambahkan 1,0 mL larutan Na2CO3 jenuh dan 0,5 mL pereaksi Folin
denis, kemudian diencerkan dengan aquabidestillata hingga tanda.
Larutan dihomogenkan dan diukur serapannya pada panjang gelombang
maksimum dan setelah operating time tercapai, kemudian direplikasi
sebanyak 3 kali. Dihitung dengan menggunakan persamaan kurva baku
yang didapat sehingga diketahui kadar tanin dari ekstrak daun jambu biji
f. Penetapan kadar tanin gel ekstrak daun jambu biji
Sebanyak lebih kurang 3 g gel ekstrak daun jambu biji
ditimbang dan dilarutkan dengan 5 mL HCl 1M, kemudian dimasukkan
dalam corong pisah. Etil asetat ditambahkan sebanyak 10 mL, digojog
sampai terbentuk dua fase. Fase etil asetat ditampung, fase air diekstraksi
lagi dengan ditambahkan etil asetat sebanyak 10 mL. Hasil fase etil asetat
yang pertama dan kedua digabung dimasukkan dalam corong pisah
ditambah NaCl 5% sebanyak 10 mL, dan digojog sampai terbentuk dua
fase, fase etil asetat ditampung. Fase etil asetat kemudian diuapkan
dengan waterbath untuk menghilangkan etil asetat. Ekstrak kering
dilarutkan dengan aquabidestillata dimasukkan ke dalam labu ukur 10,0
mL. Diencerkan dengan aquabidestillata hingga tanda.
Sebanyak 1,0 mL dimasukkan dalam labu ukur 10,0 mL
ditambahkan 1,0 mL larutan Na2CO3 jenuh dan 0,5 mL pereaksi Folin
denis, kemudian diencerkan dengan aquabidestillata hingga tanda.
Larutan dikocok dan diukur serapannya pada panjang gelombang
maksimum setelah operating time tercapai, kemudian direplikasi
sebanyak 3 kali untuk masing-masing formula. Dihitung dengan
persamaan kurva baku yang didapat sehingga diketahui kadar tanin dari
G. Analisis Hasil
Data yang diperoleh dalam penelitian ini adalah sifat fisis dan stabilitas
gel antioksidan ekstrak daun jambu biji dengan adanya peningkatan konsentrasi
gliserin. Data sifat fisis meliputi daya sebar dan viskositas 48 jam setelah
pembuatan, serta viskositas 4 minggu penyimpanan, sedangkan stabilitas berupa
pergeseran viskositas dan perubahan kadar tanin. Data yang diperoleh, selanjutnya
dianalisis menggunakan software R versi 3.1.0. untuk melihat signifikansi
perbedaan dari data yang diperoleh.
Uji normalitas menggunakan uji Shapiro-Wilk dilakukan untuk data daya
sebar 48 jam, viskositas 48 jam, viskositas 4 minggu penyimpanan, kadar tanin 48
jam, dan kadar tanin 4 minggu penyimpanan. Data dikatakan terdistribusi normal
apabila p-value > 0,05. Kemudian dilanjutkan dengan uji Levene’s Test, jika
-value > 0,05 maka data dikatakan memiliki kesamaan varians.
Untuk melihat pengaruh peningkatan konsentrasi gliserin terhadap sifat
fisis, dilakukan analisis statistik menggunakan ANAVA satu arah dengan taraf
kepercayaan 95%, dan dilanjutkan uji post hoc menggunakan uji T tidak
berpasangan untuk mengetahui signifikansi perbedaan sifat fisis dari 4 formula gel
antioksidan ekstrak daun jambu biji. Hasil uji post hoc menggunakan T tidak
berpasangan dikatakan data dua kelompok berbeda signifikan bila p-value < 0,05.
Untuk melihat pengaruh peningkatan konsentrasi gliserin terhadap stabilitas
sediaan (pergeseran viskositas dan perubahan kadar tanin), digunakan uji T
berpasangan. Data antar dua kelompok yang dibandingkan dikatakan berbeda
Selain data-data di atas, data iritasi primer dapat dijadikan data
pendukung dalam penelitian ini. Data iritasi primer didapatkan dengan
pengamatan secara visual, ditentukan terjadinya eritema dan edema diberi skor
menggunakan Tabel III dan Tabel IV digunakan untuk menunjukkan kriteria
iritasi menggunakan persamaan.
Tabel III. Sistem klasifikasi untuk reaksi kulit (Benson dan Watkinson, 2012)
Reaksi eritema Skor
Tidak ada eritema 0
Eritema yang sangat ringan (hampir tidak kelihatan) 1 Eritema yang dapat didefinisikan dengan baik atau cukup 2 Eritema sedang hingga berat 3 Eritema berat (beet redness) sampai pembentukan sedikit eschar
(luka mendalam)
4
Reaksi edema Skor
Tidak ada edema 0
Edema sangat ringan (hampir tidak kelihatan) 1 Erema ringan (area meluas dengan peningkatan tertentu) 2 Edema sedang (meluas >1mm) 3 Edema berat (meluas >1mm dan meluas sampai ke area di luar
paparan)
4
Total skor yang mungkin untuk iritasi primer 8
Indeks iritasi primer untuk sediaan juga dihitung dengan rumus sebagai berikut :
Indeks iritasi primer = Σ eritema 24,48,72 jam + Σ edema 24,48,72 jam
jumlah hewan uji
Tabel IV. Interpretasi nilai Primary Irritation Index (PII) (Benson dan Watkinson, 2012)
31
BAB IV
HASIL DAN PEMBAHASAN
A. Identifikasi Ekstrak Daun Jambu Biji (Psidium guajava L.)
Identifikasi bertujuan untuk memastikan kebenaran identitas ekstrak daun
jambu biji yang akan digunakan. Ekstrak daun jambu biji yang digunakan berasal
dari PT. Industri Jamu Borobudur Semarang yang telah melalui uji identifikasi
dan dibuktikan dengan Certificate of Analysis (CoA) (Lampiran 1). Ekstrak daun
jambu biji yang diperoleh berbentuk serbuk halus, berwarna coklat tua, bau
aromatik, dan rasa pahit. Ekstrak daun jambu biji menunjukkan kesesuaian
dengan Certificate of Analysis (CoA) (Lampiran 1), sehingga dapat disimpulkan
bahwa ekstrak daun jambu biji dari PT. Industri Jamu Borobudur Semarang
adalah benar ekstrak daun jambu biji.
B. Identifikasi Tanin dalam Ekstrak Daun Jambu Biji (Psidium guajava L.) Secara Kualitatif
Untuk mengetahui ada tidaknya kandungan tanin dalam ekstrak daun
jambu biji maka dilakukan secara kualitatif menggunakan gelatin dan FeCl3. Hasil
yang diperoleh menunjukkan adanya tanin pada sampel.
Tabel V. Hasil uji kualitatif tanin
Sampel Jenis Pereaksi Hasil + NaCl + gelatin + NaCl + FeCl3
Asam tanat Endapan putih Hitam kebiruan + Ekstrak daun jambu biji Endapan putih Hitam kebiruan +
Keterangan : + menunjukkan adanya tanin pada sampel
Menurut Robinson (1995) adanya endapan putih karena sifat tanin yang
32
berwarna hitam kebiruan karena gugus fenol dari struktur tanin berikatan dengan
FeCl3.
C. Pembuatan Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.)
Pada penelitian ini, daun jambu biji diformulasikan dalam sediaan gel
dengan variasi peningkatan konsentrasi gliserin untuk melihat pengaruhnya
terhadap sifat fisis dan stabilitas, yang meliputi viskositas dan daya sebar. Faktor
yang menjadi perhatian pada pembuatan gel antioksidan ekstrak daun jambu biji
ini adalah humectant yang digunakan, di mana humectant merupakan bagian yang
sangat berpengaruh terhadap kualitas fisis dari sediaan gel. Penelitian ini
menggunakan gliserin sebagai humectant. Humectant menjaga kestabilan gel
terutama saat penyimpanan dengan cara mengabsorbsi air dari lingkungan dan
penguapan air dari sediaan. Selain sebagai humectant, gliserin dapat berfungsi
sebagai emolien, meningkatkan elastisitas kulit serta memperbaiki kelembutan
sediaan sehingga lebih nyaman untuk digunakan.
Gelling agent yang digunakan pada formula gel ini adalah carbopol 940
dengan konsentrasi 1%, di mana termasuk dalam rentang konsentrasi yang biasa
digunakan sebagai gelling agent yaitu 0,5 - 2 %. Carbopol 940 memiliki beberapa
kelebihan seperti aman dan efektif, tidak mempengaruhi efek biologis zat aktif,
dan sifat thickening yang sangat baik sehingga banyak digunakan dalam produk
topikal (Hosmani, Thorat, Katsure, 2006). Carbopol dengan konsentrasi 1% b/v
sehingga perlu ditambahkan basa amin untuk menaikkan pH sediaan agar didapat
pH 5 – 6,5, dimana merupakan rentang pH kulit.
Basa amin yang digunakan adalah trietanolamin (TEA). Penambahan
trietanolamin untuk menetralkan sifat asam dari carbopol sehingga dapat
membantu carbopol 940 untuk uncoiled. Mekanisme carbopol 940 untuk uncoiled
adalah penetralan gugus asam karboksilat pada rantai polimer yang
mengakibatkan terbentuknya muatan negatif di sepanjang rantai polimernya.
Adanya gaya tolak-menolak antar muatan negatif menyebabkan carbopol 940
benar-benar uncoiled ke dalam struktur yang lebih luas, sedangkan rantai carbopol
940 tetap terjalin satu sama lain menghasilkan matrik tiga dimensi yang
membentuk gel yang sangat kental dalam waktu seketika (Suhaime, Tripathy,
Mohammed, dan Majeed, 2012).
Pada penelitian ini ekstrak daun jambu biji yang digunakan sebanyak 3
gram ekstrak cair. Propilen glikol pada formula ini digunakan sebagai enhancer
dengan konsentrasi 5%. Karena gel yang dibuat termasuk hidrogel yang sebagian
besar mengandung air sehingga rentan dengan pertumbuhan mikroba maka
ditambahkan metil paraben sebagai pengawet. Metil paraben yang digunakan
sebanyak 0,1% dan masih diperbolehkan dalam kosmetik, berdasarkan keputusan
Badan POM No. HK. 00.05.4.1745. Gel antioksidan esktrak daun jambu biji
dibuat dengan bantuan mixer untuk mencampurkan massa gel dengan
bahan-bahan lain dalam formula menggunakan kecepatan putar skala satu selama 3
menit, karena dengan kecepatan putar rendah dan waktu pengadukan yang singkat
D. Uji Sifat Fisis Gel Antioksidan Ekstrak Daun Jambu Biji (Psidium guajava L.)
Uji sifat fisis dilakukan untuk menjamin kualitas dari sediaan yang telah
dibuat serta mendapatkan suatu sediaan yang memenuhi syarat sediaan yang baik,
Uji sifat fisis yang dilakukan meliputi organoleptis, pH, daya sebar dan viskositas.
Uji sifat fisis dilakukan 48 jam setelah pembuatan. Hal ini dimaksudkan bahwa
waktu setelah 48 jam gel telah membentuk sistem yang stabil, di mana
matrik-matrik penyusun gel sudah menempati posisinya tanpa dipengaruhi oleh energi
dan gaya geser selama proses pembuatan sehingga tidak mempengaruhi hasil
pengujiannya.
1. Uji organoleptis dan pH
Uji organoleptis dilakukan dengan mengamati warna dan bau dari
sediaan gel 48 jam setelah pembuatan dan 4 minggu penyimpanan, serta
dilakukan uji pH menggunakan pH universalstick.
Tabel VI. Hasil uji organoleptis dan pH
Kriteria 48 jam jam setelah pembuatan 4 minggu penyimpanan
F1 F2 F3 F4 F1 F2 F3 F4
Warna coklat coklat coklat coklat coklat coklat coklat coklat Bau khas khas khas khas khas khas khas khas
pH 6 6 6 6 6 6 6 6
Keterangan : F1 (Gliserin 0%), F2 (Gliserin 7,5%), F3 (Gliserin 15%), F4 (Gliserin 30%)
Berdasarkan Tabel VI, hasil uji organoleptis dan uji pH 48 jam
setelah pembuatan dan 4 minggu penyimpanan, tidak mengalami perubahan
dari warna, bau dan pH. pH dari sediaan gel antioksidan ekstrak daun jambu
biji memenuhi pH kulit yaitu antara 4 – 6,5, sehingga sediaan yang dibuat
Tabel VII. Sifat fisis dan stabilitas gel antioksidan ekstrak daun jambu biji (Psidium guajava L.)
Formula Viskositas (d.Pa.s) Pergeseran Viskositas (%)
Pengujian viskositas dilakukan untuk melihat tahanan sediaan gel
untuk mengalir, di mana semakin besar viskositas, maka sediaan gel semakin
sulit mengalir karena semakin besar tahanannya. Besarnya suatu viskositas
tergantung pada tujuan penggunaan sediaan tersebut. Pada penelitian ini
sediaan ditujukan untuk melindungi kulit dari radikal bebas, maka diperlukan
sediaan yang mampu bertahan lama di kulit sehingga menghasilkan efek yang
diinginkan. Hal tersebut terkait dengan viskositas dan daya lekat dari sediaan
yang dibuat, semakin besar viskositas, maka semakin lama daya lekat sediaan
pada kulit.
Viskositas merupakan karakteristik yang penting karena
mempengaruhi pelepasan zat aktif dari sediaan, pengemasan, penyimpanan,
dan aplikasi sediaan pada kulit. Viskositas sediaan gel sebaiknya tidak terlalu
kental dan terlalu encer. Apabila viskositasnya terlalu kental maka akan sulit
diaplikasikan pada kulit secara merata, begitupun sebaliknya viskositas
terlalu encer maka saat diaplikasikan pada kulit waktu kontak gel dengan
Viskositas yang diinginkan pada penelitian ini adalah 200 - 300
d.Pa.s. Dari Tabel VII diketahui bahwa formula 1 tidak masuk dalam range
viskositas, yaitu 200-300 d.Pa.s., hal ini terjadi karena pada formula 1 tidak
digunakan gliserin. Data viskositas yang didapat kemudian dilakukan uji
statistik untuk mengetahui apakah peningkatan konsentrasi gliserin memberi
pengaruh signifikan terhadap viskositas gel antioksidan ekstrak daun jambu
biji. Pertama-tama dilakukan uji normalitas menggunakan uji Shapiro-Wilk
untuk melihat apakah data viskositas terdistribusi normal atau tidak. Hasil
yang didapat semua formula memiliki p-value > 0,05 sehingga data viskositas
terdistribusi normal. Selanjutnya dilakukan uji Levene’s test, hasil didapatkan
Pr(>F) > 0,05 sehingga disimpulkan bahwa data viskositas memiliki
kesamaan varians.
Untuk melihat pengaruh peningkatan konsentrasi gliserin terhadap
peningkatan viskositas maka akan dianalisis statistik menggunakan ANAVA
dengan uji T tidak berpasangan sebagai uji post hoc. Hasil didapatkan terjadi
peningkatan viskositas secara signifikan dengan adanya peningkatan
konsentrasi gliserin. Gliserin sebagai humectant dapat meningkatkan
viskositas dari sediaan karena gliserin mampu mengikat air sehingga cairan
tersebut tertahan dan diikat oleh gelling agent. Hal tersebut meningkatkan
ukuran molekul dari gelling agent dan menyebabkan terjadinya peningkatan
tahanan untuk mengalir (Martin, Swarbrick, dan Cammarata, 1993).
Pengukuran viskositas dilakukan kembali setelah 4 minggu
diinginkan adalah kurang dari 10%. Pada Tabel VII semua formula
memenuhi syarat pergeseran viskositas kurang dari 10% sehingga dapat
disimpulkan bahwa keempat formula memiliki stabilitas yang baik.
3. Uji daya sebar
Pengujian daya sebar dilakukan untuk mengetahui kemampuan
sediaan menyebar secara merata pada kulit saat diaplikasikan. Pengujian daya
sebar penting dilakukan terkait kemudahan aplikasi, penghantaran obat ke
tempat aksi, ekstrudabilitas gel dari kemasan, serta penerimaan oleh
konsumen (Garg et al., 2002). Menurut Garg et al. (2002) daya sebar
berbanding terbalik dengan viskositas, semakin besar viskositas maka daya
sebar semakin rendah, dan begitupun sebaliknya semakin rendah viskositas
maka daya sebar semakin tinggi.
Pengujian daya sebar dilakukan pada 1 gram gel pada kaca bulat
berskala yang diberi beban 125 gram dan didiamkan selama 1 menit. Daya
sebar dihitung dari rata-rata diameter terpanjang dari empat sisi. Gel yang
baik memiliki nilai daya sebar yang tidak terlalu besar maupun terlalu kecil.
Apabila daya sebar terlalu besar maka penggunaan sediaan menjadi tidak
efektif pada tempat pengaplikasian karena akan menyebar ke bagian lainnya,
sedangkan jika daya sebar terlalu kecil maka akan menemui kesulitan saat
mengaplikasikan karena sediaan akan sulit menyebar secara merata di kulit.
Daya sebar yang diinginkan pada penelitian ini adalah 3-5 cm. Dari
daya sebar, yakni antara 3-5 cm, di mana diameter daya sebar kurang dari 5
cm gel bersifat semistiff (semi kaku). Data daya sebar yang didapat kemudian
dilakukan uji statistik untuk mengetahui apakah peningkatan konsentrasi
gliserin memberi pengaruh signifikan terhadap daya sebar gel ekstrak daun
jambu biji. Pertama-tama dilakukan uji normalitas menggunakan uji
Shapiro-Wilk untuk melihat apakah data daya sebar terdistribusi normal atau tidak.
Hasil dari uji Shapiro-Wilk didapatkan bahwa p-value > 0,05 sehingga
disimpulkan semua data daya sebar terdistribusi normal. Selanjutnya
dilakukan uji Levene’s test, hasil didapatkan Pr(>F) 0,8213 sehingga
disimpulkan bahwa data daya sebar memiliki kesamaan varians.
Untuk melihat pengaruh peningkatan konsentrasi gliserin terhadap
penurunan daya sebar maka akan dianalisis statistik menggunakan ANAVA
dengan uji T tidak berpasangan sebagai uji post hoc. Hasil yang didapat
peningkatan gliserin memberikan pengaruh signifikan terhadap daya sebar.
Hal tersebut sesuai teori di mana nilai daya sebar berbanding terbalik dengan
nilai viskositas sediaan. Semakin tinggi konsentrasi gliserin yang
ditambahkan dalam formula maka viskositas semakin besar dan daya sebar
semakin kecil, begitupun sebaliknya semakin rendah konsentrasi gliserin
maka viskositas semakin rendah dan daya sebar semakin besar.
E. Uji Iritasi Primer Draize Test
Uji iritasi primer dilakukan dengan tujuan untuk mengetahui keamanan
Iritasi primer adalah reaksi yang timbul sesaat setelah diberikan paparan sediaan.
Uji iritasi yang dilakukan pada penelitian ini menggunakan metode Draize Test, di
mana merupakan uji iritasi yang telah mapan dan dapat digunakan sebagai uji
iritasi dalam sediaan topikal. Metode Draize Test biasanya menggunakan kelinci
karena berdasarkan kulit kelinci lebih sensitif daripada kulit manusia dan lebih
aman ketika digunakan untuk penapisan bagi senyawa yang bersifat iritan
(Zulkarnain, Meiroza, Aliva, 2013).
Pengujian dilakukan dengan mengoleskan gel pada punggung kelinci
yang telah dicukur dan dibersihkan bulunya. Kemudian diamati eritema dan
edema yang mungkin terjadi pada punggung kelinci selama 24, 48, dan 72 jam
setelah pengaplikasian gel, kontrol positif, dan kontrol negatif. Kontrol positif
digunakan untuk membandingkan bahan-bahan yang telah terbukti mengiritasi
kulit dengan gel antioksidan ekstrak daun jambu biji. Kontrol negatif
dimaksudkan untuk membandingkan apakah terjadi iritasi atau tidak antara kulit
normal dan kulit yang diberi sediaan (gel dan kontrol positif).
Hasil menunjukkan formula 1, 2, 3, dan 4 tidak terdapat eritema dan
edema pada punggung kelinci setelah pemaparan 24 jam sampai 72 jam dan
memberikan indeks iritasi primer bernilai 0 (Lampiran 7), sedangkan hasil kontrol
positif menggunakan sodium lauryl sulphate (SLS) 2% terjadi edema dan diberi
skor 2. Hasil tersebut menunjukkan gel antioksidan ekstrak daun jambu biji
formula 1, 2, 3, dan 4 tidak menimbulkan iritasi pada kulit dan aman digunakan