BAB II
TINJAUAN PUSTAKA
2.1. Uraian Tumbuhan
2.1.1. Klasifikasi tumbuhan
Menurut Pujowati (2006) klasifikasi dari tumbuhan beluntas sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dycotyledonae Bangsa : Compositales Suku : Compositae Marga : Pluchea
Spesies : Pluchea indica(L.) Less 2.1.2. Morfologi tumbuhan
2.1.3. Habitat dan daerah tumbuhan
Pluchea indica (L.) Less pada umumnya di Indonesia dikenal dengan nama beluntas, khususnya bagi masyarakat Sumatra, Jawa dan Madura. Sulawesi disebut lamutasa dan di Timor disebut lenabou. Dalam pengobatan Cina dikenal dengan luan yi dan di Eropa dikenal dengan marsh heabane (Hariana, 2005). Beluntas umumnya tumbuh liar di daerah kering pada tanah yang keras atau berbatu atau ditanam sebagai tanaman pagar. Tumbuhan ini memerlukan cukup cahaya matahari atau sedikit naungan, banyak ditemukan pada daerah pantai dekat laut, terdapat sampai 1000 m di atas permukaan laut (Ardiansyah, 2005).
2.1.4. Kandungan kimia beluntas
Daun beluntas mengandung alkaloid, flavonoida, tanin, minyak atsiri, asam chlorogenik, kalium, aluminium, kalsium, magnesium dan fosfor. Akarnya mengandung flavonoida dan tanin (Dalimartha, 1999).
2.1.5. Manfaat tumbuhan
Tumbuhan Beluntas dapat digunakan untuk menghilangkan bau badan dan bau mulut, kurang nafsu makan, gangguan pencernaan pada anak, TBC kelenjar (skrofuloderma), nyeri pada rematik, nyeri tulang, sakit pinggang, demam, dating haid tidak teratur dan keputihan (Dalimartha, 1999).
2.2. Kandungan Senyawa Kimia 2.2.1. Alkaloid
2.2.2. Flavonoida
Flavonoida umumnya terdapat pada tumbuhan sebagai glikosida. Flavonoid berupa senyawa fenol dan telah diketahui memiliki respon terhadap mikroba (Robinson, 1995). Aktivitasnya dikarenakan kemampuannya membentuk kompleks dengan protein seluler dan dinding sel bakteri (Cowan, 1999).
2.2.3. Tanin
Tanin pada tanaman merupakan senyawa fenolik yang larut dalam air yang memiliki berat molekul antara 300-3000 dan menghasilkan reaksi warna biru dengan besi (III) klorida. Tanin berasal dari bahasa Prancis ‘tanin’ yang
merupakan fenol alami (Khanbabaea, 2001). Secara kimia tanin tumbuhan terbagi dua, yaitu tanin terkondensasi (tanin katekin) dan tanin terhidrolisis (Robison, 1995).
Tanin memiliki kemampuan untuk mengendapkan protein, memiliki aktivitas sebagai antioksidan, antitumor (Robinson, 1995). Sifat antibakteri tanin berhubungan dengan kemampuannya membentuk komplek dengan protein bakteri (Cowan, 1999).
2.2.4. Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Glikosida mudah terhidrolisis oleh asam mineral atau enzim. Hidrolisis oleh asam memerlukan panas, sedangkan hidrolisis oleh enzim tidak memerlukan panas (Sirait, 2007).
Berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi:
b. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C, yakni gula melekat pada aglikon melalui ikatan karbon-karbon.
c. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan S. Contoh: sinigrin(C10H16NS2K) yang termasuk ke dalam glikosida
glukosinolat dari tumbuhan Brassicaceae.
d. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui jembatan N. Contoh: nikleosidin, kronotosidin.
2.2.5. Saponin
Saponin tersebar luas diantara tanaman tingkat tinggi. Saponin merupakan senyawa berasa pahit, menusuk, menyebabkan bersin dan mengakibatkan iritasi terhadap selaput lendir. Saponin mula-mula diberi nama demikian karena sifatnya yang menyerupai sabun (bahasa Latin sapo berarti sabun). Saponin adalah senyawa aktif permukaan yang kuat dan menimbulkan busa jika dikocok dalam air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah merah. Saponin sangat beracun dalam larutan yang sangat encer, untuk ikan dan tumbuhan yang mengandung saponin telah digunakan oleh penduduk sebagai racun ikan selama beratus-ratus tahun. Beberapa saponin bekerja sebagai antimikroba (Robinson, 1995).
2.2.6. Steroid/triterpenoid
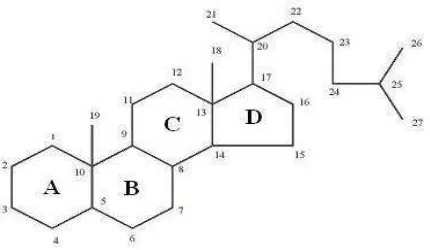
Steroid adalah triterpena yang kerangka dasarnya sistem cincin siklopentana perhidropenantren (Harbone, 1987). Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis masuk jalur asam mevalonat yang diturunkan dari hidrokarbon C30 asiklik, yaitu
dengan kebanyakan triterpen dan sterol memberikan warna hijau-biru (Harborne, 1987). Steroid pada umumnya berupa alkohol dengan gugus hidroksil pada C3
sehingga steroid sering juga disebut sterol (Robinson, 1995). Gambar struktur dasar dapat dilihat pada Gambar 2.3.
Gambar 2.3Struktur dasarsteroid(Robinson, 1995)
2.3. Ekstraksi
Ekstraksi adalah penyarian komponen aktif dari suatu jaringan tumbuhan atau hewan dengan menggunakan pelarut yang cocok (Handa, 2008). Beberapa metode ekstraksi dengan menggunakan pelarut (Depkes, 2000) yaitu:
1. Cara dingin a. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kalipengocokan atau pengadukan pada temperatur kamar. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus menerus).Remaserasi berarti dilakukan penyarian berulang dan seterusnya.
b. Perkolasi
tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1–5 kali bahan.
2. Cara panas a. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
b. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40–50oC.
c. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan alat soklet dengan pelarut yang selalu baru sehingga terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
d. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas mendidih, temperatur terukur 96–98oC)
selama waktu tertentu (15–20 menit). e. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama (≥ 30 menit) dan temperatur sampai titik didih air.
2.4. Fraksinasi (Ekstaksi Cair-Cair)
organik), yang tidak tercampurkan. Pada proses ini terjadi pemisahan satu atau lebih zat terlarut (solute) kedalam pelarut yang kedua (Basset, 1994).
Pemisahan yang dilakukan bersifat sederhana, bersih, cepat dan mudah, yang dapat dilakukan dengan cara mengocok-ngocok dalam sebuah corong pisah selama beberapa menit (Basset, 1994). Analit-analit yang mudah terekstraksi dalam pelarut organik adalah molekul-molekul netral yang berikatan secara kovalen dengan substituent yang bersifat nonpolar atau agak polar. Senyawa-senyawa yang mudah mengalami ionisasi dan Senyawa-senyawa polar lainnya akan tertahan dalam fase air (Rohman, 2007).
Pelarut yang dipilih untuk ekstraksi pelarut ialah pelarut yang mempunyai kelarutan yang rendah dalam air, dapat menguap sehingga memudahkan penghilangan pelarut organik setelah dilakukan ekstraksi dan mempunyai kemurnian yang tinggi untuk meminimalkan adanya kontaminasi sampel (Rohman, 2007).
2.5. Bakteri
2.5.1. Uraian umum
Bakteri merupakan sekelompok mikroba atau mikroorganisme yang bersel satu, berkembangbiak dengan membelah diri, karena bentuknya sangat kecil sehingga hanya dapat dilihat dengan menggunakan mikroskop. Nama bakteri berasal dari kata “bakterion” yang berarti tongkat atau batang
(Dwidjoseputro,1987). Bakteri pada umumnya terdiri dari tiga bentuk dasar, yaitu: bentuk bulat (kokus), batang (basilus) dan spiral (Fardiaz, 1992; Pratiwi, 2008).
a. Bakteri Gram positif, yaitu bakteri yang dapat mengikat zat warna utama (kristal violet)sehingga tampak berwarna ungu tua.
b. Bakteri Gram negatif, yaitu bakteri yang kehilangan warna utama (Kristal violet) ketika dicuci denngan alkohol dan menyerap zat warna kedua sewaktu pemberian safranin tampak berwarna merah (Suryanto, 2006).
2.5.2. Bakteri Escherichia coli
Eschericia coli merupakan bakteri Gram negatif, aerob atau anaerob fakulatif, berbentuk batang, tidak bergerak. Escherichia coli biasanya terdapat dalam saluran cerna sebagai flora normal (Dwidjoseputro, 1987). Bakteri ini tumbuh baik pada suhu 37oC, membentuk koloni yang bundar, halus dan tepi rata.
Bakteri ini dapat menjadi patogen bila berada di luar usus atau di lokasi lain dalam jumlah yang banyak (Jawetz, et al., 2001). Sistematika bakteri Escherichia coli (Dwidjoseputro, 1987) adalah sebagai berikut:
Divisi : Schizophyta Kelas : Schizomycetes Ordo : Eubacterales Famili : Enterobacteriaceae Genus : Escherichia
Spesies : Escherichia coli
2.5.3. Bakteri Bacillus subtilis
Divisi : Firmicutes Kelas : Bacilli Ordo : Bacillales Famili : Bacillaceae Genus : Bacillus
Spesies : Bacillus subtilis
2.6. Fase Pertumbuhan Mikroorganisme
Fase pertumbuhan menurut (Pratiwi, 2008) terbagi menjadi empat macam, yaitu:
a. Fase lag (fase adaptasi)
Merupakan fase penyesuaian mikroorganisme pada suatu lingkungan baru dan bakteri belum mengadakan pembiakan. Ciri fase lag adalah tidak adanya peningkatan jumlah sel tetapi peningkatan ukuran sel.
b. Fase log
Merupakan fase dimana mikroorganisme tumbuh dan membelah pada kecepatan maksimum tergantung sifat media dan kondisi pertumbuhan. Sel baru terbentuk dengan laju konstan dan massa yang bertambah secara eksponensial. c. Fase stasioner (konstan)
Merupakan fase pertumbuhan mikroorganisme berhenti dan terjadi keseimbangan antara jumlah sel yang membelah dengan jumlah sel yang mati. d. Fase kematian
2.7. Faktor Pertumbuhan Mikroorganisme
Faktor yang dapat mempengaruhi pertumbuhan dapat dibedakan menjadi faktor fisik dan faktor kimia. Faktor fisik meliputi temperatur, pH dan tekanan osmosis. Faktor kimia meliputi karbon, oksigen, trace elementdan faktor-faktor pertumbuhan organik termasuk nutrisi yang ada dalam media pertumbuhan (Pratiwi, 2008).
2.8. Antibakteri
Antibakteri adalah senyawa yang digunakan untuk mengendalikan pertumbuhan bakteri yang bersifat merugikan. Antimikroba meliputi golongan antibakteri, antimikotik dan antiviral (Ganiswara, 1995). Senyawa antibakteri dapat bekerja secara bakteriostatik dan bakterisidal (Pelezar, 1988). Obat yang digunakan untuk membasmi bakteri penyebab infeksi pada manusia harus memiliki sifat toksisitas yang selektif yaitu toksis terhadap bakteri tetapi relatif tidak toksis terhadap hospes (Ganiswara, 1995). Target kerja antibakteri (antibiotik) berdasarkan spectrum atau kisaran kerjanya antibiotik dapat dibedakan menjadi berspektrum sempit (narrow spectrum) dan antibiotik berspektrum luas (broad spectrum). Antibiotik berspektrum sempit hanya mampu menghambat segolongan jenis bakteri saja, contohnya hanya mampu menghambat atau membunuh bakteri Gram negatif saja atau Gram positif saja. Sedangkan antibiotik Gram berspektrum luas dapat menghambat atau membunuh bakteri dari golongan Gram positif maupun Gram negatif (Pratiwi, 2008).
a. Antibiotik yang menghambat sintesis dinding sel
Antibiotik ini adalah antibiotik yang merusak lapisan peptidoglikan yang menyusun dinding sel bakteri Gram positif maupun Gram negatif, contohnya penisiln.
b. Antibiotik yang merusak membran plasma
Antibiotik yang bersifat merusak membrane plasma umum terdapat pada antibiotik golongan polipeptida yang bekerja dengan mengubah permeabilitas membrane plasma sel bakteri. Contohnya adalah polimiksin B yang melekat pada fosfolipid membran.
c. Antibiotik yang menghambat sintesis protein
Aminoglikosida merupakan kelompok antibiotik yang gula aminonya tergabung dalam ikatan glikosida. Antibiotic ini memiliki spektrum luas dan bersifat bakterisidal dengan mekanisme penghambatan pada sintesis protein. d. Antibiotik yang menghambat sintesis asam nukleat (DNA/RNA)
Penghambatan pada sintesis asam nukleat berupa penghambatan terhadap transkripsi dan replikasi mikroorganisme. Yang termasuk antibiotik penghambat sintesis asam nukleat ini adalah antibiotic golongan kuinolon dan rifampisin. e. Antibiotik yang menghambat sintesis metabolit esensial
Penghambatan terhadap sintesis metabolit esensial antara lain dengan adanya kompetitor berupa antimetobolit, yaitu substansi yang secara kompetitif menghambat metabolit mikroorganisme, karena memiliki struktur yang mirip dengan substrat normal bagi enzim metabolism. Contohnya adalah antimetabolit sulfanilamid dan Para Amino Benzoic Acid(PABA).
dan kadar bunuh minimal (KBM). Antimikroba tertentu aktivitasnya dapat meningkat dari bakteriostatik menjadi bakterisid bila kadar antimikrobanya ditingkatkan melebihi KHM (Ganiswara, 1995). Ada beberapa hal yang harus dipenuhi oleh suatu bahan antimikroba, seperti mampu mematikan mikroorganisme, mudah larut dan bersifat stabil, tidak bersifat racun bagi manusia dan hewan, efektif pada suhu kamar dan suhu tubuh, tidak menimbulkan karat dan warna, berkemapuan menghilangkan bau yang kurang sedap, murah dan mudah didapat (Pelezar, 1988).
2.9. Metode Pengujian Aktivitas Antimikroba
Pengujian aktivitas bahan antimiroba secara in vitro dapat dilakukan melalui dua cara, yaitu metode difusi dan metode dilusi. Pembagian metode difusi dan dilusi, yaitu (Pratiwi, 2008):
1. Metode difusi
a. Metode disc diffusion (tes Kirbydan Bauer)
Piringan yang berisi agen antimikroba diletakkan pada media agar yang telah ditanami mikroorganisme yang akan berdifusi pada media agar tersebut. Area jernih mengindikasikan adanya hambatan pertumbuhan mikroorganisme oleh agen antimikroba pada permukaan media agar.
b. E-test
Metode E-test digunakan untuk mengestinasi MIC (minimuminhibitory concentration) atau KHM, yaitu konsentrasi minimal satu agen antimkroba untuk
c. Ditch-plate technique
Pada metode ini sampel uji berupa agen antimikroba yang telah diletakkan pada parit yang dibuat dengan cara memotong media agar dalam cawan petri pada bagian tengah secara membujur dan mikroba uji (maksimum 6 jenis) lalu digoreskan ke arah parit yang berisi agen antimikroba.
d. Cup-plate technique
Metode ini serupa dengan metode disc diffusion, dibuat sumur pada media agar yang telah ditanami dengan mikroorganisme dan pada sumur tersebut diberi agen antimikroba yang akan diuji.
2. Metode dilusi
Metode dilusi dibagi menjadi dua, yaitu dilusi padat (solid dilution) dan dilusi cair (broth dilution).
a. Metode dilusi cair/broth dilution test (serial dilution)
Metode ini untuk mengukur MIC atau KHM dan MBC atau KBM. Cara yang dilakukan adalah dengan membuat seri pengenceran agen antimikroba pada medium cair yang ditambahkan dengan mikroba uji.
b. Metode dilusi padat/solid dilution test
Metode ini serupa dengan metode dilusi cair namun menggunakan media padat (solid).
2.10. Sterilisasi
a. Sterilisasi panas basah
Strerilisasi panas basah dapat dilakukan pada suhu air mendidh 100oC selama 10 menit yang efektif untuk sel-sel vegetatif, namun tidak efektif untuk endospora bakteri. Sterilisasi panas basah menggunakan temperature di atas 100oC dilakukan dengan uap yaitu menggunakan autoklaf. Proses sterilisasi dengan cara mendenaturasi atau mengkoagulasi protein pada enzim dan membran sel mikroorganisme (Pratiwi, 2008), dengan suhu 121oC ( dengan tekanan 15 psi) selama 15-20 menit (Irianto, 2006).
b. Sterilisasi panas kering
Metode sterilisasi ini tidak memerlukan air sehingga tidak ada uap air yang membasahi alat atau bahan yang disterilkan (Pratiwi, 2008). Ada dua metode sterilisasi panas kering yaitu dengan insenerasi, yaitu pembakaran menggunakan api dari bunsen dengan temperatur sekitar 350oC dan dengan udara panas oven