BAB III
METODE PERCOBAAN
3.1. Tempat dan Waktu Percobaan
Percobaan ini dilakukan di Laboratorium Instrument PT. Kimia Farma (Persero) Tbk. Plant Medan Jalan Raya Tanjung Morawa Km. 9 pada bulan Februari 2017.
3.2. Alat dan Bahan 3.2.1 Alat
Alat - alat yang digunakan dalam percobaan ini adalah alat - alat gelas (erlenmeyer 250 ml, gelas ukur 25 ml, labu tentukur 50 dan 100 ml, pipet volume 1 ml), botol vial, digital analytical balance, mortir, pipet tetes, saringan milipore 0,45 µm stamfer, seperangkat alat HPLC Alliance Type E2695, spuit 1 ml, dan ultarsonic digital Merk ELMA type D-78224.
3.2.2. Bahan
Bahan – bahan yang digunakan dalam percobaan ini adalah aquabidest, baku pembanding parasetamol BPFI, metanol, tablet parasetamol generik produksi PT. Kimia Farma (Persero) Tbk. Plant Medan.
3.3. Metode Pengambilan Sampel
3.4. Prosedur Percobaan 3.4.1 Preparasi Sampel Uji
Ditimbang 20 tablet parasetamol, gerus hingga halus. Ditimbang serbuk ± 60 mg (setara dengan 50 mg parasetamol) sebanyak 2 kali (duplo) dan dimasukkan masing – masing ke dalam labu tentukur 100 ml. Ditambahkan ± 20 ml pelarut, disonikan dengan ultrasonic bath selama 15 menit, kemudian ditambahkan pelarut sampai volume tepat 100 ml dan dihomogenkan. Disaring larutan dengan saringan milipore 0,45 µm, kemudian dimasukkan ke dalam botol vial. Larutan siap dianalisa.
3.4.2. Pembuatan Standar Parasetamol
Ditimbang seksama 50 mg baku pembanding, dimasukkan ke dalam labu tentukur 100 ml. Ditambahkan 20 ml pelarut, disonikan dengan ultrasonic bath selama 15 menit, ditambahkan pelarut sampai volume tepat 100 ml kemudian dihomogenkan. Dipipet 1 ml larutan, dimasukkan ke dalam labu tentukur 50 ml, ditambahkan pelarut sampai garis tanda, dan dihomogenkan. Disaring larutan dengan saringan milipore 0,45 µm, dimasukkan ke dalam botol vial. Larutan siap dianalisa.
3.4.3. Pembuatan Fase Gerak dan Pelarut 3.4.3.1 Metanol : Aquabidest (1:3)
3.4.4. Analisis Tablet Parasetamol
Dihidupkan alat KCKT. Dilakukan purging dan conditioning pada alat HPLC sebelum alat digunakan. Dialirkan fase gerak (metanol : aquabidest) (1:3) dengan menggunakan pompa dengan laju alir 1,2 ml/menit ke dalam kolom tipe bondapack C18 dan diatur panjang gelombang pada 243 nm. Kemudian
disuntikkan secara terpisah larutan standar parasetamol sebanyak 6 kali dan larutan sampel parasetamol sebanyak dua kali dengan volume penyuntikan masing
– masing 20 µl. Pemisahan zat aktif terjadi melalui mekanisme kromatografi dan
hasil pemisahan dibaca oleh detektor dan dapat dilihat grafik kromatogram yang terbentuk di layar komputer.
3.5. Perhitungan kadar
Perhitungan penetapan kadar tablet parasetamol dapat menggunakan
rumus sebagai berikut: Kadar
=
x x Kst
Untuk [Sp] = [St] berlaku rumus:
Kadar
=
x Kst
Keterangan:
AUC Sp : Luas Area Sampel
AUC Std : Luas Area Standar (Baku Pembanding) [Sp] : Konsentrasi Sampel
[St] : Konsentrasi Standar
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Analisis Standar Parasetamol (Baku Pembanding)
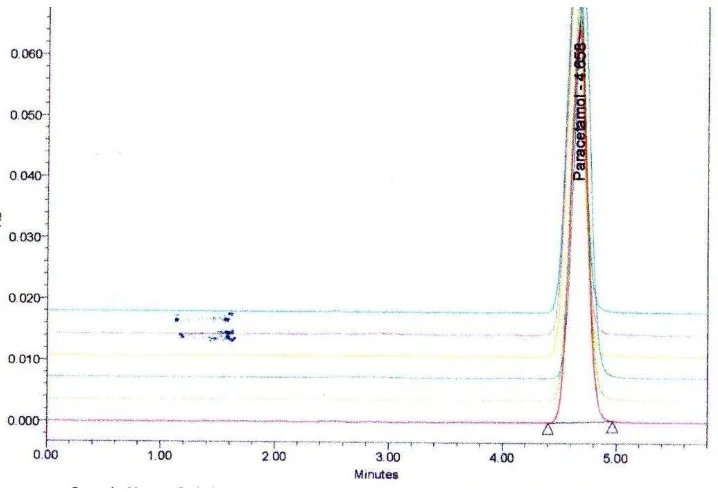
Analisis standar parasetamol (baku pembanding) dilakukan dengan penyuntikan larutan standar parasetamol sebanyak 6 kali dengan volume penyuntikan masing – masing 20 µl dan konsentrasi larutan sebesar 0,01 mg/ml. Maka diperoleh kromatogram dengan waktu retensi 4,647 menit (waktu retensi diperoleh dari hasil rata – rata waktu retensi pada 6 kali penyuntikan standar parasetamol). Kromatogram dapat dilihat pada gambar 2 dibawah ini.
Hasil analisis KCKT untuk standar parasetamol dapat dilihat pada tabel berikut:
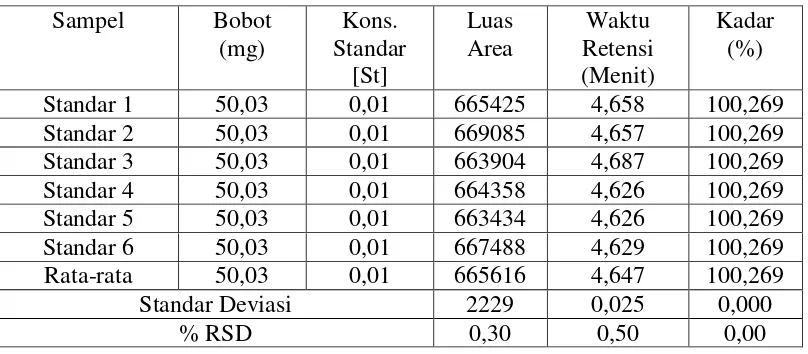
Tabel 1. Hasil KCKT Untuk Standar Parasetamol (Baku Pembanding) Sampel Bobot
Hasil pengujian untuk standar parasetamol dari 6 kali penyuntikan diperoleh luas area rata – rata 665616, % RSD sebesar 0,30%, dan kadar rata – rata sebesar 100,269% (perhitungan kadar dapat dilihat pada lampiran 1 halaman 20). Semakin kecil hasil % RSD yang diperoleh maka tingkat kesalahan pada pengujian semakin kecil.
Presisi merupakan ukuran keterulangan metode analisis dan biasanya dikaitkan sebagai nilai simpangan baku relatif. Biasanya dilakukan pengulangan 6-15 kali pada sampel tunggal, dimana pada KCKT nilai RSD yang dipersyaratkan lebih kecil dari 2% (Gandjar, 2008).
4.2 Hasil Analisis Sampel Parasetamol
waktu retensi 4,667 menit (waktu retensi diperoleh dari hasil rata – rata waktu retensi pada 2 kali penyuntikan sampel parasetamol). Kromatogram dapat dilihat pada gambar 3 dibawah ini.
Gambar 3. Kromatogram hasil penyuntikan larutan sampel parasetamol
Perbedaan antara waktu retensi standar dengan sampel dari hasil pengujian tidak terlalu besar (mirip).
Waktu retensi merupakan lamanya waktu yang dibutuhkan solut untuk melewati kolom. Hasil dikatakan baik jika waktu retensi sampel mirip atau sama dengan standar (Mahdiyar, 2014).
Hasil analisis KCKT untuk sampel tablet parasetamol generik dapat dilihat pada tabel berikut:
Hasil pengujian untuk sampel parasetamol dari 2 kali penyuntikan diperoleh luas area rata – rata 658484, % RSD sebesar 0,20%, dan kadar rata – rata sebesar 99,234% (perhitungan kadar sampel dapat dilihat pada lampiran 2 halaman 21).
Analisis kuantitatif dapat ditentukan berdasarkan luas puncak dan tinggi puncak. Pengukuran luas puncak tidak banyak dipengaruhi oleh kondisi kromatografi dibandingkan dengan tinggi puncak. Oleh karena itu, pengukuran luas puncak merupakan pilihan yang terbaik dalam analisis kuantitatif secara KCKT (Johnson dan Stevenson, 1991).
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Kadar tablet parasetamol generik produksi PT. Kimia Farma (Persero) Tbk. Plant Medan diperoleh sebesar 99,234% dan telah memenuhi persyaratan sesuai dengan Farmakope Indonesia Edisi V yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
5.2. Saran