PENGARUH PEMBERIAN SEDIMEN BAKAU DAN SEDIMEN RAWA TERHADAP POPULASI BAKTERI PADA AIR ASAM TAMBANG
Nur Qalbi*, Fahruddina, Asadi Abdullaha *
Alamat Korespondensi e-mail:qalbiguntur@gmail.com
a
Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Hasanuddin, Makassar
ABSTRAK
Penelitian tentang pengaruh pemberian sedimen bakau dan sedimen rawa terhadap populasi bakteri pada air asam tambang telah dilaksanakan. Penelitian ini bertujuan untuk menanggulangi masalah air asam tambang dengan memanfaatkan bakteri pereduksi sulfat dalam sedimen bakau dan sedimen rawa, secara khusus penelitian ini bertujuan untuk mengetahui perubahan jumlah total bakteri pada air asam tambang setelah diberi perlakuan sedimen bakau dan sedimen rawa. Pengolahan limbah AAT dengan menggunakan sedimen bakau dan sedimen rawa yang ditambahkan kompos sebagai bumber karbon. Hasil pengamatan menunjukkan bahwa sedimen bakau dapat meningkatka pH AAT dari 2,077 menjadi 6,957. Sedimen rawa juga mampu menaikkan nilai pH dari 1,796 menjadi 6,224, sedangkan kontrol hanya mampu menaikkan pH menjadi 2,367. Sedimen bakau juga mampu menurunkan kadar sulfat pada AAT dari 54,697 ppm menjadi 2,524 ppm. Sedimen rawa juga mampu menurunkan kadar sulfat dari 53,295 ppm menjadi 2,805 ppm, sedangkan kontrol hanya mampu menurunkan kadar sulfat dari 52,734 ppm menjadi 47,965 ppm. Pada pengamatan jumlah total mikroba, jumlah total mikroba pada sedimen bakau meningkat dari 20 sei/ml menjadi 495 sel/ml. Jumlah total mikroba pada sedimen rawa juga meningkat dari 40 sel/ml menjadi 280 sel/ml, sedangkan jumlah total mikroba pada kontrol juga meningkat dar 25 sel/ml menjadi 185 sel/ml.
Kata kunci : Tambang, Sedimen Bakau, Sedimen Rawa, Bakteri, Sulfat ABSTRACT
“Influence of Mangrove Sediments and Marsh Sediments to change in Bacterial Population and Content of Sulfate in Acid mine Drainage” By Nur Qalbi (H41110260) . This research aims to overcome the problem of acid mine drainage by using sulfate reducing bacteria on mangrove sediments and marsh sediments. Spesifically, this research aims to know the change of total number bacteria and raise the pH on water acid mine drainage after given a treatment of mangrove sediments and marsh sediments. Processing AMD waste by using mangrove sediments and marsh sediments added compost as a carbon source. Observations
indicate that mangrove sediments can improve pH AMD from 2,077 to 6,957. Marsh sediments can also raise the pH value from 1,796 to 6,224. While control only able to raise pH 2,367. Mangrove sediments was able to reduce levels of sulfate from 54,697 ppm to 2,524 ppm. Marsh sediments was also able to reduce of sulfate from 53,295 ppm to 2,805 ppm, while control only able to reduce sulfate from 52,734 ppm to 47,965 ppm. In observation of the total number microba on mangrove sediments increase from 20 sel/ml become 810 sel/ml. Total number microba on marsh sediments also increase from 40 sel/ml become 355 sel/ml, while total number microba on control only increase from 25 sel/ml become 185 sel/ml.
Kata kunci : Sediments, acid mine, sulfate reducing bacteria PENDAHULUAN
Indonesia yang kaya akan sumberdaya mineral telah menghasilkan ratusan juta dollar bagi pemasukan pendapatan negara melalui berbagai pajak dan royalti sektor pertambangan setiap tahunnya. Pendapatan yang diperoleh dari pajak pertambangan hampir mencapai 50% dari seluruh hasil pendapatan negara (Hadi, 2002). Namun demikian, kegiatan pertambangan tetap saja mempunyai dua sisi yang saling berlawanan, sebagai salah satu sumber kemakmuran yang tidak diragukan lagi dan disisi lain menyebabkan kerusakan lingkungan alam dan sosial.
Salah satu persoalan terbesar yang dihadapi industri pertambangan adalah terbentuknya air asam tambang (AAT). Air asam tambang terbentuk karena terangkatnya mineral-mineral sulfida terutama pirit, yang kemudian bereaksi dengan air dan udara terbuka menghasilkan asam sulfat yang bersifat sangat masam, air asam tambang (AAT) akan sangat berbahaya apabila langsung mengalir ke sungai, danau dan lingkungan aquatik lainnya karena AAT memiliki pH yang sangat rendah dan mengandung logam-logam yang dapat bersifat racun seperti Fe,
Al dan Mn. Oleh karena itu AAT perlu dikelola secara baik sehingga tidak membahayakan jika dialirkan ke lingkungan luar, khususnya perairan lahan basah buatan dan penggunaan bakteri pereduksi sulfat (BPS) merupakan alternatif untuk mengendalikan AAT (Habib, 2007).
Penanggulangan AAT dengan menggunakan senyawa kimia sangat tidak efisien dan biaya yang dikeluarkan sangat mahal (Hards dan Hinggins, 2004). Salah satu alternatif adalah bioremediasi dengan menggunakan sulfur reducer bacteria (SRB) untuk mendekontaminasi sulfat, disamping itu SRB juga mampu menurunkan konsentrasi logam berat misalnya besi, seng, tembaga, dll, menetralkan air dan menurunkan konsentrasi sulfat (Hards and Hinggins, 2004). Dalam aktivitas metabolismenya, SRB mereduksi sulfat menjadi logam sulfid yang tidak larut. Prespitasi logam menjadi sulfida ini menghilangkan logam dari dalam perairan. Beberapa spesies SRB dapat mereduksi logam berat menjadi immobil, misalnya
Desulfovibrio vulgaris yang dapat
mereduksi uranium VI (UVI) menjadi U (IV) (Hards dan Hinggins, 2004).
Hasil penelitian Fitriwani (2010) menunjukkan bahwa pemberian sedimen estuaria, sedimen rawa maupun sedimen bakau terhadap air asam tambang (AAT) mampu meningkatkan pH air asam tambang, menurunkan kadar sulfat dan meningkatkan pertumbuhan populasi bakteri pereduksi sulfat (BPS).
Perlakuan sedimen bakau diharapkan dapat mengatasi limbah air asam tambang dengan indikasi adanya kenaikan pH yang menandakan bahwa populasi bakteri pereduksi sulfat meningkat dan menekan pertumbuhan bakteri Thiobacillus ferroxidans yang tumbuh optimal pada kondisi lingkungan yang asam. Penelitian ini penting dilakukan untuk mengetahui dinamika pertumbuhan populasi bakteri pada air asam tambang yang telah diberi perlakuan sedimen bakau dan sedimen rawa. METODE PENELITIAN
Alat yang digunakan pada penelitian ini adalah alat gelas seperti cawan petri (Pyrex), erlenmeyer (Pyrex), gelas ukur (Pyrex), botol pengencer, bunsen, spoit, botol sampel, pH meter (orion), spektrofotometer (Spectronic) , inkubator (Heraeus), neraca ohaus (Ohaus), oven (Heraeus), autoklaf (All American) dan enkas.
Bahan yang digunakan dalam penelitian ini yaitu, Sampel air asam tambang artifisial, Sampel sedimen bakau yang diperoleh dari komunitas hutan bakau dan sedimen rawa yang diperoleh dari ekosistem rawa di jalan sahabat UNHAS, Kompos yang diperoleh dari canopy, Media terdiri atas: Media Nutrient Agar (NA) sintetik (APHA, 1985) (komposisi: Beef 3 g,
pepton 5 g dan agar 15 g/ 1000 ml, Bahan-bahan lain yaitu alkohol, spritus dan aquadest.
Cara Kerja Sterilisasi alat
Semua alat-alat yang akan digunakan disterilkan terlebih dahulu, alat-alat gelas seperti erlenmeyer dan botol pengencer serta alat-alat plastik yang tidak tahan panas disterilkan dengan menggunakan autoklaf dengan suhu 1210 C dengan tekanan 2 atm selama 15 menit. Sedangkan cawan petri disterilkan dengan menggunakan oven dengan suhu 1800 C selama 2 jam.
Pengambilan sampel sedimen wetland Sedimen diambil pada lahan vegetasi bakau dan sedimen rawa pada kedalaman 5-10 cm kemudian dimasukkan kedalam botol sampel yang selanjutnya dibawa dan diperlakukan di laboratorium.
Karakterisasi Sedimen
Setiap jenis sedimen wetland yang digunakan dalam perlakuan, dilakukan karakterisasi yang dimaksudkan untuk mengetahui kondisi awal bagi proses reduksi sulfat AAT. Karbon organik total diukur dengan metode TOC meter (Nur, 1989), kadar nitrogen total menggunakan Micro Kjehldahl (Black et al.1965), kadar fosfor total dengan metode Stanus Khlorida (Greenberg et al.,1985).
Pembuatan Perlakuan
Pengolahan AAT dan sedimen selanjutnya dibuat dengan perlakuan berikut:
1. AAT + sedimen bakau + kompos (60% + 30% + 10%)
2. AAT + sedimen rawa + kompos (60% + 30% + 10%)
3. AAT, tanpa kompos maupun sedimen (100%)
Kompos dan sedimen dimasukkan ke dalam wadah perlakuan dan dimasukkan AAT 600 ml secara perlahan-lahan pada dinding botol, kemudian wadah tersebut di tutup rapat. Botol perlakuan di inkubasi selama 30 hari (tergantung waktu keberhasilan proses pengolahan) pada suhu ruangan. Selama inkubasi, dilakukan pengamatan setiap 5 hari, pengamatan dimulai pada hari ke-0, parameter-parameter yang diamati adalah sebagai berikut:
1. Jumlah total mikroorganisme dengan metode standar plate count (SPC) (Jutono,1992).
2. Reduksi sulfat menggunakan metode titrasi (Greenberg et al., 1985).
3. Pengamatan kenaikan pH dengan pH meter (Greenberg et al., 1985).
a. Menghitung total mikroba dengan metode standar plate count
- Pengenceran
AAT diencerkan secara desimal tergantung derajat kontaminasi bahan. - Pembuatan media NA (APHA, 1985)
Komposisi: ekstrak beef 3 g, pepton 5 g dan agar-agar 15 g/ 1000 ml.
Bahan media dimasukkan ke dalam erlenmeyer 1000 ml selanjutnya ditambahkan aquadest dan dihomogenkan diatas penangas air hingga larutan homogen, selanjutnya media ditutup dengan kapas dan aluminium foil, kemudian di sterilkan dengan menggunakan autoklaf pada suhu 1210C selama + 15 menit.
- Penanaman, inkubasi dan perhitungan jumlah koloni
Diambil setiap 1 ml air asam tambang 10-1, 10-2, 10-3 dimasukkan kedalam cawan petri kemudian medium NA dituangkan dan di ratakan, selanjutnya media didiamkan hingga memadat, selanjutnya diinkubasi selama 24 jam pada suhu 370C, kemudian dihitung jumlah koloni mikroba yang tumbuh pada medium NA tersebut.
b. Pengukuran kadar sulfat air
Pengukuran kadar asam sulfat pada sampel air asam tambang dilakukan dengan metode titrasi.
- Larutan KOH 0,1 N
KOH sebanyak 6,5 g dilarutkan dalam aquades hingga 1 liter. Kemidian distandardisasi
- Larutan indikator phenolphtalein 1% 1 g phenolphtalein dalam 100 ml alkohol (etil alkohol) 70%
- Akhir titrasi tercapai apabila terbentuk warna merah muda yang tidak hilang selama ½ menit.
c. Pengukuran pH
Tahap-tahap pengukuran pH secara umum adalah sebagai berikut. (dilakukan pada pH meter yang telah di kalibrasi). pH meter terlebih dahulu dinyalakan hingga stabil (15-30 menit). Elektroda kemudian dibilas dengan aquadest dan mengeringkannya dengan kertas tisue. Selanjutnya elektroda dicelupkan beberapa saat hingga diperoleh pembacaan yang stabil kemudian hasil sampel pH tersebut dicatat (Apriantono, 1989).
HASIL DAN PEMBAHASAN
Isolat Bakteri Pereduksi Sulfat
Air asam tambang merupakan salah satu bentuk pencemaran lingkungan oleh industri pertambangan yang bersifat asam dengan pH yang rendah sehingga membahayakan biota yang berada pada lingkungan tersebut. Salah satu cara yang efiektif untuk mengatasi hal tersebut adalah dengan menggunakan sumberdaya biologi yang berupa bakteri pereduksi sulfat yang berasal bari sedimen wetland (sedimen bakau dan sedimen rawa) yang diharapkan mampu menaikkan pH air asam tambang tersebut sehingga mencapai pH netral dan tidak lagi membahayakan makhluk hidup yang berada pada lingkungan tersebut.
Pengolahan AAT dengan perlakuan wetland akan lebih murah dan mengurangi tenaga kerja dibandingkan jika pengolahan AAT dengan cara penambahan kapur. Remediasi dengan wetland merupakan gabungan dari kemampuan mikroba yang meliputi: adsorbsi logam, bioakumulasi logam, oksidasi logam dan reduksi fulfat.
Isolat bekteri pereduksi sulfat ini diambil dari dua jenis sedimen yang berbeda yaitu sedimen bakau yang diperoleh dari Maros dan sedimen Rawa yang diperoleh dari Jln. Sahabat, Makassar.
Perlakuan dibuat dalam bioreaktor sederhana berupa botol bening dengan maksud agar memudahkan mengamati perubahan warna terhadap larutan yang berada dalam bioreaktor tersebut untuk masing-masing perlakuan yang berbeda. Dalam perlakuan yang diberikan terlebih dahulu diisi kompos kedalam bioreaktor
tersebut sebagai sumber nutrisi bagi bakteri kemudian dimasukkan sedimen yang merupakan sumber bakteri pereduksi sulfat kemudian yang terakhir adalah menuangkan air asam tambang secara perlahan melalui dinding botol. Selanjutnya diinkubasi selama 25 hari pada suhu ruangan dengan kondisi anaerob. Pengamatan dilakukan setiap 5 hari terhitung sejak awal perlakuan yaitu hari ke-0. Perlakuan dilakukan dengan dua kali pengulangan dan sebagai kontrol hanya diberikan air asam tambang tanpa penambahan apapun baik itu kompos maupun sedimen.
Perubahan jumlah populasi mikroba, pH, dan kadar sulfat merupakan indikator yang akan digunakan sebagai petunjuk untuk mengetahui kemampuan bakteri pereduksi sulfat untuk menaikkan pH air asam tambang dengan kemampuannya mereduksi sulfat serta pengaruhnya terhadap perubahan jumlah populasi mikroba pada setiap perlakuan yang diberikan selama waktu inkubasi.
Populasi mikroba
Grafik 1. Total mikroba pada sedimen bakau
Grafik 2. Total mikroba pada sedimen rawa Grafik 1 menunjukkan adanya
perubahan jumlah total mikroba pada sedmen bakau. Pertambahan jumlah yang sangat meningkat tajam terlihat pada hari
ke-20 dimana jumlahnya mencapai 210 sel/ml dan terus menunjukkan penurunan pada hari berikutnya hingga pada akhir pengamatan yaitu hari ke-25 total mikroba adalah 495 sel/ml. Sedangkan grafik kontrol
0, 20 5, 10 10, 25 15, 225 20, 810 25, 495 0, 25 5, 10 10, 10 15, 35 20, 15 25, 185 0 100 200 300 400 500 600 700 800 900 0 5 10 15 20 25 30 sel /m l Waktu (hari) Sedimen Bakau kontrol 0, 40 5, 25 10, 15 15, 105 20, 355 25, 280 0, 25 5, 10 10, 10 15, 35 20, 15 25, 185 0 50 100 150 200 250 300 350 400 0 5 10 15 20 25 30 sel /m l Waktu (hari) Sedimen rawa kontrol
menunjukkan bahwa jumlah total mikroba cenderung tidak mengalami perubahan yang signifikan tetapi terlihat adanya sedikit peningkatan pada akhir pengamatan yaitu hari ke-25 yaitu 185 sel/ml.
Grafik 2 menunjukkan jumlah total mikroba pada sedimen rawa yang mengalami peningkatan tajam pada hari ke-20 yaitu mencapai 355 sel/ml dan menunjukkan adanya penurunan pada hari ke-25 yaitu 185 sel/ml. Sedangkan grafik kontrol tigak menunjukkan adanya perubahan yang signifikan kecuali pada akhir pengamatan mengalami peningkatan yaitu 185 sel/ml.
Pada awal pengamatan yaitu dari hari ke-0 hingga hari ke-15 terlihat jumlah total mikroba yang masih sedikit bahkan jumlahnya menurun yang disebabkan oleh beberapa jenis mikroba yang tidak mampu bertahan hidup pada kondisi yang sangat asam sehingga jumlah total mikroba cenderung turun sampai pada hari ke-5 baik itu pada sedimen bakau maupun sedimen rawa, mikroba sedang berada pada fase lag dimana mikroba- mikroba yang masih mampu bertahan pada kondisi ini melakukan adaptasi terhadap kondisi lingkungan sehingga dapat bertahan hidup. Pada hari ke-20 baik sedimen bakau maupun sedimen rawa memperlihatkan grafik yang meningkat tajam dimana fase ini disebut fase log atau eksponensial. Mikroba yang telah mampu beradaptasi akan memanfaatkan sumber nutrisi yang ada dengan sebaik-baiknya untuk terus membelah sehingga jumlah sel semakin meningkat, tetapi pada hari ke-25 grafik kembali menunjukkan adanya penurunan dimana fase ini disebut fase
kematian yang terjadi akibat nutrisi dalam botol bioreaktor mulai habis.
Peningkatan jumlah sel yang sangat pesat pada hari ke-20 mengindikasikan bahwa jumlah sel yang mengalami peningkatan adalah bakteri yang memiliki kemampuan untuk memanfaatkan yaitu mereduksi sulfat menjadi sulfida yaitu jenis bakteri pereduksi sulfat (BPS) yang berasal dari sedimen wetland (sedimen bakau dan sedimen rawa). BPS ini terus mengalami pertambahan jumlah sel karena lingkungan yang ekstrim ini justru menjadi lingkungan yang mendukung pertumbuhan bagi bakteri jenis ini.
Sel bertambah dengan pesat hanya dengan membelah diri pada lingkungan yang mendukungnya. Survival of the fittest yang berarti jenis yang menang adalah yang mampu membelah diri paling cepat. Kemampuan membelah lebih cepat memungkinkan populasi bakteri tertentu menyesuaikan diri segera terhadap perubahan-perubahan dalam lingkungan (Mills, 2002).
Nilai pH
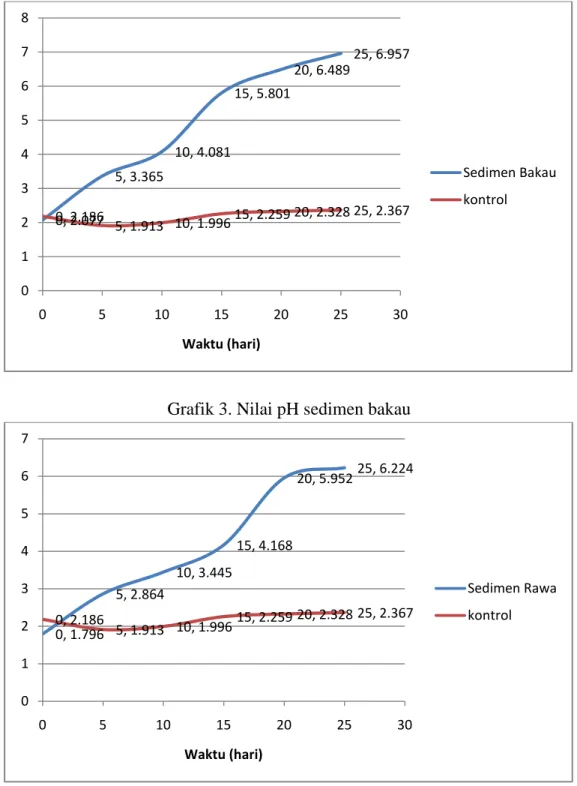
Grafik 3. Nilai pH sedimen bakau
Grafik 4. Nilai pH sedimen rawa Grafik 3 menunjukkan nilai pH pada
AAT yang diberi perlakuan sedimen bakau. Grafik menunjukkan adanya peningkatan pH yang terus bertambah hingga akhir
pengamatan yaitu hari ke-25. Nilai pH pada hari ke-0 menunjukkan nilai 2,077 yang bersifat sangat asam dan terus mengalami peningkatan pada hari-hari selanjutnya hingga pada hari ke-25 nilai pH
0, 2.077 5, 3.365 10, 4.081 15, 5.801 20, 6.489 25, 6.957 0, 2.186 5, 1.913 10, 1.99615, 2.259 20, 2.328 25, 2.367 0 1 2 3 4 5 6 7 8 0 5 10 15 20 25 30 Waktu (hari) Sedimen Bakau kontrol 0, 1.796 5, 2.864 10, 3.445 15, 4.168 20, 5.95225, 6.224 0, 2.186 5, 1.913 10, 1.99615, 2.259 20, 2.328 25, 2.367 0 1 2 3 4 5 6 7 0 5 10 15 20 25 30 Waktu (hari) Sedimen Rawa kontrol
menunjukkan angka 6,957. Sedangkan grafik kontrol yaitu tidak ada penambahan sedimen maupun kompos terlihat tidak mengalami peningkatan nilai pH yang signifikan. Pada awal pengamatan hari ke-0 nilai pH adalah 2,186 hingga pada akhir pengamatan yaitu hari ke-25 nilai pH hanya mencapai 2,367 yaitu masih sangat asam.
Grafik 4 menunjukkan nilai pH dengan perlakuan sedimen rawa yang terus mengalami peningkatan hingga hari ke-25. Pengamatan pada hari ke-0 menunjukkan nilai pH 1,796 yang sangat asam dan terus mengalami peningkatan nilai pH yang terus mendekati pH netral hingga pada akhir pengamatan menunjukkan nilai pH 6,224. Sedangkan grafik kontrol tidak menunjukkan perubahan yang signifikan dimana awal pengamatan hari ke-0 nilai pH adalah 2,186 hingga pada akhir pengamatan yaitu hari ke-25 nilai pH hanya mencapai 2,367 yaitu masih sangat asam.
Berdasarkan hasil pengamatan tersebut menunjukkan bahwa terjadi peningkatan pH baik pada perlakuan sedimen bakau maupun sedimen rawa dimana pH yang awalnya sangat asam kemudian terus mengalami peningkatan menjadi normal. Peningkatan pH ini dapat terjadi karena aktivitas bakteri pereduksi sulfat (BPS) yang mereduksi sulfat menjadi sulfida. Peningkatan aktivitas bakteri ini juga sejalan dengan peningkatan jumlah total mikroba yang terus melakukan pembelahan karena kondisi lingkungan yang mendukung pertumbuhannya.
Dari proses reduksi sulfat oleh kelompok BPS dihasilkan sulfida dan bikarbonat yang berpengaruh terhadap kenaikan pH, sulfida akan bereaksi dengan ion-ion logam terlarut untuk membentuk sulfida logam tak terlarut (Voordouw, 1995).
Kadar Sulfat
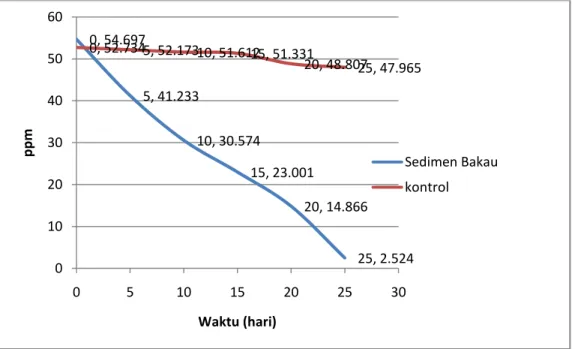
Grafik 5. Kadar sulfat sedimen bakau
0, 54.697 5, 41.233 10, 30.574 15, 23.001 20, 14.866 25, 2.524 0, 52.7345, 52.17310, 51.61215, 51.331 20, 48.80725, 47.965 0 10 20 30 40 50 60 0 5 10 15 20 25 30 ppm Waktu (hari) Sedimen Bakau kontrol
Grafik 6. Kadar sulfat sedimen rawa Grafik 5 menunjukkan adanya penurunan
kadar sulfat dengan perlakuan sedimen bakau. Kadar sulfat awal adalah 54,697 ppm kemudian secara bertahap mengalami penurunan sampai pada hari ke-25 dengan kadar sulfat yang terendah yaitu 2,524 ppm. Sedangkan kadar sulfat kontrol tidak mengalami penurunan yang berarti yaitu hari ke-0 52,734 ppm dan pada akhir pengamatan nilai kadar sulfat kontrol ini menjadi 47,965 ppm.
Grafik 6 menunjukkan kadar sulfat dengan perlakuan sedimen rawa. Selama pengamatan grafik menunjukkan adanya penurunan kadar sulfat yang sangat drastis yaitu 53,295 ppm pada hari ke-0 hingga mencapai 2,805 ppm pada akhir pengamatan yaitu hari ke-25. Sedangkan kadar sulfat kontrol menunjukkan nilai 52,734 ppm pada awal pengamatan dan pada akhir pengamatan menunjukkan nilai 47,965 ppm.
Penurunan konsentrasi sulfat ini disebabkan oleh adanya aktivitas bakteri
pereduksi sulfat ((BPS) yang berasal dari sedimen bakau dan sedimen rawa pada masing-masing perlakuan. BPS ini dapat menggunakan sulfat sebagai akseptor elektron untuk aktivitas metabolismenya (Higgins et al., 2003). Karena sulfat menerima elektron maka senyawa ini akan mengalami reduksi menjadi sulfida sehingga konsentrasi sulfat mengalami penurunan.
Adanya penurunan kadar sulfat dapat terjadi karena adanya kelompok BPS yang disebut juga sulfidogen, mempunyai ciri berupa kemampuan untuk memindahkan elektron atau hidrogen kepada sulfat yang berperan sebagai akseptor elektron terminal. Dari proses reaksi redoks tersebut, sulfat tereduksi menjadi sulfida. Reduksi sulfat yang terjadi pada kondisi anaerob tersebut serupa dengan respirasi yang menggunakan oksigen sebagai akseptor elektron pada kondisi aerob, sehingga disebut respirasi sulfat atau reduksi sulfat dissimilatori (Schlegel, 1994). Produk utama dari reduksi sulfat tergantung pada
0, 53.295 5, 44.88 10, 26.928 15, 20.757 20, 14.305 25, 2.805 0, 52.7345, 52.17310, 51.61215, 51.331 20, 48.80725, 47.965 0 10 20 30 40 50 60 0 5 10 15 20 25 30 ppm Waktu (hari) Sedimen Rawa kontrol
substrat yang dipakai. Jika substrat sebagai donor elektron yang dipakai hidrogen, maka produknya adalah hidrogen sulfida. Bila bahan-bahan organik sederhana terutama laktat sebagai donor elektron maka produknya adalah sulfida.
Berdasarkan hasil pengamatan yang dilakukan menunjukkan bahwa penurunan kadar sulfat seiring dengan peningkatan nilai pH dan peningkatan jumlah total mikroba khususnya bakteri pereduksi sulfat. Meningkatnya jumlah BPS menyebabkan reduksi sulfat yang semakin meningkat sehingga menurunkan konsentrasi sulfat dan penurunan konsentrasi sulfat menyebabkan pH semakin meningkat karena tingginya konsentrasi sulfat menyebabkan pH menjadi sangat asam.
BPS mereduksi sulfat hanya pada kondisi anaerob. Pertumbuhan (waktu tumbuh) sangat tergantung pada toleransi bakteri tersebut dengan keadaan sekelilingnya dan terciptanya kondisi anaerob. Kondisi itulah yang menyebabkan kecepatan tumbuh masing-masing isolat berbeda-beda dengan komposisi unsur hara media yang sama. Sulfida yang dihasilkan dari reduksi sulfat tersebut segera bereaksi dengan kation-kation logam dan hidrogen untuk membentuk sulfida logam dan hidrogen sulfida (Bayoumy et al., 1998). Sulfida yang tidak larut tersebut mengendap dan menempel pada dinding tabung menyebabkan dinding tabung berwarna hitam. Terbentuknya sulfida melalui proses reduksi elektron dari sulfat dengan proses respirasi dissimilasi pada kondisi tanpa oksigen (Moodie and Ingledew, 1991).
Penurunan kadar asam terjadi karena adanya reduksi sulfat menjadi H2S. asam
sulfat adalah bentuk sulfat dalam air yang sangat berpengaruh terhadap penurunan pH atau peningkatan sifat perairan dengan cepat dan biasanya mencapai kestabilan antara pH 2,5 – 3,0. Keasaman air dapat berkembang dengan dihasilkannya besi sulfat yang merupakan oksidator kuat. Dengan demikian ion besi (III) mampu melarutkan mineral-mineral sulfid logam seperti timbal, tembaga, seng, dan kadmium (Greenberg, et al., 1992). Dengan adanya penurunan asam tersebut menyebabkan meningkatnya bakteri yang tahan terhadap kondisi asam seperti thiobacillus ferroxidans bahkan terus meningkatkan keasaman lingkungan.
Menurut Zaid (1995), BPS merupakan sekelompok hetrofilik yang menggunakan senyawa organik sederhana sebagai sumber karbon, terdapat terutama dalam lumpur kotor yang terkandung bahan-bahan organik dari penguraian anaerob. Dengan kemampuan metabolisme kelompok BPS hidup dan berperan pada sedimen perairan dengan menetralisir atau mengurangi keasaman dan meningkatkan pH yang merupakan refleksi dari pengurangan sulfat dalam perairan. Pada proses reduksi ion sulfat selain dihasilkan hidrogen sulfida (H2S) juga dilepaskan ion
hidroksi (OH-). Semakin banyak ion sulfat tereduksi maka semakin banyak pula ion hidroksil yang dihasilkan, sehingga pH semakin meningkat, sebagaimana reaksi berikut:
4H2O + SO4 H2S + 2H2O + 2OH
Pertumbuhan mikroba baik yaitu BPS maupun secara total mengalami peningkatan yang signifikan seiring dengan peningkatan nilai pH dan penurunan
konsentrasi sulfat, namun kita liat puncak total mikroba paling tinggi pada hari ke-20 dan mulai menurun pada hari ke-25. Populasi mikroba mulai menurun pada hari ke-25 disebabkan oleh beberapa hal yaitu sumber karbon dari kompos yang mulai habis dan juga konsentrasi sulfat dalam kolom mulai habis tereduksi seiring aktivitas mikroba yang semakin meningkat sehingga secara otomatis populasi BPS juga akan menurun. Dengan demikian tidak ada kekhawatiran bahwa kelompok bakteri pereduksi sulfat (BPS) akan mengalami blooming dan membuat lingkungan menjadi sangat basa. Dari hasil pengamatan dan grafik juga menunjukkan kemampuan BPS pada sedimen bakau lebih cepat dalam meningkatkan nilai pH dan menurunkan konsentrasi sulfat.
KESIMPULAN
Berdasarkan hasil pengamatan pemberian sedimen bakau dan sedimen rawa terhadap pertumbuhan populasi bakteri pada air asam tambang dapat disimpulkan bahwa:
1. Pemberian sedimen bakau maupun sedimen rawa pada air asam tambang mampu meningjatkan jumlah total mikroba, dibanding kontrol.
2. Pemberian sedimen bakau maupun sedimen rawa mampu meningkatkan pH dan menurunkan konsentrasi sulfat air asam tambang, dibanding kontrol. DAFTAR PUSTAKA
Apriantono, A. 1989. Petunjuk Laboratorium Analisis Pangan. Pusat antar Universitas Pangan dan Gizi Institut Pertanian Bogor. Bogor.
Black, C.A., D. D. Evans, J. L. White, L.E. Ensminger, F.E. Clarck and R.R. Dinauer. [Editor]. 1965. Methods of Soil Analysis. American Society of Agronomy, Inc. Wisconsin. Greenberg, A. E., P. R. Trussell and L. S.
Clesceri. 1985. Standard Methods for the Examination of Water and Wastewater. American Public Health Association. Washington. Habib, M. 2007. Peran Bakteri Pereduksi
Sulfat Pada Pengendalian Air
Asam Tambang.
www.bdpunib.org. (27 Februari 2013).
Hadi, S. 2002. Tinjauan Oseanografi Dalam Pembuatan Tailing di Dasar Laut. Pusat Penelitian
Kelautan ITB.
www.jatam.org/makalah3.htm. ( 27 Februari 2013).
Hards, B. C and J. P. Hinggins. 2004. Bioremediation of Acid Rock Drainage Using SRB. Jacques Whit Environment Limited. Ontario.
Mills, C. 2002. The Role of Micro-Organism in Acid Rock Drainage. www. Envirimine.com. ( 30 Februari 2013).
Moodie, A. D and W. J. Ingledew. 1991. Microbial Anaerobic Respiration. Academic Press Limited.
Nur, M. A. 1989. Teknik Penuntun Praktikum Kimia. Pusat Antar Universitas, Bioteknologi. Institut Pertanian Bogor, Bogor.
Sclegel, H. G dan K. Schmidt. 1994. Mikrobiologi Umum. Gadjah Mada University Press. Yogyakarta.
Voordouw, G. 1995. Minireview, the Genus Desulfovibrio. The Centennial. Appl. Environ. Microbial.