LAPORAN RESMI
PRAKTIKUM REKAYASA BAHAN – P1
PERCOBAAN LOGAM
KOROSI BASAH DAN KOROSI ATMOSFERIK
DIONISIUS ANDY K NRP 2412.100.106
ASISTEN
NUR KHOLIS JAUHARI NRP 2411.100.093
PROGRAM STUDI S1 TEKNIK FISIKA JURUSAN TEKNIK FISIKA
FAKULTAS TEKNOLOGI INDUSTRI
INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
v
HALAMAN PENGESAHAN
LAPORAN RESMI
PERCOBAAN LOGAM KOROSI BASAH DAN
KOROSI ATMOSFERIK
OLEH :
DIONISIUS ANDY K
NRP. 2412.100.106
Surabaya, 17 Desember 2014
Mengetahui/Menyetujui
Asisten
Praktikan
vi
vii
PERCOBAAN LOGAM KOROSI BASAH DAN KOROSI ATMOSFERIK
Nama : DIONISIUS AK NRP : 2412100106
Nama Asisten : NUR KHOLIS JAUHARI
ABSTRAK
Percobaan ini bertujuan untuk mengetahui lebih dalam mengenai korosi pada logam sekaligus dapat mengetahui perbedaan laju korosi dari korosi basah dan atmosferik. Korosi basah adalah korosi yang temapt terjadinya korosi pada larutan sedangkan korosi atmosferik adalah korosi yang terjadi pada udara terbuka. Pada percobaan didapatkan hasil bahwa larutan asam memiliki laju korosi yang lebih besar dibandingkan dengan larutan basa, yaitu laju korosi terbesar terjadi pada larutan HCl. Sedangkan pada akuades, korosi lebih cepat terjadi pada kondisi atmosferik
viii
ix
PERCOBAAN LOGAM KOROSI BASAH DAN KOROSI ATMOSFERIK
Nama : DIONISIUS AK NRP : 2412100106
Nama Asisten : NUR KHOLIS JAUHARI
ABSTRACT
This experiment aims to find out more about the corrosion of the metal as well as to determine differences in the rate of corrosion of wet and atmospheric corrosion. Wet corrosion is corrosion temapt the corrosion of solution while atmospheric corrosion is corrosion that occurs in the open air. In the experiment showed that the acidic solution has a greater corrosion rate compared with an alkaline solution, which is the largest corrosion rates occur in aqueous HCl. While in distilled water, corrosion occurs faster in atmospheric conditions
x
xi
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan rahmat dan anugrahnya, sehingga laporan resmi ini dapat diselesaikan sesuai dengan jadwal yang telah ditentukan. Laporan resmi ini merupakan salah satu persyaratan yang harus dipenuhi setiap praktikan sebelum beranjak ke praktikum berikutnya.
Dalam kesempatan ini penulis mengucapkan banyak terima kasih kepada :
1. Kedua orang tua dan teman-teman yang telah memberikan segala dukungan baik moril maupun materil serta perhatiannya.
2. Dosen pengajar mata kuliah Rekayasa Bahan yang telah membimbing dan memberikan ilmunya.
3. Asisten yang setia membimbing dan mendampingi dari mulai praktikum hingga penyelesaian laporan resmi. Dalam penyusunan laporan resmi ini tentunya masih jauh dari sempurna baik menyangkut isi maupun bahasa yang digunakan sehingga tidak menutup kemungkinan bagi penulis untuk menerima kritik maupun saran yang membangun demi kesempurnaan. Akhir kata, semoga laporan resmi ini dapat bermanfaat bagi penulis khususnya dan bagi semua pihak pada umumnya, semoga laporan ini dapat menambah ilmu pengetahuan dan membuka wawasan bagi yang membacanya.
xii
xii
xiii
DAFTAR GAMBAR
Gambar 2.1 Korosi Seragam 3
Gambar 2.2 Korosi Kawah 4
Gambar 2.3 Korosi Celah 4
Gambar 2.4 Korosi Batas Butir 5
Gambar 2.5 Korosi Tegangan 5
Gambar 2.6 Korosi Erosi 6
Gambar 2.7 Selectif Corrosion 7
Gambar 2.8 Korosi Galvanik 8
Gambar 2.9 Mekanisme Korosi 9 Gambar 4.1 Grafik Hubungan antara Konsentrasi dengan Laju
Korosi pada Korosi Atmosferik 15 Gambar 4.2 Grafik Hubungan antara Konsentrasi dengan Laju
xiv
xv
DAFTAR TABEL
xvi
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Definisi dari korosi adalah perusakan atau penurunan mutu material, sebagai akibat dari reaksi dengan lingkungan nya, atau degradasi logam akibat reaksi redoks antara suatu logam dengan berbagai zat di lingkungannya yang menghasilkan senyawa- senyawa yang tidak dikehendaki.
Pada laporan ini material yang akan dibahas adalah logam, Salah satu material logam yang memiliki aplikasi yang sangat luas di berbagai bidang adalah besi, akan tetapi besi merupakan salah satu material logam yang mudah mengalami korosi, karena serangan kimia oleh lingkungan (uap air,oksigen di atmosfer, oksida asam yang terlarut dalam air), akam membuat beri mengalami oksidasi, sehingga membentuk senyawa oksida besi. Dan menyebabkan besi menjadi berkarat.
Korosi yang terjadi pada logam akan berdampak pada performa dari logam tersebut, yaitu performa mekanik, elektrik maupun termal nya akan berkurang, sehingga akan menyebabkan kerugian. sehingga pengetahuan tentang korosi pada logam sangat dibutuhkan. Makadari itu pada praktikum kali ini adakan dibahas tentang jenis jenis korosi, pengaruh lingkungan pada logam, serta laju korosi.
1.2 Rumusan Masalah
Adapun rumusan masalah yang ingin dibahas didalam praktikum kali ini adalah sebagai berikut :
a. apa saja jenis-jenis korosi ?
2
1.3 Tujuan
Adapun tujuan yang ingin dicapai dalam praktikum kali ini adalah sebagai berikut :
a. Praktikan mengenal jenis-jenis korosi,
BAB II
DASAR TEORI
2.1 Jenis-Jenis Korosi
Korosi adalah degradasi (perusakan atau penurunan kualitas) material akibat interaksi dengan lingkungan. Untuk logam, reaksinya disebut reaksi elektrokimia sedangkan untuk non logam disebut degradasi atau pelapukan. Secara umum, kata korosi identik dengan karat. Jenis-jenis korosi pada logam antara laian adalah sebagai berikut.
Korosi Seragam
Korosi seragam adalah korosi yang terjadi pada permukaan material akibat bereaksi dengan oksigen Biasanya korosi seragam ini terjadi pada material yang memiliki ukuran butir yang halus dan homogenitas yang tinggi.
Gambar 2.1 Korosi Seragam
Korosi Sumuran atau Kawah
Korosi sumuran adalah korosi yang terjadi akibat cacat pada permukaan material seperti celah atau lubang kecil. Pada daerah cacat ini akan lebih anodik dibandingkan permukaan material sehingga korosi akan menuju bagian dalam material.
4
Gambar 2.2
Korosi Kawah
Korosi Celah
Korosi celah adalah korosi yang di temukan pada daerah berkonsentrasi rendah atau korosi yang terjadi pada celah yan terbentuk akibat pendempetan material. Pada celah, kadar oksigen lebih rendah dari lingkungannya sehingga elektron akan berpindah pada kadar oksigen yang tinggi sehingga terjadi korosi. Korosi celah sering terjadi pada sambungan paku.
Gambar 2.3
Korosi Celah
korosi batas butir
10
Dimana presipitat krom karbida terbentuk karena karbon meningkat yang ada di sekitarnya, sehingga krom disekitarnya akan berkurang dan terjadi korosi. Proses terbentuknya presipitat karbon karbida disebut sentisiasi. Terjadi pada temperatur 500-800 sehingga kekurangan krom yang memudahkan terjadinya korosi.
Gambar 2.4
Korosi Batas Butir
Korosi Tegangan
Korosi tegangan adalah korosi yang di sebabkan adanya tegangan tarik yang mengakibatkan terjadinya retak. Tegangan ini di sebabkan pada temperatur dan deformasi yang berbeda.
Berikut retak serta bentuk penjalarannya yang di akibatkan oleh korosi tegangan :
Gambar 2.
5 Korosi Tegangan
4
Korosi Erosi
Korosi erosi adalah korosi yang di sebabkan
oleh erosi yang mengikis lapisan pelindung
material , zat erosi itu dapat berupa fluida yang
mengandung material
abrasive
. Korosi tipe ini
sering di temui pada pipa-pipa minyak.
Gambar 2.
6 Korosi Erosi
Selectif Corrosion
Selectif corrosion adalah korosi yang menyerang unsur di dalam logam akibat perbedaan potensial unsur utamanya. Korosi ini di sebabkan karena komposisi yang tidak merata pada material. Korosi ini biasa terjadi pada pipa-pipa besi cor.
10
Korosi Galvanik
Korosi galvanik adalah korosi yang terjadi pada dua logam yang berbeda jenis jika di hubungkan. Korosi ini juga terjadi karena pasangan elektrikal pada dua logam atau paduan logam yang memiliki perbedaan komposisi. Logam yang lebih anodik akan terkorosi sementara logam lainnya yang lebih katodik akan terlindungi. Posisi logam pada deret volta akan menentukan apakan suatu logam lebih anodik atau katodik
Gambar 2. 8 Korosi Galvanik
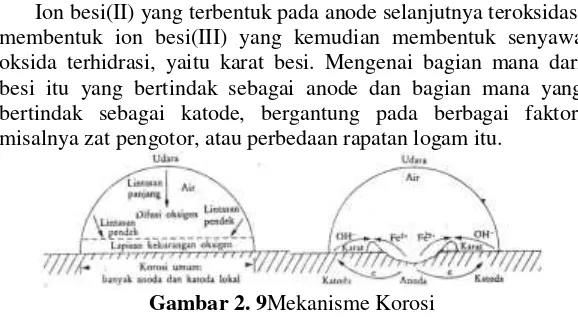
2.2 Mekanisme Korosi
Korosi merupakan proses elektrokimia. Pada korosi besi, bagian tertentu dari besi itu berlaku sebagai anode, di mana besi mengalami oksidasi.
Fe(s) ↔ Fe2+(aq) + 2e ... 1
Elektron yang dibebaskan di anode mengalir ke bagian lain dari besi itu yang bertindak sebagai katode, di mana oksigen tereduksi.
O2(g) + 4H +
(aq) + 4e ↔ 2H2O(l) ... 2
4
atau
O2(g) + 2H2O(l) + 4e ↔ 4OH
-(aq) ... 3
Ion besi(II) yang terbentuk pada anode selanjutnya teroksidasi membentuk ion besi(III) yang kemudian membentuk senyawa oksida terhidrasi, yaitu karat besi. Mengenai bagian mana dari besi itu yang bertindak sebagai anode dan bagian mana yang bertindak sebagai katode, bergantung pada berbagai faktor, misalnya zat pengotor, atau perbedaan rapatan logam itu.
Gambar 2. 9Mekanisme Korosi
2.3 Laju Korosi
Karena hampir semua korosi adalah merupakan suatu reaksi elektrokimia, semua yang mempengaruhi kecepatan suatu reaksi kimia atau jumlah arus yang mengalir akan mempengaruhi laju korosi. Hukum Ohm dapat diterapkan untuk bagian elektrik dari sel korosi. Laju korosi berbanding lurus dengan sejumlah arus yang mengalir pada sel korosi elektrokimia. Jika arus dapat diukur, suatu kalkulasi yang tepat dari kehilangan metal dapat ditentukan. Ini berarti bahwa suatu pengukuran dalam ampere atau milliampere secara matematis dihitung dalam kilogram (pound) per tahun. Suatu Amp tahun adalah satu Ampere yang mengalir selama periode satu tahun. Logam yang berbeda memiliki laju korosi yang berbeda.
Jika diketahui penurunan massa dari suatu material yang terkorosi maka laju korosi dapat dihitung dengan menggunakan rumus sebagai berikut.
10
Dengan K adalah konstanta yang nilainya sebesar 3,45 x 106 untuk mils per year (mpy) dan 8,76 x 104 untuk milimeter per year (mm/y). W adalah pengurangan massa akibat korosi (mg). D adalah massa jenis material (gram/cm3). A adalah luas spesimen yang terkorosi. Dan t adalah lama pengujian.
4
“Halamanini memang dikosongkan”
11
BAB III
METODOLOGI PERCOBAAN
3.1 Alat dan Bahan 3.1.1 Alat
Alat yang digunakan dalam percobaan ini adalah sebagai berikut:
Berikut adalah prosedur percobaan bahan logam: a. Peralatan dan bahan disiapkan.
b. Larutan NaOH dengan molaritas sebesar 0,5 M, 1 M, dan 3 M dibuat masing-masing dalam sebuah gelas plastik. c. Larutan HCl dengan molaritas sebesar 0,5 M, 1 M, dan 3
M dibuat masing-masing dalam sebuah gelas plastik. d. Larutan NaCl dengan molaritas sebesar 0,5 M, 1 M, dan 3
M dibuat masing-masing dalam sebuah gelas plastik. e. Gelas berisi aquades disiapkan dan kesepuluh gelas
tersebut ditandai.
f. 20 buah paku dibersihkan dan diamplas hingga bersih mengkilat.
12
hingga basah ke dalam masing-masing larutan.
i. Paku-paku yang telah dicelup diletakkan di atas wadah plastik kemudian waktu peletakkannya dicatat.
j. Untuk korosi basah, masing-masing paku dimasukkan ke dalam tiap larutan dan waktu saat paku dimasukkan dicatat.
k. Semua paku dibiarkan selama 3 hari.
l. Setelah 3 hari, keadaan masing-masing paku dicatat. m.Masing-masing paku dibersihkan kembali dengan amplas,
dan waktu saat paku dibersihkan dicatat.
n. Masing-masing paku ditimbang dan dicatat beratnya. o. Laju korosi masing-masing paku dihitung.
13
BAB IV
ANALISA DATA DAN PEMBAHASAN
4.1 Analisa Data
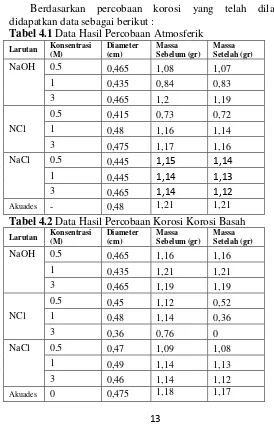
Berdasarkan percobaan korosi yang telah dilakukan didapatkan data sebagai berikut :
Tabel 4.1 Data Hasil Percobaan Atmosferik
Larutan Konsentrasi
Tabel 4.2 Data Hasil Percobaan Korosi Korosi Basah
14
Untuk menghitung laju korosi masing-masing paku pada setiap larutan, maka digunakan rumus laju korosi sebagai berikut.
asumsi semua paku memiliki panjang 2,9 cm. Dengan pendekatan volume paku ekivalen dengan volume tabung, maka
Dan luas permukaan paku adalah Dengan menggunakan rumus laju korosi di atas, maka laju korosi pada percobaan korosi atmosferik dan korosi basah adalah sebagai berikut.
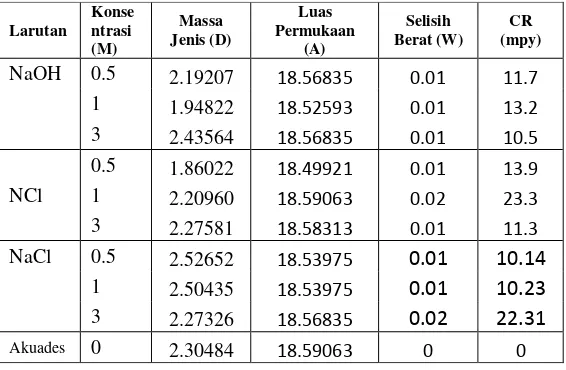
Tabel 4.3 Data Hasil Penghitungan Korosi Atmosferik
15
Tabel 4.3 Data Hasil Penghitungan Korosi Basah
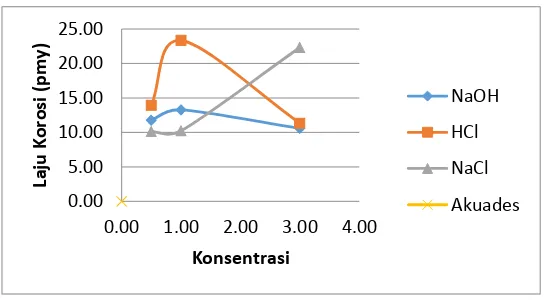
Melalui data tersebut diatas dapat dilihat pada grafik perbedaan laju korosi atmosferik maupun korosi basah untuk setiap larutan pada gambar 4.1 dan 4.2 berikut.
Gambar 4.1 Grafik Hubungan antara Konsentrasi dengan Laju Korosi pada Korosi Atmosferik
0.00
0.00 1.00 2.00 3.00 4.00
Laj 1 2.80637 18.52593 0.00 0.0 3 2.41534 18.56835 0.00 149.56 0.5 2.42734 18.54679 0.60 638.6 HCl 1 2.17150 18.59063 0.78 925.8
3 2.57363 18.43223 0.76 767.6
NaCl 0.5 2.16555 18.57570 0.01 11.9 1 2.08377 18.60587 0.01 12.3 3 2.36443 18.56109 0.02 21.8
16
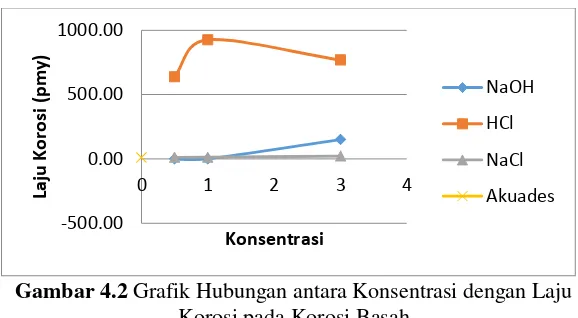
Gambar 4.2 Grafik Hubungan antara Konsentrasi dengan Laju Korosi pada Korosi Basah
4.2 Pembahasan
Dari percobaan dan perhitungan laju korosi yang telah dilakukan, laju korosi terbesar ada pada paku yang direndam pada larutan HCL dengan konsentrasi 1 M, yaitu memiliki laju korosi sebesar 925 mpy. Hal ini disebabkan karena HCl merupakan asam kuat yang bersifat korosif sehingga mempunyai kemampuan oksidasi yang tinggi. Sedangkan pada larutan NaOH dengan kosentrasi 0.5 dan 1 M laju korosinya nol, tetapi pada konsentrasi 3 M laju korosinya 149.56 mpy, hal tersebut sesuai degan teori karena semakin meningkat konsentrasi suatu larutan maka akan semakin banyak elektroda yang dihasilkan untuk reaksi redoks, sehingga laju korosi meningkat. Pada larutan NaCl laju korosi juga meningkat seiring dengan peningkatan konsentrasi larutan, dan ljau korosi paling kecil ada pada akuades.
Secara umum, laju korosi pada percobaan korosi atmosferik lebih kecil dari percbaan korosi basah. Hal ini disebabkan karena pada percobaan korosi basah selalu terjadi reduksi H2O pada sampel logam paku yang akan menyebabkan laju korosi menjadi lebih besar.
Jika diurutkan dari larutan yang memiliki tingkat keasaman tinggi (paling korosif) sampai lariat yang netral, maka urutan dari larutan yang dipakai sebgai larutan uji korosi adalah sebagai berikut HCL, NaCl, NaOH dan H2O, seharusnya laju korosi paku
17
18
19
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Beberapa hal yang dapat disimpulkan dari percobaan ini adalah sebagai berikut :
1. Korosi lebih cepat terjadi pada larutan yang bersifat asam
dibandingkan dengan larutan yang bersifat basa,
2. Semakin asam suatu larutan maka laju korosi semakin
besar,
3. Laju korosi pada percobaan korosi basah lebih cepat
daripada percobaan korosi atmosferik.
5.2 Saran
Adapun saran yang dapat diberikan setelah melakukan percobaan sebagai berikut :
1. Skala pada gelas ukur agar lebih kecil lagi sehingga dapat menakar larutan yang bervolume kecil.
20
29 DAFTAR PUSTAKA