BAB II
TINJAUAN PUSTAKA
2.1 Selulosa
2.1.1 Struktur Selulosa
Selulosa merupakan salah satu polimer yang tersedia melimpah di alam. Produksi selulosa sekitar 100 milyar ton setiap tahunnya. Sebagian dihasilkan dalam bentuk selulosa murni seperti yang terdapat dalam rambut biji tanaman kapas.Namun paling banyak adalah yang berkombinasi dengan lignin dan polisakarida lain seperti hemiselulosa dalam dinding sel tumbuhan berkayu, baik pada kayu lunak dan keras, jerami atau bambu. Selain itu selulosa juga dihasilkan oleh bakteri Acetobacter xylinum secara ekstraseluler (Klemm, dkk., 1998a). Senyawa ini juga dijumpai dalam plankton bersel satu atau alga di lautan, juga pada jamur dan bakteri (Potthast, dkk., 2006; Zugenmaier, 2008).Sebagai bahan baku kimia, selulosa telah digunakan dalam bentuk serat atau turunannya selama
sekitar 150 tahun (Habibi, dkk., 2010).
Selulosa pertama kali dijelaskan oleh Anselme Payen pada 1838 sebagai serat padat yang tahan dan tersisa setelah pemurnian jaringan tanaman dengan asam dan amonia (Brown dan Saxena, 2007). Payen mengamati bahwa bahan yang telah dimurnikan mengandung satu jenis senyawa kimia yang seragam, yaitu karbohidrat. Hal ini berdasarkan residu glukosa yang mirip dengan pati. Payen
β-1,4-glikosida
juga mengatakan bahwa selulosa adalah isomer dari bahan penyusun pati (Zugenmaier, 2008).
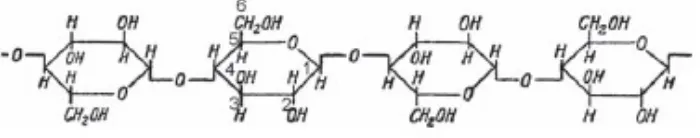
Selulosa tersusun dari unit-unit anhidroglukopiranosa yang tersambung dengan ikatan β-1,4-glikosidik membentuk suatu rantai makromolekul tidak bercabang. Setiap unit anhidroglukopiranosa memiliki tiga gugus hidroksil (Potthast, dkk., 2006; Zugenmaier, 2008), seperti yang terlihat pada Gambar 2.1. Selulosa mempunyai rumus empirik (C6H10 O5)n dengan n ~ 1500 dan berat
molekul ~ 243.000 (Rowe, dkk., 2009).
Gambar 2.1. Struktur selulosa (Zugenmaier, 2008)
juga higroskopis. Bahkan dalam keadaan basah, serat selulosa alami tidak kehilangan kekuatannya (Zugenmaier, 2008).
Turunan selulosa telah digunakan secara luas dalam sediaan farmasi seperti etil selulosa, metil selulosa, karboksimetil selulosa, dan dalam bentuk lainnya yang digunakan dalam sediaan oral, topikal, dan injeksi. Sebagai contoh, karboksimetil selulosa merupakan bahan utama dari SeprafilmTM, yang digunakan
untuk mencegah adesi setelah pembedahan. Baru-baru ini, penggunaan selulosa mikrokristal dalam emulsi dan formulasi injeksi semipadat telah dijelaskan. Penggunaan bentuk-bentuk selulosa dalam sediaan disebabkan sifatnya yang inert dan biokompatibilitas yang sangat baik pada manusia (Jackson, dkk., 2011).
2.1.2 Sifat Fisika Kimia
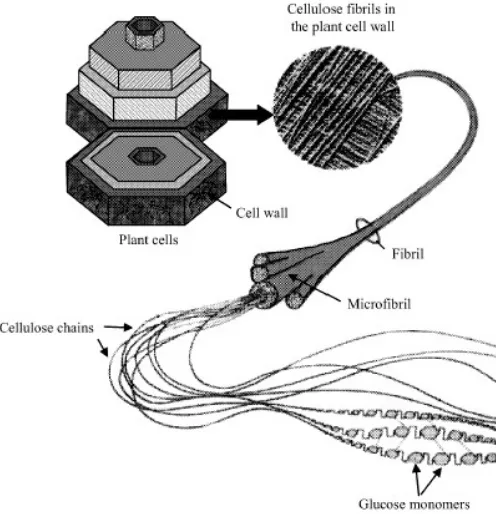
Bahan berbasis selulosa sering digunakan karena memiliki sifat mekanik yang baik seperti kekuatan dan modulus regang yang tinggi, kemurnian tinggi, kapasitas mengikat air tinggi, dan struktur jaringan yang sangat baik (Gea, dkk., 2011). Pada Gambar 2.2 dapat dilihat lapisan-lapisan dinding sel kayu dan selulosa mikrofibril. Dinding sel kayu dibagi dalam beberapa lapisan yaitu lamela tengah (LT), dinding sel primer (P), dan dinding sel sekunder (S) (dinding sekunder terbagi dalam lapisanS1, S2, dan S3). Lapisan-lapisan ini mempunyai struktur dan komposisi kimia yang berbeda.
Selulosa merupakan polimer yang relatif stabil dikarenakan adanya ikatan hidrogen. Selulosa tidak larut dalam pelarut air dan tidak memiliki titik leleh. Serat selulosa juga memiliki fleksibilitas dan elastisitas yang baik sehingga dapat mempertahankan aspect ratio (perbandingan panjang terhadap diameter (P/d)) yang tinggi selama proses produksi. Selulosa nanoserat memiliki beberapa
Serat selulosa dalam dinding sel tanaman
Sel tanaman
Dinding sel
Serat Mikroserat
Monomer-monomer glukosa Rantai selulosa
S S1 S2 S3 P LT
keuntungan seperti: densitas rendah, sumber yang dapat diperbaharui, biodegradable, mengurangi emisi karbondioksida di alam, kekuatan dan modulus yang tinggi, permukaan yang relatif reaktif sehingga dapat digunakan untuk grafting beberapa gugus kimia, dan harga yang murah (Frone, dkk., 2011).
Gambar 2.2. Kumpulan rantai selulosa dalam mikrofibril yang membentuk dinding sel tanaman (Modifikasi dari Djerbi, 2005).
2.1.3 Sumber Selulosa
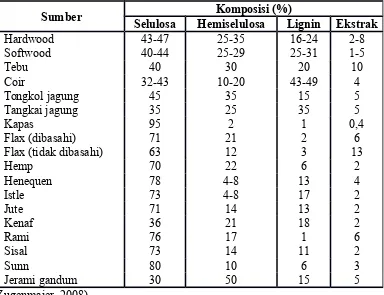
seperti tongkol jagung (Ohwoavworhua dan Adelakun, 2005b), rambut biji dari Cochlospermum planchonii (Ohwoavworhua dan Adelakun, 2005a), ampas tebu (Sun, dkk., 2004), jerami (Ilindra dan Dhake, 2008), lenan (Leppanen,dkk., 2009).
Tabel 2.1. Senyawa kimia yang terdapat dalam beberapa bahan yang mengandung selulosa
Flax (tidak dibasahi) 63 12 3 13
secara mekanis. Secara kimia proses pulping dapat dilakukan dengan proses sulfit, basa, dan sulfat untuk melarutkan lignin dan hemiselulosa, dan meninggalkan senyawa selulosa sebagai bentuk padatan. Proses sulfit menggunakan campuran asam sulfit (H2SO3) dan ion bisulfit (HSO3-) untuk melarutkan lignin sebagai asam
lignosulfonat yang dapat larut dalam larutan pemasak. Pada proses basa kayu dimasak dengan larutan NaOH. Proses sulfat (Kraft) menggunakan larutan NaOH dan Na2S. Penggunaan kedua bahan ini akan meningkatkan delignifikasi dan
kekuatan pulp (Klemm, dkk., 1998a). Metode lain yang dapat digunakan untuk delignifikasi adalah dengan metode ledakan uap (steam explosion). Pada metode ini potongan kayu akan diberikan tekanan dan suhu yang tinggi dengan menggunakan autoklaf (Othmer, 1993).
Sumber lain selulosa adalah hasil biosintesis selulosa oleh mikroorganismeseperti bakteri, alga, dan jamur. Alga dan jamur menghasilkan selulosa melalui sintesis in vitro secara enzimatik dari selobiosil fluorida, dan kemosintesis dari glukosa dengan pembukaan cincin polimerisasi turunan benzil dan pivaloyl. Dari ketiga mikroorganisme tersebut, hanya spesies Acetobacter xylinum yang diketahui dapat menghasilkan selulosa dalam jumlah besar. Sumber selulosa lain adalah dari hewan, yang disebut tunicin atau selulosa hewan karena diperoleh dari organisme bahari tertentu dari kelas Tunicata (Gea, 2010).
2.1.4 Struktur Kristal dari Selulosa
struktur selulosa bisa dilakukan dengan difraksi X-Ray, NMR, dan FTIR (Klemm, dkk., 1998a; Gea, 2010).
Selulosa I merupakan bentuk asli selulosa yang terdiri dari dua kristal allomorf, yaitu Iα dan Iβ. Berdasarkan pengujian difraksi elektron selulosa Iαmemiliki satu unit sel triklinik, sedangkan selulosa Iβ memiliki dua unit sel monoklinik, keduanya tersusun dalam satu susunan rantai paralel, dengan rasio berbeda dalam satu serat, tergantung pada asalnya. Selulosa Iα banyak terdapat pada selulosa bakteri dan valonia, sedangkan Iβ pada selulosa kapas atau kayu (Klemm, dkk., 1998a).
Selain selulosa I, terdapat selulosa II yang terbentuk dengan pengendapan selulosa dari larutan ke dalam medium air pada suhu kamar atau sedikit lebih tinggi dari suhu kamar pada proses pemintalan serat selulosa buatan manusia secara teknis. Selulosa II ini juga diperoleh dari proses merserisasi kapas, yang terjadi melalui pembentukan natrium selulosa melalui interaksi polimer dengan cairan natrium hidroksida dan peruraian dengan netralisasi atau penghilangan natrium hidroksida. Proses transformasi dari selulosa I menjadi selulosa II biasanya irreversible, walaupun ada yang menyatakan bahwa natrium selulosa dapat diretransformasi sebagian menjadi selulosa I. Sistem ikatan hidrogen selulosa II lebih rumit daripada selulosa I dan menghasilkan densitas tautan silang intermolekul yang lebih tinggi (Mandal, 2011; Klemm, dkk., 1998a).
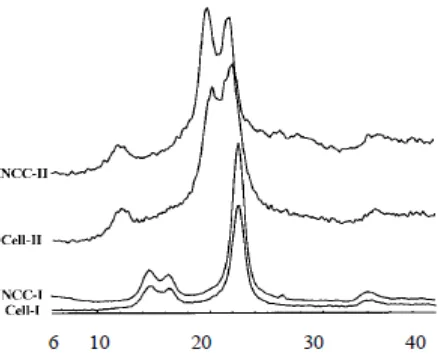
Gambar 2.3. Difraktogram difraksi X-Ray dari selulosa dan selulosa nanokristal linter (Li, dkk., 2003).
Li, dkk. (2003) melakukan kondensasi selulosa alam (linter) yang memiliki struktur kristal I dengan NaOH 18% dan menghasilkan struktur kristal baru, yaitu struktur kristal II. Perlakuan terhadap selulosa nanokristal (nanocrystalline cellulose, NCC) dengan struktur kristal I menggunakan NaOH 4% juga menghasilkan NCC dengan struktur kristal II. Struktur kristal selulosa dan NCC dari penelitian Li, dkk. (2003) ini dapat dilihat pada Gambar 2.3.
Struktur selulosa III dan IV diturunkan dari selulosa I atau II, disebut dengan selulosa IIII, IVI, dan IIIII dan IVII. Selulosa III diperoleh dari perlakuan
selulosa I atau II dengan cairan amoniak dibawah -30 oC dan rekristalisasi sampel
dengan evaporasi amoniak (Klemm, dkk., 1998a).
2.1.5 Biosintesis
Hemiselulosa Ada 3 (tiga) cara sintesis selulosa adalah sebagai berikut:
1. Biosintesis dalam organisme hidup 2. Sintesis enzimatik in vitro
3. Sintesis kimia dengan polimerisasi dari monomer yang sesuai (Klemm, dkk., 1998b).
Biosintesis selulosa merupakan proses yang sangat kompleks, tidak hanya pada pembentukan rantai β-1,4-glukan, tetapi juga pada penetapan susunan supramolekuler dan serat dalam polimer padat yang terbentuk. Mekanisme pembentukan selulosa dianggap berbeda pada tumbuhan tinggi dan bakteri atau alga. Biosintesis selulosa pada tumbuhan tinggi dapat dilihat pada Gambar 2.4. Proses biosintesis diawali dengan konversi β-fruktosa-6-P menjadi α-glukosa-6-fosfat oleh enzim glukosa-6-α-glukosa-6-fosfat isomerase, kemudian menjadi α-glukosa-1-P oleh enzim fosfoglukomutase. α-glukosa-1-P diubah menjadi UDP (uridin difosfatase)-glukosa oleh UTP (uridin trifosfatase)-glukosa-1-fosfat uridil transferase. Dengan bantuan enzim selulosa sintase UDP-glukosa diubah menjadi selulosa. Selain dari fruktosa, selulosa juga bisa dihasilkan dari sukrosa. Enzim sukrosa sintase akan mengubah sukrosa menjadi UDP-glukosa, selanjutnya menjadi selulosa dengan bantuan selulosa sintase (Brown dan Saxena, 2007).
Gambar 2.4. Sintesis selulosa yang dipengaruhi oleh enzim pada Populus trimula
(L) (Modifikasi dari Brown dan Saxena, 2007)
Sintesis selulosa in vitrosecaraenzimatik diketahui ada 2 (dua) cara:
1. Mereaksikan UDP-glukosa dengan selulosa sintase yang dimurnikan 2. Kondensasi glukosa atau turunannya oleh selulase (Klemm, dkk., 1998b)
2.2 Selulosa Mikrokristal
Selulosa mikrokristal telah dibuat dari beberapa sumber alam, seperti dari serat rami, kulit kapas, ampas tebu, jerami, lenan dengan cara menghidrolisis α-selulosa dengan larutan asam encer pada suhu tinggi. Pada proses hidrolisis asam, bagian non kristalin terhidrolisis dan bagian kristal dilepaskan (Terinte, dkk., 2011). Hidrolisis α-selulosa ini akan mengakibatkan pemendekan rantai, sehingga selulosa mikrokristal memiliki rumus molekul (C6H10O5)n, dimana n ~ 220,
dengan berat molekul: ~ 32.400 (Ohwoavworhua dan Adelakun, 2005a; Bhimte dan Tayade, 2007; Ilindra dan Dhake, 2008; Leppanen, dkk., 2009; Rowe, dkk., 2009).
industri makanan, komposit dalam kayu, industri plastik, dan kosmetik (Terinte, dkk., 2011). Selulosa mikrokristal dianggap sebagai bahan tambahan terbaik untuk pembuatan tablet cetak langsung(Bhimte dan Tayade, 2007; Bushra,dkk., 2008), bisa sebagai bahan pengisi, pengikat pada tablet dengan konsentrasi 20%-90%, penghancur tablet dengan konsentrasi 5%–20%(Soekemi, dkk., 1987; Gohel dan Jogani, 2005; Rowe, dkk., 2009).
Karakteristik selulosa mikrokristal menurut USP 32-NF 27 meliputi uji identifikasi, sifat fisika dan kimia, cemaran mikroba, dan lethal dose 50% (LD50).
Spesifikasi selulosa mikrokristal menurut USP 32-NF 27 dapat dilihat pada Tabel 2.2 berikut ini.
Tabel 2.2. Spesifikasi selulosa mikrokristal menurut USP 32-NF 27
Pengujian USP 32-NF 27
Organoleptik Berwarna putih, tidak berbau dan berasa Identifikasi Berwarna biru violet dengan ZnCl2
Selulosa mikrokristal banyak digunakan sebagai eksipien pada pembuatan tablet cetak langsung. Sifat alir dari bahan tambahan adalah penting untuk diketahui. Hal ini berkaitan dengan penanganan dan pencetakan bahan serbuk, khususnya untuk bahan tambahan tablet cetak langsung. Kemampuan mengalir suatu bahan serbuk dapat dilihat pada Tabel 2.3 di bawah ini.
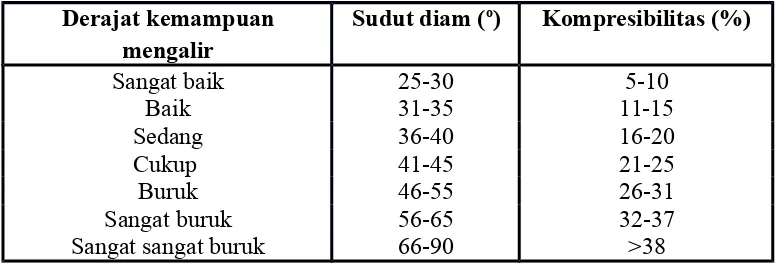
Tabel 2.3. Tabel kemampuan mengalir serbuk menurut Carr
Derajat kemampuan
Berdasarkan Table 2.3 di atas, sudut diam memberikan penilaian terhadap pergesekan internal dan kohesif. Nilai sudut diam hingga 40o menunjukkan
potensi untuk mengalir sedangkan sudut yang lebih besar dari 50o menunjukkan
serbuk tidak dapat mengalir bebas,sedangkan bahan dengan kompresibilitas lebih dari 38% akan sulit untuk keluar dari hopper(Bhimte dan Tayade, 2007).
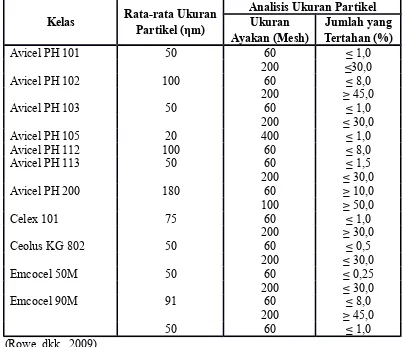
Selulosa mikrokristal dapat diperoleh secara komersial dengan berbagai kualitas dan merek dagang, diantaranya Avicel PH, Cellets, Celex, hellolosum mikrokristallinum, Celphere, Ceolus KG, Comprecel, Emcocel, Ethisphere, Fibrocel, Pharmacel, dan lain-lain. Selulosa mikrokristal tersedia dalam berbagai kelas (grade) berdasarkan analisis ukuran partikel (Tabel 2.4) (Rowe, dkk, 2009).
Tabel 2.4. Beberapa merek dagang dan kelas dari selulosa mikrokristal
Polimer alam seperti protein, selulosa, dan karet telah dikenal dan
dimanfaatkan manusia berabad-abad untuk berbagai keperluan. Polimer tinggi adalah
molekul besar yang dibangun oleh pengulangan kesatuan kimia yang kecil dan
sederhana. Akibatnya, molekul-molekul polimer umumnya mempunyai berat molekul
yang sangat besar. Apabila satuan itu berulang lurus seperti rantai, maka
molekul-molekul polimer seringkali digambarkan sebagai molekul-molekul rantai atau rantai polimer.
Panjang rantai polimer dapat dinyatakan dalam DP dari polimer yang bersangkutan,
yaitu jumlah kesatuan berulang dalam rantai polimer. Jumlah unit glukosa di dalam
molekul selulosa dapat dilihat melalui derajat polimerisasinya (Purwaningsih, 2012).
Berat molekul dari suatu makromolekul adalah perkalian DP dengan berat molekul
unit strukturnya (Stevens, 2001).
DP selulosa sangat bervariasi, bergantung pada sumber dan perlakuan yang
diberikan. Perlakuan kimia secara intensif seperti pembuatan pulp, pengelantangan,
dan transformasi akan sangat menurunkan harga DP. Proses delignifikasi dan
ekstraksi juga dapat menurunkan DP selulosa. Selain itu, semakin tua umur pohon,
maka DP juga semakin menurun (Wegener, 1985).
Penentuan DP biasanya dilakukan dengan menentukan viskositas sampel
setelah sampel dilarutkan dalam pelarut kompleks berair, seperti cuprammonium
hidroksida (Cuam) atau cupri etilen diamin (CED). DP dari polimer sangat
menentukan tingkat viskositas larutan pada konsentrasi polimer yang diberikan
(Klemm, 1998).
2.4 Selulosa Nanokristal
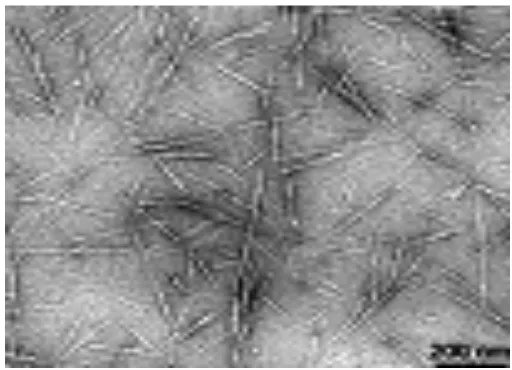
bahwa degradasi diinduksi dengan pendidihan serat selulosa dalam larutan asam mencapai suatu batas setelah perlakuan dalam waktu tertentu. Gambar 2.5transmission electron microscopy (TEM) dari suspensi kering menunjukkan adanya partikel berbentuk jarum dan analisis selanjutnya dengan difraksi elektron menunjukkan adanya kesamaan struktur kristal seperti serat aslinya (Habibi, dkk.,, 2010).
Gambar 2.5. Gambar TEM selulosa nanokristal dari sisal (Garcia, dkk., 2006)
Selulosa nanokristal telah diisolasi dari berbagai sumber selulosa, termasuk tanaman, selulosa mikrokristal, hewan, bakteri, dan alga. Kapas adalah salah satu sumber selulosa yang memiliki kandungan selulosa tinggi (94%) (Oksman dan Mathew, 2007; Klemm, dkk., 2011).
2.4.1 Pembuatan dan Karakterisasi Selulosa Nanokristal
Proses utama untuk menghasilkan selulosa nanokristal dari serat selulosa adalah berdasarkan hidrolisis asam. Bagian amorf akan lebih mudah dihidrolisis, sedangkan bagian kristal yang lebih tahan terhadap serangan asam akan tersisa (Habibi, dkk., 2010).
Prosedur khas yang dilakukan untuk menghasilkan selulosa nanokristal adalah menghidrolisis selulosa murni dengan asam kuat dalam kondisi temperatur, pengadukan, dan waktu yang terkendali. Proses kimia dimulai dengan penghilangan ikatan antar polisakarida pada permukaan serat selulosa dan diikuti dengan pecah dan rusaknya bagian amorf sehingga melepaskan bagian kristal selulosa. Setelah hidrolisis dilakukan, suspensi yang dihasilkan diencerkan dengan air, dan dicuci dengan beberapa kali sentrifugasi. Kemudian dialisis dilakukan untuk menghilangkan molekul asam bebas dari dispersi dan memisahkan partikel yang berukuran lebih kecil dan lebih besar dari pori-pori membran dialisis yang digunakan. Tahap selanjutnya adalah proses mekanik seperti sonikasi yang akan menghilangkan pengotor yang masih melekat pada selulosa nanokristal sehingga diperoleh nanokristal yang terdispersi dalam suspensi yang stabil. Struktur, sifat, dan tahap pemisahan tergantung pada asam mineral dan konsentrasi yang digunakan, temperatur dan waktu hidrolisis, serta intensitas ultrasonikasi (Habibi, dkk., 2010; Klemm, dkk., 2011).
asam klorida dan asam sulfat memberikan bentuk sferis pada nanokristal. Bentuk sferis memiliki gugus sulfat yang lebih sedikit pada permukaannya (Habibi, dkk., 2010).
Konsentrasi asam sulfat yang digunakan tidak banyak bervariasi dari konsentrasi 65% (b/b), temperatur dapat berada pada rentang suhu kamar sampai 70oC, waktu hidrolisis dapat berbeda dari 30 menit sampai 1 malam tergantung
suhu yang digunakan. Hidrolisis dengan asam klorida dapat dilakukan pada temperatur refluks dengan konsentrasi asam antara 2,5-4 N dengan variasi suhu tergantung pada sumber selulosa yang digunakan (Habibi, dkk., 2010). Bondeson, dkk. (2006) telah meneliti kondisi optimum hidrolisis dengan menggunakan selulosa mikrokristal dari Norway spruce (Picea abies) sebagai bahan awal selulosa. Faktor yang divariasikan selama proses adalah konsentrasi selulosa mikrokristal dan asam sulfat, waktu dan temperatur hidrolisis, dan waktu tritmen dengan ultrasonik. Penelitian ini menunjukkan bahwa konsentrasi asam sulfat 63,5% (b/b) dengan waktu hidrolisis sekitar 2 jam, telah menghasilkan selulosa nanokristal dengan rendemen 30% dari berat awal dan memiliki panjang 200-400 nm dan lebar kurang dari 10 nm. Perpanjangan waktu hidrolisis menghasilkan nanokristal yang lebih pendek dan menambah muatan permukaan. Ukuran dan morfologi nanokristal tergantung pada sumber selulosa: selulosa tunicate dan alga memiliki panjang beberapa mikron, sedangkan serat kayu menghasilkan nanokristal yang lebih pendek (Klemm, dkk., 2011; Frone, dkk., dkk., 2011).
Yu, dkk. (2012) telah membuat selulosa nanokristal dari pulp bambu. Pada proses ini digunakan asam sulfat dengan konsentrasi 46%, suhu dan waktu hidrolisis berturut-turut 55oC dan 30 menit. Selulosa nanokristal yang dihasilkan
memiliki panjang 200-500 nm dan diameter kurang dari 20 nm. Hasil uji FTIR menunjukkan spektrum yang sama dengan pulp bambu. Derajat kristalinitas selulosa nanokristal bambu 71,98%. Hal ini dikarenakan bagian amorf telah banyak dihilangkan pada saat hidrolisis dengan asam sulfat. Selulosa nanokristal yang diperoleh dari hasil hidrolisis Luffa cylindrica dengan asam sulfat 65% memiliki bentuk whisker dengan derajat kristalinitas 96,5%.
Chang, dkk. (2010) telah membuat selulosa nanokristal dari cotton linter dengan menggunakan variasi konsentrasi asam sulfat 50%-60%, temperatur 45– 55oC, dan waktu hidrolisis 5-15 menit. Hasil selulosa nanokristal yang terbaik
adalah yang diperoleh dari hidrolisis dengan asam sulfat 60%, temperatur 45oC,
dan waktu reaksi 5 menit. Selulosa nanokristal ini memiliki bentuk jarum, gugus fungsi yang tidak berbeda dengan selulosa kapas, dan temperatur degradasi yang lebih rendah dari kapas dan selulosa nanokristal lain.
Selulosa nanokristal mempunyai rasio luas permukaan dan volume yang sangat besar (Habibi, dkk., 2010; Liu, dkk., 2010). Luas permukaan yang sangat besar ini merupakan suatu keuntungan dari selulosa nanokristal yaitu memungkinkan untuk lebih banyak obat dapat berikatan dan berinteraksi dengan permukaannya (Jackson, dkk., 2011).
2.4.2 Aplikasi Selulosa Nanokristal
konstruksi, biomedik, kosmetik, industri kertas, pengemasan, bahan bangunan, tekstil, dan lain-lain (Frone, dkk., 2011).
Sifat mekanik film nanokomposit tergantung pada ukuran dan morfologi dari dua bahan yang digunakan, yaitu selulosa nanokristal dan matriks polimer, juga teknik pembuatannya. Aspect ratio merupakan faktor utama yang mengendalikan sifat mekanik dari nanokomposit. Pengisi dengan aspect ratio yang tinggi memberikan efek penguatan yang sangat baik. Telah dilaporkan bahwa modulus tertinggi meningkat dalam matriks karet dari poli(S-co-BuA) dan stabilitas termal diperoleh dengan menggunakan whiskers tunicin (P/d ~ 67) dibandingkan dengan whisker bakteri (P/d ~ 60) dan Avicel (P/d ~ 10) (Peng, dkk., 2011).
Selulosa nanokristal dapat digunakan sebagai bahan tambahan pada sistem penyampaian obat. Bahan ini berikatan dengan obat yang larut dalam air dan terionisasi (tetrasiklin dan doksorubisin) yang memberikan pelepasan obat dengan segera. Setil trimetilamonium bromide berikatan dengan permukaan selulosa nanokristal, sehingga meningkatkan potensial zeta dari -55 mV ke 0 mV dan mengakibatkan obat-obat hidrofob seperti paclitaxel, docetaxel, dan etoposida dilepaskan dengan cara terkendali lebih dari dua hari (Jackson, dkk., 2011).
2.5 Arenga pinnata (Wurmb) Merr.
Sistematika dan identifikasi tanaman aren adalah sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta Class : Dicotyledoneae
Ordo : Arecales
Famili : Arecaceae
Genus : Arenga
Spesies : Arenga pinnata (Wurmb) Merr. Nama lokal : Aren (Corner dan Watanabe, 1969)
Tanaman aren (Arenga pinnata (Wurmb) Merr.) atau Arenga saccharifera Labill merupakan tumbuhan palam rumbai yang terkenal. Tumbuhan ini banyak didapati di seluruh Nusantara. Pohon aren ini tumbuh mulai dari ketinggian di atas permukaan laut hingga 1220 m lebih di alam liar dan tidak jarang dibudidayakan. Pohon aren mempunyai tinggi batang mencapai 25 m dengan diameter 65 cm. Bunga aren ini terdiri dari bunga jantan dan betina. Kedua bunga terpisah pada masing-masing tandan (spadix). Bunga jantan berwarna kecoklatan dan bunga betina kehijauan. Bunga betina menghasilkan sedikit atau tidak menghasilkan nira sama sekali, oleh karena itu bunga betina dibiarkan menjadi buah (Heyne, 1987).
Kolang-kaling dapat dihasilkan rata-rata sebanyak 100 kg/pohon/tahun bila tidak disadap niranya (Anonim, 2009). Kolang-kaling merupakan makanan berserat, memiliki kadar air sangat tinggi, hingga mencapai 93,8% dalam setiap 100 gramnya. Kolang-kaling juga mengandung protein, karbohidrat, dan serat kasar. Komponen utama polisakarida yang terdapat dalam kolang-kaling adalah polisakarida yang larut air yaitu galaktomanan (Rao, dkk., 1961; Tarigan dan Kaban, 2010). Galaktomanan yang terdapat dalam kolang-kaling memiliki perbandingan manosa:galaktosa sebesar 2,26:1 (Koiman, 1971).
Kulit buah (exocarp) berwarna hijau ketika masih muda dan kuning kecoklatan bila sudah tua. Daging buah (mesocarp) berwarna kuning keputihan, lunak dan dapat menyebabkan gatal, kulit biji (endocarp) relatif tipis, berwarna kuning kecoklatan waktu masih muda, menjadi hitam dan sangat keras bila sudah tua (Miller, 1964).
Aren merupakan tanaman serbaguna. Bisa dikatakan semua bagian dari tanaman aren dapat dimanfaatkan. Akarnya untuk bahan anyaman dan cambuk, batang yang dibelah sebagai talang (saluran air), kayunya digunakan untuk tongkat jalan, tulang daun untuk keranjang dan sapu, daun muda sebagai pengganti kertas rokok, serabut pelepah untuk tali ijuk, keranjang, sapu, dan sikat, empulur batang diolah menjadi pati yang dapat digunakan untuk pembuatan kue. Biji buahnya dibuat manisan dan dimakan (kolang-kaling). Cairan pada tongkol bunga jantan disadap karena mengandung gula, biasa disebut nira. Nira ini kemudian dibuat gula aren, kalau dikhamirkan menghasilkan sagu air, tuak (arak) atau cuka (Yuniarti, 2008). Selain itu, hasil fermentasi, destilasi, dan dehidrasi dari
nira dapat menghasilkan bioetanol dengan kadar etanol sekitar 95% (Effendi, 2010).
2.6 Tandan Aren
Tandan buah pohon aren (Gambar 2.6) terdiri dari banyak tangkai yang panjangnya kira-kira 2 kaki (60,96 cm). Semua tandan bergantungan pada sebuah tangkai yang lebih besar dan penuh dengan buah yang berwarna hijau bila masih muda dan coklat kekuning-kuningan bila masak. Kadang-kadang pada satu pohon terdapat 4 sampai 5 tandan buah aren yang masing-masing mempunyai bobot sekitar 100 kg (Heyne, 1987).
Gambar 2.6. Tandan buah aren (http://www.pantonanews.com)
kaling yang pemasarannya menjangkau Jakarta, Medan, Batam, Pekan Baru, Aceh, bahkan sampai ke Malaysia. Buah kolang kaling diperoleh dari para pengumpul yang berasal dari daerah Langkat, Dairi, Padang Sidempuan, dan Pakpak Barat (Anonim, 2012). Buah aren yang bijinya akan diolah menjadi kolang kaling dibawa ke pabrik masih lekat pada tandannya.
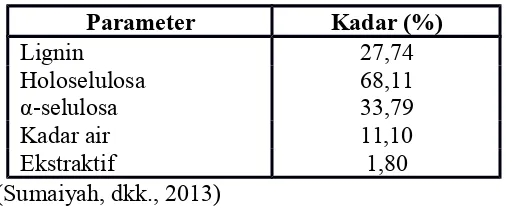
Tandan aren ini merupakan bagian dari tanaman aren yang berkayu dan memiliki sifat fisik yang kuat karena menjadi tempat bergantung banyak buah. Beberapa komponen senyawa kimia yang terdapat pada tandan aren dapat dilihat Tabel 2.5.
Tabel 2.5. Komponen kimia tandan aren
Parameter Kadar (%)
Lignin 27,74
Holoselulosa 68,11
α-selulosa 33,79
Kadar air 11,10
Ekstraktif 1,80
(Sumaiyah, dkk., 2013)
Pada industri kolang-kaling terdapat limbah padat berupa tandan dan kulit buah aren. Tandan aren yang telah diambil buahnya dibiarkan bertumpuk dan mengering. Pemanfaatan tandan aren ini masih sangat terbatas, yaitu hanya sebagai kayu bakar. Dengan mengetahui kandungan bahan kimia dari tandan aren, maka tandan aren ternyata dapat digunakan sebagai salah satu sumber selulosa untuk diolah menjadi selulosa mikrokristal dan nanokristal yang akan dimanfaatkan dalam bidang farmasi.
2.7 Tablet
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul. Tablet dapat dibuat dalam berbagai ukuran, bentuk dan penandaan permukaan tergantung pada desain cetakan (Ditjen POM, 1995).
Tablet tersedia dalam berbagai bentuk antara lain tablet kunyah, tablet effervescent, tablet hisap, tablet sublingual, dan tablet vagina. Proses produksi sediaan tablet merupakan tahapan yang kompleks. Bahan dasar (zat aktif dan eksipien) dalam bentuk serbuk akan diubah menjadi bentuk tablet, yang secara fisik terlihat bahwa terjadi perubahan karakter fisik dari bentuk serbuk menjadi bentuk tablet yang kompak. Metode pembuatan tablet dapat dibedakan menjadi : a. Metode Granulasi Basah (Wet Granulation)
Jika bahan aktif tahan terhadap air atau pelarut dan terhadap panas maka dapat dipilih metode granulasi basah. Metode granulasi yang paling banyak digunkan di industri farmasi adalah metode granulasi basah. Inti dari metode granulasi basah adalah adanya penambahan air atau cairan dalam proses granulasinya (baik cairan bahan pengikat maupun cairan yang hanya berfungsi sebagai pelarut atau pembawa bahan pengikat).
b. Metode Granulasi Kering (Dry Granulation)
c. Metode Kempa Langsung (Direct Compression)
Kempa langsung didefinisikan sebagai proses pembuatan tablet dengan langsung mengempa campuran serbuk (zat aktif dan eksipien), dan tidak ada proses sebelumnya kecuali penimbangan dan pencampuran bahan. Metode pembuatan tablet secara kempa langsung merupakan metode yang sangat disenangi. Hal ini karena kempa langsung memberi beberapa keuntungan diantaranya ialah lebih ekonomis, karena tahapan produksinya lebih singkat, peralatan yang dibutuhkan tidak banyak, membutuhkan tenaga yang sedikit dan karena prosesnya singkat maka stabilitasnya tetap terjaga (Bushra, dkk., 2008). Tablet yang dibuat secara kempa langsung memberikan level mikroba yang lebih rendah dibandingkan dengan cara granulasi basah (Ibrahim dan Olurinola, 1991).
2.8 Eksipien Tablet
2.8.1Avicel
Avicel merupakan salah satu merek dagang dari selulosa mikrokristal yang
paling banyak dan sering digunakan sebagai bahan tambahan pada tablet cetak
langsung, karena bahan ini dapat berfungsi sebagai bahan pengisi, pengikat, dan
sekaligus penghancur tablet. Avicel memiliki beberapa kelas tingkatan
berdasarkan ukuran partikel dan persentase jumlah bahan yang tertahan setelah
diayak dengan ayakan berukuran tertentu, misalnya Avicel PH 102 memiliki
ukuran partikel 100 ηm dengan jumlah partikel yang tertahan setelah diayak
dengan ayakan 60 mesh adalah < 1,0% dan dengan ayakan 200 mesh tertahan
sebesar < 30,0%. Untuk kelas Avicel yang lain dapat dilihat pada Tabel 2.4
(Rowe, dkk., 2009).
Spesifikasi Avicel PH 102 dapat dilihat pada Tabel 2.6 di bawah ini.
Nilai-nilai yang tertera pada Tabel 2.6 sesuai dengan persyaratan pengujian selulosa
mikrokristal yang ditetapkan oleh USP 32-NF 27 (Tabel 2.2).
Tabel 2.6. Spesifikasi Avicel PH 102 (berdasarkan sertifikat analisis yang dikeluarkan oleh pabrik)
Pengujian Spesifikasi Avicel PH 102
Organoleptik Berwarna putih, tidak berbau dan berasa Identifikasi Berwarna biru violet dengan ZnCl2
Pati Tidak ada (tidak berwarna biru dengan larutan iodin)
Laktosa adalah gula yang diperoleh dari susu. Dalam bentuk anhidrat atau
formulasi adalah 65%-85%. Laktosa merupakan serbuk atau massa hablur, keras,
putih, atau putih krem. Tidak berbau dan berasa sedikit manis, stabil di udara,
tetapi mudah menyerap bau. Mudah larut dalam air dan lebih mudah larut dalam
air mendidih, praktis tidak larut kloroform, etanol, dan eter (Rowe, dkk., 2009).
Secara kimia laktosa terdiri atas dua bentuk isomer, α dan β. α-laktosa
monohidrat tersedia komersial sebagai serbuk tak berasa dalam suatu rentang
ukuran partikel 200-400 mesh. Ada dua jenis laktosa yaitu yang berukuran 60-80
mesh (kasar) dan 80-100 mesh (biasa). Umumnya formulasi yang menggunakan
laktosa menunjukkan laju pelepasan obat yang baik. Granulnya cepat kering dan
waktu hancurnya tidak terlalu peka terhadap perubahan kekerasan tablet
(Lachman, 1964).
Lactose spray dried (LSD) saat ini tersedia untuk digunakan sebagai bahan
pengikat-pengisi dalam tablet cetak langsung. LSD dibuat dari atomisasi dan
pengeringan suspensi kristal α-laktosa monohidrat dalam larutan laktosa. 10-20%
laktosa ada dalam larutan dan sisanya 80-90% dalam bentuk kristal.Proses
pengeringan dengan spray dryer menghasilkan partikel dalam bentuk sferis.
(Rowe, dkk., 2009).
2.8.3 Magnesium Stearat
Magnesium stearat (C36H70MgO4) merupakan campuran magnesium
dengan asam organik padat yang mengandung magnesium stearat dan magnesium
palmitat. Bahan ini digunakan sebagai bahan pelicin (lubrikan) dalam kapsul dan
tablet dengan konsentrasi 0,25%-5,0% w/w. Pemerian berupa serbuk, halus, licin,
putih, dan mudah melekat pada kulit, bau lemah khas, dan bebas dari butiran.
Kelarutannya praktis tidak larut dalam air, etanol 95%P dan dalam eter P, sukar
larut dalam benzen dan etanol (95%) (Rowe, dkk., 2009).
Penggunaan magnesium stearat secara umum adalah pada sediaan
kosmetik, makanan, dan formula farmasetik. Pada pembuatan kapsul dan tablet,
magnesium stearat digunakan dengan konsentrasi 0,25%-5,0%. Selain itu bahan
inijuga digunakan sebagai bahan pembawa dalam krim (Rowe, dkk., 2009).
2.8.4 Talkum
Talkum merupakan magnesium silikat hidrat yang dimurnikan, dengan rumus Mg6(Si2O5)4(OH)4.Penggunaannya adalah sebagai bahan anticaking, pelicin, pengisi tablet dan kapsul, sertapelincir. Sifat talkum sebagai glidan lebih baik daripada amilum, namun talkum dapat menurunkan disintegrasi dan disolusi tablet. Pada proses pencetakan tablet, talkum bersifat sebagai antiadherent yang dapat mencegah melekatnya (sticking) permukaan tablet pada punch atas dan punch bawah (Rowe, dkk., 2009).
2.9 Natrium Diklofenak
NH Cl
Cl
H
O
O
Na
Gambar 2.7. Struktur kimia NatriumDiklofenak
Rumus Molekul : C14H10Cl2NO2Na
Berat Molekul : 318,3
Nama Kimia : Natrium {0-[2,6 diklofenil aminofenil} asetat Pemerian : Serbuk kristal, putih atau agak kekuningan, agak
higroskopis (The USP Convention, 2009).
Natrium diklofenak (Gambar 2.7) dapat diabsorpsi dengan cepat dalam saluran cerna setelah pemberian oral. Obat ini terikat 99% pada protein plasma dan dimetabolisme oleh hati sehingga memiliki waktu paruh yang pendek yaitu 2 jam (Neal, 2006).
Cara kerja sebagian besar AINS berdasarkan hambatan sintesis prostaglandin, dimana kedua jenis enzim cyclo-oxygenase (COX) dihambat. Obat-obat AINS yang ideal hendaknya hanya menghambat COX-2 (peradangan), tidak menghambat COX-1 (perlindungan mukosa lambung) dan lipo-oxygenase (pembentukan leukotrien) (Tjay dan Kirana, 2002). Diklofenak adalah penghambat COX yang memiliki afinitas lebih besar untuk COX-2 dibanding COX-1. Obat ini menghambat biosintesa prostaglandin dan juga mengurangi pembentukan leukotrien, yang dapat memberikan kontribusi kepada aktivitas
inflamasi. Waktu paruh dari diklofenak adalah pendek pada sebagian besar spesies, termasuk manusia, tetapi terakumulasi di situs peradangan, dimana mencapai konsentrasi yang lebih tinggi di jaringan non-peradangan, dan sama dengan yang dicapai dalam plasma (Veterinaria, 2006).
2.10 Disolusi
Disolusi adalah proses pelarutan suatu zat padat menjadi terlarut dalam suatu pelarut. Dalam sistem biologik disolusi obat dalam media berairmerupakan suatu bagian penting sebelum obat diabsorbsi ke jalur sitemik. Laju disolusi obat-obat dengan kelarutan dalam air sangat kecil dari bentuk sediaan padat yang utuh atau terdesintegrasi dalam saluran cerna sering mengendalikan laju absorbsi sistemik obat (Shargel, 1988).
Ada beberapa proses fisikokimia dalam penentuan laju disolusi obat dari sediaan padat. Proses ini termasuk proses pembasahan, penetrasi medium disolusi ke dalam sediaan, pengembangan, disintegrasi dan deagregasi sediaan (Abdou, 1989).
Faktor-faktor yang mempengaruhi disolusi dibagi atas 3 kategori yaitu : 1. Faktor-faktor yang berhubungan dengan sifat fisikokimia obat, meliputi : a. Efek kelarutan obat.
Kelarutan obat dalam air merupakan faktor utama dalam menentukan laju disolusi. Jika kelarutan obat besar dalam air, maka akan menghasilkan laju disolusi yang cepat.
Ukuran partikel yang lebih kecil akan dapat memperbesar luas permukaan obat yang berhubungan dengan medium, sehingga akan meningkatkan laju disolusi.
2. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi : a. Efek formulasi.
Laju disolusi suatu bahan obat dapat dipengaruhi oleh bahan tambahan yang
digunakan. Bahan tambahan seperti bahan pengisi, pengikat, dan penghancur
yang bersifat hidrofil dapat memberikan sifat hidrofil pada bahan obat yang
hidrofob, oleh karena itu disolusi obat meningkat, sedangkan bahan tambahan
yang bersifat hidrofob dapat mengurangi laju disolusi.
b. Efek faktor pembuatan sediaan.
Metode granulasi dapat mempercepat laju disolusi obat-obat yang kurang
larut. Penggunaan bahan pengisi yang bersifat hidrofil seperti laktosa dapat
menambah hidrofilisitas bahan aktif dan menambah laju disolusi.
3. Faktor-faktor yang berhubungan dengan uji disolusi, meliputi :
a. Tegangan permukaan medium disolusi.
Tegangan permukaan mempunyai pengaruh nyata terhadap laju disolusi
bahan obat. Untuk dapat meningkatkan proses penetrasi medium disolusi ke
dalam matriks, dapat ditambahkan surfaktan ke dalam medium disolusi untuk
menurunkan sudut kontak antara obat dan medium.
b. Viskositas medium.
Viskositas medium yang semakin tinggi akan menurunkan laju disolusi dari
bahan obat.
c. pH medium disolusi.
Larutan asam cenderung memecah tablet sedikit lebih cepat dibandingkan
dengan air, oleh karena itu mempercepat laju disolusi (Gennaro, 2000).
Obat-obat asam lemah memiliki laju disolusi yang kecil dalam medium asam,
karena bersifat nonionik, tetapi laju disolusinya besar pada medium basa
karena terionisasi dan pembentukan garam yang larut (Martin, 1993).
Menurut USP 32, ada dua metode disolusi yang sering digunakan untuk
melakukan uji disolusi, yaitu:
a. Metode Keranjang (Basket )
Metode keranjang terdiri atas keranjang silindrik yang ditahan oleh tangkai
motor. Keranjang menahan sediaan obat dan berputar dalam suatu labu bulat
yang berisi medium pelarutan. Keseluruhan labu tercelup dalam suatu bak yang
bersuhu konstan 37oC. Kecepatan berputar dan posisi keranjang harus
memenuhi rangkaian syarat khusus dalam USP.
b. Metode Dayung (Paddle)
Metode dayung terdiri atas suatu dayung yang dilapisi khusus, yang berfungsi
memperkecil turbulensi yang disebabkan oleh pengadukan. Dayung diikat
secara vertikal ke suatu motor yang berputar dengan suatu kecepatan yang
terkendali. Tablet atau kapsul diletakkan dalam labu pelarutan yang beralas
bulat yang juga berfungsi untuk memperkecil turbulensi dari media pelarutan.
metode keranjang, suhu dipertahankan pada 37oC. Posisi dayung ditetapkan
dalam USP.
2.11 Kinetika Pelepasan Obat
Pelepasan obat dari suatu sediaan dapat diramalkan dengan mengetahui
kinetika pelepasan obat. Ada 3 model sistem pelepasan obat yang umum, yaitu
order nol, order satu, dan Higuchi (Martin, dkk., 1993; Dash, dkk., 2010).
Pada model order nol pelarutan obat dari bentuk sediaan yang melepaskan
obat secara perlahan dapat mengikuti persamaan 2.1 berikut ini:
Qt = Q0 + K0t ... (2.1)
Dimana Qt = jumlah obat larut pada waktu t
Q0 = jumlah obat mula-mula dalam larutan (biasanya Q0 = 0)
K0= konstanta pelepasan order nol yang dinyatakan dalam unit
konsentrasi/waktu
Untuk mempelajari kinetika pelepasan, data yang diperoleh dari uji pelepasan in
vitro diplot sebagai jumlah obat yang dilepaskan versus waktu (Dash, dkk., 2010).
Mekanisme pelepasan obat di sini konstan dari waktu ke waktu dengan tidak
bergantung pada konsentrasi obat dalam sediaan. Sistem ini merupakan sistem
pelepasan obat yang ideal untuk sediaan sustained release (Martin, dkk., 1993).
Model order kesatu digunakan untuk menjelaskan absorpsi dan atau
eliminasi obat, walaupun sulit untuk menggambarkan mekanisme ini. pelepasan
obat yang diikuti kinetika order pertama dinyatakan dalam persamaan 2.2 berikut:
Log C = log C0 - Kt/2,303 ... (2.2)
Dimana C0 = konsentrasi obat mula-mula
K = konstanta laju order pertama
t = waktu
Data disolusi yang diperoleh diplot sebagai log persentase kumulatif sisa obat vs
waktu yang menghasilkan garis lurus dengan slope –K/2,303 (Dash, dkk., 2010).
Kinetika orde satu memiliki kecepatan pelepasan obat yang bergantung pada
konsentrasi obat dalam sediaan. Kecepatan pelepasan obat pada waktu tertentu
sebanding dengan konsentrasi obat yang tersisa dalam sediaan pada saat itu
(Martin, dkk., 1993).
Model Higuchi merupakan model matematika yang bertujuan untuk
menjelaskan pelepasan obat dari sistem matriks yang diusulkan oleh Higuchi pada
1961. Model ini berdasarkan pada hipotesis bahwa (i) konsentrasi obat mula-mula
dalam matriks lebih tinggi dari kelarutan obat; (ii) difusi obat terjadi hanya dalam
satu dimensi (efek tepi harus diabaikan); (iii) partikel obat jauh lebih kecil dari
ketebalan sistem; (iv) pengembangan matriks dan disolusi diabaikan; (v)
difusifitas obat kontan; dan (vi) kondisi sink selalu tercapai dalam lingkungan
pelepasan obat. Model ini dinyatakan dalam persamaan 2.3 di bawah ini:
ft = Q = KH x t½ ... (2.3)
Dimana Q = jumlah obat yang dilepaskan dalam waktu t
KH = konstanta disolusi Higuchi
Data dari uji disolusi diplot sebagai persentase kumulatif obat versus akar waktu