Utama. Halaman 131 – 132.
Lampiran 1. Gambar Sampel
1.Sampel Minuman Berenergi merek Kratingdaeng-S®
Lampiran 2.Spesifikasi Sampel Spesifikasi sampel:
Minuman Berenergi Merek Kratingdaeng-S®
Minuman Berenergi Merek Hemaviton®
Taurine 800 mg Taurine 1000 mg
Glucoronolactone 1,3,7 Trimethylxanthine 50 mg
Kafein 50 mg Inositol 50 mg
Inositol 50 mg Ginseng extract 10 mg
Niasin 20 mg Nicotinamide 20 mg
Panotenat 5 mg Vitamin B6 5 mg
Vitamin B6 5 mg Dexpanthenol 5 mg
Sukrosa 25 g Vitamin B12 5 mcg
Air Mengandung gula alami dan sorbitol
Natrium Benzoat Tartrazin Cl 19140
Sampel
Kratingdaeng-S® Hemaviton®
Nomor Bets Tanggal
Panjang gelombang maksimum bahan-bahan dalam sampel: Bahan Panjang gelombang
maksimum (nm)
Rujukan
Taurine 570 Draganov, dkk., 2014
Kafein 273 Moffat, dkk., 2005
Inositol 261 Moffat, dkk., 2005
Niasinamid 261 Moffat, dkk., 2005
Vitamin B6 290 Moffat, dkk., 2005
Vitamin B12 361 Moffat, dkk., 2005
Sukrosa 190 Sumantri, dkk., 2013
Natrium Benzoat 230 Moffat, dkk., 2005
Asam sitrat 520 Napitupulu, 2011
Ponceau 4R 506 Kartadarma, dkk., 2007
Vitamin B5 200 Engel, 2009
Lampiran 3. Hasil Uji Kualitatif Vitamin C pada sampel Kratingdaeng-S® dan Hemaviton®
1. Uji Kualitatif sampel Kratingdaeng-S® dengan pembanding Baku Vitamin C BPFI
2. Uji Kualitatif sampel Hemaviton® dengan pembanding Baku Vitamin C BPFI
Analit Sebelum Penambahan NaOH + FeCl3
Setelah Penambahan NaOH + FeCl3 Baku Vitamin C
(a) Larutan kuning lemah
Terbentuk endapan ungu tua
Kratingdaeng-S®
(b) Larutan kuning terang Terbentuk endapan ungu a
b
c
Hasil Uji Kualitatif dengan Pembanding warna Baku Vitamin C
Lampiran 4.Gambar Alat Spektrofotometer Ultraviolet (UV) Hemaviton®
Lampiran 5. Perhitungan Pembuatan HCl 0,1N
HCl pekat = 37% setara dengan 12 N V1 x N1 = V2 x N2
V1 x 12 N = 1000 mL x 0,1 N
V1 = 12N
N 1 , 0
mL 1000
x
Lampiran 6. Bagan Alir Prosedur Penelitian
dimasukkan ke dalam labu tentukur 25 mL
dilarutkan dan dicukupkan dengan HCL 0,1N
LIB II Kafein 100 μg/mL
Standar 1
maksimumpada λ 200-400nm
Standar 6
28 μg/mL
Kafein BPFI
ditimbang 25 mg
dimasukkan ke dalam labu tentukur 25 mL
dilarutkan dan dicukupkan dengan HCL 0,1N
Lampiran 6. (Lanjutan)
dimasukkan ke dimasukkan ke
diambil 4,8 mL diambil 2,5 mL
dimasukkan ke dalam labu tentukur 25 mL
dilarutkan dan dicukupkan dengan HCL 0,1N
LIB II vitamin C 100 μg/mL
Standar 1
Vitamin C BPFI
ditimbang 25 mg
dimasukkan ke dalam labu tentukur 25 mL
dilarutkan dan dicukupkan dengan HCL 0,1N
Lampiran 6. (Lanjutan)
Persamaan regresi
dibuat kurva kalibrasi Larutan Standar Kafein
(8; 12; 16; 20; 24; 28μg/mL)
diukur serapan pada λ 200-400 nm ditransformasikan ke serapan derivat pertama
ditransformasikan ke serapan derivat kedua
ditentukan zero crossing
ditentukan panjang gelombang analisis
Lampiran 6. (Lanjutan)
Persamaan regresi vitamin C
dibuat kurva kalibrasi Larutan Standar Vitamin C
(8; 16; 24; 32; 40; 48μg/mL)
diukur serapan pada λ 200-400 nm ditransformasikan ke serapan derivat pertama
ditransformasikan ke serapan derivat kedua
ditentukan zero crossing
ditentukan panjang gelombang analisis
Lampiran 6. (Lanjutan)
Sampel
diambil 25 mL
dimasukkan ke dalam beaker gelas disaring
dibuang filtrat pertama diambil 1 mL
dimasukkan ke dalam labu tentukur 25 mL dilarutkan dan dicukupkan dengan HCL 0,1N
diukur pada λ 293,4 nm (kafein)
diukur pada λ 214 nm (vitamin C)
Absorbansi
Kandungan kafein dan vitamin C
Lampiran 7. Kurva Serapan Kafein dan Vitamin C
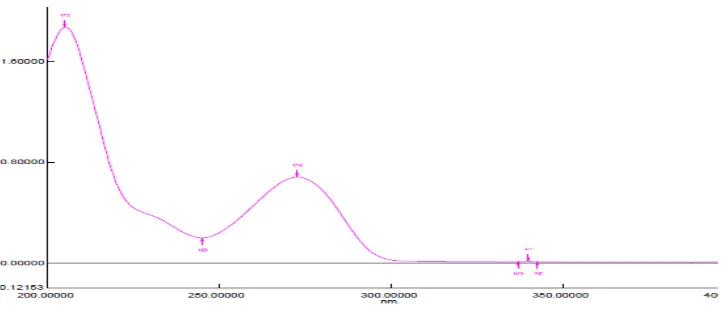
Gambar 7.1Kurva serapan kafein konsentrasi 8 μg/mL
Gambar 7.3Kurva serapan kafein konsentrasi 16 μg/mL
Lampiran 7. (Lanjutan)
Gambar 7.4Kurva serapan kafein konsentrasi 20 μg/mL
Gambar 7.6Kurva serapan kafein konsentrasi 28 μg /mL
Lampiran 7. (Lanjutan)
Gambar 7.8Kurva serapan vitamin Ckonsentrasi 16 μg /mL
Gambar 7.9Kurva serapan vitamin Ckonsentrasi 24μg /mL
Lampiran 7. (Lanjutan)
Gambar 7.11Kurva serapan vitamin Ckonsentrasi 40 μg /mL
Gambar 7.12Kurva serapan vitamin Ckonsentrasi 48μg /mL
Gambar 8.1Kurva serapan derivat pertama kafein konsentrasi 8 μg /mL
Gambar 8.2Kurva serapan derivat pertama kafein konsentrasi 12 μg /mL
Gambar 8.3 Kurva serapan derivat pertama kafein konsentrasi16 μg /mL
Gambar 8.4 Kurva serapan derivat pertama kafein konsentrasi 20 μg /mL
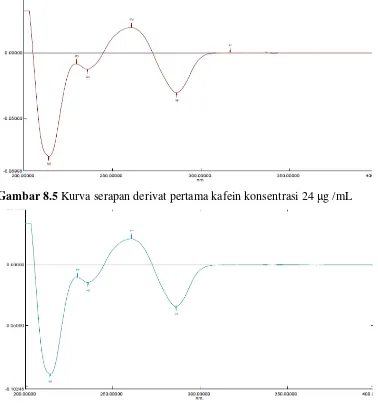
Gambar 8.5 Kurva serapan derivat pertama kafein konsentrasi 24 μg /mL
Gambar 8.6 Kurva serapan derivat pertama kafein konsentrasi 28 μg /mL
Gambar 8.7 Kurva serapan derivat pertama vitamin C konsentrasi 8 μg /mL
Gambar 8.8 Kurva serapan derivat pertama vitamin C konsentrasi 16 μg /mL
Gambar 8.9 Kurva serapan derivat pertama vitamin C konsentrasi 24 μg /mL
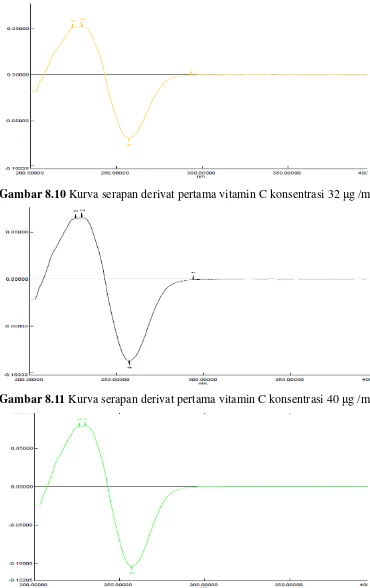
Gambar 8.10 Kurva serapan derivat pertama vitamin C konsentrasi 32 μg /mL
Gambar 8.11 Kurva serapan derivat pertama vitamin C konsentrasi 40 μg /mL
Gambar 8.12 Kurva serapan derivat pertama vitamin C konsentrasi 48 μg /mL
Gambar 9.1Kurva serapan derivat kedua kafein konsentrasi 8 μg /mL
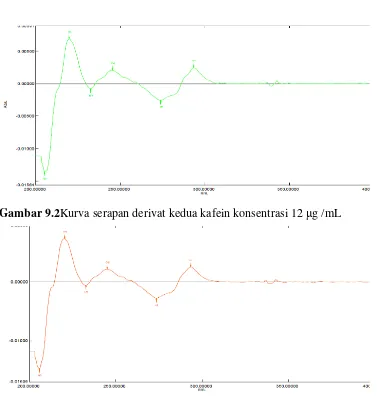
Gambar 9.2Kurva serapan derivat kedua kafein konsentrasi 12 μg /mL
Gambar 9.3Kurva serapan derivat kedua kafein konsentrasi16 μg /mL
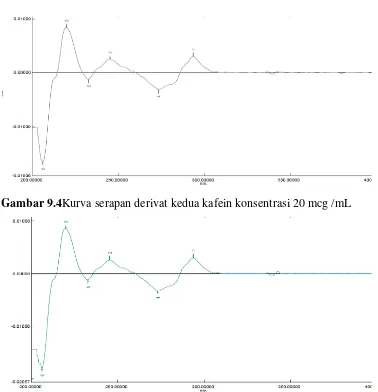
Gambar 9.4Kurva serapan derivat kedua kafein konsentrasi 20 mcg /mL
Gambar 9.5Kurva serapan derivat kedua kafein konsentrasi 24 μg /mL
Lampiran 9.(Lanjutan)
Gambar 9.7Kurva serapan derivat kedua vitamin C konsentrasi 8 mcg /mL
Gambar 9.9Kurva serapan derivat kedua vitamin C konsentrasi 24 μg /mL
Lampiran 9.(Lanjutan)
Gambar 9.10Kurva serapan derivat kedua vitamin C konsentrasi 32 μg /mL
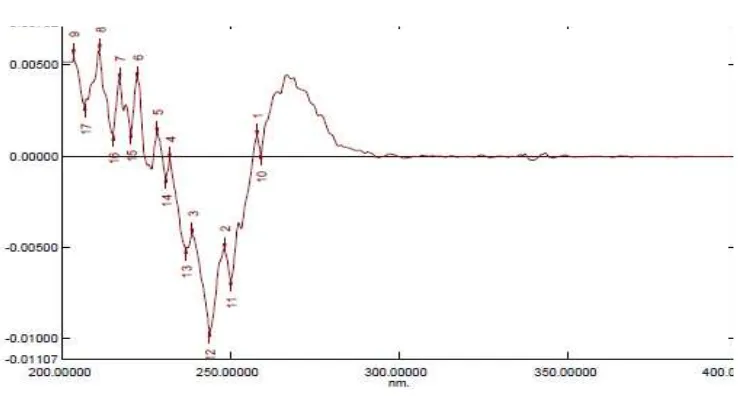
Gambar 9.12Kurva serapan derivat kedua vitamin C konsentrasi 48 μg /mL
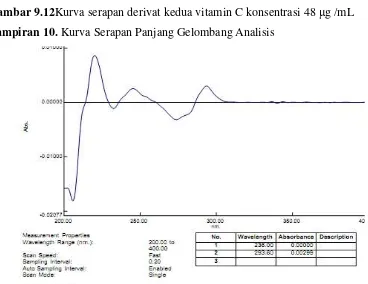
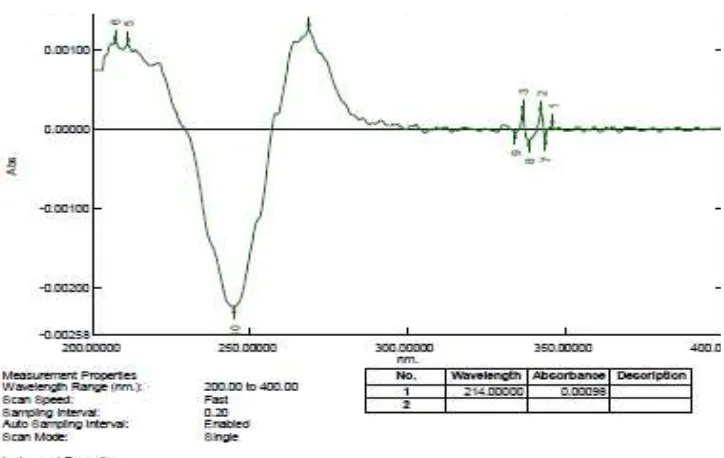
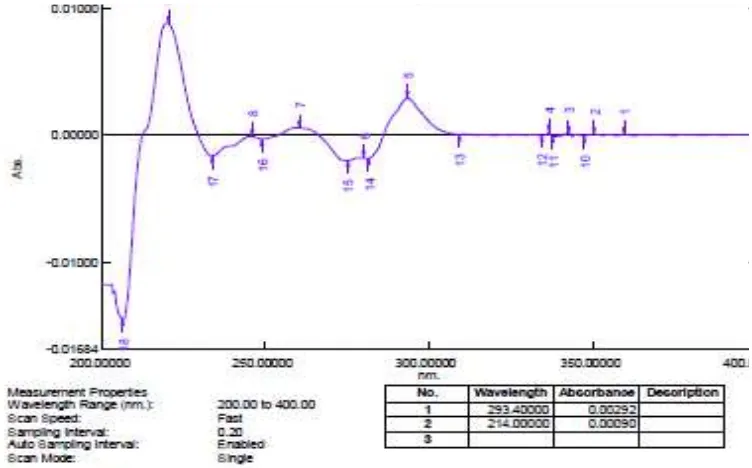
Lampiran 10. Kurva Serapan Panjang Gelombang Analisis
Lampiran 10. (Lanjutan)
Lampiran 11. Data Kalibrasi Kafein BPFI, Persamaan Regresi dan Koefisien Korelasi
Kalibrasi Serapan Derivat Kedua Kafein pada Panjang Gelombang 293,4 nm No. Konsentrasi (μg/mL)(X) Absorbansi(Y)
1. 0,0000 0,00000
Perhitungan Persamaan Garis Regresi
No. X Y XY X2` Y2
1. 0,0000 0,00000 0,0000 0,0000 0,000000000 2. 8,0000 0,00237 0,01896 64,0000 0,000005617 3. 12,0000 0,00378 0,04536 144,0000 0,000014288 4. 16,0000 0,00489 0,07824 256,0000 0,000023912 5. 20,0000 0,00612 0,12240 400,0000 0,000037454 6. 24,0000 0,00736 0,17664 576,0000 0,000054169 7. 28,0000 0,00860 0,24080 784,0000 0,000073960
ΣX = 108
=
(0,6824)
−
(108)(0,03312)/7
(2224)
−
(108)²/7
= 30,73 . 10−5
��= ���+�
�= �� − ���= (0,00473)−(307,3 . 10−6)(15,42857) = −1. 10−5
Perhitungan Koefisien Korelasi(r) r= (∑ ��)−(∑ �)(∑ �)/�
��(∑ �2)−(∑ �)2/���(∑ �2)−(∑ �)2/��
Lampiran 11. (Lanjutan)
r= (0,6824) – (108)(0,03312) /7
�[(2224)−(108)2/7]�0,000209400−(0,03312)2/7�
r
=
0,17141 0,17147r = 0,9996
Lampiran 12. Data KalibrasiVitamin C, Persamaan Regresi dan Koefisien Korelasi
Kalibrasi Serapan Derivat Kedua Vitamin C pada Panjang Gelombang214 nm No. Konsentrasi (μg/mL)(X) Absorbansi(Y)
1. 0,0000 0,00000
Perhitungan Persamaan Garis Regresi
Lampiran 12. (Lanjutan)
Perhitungan Koefisien Korelasi(r) r= (∑ ��)−(∑ �)(∑ �)/�
��(∑ �2)−(∑ �)2/���(∑ �2)−(∑ �)2/��
r= (0,66488)−(168)(0,01921)/7
�[(5824)−1682/7][(75,91.10−7)−(0,01921)2/7]
r = 0,20380
0,20387
r = 0,9996
Lampiran 15. Kurva Serapan Derivat Kedua Sampel
Gambar 15.1Kurva Serapan Sampel Kratingdaeng-S® -1
Lampiran 15. (Lanjutan)
Gambar 15.3 Kurva Serapan Sampel Kratingdaeng-S® -3
Lampiran 15. (Lanjutan)
Gambar 15.5 Kurva Serapan Sampel Kratingdaeng-S® -5
Lampiran 15. (Lanjutan)
Gambar 15.8 Kurva SerapanSampel Hemaviton® -2
Lampiran 15. (Lanjutan)
Gambar 15.10 Kurva SerapanSampel Hemaviton® -4
Lampiran 15. (Lanjutan)
Gambar 15.12 Kurva SerapanSampel Hemaviton® -6
Lampiran 16.Hasil Analisis Kandungan Jumlah Kafeindan Vitamin Cdalam Sampel
1. Sampel Merek Kratingdaeng-S®
No
2. Sampel Merek Hemaviton®
Lampiran 17.Contoh Perhitungan Kandungan Kafein dan Vitamin C dalamSampelKratingdaeng-S®
Volume sampel 1 yang digunakan = 1 mL
Absorbansi analisis (Y) kafein (293,4 nm)= 0,00402
Persamaan regresi pada absorbansi maksimum dengan panjang gelombang kafein pada λ293,4 nm : Y = 30,73X – 1 . 10-5
Sehingga untuk mendapatkan kadar (X) sampel, digunakan subtitusi Yterhadappersamaan regresi pada masing-masing panjang gelombang.
Konsentrasi Kafein : Y = (30,73X – 1). 10-5 V : volume larutan pengenceran (mL) Fp : faktor pengenceran
W : volume sampel (mL)
Kandungan kafein dalam sampel = 13,1142μg /mL× 25 mL × 1 1 mL
= 327,85 mcg/mL
= 324,70 μg /mL
Lampiran 17.(Lanjutan)
Volume sampel Kratingdaeng-S®= 150 mL
Jumlah Kandungan kafein = Kandungan kafein sebenarnya x volume sampel = 324,70 μg /mL x 150 mL
= 48705 μg = 48,705 mg Absorbansi analisis vitamin C (214 nm) = 0,00147
Persamaan regresi pada absorbansi maksimum dengan panjang gelombang vitamin C pada λ 214 nm : Y = (11X+1) . 10-5 V : volume larutan pengenceran (mL) Fp : faktor pengenceran
W : volume sampel (mL)
KandunganVitamin C dalam sampel = 13,2727 μg /mL × 25 mL × 1 1 mL
= 331,81 μg /mL
KandunganVitamin C sebenarnya = KandunganVitamin C dalam sampel x persen baku Vitamin C
= 331,31μg /mL
Lampiran 17.(Lanjutan)
Volume sampel Kratingdaeng-S®= 150 mL
Jumlah Kandungan Vitamin C = KandunganVitamin C sebenarnya x volume sampel
= 331,31 μg /mL x 150 mL = 49696 μg
Lampiran 18.Contoh Perhitungan Kandungan Kafein dan Vitamin C dalamSampel Hemaviton®
Volume sampel 1 yang digunakan = 1 mL
Absorbansi analisis (Y) kafein (293,4 nm)= 0,00412
Persamaan regresi pada absorbansi maksimum dengan panjang gelombang kafein pada λ293,4 nm: Y = 30,73X – 1 . 10-5
Sehingga untuk mendapatkan kadar (X) sampel, digunakan subtitusi Y terhadap persamaan regresi pada masing-masing panjang gelombang.
Konsentrasi Kafein : Y = (30,73X – 1). 10-5 V : volume larutan pengenceran (mL) Fp : faktor pengenceran
W : volume sampel (mL)
Kandungan kafein dalam sampel = 13,4396μg /mL× 25 mL × 1 1 mL
Lampiran 18.(Lanjutan)
Kandungan kafein sebenarnya = Kandungan kafein dalam sampel x persen baku = 327,85 μg /mL x 99,04%
= 332,76μg /mL
Volume sampel Kratingdaeng-S®= 150 mL
Jumlah Kandungan kafein = Kandungan kafein sebenarnya x volume sampel = 332,76μg /mL x 150 mL
= 49914μg = 49,914 mg
Absorbansi analisis vitamin C (214 nm) = 0,00150
Fp : faktor pengenceran W : volume sampel (mL)
Lampiran 18.(Lanjutan)
Kandungan vitamin C dalam sampel = 13,5454 μg /mL× 25 mL × 1 1 mL
= 338,63μg /mL
Kandungan vitamin C sebenarnya= Kandungan vitamin C dalam sampel x persen baku vitamin C
= 338,63μg /mL x 99,85% = 338,12 μg /mL
Volume sampel Kratingdaeng-S®= 150 mL
Jumlah kandunganvitamin C = Kandungan vitamin C sebenarnya x volume sampel = 338,12μg /mL x 150 mL
Lampiran 19.Perhitungan Statistik Kandungan Kafein dan Vitamin C dalamSampel Merek Kratingdaeng-S®
1. Kafein
Data diterima jika t hitung < t tabel
t hitung 4 =
�
�−��� √�⁄
�
=
�
−0,14
0,0903⁄√6
�
= 3,7976Lampiran 19.(Lanjutan)
t hitung 5 =
�
�−�Dari hasil perhitungan tersebut diperoleh bahwa semua t hitung < t tabel, maka semua data tersebut diterima.
Kandungan kafein dalam sampel merek Kratingdaeng-S®:
=
�0,46366−1
=
0,3044Lampiran 19.(Lanjutan)
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1=5,maka t(α/2,dk) = 4,0321
Data diterima jika t hitung < t tabel
t hitung 1 =
�
�−�Dari hasil perhitungan tersebut diperoleh bahwa semua t hitung < t tabel, maka semua data tersebut diterima.
Kandungan vitamin C pada sampel merek Kratingdaeng-S® :
μ = � ± (tα/2, dk) x SB/√n)
Lampiran 20.Perhitungan Statistik Kandungan Kafein danVitamin C dalamSampel Merek Hemaviton®
1. Jumlah Kafein
Data diterima jika t hitung < t tabel
t hitung 5 =
�
�−��� √�⁄
�
=
�
−0,141
0,1188⁄√6
�
= 2,9072Lampiran 20.(Lanjutan)
t hitung 6 =
�
�−��� √�⁄
�
=
�
0,1010,1188⁄√6
�
= 2,0824Dari hasil perhitungan tersebut diperoleh bahwa semua t hitung < t tabel, maka semua data tersebut diterima.
Jumlah kandungan kafein dalam sampel merek Hemaviton® :
μ = � ± (tα/2, dk) x SB/√n)
= 49,813 mg ± (4,0321 x 0,1188/√6) = (49,813 ± 0,1955) mg
2. Jumlah Vitamin C
Pada interval kepercayaan 99% dengan nilai α = 0,01, dk = n-1=5, maka t(α/2,dk) = 4,0321
Data diterima jika t hitung < t tabel
Lampiran 20.(Lanjutan)
t hitung 1 =
�
�−�Dari hasil perhitungan tersebut diperoleh bahwa semua t hitung < t tabel, maka semua data tersebut diterima.
Jumlah kandungan vitamin C pada sampel merek Hemaviton®:
μ = � ± (tα/2, dk) x SB/√n)
Lampiran 21. Kurva Serapan Uji Perolehan Kembali Kafein dan Vitamin C dalam Sampel Kratingdaeng-S®
Gambar 21.2Kurva Serapan Uji Perolehan KembaliKafein dan Vitamin C dalam Sampel Kratingdaeng-S® -2
Lampiran 21.(Lanjutan)
Gambar 21.4 Kurva Serapan Uji Perolehan KembaliKafein dan Vitamin C dalam Sampel Kratingdaeng-S® -4
Lampiran 21.(Lanjutan)
Gambar 21.6Kurva Serapan Uji Perolehan KembaliKafein dan Vitamin C dalam Sampel Kratingdaeng-S® -6
Lampiran 22. Hasil Uji Perolehan Kembali Kafein dan Vitamin C Setelah Penambahan Masing-Masing Larutan Standar Pada Sampel Kratingdaeng-S®
1. Hasil Analisis Kafein Setelah Penambahan Larutan Standar Kafein
Sampel
Sampel
Lampiran 23. Contoh Perhitungan Uji Perolehan Kembali dengan menggunakan Sampel Kratingdaeng-S®
Volume sampel 1 yang digunakan = 1 mL Absorbansi analisis (Y) :
Kafein (293,4 nm) = 0,00783 Vitamin C (214 nm) = 0,00282
Persamaan regresi pada absorbansi maksimum dengan panjang gelombang kafein pada λ293,4 nm: Y = (30,73X – 1) . 10-5
Persamaan regresi pada absorbansi maksimum dengan panjang gelombang vitamin C pada λ214nm : Y = (11X + 1) . 10-5
0, 00783 = (30,73X – 1) . 10-5 X = 25,5125 μg /mL Konsentrasi Vitamin C: Y = (11X + 1) . 10-5
0, 00282 = (11X + 1) . 10-5 X = 25,5454 μg /mL
1. Perhitungan Uji Perolehan Kembali Kafein
Konsentrasi awal setelah penambahan larutan baku = 25,5125 μg /mL Konsentrasi = Konsentrasi (μg /mL )
Volume sampel (mL ) × volume (mL) × Faktor pengenceran
= 25,5125 μg /mL × 25 mL × 1 1 mL
= 638,63 μg /mL
Lampiran 23.(Lanjutan)
CF = konsentrasi kafein x persen baku = 638,63 μg /mL x 99,04%
= 632,49 μg /mL
Kadar sampel setelah ditambah larutan baku (CF ) = 632,49 μg /mL
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 324,83 μg /mL Kadar larutan standar yang ditambahkan (C*A)
C*A =
Konsentrasi baku yang ditambahkan
Volume sampel
×
ml yang ditambahkan=
100 μg /mLMaka persen perolehan kembali kafein = CF − CA
CA∗
×
100%=
(632,49−324,83)μg /mL330 μg /mL
×
100%= 93,23%
2. Perhitungan Uji Perolehan Kembali Vitamin C
Konsentrasi awal setelah penambahan larutan baku = 25,5454μg /mL Konsentrasi = Konsentrasi (μg /mL )
Volume sampel (mL ) × volume (mL) × Faktor pengenceran
Lampiran 23. (Lanjutan)
= 25,5454μg /mL× 25 mL × 1
Kadar rata-rata sampel sebelum ditambah larutan baku (CA) = 330,93 μg /mL Kadar larutan standar yang ditambahkan (C*A)
C*A = Konsentrasi baku yang ditambahkan
Volume sampel
×
mL yang ditambahkan=
100 μg /mL1 mL
×3,3 mL
Maka persen perolehan kembali Vitamin C = CF − CA
CA∗
×
100%=
�637,67–330,93�μg /mL330 μg /mL ×100%
= 92,95%
Lampiran 24. Perhitungan Simpangan Baku Relatif (SBR) Kandungan Kafein No. Persen Perolehan Kembali
= 0,0813
Lampiran 25. Perhitungan Simpangan Baku Relatif (SBR) Kandungan Vitamin C No. Persen Perolehan Kembali