PENGARUH WAKTU DAN LUAS PERMUKAAN TERHADAP KETEBALAN PRODUK PADA ELEKTROPLATING ACID ZINC
Teks penuh
Gambar
Dokumen terkait
Penelitian dan pengujian ini bertujuan untuk mengetahui pengaruh waktu tahan celup proses elektroplating terhadap ketebalan pelapisan dan kekasaran permukaan pada baja karbon
Penelitian dan pengujian ini bertujuan untuk mengetahui pengaruh waktu tahan celup proses elektroplating terhadap ketebalan pelapisan dan kekasaran permukaan pada
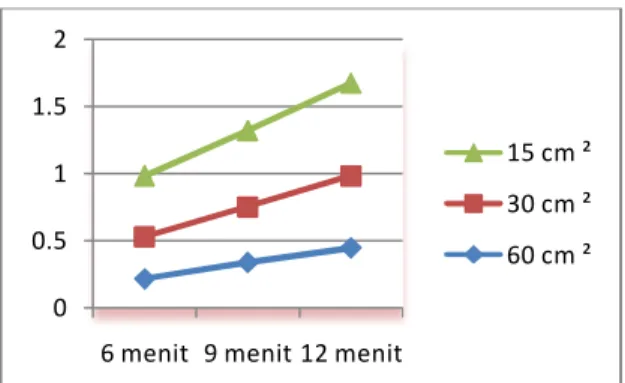
Berdasarkan uraian di atas timbul suatu pertanyaan : “ Sejauh mana pengaruh waktu tahan celup terhadap ketebalan lapisan tembaga kekasaran permukaan lapisan
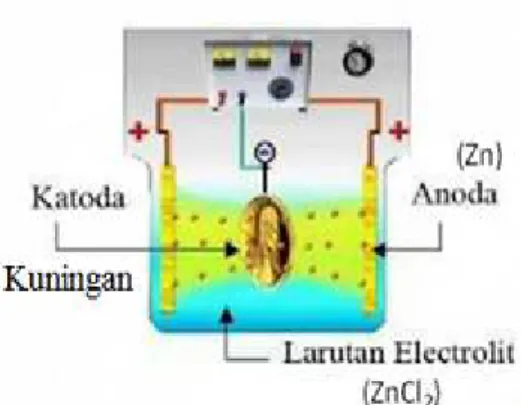
atau satu kali pakai dalam proses elektroplating yang meliputi : spesimen uji.. (katoda), larutan elektrolit dan bahan
Penelitian untuk mengetahui pengaruh suhu dan waktu elektroplating terhadap nilai ketebalan dan kekasaran permukaan, menggunakan spesimen berupa plat baja karbon
Menyatakan bahwa skripsi dengan judul "Pengaruh Preparasi Kekasaran Permukaan Dan Tegangan Listrik Terhadap Kuat Lekat Dan Ketebalan Lapisan Hasil Elektroplating Pada Baja
Pada penelitian ini penulis melakukan proses elektroplating dengan menggunakan pelapisan tembaga pada plat baja karbon tinggi yang selanjutnya akan diuji untuk
Pengaruh Variasi Tegangan Listrik dan Waktu Proses Elektroplating terhadap Ketebalan serta Kekerasan Lapisan pada Baja... Karbon Rendah dengan Krom Doctoral dissertation, UNIVERSITAS