BAB II
TINJAUAN PUSTAKA
II.1 Migren
II.1.1 Epidemiologi
Migren dilaporkan mengenai sekitar 12% populasi dewasa di Negara Barat.
Penelitian epidemiologi yang dilakukan di Amerika menemukan bahwa prevalensi
migren adalah 13,2% dengan prevalensi pada wanita (17,5%) lebih tinggi
dibandingkan pria (8,6%). Pada penelitian epidemiologi di Denmark, ditemukan
insiden migren adalah 8,1/1000 orang/tahun, dan pada penelitian yang
dilakukan di Jerman, ditemukan bahwa prevalensi migren kronik yang
berdasarkan kriteria international classification headache disorder (ICHD)-II yang
telah direvisi adalah 0,5%, dan 2 % jika berdasarkan kriteria transformed
migraine. (Jensen et al., 2008; Katsarava, 2010; Lipton et al., 2007)
Berdasarkan penelitian multisenter Sjahrir (2004) pada 5 RS besar di
Indonesia (Medan, Bandung, Makasar dan Denpasar), ditemukan bahwa
prevalensi migren tanpa aura adalah 10% dan migren dengan aura 1,8%.
Distribusi prevalensi migren berdasarkan usia memiliki puncak bimodal, dimana
puncak prevalensi ditemukan pada usia 20-30 tahun-an dan sekitar usia 50
tahun. Rasio migren pria:wanita adalah 1:2 hingga 1:3. (Sjahrir, 2008; Victor et
al., 2009)
II.1.2 Klasifikasi
Migren seacara garis besar diklasifikasikan menjadi: (Machfoed et al., 2010)
2. Migren dengan aura
3. Sindroma periodik pada anak yang sering menjadi prekursor migren
4. Migren retinal
5. Komplikasi migren
6. Probable migren
7. Migren tanpa aura
II.1.3 Kriteria diagnostik
1. Migren Tanpa Aura merupakan nyeri kepala berulang dengan manifestasi
serangan selama 4-72 jam. Karakteristik nyeri kepala unilateral, berdenyut,
intensitas sedang atau berat, bertambah berat dengan aktivitas fisik yang
rutin dan diikuti dengan nausea dan/atau fotofobia dan fonofobia
(Machfoed et al., 2010)
Kriteria diagnostik :
A. Sekurang-kurangnya terjadi 5 serangan yang memenuhi kriteria
B-D
B. Serangan nyeri kepala berlangsung 4-72 jam (tidak diobati atau
tidak berhasil diobati)
C. Nyeri kepala mempunyai sedikitnya dua diantara karakteristik
berikut:
1. Lokasi unilateral
2. Kualitas berdenyut
4. Keadaan bertambah berat oleh aktivitas fisik atau penderita
menghindari aktivitas fisik rutin (seperti berjalan atau naik
tangga)
D. Selama nyeri kepala disertai slaah satu dibawah ini:
1. Nausea dan/atau muntah
2. Fotofobia dan fonofobia
E. Tidak berkaitan dengan kelainan lain
2. Migren dengan aura merupakan serangan nyeri kepala berulang, dimana
didahului gejala neurologi fokal yang reversibel secara bertahap 5-20 menit
dan berlangsung kurang dari 60 menit, dengan gambaran nyeri kepala yang
menyerupai migren tanpa aura (Machfoed et al., 2010)
Kriteria diagnostik:
A. Sekurang-kurangnya terjadi 2 serangan yang memenuhi kriteria
B-D
B. Adanya aura yang terdiri paling sedikit satu dari dibawah ini, tetapi
tidak ditemukan kelemahan motorik:
1. Gangguan visual yang revesibel seperti: positif (cahaya yang
berkedip-kedip, bintik-bintik atau garis-garis) dan negatif
(hilangnya penglihatan)
2. Gangguan sensoris yang reversibel termasuk positif (pins and
needles), dan/atau negatif (hilang rasa/kebas)
D. Nyeri kepala memenuhi kriteria B-D (migren tanpa aura) yang
dimulai bersamaan dengan aura atau sesudah aura selama 60
menit
E. Tidak berkaitan dengan kelainan lain
3. Migren kronik yaitu nyeri kepala yang berlangsung ≥ 15 hari dengan paling
tidak ada 8 hari serangan migren atau probable migren dalam satu bulan
selama lebih dari 3 bulan dan tidak adanya riwayat penggunaan obat
berlebihan (Machfoed et al., 2010)
Kriteria diagnostik:
A. Nyeri kepala (tension type headache dan/atau migren) dalam > 15
hari perbulannya dan berlangsung lebih dari 3 bulan
B. Didapati pada pasien yang mendapat > 5 serangan yang
memenuhi kriteria migren tanpa aura
a. Mempunyai gejala paling tidak 2 dari dibawah ini:
1. Lokasi unilateral
2. Berdenyut
3. Intensitas nyeri sedang-berat
4. Bertambah berat apabila melakukan aktivitas fisik rutin
seperti berjalan atau naik tangga
b. Mempunyai gejala paling tidak 2 dari dibawah ini:
1. Mual dan/atau muntah
C. Didapati perbaikan apabila diberikan obat triptan atau ergot pada
saat sebelum yang diduga akan timbul gejala B.a. diatas
D. Tidak ada penggunaan obat berlebihan dan tidak berkaitan dengan
penyebab gangguan lain
II.1.4 Patogenesa
Pada tahun 1940-1950 an, Wolf et al., merupakan yang pertama kalinya
memperkenalkan teori vaskular sebagai dasar patofisologi migren, yang
kemudian teori ini mulai ditinggalkan dan berkembang lebih kompleks menuju
teori neurogenik yang dikenal dengan teori sensitisasi sentral yang menganggu
input sensorik dibatang otak terutama pada nukleus trigeminal kaudalis (gambar
1.). (Silberstein et al, 2005; Sjahrir, 2008)
Beberapa eksperimen menyatakan bahwa nyeri pada migren mungkin
suatu bentuk inflamasi neurogenik steril, dimana inflamasi neurogenik steril ini
dihasilkan akibat aktivasi neuron sensorik primer. Serabut trigeminal
mempersarafi struktur kranial dan pembuluh darah kranial yang jika teraktivasi
akan mengakibatkan pelepasan neuropeptida sepeti substansi P, neurokinin A
dan CGRP. Pada penelitian immunohistikimiawi, ditemukan bahwa nervus
trigeminal mengandung 40% CGRP, 18% substansi P, 15% NOs, dan 20%
pituitary adenilate cyclase activating peptide (PACAP). (Edvinsson, 2001; Sjahrir,
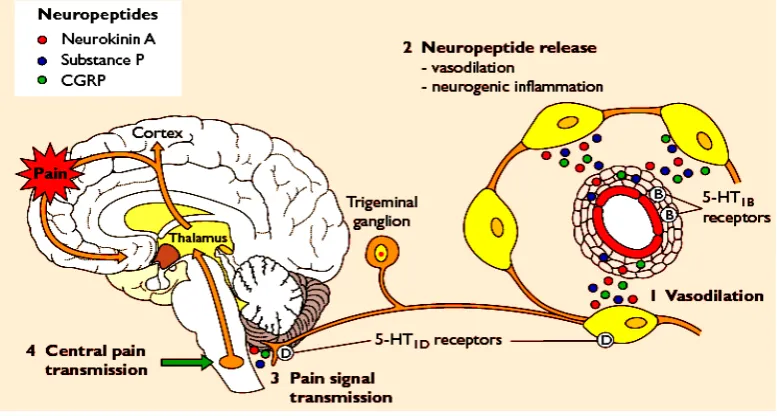
Current theories suggest that there are several key steps in the generation of migraine pain: (1) Intracranial
meningeal blood vessel dilation which activates perivascular sensory trigeminal nerves. (2) Vasoactive
neuropeptide release from activated trigeminal sensory nerves. These peptides can worsen and perpetuate any
existing vasodilation, setting up a vicious cycle that increases sensory nerve activation and intensifies headache
pain. The peptides include substance P (increased vascular permeability), neurokinin A (dilation and permeability
changes) and calcitonin gene-related peptide (CGRP; long-lasting vasodilation). (3) Pain impulses from activated
peripheral sensory nerves are relayed to second-order sensory neurons within the trigeminal nucleus caudalis in
the brain stem and upper cervical spinal cord (C1 and C2, trigeminocervical complex). (4) Headache pain signals
ascend to the thalamus, via the quintothalamic tract which decussates in the brain stem, and on to higher cortical
centers where migraine pain is registered and perceived.
Gambar 1. Postulat Mekanisme Patofisiologi Migren
Dikutip dari: Silberstein et al. 2005. Atlas of Migraine adn Other headache. Second Edition. New York; Tylor and Francis Group
Reseptor CGRP ditemukan pada sel mast dan sel mononuklear lainnya,
ganglion trigeminal, second order sensory neuron didalam nukleus trigeminal dan
didalam sel otot polos arterial. Aktivasi reseptor CGRP dalam sel otot polos
arterial mengakibatkan vasodilatasi arteri serebral dan ekstraserebral. Aktivasi
mediator inflamasi lainnya (IL-6), TNF-α, dan NO). Pada ganglion trigeminal,
CGRP mengakibatkan peningkatan sintesa CGRP dan menstimulasi pelepasan
NO dan sitokin inflamasi seperti TNF-α dan MCP-1 (Monocyte Chemotactic
Protein-1). Diduga bahwa peningkatan reseptor CGRP didalam ganglia
trigeminal, mengakibatkan terjadinya sensitisasi pada ganglion trigeminal ketika
diaktivasi oleh CGRP. Peningkatan sintesis CGRP dan yang diikuti dengan
inflamasi neurogenik, diduga mengakibatkan peningkatan sensitisasi nosiseptif.
Prostaglandin dan NO juga merupakan mediator endogen yang dapat diproduksi
secara lokal dan dapat mensensitisasi nosiseptor. (Silberstein et al, 2005;
Thalakoti et al, 2007;Theoharides et al, 2005)
Ada bukti kuat bahwa disfungsi midbrain terutama periaquaductal grey
matter (PAG) dan nukleus trigeminal spinalis (yang berperan dalam modulasi
pathway antinosiseptif dari brain stem) berperan dalam patofisiologi migren,
terutama migren kronik. Beberapa penelitian telah menemukan bahwa regio
tertentu di batang otak seperti nucleus raphe dorsalis (NRD) dan nucleus raphe
magnus (NRM), locus coeruleus (LC) dan PAG terlibat pada genesis migren.
Pada penelitian binatang, ditemukan bahwa stimulasi listrik pada area LC dan
NRD mengakibatkan perubahan mikrosirkulasi area kortikal yang ipsilateral dan
juga pada sirkulasi ekstrakranial. Implant elektroda stimulasi yang diletakkan
pada PAG manusia, ditemukan dapat menginduksi terjadinya nyeri kepala. Pada
penelitian yang menggunakan positron emission tomography (PET), menemukan
aktivasi NRD, LC dan PAG selama serangan migren yang terjadi secara spontan,
dan terlihat perubahan intensitas nyeri dan aliran darah serebral pada pemberian
triptan, tetapi aktivitas batang otak masih persisten. Pada penelitian in vitro
LC banyak mengandung CGRP (80%) dan sejumlah kecil PACAP (40%),
sedangakan sejumlah immunoreactive substansi P, CGRP dan PACAP
ditemukan pada serabut saraf di NRM, LC dan PAG. (Sjahrir, 2008;Tajti et al.,
2000)
Pada penelitian anatomi, ditemukan proyeksi dari PAG ke NRM dalam
rostroventral medula oblongata, dan NRM mengirimkan serabut saraf yang
mengandung serotoninergik dan LC mengirimkan serabut saraf yang
mengandung noradrenergik ke nukleus trigeminal kaudalis. Temuan anatomikal
ini mengindikasikan bahwa brain stem memiliki peranan dalam transmisi nyeri
pada sistem trigeminovaskular. (Tajti et al., 2000)
II.2 Tension Type Headache II.2.1 Epidemiologi
Tension type headache adalah jenis nyeri kepala primer yang terbanyak
dengan range life time prevalence pada populasi yang bervariasi, yaitu 30-78%.
Berdasarkan population based studies, rata-rata prevalensi TTH episodik dan
kronik dalam 1 tahun adalah 38,3% dan 2,2%. Pada Penelitian epidemiologi di
Denmark, ditemukan insiden TTH adalah 14,2/1000 orang/tahun, dan life time
prevalence TTH adalah 86%, dengan kebanyakan pasien (59%) dengan TTH
episodik infrequent, 24-37% pasien dengan beberapa serangan dalam 1 bulan,
10% dengan serangan setiap minggu dan 2-3% populasi dengan TTH kronik.
Rata-rata onset usia terjadinya TTH adalah 25-30 tahun dengan puncak
prevalensi ditemukan pada usia 30-39 tahun dan menurun secara perlahan
seiring dengan usia. Rasio pria:wanita adalah 1:3. (Bendtsen et al.,, 2009;
Dari hasil pengamatan pasien-pasien yang berobat jalan di praktek
swasta di Medan, menemukan profil rincian insiden pasien TTH adalah 44,1%
dengan TTH kronik dan 9,8% dengan TTH episodik. Pada poliklinik Sefalgia
Bagian Neurologi FK. USU/RS H. Adam Malik Medan, ditemukan penderita TTH
mencapai 78%, sedangkan di Bagian Neurologi FK UNPAD/RS Hasan Sadikin
mencapai 65%. Pada penelitian yang dilakukan dalam waktu 6 bulan
(Januari-Mei 2004) di poliklinik Sefalgia Bagian Neurologi/RS H. Adam Malik Medan
ditemukan 89,1% pasien TTH, dengan 58,2% TTH episodik, 16,4% TTH kronik,
dan 14,5% probable TTH (Iqbal et al., 2004; Sjahrir, 2004)
II.2.2 Klasifikasi
1. Tension type headache episodik yang infrequent
2. Tension type headache episodik yang frequent
3. Tension type headache kronik
4. Probable tension type headache
II.2.3 Kriteria Diagnostik
1. Tension type headache episodik yang infrequent yaitu nyeri kepala yang
berlangsung beberapa menit sampai beberapa hari. Nyeri kepala bilateral,
menekan atau mengikat, tidak berdenyut. Intensitas ringan atau sedang,
tidak bertambah pada aktivitas fisik rutin, tidak ada mual/muntah, tetapi
mungkin terdapat fotofobia/fonofobia (Machfoed et al., 2010)
A. Paling tidak terdapat 10 episode serangan dengan rata-rata kurang
dari 1hari/bulan selama paling tidak 3 bulan (kurang dari 12
hari/tahun) dan memenuhi kriteria B-D
B. Nyeri kepala berlangsung 30 menit hingga 7hari
C. Nyeri kepala paling tidak terdapat 2 gejala khas:
1. Lokasi bilateral
2. Menekan atau mengikat (tidak berdenyut)
3. Intensitas nyeri ringan atau sedang
D. Tidak diperberat oleh aktivitas rutin seperti berjalan atau naik tangga
2. Tension type headache episodik yang frequent Kriteria diagnostik: (Machfoed et al., 2010)
A. Paling tidak terdapat 10 episode serangan dengan rata-rata 1-15
hari/bulan selama paling tidak 3 bulan (12-180 hari/tahun) dan
memenuhi kriteria B-D
B. Nyeri kepala berlangsung 30 menit hingga 7hari
C. Nyeri kepala paling tidak terdapat 2 gejala khas:
1. Lokasi bilateral
2. Menekan atau mengikat (tidak berdenyut)
3. Intensitas nyeri ringan atau sedang
4. Tidak diperberat oleh aktivitas rutin seperti berjalan atau naik
tangga
2. Fotofobia dan fonofobia secara bersamaan
E. Tidak berkaitan dengan kelainan lain
3. Tension type headache kronik yaitu nyeri kepala yang berasal dari TTH
episodik, dengan serangan tiap hari atau serangan episodik nyeri kepala
yang lebih sering yang berlangsung beberapa menit sampai beberapa hari.
Nyeri kepala bersifat bilateral, menekan atau mengikat dalam kualitas dan
intensitas ringan atau sedang, dan nyeri tidak memberat dengan aktivitas
fisik yang rutin. Kemungkinan terdapat mual, fotofobia atau fonofobia ringan
(Machfoed et al., 2010)
Kriteria diagnostik:
A.
Nyeri kepala timbul ≥ 15 hari/bulan, berlangsun
g > 3 bulan (
≥
180
hari/tahun) dan juga memenuhi kriteria B-D
B. Nyeri kepala berlangsung beberapa jam atau terus menerus
C. Nyeri kepala memiliki paling tidak 2 karakteristik berikut:
1. Lokasi bilateral
2. Menekan atau mengikat (tidak berdenyut)
3. Intensitas nyeri ringan atau sedang
4. Tidak memberat dengan aktivitas fisik yang rutin
D. Tidak didapatkan:
1. Lebih dari satu: fotofobia, fonofobia atau mual yang ringan
2. Mual yang sedang atau berat, maupun muntah
II.2.4 Patogenesa
Nyeri miofasial memiliki peranan pada TTH. Nyeri miofasial didefenisikan
sebagai nyeri yang berasal dari otot striata termasuk fascia dan insersi
tendonnya. Gejala yang menonjol pada pasien dengan TTH yaitu nyeri tekan
yang bertambah pada palpasi jaringan miofasial perikranial. Berdasarkan
hipotesa updated pain model pada TTH, dinyatakan bahwa TTH terjadi akibat
referred nyeri dari trigger point di otot posterior servikal, kepala dan bahu yang
dimediasi melalui medula spinalis dan nukleus trigeminal kaudalis. Penelitian
pada binatang dan manusia, menemukan bahwa aferen somatik nosiseptif dari
otot servikal atas (C1-C3) dan nervus trigeminal (n.V1 (oftalmikus) dan V3
(mandibula)) berkonvergensi kedalam nukleus trigeminal kaudalis yang sama,
sehingga diasumsikan bahwa struktur supraspinal menjadi salah interpretasi
terhadap impuls yang diterima dan lokasi nyeri diartikan menjadi berasal dari
struktur yang jauh dari asal stimulus nyeri (muscle reffered pain). Mekanisme
timbulnya nyeri miofasial dan nyeri tekan adalah: (Bendsten, 2000; Ferdinanz et
al.,2007; Sjahrir, 2008)
1.
Sensitisasi nosiseptor miofasial perifer
2.
Sensitisasi second order neuron pada level kornu dorsalis medula
spinalis/ nukleus trigeminal
3.
Sensitisasi neuron supraspinal (hipersenitivitas supraspinal terhadap
stimulus nosiseptif)
4.
Berkurangnya aktivitas antinosiseptif dari struktur supraspinal
tebal bermielin (Aα dan A ) nor
malnya memediasi sensasi innocuous.
Berbagai rangsangan noxious dan innocuous seperti iskemik, stimulus
mekanikal dan mediator kimiawi dapat mengeksitasi dan sensitisasi
serabut saraf
Aδ
dan C, dan berperan dalam peningkatan nyeri tekan
pada TTH (gambar 2.). Mediator kimiawi yang mensensitisasi nosiseptif
nerve endings, terutama yang efektif menstimulasi nosiseptor otot skeletal
adalah substansi endogen seperti serotonin (dilepaskan oleh platelet),
bradikinin ( dari pemecahan molekul prekursor plasma kallin ) dan ion
kalium (dilepaskan oleh sel otot ketika terjadi proses patologis (injury,
iskemia, vascular damage)), serta pelepasan neuropeptida seperti
substansi P, CGRP dan neurokinin A. (Bendsten, 2000; Fernandez et al.,
2007; Sjahrir, 2008)
Pelepasan mediator kimiawi yang berkepanjangan mengakibatkan
aktivasi reseptor post sinaptik yang normalnya terblok, yaitu reseptor
NMDA. Aktivasi reseptor NMDA menimbulkan peningkatan influks
kalsium, yang menginisiasi terjadinya kejadian biokimiawi berupa
peningkatan produksi NO, prostaglandin dan protein kinase. Hal ini
mengakibatkan perubahan metabolik dalam jangka panjang dan
peningkatan eksitabilitas sel yang terlibat. (Bendsten, 2000)
Peningkatan eksitabilitas neuron kornu dorsalis mengakibatkan
perubahan persep
si nyeri, dimana serabut saraf A yang normalnya
menginhibisi serabut saraf Aδ dan C melalui mekanisme presinaptik pada
order neuron dan mengakibatkan input impuls nosiseptif menjadi lebih
panjang (gambar 2.). ( Bendsten, 2000; Fernandez et al., 2007)
Sensitisasi pada second order neuron, mengakibatkan tranmisi
stimulus nosiseptif pada struktur supraspinal meningkat (sensitisasi
neuron supraspinal) dan hal ini yang diduga mengakibatkan nyeri tekan
perikranial yang abnormal pada TTH (gambar 2.). Sensitisasi pada neuron
supraspinal mengakibatkan penurunan inhibisi atau peningkatan fasilitasi
transmisi nosiseptif dalam kornu dorsal spinalis yang bermanifestasi
sebagai generalized pain hypersensitivity yang ditemukan pada TTH
kronik. (Bendsten, 2000; Fernandez et al., 2007)
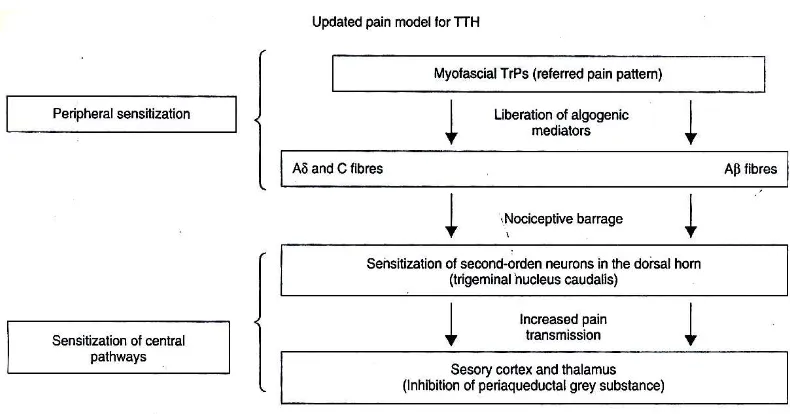
Updated pain model for tension type headache (TTH) in which peripheral sensitization provoked by muscle trigger
points (TrPs) can lead to sensitization of dorsal horn neurons.
Gambar 2. Updated pain model pada TTH
Terdapat 2 struktur pain modulatory, yaitu PAG pada mesensefalon yang
berperan dalam inhibisi descending pathways ke kornu dorsalis medula spinalis,
dan rostral ventromedial medulla (RVM) di batang otak yang mengandung sel
yang dapat menginhibisi atau menfasilitasi transmisi nosiseptif di dalam kornu
dorsalis medula spinalis. Ambang batas refleks fleksi nosiseptif ditemukan
menurun pada TTH kronik, dibandingkan kontrol, yang menandakan disfungsi
sistem antinosiseptif pada TTH kronik. (Bendtsen, 2000; Fernandez et al., 2007)
Faktor-faktor miofasial dan sensitisasi perifer dari nosiseptor memegang
peranan dalam kejadian TTH episodik, sedangkan sensitisasi sentral berperan
terhadap TTH kronik. (Sjahrir, 2008)
II.3 Adiponektin II.3.1 Defenisi
Adiponektin adalah protein yang disekresikan dari sel adiposit, berukuran
30 kDa dengan sekuensi 244 asam amino dan memiliki domain terminal kolagen
dan carboxyl. (Assaad, 2007; Dadson et al., 2011)
II.3.2 Regulasi
Transkripsi adiponektin diregulasi oleh peroxisome proliferator-activated
receptor (PPAR ), C/EBP, SREBP, E47, dan protein Idγ. Salah satu
mekanisme yang mengaktivasi transkripsi adiponektin adalah melalui regulasi
SREBP-1c, dimana Id3 dan E47 merupakan regulator SREBP-1c. Interaksi E47
dengan SREBP-1c, akan mempotensiasi SREBP-1c dalam memediasi aktivasi
promoter adiponektin dan Id3 menginhibisi aktivasi SREBP-1c ini. Juga telah
thiazolidinedione yang merupakan kelas PPAR agonist dapat meningkatkan
induksi ekspresi adiponektin, dan sitokin proinflamasi seperti TNF-α merupakan
faktor yang ditemukan dapat menurunkan ekspresi adiponektin pada pasien yang
obese atau diabetes. (Dadson et al., 2011; Kadowaki et al., 2005)
Translasi berperan dalam membentuk kompleks oligomer adiponektin
yang fungsional. Multimerisasi adiponektin tahap awal melibatkan domain
globular non-kolagen dan membentuk trimer. Selanjutnya ikatan rantai disulfida
dengan Cys36 dan Cys39 akan membentuk adiponektin dengan berat molekul
yang lebih berat berdasarkan bentruk trimer-nya. Modifikasi post-translasi
termasuk hidroklasi dan glikolasi dari 4 residu lisin (lys68, lys71, lys80, lys104)
pada domain kolagen diperlukan dalam membentuk komplek oligomer HMW.
Disulfide bond A oxidoreductase-like protein (DsbA-L) ditemukan meregulasi
proses multimerisasi adiponektin. (Dadson et al., 2011)
Sekresi adiponektin secara spesifik diregulasi oleh protein retikulum
endoplasma yaitu ER44 dan Ero 1-Lα. Ikatan kovalen yang dibentuk oleh ER44
dan Cys 39 mengakibatkan penahanan adiponektin didalam retikulum
endoplasma, sedangkan ikatan disulfida yang dibentuk oleh ER44 dan Erol-Lα
mengakibatkan sekresi adiponektin ke sirkulasi. Bentuk oligomerik adiponektin
dalam plasma yang bersirkulasi dapat ditemukan dalam bentuk HMW (oligomer),
medium molecular weight/MMW (hexamer) dan low molecular weight/LMW
(Trimer). Kombinasi semua bentuk oligomerik ini disebut dengan full length
adiponectin (fAd), dan pemecahan pada terminal domain globular dari fAd oleh
protease disebut dengan globular adiponektin (gAd). (Assaad, 2007; Dadson et
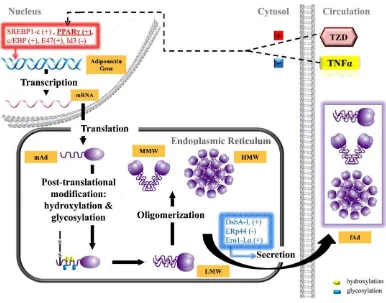
Several transcription factors(top left) which mediate adiponectin gene transcription are regulated toincrease
(thiazolidinedione, TZD) or decrease (tumor necrosis factor-alpha, TNF-α) adiponectin expression. Monomeric adiponectin (mAd) isposttranslationally modified and further oligomerized to form trimers (lowmolecular weight,
LMW), hexamers (medium, MMW) and oligomeric (high,HMW) forms. Various mechanisms (bottom right) mediate
this oligomerization and secretion resulting in secretion of HMW, MMW, and LMW forms.
Gambar 3. Regulasi Adiponektin
Dikutip dari Dadson et al.., 2011. Adiponectin action: a combination of endocrine and autocrine/paracrine effects. Frontiers in Endocrinology-Cellular Endocrinology;2(62)
II.3.3 Reseptor
Efek selular adiponektin terjadi akibat ikatan reseptor adiponektin dengan
domain transmembran. Adiponektin memiliki 2 isoform reseptor yaitu adiponektin
reseptor 1 (AdipoR1) dan adiponektin reseptor 2 (AdipoR2) yang memiliki pola
distribusi yang berbeda pada berbagai jaringan. Adiponektin reseptor 1 memiliki
gAd dan fAd. Ekspresi AdipoR1lebih dominan ditemukan pada otot skeletal,
sedangkan ekspresi AdipoR2 lebih dominan ditemukan pada hati, dan kedua
reseptor ini juga ditemukan pada Reseptor adiponektin juga ditemukan pada
adiposit dan makrofag. (Assaad, 2007; Dadson et al.., 2011)
II.3.4 Fisiologi
Adiponektin bersirkulasi dengan range konsentrasi 3-γ0 μg/ml pada
individu yang sehat. Adiponektin diperkirakan ± 0,01% total protein plasma dan
merupakan salah satu sekresi adipositokin yang ditemukan paling tinggi pada
sirkulasi dibandingkan adipositokin lainnya. Waktu paruh adiponektin pada
berbagai penelitian adalah bervariasi, dimana pada penelitian dengan tracking
fluorescently labeled recombinant adiponectin, ditemukan waktu paruh
adiponektin adalah 75 menit, sedangkan pada penelitian binatang sebelumnya
dengan menggunakan recombinant human adiponectin, ditemukan bahwa
adiponektin memiliki waktu paruh 14 jam, adiponektin HMW memiliki waktu paruh
13 jam dan LMW memiliki waktu paruh 17,5 jam. (Assaad, 2007; Dadson et al.,
2011; Peterlin et al., 2007)
Adiponektin berperan dalam regulasi metabolisme glukosa dan asam
lemak, melalui peningkatkan sensitivitas kerja insulin, yang melibatkan aktivasi
adenosine monophosphate-activated protein kinase (AMPK) yang diketahui
meregulasi konsentrasi selular malonyl coenzyme A (CoA) melalui inhibisi acetyl
CoA carboxylase yang dapat mengakibatkan penurunan kadar malonyl CoA
intraselular dan selanjutnya akan menurunkan lipogenesis yang berhubungan
dengan peningkatan oksidasi mitochondrial fatty acid beta. Adiponektin juga
phosphoenolpyruvate carboxylase dan glucose-6-phosphatase yang merupakan
2 enzim yang terlibat pada neoglukogenesis. (Ahima, 2006; Bastard et al, 2006)
Adiponektin memiliki efek anti aterogenik, dimana adiponektin
menginhibisi ekspresi vascular cell adhesion molecule (VCAM)-1, intercelullar
adhesion molecule (ICAM)-1 dan E-selectin, sehingga mensupresi adherence
dari monosit dan platelet pada endotelium, serta adiponektin juga menginhibisi
ekspresi reseptor scavenger kelas A-1 Makrofag, yang mengakibatkan
penurunan oksidasi low density lipoprotein oleh makrofag dan menginhibisi
pembentukan foam cell. (Ekmekci et al, 2006; Kadowaki et al, 2005)
Adiponektin juga memiliki efek antiinflamasi, yaitu; menginhibisi IL-6 dan
TNF yang menginduksi IL-8, serta menginduksi IL-10, dan IL-1RA (reseptor
antagonis). Sitokin pro-inflamasi seperti IL-1, IL-6, 1L-8 dan TNF diprodusi oleh
sel imun yang teraktivasi dan amplifikasi sitokin ini ditemukan sebagai respon
inflamasi, sedangkan IL-1RA dan IL-10 terlibat dalam reduksi respon inflamasi.
(Peterlin et al, 2007)
(IL)-6. C-reactive protein (CRP) is negatively regulated adiponectin. NF-kB, Nuclear factor kappa beta; VCAM-1,
vascular cell adhesion molecule-1.
Gambar 4. Peranan adiponektin dalam cascade inflamasi
Dikutip dari: Peterlin et al. 2007. Migraine and Adiponectine: Is There a Connection?. Cephalalgia;27
Adiponektin juga diduga memiliki efek inflamasi, dimana efek
pro-inflamasi dan anti-pro-inflamasi dari adiponektin ini ditentukan oleh bentuk
adiponektin. Globular adiponektin mengaktivasi pahways proinflamasi NF-κ dan
menginduksi sekresi NO dan sitokin proinflamasi seperti IL-6 dan TNF-α.
Adiponektin HMW ditemukan mengaktivasi NF-ƙ yang akan menginduksi
sekresi IL-6, sedangkan adiponektin LMW ditemukan menurunkan sekresi IL-6.
(Ahima, 2006; Peterlin et al, 2008)
II.4 Hubungan Adiponektin dengan Nyeri Kepala
Hubungan adiponektin dengan nyeri kepala hanya ditemukan pada
penelitian Peterlin dkk. (2008), yang menemukan bahwa kadar total adiponektin
ditemukan lebih tinggi pada kelompok pasien dengan CDH (10,1±4,0 μg/mL)
dibandingkan pasien dengan migren episodik (8,6±3,5 μg/mL) dan kontrol
(7,5±4,0 μg/mL) (p=0,0β4). Kadar adiponektin HMW ditemukan lebih tinggi pada
CDH (6,1±2,8 μg/mL) dibandingkan migren episodik (4,2±1,7 μg/mL) dan kontrol
(3,9±1,5 μg/mL) (p=0,003), serta kadar adiponektin MMW juga ditemukan lebih
tinggi pada CDH (2,0±1,2 μg/mL) dibandingkan migren episodik (1,5±0,7 μg/mL)
dan kontrol (1,1±0,4 μg/mL) (p=0,009). Tetapi tidak ditemukan perbedaan yang
bermakana dari adiponektin LMW pada CDH, migren atau kontrol (P =0,22).
Sehingga diduga terdapat efek pro-inflamasi dari adiponektin pada nyeri kepala
Aktivitas biologi adiponektin bergantung pada struktur kompleks
oligomernya. Berdasarkan penelitian in vitro, telah ditemukan bahwa adiponektin
HMW mengaktivasi pathways NF-ƙ dan selanjutnya menginduksi sekresi IL-6.
Nuclear factor-ƙ dan IL-6 diketahui memiliki implikasi pada inflamasi neurogenik
pada migren. Pada penelitian in vitro lainnya, juga menemukan bahwa kadar gAd
10 µg/ml dapat mengakibatkan peningkatan aktivasi NF-ƙ sebesar 13,6 kali
dibandingkan adiponektin HMW, dan aktivasi NF-ƙ ini menginduksi ekspresi
dari berbagai pro-inflamasi dan adhesion molecule genes. (Haugen et al, 2007;
Peterin et al., 2007; Tomizawa et al., 2008)
Adiponektin baik dalam bentuk gAd dan fAd juga telah ditemukan dapat
meningkatkan produksi NO, dan NO berperan dalam meningkatkan sensitisasi
sentral pada patofisiologi nyeri kepala primer, termasuk migren dan TTH kronik.
(Ashina et al, 2000; Jensen, 2001; Peterlin et al, 2007; Sjahrir, 2008)
Pendapat lain mengenai hubungan adiponektin terhadap nyeri kepala
adalah, bahwa adipokines seperti TNF-α, IL-1 , IL-6, IL-8 yang merupakan
pro-inflamasi, ditemukan meningkat pada obesitas, sedangkan kadar adiponektin
yang disekresikan dari sel adiposit ditemukan menurun pada subjek dengan
obesitas, sehingga diduga efek adiponektin sebagai anti-inflamasi pada individu
obesitas menjadi terbatas. (Aprahamian et al., 2011; Assaad, 2007; Peterlin et
al., 2007). Pada penelitian yang lain, telah ditemukan bahwa obesitas merupakan
salah satu faktor resiko untuk terjadinya headache chronification. (Scher et al.,
II.5. Kerangka Teori
Peterlin et al. (2007): Adiponektin HMW mengaktivasi pathways NF-kB dan menginduksi sekresi IL-6, sedangkan adiponektin LMW menginhibisi sekresi IL-6
Peterlin et al. (2007): Adiponektin baik dalam bentuk gAd dan fAd meningkatkan produksi NO
Peterlin et al. (2007): Level adiponektin didalam sirkulasi ditemukan menurun pada
Haugen dkk (2007) dan Tomizawa dkk (2008): Adiponektin HMW dan gAd meningkatkan aktivasi NF- ƙ
Peterlin et al. (2007): NF-kB dan IL-6 memiliki implikasi pada inflamasi neurogenik pada migren
II.6.Kerangka Konsep
Adiponektin
Migren dan TTH PRO-INFLAMASI
TNF-α IL-6 NO