STUDI POTENSI ISOLAT KAPANG TANAH DARI WONOREJO SURABAYA DALAM MENDEGRADASI LIGNIN
Yuni Miftachul Rohmah*, Nengah Dwianita Kuswytasari1, Maya Shovitri1
Jurusan Biologi, Fakultas Matematika Dan Ilmu Pengetahuan Alam Institut Teknologi Sepuluh Nopember Surabaya
Gedung H Kampus ITS Sukolilo, Surabaya 60111, Indonesia
Abstrak
Tujuan penelitian ini adalah untuk mengtahui kemampuan degradasi lignin dari isolat kapang tanah Wonorejo Surabaya, yang terdiri dari 18 genus, yaitu Aspergillus, Penicillium, Trichoderma, Paechylomyses, Stachybotrys, Verticillium, Chaetomium, Myselia sterilia, Curvularia, Acremonium, Mortierella, Scopuloriopsis, Gliomastix, Absidia, Fusarium, Gliocladium, Exophiala dan Cephaliospora. Uji awal adalah deteksi zona bening dengan menggunakan medium padat dengan pewarna larutan FeCl3 dan K3[Fe(CN)6]. Kapang yang memiliki zona bening kemudian ditumbuhkan pada medium cair dan diinkubasi selama 10 hari. Degradasi lignin yang terjadi selama masa tersebut diukur berdasarkan nilai serapan lignin pada panjang gelombang 232 nm. Berdasarkan parameter zona bening dan presentase penurunan lignin, hasil penelitian menunjukkan hanya 4 isolat kapang yang mampu mendegradasi lignin. Isolat tersebut adalah Gliomastix sp.2 1,4 cm/46,95%, Myselia sterilia sp.2 1,29 cm/44,76%, Penicillium sp.1 1,16 cm/40,63%, dan Mortiriella sp. 1,06 c/18,73%. Angka tersebut menunjukkan rasio zona bening dan persentase penurunan lignin.
Kata kunci: zona bening, kapang tanah Wonorejo Surabaya, degradasi lignin. Abstract
The study was aimed to assess the ability of mold isolates from Wonorejo Surabaya to degrade lignin, which consists of 18 genera, namely Aspergillus, Penicillium, Trichoderma, Paecylomyces, Stachybotrys, Verticillium, Chaetomium, mycelia sterilia, Curvularia, Acremonium, Mortiriella, Scopulariopsis, Gliomastix, Absidia, Fusarium, Gliocladium, Exophiala and Cephaliospora. Initial test is the detection clear zone by using a solid medium with a dye solution of FeCl3 and K3 [Fe (CN) 6]. Mold that has a clear zone then grown in a liquid medium and incubated for 10 days. Lignin degradation that occurred during this period is measured based on the value of lignin absorption at a wavelength of 232 nm. Based on the parameters of clear zone and the percentage reduction in lignin, the results showed only 4 isolates of mold that can degrade lignin. Isolates were Gliomastix sp.2 1.4 cm/46, 95%, Myselia sterilia sp.2 1.29 cm/44, 76%, Penicillium sp.1 1.16 cm/40, 63%, and Mortiriella sp. C/18 1.06, 73%. The figure shows the ratio of clear zone and the percentage reduction in lignin.
Key words: clear zone, soil molds Wonorejo Surabaya, lignin degradation. *Coresponding Author Phone: 85852081508
1
1. Pendahuluan
Lignin merupakan polimer yang strukturnya heterogen dan kompleks yang terdiri dari koniferil alkohol, sinaphil alkohol, dan kumaril alkohol sehingga sulit untuk dirombak. Sekitar 30% material pohon adalah lignin yang berfungsi sebagai penyedia kekuatan fisik pohon, pelindung dari biodegradasi dan serangan mikroorganisme (Schlegel, 1994; Singh, 2006). Kapang merupakan salah satu mikroorganisme yang mampu mendegradasi lignin (Singh, 2006; Grainger & Lynch, 1984).
Kapang dapat mendegradasi lignin karena mampu mensintesis enzim ligninase. Ada tiga enzim ligninase dari kapang yaitu lignin peroxidase (LiP), mangan peroxidase (MnP), dan laccase. Beberapa kapang ada yang hanya mampu mensintesis dua atau satu enzim saja (Singh, 2006). White rot fungi merupakan mikroorganisme yang paling aktif dalam pendegradasian lignin, yang menghasilkan CO2 dan H2O dalam mendegradasi lignin. Phanerochaeta
chrysosporium merupakan kelompok white rot fungi yang sering dipelajari dan diteliti
oleh para ilmuan dalam mendegradasi lignin. Diketahui Phanerochaete chrysosporium mampu mensintesis enzim lignin peroksidase (LiP) dan mangan peroksidase (MnP) dalam mendegradasi lignin (Hattaka, 1994). Beberapa kelompok kapang telah diketahui kemampuannya dalam mendegradasi lignin yaitu Aspergillus awamori (Sintawardani, 1997), Penicillium chrysogenum, Fusarium
solani (Grainger & Lynch, 1984), dan Fusarium oxysporum (Singh, 2006).
Lignin peroksidase (LiP) dan mangan peroksidase (MnP) adalah enzim peroksidase ekstraseluler yang menggunakan H2O2 dalam mendegradasi lignin. LiP mampu memecah ikatan Cα-Cβ pada lignin (Hattaka, 1994), sedangkan MnP telah ditemukan sebagai salah satu enzim yang dihasilkan jamur pelapuk putih yang mampu mendepolimerisasi lignin dan demetilisasi lignin (Hattaka, 1994; Samsuri, 2004). Laccase merupakan enzim yang mengandung
tembaga dengan menggunakan molekul oksigen dalam mendegradasi lignin (Hattaka, 1994).
Enzim ligninase yang dihasilkan oleh kapang mempunyai peluang besar untuk diaplikasikan di industri-industri, terutama industri pulp dan kertas. Selama ini, industri pulp dan kertas menggunakan bahan kimia untuk mengolah kayu menjadi produk akhirnya. Dari salah satu sisi, penggunaan bahan kimia ini meningkatkan kualitas pulp, tetapi dari sisi lain buangan sisa bahan kimia yang umumnya mengandung klor dan klorit dapat mencemari lingkungan. Oleh sebab itu, diperlukan cara dalam pengolahan pulp yang ramah lingkungan, antara lain secara biologi dengan memanfaatkan mikroorganisme untuk melemahkan struktur kayu (Astin, 2007). Enzim ligninase juga berperan untuk degradasi polutan seperti pewarna yang dihasilkan dari industri tekstil (Wilkolazka et
al, 2002) dan biokonversi lignin yang
memanfaatkan bagase tanaman tebu untuk bioethanol (Samsuri dkk., 2004).
Uji degradasi lignin oleh kapang dapat dideteksi dengan parameter rasio zona bening, yaitu diamater zona bening dibagi diameter koloni kapang. Zona bening merupakan zona yang terbentuk pada medium di sekeliling koloni kapang, setelah masa inkubasi. Zona bening terbentuk akibat sekresi enzim ligninase yang menguraikan substrat lignin pada medium tersebut, menjadi senyawa yang lebih sederhana seperti CO2 dan H2O (Pointing, 1999; Singh, 2006). Uji degradasi lignin dapat juga dideteksi dengan menggunakan spektrofotometer dengan panjang gelombang 232 nm. Menurut Agustina (2007) dan Clarina (2007), panjang gelombang 232 nm merupakan panjang gelombang untuk mengukur keberadaan lignin pada suatu medium cair.
Kapang merupakan salah satu mikroorganisme yang mampu mendegradasi lignin (Singh, 2006; Grainger & Lynch, 1984). Dalam penelitian Kuswytasari, dkk (2011) telah berhasil diisolasi dan dipurifikasi 37 isolat kapang tanah dari Wonorejo Surabaya . Isolat tersebut menjadi
koleksi Laboratorium Mikrobiologi dan Bioteknologi Jurusan Biologi ITS. Isolat tersebut berasal dari genus Penicillium, Aspergillus, Paecilomyces, Fusarium, Verticillium, Trichoderma, Scopulariopsis, Curvularia, Stachybotrys, Gliocladium, Gliomastix, Acremonium, Chaetomium, Mortiriella, Absidia, Exophiala, dan Cephaliophora. Penelitian ini merupakan penelitian lanjutan untuk mengetahui potensi isolat kapang tanah tersebut dalam mendegradasi lignin.
2. Metodologi
Penelitian dilakukan pada bulan Agustus sampai September 2011 di Laboratorium Mikrobiologi dan Bioteknologi Biologi ITS. Tiga puluh tujuh (37) isolat kapang di dapatkan dari koleksi kultur murni Laboratorium Mikrobiologi dan Bioteknologi Jurusan Biologi ITS. Isolat kapang diisolasi dari kawasan pesisir Wonorejo Surabaya oleh peneliti sebelumnya (Kuswytasari dkk, 2011). Isolat kapang disubkultur di media PDA-C pada Petri dish.
Media yang digunakan terdiri dari medium dasar, LAC (Lignin Agar
Chloramphenicol ), LC (Lignin
Chloramphenicol). Medium Potato Dextrose Agar - Chloramphenicol (PDA-C) adalah
medium yang mengandung PDA dengan
chloramphenicol.
Medium Dasar yang digunakan terdiri dari larutan garam mineral dan yeast ekstrak. Komposisi medium dasar dalam 1 liter aquades terdiri dari 1 gr MgSO4. 7H2O; 1,5 gr KH2PO4; 0,2 gr CaCl2.2H2O; 0,2 gr FeSO4. 7H2O; 0,2 gr MnSO4; 2 gr yeast ekstrak. Komposisi Media dasar dimodifikasi dari Fauzan (2009), Yang et al (2005), Thorn (1996) dan Pointing (1999).
Medium Lignin Agar
Chloramphenicol (LAC) adalah medium
yang mengandung medium dasar sebanyak 1 liter, lignin alkali (Sigma) 0,25 % (w/v), 16 gr agar, dan 100 mg chloramphenicol. Medium dimodifikasi dari Thorn (1996), Pointing (1999) dan Marginingrum (2001).
Medium Lignin Chloramphenicol (LC) adalah medium yang mengandung medium dasar sebanyak 1 liter, lignin alkali (Sigma) 0,25 % (w/v), dan 100 mg
chloramphenicol. Semua bahan dicampur,
dihomogenkan hingga larut dan dipanaskan hingga mendidih. Setelah mendidih, erlenmeyer ditutup dengan alumunium foil dan plastik wrap. Medium dimodifikasi dari Thorn (1996), Pointing (1999) dan Marginingrum (2001).
Isolat kapang subkultur berusia 7 hari diinokulasikan pada cawan petri yang berisi 20 ml medium LAC. Kemudian diinkubasi 2-10 hari pada suhu kamar di tempat gelap sampai pertumbuhan diameter koloni kapang mencapai ± 3 cm. Setelah diinkubasi, dilakukan pewarnaan pada cawan petri dengan menambahkan 0,5% (w/v) larutan FeCl3 dan K3[Fe(CN)6]. Terbentuknya zona bening pada media diamati. Bagian yang terdegradasi akan dikelilingi warna bening sedangkan yang tidak terdegradasi berwarna biru kehijauan. Selanjutnya dilakukan pengukuran diameter koloni dan diameter zona bening. Aktivitas ligninase dihitung sebagai rasio antara diameter zona bening dibagi diameter koloni. Isolat kapang tanah yang memiliki rasio zona bening dilanjutkan ke uji degradasi lignin. Kontrol adalah medium LAC tanpa inokulasi isolat kapang tanah. Metode dimodifikasi dari Pointing (1999).
Lignin yang terlarut dalam medium LC (0,25% w/v) diukur dengan meggunakan spektrofotometer pada panjang gelombang 232 nm. Nilai serapan ini disebut dengan nilai serapan awal. Hasil pengukuran nilai serapan lignin pada hari ke-10 dibandingkan dengan nilai serapan lignin awal. Starter kapang diinokulasikan sebanyak 15 ml ke dalam 135 ml medium LC pada erlenmeyer 250 ml. Kultur diinkubasi pada suhu kamar selama 10 hari dengan rotary shaker (Health, H-M-SR®) pada goyangan 130 rpm. Pada hari ke-10 lignin yang terdegradasi diukur nilai serapan lignin. Kultur disaring dengan kertas saring. Supernatan yang diperoleh diencerkan terlebih dahulu, kemudian diambil sebanyak 5 ml dan diukur nilai
serapan lignin menggunakan spektrofotometer (Techom UV Vis 1100,
Jepang) pada panjang gelombang 232 nm. Kontrol merupakan medium LC tanpa diinokulasikan starter tahap 3 dan diukur nilai serapan lignin pada panjang gelombang 232 nm setelah inkubasi 10 hari. Pada uji degradasi lignin dilakukan pengukuran pH medium dengan menggunakan kertas indikator universal sebelum diinokulasikan kapang dan setelah diinokulasikan kapang dengan dinkubasi selama 10 hari. Metode dimodifikasi dari Agustina (2007) dan Illa Clarina (2007). Uji skrining degradasi lignin dianalisa dengan menggunakan metode deskriptif . Sedangkan untuk degradasi lignin menggunakan Rancangan Acak Lengkap. Penelitian ini menggunakan tiga kali ulangan. Data kemampuan degradasi lignin yang diperoleh pada tiap perlakuan selanjutnya diuji dengan Analysis of Variance (ANOVA) One Way. Jika
berpengaruh dilanjutkan dengan uji Dunnet. 3. Hasil dan Pembahasan
Teknik Inokulasi pada Medium Lignin Agar Chloramphenicol (LAC)
Pada penelitian ini sebelum dilakukan uji skrining degradasi lignin, dilakukan penentuan teknik inokulasi ke dalam medium LAC sebagai uji pendahuluan. Teknik inokulasi yang pertama yaitu dengan menginokulasikan spora isolat kapang dari medium PDA-C ke tengah medium LAC sebesar 1 titik menggunakan jarum tanam tajam. Teknik yang kedua yaitu menginokulasikan spora isolat kapang dari medium PDA-C ke tengah medium LAC dengan diameter 1 cm (agar plug) menggunakan jarum tanam tajam yang telah dimodifikasi (berbentuk lingkaran pada ujungnya dengan diameter 1 cm). Isolat kapang yang diujikan adalah Gliomastix sp. 2. Medium LAC yang telah diinokulasi kapang, kemudian diinkubasi selama 2 hari. Uji pendahuluan ini dilakukan untuk mengetahui pengaruh teknik inokulasi terhadap terbentuknya zona bening pada medium LAC oleh kapang.
Hasil menunjukkan terdapat perbedaan rasio zona bening. Rasio zona bening yang terbesar terjadi pada teknik inokulasi 1 titik. Pada teknik inokulasi 1 titik, menghasilkan diameter kapang 1,5 cm, zona bening 1,9 cm, dan rasio zona bening 1,26 cm. Sedangkan teknik inokulasi diameter 1 cm menghasilkan diameter kapang 2,5 cm, zona bening 2,9 cm, dan rasio zona bening 1,16 cm (Gambar 1).
Gambar 1 A. Inokulasi kapang dengan 1 titik (Teknik 1). B. Inokulasi kapang dengan diameter 1 cm (Teknik 2). C. Rasio zona bening dari ke-2 teknik.
Adanya perbedaan pertumbuhan diameter dan rasio zona bening antara teknik 1 dan 2, diperkirakan karena adanya sumber karbon lain yang berasal dari PDA-C yang ikut terinokulasi pada teknik 2, sehingga kapang akan menggunakan sumber karbon dari PDA-C terlebih dahulu, baru kemudian menggunakan sumber karbon dari proses degradasi lignin. Sedangkan pada teknik 1, kapang menggunakan sumber karbon satu-satunya yaitu lignin pada medium LAC. Kapang harus mensekresikan enzim ligninanse terlebih dahulu untuk memecah lignin menjadi senyawa yang sederhana seperti asam organik, CO2, dan H2O, yang kemudian akan diabsorbsi oleh kapang. Jadi, dapat diperkirakan bahwa waktu degradasi lignin pada teknik 1 lebih cepat dan enzim yang disekresikan lebih banyak daripada teknik 2. 1.26 1.16 1.1 1.12 1.14 1.16 1.18 1.2 1.22 1.24 1.26 1.28 A B. Teknik1 C. Teknik 2
Uji Skrining Degradasi Lignin
Uji skrining degradasi lignin adalah uji untuk mengetahui kemampuan isolat kapang dalam menguraikan lignin pada media selektif padat, dengan mengukur zona bening yang dibentuknya. Menurut Pointing (1999), uji degradasi lignin oleh kapang dapat dideteksi dengan pengukuran zona bening. Zona bening merupakan zona yang terbentuk pada medium selektif padat setelah masa inkubasi tertentu di sekeliling koloni kapang, akibat sekresi enzim ligninase. Enzim tersebut akan menguraikan lignin pada medium menjadi senyawa yang lebih sederhana (Pointing, 1999; Singh, 2006), sehingga menimbulkan perbedaan warna antara zona yang sudah terurai dengan yang belum di sekitarnya. Zona bening yang ada di sekitar koloni kapang terbentuk karena pewarna Potassium Ferricianida dan FeCl3 tidak mampu berikatan dengan lignin yang sudah diuraikan oleh enzim ligninase.
Gambar 2 Rasio Zona Bening Ligninase Kapang Wonorejo Surabaya
Gambar 2 menunjukkan bahwa dari 37 isolat kapang, hanya 4 isolat kapang yang menghasilkan zona bening. Berdasarkan rasio yang tertinggi urutan ke-4 isolat kapang tersebut adalah Gliomastix sp.2 (1,4 cm),
Myselia sterilia sp.2 (1,29 cm), Penicillium
sp.1 (1,16 cm), dan Mortiriella sp. (1,06 cm). Dengan asumsi bahwa semakin besar nilai rasio zona bening, semakin banyak enzim yang disekresikan, maka urutan tersebut juga menunjukkan urutan potensi isolat kapang pendegradasi lignin. Gambar 4.3 menunjukkan zona bening disekeliling koloni isolat kapang tersebut.
Gambar 3 Gambar Kapang yang menghasilkan zona bening
Penelitian mengenai uji zona bening ligninase pada medium padat yang mengandung lignin alkali belum banyak dilakukan, sehingga hasil penelitian ini belum bisa dibandingkan dengan penelitian-penelitian sebelumnya. Dari keempat genus isolat kapang tersebut,yang paling sering ditemukan dalam penelitian enzim ligninase pada medium cair adalah Penicillium (Yang
et al. (2005), Rodriguez (1996), Zeng et al.
(2006), dan Subowo (2010)). Genus Gliomastix, Mortiriella, dan Myselia sterilia masih belum ditemukan penelitian mengenai degradasi lignin. Sehingga hasil penelitian ini dapat digunakan sebagai wacana baru tentang potensi ke-4 isolat tersebut dalam mendegradasi lignin. 0 0.5 1 1.5 Aspergillus niger Aspergillus flavus Aspergillus fumigatus Gliomastix sp.1 Myselia sterilia sp.1 Myselia sterilia sp.3 Penicillium sp.2 Penicillium sp.4 Trichoderma sp.2 Paecylomyces sp.2 Paecylomyces sp. 4 Stacybotrys sp.1 Stacybotrys sp.3 Mortiriella sp. Scopuloriopsis sp.1 Cephaliospora sp. Absidia sp. Acremonium sp. Exophiala sp. Penicillium sp.1 Myselia sterilia sp.2 Mortiriella sp. Gliomastix sp.2
Menurut Betts & Darth (1988),
Aspergillus flavus mempunyai kemampuan
dalam mendegradasi lignin. Namun pada hasil uji skrining degradasi lignin (Gambar 4.2), isolat A. flavus tidak dapat mendegradasi lignin. Ini menunjukkan bahwa perbedaan genus, spesies dan strain kapang memberikan pengaruh terhadap kuantitas dan aktivitas enzim yang dihasilkan. Hal tersebut didukung oleh Subowo (2010) yang melaporkan bahwa
Penicillium sp. M3P1 memiliki aktivitas 5,
36% dalam mendegradasi lignin, sedangkan
Penicillium sp. R75 sebesar 17, 56%. Pada
suhu kamar, Penicillium sp. strain R75 memiliki kemampuan mendegradasi lignin lebih tinggi dibanding Penicillium sp. strain M3P1.
Dari penelitian ini terlihat bahwa
Paecilomyces sp., Fusarium sp., dan Chaetomium sp. tidak berpotensi dalam mendegradasi lignin. Tetapi menurut penelitian yang lain, ke-3 spesies tersebut berpotensi sebagai kapang pendegradasi
lignin. Menurut Kluczek et al. (2003)
Paecilomyces inflatus, F. proliferatum
(Regalado et al., 1997), F. oxyporum (Singh,
2006), F. solani (Lozovoya, 2006), dan
Chaetomium globusum (El-Zayat, 2008)
berpotensi dalam mendegradasi lignin.
Pada uji skrining degradasi lignin terdapat 33 isolat kapang yang tidak menghasilkan zona bening, tetapi isolat kapang tersebut mampu tumbuh pada medium selektif lignin. Hal ini dapat dilihat pada, Trichoderma sp.1 (T2.I3) yang memiliki diameter paling besar dari seluruh kapang yaitu 4,7 cm, diikuti oleh A. flavus (T4.3) yang memilki diameter 4,2 cm (Lampiran VI). Melihat pertumbuhan tersebut, maka diduga kedua isolat tersebut membentuk zona bening, namun tidak terlihat atau berada di bawah koloni kapang. Jika kapang tersebut memiliki zona bening yang besarnya sama dengan diameter koloni kapang, maka nilai rasio zona beningnya sama dengan 1. Menurut Purwadaria (2003) dalam penelitiannya mengenai aktivitas selulase pada medium padat, isolat kapang dimungkinkan mampu menghasilkan enzim,
namun aktivitasnya kecil sehingga zona bening tidak terlihat atau berada di bawah koloni kapang.
Kemungkinan lain adalah penggunaan sumber karbon selain lignin oleh isolat kapang, sehingga isolat kapang masih dapat tumbuh dalam medium selektif. Menurut Grainger & Lynch (1984), lignin ekstratif di pasaran disebut dengan Indulin AT. Seperti lignin kraft dan lignin alkali, dalam proses pemurniannya masih terkontaminasi oleh sedikit karbohidrat seperti selulosa dan hemiselulosa. Karbohidrat inilah yang digunakan oleh isolat kapang untuk pertumbuhannya.
Uji Degradasi Lignin
Uji degradasi lignin di medium cair merupakan suatu konfirmasi dari uji skrining degradasi lignin pada medium padat. Gambar 4.4 menunjukkan penurunan lignin dari ke-4 isolat kapang (Gliomastix sp.2, Myselia sterilia sp.2, Penicillium sp.1, dan Mortiriella sp.) yang berpotensi mendegradasi lignin. Uji degradasi lignin diukur berdasarkan nilai absorbansi pada panjang gelombang 232 nm (Agustina, 2007 dan Illa Clarina,2007). Menurut Subowo (2010) besarnya persen penurunan nilai lignin menyatakan seberapa besar kemampuan enzim dalam menguraikan lignin. Lampiran VIII menunjukkan data mentah penurunan lignin oleh isolat kapang yang berpotensi mendegradasi lignin.
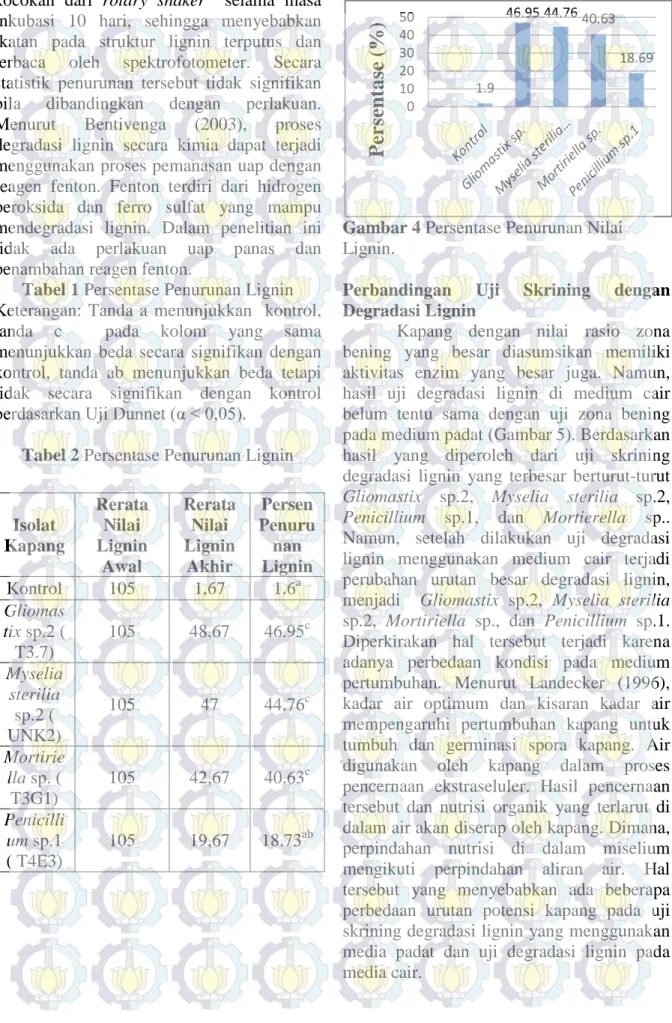
Berdasarkan Gambar 4 terlihat bahwa isolat yang berbeda akan menyebabkan penurunan lignin yang bebeda pula. Walaupun secara statistik perbedaan tersebut tidak signifikan. Secara berurutan, isolat kapang pendegradasi lignin yang tertinggi yaitu Gliomastix sp.2 sebesar 46,95%, kemudian Myselia sterilia sp.2 sebesar 44,76%, diikuti oleh
Mortierella sp. 40,63%, dan Penicillium
sp.1 sebesar 18,73%.
Kontrol merupakan medium LC tanpa diinokulasikan isolat kapang. Pada kontrol terlihat ada angka yang menunjukkan penurunan, sehingga diasumsikan terjadi penurunan lignin karena faktor fisik akibat A
kocokan dari rotary shaker selama masa inkubasi 10 hari, sehingga menyebabkan ikatan pada struktur lignin terputus dan terbaca oleh spektrofotometer. Secara statistik penurunan tersebut tidak signifikan bila dibandingkan dengan perlakuan. Menurut Bentivenga (2003), proses degradasi lignin secara kimia dapat terjadi menggunakan proses pemanasan uap dengan reagen fenton. Fenton terdiri dari hidrogen peroksida dan ferro sulfat yang mampu mendegradasi lignin. Dalam penelitian ini tidak ada perlakuan uap panas dan penambahan reagen fenton.
Tabel 1 Persentase Penurunan Lignin Keterangan: Tanda a menunjukkan kontrol, tanda c pada kolom yang sama menunjukkan beda secara signifikan dengan kontrol, tanda ab menunjukkan beda tetapi tidak secara signifikan dengan kontrol berdasarkan Uji Dunnet (α < 0,05).
Tabel 2 Persentase Penurunan Lignin
Gambar 4 Persentase Penurunan Nilai Lignin.
Perbandingan Uji Skrining dengan Degradasi Lignin
Kapang dengan nilai rasio zona bening yang besar diasumsikan memiliki aktivitas enzim yang besar juga. Namun, hasil uji degradasi lignin di medium cair belum tentu sama dengan uji zona bening pada medium padat (Gambar 5). Berdasarkan hasil yang diperoleh dari uji skrining degradasi lignin yang terbesar berturut-turut
Gliomastix sp.2, Myselia sterilia sp.2, Penicillium sp.1, dan Mortierella sp..
Namun, setelah dilakukan uji degradasi lignin menggunakan medium cair terjadi perubahan urutan besar degradasi lignin, menjadi Gliomastix sp.2, Myselia sterilia sp.2, Mortiriella sp., dan Penicillium sp.1. Diperkirakan hal tersebut terjadi karena adanya perbedaan kondisi pada medium pertumbuhan. Menurut Landecker (1996), kadar air optimum dan kisaran kadar air mempengaruhi pertumbuhan kapang untuk tumbuh dan germinasi spora kapang. Air digunakan oleh kapang dalam proses pencernaan ekstraseluler. Hasil pencernaan tersebut dan nutrisi organik yang terlarut di dalam air akan diserap oleh kapang. Dimana, perpindahan nutrisi di dalam miselium mengikuti perpindahan aliran air. Hal tersebut yang menyebabkan ada beberapa perbedaan urutan potensi kapang pada uji skrining degradasi lignin yang menggunakan media padat dan uji degradasi lignin pada media cair. Isolat Kapang Rerata Nilai Lignin Awal Rerata Nilai Lignin Akhir Persen Penuru nan Lignin Kontrol 105 1,67 1.6a Gliomas tix sp.2 ( T3.7) 105 48,67 46.95c Myselia sterilia sp.2 ( UNK2) 105 47 44.76c Mortirie lla sp. ( T3G1) 105 42,67 40.63c Penicilli um sp.1 ( T4E3) 105 19,67 18.73ab 1.9 46.95 44.76 40.63 18.69 0 10 20 30 40 50
P
er
se
n
ta
se
(
%
)
Gambar 5 Perbandingan Rasio Zona Bening pada Uji Skrining Lignin dengan Penurunan Nilai Lignin pada Uji Degradasi Lignin.
Beberapa spesies Penicillium mampu mendegradasi selulosa dan lignin. Penurunan lignin oleh isolat Penicillium pada penelitian ini sebesar 18, 69% dan menempati urutan ke-4 dari keseluruhan kapang yang diuji. Kemampuannya hampir sama besar dengan
Penicillium sp. R75 sebesar 17, 56% dari
penelitian Subowo (2010).
Myselia sterilia pada penelitian ini
merupakan kapang yang hanya terdiri dari miselium saja dan tidak mengalami sporulasi, sehingga tidak dapat diidentifikasi. Namun berdasarkan uji skrining lignin dan degradasi lignin, Myselia sterilia sp.2 berpotensi dalam mendegradsi lignin. Diduga Myselia sterilia sp.2 adalah jamur kelompok White Rot Fungi yang berpotensi dalam mendegradasi lignin.
Dari ke-2 uji yaitu uji skrining dan degradasi lignin menunjukkan genus Gliomastix, Myselia sterilia, dan Mortierella konsisten mendegradasi lignin walaupun potensi tersebut belum dipublikasikan sebelumnya. Studi terdahulu banyak melaporkan tentang potensi lain dari ke-3 genus tersebut. Gliomastix morarum
diketahui berpotensi dalam mendegradasi selulosa Deacon (2006). Misalnya
Gliomastix gueg dilaporkan mampu
memproduksi enzim uricase. Uricase merupakan enzim yang berguna dalam dunia medis untuk pengobatan dan biokimia klinis sebagai reagen diagnostik untuk pengukuran asam urat dalam darah (Atalla, 2010).
Mortierella sp. diketahui toleran terhadap
logam berat yaitu ZnCl2 (25 ppm) dan NiCl2 (12 ppm) (Iram, 2009).
Pengaruh pH dalam Uji Degradasi Lignin Kondisi lingkungan merupakan salah satu faktor yang mempengaruhi proses degradasi lignin. Menurut Isroi et al (2010) dan Kuncoroadi (2005), pH, aerasi, dan suhu merupakan faktor yang mempengaruhi proses degradasi lignin. Pada penelitian ini faktor lingkungan yang diukur adalah pH.
Isolat kapang pH awal medium pH Medium setelah Dishaker selama 10 hari Kontrol 5 5 Gliomastix sp.2 4 Myselia sterilia sp.2 6 Mortiriella sp. 6 Penicillium sp.1 6
Adanya aktivitas degradasi lignin dapat menyebabkan terjadinya perubahan pH dalam lingkungan medium (Widyastuti, 2007). Tabel 2 menunjukkan perubahan pH selama 10 hari inkubasi. Perubahan pH menurun menjadi 4 dikarenakan akumulasi asam organik (asam vanilat dan asam formik), sedangkan perubahan pH naik menjadi 6 dikarenakan akumulasi produk H2O (Singh, 2006). Disisi lain perubahan pH sangat mempengaruhi kerja enzim ligninase.
Menurut Isroi et al. (2010) dan Singh (2006), Mangan Peroksidase (MnP) dan Lignin Peroksidase ke-2 enzim yang berpotensi dalam mendegradasi lignin. Berdasarkan hal tersebut dapat diketahui bahwa pada medium lignin cair (Medium LC) yang memilki pH 5 merupakan pH yang sesuai yang dibutuhkan kapang untuk mendegradasi lignin. Gliomastix merupakan genus yang konsisten menempati nilai degradasi tertinggi pada uji skrining dan degradasi lignin. Hal tersebut mungkin
1.4 1.2 1.06 1.16 46.9544.7640.63 18.69 0 10 20 30 40 50 Rasio Zona Bening Persentase (%) Penurunan Lignin
ditunjang oleh kisaran pH optimum enzim ligninase 4-5,5 (Tabel 2).
Disamping itu, pH tersebut sesuai untuk pertumbuhan kapang. Menurut Lim (1998), Di laboratorium umumnya kapang akan tumbuh pada kisaran pH yang cukup luas yaitu antara 4,5-8,0 dengan pH optimum antara 5,5-7,5 atau bergantung pada jenis kapangnya. Pengaruh pH terhadap pertumbuhan kapang tidak dapat dinyatakan secara umum karena bergantung pada beberapa faktor, seperti ketersediaan ion logam tertentu, permeabilitas membran sel yang berhubungan dengan permukaan ion, produksi CO2, NH3 dan asam organik. Menurut Widyastuti (2007), pH media berpengaruh terhadap pertumbuhan dan produksi enzim. Pada umumnya kapang tumbuh dan menghasilkan berbagai macam enzim pada kisaran pH asam.
Sistem aerasi pada medium cair mempercepat proses degradasi, dibandingkan dengan kultur media padat. Pemberian aerasi dapat meningkatkan jumlah dan transfer oksigen antara sel dan media, yang optimal untuk enzim oksidatif ekstraseluler pada kapang. Enzim oksidatif ekstraseluler yang optimal dihasilkan oleh kapang dapat meningkatkan aktivitas degradasi.
Pada penelitian ini tidak dilakukan pengukuran suhu sebagai faktor lingkungan yang mempengaruhi proses degradasi. Diketahui bahwa kapang mampu memproduksi enzim ligninase pada suhu yang berbeda dalam memdegradasi lignin. Pada penelitian ini isolat kapang diperkirakan mampu memproduksi enzim ligninase pada kisaran suhu kamar. Xu et al (2001) melaporkan bahwa suhu optimal yang diperlukan oleh P.chrysosporium dalam memproduksi enzim lignin peroxidase dan mangan peroxidase 39oC. Disisi lain suhu optimum pertumbuhan miselium oleh
P.chrysosporium adalah 37oC, sedangkan dalam memproduksi enzim lignin peroxidase pada suhu 30oC (Asther et al., 1988). Aktivitas enzim laccase pada Marasmius
quercophilus pada suhu tinggi yaitu 75oC (Singh, 2006). Menurut El-Zayat (2008), melaporkan bahwa Chaetomium globusum
mampu memproduksi enzim laccase pada suhu 30oC. Menurut Han (2005), Tremetes
versicolor mampu memproduksi enzim
laccase pada suhu 50oC. Menurut Isroi (2010) melaporkan bahwa adanya perbedaan suhu optimum dalam mendegradasi lignin tergantung dari strain dan fisiologi kapang itu sendiri dalam mendegradasi lignin.
DAFTAR PUSTAKA
Dekomposer dalam Proses Dekomposisi Seresah Mangrove. Prosiding
Seminar Biologi FMIPA Universitas Airlangga: Surabaya.
Agustina, I. 2007. Studi Pendahuluan Enzim Lignolitik Jamur Tremetes versicolor.
Tugas Akhir. Kimia FMIPA ITS:
Surabaya.
Akhtar M., R.A. Blanchette and T.K. Kirk. 1997. Fungal Delignification and Biomechanical Pulping of wood.
Advances in Biochemical Engineering Biotechnology.
57:159-195.
Andriyadi, R. D., 2011. Isolasi dan Identifikasi Kapang Tanah dari Kawasan Wonorejo. Tugas Akhir. Institut Teknologi Sepuluh Nopember : Surabaya.
Arisandi, P. 2002. Studi Struktur Komunitas dan Keanekaragaman Mangrove Berdasarkan Tipe Perubahan Garis Pantai di Pantai Utara Jawa Timur.
Tugas Akhir. Biologi FMIPA
Universitas Airlangga: Surabaya. Asther, M., Capdevila, C. and Corrieu, G.
1988. Control of Lignin Peroxidase Production by Phanerochaeta
chrysosporium INA-12 by
Temperature Shifting. Applied and
Environmental Microbiology.
5:3194-3196.
Astin,2007. Kinetika Reaksi Degradasi Lignin Melalui Degradasi
Hemiselulosa Oleh Enzim Xylanase dari Aspergillus niger. Tesis. Teknik Kimia ITS, Surabaya: Hal 1-2.
Atalla, M., Hamed E. M., Farag, M. M., and Ahmed, N. E. 2010. Purification and Characterization of Uricase Enzyme Produced by Gliomastix gueg.
Journal Biotechnology. 2(11): 1-3.
Benson. 1998. Microbiological Applications:
Laboratory Manual in General Microbiology. 7th Edition.
McGraw-Hill.Inc, America: Hal 40-41.
Bentivenga, G., Bonini, C., D’Auria, M., and Bona, A. D. 2003. Degradation of Steam-exploded Lignin from Beech by Using Fenton’s Reagen. Biomass
and Bioenergy. 24: 233-238.
Fadilah, S. Distantina, E. K. Artati, dan A. Jumari. 2008. Biodelignifikasi Batang Jagung dengan Jamur Pelapuk Putih Phanerochaeta
chrysosporium. Ekuilibrium. 7(1):
7-11.
Green, F. and Higley, T.L. 1997. Mecanism of Brown-Rot Decay: Paradigma or Paradox. Biodegradation. 39: 113-124.
Gugnani, H. C. 2003. Ecology and Taxonomy of Pathogenic Aspergilli.
Frontiers in Bioscience. 8 : 346-357.
Hattaka, A. 1994. Modifying Enzymes from Selected White-Rot Fungi: Production and Role in Lignin Degradation. Microbiology. 13: 125-135.
Han, M. J., H. T. Choi, and H. Song. 2005. Purification and Aharacterization of Laccase from the White Rot Fungus
Tremetes versicolor. Journal Microbiology. 43(6): 555-560
Iram, S., I. ahmad, and D. Stuben. 2009. Analysis of Mines and
Contaminated agricultural Soil Samples for Fungal Diversity and Tolerance to Heavy Metals.
Journal Botany. 41(2): 885-895.
Isroi, Millati R., Syamsiah S., Niklasson C., Cahyanto M. N., Lundquist K., and Taherzadeh M. J. 2010. Biological Pretreatment of Lignocelluloses with White Rot Fungi and It,s Applications. Review. 6(4):1-36
Kluczek, B., Toumela M., Hattaka A., and Hofricter M. 2003. Lignin Degradation in a compost environtment by the deuteromycete
Paecilomyces inflatus. Journal Microbiology Biotechnol. 61:
374-379.
Kuncoroadi, D. 2005. Kemampuan Isolat
Jamur Kayu Famili Fomitopsidaceae,
Ganodermataceae, dan Hymenochaetaceae Dari Kebun
Raya Purwodadi Dalam Mendegradasi Pewarna Azo Dan Anthraquinone. Tugas Akhir.
Institut Teknologi Sepuluh Nopember : Surabaya.
Kuswytasari, N. D., Shovitri, M., and andriyadi, R. D. 2011. Soil Molds Diversity in The Coastal Wonorejo Surabaya. Proceeding International
Conference on mathematics and Science (ICOMS): Surabaya.
Landecker, 1996. Fundamental Of The
Fungi. Prentice Hall. New Jersey:
470-476.
Lim, D. 1998. Microbiology. McGraw Hill Publishing Company. New York. Lozovoya V.V., A.V. Lygin, O. V. Zernova,
S. Li, J.M. Widholm. 2006. Lignin Degradation by Fusarium solani f. sp. Glycines. Plant Disease. 9(1): 77-82.
Marginingrum, D. dan N. Karningsih. 2001. Studi Degradasi Lignin ekstraktif Menggunakan Bakteri Serratia
marcescens dengan Menggunakan
Metode Reaktor Batch. Prosiding
Seminar Nasional Kimia Pusat Penelitian Geoteknologi LIPI.
Surakarta: 149-157.
Munir, E. 2006. Pemanfaatan Mikroba
dalam Bioremediasi: Suatu Teknologi Alternatif untuk Pelestarian Lingkungan. Pidato
Pengukuhan Guru Besar Tetap dalam Bidang Mikrobiologi FMIPA USU, Sumatera Utara: Hal 5
Nybakken, W.J. 1992. Biologi laut Suatu
Pendekatan Ekologis. Gramedia
Pustaka Utama, Jakarta: Hal 301. 327.
Okafor, N. .2007. Modern Industrial
Microbiology and Bitechnology.
Science Publishers: USA. Hal 95 Orth, A.B., D.J. Royse, and M. Tien. 1993.
Ubiquity of Lignin Peroxidase among Various Wood-Degrading Fungi. Journal Applied and Environmental Microbiology. 59
(12) : 4017-4023.
Pelczar dan Chan. 2004. Dasar-Dasar
Mikrobiologi. UI-Press: Jakarta. Hal
193-196
Pointing S.B. 1999. Qualitative Methods for The Determination of Lignocellulotik Enzyme Production by Tropical Fungi. Juornal Fungal Diversity. 2: 17-33.
Purwadaria, T., P. A. Marbun, A. P. Sinarat, dan P. P. Ketaren. 2003. Perbandingan Aktivitas Enzim Selulase dari Bakteri dan kapang
Hasil Isolasi dari Rayap. Jurnal LIPI. 8 (4): 213-219.
Purwati. 2009. Profil Protein Mikroorganisme Rhizosfer marina dan Pluchea indica di Wonorejo Surabaya. Tugas Akhir. Biologi ITS: Surabaya. Hal 3.
Redriguez, A., Falcon, M.A., Carnicero, A., Perestelo, F., Fuente G. D., Trojanowski, J. 1996. Laccase Activities of Penicillium
chrysogenum in Relation to Lignin
Degradation. Microbiology Biotechnology. 45: 399-403.
Regalado V., Rodrigeuz A., Perestelo A., Carnicero A., Fuente G. D. and Falcon M. A. 1997. Lignin Degradation and Modification by the Soil-Inhabiting Fungus Fusarium
proliferatum. Journal Applied and Environmental Microbiology. 63 (9):
3716-3718
Samsuri M., B. Prasetya, E. Hermiati. 2004. Biodegradasi Bagasse oleh Jamur Pelapuk Putih (White Rot Fungi) dan Potensi Pemanfaatannya untuk Etanol. Kimia Dalam Industri dan Lingkungan. Prosiding Nasional Indonesia XIII: Yogyakarta. Hal
405-410.
Saraswati. 2000. Organisme Perombak
Bahan Organik.
http://balittanah.litbang.deptan.go.id/ dokumentasi/buku/pupuk/pupuk10.pd f. Diakses pada 5 Mei 2011. Hal 216. Schlegel, H. .1994. Mikrobiologi Umum. Edisi Keenam, Alih bahasa. Gadjah Mada University Press: Yogyakarta. Hal 484-487.
Siagian, R.M., H. Roliadi, S.Suprapti, dan S. Komarayati. 2003. Studi Peranan Fungi Pelapuk Putih Dalam Proses Biodelignifikasi Kayu Sengon
(Paraserianthes Falcataria (L) Nielsen). Jurnal Ilmu dan kayu
Tropis. 1(1) : 47-56.
Singh, H. 2006. Mycoremidiation. John Wiley & Sons, Inc: America. Hal 358-375.
Sintawardani, N & J. Triastuti. Penggunaan kapang Aspergillus awamori untuk Pengolahan Lindi Hitam. Telaah
Seminar Nasional Mikrobiologi Lingkungan 11 Bogor-LIPI. Jilid
XVIII No. 2: 25-31.
Subowo, Y. B. 2010. Uji Aktivitas Selulase dan Ligninase dari Beberapa Jamur dan Potensinya sebagai Pendukung Pertumbuhan Tanaman Terong (Solanum melongena). Berita Biologi
LIPI Mikrobiologi. Cibinong. 10(1):
1-6.
Sulistinah, N. 2008. Potensi Melanotus sp. dalam Mendegradasi Lignin. Jurnal
Biologi Umum. XII (1): 6-8.
Thorn, R. G., C. A. Reddy, D. Harris, E. A. Paul. 1996. Isolation of Saprophytic Basidiomycetes from Soil. Journal
Applied and Environmental Microbiology. 62 (11): 4288-4292.
Waluyo, Lud. 2006. Teknik dan Metode
Dasar Mikrobiologi. Universitas
Muhamadiyah Malang Press: Malang. Hal 264-265.
Whidyastuti, N. 2007. Produksi Kitinase Ekstraseluler Aspergillus rugulosus 501 secara optimal pada media cair.
Berita Biologi LIPI Mikrobiologi:
Cibinong. 8(6): 547-553
Wilkolazka A.J., K. R. Janina, M. Elzbieta, and W. Wladyslaw. 2002. Fungi and Their Ability to Decolourize Azo and Anthraquinonic Dyes. Journal Enzym
and Microbial Technology. 30:
566-572.
Xu, F., Chen, H. and Li, Z. 2001. Solid-State Production of Lignin Peroxidase (LiP) and Mangan Peroxidase (MnP) by Phanerochaeta chrysosporium using steam-exploded straw as substrate. Bioresource Technology. 80: 149-151.
Yang JinShui, HongLi Yuan, HeXiang Wang, and WenXin Chen. 2005. Purification and Characterization of Lignin Peroxidases fro Penicillium
decumbens P6. Journal of
Microbiology and Botechnology. 21:
435-440.
Zeng, G. M., Yanyu, H., Huang, H. L., Huang, D. L., Cheng, Y. N., Huang, G. H., and Li, J.B. 2006. Laccase activities of a soil Fungus Penicillium
simplicissimum in Relation to Lignin
Degradation. World Journal of Microbiology & Biotechnology. 22: