PERBANDINGAN
MODEL
ISOTERM
BIOSORPSI
Cd
TERLARUT
DALAM
AIR
DENGAN
BIOSORBENT
ASPERGILLUS
NIGER
Adrian
Nur11,
Supranto21,
danRochmadi21
') Jurusan Teknik Kimia Fakultas Teknik UNS
JI. Ir.
Sutami
No. 36A SurakartaTelp. (0271)
6321122>Jurusan
Teknik Kimia Fakultas Teknik UGMJI. Grafika No. 2
Kampus
UGMJogjakarta
Abstract: Due to the
increasing
awareness of the deleteriousecological
effects of toxic Cd, theadsorption
of Cd from aqueous solutionsby
Aspergillus
niger
biomass was studied. The aim of thiswork was to find the exact
adsorption
isotherm model topredict
thesingle system adsorption
by
the
Aspergilfus
niger
biomass.The batch
sorption
experiments
were carried out in 50 ml conical flasks.Weighed
amounts(8,5
to57,
2mg)
ofAspergillus niger
biomass were introduced into a number of conicalflasks,
to which25 ml of Cd solutions of
increasing
concentrations from20,28
to24,435
mg/L
were added. Theamount of Cd accumulated on biomass was calculated as the difference between the amount
present
in control
experiments
and thatremaining
in solution afterequilibrium
with biomass.Four
adsorption
isotherm models,namely
Freundlich Isotherm Model,Langmuir
Isotherm
Model,
Sips
IsothermModel,
dan Toth IsothermModel,
were fitted to theexperimental
data.The Toth Isotherm Model and The
Sips
IsothermModel·
weresuperior,
whichprovided
the least average relative error(6,035
% and6,013
%).
The maximumsorption
was seen atpH
6. ltis 143.093mglg
sorbent.Keywords:
biosorption,
isothermmodels,
Cadmium PendahuluanPenggunaan
logam
berat Cd terusmeningkat
walaupun
logam
berat tersebuttermasuk dalam
prioritas
yangtinggi
untuksegera
ditanggulangi
[1].
Logam
berat Cd tidakdapat
dihancurkan olehmikroorganisme,
danjika
terakumulasi secara berlebihan dalamtubuh manusia
dapat
mengakibatkan
tekanan darahtinggi
dan kerusakanginjal.
Studi kasuspada sungai
DonanCilacap
yang diteliti oleh PT BinaKarya
cabang
Semarang
pada
bulanApril
1999sampai
Maret2000,
memperlihatkan
bahwapada
bulan-bulan tertentu, kadarlogam
Cd di atasambang
batasyang
ditetapkan
olehpemerintah
[2].
T
eknologi
pengambilan
logam
berat telahuanyak berkembang,
seperti
presipitasi,
pertukaran
ion,
osmosisbatik,
danbiosorpsi
[1].
Teknologi
presipitasi
dijalankan
dengan
cara yang sederhana danmudah,
namunteknologi
ini tidakbanyak
berhasil untukkonsentrasi yang reridah.
Teknologi
pertukaran
iondapat bekerja
pada
konsentrasirendah,
namunteknologi
ini membutuhkanbiaya
operasi
yangcukup
tinggi.
Biaya
operasi
akan semakin
tinggi
biladigunakan
teknotogi
osmosis balik.Salah satu
teknologi
altematif adalahteknologi penjerapan
dengan
biosorpsi.
PadaEkuilibrium, Vol
1,
No1,
2002: 16- 21konsentrasi yang
rendah,
kapasitas
pemungutan
danpenjerapan
logam
dengan
biomassatetap
baik. Selainitu,
bahanpenjerap
(biosorben)
yangberupa
biomassaini
banyak
tersedia di alam(seperti
ganggangdan
mikroba)
dandapat
diperoleh
dari limbahpertanian
dan industrifermentasi,
yang akandapat
menekanbiaya
operasi.
Pada
penelitian
terdahulu,sejumlah
logam
beratdapat
dijerap
dengan
baik olehbiomassa
[3)[41[5]. Aspergillus
niger
sendirisebagai
biosorben terbukti mampumenjerap
uranium dan thorium sertamenjerap
Zn[6][7].
Tujuan
penelitian
ini adalah untukmemperoleh
model isoterm yangtepat
untukmemprediksikan
kemampuanpenjerapan
Aspergillus
niget terhadap
logam
berat Cd.DasarTeori
Tsezos dan
Volesky
mempostulatkan
beberapa mekanisme
penjerapan
logam
berat oleh biomassa,yaitu
:1. Pembentukan senyawa
kompleks
pada
chitinPembentukan senyawa
kompleks
terjadi
antara ionlogam
terlarutdengan
chitinpada dinding
sel. Jumlah gugus aminoyang
dibawa oleh chitin menentukankemampuan
pengambilan
ionlogam. Gugus
amino tersebut16
(2)
Selain Model Jsoterm
Sips, dapat
juga
digunakan
Model lsotermToth,
dengan
asumsi yang sama,yaitu
asumsipenjerapan
terjadi
melalui proses kimiadengan
tingkat
energi
yang
heterogen
[11].
Model lsoterm Tothjuga
merupakan
modelempiris.
Persamaannya
adalah :(3)
(4)
1qmaksksCm
Q=
(1+ksC?
J
q =qmaks
krC
1(1
+(k
Tc)'
}t
Metode dan Peralatan Penelitian
Biomassa
kering
A.niger diperoleh
dari hasilpembiakan
kultur A.niger
yangdidapat
dari Lab.
Mikrobiologi
PG,
PAU-UGMdengan
mediayeast
ekstrak L21(OXOtD),
pepton
L44(OXOID)
dan Glukosa/Dektrosa(OXOID) [12].
Kultur A.niger
ditanamkanpada
50 ml starter YEP(yeast
eksltc1k ?ogFL
Lianpepton
20g/L)
dan ditambahkan 3 mlglukosa
40 %. YEP danglukosa
sebelumnya
disterilkanpada
autoklaf suhu 121°C
selama 15 menit. Penanaman dilakukanpada
ruang inokulasi yangsebelumnya
disteriikandengan
UV selama 15 menit dandisemprotkan
alkohol 95 %. Kawat yangdigunakan
disterilkandengan
mencelupkan
pada
alkohol 95 % dan dibakarpada
nyala
lampu
spritus.
Media yang telahditanami,
diinkubasipada
inkubator shakerdengan
kecepatan
175 rpm 28°C
selama 24jam.
Sel yang tumbuh ditandaidengan
butirmiselia
seperti
manik-manik berwarnaputih
coklat. Mediadengan
volum yang lebih besar dibuatdengan
menambahkan 1 O ml starter dan 10 mlglukosa
steril 40 %pada
250 ml media YEPsteril,
pada
ruang inokulasiseperti
pada
pembuatan
starter. Media yang telah ditanamidengan
stater,
diinkubasikan dalam inkubator shakerpada
175 rpm 28°C
selama24
jam.
Biomassa sel yangdiperoleh
dimasukkan
pada
autoclat 121"C
selama 15 menit dandipisahkan
darimedianya
dengan
sentrifuge
3500 rpm selama 25 menit dan dicucidengan
aquades
2 kali.Selanjutnya
biomassadikeringkan
dalam freezedryer
selama 2 X 24jam.
Biornassa dikontakkandengan
larutan. Cddengan
konsentrasitertentu selama waktu
kesetimbangan.
Persamaannya
adalah :mempunyai
sepasang elektron yangdapat
digunakan
untuk berikatan koordinasi kovalen danmempunyai
sifatsebagai
basa Lewis yangkuat,
sehingga
dapat
bereaksidengan
ionlogam.
2.
Adsorpsi logam pada jaringan
chitin.
Senyawa
kompleks
chitin-logam
yangterjadi
pada
proses pertama, membentuk suatu sifatsebagai
tempat
inti{nucleation
site)
yangdapat
menyimpan
logam.
Akibatnya,
semakinbanyak
senyawakompleks
chitin-logam terbentuk,
semakin besarpula
logam
yang
dapat
terjerap.
Selain itudinding
seljuga
mempunyai
struktur yang porous yangdapat
bersifatsebagai
adsorben.3.
Presipitasi logam pada dinding
setSenyawa
kompleks
chitin-logam
.dapat
terhidrolisa yang
menghasilkan
presipitasi
logam
pada
dinding
sel. Chitin yang bebas akan berikatan kembalidengan
logam
y'aiig baru[8].
Jika
langkah
kedua danketiga
dariproses di atas
merupakan
langkah
yang dominan dalampenjerapan,
maka model yangdapat
digunakan
adalah model lsoterm Freundlich. Model lsotermFreundlich
merupakan
persamaanempirik
dengan
asumsipenjerapan
secara fisis[9][10). Penjerapan
terjadi
pada
dinding
sel(mikropresipitasi)
dengan
tingkat
energi
yang berbeda.Persamaannya
adalah :?
(1)
q=kFC·"
Jika
langkah
pertama
yangmendominasi proses
penjerapan,
makadapat
digunakan
Model lsotermLangmuir,
Sips
danToth. Model lsoterm
Langmuir
menggunakan
pendekatan
kinetika,
yaitu
kesetimbangan
terjadi jika kecepatan
adsorpsi
samadengan
desorpsi.
Asumsi yangdipakai
adalahpenjerapan
terjadi
secara kimia(langkah
pertama)
dengan
tingkat energi pada
seluruhpermukaan
homogen
sehingga
afinitas molekulterjerap
sama untuksetiap
lokasi[9)[10}.
Logam
yangterjerap
membentuklapisan
tunggal
(mono/ayer)
dan tidak ada interaksi antarmolekul terjerap.
Persamaannya
adalah :qmaksbC
q
=(1+bC)
Untuk model
penjerapan
secara kirniadengan
tingkat
energi
yangheterogen,
digunakan
Model lsoterm
Sips
yangmerupakan
persamaan
empirik
[9].
Penjerapan
terjadi
rneialuipernbentukkan
senyawakompleks
chitin-logam
berat.Perbandingan
model lsotermBiosorpsi
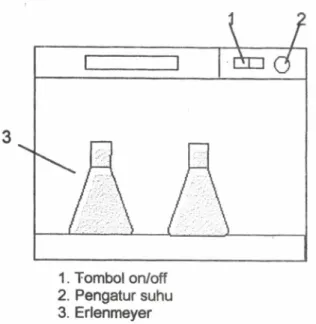
Cd terlarut dalam airGambar 1. Rangkaian alat :shaker bath
1. Tombol on/off 2.
Pengatur
suhu 3.Erlenmeyer
Konsentrasi akhir larutan dianalisa. Susunan
alat terlihat
pada gambar
1.Untuk menentukan waktu
kesetimbangan
dilakukandengan
cara biomassa mati 10 mg ditambahkanpada
25 ml larutanlogam
dengan
konsentrasi awal 50 ppm danpH
6. Larutan dianalisapada
waktu-waktu tertentusampai
diperoleh
waktukesetimbangan.
Untuk
mengetahui
pengaruh
pH,
larutan
dengan
volum 25 ml dan konsentrasi bervariasi antara8,5
sampai
57,2
mg/L
dengan
pH 4, 6, dan 8ditempatkan
pada
erlenmeyer
50 ml. Larutan ditambahkan biomassakering dengan
berat yang bervariasi antara20,28
sampai
24,435
mg. Data-data tersebutdigunakan
untukmenguji
modelkesetimbangan
tunggal
dengan
penyelesaian
persamaan-persamaan
(1) sampai (
4).
'
Pengaruh
pH
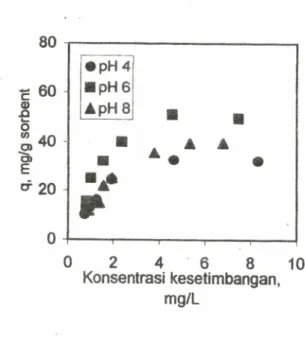
larutanGambar 3
memperlihatkan
bahwapH
6merupakan
pH
yangpaling
optimal
dibandingkan
pada pH
4 danpH
8. Penurunan!ogam
terjerap
dengan
penurunanpH
6sampai
pH
4 disebabkan oleh chitin yangmerupakan
bagian
utama dalampembentukan
chitin-logam,
terhidrolisadengan
penurunanpH [7].
Lebih dari 90 % dari total
penjerapan
berlangsung
pada
1jam
pertamanya.
Hasilpenelitian
ini lebih baikdaripada
penjerapan
Zndengan
biosorben yang sama yangmenjerap
80 % dari totalpenjerapan
dalam 1jam
[7].
Gamber 2menampilkan
hasilpercobaan
waktukesetimbangan,
yangmemperlihatkan
bahwakecepatan
biosorpsi
logam
berat Cd oleh A.niger
terbagi menjadi
phase
penjerapan
cepat
danphase
penjerapan
lambat. Phasepenjerapan
cepat
yaitu
pada
1jam
pertama danphase
penjerapan
lambat setelah 1jam
tersebut.Kecepatan
biosorpsi
mencapai
jenuh pada
8jam
kemudian.Kecepatan
biosorpsi
yangtinggi
pada
disebabkan oleh ukuran sel biomassa yang relatif kecilsehingga
permukaan
bidang
sentuhcukup
luas.Kemungkinan
terjadinya
interaksi antara ionlogam
dengan
pusat
aktifdinding
sel masihsangat
besar. Penambahanlogam
yangterjerap
menjadi
semakinlambat,
pada
keadaan
hampir
seluruhpusat
dinding
seltelah
jenuh.
Keadaan ini yangterjadi
pada
phase
kedua. Jumlah Cd yangterjerap
mengalami
penurunan setelah 44jam
dikontakkandengan
adsorben. Penurunan ini disebabkan sifat biosorben yangkompleks
danlemahnya
ikatan yangterjadi,
sehingga
logam
yang telah
terjerap
terlepas
kembali. Sebablain penurunan
logam
yangterjerap
adalahproses
biodegradasi
biosorben yangmenurunkan
kemampuan
adsorben untukmengikat
logam.
u 40 10 20 30Waktu,jam
40 -r---, 3555
30?
25?20
-?15
a 10 5 0 --???????????? 0H3sit Penelitian dan Diskusi Waktu
Kesetimbangan
3
Gambar2 Hasil percobaan waktu kesetimbangan
80
epH4
c 60•pH6
Q)&pH8
• .0 • ... 0 u, 40 • • • 0)••
O> • • E.,,
cf 20aa
0 0 2 4 6 8 10 Konsentrasikesetimbangan,
mg/L
Gambar 3. BiosorpiCd Berbagai pH
Logam
terjerap
menurundengan
kenaikan
pH
6sampai
pH
8. Adsorbat dalam hal ini ionlogam
berat Cd telah terhidrolisa dan mulaiterpresipitasi.
Cddengan
pH
di atas7 muncul dalam bentuk
Cd(OHt
danCd(OH)l
sertaterpresipitasi
sebagai
Cd(OH)2
[13].
Keadaan inimenghambat
prosesadsorpsi.
Hasil
penelitian
ini sesuaidengan
penelitian
sebelumnya
yaitu
penjerapan
Zndengan
biomassa A.niger
yangjuga
menunjukkan
pH optimal terjadi pada pH
6[7].
ModelKesetimbangan
Tabel 1
memperlihatkan
hasilperhitungan
modelkesetimbangan.
Secara umum modelSips,
danToth,
lebih baikdaripada
modelFreundlich dan
Langmuir.
Jikamembandingkan
modelSips
dan Tothdengan
modelFreundlich,
makadapat
diambilkesimpulan
bahwapenjerapan
biosorpsi
lebih dominanterjadi
secarakimia,
sesuaidengan
asumsi dalam penyusunan modelSips
dan Toth. Hasil tersebutmenyimpulkan
bahwamekanisme
biosorpsi
didominasi olehpembentukan
senyawakompleks
secarakimia. Pembentukan senyawa
kompleks terjadi
antara ion
logam
terlarutdengan
chitinpada
dinding
sel. Jumlah gugus amino yang dibawa chitin menentukankemampuan
pengambilan
ionlogam.
Gugus
amino tersebutmempunyai
sepasang elektron yang
dapat
berikatankovalen dan
mempunyai
sifatsebagai
basaLewis yang
kuat,
sehingga
dapat
bereaksidengan
ionlogam.
Tabel 1. Konstanta dan Ralat
Berbagai
Model lsoterm•soterm
Kon st.pH4
pH6
pH8
kF
13.938 19.869 14.029 Freund- n 2.080 1.729 1.609 lich Ralat(%)
12.883 21.466 12.491 Ralat rerata(%)
15.613 Qmaks 52.502 143.093 90.836 b 0.342 0.147 0.163Lang-
Ralat 6.837 19.733 10.410 muir(%)
Ralat rerata(%)
12.327 Qmaks 33.984 51.757 42.803ks
0.671 0.673 0.372 m 0.521 0.466 0.508Sips
Ralat 4.726 7.676(%)
5.704 Ralat rerata(%)
6.03! qmaks 32.443 50.831 40.364kT
0.406 0.409 0.320 Toth t 5.955 3.826 3.815 Ralat 2.066 10.466 5.508(%)
Ralat rerata(%)
6.013Jika
membandingkan
modelSips
danToth
dengan
modelLangmuir,
dapat
diambilkesimpulan
bahwabiosorpsi
mempunyai
tingkat
energi
yangheterogen,
sesuaidengan
asumsi model
Sips
dan Toth.Hasil
pemodelan
dapat
dilihatpada
gambar
4 dan 5. ·Perbandingan
model lsotermBiosorpsi
Cd terlarut dalam airdengan
biosorbentAspergillus
Niger(Adrian
Nur)
•
3.
Kapasitas
maksimumpenjetapan
jika
dihitung dengan
lsotermLangmuir
adalah143,093
mg/g
sorbent.4. Model
kesetimbangan
Sips
dan Tothpaling
sesuai untukmemprediksikan
proses
biosorpsi
sistemtunggal,
dengan
ralat rata-rata
masing-masing
6,035
% dan6,013%
5. Proses
biosorpsi
Cd oleh A.niger
terjadi
·
secara kimia
dengan
tingkat
energi
yangheterogen.
Ucapan
Terima KasihPenulis
mengucapkan
terima kasihkepada
Bapak
Ir.Wahyudi
BudiSediawan,
SU.,
Ph.D.,
danBapak
Ir.Surya
Purwono,
MA.Sc.,
Ph. D., atas saran-sarannya. Penulisjuga
mengucapkan
terima kasihkepada
seluruhpihak
yang telah membantupenelitian
10 • pH4 • pH6 A pH8 --Model Sips pH4 --Model Sips pH6 --Model Sips pH8 4 6 8C, mg/L
BiosorpsiCd dengan Model lsoterm Sips ini.
70 60
_so
C G>?40
en 0) a Jo Ec-20
10 0 0 2 Gambar4. • 70 60 -50 C140
c,,"o,30
E er 20 10 0 0 2 • pH4 • pH6 A pH8 -- Model Toth pH4 --ModelToth pH6 -- Model Toth pH8 4 6 8C,mg/L
10 Daftar Notasib konstanta isoterm
Langmuir,
Umg
C konsentrasi
kesetimbangan
Znpada
larutan,
mg/L
CN chitin
kF
konstanta isotermFreundlich,
(mg/g)(Umg)"
ks
konstanta isotermSips,
(Umgr
kT
konstanta isotermToth,
(Umg)1
m konstanta isotermSips
n konstanta isoterm Freundlich
q
kapasitas
penjerapan
Cdpada
konsentrasi
tertentu,
mg/g
sorben qmakskapasitas
penjerapan
maksi-mum Cdmono/ayer,
mg/g
sorbenkonstanta isoterm Toth Daftar Pustaka
[1] Volesky,
8.,
"Biosorption
for the NextCentury", http
://www.mcgill.ca/
biosorption,
1999Berdasarkan hasil
penelitian
inidapat
ditarik
kesimpulan sebagai
berikut :1. Waktu
kesetimbangan
biosorpsi
Cd oleh A.niger tercapai
dalam waktukurang
lebih 8jam, dengan
prosesberlangsung
cepat
yiatu
90 % totalpenjerapan
terjadi pada
1jam pertamanya.
2. Keasaman larutan untuk
penjerapan
maksimaltercapai
pada pH
6Gambar 5.
Kesimpulan
BiosorpsiCd dengan Model lsoterm Toth
[2]
PT BinaKarya cabang
Semarang,
"Laporan
AkhirPengukuran
KualitasLingkungan
Pertamina UnitPengolahan
IVCilacap·,
Semarang,
2000,
hal lll-1?111-33[3]
Gadd,
G.M., "Biosorption",
Chemistry
andIndustry,
13, 1990,
hal 421-426.[4] Prasetya,
I.,
"Pengambilan
IonLogam
Berat dari Larutan secaraBiosorpsi",
MediaTeknik,
2 &
3, 14, 1992,
hal 98-101[5]
Mawardi,
Sugiharto,
E.,
Mudjiran,
H.,
danPrijambada,
1.0.,
"Biosorpsi
Timbal oleh•
Biomassa