4
II. TINJAUAN PUSTAKA
A. Minyak Ikan
Minyak ikan adalah minyak yang diperoleh dari jaringan-jaringan tubuh ikan. Minyak ikan dianjurkan untuk diet kesehatan karena banyak mengandung omega-3 asam eikosapentanoat (EPA) dan asam dokosaheksanoat (DHA) yang dapat mengurangi masalah peradangan pada tubuh. Omega-3 sebenarnya tidak diproduksi oleh tubuh ikan itu sendiri, tetapi merupakan akumulasi dari konsumsi mikroalga yang memproduksi asam lemak (Wikipedia, the free encyclopedia, 2008).
Komposisi minyak ikan utamanya mengandung trigliserida dari tiga buah asam lemak (gliserol yang dikombinasi dengan molekul asam yang sama atau berbeda) dengan fosfolipid, gliserol eter dan ester wax. Karakteristik minyak adalah bahwa mereka mengandung berbagai asam lemak rantai panjang dengan jumlah atom karbon yang berkisar antara 14 sampai 22, dan tingkat ketidakjenuhan yang berkisar antara satu sampai enam buah ikatan rangkap per molekul (Fisheries and Aquaculture Department, 1986).
Kandungan minyak dan komposisi asam lemak berbeda pada tiap jenis ikan. Bahkan perbedaan juga ditemukan pada ikan yang sejenis dengan faktor yang mempengaruhi adalah pola makan, temperatur, pengaruh musim, usia dan jenis kelamin. Komposisi asam lemak sangat dibutuhkan oleh para ahli gizi untuk membuat formulasi nilai gizi, pelabelan nutrisi, pemrosesan dan pengembangan produk (Üstün, 1996). Adapun perbandingan komposisi asam lemak omega-3 dapat dilihat pada Tabel 1 di bawah ini.
Tabel 1. Tabel perbandingan komposisi omega-3 pada beberapa sumber minyak/lemak Sumber lemak/minyak a Komposisi omega-3 (%) Ikan 13-15 Linseed 26-58 Kedelai 2-10 Rapeseed 1-10 a Jenkins (2008)
5 B. Asam Lemak Omega-3
Asam lemak omega-3 merupakan kelompok asam lemak tak jenuh yang memiliki ikatan rangkap pada posisi n-3, yaitu pada rantai nomor tiga terhitung dari ujung metil dari asam lemak. Asam lemak omega-3 yang esensial untuk manusia adalah α asam linolenat (18:3, n−3; ALA), asam eikosapentanoat (20:5, n−3; EPA) dan asam dokosaheksanoat (22:6, n−3; DHA) (Wikipedia, the free encyclopedia, 2008).
Asam lemak omega-3 adalah asam lemak yang memiliki posisi ikatan rangkap pertama pada rantai karbon nomor tiga dari ujung gugus metilnya. Asam-asam lemak alami yang termasuk kelompok asam lemak omega-3 adalah asam linolenat (C18:3), asam eikosapentanoat (C20:5) atau EPA dan asam dokosaheksanoat (C22:6) atau DHA, sedangkan yang termasuk kelompok asam lemak omega-6 adalah asam linoleat (C18:2) dan asam arakidonat (C20:4). Rumus molekul dari asam lemak omega-3 yang banyak terdapat dalam minyak ikan tertera pada Gambar 1.
CH3-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH-(CH2)7 Asam Linolenat (C18:3)
-COOH
CH3-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH-CH2-CH=
CH-(CH2)3
Asam Eikosa Pentanoat(C20:5)
-COOH
CH3-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH-CH2
-CH=CH-CH2-CH=CH-(CH2)2
Asam Dokosa Heksanoat (C22:6)
-COOH
Gambar 1. Rumus molekul dari asam lemak omega-3 (Ackman, 1982)
Asam lemak omega-3 sangat penting untuk membantu fungsi kerja otak, terutama untuk proses pertumbuhan dan perkembangan otak. Asam lemak esensial ini banyak terakumulasi di dalam otak terutama penting untuk fungsi kognitif otak dan mengatur perilaku manusia. Kekurangan asam lemak omega-3 dalam tubuh manusia dapat menyebabkan kelelahan, daya ingat lemah, kulit kering, gangguan hati, depresi dan sirkulasi yang tidak teratur (DeBusk, 2007).
6 Asam lemak omega-3 yang terpendek (asam linolenat) ditemukan di dalam tumbuhan dan minyak tumbuhan, termasuk sayuran, walnut, minyak biji mustard, minyak kedelai, minyak jagung dan minyak flaxseed (terdiri atas 50% asam linolenat). Asam lemak omega-3 yang lebih panjang, asam eikosapentanoat (EPA) dan asam dokosaheksanoat (DHA) ditemukan di dalam alga yang dimakan oleh ikan dan ikan paus herbivora. Manusia memperoleh asam lemak ini dari mengonsumsi ikan (misalnya salmon) (Jenkins, 2008). Beberapa jenis asam lemak omega-3 dan omega-6 yang terletak di dalam makanan dapat dilihat pada Tabel 2.
Tabel 2. Beberapa jenis asam lemak omega-3 dan omega-6 dalam makananb Asam Lemak Tipe Singkatan Sumber Terbesar dalam
Makanan α-linolenat N-3 ALA Flax, kanola, minyak ikan eikosapentanoat N-3 EPA Minyak ikan
dokosaheksanoat N-3 DHA Minyak ikan
linoleat N-6 LA Minyak kedelai, safflower, bunga matahari, minyak jagung
arakidonat N-6 AA Sisa-sisa daging, ikan, unggas
b
Addis (2000)
Seto et al., (1984) mengemukakan bahwa produsen utama asam lemak omega-3 sebenarnya bukan ikan, melainkan mikroorganisme laut yang menjadi makanannya antara lain Chlorella, Diatomea, dan Dinoflagellata yang merupakan fitoplankton. Mikroorganisme tersebut di samping mensintesis asam lemak omega-3 juga dapat mensintesa asam lemak omega-6. Sintesa asam lemak ini sangat efisien karena mikroorganisme tadi mempunyai siklus rantai makanan yang pendek. Tetapi sebenarnya sintesis asam lemak omega-3 tidak hanya dilakukan oleh fitoplankton tersebut, melainkan juga oleh bakteri, kapang, algae, dan fitoplankton lain yang mempunyai tingkat efisiensi sintesis yang berbeda.
Kadar asam lemak omega-3 pada beberapa jenis ikan per 100 gram daging dapat dilihat pada Tabel 3.
7 Tabel 3. Kadar omega-3 pada beberapa jenis ikan per 100 gram daging ikanc
Jenis ikan Kadar lemak (gram) Asam arakidonat (g) EPA (gram) DHA (gram) Tuna 6,80 0,14 0,63 1,70 Herring 6,20 0,03 0,33 0,58 Mackerel 9,80 0,12 0,85 1,10 Salmon 13,20 0,06 1,00 0,72 Cod 0,73 0,02 0,08 0,15 Sarden 10,20 0,22 1,70 0,64 c
Barlow dan Stansby (1982)
C. Hidrolisis
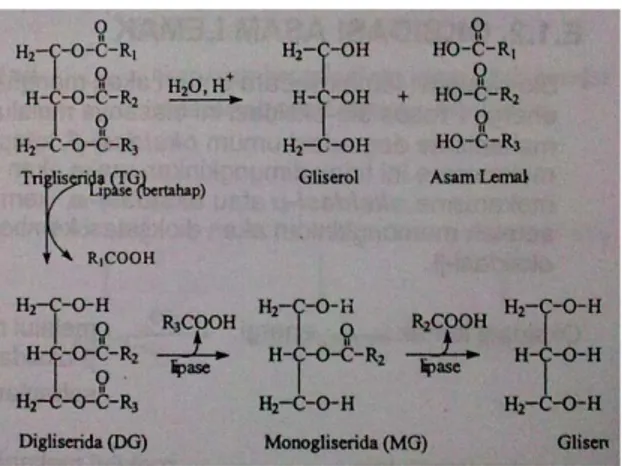
Hidrolisis merupakan reaksi kimia yang melibatkan molekul air di mana molekul tersebut terpecah menjadi ion hidrogen dan hidroksida yang kemudian akan bereaksi lebih lanjut. (Wikipedia, the free encyclopedia, 2009a). Dalam reaksi hidrolisis, lemak atau minyak akan diubah menjadi asam-asam lemak bebas dan gliserol (Herlina, 2002). Mekanisme reaksi hidrolisis trigliserida dengan bantuan lipase dapat dilihat pada Gambar 2.
Gambar 2. Mekanisme reaksi hidrolisis trigliserida (Hudiyono, 2009) Menurut Freidfelder (1987), pada umumnya reaksi hidrolisis berlangsung ketika garam dari basa lemah atau garam dari asam lemah dilarutkan ke dalam air. Air akan melakukan autoionisasi menjadi ion hidroksil negatif dan ion hidrogen. Kemudian garam akan terpecah menjadi ion positif dan ion negatif. Hanya saja, dalam kondisi normal, reaksi hidrolisis antara air dan beberapa
8 komponen organik hanya sedikit yang terjadi. Umumnya reaksi ini membutuhkan katalis berupa asam, basa atau secara enzimatis.
D. Lipase
Enzim-enzim hidrolisis telah banyak digunakan dalam sintesa organik karena ketersediaan bahan baku dan penanganan yang mudah. Enzim ini tidak membutuhkan koenzim, stabil dan toleran terhadap pelarut organik. Potensi mereka untuk melakukan sintesis regioselektif dan enantioselektif menjadikan mereka sebagai alat yang berharga (Schuchardt, 1997).
Asam lemak tak jenuh sangat labil terhadap panas dan oksidasi. Reaksi enzim telah menarik perhatian karena enzim dapat melakukan proses pada temperatur dan tekanan lingkungan serta di bawah tekanan nitrogen. Beberapa lipase tidak bereaksi secara baik pada asam lemak tak jenuh dan asam lemak tak jenuh dapat dipekatkan melalui keuntungan ini. Misalnya, ketika minyak ikan, minyak borage dan minyak yang mengandung asam arachidonat dari
Mortierella dihidrolisis dengan menggunakan lipase dari Candida rugosa atau Geotrichum candidum, kandungan DHA, asam α-linolenat dan asam arakidonat
meningkat di dalam gliserida (Shimada, 1998).
Lipase (triasilgliserol asil hidrolase, EC 3.1.1.4) telah menjadi katalis yang penting dalam sintesis organik. Karena reaksi hidrolisis merupakan reaksi kesetimbangan di dalam sistem non aqueous, biokatalis ini juga dapat mengkatalisis formasi ester dari donor asil dan alkohol. Lipase tidak membutuhkan kofaktor (Ghanem, 2004).
Lipase memiliki kemampuan untuk mengkatalisis reaksi kebalikan (esterifikasi, interesterifikasi dan transesterifikasi) yang ada dengan menggantikan media aqueous dengan media non aqueous. Lipase juga menunjukkan selektivitas yang tinggi termasuk stereo selektivitas dan memberikan hasil akhir produk yang murni dan berkualitas baik (Hilal, 2006).
Lipase dikenal bereaksi lemah terhadap asam lemak tak jenuh, seperti asam α-linolenat (GLA, 18:3n-6), asam arakidonat (20:4n-6), asam eikosapentanoat
9 (EPA, 20:5n-3), dan asam dokosaheksanoat (DHA, 22:6n−3) dan asam lemak ini dapat diperkaya melalui hidrolisis selektif dan melalui esterifikasi selektif (Shimada, 1997).
Menurut N. N. Gandhi (1996) ada dua katagori di mana lipase dapat digunakan sebagai katalis yaitu :
a. Hidrolisis RCOOR’ + H2
b. Sintesis
O RCOOH + R’OH
Reaksi sintesis dapat dipisahkan menjadi : i. Esterifikasi
RCOOH + R’OH RCOOR’ + H2
ii. Interesterifikasi
O
RCOOR’ + R”COOR’” RCOOR’” + R”COOR’ iii. Alkoholisis
RCOOR’ + R”OH RCOOR” + R’OH iv. Asidolisis
RCOOR’ + R”COOH R”COOR’ + RCOOH
Lipase mikroba diproduksi dari fermentasi bakteri, kapang dan khamir, seperti Rhizopus delemar, Aspergilus niger, Geotrichum candidum, Candida
rugosa, dan Chromobacterium viscocum (Gandhi, 1997). Lipase berdasarkan
cara kerjanya dibagi menjadi tiga yaitu:
a. Lipase non spesifik yaitu lipase yang dapat mengkatalis seluruh ikatan ester pada trigliserida
b. Lipase spesifik 1,3 atau 2 yaitu lipase yang dapat mengkatalis trigliserida pada ikatan 1,3 atau 2
c. Lipase spesifik yaitu lipase yang hanya mengkatalis jenis asam lemak tertentu (Herawan, 1993).
Menurut Amano Enzyme (2007), lipase dapat mengkatalisis reksi hidrolisis, sintesis dan transfer reaksi dari trigliserida yang terdiri atas asam lemak dengan gliserin sebagai substratnya. Spesifisitas substrat lipase dapat diklasifikasikan sebagai berikut:
10 a. Spesifisitas posisi pada hidrolisis ester
Ketika lipase bekerja pada trigliserida untuk melepaskan asam lemak, posisi dari ester yang dihidrolisis lipase tergantung pada jenis lipase yang diaplikasikan. Terdapat tiga macam lipase di mana salah satu tipe bekerja pada posisi α- dan α’-. Tipe lipase lainnya bekerja pada posisi β dan tipe yang terakhir bekerja pada ketiga posisi tersebut. Di sini, posisi pusat trigliserida tempat di mana sisa asam lemak melekat dikenal sebagai posisi β, sedangkan posisi terluar dikenal sebagai posisi α dan α’. b. Spesifisitas untuk panjang rantai asam lemak
Panjang rantai asam lemak yang terhubung pada trigliserida yang direpresentasikan dalam jumlah atom karbon memiliki jumlah atom karbon bervariasi mulai dari 2 sampai 24 atom karbon. Meskipun lipase dapat dikategorikan menjadi lipase yang menghidrolisis ester asam lemak rantai pendek secara efisien dan lipase yang dapat menghidrolisis ester asam lemak rantai sedang-panjang secara efektif. Hanya saja, batasan pembagiannya masih belum jelas.
Menurut Halldorsson (2003), lipase dapat digunakan untuk membuat konsentrat EPA dan DHA dari seluruh bagian komposisinya dengan efisien dan memiliki yield yang tinggi. Pada umumnya, lipase seperti R. miehei lipase, memiliki regioselektif pada ikatan 1,3 dan hanya beraksi pada posisi akhir primer dari gliserol dan transformasi yang melibatkan posisi di tengah tergantung dari proses migrasi asil yang berlangsung.
Purifikasi asam dokosaheksanoat (DHA) telah diuji coba dengan menggunakan metode enzimatis dua langkah yang terdiri atas hidrolisis minyak ikan dan selektif esterifikasi yang menghasilkan asam lemak bebas. Ketika lebih dari 60% minyak tuna dihidrolisis dengan menggunakan Pseudomonas
sp. Lipase (Lipase-AK), kandungan DHA dalam fraksi asam lemak bebas sama
persis dengan kandungan DHA pada minyak tuna sebelumnya. Enzim lipase ini menunjukkan aktivitas yang lebih kuat pada ester DHA dibandingkan pada
11 ester asam eikosapentanoat dan sesuai untuk persiapan asam lemak bebas yang kaya DHA (Shimada, 1997).
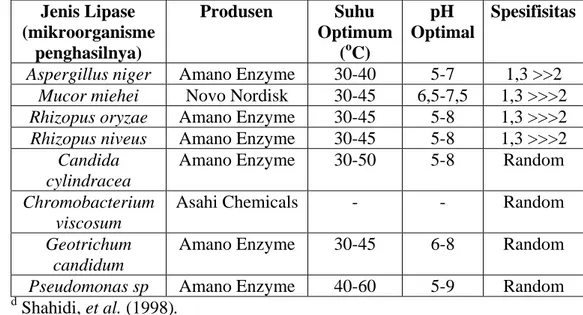
Tabel 4. Aktivitas mikrobial dan karakteristik lipased Jenis Lipase (mikroorganisme penghasilnya) Produsen Suhu Optimum (oC) pH Optimal Spesifisitas
Aspergillus niger Amano Enzyme 30-40 5-7 1,3 >>2
Mucor miehei Novo Nordisk 30-45 6,5-7,5 1,3 >>>2
Rhizopus oryzae Amano Enzyme 30-45 5-8 1,3 >>>2
Rhizopus niveus Amano Enzyme 30-45 5-8 1,3 >>>2
Candida cylindracea
Amano Enzyme 30-50 5-8 Random
Chromobacterium viscosum
Asahi Chemicals - - Random
Geotrichum candidum
Amano Enzyme 30-45 6-8 Random
Pseudomonas sp Amano Enzyme 40-60 5-9 Random
d
Shahidi, et al. (1998).
E. Pelarut Organik
Pelarut merupakan cairan atau gas yang melarutkan padatan, cairan lain atau gas lain sehingga terbentuk suatu larutan. Pelarut yang umum digunakan adalah air, sedangkan pelarut lainnya adalah bahan organik yang mengandung karbon dan dikenal sebagai pelarut organik. Pelarut organik ini biasanya memiliki titik didih yang rendah dan dapat menguap dengan mudah melalui proses destilasi, kemudian meninggalkan kandungan bahan lain yang ada di dalamnya (Wikipedia, the free encyclopedia, 2009b).
Pelarut dapat menyebabkan modifikasi bentuk enzim, yaitu mengubah efisiensi katalitiknya dan spesifitasnya. Berdasarkan Ueji dan Takashi (1999), penggunaan media non konvensional akan meningkatkan enantioselektivitas pada reaksi katalisis oleh biokatalis. Keuntungan lain penggunaan pelarut non aqueous adalah resiko kontaminasi mikrobial lebih rendah daripada pada sistem aqueous. Ketertarikan khusus terhadap media non konvensional pada reaksi hidrolisis dengan kadar air yang rendah dapat digunakan untuk reaksi sintesis
12 yang menyediakan kelarutan yang terbaik pada substrat hidrofobik dengan lipase sebagai katalis (Krieger et al., 2004).
Stabilitas protein lebih rendah dalam air yang tak larut dalam pelarut yang ada pada -2,5<logP<0 seperti aseton dan eter daripada pada pelarut hidrofobik (2<logP<4) seperti alkana atau haloalkana. Pelarut organik hidrofobik tidak dapat memotong ikatan air dari permukaan enzim. Ketika pelarut organik memotong air dari enzim, berakibat pada tidak adanya ikatan antara molekul. Oleh sebab itu, penerimaan stabilitas enzim lipase pada penggunaan pelarut hidrofilik jarang dilakukan (Krieger et al., 2004).
Peptida dan dan protein merupakan molekul kompleks dimana kelarutannya pada beberapa pelarut aqueous dan organik harus ditentukan secara empiris. Karakteristik kelarutannya seperti: crosslinker; pelabelan pelarut biotin dan
flourophore; dan pelarut kimia dapat ditentukan dengan mudah dengan
menghitung nilai log P. Nilai log P merupakan logaritma koefisien partisi (P) yang didefinisikan sebagai rasio konsentrasi bahan organik dengan bahan aqueous (Anonim, 2007)
Menurut Herees et al, (2008), stabilitas dan aktivitas enzim merupakan fungsi dari pelarut organik. Untuk menghitung pengaruh pelarut organik terhadap aktivitas enzim, digunakan konsep log P. Nilai log P suatu pelarut merupakan logaritma dari koefisien partisi suatu pelarut di dalam larutan standar 1-oktanol dan air. Tabel 5 menjelaskan hubungan koefisien partisi dengan laju reaksi.
Tabel 5. Laju reaksi sebagai fungsi dari pelarute
Pelarut Nilai log P Laju reaksi (x 104 mol L-1s-1)
Dekana 5,6 9,33 n-Heptana 4 8,17 n-Heksana 3,5 3,33 Toluena 2,5 2 e Herees et al., (2008)
Karakterisasi pelarut toluena dapat dilihat lebih jelas pada Tabel 6. Pelarut toluena utamanya dipilih karena sifatnya yang non polar dan memiliki nilai log P sebesar 2,5.
13 Tabel 6. Karakteristik pelarut toluenaf
Karakteristik Toluena Rumus kimia C7H8 Sifat Nonpolar Berat molekul 92,14 Log P 2,5 Titik didih (oC) 110,6 Titik leleh (oC) -93 Densitas (g/mL) 0,867
Kelarutan di dalam air (g/100g) 0,05
Konstanta dielektrik 2,38(25)
Titik nyala (oC) 4
f
Myers (2009)
Menurut Klibanov (1986), penggunaan pelarut organik pada reaksi hidrolisis ester mempunyai beberapa keuntungan selain penggunaan air, yaitu:
a. Substrat organik merupakan bahan yang mudah larut, di mana enzim tidak dapat larut. Oleh karena itu, produk dan enzim mudah didapatkan kembali dengan metode non ekstraksi sehingga rendemen produk akan meningkat.
b. Substrat yang sensitif terhadap air dapat digunakan.
c. Kesetimbangan reaksi berubah, dan ester dan amida dapat dipersiapkan. d. Enzim lebih stabil pada suhu tinggi ketika air yang dapat menghidrolisis
ikatan peptida enzim tidak ada.
e. Enzim menjadi lebih rigid dan menjadi lebih selektif.
f. Tidak ada pengaruh pH sehingga peralatan yang sederhana dapat digunakan.
F. Pengaruh Suhu
Suhu dapat berpengaruh positif terhadap reaksi hidrolisis maupun sebaliknya. Kenaikan suhu akan meningkatkan laju reaksi. Pada reaksi
14 menggunakan suhu tinggi struktur tersier enzim terganggu akibat terjadi denaturasi. Pada suhu 50oC nilai tingkat konversinya berubah menjadi cukup rendah. Sedangkan suhu 45oC merupakan suhu optimum reaksi hidrolisis sebab pada suhu diatas 45oC tingkat konversinya turun secara tiba-tiba dikarenakan enzim mengalami denaturasi (Kamarudin et al., 2008).
Menurut Lehninger (1982), kestabilan enzim erat kaitannya dengan komposisi enzim yang umumnya merupakan protein. Protein akan mengalami denaturasi pada suhu tinggi dan menyebabkan lepasnya ikatan-ikatan sekunder dan tertier antara asam-asam amino penyusunnya. Bila hal ini terjadi pada enzim, maka enzim akan mengalami deformasi atau perubahan bentuk yang akan menyebabkan kerusakan pada sisi aktifnya dan menginaktifkan enzim tersebut.
Suhu berpengaruh terhadap aktivitas dan stabilitas enzim lipase, suhu yang sesuai untuk penggunaan enzim lipase sebagai katalis adalah dibawah 70oC karena pada suhu tinggi menyebabkan terjadinya migrasi alkil secara non-enzimatik, oksidasi, isomerisasi dan denaturasi enzim (Wanasundara dan Shahidi, 1998).
Suhu juga berpengaruh terhadap kecepatan reaksi pembentukan asam lemak bebas. Peningkatan suhu reaksi pada reaksi hidrolisis akan mempercepat kenaikan konsentrasi asam lemak bebas, memperbesar penurunan konsentrasi air, atau dengan kata lain dapat menaikkan hasil konversi. Karena dengan naiknya suhu reaksi, maka suplai energi untuk mengaktifkan katalis dan terjadinya tumbukan antar pereaksi untuk menghasilkan reaksi juga akan bertambah, sehingga produk yang dihasilkan menjadi lebih banyak. Nilai konstanta kecepatan reaksi (k) naik dengan kenaikan suhu reaksi (rata-rata kenaikannya 2 kali dari nilai awal), hal ini sesuai dengan teori Arrhenius dan pernyataan Westerterp (1984), bahwa kenaikan suhu akan menaikan nilai konstanta kecepatan reaksi, di mana kenaikan 10°C suhu reaksi menaikan konstanta kecepatan reaksi sebanyak 2 kali dari nilai awal. Sedangkan apabila suhu reaksi yang digunakan terlalu rendah maka laju reaksi berjalan lambat akibatnya tumbukan antar pereaksi rendah dan minyak tidak terhidrolisis secara
15 sempurna. Hidrolisis yang berlangsung secara tidak sempurna akan menyebabkan lebih sedikitnya produk yang terbentuk atau asam lemak bebas hasil reaksi hidrolisis menjadi berkurang jumlahnya dibandingkan dengan reaksi sebenarnya.
G. Pengaruh pH
Enzim sangat sensitif terhadap perlakuan medium pH, karena memungkinkan perubahan status ionisasi enzim, yang akan mempengaruhi aktivitas dan selektifitas. Menurut Lehninger (1982), profil aktivitas pH enzim menggambarkan pH pada saat gugus pemberi atau penerima proton yang penting pada sisi katalitik enzim berada dalam tingkat ionisasi yang diinginkan. pH optimum enzim tidak perlu sama dengan pH lingkungan normalnya. Worthington Biochemical Corporation (2009) juga menyatakan bahwa nilai pH yang terlalu tinggi atau terlalu rendah akan berakibat pada turunnya aktivitas sebagian besar enzim. pH juga merupakan faktor yang mempengaruhi stabilitas enzim.
Berdasarkan Stauffer (1989), ketertarikan studi mengenai tingkat enzim sebagai fungsi pH dikarenakan karena beberapa faktor yaitu :
a. Status protonasi sisi rantai asam amino pada sisi aktif kompleks enzim substrat (ES) mungkin akan berubah. Hasilnya perubahan kemampuan enzim substrat untuk menjadi produk.
b. Perubahan ionik molekul substrat atau perubahan ionik sisi aktif yaitu kecenderungan dua molekul tersebut unutk menjadi kompleks ES. c. Perubahan pH dari netral yang memungkinkan melemahkan kekuatan
stabilitas bentuk protein, yang berakibat peningkatan denaturasi enzim (kehilangan aktivitas).
Berdasarkan studi Microbial Lipase Potential Biocatalist for the future
industry, titik isoelektrik lipase adalah 4,3. Stabilitas lipase berada pada pH
16 H. Pengaruh Penambahan Air
Laju reaksi hidrolisis membutuhkan sejumlah air. Namun, terlalu banyak air akan berakibat pada reaksi hidrolisis trigliserida yang berlebihan yang berakibat pada peningkatan asam lemak bebas dan gliserida parsial (monogliserida dan digliserida). Sedikit air baik untuk reaksi transesterifikasi. Pengaturan kadar air pada sistem ini menjadi sangat penting karena semua proses didasarkan pada termodinamika dari kesetimbangan reaksi kimia yang bersifat bolak-balik di mana air berperan penting. Selain itu, air diperlukan untuk integritas tiga dimensi struktur molekul enzim. Oleh sebab itu, aktivitas lipase merupakan fungsi dari kadar air. Salah satu hipotesa menyatakan bahwa dimensi molekul enzim membutuhkan lapisan hidrasi sedikit yang akan bereaksi sebagai komponen utama pada enzim microenvironment pada media organik. Lapisan ini akan bertindak sebagai buffer di antara permukaan enzim dan media reaksi (Dordick, 1989).
Menurut Herees et al, (2008), enzim lipase cenderung bekerja pada permukaan antar cairan (liquid-liquid interface) dibandingkan dengan suatu titik tertentu di dalam campuran reaksi. Penggunaan bahan yang dapat menggabungkan senyawa-senyawa yang akan bereaksi pada reaksi hidrolisis akan membantu meningkatkan aktivitas dari enzim lipase yang digunakan.
Klibanov (1986) menyatakan bahwa sedikit air diperlukan untuk mencapai aktivitas maksimal pada pelarut hidrofobik daripada pelarut hidrofilik. Pada aktivitas kadar air yang rendah, semakin rendah polaritas suatu pelarut menyebabkan semakin tingginya aktivitas enzim. Ketika aktivitas katalitik enzim diplotkan terhadap jumlah air yang terikat dengan enzim, suatu pola muncul untuk beberapa pelarut yang berbeda. Salah satunya dapat disebutkan bahwa aktivitas enzimatik pada media organik ditentukan bukan oleh interaksi pelarut dengan enzim tetapi oleh keberadaan air dalam enzim.
Selain itu, rumus terjadinya reaksi hidrolisis menurut NN. Gandhi (1996) dapat dilihat pada Gambar 3.
RCOOR’ + H2
Gambar 3. Reaksi hidrolisis pada senyawa ester O RCOOH + R’OH
17 Berdasarkan Gambar 3, dapat dilihat bahwa reaksi hidrolisis membutuhkan satu molekul air setiap kali melepaskan satu gugus alkil dari senyawa esternya. Hal ini menunjukkan bahwa penambahan air diperlukan untuk menyediakan pereaksi yang diperlukan agar terjadi reaksi hidrolisis dari minyak ikan yang digunakan. Tanpa adanya air di dalam campuran reaksi, maka tidak akan terjadi reaksi hidrolisis.