Metabolisme hidrogen peroksida
dan peranannya pada infeksi telinga
Edi Handoko, Wiro Anton Sumilat LaboratoriumIlmu Penyakit Telinga Hidung Tenggorok
Fakultas Kedokteran Universitas Brawijaya/ Rumah Sakit Dr. Saiful Anwar
Malang - Indonesia
ABSTRAK
Latar belakang: Hidrogen peroksida (H2O2) telah lama digunakan di bidang medis sebagai obat cuci luka, debriding agent, pembersih serumen, mengobati telinga berair dan membersihkan tuba
ventilasi yang tersumbat. Tujuan: Mengetahui keamanan penggunaan hidrogen peroksida sebagai cairan pencuci telinga terhadap fungsi koklea dan vestibuler telinga dalam. Tinjauan pustaka: Dilaporkan bahwa H2O2 memiliki efek bakterisidal, sehingga mampu membunuh bakteri. Penggunaan H2O2 agaknya tidak selamanya aman. Beberapa percobaan pada binatang menunjukkan H2O2 memiliki efek yang merugikan terhadap fungsi koklea dan vestibuler telinga dalam. Kesimpulan: H2O2 dapat memperlambat aktivitas gerak silia, meningkatkan permeabilitas membran, meningkatkan sekresi
mukus, akhirnya menyebabkan kerusakan DNA dan kematian sel.
Kata kunci: hidrogen peroksida, metabolisme, infeksi telinga, aktivitas gerak silia
ABSTRACT
Background: Hydrogen peroxide (H2O2) had been used as wound cleaner, debriding agent, earwax cleaner, treatment of ear watering and cleaner of blocked ventilating tube. H2O2 has been reported has a bactericidal effect. Purpose: To provide information about the safety of usage hydrogen peroxide for
the cochlear and vestibular function. Review: The usage of H2O2 seemed not always safe. Some experiments to animal had shown that H2O2 had negative effect towards cochlear and vestibular function. Conclusion: H2O2 could delay the cilia motility, increase membrane permeability and mucous secretion, cause DNA damage and cell death.
Key words: hydrogen peroxyde, metabolism, ear infection, ciliar activity
Alamat korespondensi: Edi Handoko, Laboratorium Ilmu Penyakit THT FK Universitas Brawijaya, Malang. E-mail: [email protected]
PENDAHULUAN
Sejak diproduksi pertama kali tahun 1800 di Inggris, hidrogen peroksida atau H2O2 telah digunakan di seluruh dunia untuk bahan pemutih produk tekstil dan kertas, dipakai pada pemrosesan makanan, bidang pertanian, petrokimia, desinfektan, deterjen, waste water, bahkan sebagai komponen oksidan bahan bakar roket.1
H2O2 telah lama dikenal dan digunakan di bidang medis. Pemakaiannya adalah
sebagai obat cuci luka dan debriding agent. Di bidang THT, H2O2 digunakan sebagai
pembersih serumen, mengobati telinga berair dan membersihkan tuba ventilasi yang tersumbat. Dilaporkan bahwa H2O2 memiliki efek bakterisidal, sehingga
mampu membunuh bakteri. Namun,
penggunaan H2O2 agaknya tidak selamanya aman. Beberapa percobaan pada binatang menunjukkan H2O2 memiliki efek yang merugikan terhadap fungsi koklea dan vestibuler telinga dalam.2
H2O2 ternyata terbentuk alami dalam
tubuh sebagai produk metabolisme
oksidatif sel, terutama sel fagosit lekosit. Beberapa penelitian melaporkan peranan radikal bebas dan oksidan termasuk H2O2 dalam patogenesis otitis media.3,4
Berdasarkan hal-hal di atas, penulis ingin mengetahui metabolisme H2O2 dalam tubuh manusia dan peranannya pada infeksi
telinga, sehingga dapat memahami dan menerapkannya secara tepat.
TINJAUAN PUSTAKA
Hidrogen peroksida
H2O2 pertama kali diisolasi melalui reaksi barium peroksida dan asam nitrat oleh Louis Jacques Thenard pada tahun
1818. Proses ini digunakan untuk
menghasilkan H2O2 sejak akhir abad ke-19 sampai pertengahan abad ke-20. H2O2
murni ditemukan pertama kali oleh Richard Wolffenstein pada tahun 1894 melalui
destilasi vakum. Nama lainnya adalah dioksida dihidrogen, dihidrogen dioksida, hidrogen dioksida atau dioksidan. H2O2 sangat melimpah di alam, terutama terbentuk oleh rangsangan cahaya matahari pada air dan ditemukan pada air hujan dan salju.5
Sifat fisik dan kimiawi
Tabel 1. Potensial oksidasi beberapa oksidan.1
Oksidan Potensial oksidasi (V)
Florin 3,0
Radikal hidroksil 2,8
Ozon 2,1 eksotermik menjadi air dan oksigen secara spontan dengan reaksi:
2 H2O2 2 H2O2 + O2
Proses ini sangat termodinamika.
Faktor-faktor yang mendukung
dekomposisi ini adalah peningkatan suhu
(2,2 faktor meningkat setiap 10ºC), peningkatan pH (khususnya pada pH>6-8), peningkatan kontaminasi (khususnya logam transisi seperti tembaga, mangan dan besi) sebagai katalisator, adanya stabilisator dan yang lebih kurang adalah pemaparan
dengan sinar ultraviolet.1 Untuk
mengurangi dekomposisi selama
transportasi dan penyimpanan, maka digunakan stabilisator. Stabilisator yang biasa digunakan adalah colloidal stannate, natrium pirofosfat, organofosfonat, juga ditambah dengan nitrat dan asam fosforik.1 Pembebasan oksigen dan energi dalam dekomposisi ini memiliki efek berbahaya. H2O2 konsentrasi tinggi dengan jumlah banyak bila kontak dengan bahan yang
mudah terbakar dapat langsung terbakar dipicu oleh oksigen yang dilepaskan.1
Konsentrasi
Konsentrasi H2O2 adalah: 1) 3-3,5% (kadar farmasi) sediaan dengan konsentrasi ini banyak dijual di apotek, toko obat dan supermarket. Sediaan ini mengandung sejumlah stabilisator, seperti asetanilid, fenol, natrium stanat dan tetranatrium fosfat yang bersifat toksik, sehingga tidak direkomendasikan untuk pemakaian dalam tubuh; 2) 6% (kadar kecantikan) banyak digunakan di salon kecantikan sebagai
pelarut zat warna rambut. Tidak
direkomendasikan untuk pemakaian dalam tubuh; 3) 30% (kadar regen) digunakan dalam percobaan di laboratorium dan biasanya mengandung stabilisator; 4) 30-32% (kadar elektronik) digunakan untuk membersihkan komponen elektronik; 5)
Menurut code of federal regulation,
konsentrasi H2O2 terbagi atas: 1) <8% tidak berbahaya. Digunakan sebagai baking soda
pasta gigi, sterilisasi kontak lens, deterjen dan lain-lain; 2) 8-27,5%, Oxidizer class-1
(bahaya terbakar); 3) 27,5–52%, Oxidizer
class-2, corrosive (bahaya terhadap
kesehatan, yaitu dapat membakar
kulit/jaringan), unstable/reactive class-1
(bahaya ledakan); 4) 52-91%, Oxidizer class-3, corrosive and unstable/reactive
class-3; 5) >91%, Oxidizer class-4, corrosive and unstable/reactive class-4.6
Efek yang merugikan
H2O2 adalah suatu senyawa yang iritan terhadap mata, membran mukosa dan kulit. Pemaparan singkat pada mata dapat mengakibatkan rasa perih dan mata berair,
walaupun dengan konsentrasi 1-3%.
Kontak kulit akan menyebabkan pemutihan
kulit sementara. Inhalasi pada kadar yang tinggi akan menyebabkan iritasi yang berat pada hidung dan saluran napas. Bila tertelan, maka akan terjadi iritasi sampai kerusakan berat pada saluran cerna. Keracunan sistemik akan menyebabkan sakit kepala, pusing, muntah, diare, tremor, mati rasa, kejang, edema paru, kehilangan kesadaran sampai syok.7
Cara penyimpanan
H2O2 sebaiknya disimpan dalam ruangan dingin, kering, dengan ventilasi yang baik, dan dijauhkan dari bahan-bahan
yang mudah terbakar. Tempat
penyimpanan seharusnya terbuat dari bahan yang tidak bereaksi, seperti stainless steel, kaca, beberapa jenis plastik dan campuran aluminium yang berwarna gelap.6
Hidrogen peroksida dan reactive oxygen species (ROS)
H2O2 dengan ion oksigen dan radikal bebas termasuk dalam reactive oxygen
species (ROS). ROS adalah produk
metabolisme oksigen dalam tubuh normal yang bersifat sangat reaktif, yang disebut radikal bebas adalah radikal superoksid (O2-), radikal hidroksil, (OH-) dan radikal hidroperoksil (HO2-). H2O2 sendiri bukan suatu radikal bebas.4 Nilai produksi dan pembersihan ROS berada dalam keadaan
seimbang pada tubuh yang sehat. Bila ada penambahan oksidan eksogen seperti asap rokok, polusi udara, sinar ultraviolet, radiasi, obat seperti cisplatin dan
aminoglikosida, atau asupan kalori yang berlebihan, maka keseimbangan ini akan bergeser ke arah pembentukan ROS yang lebih banyak.5
amino protein yang berujung pada kematian sel.4,8
H2O2 secara elektris mempunyai sifat netral, sehingga tidak dihambat saat berdifusi melewati membran sel. Masa hidup H2O2 in vivo sangat singkat, yaitu dalam waktu milidetik. Kestabilannya dipengaruhi oleh pH dalam lingkungan oksidasi seperti ekstraseluler, H2O2 lebih stabil daripada dalam lingkungan reduksi seperti intraseluler.2
Produksi hidrogen peroksida
Sumber utama H2O2 sel adalah mitokondria. Selama proses respirasi seluler di mitokondria, O2 akan berperan dalam pembentukan adenosine trifosfat
(ATP), akan tetapi sebagian O2 akan tereduksi membentuk superoksid, O2 yang reaktif. Ini diperkirakan akibat kehilangan satu elektron dalam rantai transpor elektron mitokondria. Proses ini selanjutnya akan mereduksi O2 (dismutasi) lagi menjadi H2O2, dengan perantaraan enzim superoksid dismutase (SOD) dan H2O2 akan tereduksi menjadi radikal hidroksil, OH-, suatu oksidan yang luar biasa reaktif. Hal ini bisa terjadi spontan, akibat pengaruh beberapa enzim atau pemaparan radiasi ionisasi. Perubahan ini lebih mudah terjadi bila adanya unsur logam seperti besi atau tembaga. Selain terbentuk dari dismutasi superoksid, ia juga terbentuk oleh glikolat oksidase dalam peroksisom.4,9
Bakteri pun dapat menghasilkan H2O2. Penelitian oleh Seki,10 menyimpulkan
bahwa Streptococcus pyogenes
menghasilkan H2O2 dengan mengkonsumsi glukosa, melalui perantaraan tiga enzim, yaitu NADH oksidase (di sitoplasma),
laktat oksidase (di membran sel) dan -gliserofosfat oksidase. Penelitian in vivo
dan in vitro, menyimpulkan bahwa H2O2 merupakan faktor virulensi yang penting untuk merusak jaringan tubuh manusia.
Selain itu H2O2 yang dihasilkan suatu bakteri dapat menghambat pertumbuhan bakteri lainnya. Pericone,11 menunjukkan bahwa kuman Streptococcus pneumonia
yang diisolasi dari nasofaring menghasilkan H2O2, diperantarai enzim piruvat oksidase (SpxB) dalam keadaan aerob. Produk ini
dapat membunuh (bakterisidal)
Haemophillus influenzae, menghambat
pertumbuhan (bakteriostatik) Moraxella catarrhalis dan Neisseria meningitidis. Organisme dalam mulut yang dapat dibunuh atau dihambat oleh H2O2 adalah
Neisseria gonorrhea, Staphylococcus
aureus dan Corynebacterium diphteria. Takoudes dan Haddad,3 menyatakan bahwa bakteri Streptococcus pneumonia
dan netrofil yang diisolasi dari penderita otitis media akan melepaskan H2O2 yang selanjutnya akan berubah menjadi radikal bebas.
Lactobacillus di kolon dan vagina dapat menghasilkan H2O2, yang akan membunuh bakteri dan virus patogen lain.6 Melalui penelitian oleh Bolm,12 dilaporkan bahwa H2O2 yang dihasilkan oleh Streptococcus
pneumonia, Streptococcus viridans,
Streptococcus group B dan C, serta
Pneumonoccus dapat membunuh larva
nematoda Caenorhabditis elegans.
Pemberian obat tertentu dapat
merangsang pembentukan H2O2.
Ciprofloxacin dapat merangsang
terbentuknya ROS termasuk H2O2 dalam tubuh bakteri, yang akan menyebabkan kerusakan DNA bakteri tersebut. Hal senada disimpulkan oleh Goswami,13 pada penelitian mereka terhadap bakteri
Escheria coli, bahwa O2 dan H2O2 terlibat dalam aksi antibakterial Ciprofloxacin. Walaupun demikian, mereka belum dapat
menjelaskan dengan lengkap
mekanismenya.
Peran hidrogen peroksida dalam jaringan tubuh manusia
H2O2 berperan pada proses luka pada pembuluh darah kecil, yang mengakibatkan peningkatan permeabilitas endotel. Hal ini menunjukkan bahwa H2O2 bersifat toksik pada endotel. Selain itu, dapat menghambat transpor anion, merangsang aktivitas pompa natrium-kalium membran sel dan kerusakan DNA.14 Menurut penelitian Lee
et al,15 setelah pemberian H2O2 1% dan 3% dalam larutan salin dengan nebuliser sebanyak tiga kali dalam 24 jam pada tikus. Peningkatan permeabilitas vaskuler, respons jalan napas terjadi bersamaan dengan peningkatan ekspresi protein
vascular endothelial growth factor
(VEGF). Hal yang sebaliknya terjadi setelah pemberian antioksidan, asam
endotel melalui regulasi VEGF. ROS
termasuk H2O2 juga menyebabkan
peningkatan produksi mukus, penurunan fungsi dan jumlah epitel bersilia.15
Di sisi lain, ROS dalam hal ini H2O2 memiliki sifat yang menguntungkan, yaitu sebagai bagian sistem pertahanan tubuh. H2O2 bersifat bakterisidal dihasilkan oleh lekosit fagositik, seperti netrofil dan makrofag, melalui proses yang disebut
oxidative burst atau respiratory burst.5
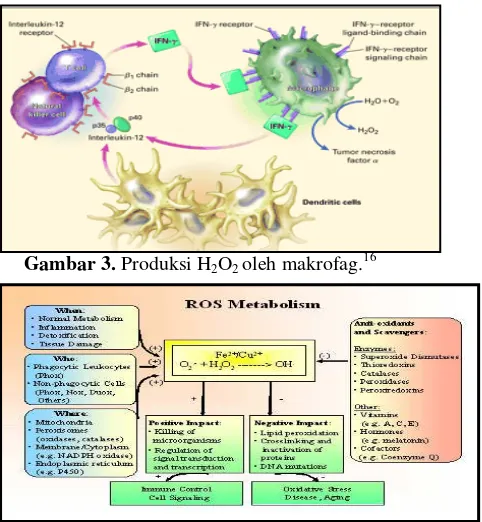
Proses ini diperantarai oleh enzim nikotinamida adenine dinukleotid fosfat tereduksi (NADPH) oksidase.16 Adanya patogen akan memicu produksi interleukin-12 oleh makrofag dan sel dendrit, yang selanjutnya menginduksi sekresi
oleh sel T dan natural killer cell. Interferon- ini akan mengaktifkan makrofag dan netrofil untuk menghasilkan TNF- dan NADPH oksidase.16
Gambar 2. Peranan NADPH oksidase dalam membentuk H2O2 (oxidative burst).21
Gambar 3. Produksi H2O2 oleh makrofag.16
Aktivitas limfosit T juga dipengaruhi oleh H2O2. H2O2 yang dilepaskan oleh makrofag akan merangsang limfosit T
untuk berikatan dengan antigen
mikroorganisme pada reseptor sel T (T cell receptor). Reseptor sel T ini nantinya lewat
MAPK pathway akan merangsang
mitokondria limfosit T menghasilkan H2O2.5
Hidrogen peroksida dalam jaringan tubuh manusia: 1) rongga mulut, esophagus dan lambung. H2O2 yang ada di minuman seperti teh hijau, teh hitam dan kopi instant, konsentrasinya dapat mencapai di atas 100 mikro-M dan bila tertelan, maka akan segera berdifusi ke dalam sel. H2O2 terdapat pada air liur akan mengoksidasi tiosianat dengan enzim peroksidase, menghasilkan produk toksik yang akan
menghambat pertumbuhan beberapa
bakteri; 2) sistem respirasi. H2O2 juga
ditemukan dalam udara ekspirasi, terutama pada penderita penyakit paru, akibat proses fagositosis yang dilepaskan oleh makrofag alveolar dan netrofil; 3) ginjal dan saluran kencing. H2O2 dapat terdeteksi di urin dengan konsentrasi bisa mencapai 100
mikro-M. Ini diperkirakan akibat
autoksidasi sel. Ada pemikiran bahwa senyawa ini terlibat dalam modulasi fungsi ginjal, namun mekanismenya belum dapat diterangkan; 4) endotel vaskuler dan sel
darah sirkulasi. Beberapa studi menegaskan ditemukannya kadar yang cukup banyak dalam plasma darah. Di sini ia dapat bereaksi dengan protein heme, askorbat dan kelompok protein-SH. H2O2 dalam plasma dapat berdifusi ke dalam eritrosit, lekosit, endotel dan platelet untuk proses metabolisme; 5) mata, telah dilaporkan adanya H2O2 dalam akuos humor dan vitreus humor manusia dan binatang, yang diperkirakan berasal dari oksidasi glutation atau askorbat. Ketidakmampuan epitel lensa, retina dan jaringan lain untuk
membuangnya menyebabkan terjadi
akumulasi.7
Antioksidan
Radikal bebas dapat dihilangkan dari
lingkungan sel dengan perantaraan
antioksidan. Enzim antioksidan yang ada yaitu superoksida dismutase (SOD),
glutation peroksidase dan katalase.4 Antioksidan non-enzim yang ada dalam tubuh yaitu glutation, -tokoferol (vitamin E), asam askorbat (vitamin C), -karoten (vitamin A), albumin, bilirubin dan asam urat. Antioksidan dan enzimnya akan merubah oksidan atau radikal bebas menjadi senyawa yang aman dan kurang reaktif.8
2O2 + 2H+ SOD O2 + H2O2
Glutation (GSH) peroksidase akan merubah H2O2 menjadi air dan glutation disulfid (GSSG):
H2O2 + 2 GSH
Glutation peroksidase
2 H2O + GSSG Katalase akan merubah H2O2 menjadi air dan oksigen:
2 H2O2
Katalase
H2O + O2
Peran hidrogen peroksida pada otitis media
H2O2 dipikirkan berperan dalam proses infeksi di telinga, baik secara langsung atau lewat produk dismutasi yang dihasilkan,
yaitu OH-. Yilmaz4 di Turki, melakukan penelitian terhadap cairan telinga tengah
dan darah perifer dari 24 penderita otitis media efusi (OME) yang dilakukan operasi insersi tuba ventilasi dan adenoidektomi. Mereka mendapatkan bahwa kadar oksidan
dalam hal ini produk oksidasi,
malondialdehid, meningkat sebelum
operasi dan menurun setelah operasi. Sebaliknya kadar antioksidan, yaitu asam askorbat, -tokoferol dan glutation, rendah sebelum operasi dan lalu meningkat setelah operasi. Proses inflamasi otitis media akan meningkatkan produksi radikal bebas O2 dan OH- lekosit. Produk ini akan mengakibatkan peroksidasi lipid (lipid peroxidation) membran sel mukosa, yang menghasilkan malondialdehid sebagai
produk oksidasi. Ketidakseimbangan
produksi oksidan (radikal bebas) dan antioksidan akan menimbulkan keadaaan yang disebut stres oksidatif (oxidative
stress), yang dalam waktu tertentu akan
menyebabkan kerusakan sel/jaringan
telinga tengah.
H2O2 dilaporkan dapat memperlambat aktivitas gerak silia, meningkatkan
permeabilitas membran dan meningkatkan sekresi mukus. Perlambatan gerak silia di
tuba Eustachius dan telinga tengah (TT) dapat menimbulkan OME. Lebih jauh, kerusakan DNA sel dan proteinnya dapat menyebabkan kerusakan struktur silia sel,
menghambat regenerasi seluler,
mengganggu sintesa enzim antioksidan dan glutation. Semua hal ini tentu akan semakin memperberat kerusakan jaringan di tuba Eustachius dan telinga tengah. Kemotaksis netrofil juga menurun pada penderita OME. Ini dipikirkan akibat penghambatan mediator oleh produk oksidasi atau defisiensi antioksidan.4
Pada otitis media supuratif akut (OMA), H2O2 juga diproduksi oleh lekosit
polimorfonuklear dan Streptococcus
penelitian terhadap lipoperoksidasi yang terjadi pada otitis media. Reaksi peroksidasi radikal bebas dan H2O2 pada lipid membran sel (lipoperoksidasi) akan menghasilkan lipid hidroperoksida. Produk oksidasi ini diukur pada guinea pig, setelah telinga tengahnya diinjeksi dengan suspensi
Streptococcus pneumonia. Hasilnya pada hari kelima, muncul tanda-tanda otitis media dan nilai lipoperoksidasi mencapai titik tertinggi dari rentang 30 hari
pengukuran. Kesimpulannya adalah
lipoperoksidasi berperan dalam terjadinya peradangan telinga tengah akibat infeksi.
Staphylococcus aureus sebagai salah satu kuman penyebab otitis media, dapat dibunuh oleh netrofil yang menghasilkan H2O2. Senyawa ini akan masuk ke dalam sel bakteri dan bereaksi dengan ion besi (Fe++), melalui reaksi Fenton membentuk radikal hidroksil (OH-) yang akan
membunuh bakteri tersebut.17
Obat aminoglikosida yang diberi pada otitis media memiliki efek ototoksik. Mekanisme yang dapat dijelaskan, yaitu kation aminoglikosida dalam telinga akan berikatan dengan ion membran sel rambut luar dan diinternalisasi. Dalam sel ikatan ini bereaksi dengan besi dan akan merangsang O2 membentuk O2-, yang selanjutnya dengan SOD akan membentuk H2O2. Senyawa ini akan dipecah melalui
reaksi Fenton membentuk OH- yang sangat radikal.18
Pemberian hidrogen peroksida sebagai tetes telinga
Pemberian H2O2 sebagai tetes telinga telah lama dilakukan. Secara klinis senyawa ini berguna untuk menghancurkan serumen, mengobati telinga berair dan
membersihkan tuba ventilasi yang
tersumbat. Di samping itu, ia juga mempunyai efek yang merugikan, yaitu merusak epitel neurosensori koklea, berdasarkan penelitian pada guinea pig. Perez2 mencoba membuktikan lagi pada tikus pasir yang diberi H2O2 topikal telinga, dibandingkan larutan salin, lalu diukur dengan vestibuler evoked potential (VsEPs) dan auditory brainstem response (ABR). Hasilnya H2O2 meningkatkan ambang alat bantu dengar (ABR) secara bermakna
laporan Clerici, bahwa H2O2 menyebabkan
pemendekkan sel rambut luar dan
pembentukan bleb. Percobaan melalui penyuntikan langsung ke dalam koklea
guinea pig ini telah mempengaruhi stimuli akustik pada sel rambut koklea.
Berbeda dengan ini, beberapa penelitian menunjukkan H2O2 tidak memberi efek ototoksik pada binatang percobaan. Nader19
memberikan H2O2 3% dibandingkan
dengan larutan salin pada chinchillas.
Larutan ini diberi sebanyak 2 ml, didiamkan selama lima menit lalu dialirkan keluar pada telinga chinchillas yang dipasang tuba ventilasi, dan diberi berturut-turut selama tujuh hari. Hasil pengukuran ABR pada hari ke-1 dan ke-5 menunjukkan peningkatan ambang dengan perbedaan yang tidak bermakna. Disimpulkan bahwa H2O2 yang diberi sesuai standar klinik, tidak memberi efek ototoksik pada telinga
chinchillas. Hal ini berkorelasi dengan laporan Brenman et al pada tahun 1986, seperti yang dikutip Nader,19 bahwa H2O2 efektif dalam membersihkan tuba ventilasi
manusia tanpa mengganggu sistem
pendengaran perifer. Nader19 mengutip laporan Westine, bahwa H2O2 tidak lebih efektif dari air dalam membersihkan tuba ventilasi yang tersumbat dengan cairan efusi, khususnya mukoid. Spekulasi mereka bahwa H2O2 lebih efektif dalam melarutkan darah yang menyumbat tuba tersebut,
karena darah mengandung enzim katalase yang akan merubahnya menjadi air.
Di banyak tempat, H2O2 digunakan
sebagai pelarut/pembersih serumen.
Chyuan20 dari RS Gleneagles, Singapura bikarbonat 10% paling efektif dalam
melarutkan serumen. Paparella21
mengatakan bahwa pemberian H2O2 akan
menimbulkan gelembung-gelembung
oksigen dan air yang membasahi telinga dan melunakkan serumen. Hal yang sama juga diterapkan oleh para ahli dari Universitas California dan Arizona Utara dengan memberi H2O2 tetes telinga sebanyak 2-3 kali sehari. Menurut Hain TC,22 H2O2 hanya bekerja baik pada
serumen yang tidak terlalu banyak. Mereka juga menyarankan untuk tidak memberi cairan apapun, termasuk H2O2 pada infeksi telinga dengan perforasi membran timpani. Beberapa penulis menyarankan H2O2 diberi pada otitis eksterna dengan krusta atau debris yang keras atau sekret yang cukup kental.22,23
DISKUSI
di alam atau dapat disintesis secara kimia, danmemiliki sifat fisik dan kimia tertentu. H2O2 tersedia dalam beberapa konsentrasi. Semakin tinggi konsentrasi, semakin tinggi
oxidizer class, corrosive dan
unstable/reactive class. Konsentrasi yang paling banyak dipakai di bidang kesehatan adalah 3%. H2O2 memiliki efek yang merugikan pada mata, mukosa dan kulit.
H2O2 bersama dengan ion oksigen dan radikal bebas, termasuk dalam reactive oxygen species (ROS). ROS adalah oksigen produk metabolisme normal dalam sel tubuh yang bersifat sangat reaktif. H2O2 sendiri bukan suatu radikal bebas. Sumber utama H2O2 sel adalah mitokondria.
Bakteri juga menghasilkan H2O2, di
antaranya Streptococcus pyogenes,
Streptococcus pneumonia, Streptococcus
viridans, Streptococcus group B dan C,
Lactobacillus, serta Pneumonoccus. H2O2 yang dihasilkan suatu bakteri merupakan faktor virulensi yang penting untuk merusak jaringan tubuh manusia, dan juga dapat menghambat pertumbuhan bakteri lainnya. H2O2 bersifat bakterisidal dan dihasilkan oleh lekosit fagositik, seperti netrofil dan makrofag, melalui proses yang disebut oxidative burst atau respiratory burst.
H2O2 menyebabkan peningkatan
permeabilitas melalui regulasi VEGF. Di membran sel, ia akan menyebabkan
penghambatan transpor anion, merangsang aktivitas pompa natrium-kalium membran sel. H2O2 dianggap berperan dalam proses infeksi di telinga, baik secara langsung atau lewat produk dismutasi yang dihasilkannya. H2O2 dapat memperlambat aktivitas gerak
silia, meningkatkan permeabilitas
membran, meningkatkan sekresi mukus, akhirnya kerusakan DNA dan kematian sel.
Disimpulkan bahwa H2O2 dapat digunakan untuk menghancurkan serumen, mengobati telinga dengan krusta pada otitis eksterna dan membersihkan tuba ventilasi yang tersumbat. Namun demikian, perlu kehati-hatian dalam memberi H2O2 untuk mengobati telinga dengan perforasi membran timpani.
DAFTAR PUSTAKA
1. US peroxide. Introduction to hydrogen
peroxide. [database on the internet].
Atlanta: c2008 - [cited 2009 Jul 15].
Available from:
http://www.h2o2.com/intro/overview.html.
2. Perez R, Freeman S, Cohen D, Sichel JY,
Sohmer H. The effect of hydrogen peroxide
applied to the middle ear on inner ear
function. Laryngoscope 2003; 113:2042-6.
3. Takoudes TG, Haddad J. Evidence of
oxygen free radical damage in human otitis
media. Otolaryngol Head Neck Surg 1999;
120 (5):5:638-42.
4. Yilmaz T, Kocan EG, Besler HT, Yilmaz
antioxidants in otitis media with effusion in
children. Otolaryngol Head Neck Surg
2004; 131(6):797-803.
5. Nindl G. Hydrogen peroxide from
oxidative stressor to redox regulator. Cell
Sci Rev 2004; 1(2):1-12.
6. Williams DG. The many benefits of
hydrogen peroxide. Family Health News
[homepage on the internet]. c2003 [updated
2003 Jul 17; cited 2007 Nov 8]. Available
8. Campbell K. Ototoxicity: understanding
oxidative mechanisms. J Am Acad Audiol
2003; 14(3):121-3.
9. Bowler RP, Crapo JD. Oxidative stress in
airways. Am J Respir Crit Care Med 2002;
166:38-43.
10. Seki M, Iida K, Saito M, Nakayama H,
Yoshida S. Hydrogen peroxide production
in streptococcus pyogenes: involvement of
lactate oxidase and coupling with aerobic
utilization of lactate. J Bacteriology 2004;
186(7):2046-51.
11. Pericone CD, Overweg K, Hermans PWM,
Weiser JN. Inhibitory and bactericidal
effects of hydrogen peroxide production by
Streptococcus pneumonia on other
inhibitans of the upper respiratory tract.
Infect Immun 2000; 68(7):3390-7.
12. Bolm M, Jansen WTM, Schnabel R,
Chhatwal GS. Hydrogen peroxide mediated
killing of caenorhabditis elegans: a
common feature of different streptococcal
species. Infect Immun 2004; 72(2):1192-4.
13. Goswami M, Mangoli SH, Jawali N.
Involvement of reactive oxygen species in
the action of ciprofloxacin against
Escherichia coli. Antimicrob Agents
Chemother 2006; 50(3):949-54.
14. Okayama N, Kevil CG, Correia L, Heuil
DJ, Itoh M, Grisham MB, et al. Nitric
oxide enhance hydrogen peroxide-mediated
endothelial permeability in vitro. Am J
Physiol Cell Physiol 1997; 273(5):1581-7.
15. Lee KS, Kim SR, Park SJ, Park HS, Min
KH, Lee MH, et al. Hydrogen peroxide
induced vascular permeability via
regulation of vascular endothelial growth
factor. Am J Respir Cell Mol Biol 2006;
35:190-7.
16. Himes JAL, Gallin JI. Immunodeficiency
diseases caused by defects in phagocytes. N
Engl J Med 2000; 343:1703-14.
17. Haddad J. Lipoperoxidation as a measure
of free radical injury in otitis media.
Laryngoscope 1998; 108:524-30.
18. Repine JE, Fox RB, Berger EM. Hydrogen
peroxide kills Staphylococcus aureus by
reacting with staphylococcal iron to form
hydroxyl radical. J Biol Chem 1981;
256(14):7094-6.
19. Nader M, Kourelis M, Daniel SJ. Hydrogen
peroxide ototoxicity in unblocking
Otolaryngol Head Neck Surg 2007;
136(2):216-20.
20. Chyuan HS. Earwax [homepage on the
internet]. Chinnese: Huang Ear Nose
Throat Surgery, Inc; c2008 [updated 2009
Jan 10; cited 2009 March 26]. Available
from:
http://www.entsurgery.com.sg/index.php?
21. Paparella M. Earwax [homepage on the
internet]. Minnesota: Paparella Ear Head &
Neck Institute; c2008 [update 2008 Jul 14;
cited 2008 Nov 9]. Available from:
http://www.pehni.com/patient_ed/earwax.h
tm.
22. Hain TC. Ear wax [homepage in the
internet]. Chicago: American Hearing Research Foundation; c2004 [updated 2008
Aug 20; cited 2008 Dec 7]. Available from:
http://www.american-hearing.org/disorders/hearing/ear_wax.html
.
23. Sander R. Otitis externa: a practical guide
to treatment and prevention. Am Fam