Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu BAB II
KAJIAN PUSTAKA
A. Multimedia dalam Pendidikan
Seiring dengan perkembangan teknologi informasi yang sangat cepat, berbagai perubahan dalam masyarakat yang semakin terbuka dan memiliki kompetisi yang tinggi, menuntut adanya peningkatan kualitas pendidikan. Kenyataan ini memerlukan kesiapan sumber daya manusia yang mampu berkompetisi dalam masyarakat global. Dengan demikian, pengembangan program pendidikan dengan standar mutu bertaraf global menjadi suatu kebutuhan yang tidak bisa terelakkan.
Kehadiran multimedia sebagai salah satu produk teknologi informasi dan komunikasi (TIK) di bidang pendidikan disambut gembira, karena peranannya dalam membantu mencapai tujuan pendidikan. Pendidikan bertujuan untuk mengoptimalkan kemampuan peserta didik dan membantu mengembangkan kemampuan yang sempurna baik fisik, intelektual, maupun emosionalnya. Potensi kemampuan yang dimiliki manusia ini hampir tidak terbatas. Namun hanya sebagian kecil saja dari potensi tersebut yang telah dikembangkan. Metoda dan media yang tepat untuk mengembangkan kemampuan tersebut sangatlah diperlukan.
Secara etimologis multimedia berasal dari kata “multi” (Bahasa Latin, yang berarti banyak, bermacam-macam), dan “medium” (Bahasa Latin, yang berarti sesuatu yang dipakai untuk menyampaikan atau membawa sesuatu). Multimedia
merupakan perpaduan antara berbagai media (format file) yang berupa teks, gambar, grafik, suara, animasi, video, interaksi, dan lain-lain yang telah dikemas menjadi file digital (komputerisasi), digunakan untuk menyampaikan pesan kepada publik. (Ariani dan Haryanto, 2010).
Teknologi multimedia diharapkan mampu mengatasi kendala dalam proses belajar mengajar dengan dikemasnya program-program pendidikan dalam media berbasis TIK. Meskipun Gagne dalam Munir (2010) menyatakan, bahwa tidak ada satu media yang sempurna yang dapat memenuhi semua keperluan yang diinginkan. Usaha yang maksimal untuk menjadikan produk TIK ini menjadi media yang dapat mengoptimalkan manusia, kiranya perlu terus diupayakan dan dikembangkan.
Hamalik (dalam Arsyad, 2005) mengemukakan bahwa pemakaian media pembelajaran dalam proses belajar mengajar dapat membangkitkan keinginan dan minat yang baru, membangkitkan motivasi dan rangsangan kegiatan belajar, dan bahkan membawa pengaruh-pengaruh psikologis terhadap siswa. Kemp dan Dayton (dalam Susilana dan Riyana, 2008) mengemukakan kontribusi media pembelajaran, yaitu :
a. Penyampaian pesan pembelajaran dapat lebih terstandar b. Pembelajaran dapat lebih menarik
c. Pembelajaran menjadi lebih interaktif dengan menerapkan teori belajar d. Waktu pelaksanaan pembelajaran dapat diperpendek
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
f. Proses pembelajaran dapat berlangsung kapanpun dan dimanapun diperlukan
g. Sikap positif siswa terhadap materi pembelajaran serta proses pembelajaran dapat ditingkatkan
h. Peran guru berubah kearah yang positif
Penelitian Jacobs dan Schade dalam Munir (2010) menunjukkan bahwa daya ingat orang yang hanya membaca saja memberikan persentase terendah, yaitu 1%. Daya ingat ini dapat ditingkatkan hingga 25%-30% dengan bantuan media lain, seperti televisi. Daya ingat makin meningkat dengan penggunaan media 3 dimensi seperti multimedia, hingga 60%. Ditemukan pula, bahwa multimedia memiliki kemampuan menampilkan konsep 3D (tiga dimensi) secara efisien dan efektif dengan kurikulum pembelajaran yang dirancang secara sistematik, komunikatif, dan interaktif sepanjang proses pembelajaran.
Multimedia juga merupakan media pengajaran dan pembelajaran yang efektif dan efisien berdasarkan kemampuannya menyentuh berbagai panca indera: penglihatan, pendengaran, dan sentuhan, sebagaimana dikemukakan oleh Schade dalam Munir (2010) : “Multimedia improves sensory stimulation, particulary due to the inclusion of interactivity”.
Sebagaimana media pendidikan lainnya, multimedia tetap berfungsi sebagai alat, metoda dan pendekatan yang digunakan untuk menjalin komunikasi antara guru dengan pelajar selama proses belajar mengajar. Kemampuan multimedia memberikan
pengajaran secara individu melalui sistem tutor pribadi karena kemampuan multimedia dalam mengulang informasi. Jika peserta didik kurang paham terhadap materi yang disajikan, ia dapat melihat kembali program multimedia secara berulang hingga memahaminya. Bagi pelajar, penggunaan multimedia dapat lebih memacu motivasi belajar, dapat memberikan penjelasan yang lebih baik dan lengkap terhadap sesuatu permasalahan, memudahkan untuk mengulang pelajaran, mengadakan latihan dan mengukur kemampuan, karena multimedia memberi peluang kepada pelajar untuk berinteraksi dengan program yang disajikan. Dengan demikian, kehadiran multimedia dalam proses belajar mengajar menjadi sangat dirasakan manfaatnya. Bagi perencana program multimedia perlu mendalami desain proses belajar mengajar agar program multimedia yang disusun lebih terarah dan sistematis sesuai dengan tujuan pengajaran yang ditetapkan.
Multimedia bukan satu-satunya penentu keberhasilan belajar. Faktor lain yang perlu juga diperhatikan diantaranya motivasi pelajar, keadaan sosial, ekonomi dan pendidikan keluarga, situasi pada saat proses belajar, kurikulum dan guru.
Multimedia mempunyai beberapa keistimewaan yang tidak dimiliki media lain. Di antara keistimewaan itu adalah :
1. Multimedia menyediakan proses interaktif dan memberikan kemudahan umpan balik.
2. Multimedia memberikan kebebasan kepada pelajar dalam menentukan topik proses pembelajaran.
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
3. Multimedia memberikan kemudahan kontrol yang sistematis dalam proses pembelajaran.
(Munir, 2010)
B. Literasi Sains
Literasi sains atau scientific literacy didefinisikan PISA (Programme for International Student Assessment) sebagai kapasitas siswa untuk menggunakan pengetahuan ilmiah, mengidentifikasi pertanyaan dan untuk menarik kesimpulan berdasarkan bukti-bukti agar dapat memahami dan membantu membuat keputusan (OECD, 2009). Tidak jauh beda dengan definisi tersebut, studi PISA Nasional 2006 mendefinisikan literasi sains sebagai kemampuan menggunakan pengetahuan sains, mengidentifikasi pertanyaan, dan menarik kesimpulan berdasarkan bukti-bukti, dalam rangka memahami serta membuat keputusan berkenaan dengan alam dan perubahan yang dilakukan terhadap alam melalui aktivitas manusia. Penilaian literasi sains dalam PISA tidak semata-mata berupa pengukuran tingkat pemahaman terhadap pengetahuan sains, tetapi juga pemahaman terhadap berbagai aspek proses sains, serta kemampuan mengaplikasikan pengetahuan dan proses sains dalam situasi nyata yang dihadapi peserta didik (Firman, 2007).
PISA mengidentifikasi tiga dimensi besar literasi sains, yakni proses sains, konten sains, dan konteks aplikasi sains. Proses sains merujuk pada proses mental yang terlibat ketika menjawab pertanyaan atau memecahkan masalah, seperti
mengidentifikasi dan menginterpretasi bukti serta menerangkan kesimpulan. Konten sains merujuk kepada konsep-konsep kunci yang diperlukan untuk memahami fenomena alam dan perubahan yang dilakukan terhadap alam melalui aktivitas manusia. Konteks aplikasi sains merujuk pada situasi dalam kehidupan sehari-hari yang menjadi lahan bagi aplikasi proses dan pemahaman konsep sains, misalnya kesehatan dan gizi dalam konteks pribadi serta iklim dalam konteks global (Firman, 2007).
1. Aspek Konteks Literasi sains
Konteks literasi sains dalam PISA lebih pada kehidupan sehari-hari daripada kelas atau laboratorium. Sebagaimana dengan bentuk-bentuk literasi lainnya, konteks melibatkan isu-isu yang penting dalam kehidupan secara umum seperti juga terhadap kepedulian pribadi. PISA Nasional 2009 membagi bidang aplikasi sains ke dalam lima kelompok, yakni kesehatan, sumber daya alam, lingkungan, bahaya, dan penemuan baru.
2. Aspek Konten Sains
Konten (pengetahuan) sains merujuk pada konsep-konsep kunci yang diperlukan untuk memahami fenomena alam dan perubahan yang dilakukan terhadap alam melalui aktivitas manusia. Dalam hal ini, PISA mendeskripsikan agar siswa mampu mengaplikasikan pengetahuan dalam konteks yang terkait dengan kehidupannya, dan soal-soal PISA hanya mencakup sampel pengetahuan sains, maka PISA menentukan kriteria pemilihan konten sains sebagai berikut: relevan dengan
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
kehidupan nyata, merupakan pengetahuan penting sehingga penggunaannya berjangka panjang, sesuai untuk tingkatan perkembangan anak usia 15 tahun.
3. Aspek Proses Sains
PISA menetapkan tiga aspek dari komponen proses (atau kompetensi sains) dalam penilaian literasi sains yakni mengidentifikasi pertanyaan ilmiah, menjelaskan fenomena secara ilmiah, dan menggunakan bukti ilmiah. (OECD, 2009).
CITO (Citogroep, dalam Witte dan Beers, 2003) menyatakan bahwa di dalam ujian-ujian nasional sains di Belanda bentuk pertanyaan dapat didasarkan pada sebuah konteks, untuk contoh diperkenalkan dalam bentuk suatu bagian dari sebuah artikel koran, iklan leaflet, label dengan informasi produk, suatu informasi leaflet cara penggunaan dari sebuah obat, suatu cetakan dari sebuah internet, suatu artikel ilmiah, bagian dari sebuah buku komik, dan sebuah cerita. Konteks tersebut dapat berupa sebuah proses industri, sebuah problem lingkungan, sebuah masalah dalam kehidupan sehari-hari, sebuah masalah ilmiah, dan masalah sekolah.
Dalam literasi sains terdapat berbagai kompetensi dalam setiap domain (pengetahuan, keterampilan serta sikap dan nilai) yang saling berhubungan dan saling mendukung. Rumusan kompetensi tersebut dihasilkan berdasarkan diskusi kelompok IPN (Institüt für Pädagogik der Naturwiscenschaft) (Nentwig et al., 2002) seperti dapat dilihat pada Gambar 2.1.
Literasi Sains Kompetensi Etika Kompetensi Mata Pelajaran Kompetensi Epistemologi Kompetensi Belajar Kompetensi Komunikasi
Pengetahuan Karakter (Nilai
Kompetensi mata pelajaran meliputi pengetahuan yang bersifat konseptual dan pengungkapan, meliputi rangkaian pengetahuan sains dan pemahaman menyeluruh dari berbagai ranah sains. Kompetensi epistemologi meliputi pengertian mendalam tentang pendekatan sains yang sistematis sebagai satu cara untuk melihat dunia, dibandingkan dengan teknologi, seni rupa, agama, dan lain lain.
Kompetensi belajar meliputi kemampuan untuk menggunakan strategi belajar yang berbeda dan cara mengkonstruksi pengetahuan sains. Kompetensi sosial meliputi kemampuan untuk bekerjasama dalam tim untuk mengumpulkan, menghasilkan, memproses atau menginterpretasikan secara ringkas, untuk menggunakan informasi ilmiah. Kompetensi berkomunikasi meliputi kemampuan dalam menggunakan dan memahami bahasa ilmiah, pelaporan, membaca dan berargumen akan informasi ilmiah.
Gambar 2.1. Model Pembagian Kompetensi dalam Literasi Sains
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
Kompetensi sikap/etika meliputi pengetahuan norma-norma, pemahaman tentang relativitas norma-norma pada waktu dan lokasinya, dan kemampuan untuk mencerminkan norma-norma dan mengembangkan nilai hierarki.
C. Pembelajaran Berbasis Literasi Sains
Pembelajaran berbasis literasi sains merupakan pembelajaran yang didasarkan pada pengembangan kemampuan pengetahuan sains di berbagai sendi kehidupan, mencari solusi permasalahan, membuat keputusan, dan meningkatkan kualitas hidup (Holbrook dan Rannikmae dalam Holbrook, 1998). Tujuan pengembangan pembelajaran berbasis literasi sains adalah mengembangkan kemampuan kreatif dengan menggunakan pengetahuan berikut cara kerjanya di dalam kehidupan sehari-hari dan untuk memecahkan masalah serta membuat keputusan yang dapat meningkatkan mutu kehidupan (Holbrook dan Rannikmae dalam Holbrook 1998). Karakteristik pembelajaran berbasis literasi sains adalah:
1. Literasi sains lebih dari sekedar pengetahuan dan sarana pengetahuan. 2. Literasi sains lebih dari sekedar aplikasi sains atau pengembangan sikap
positif terhadap sains.
3. Pada dasarnya, literasi sains tidak hanya berbicara mengenai sains, melainkan cara memperoleh pendidikan yang berarti melalui sains.
4. Pengajaran literasi sains merupakan pembelajaran yang menyenangkan, mendapat penghargaan perkembangan sains dan kesadarannya.
(Hoolbrok, 1998) Penerapan pembelajaran berbasis literasi sains dapat dilakukan dengan mengadopsi, mengadaptasi, dan memodifikasi tahapan-tahapan pembelajaran yang dikemukakan oleh Nentwig et al. (2002) yang disesuaikan dengan kriteria pembelajaran berbasis literasi sains (Holbrook, 1998) sebagai berikut.
1. Tahap Kontak (Contact Phase)
Pada tahap awal ini dikemukakan isu-isu atau masalah-masalah yang ada di masyarakat atau menggali berbagai peristiwa yang terjadi di sekitar siswa yang dapat bersumber dari berita, artikel, atau pengalaman siswa sendiri. Topik tersebut kemudian dikaitkan dengan materi yang akan dipelajari. Dengan begitu siswa diharapkan menyadari pentingnya memahami materi tersebut.
2. Tahap Kuriositi (Curiosity Phase)
Pada tahap ini dikemukakan permasalahan berupa pertanyaan-pertanyaan yang dapat mengundang rasa penasaran dan keingintahuan siswa. Pertanyaan ini berkaitan dengan isu atau masalah yang telah dibicarakan dan untuk mampu menjawabnya, siswa memerlukan pengetahuan dari materi yang akan dipelajari.
3. Tahap Elaborasi (Elaboration Phase)
Pada tahap ini dilakukan eksplorasi, pembentukan dan pemantapan konsep sampai pertanyaan pada tahap kuriositi dapat terjawab. Eksplorasi, pembentukan dan
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
pemantapan konsep tersebut dapat dilakukan dengan berbagai metode, misalnya ceramah bermakna, diskusi dan kegiatan praktikum, atau gabungan dari ketiganya. Melalui kegiatan inilah berbagai kemampuan siswa akan tergali lebih dalam, baik aspek pengetahuan, keterampilan proses, maupun nilai dan sikap.
4. Tahap Pengambilan Keputusan (Decision Making Phase)
Pada tahap ini dilakukan pengambilan keputusan bersama dari permasalahan yang dimunculkan pada tahap kuriositi. Dengan begitu, penyelesaian dari permasalahan yang muncul tersebut jelas dan benar-benar dapat dipahami oleh siswa tanpa ada keraguan.
5. Tahap Nexus (Nexus Phase)
Pada tahap ini dilakukan proses pengambilan intisari (konsep dasar) dari materi yang dipelajari (dekontekstualisasi), kemudian mengaplikasikannya pada konteks yang lain (rekontekstualisasi), artinya masalah yang sama diberikan dalam konteks yang berbeda dimana memerlukan konsep pengetahuan yang sama untuk pemecahannya (Nentwig et al., 2002). Tahap ini dilakukan agar pengetahuan yang diperoleh lebih aplikatif dan bermakna, tidak hanya di dalam konteks pembelajaran tetapi juga di luar konteks pembelajaran.
Teknologi Nano adalah ilmu dan rekayasa dalam penciptaan material, struktur fungsional, maupun piranti dalam skala nanometer. Dalam terminologi ilmiah, nano berarti satu per satu milyar (0,000000001). Satu nanometer adalah seper seribu mikrometer, atau seper satu juta milimeter, atau seper satu milyar meter. Jika panjang pulau jawa dianggap satu meter, maka diameter sebuah kelereng kira-kira sama dengan 10 nanometer. (Abdullah, 2009)
Yang dapat dikelompokkan dalam skala nanometer adalah ukuran yang lebih kecil dari 100 nm. Orang menyebut nanopartikel jika diameter partikel tersebut kurang dari 100 nanometer. Namun, riset nanosains tidak hanya terbatas pada nanopartikel, tetapi lebih luas ke material nanostruktur. Material nanostruktur adalah material yang tersusun atas bagian-bagian kecil, di mana tiap-tiap bagian berukuran kurang dari 100 nanometer, walaupun ukuran material secara keseluruhan cukup besar. tetapi dalam ukuran tersebut sifat bagian-bagian kecil harus tetap dipertahankan.
Memasuki tahun 2000, riset material skala nanometer memasuki babak paling progresif. Penemuan baru dalam bidang ini muncul hampir tiap minggu dan aplikasi-aplikasi baru mulai tampak dalam berbagai bidang, seperti:
1. elektronik: pengembangan piranti (device) ukuran nanometer,
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
3. kimia: pengembangan katalis yang lebih efisien, dan baterai yang kualitasnya lebih baik,
4. kedokteran: pengembangan peralatan baru pendeteksi sel kanker dengan partikel berukuran nanometer,
5. kesehatan: pengembangan obat-obatan dengan ukuran bulir beberapa nanometer sehingga dapat melarut dengan cepat dalam tubuh dan bereaksi lebih cepat, serta pengembangan obat pintar yang bisa mencari sel-sel tumor dalam tubuh dan langsung mematikan sel tersebut tanpa mengganggu sel-sel normal,
6. lingkungan: penggunaan partikel skala nanometer untuk menghancurkan polutan organik di air dan udara, dan sebagainya.
Mengapa reduksi ukuran material dalam skala nanometer menjadi begitu penting? Sifat-sifat material yang meliputi sifat-sifat fisis, kimiawi, maupun biologi berubah begitu dramatis ketika dimensi material masuk ke skala nanometer. Yang lebih menarik lagi adalah sifat-sifat tersebut ternyata bergantung ukuran, bentuk, kemurnian permukaan, maupun topologi material. Para ilmuwan percaya bahwa setiap sifat memiliki “skala panjang kritis”. Ketika dimensi material lebih kecil dari panjang tersebut maka sifat fisis fundamental mulai berubah. Sebagai gambaran, partikel tembaga yang memiliki diameter 6 nm memperlihatkan kekerasan lima kali lebih besar daripada tembaga yang berukuran lebih besar daripada 100 nm. Keramik
yang umumnya kita kenal mudah pecah dapat dibuat menjadi fleksibel jika ukuran bulir direduksi ke dalam orde nanometer.
E. Grafena
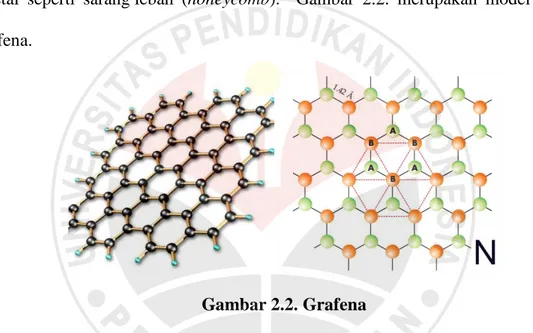
Grafena merupakan alotrop karbon yang berbentuk lembaran datar tipis di mana setiap atom karbon memiliki ikatan sp2 dan dikemas rapat dalam bentuk kisi kristal seperti sarang lebah (honeycomb). Gambar 2.2. merupakan model struktur grafena.
Gambar 2.2. Grafena
Jika karbon ini disusun ke samping menyerupai sarang lebah (honeycomb), diyakini menjadi bahan semi konduktor terbaik. Lembar grafena telah dimanfaatkan untuk pembuatan chip komputer. Tidak hanya untuk industri nanoelektronik, grafena menjadi material terkuat, yang akan memicu perkembangan industri kendaraan, pesawat terbang, LCD, dan bahan antariksa.
Nama grafena berasal dari GRAPHITE + -ENE; grafit sendiri terdiri dari banyak lembaran grafena yang ditumpuk secara bersama. Pada tahun 2010 Andre
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
Geim dan Konstantin Novoselov mendapat hadiah Nobel di bidang kimia karena karyanya dalam mengembangkan grafena 2 dimensi.
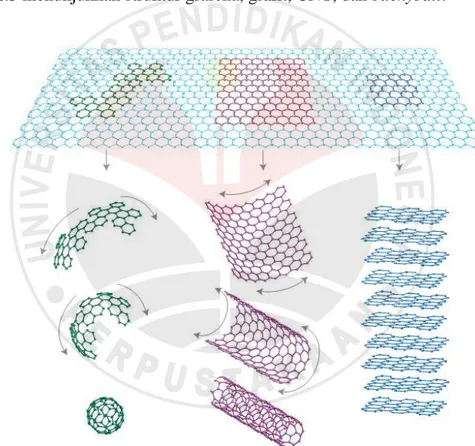
Ikatan karbon-karbon pada grafena adalah sekitar 0,142 nm. Grafena merupakan unsur struktur dasar dari alotrop karbon, meliputi grafit, tabung nano karbon, dan fulerena, yang biasa dikenal sebagai mother of all graphitic forms. Gambar 2.3 menunjukkan struktur grafena, grafit, CNT, dan buckyball.
Grafena merupakan bahan yang paling kuat yang diketahui oleh manusia menurut penelitian yang dikeluarkan oleh Universitas Columbia pada Augustus 2008. Grafena bersifat kuat, elastis, dan transparan, sebagaimana ditunjukkan pada Gambar
3. Namun, proses pemisahan grafena dari grafit masih memerlukan pengembangan teknologi lainnya sebelum ia cukup ekonomis untuk digunakan pada proses industri.
Gambar 2.4. LembarGrafena 1. Pembuatan Grafena Skala Industri
Secara industri, lembar grafena dihasilkan dengan metode reduksi oksidasi (redoks) silikon karbida (SiC) dengan cara memanaskan silikon karbida pada suhu 1100 derajat Celcius. Atom silikon akan menguap sedangkan atom karbon tersisa dan mengatur diri menjadi grafena. Senyawa silikon karbida (SiC) sendiri dihasilkan dari reaksi antara silikon dioksida (SiO2) dan karbon (C). Di Negara kita daerah penghasil senyawa SiO2terdapat di Sumatera Barat, Kalimantan Barat, Jawa Barat, Sumatera Selatan, Kalimantan Selatan, dan Pulau Bangka dan Belitung. Senyawa SiO2 di alam salah satunya berbentuk pasir kuarsa yang merupakan gabungan dari SiO2, Fe2O3, Al2O3, TiO2, CaO, MgO, dan K2O.
Selain menggunakan metode redoks, secara industri grafena juga dapat dihasilkan dengan cara reduksi hidrazin. Hidrazin merupakan suatu senyawa kimia
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
yang mengandung nitrogen (N) dan hidrogen (H) yang akan mereduksi kertas grafit oksida menjadi grafena berlapis tunggal. Kertas grafit oksida direndam dalam larutan hidrazin (N2H4) murni.
Grafena dapat disintesis dalam jumlah gram, yaitu dengan mereduksi etanol oleh logam natrium (Na), diikuti dengan pirolisis produk etoksida, kemudian mencucinya dengan air untuk menghilangkan garam-garam natrium.
Selain itu, lembaran grafena dapat dihasilkan dengan preparasi di laboratorium melalui modifikasi kimia dari grafit. Secara lebih terinci prosesnya adalah : mikrokristalin grafit direaksikan dengan campuran asam, yaitu asam sulfat (H2SO4) dan asam nitrat (HNO3). Serangkaian tahap-tahap meliputi oksidasi, hasil pengelupasannya berupa plat kecil dari grafena dengan gugus karboksil pada bagian tepinya. Kemudian, berubah menjadi gugus asam klorida (HCl) dengan penambahan tionyl klorida, kemudian dikonversi menjadi grafena amida yang sesuai dengan cara mentreatment dengan oktadecylamine. Akhirnya dihasilkan meterial berupa lembaran grafena berbentuk lingkaran dengan ketebalan 5,3 Angstrom yang larut dalam tetrahidrofuran, tetraklorometana, dan dikloroetana
2. Cara Memperoleh Grafena Secara Sederhana
Pada tahun 2004 kelompok riset dari Universitas Manchester yang dipimpin oleh Andre K. Geim dan Kostya Novoselov menemukan suatu bahan semikonduktor yang disebut "Graphene". Pada penelitiannya, Andre K. Geim dan Kostya Novoselov menghasilkan grafena dengan teknik selotip “Scotch”.
Fragmen-fragmen kecil lembaran grafena dihasilkan bersamaan dengan serpihan lainnya ketika grafit dikikis, misalnya ketika menggambar garis dengan pensil. Gores-goreskan mata pensil di atas kertas, kemudian tempelkan selotip di bekas goresan, maka akan dihasilkan satu lembar kristal karbon setebal atom tunggal. Penelitian Andre K. Geim dan Kostya Novoselov ini hanya membutuhkan waktu 2 tahun sebelum mereka mendapat Nobel.
3. Sifat Grafena
Grafena merupakan material tertipis dan terkuat yang ada di dunia saat ini.Setiap atom karbon pada grafena memiliki ikatan sp2. Ikatan karbon-karbon pada grafena ini adalah sekitar 0,142 nanometer (nm). Karena grafena berukuran nano, maka memiliki sifat yang jauh lebih kuat dibanding alotrop karbon lainnya (misal : grafit). Grafena juga memiliki sifat : kualitas kristal yang tinggi, transparan, dan konduktivitas listrik yang tinggi.
4. Aplikasi Grafena
Dr Walter de Heer dari Institute of Technology, Georgia, telah memanfaatkan grafena untuk pembuatan cip komputer. Membran grafena itu digunakan untuk membuat cip dengan sifat elektronik lebih baik dibandingkan cip saat ini. De Heer meyakini, secara industrial, grafena akan menjadi bahan semikonduktor hebat, ratusan kali lebih baik, yang menghasilkan komputasi ultracepat.
Tidak hanya dimanfaatkan untuk industri nanoelektronik, grafena yang merupakan material terkuat namun ringan ini akan memicu perkembangan industri kendaraan,
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
pesawat terbang, LCD, dan bahan pesawat antariksa. Di masa depan grafena juga dapat dimanfaatkan untuk pembuatan alat multifungsi yang praktis dan fleksibel.
Aplikasi Grafena yang lain yaitu digunakan sebagai transistor. Selain diaplikasikan pada transistor, grafena juga dapat diaplikasikan sebagai ultrakapasitor. Industri dapat mengurangi energi yang terbuang dengan memasang ultrakapasitor dalam mesin-mesin produksi dan dapat pula diterapkan pada bus, truk dan kereta api. F. Kaitan Konteks Grafena dengan Materi Ikatan Kimia
Bahan-bahan yang digunakan dalam proses pembuatan grafena skala industri, seperti CaO, Hidrazin, SiO2, ataupun logam Na adalah salah satu contoh zat yang dapat digunakan untuk menjelaskan tentang materi ikatan kimia pada kelas X, yaitu tentang ikatan Ion, Ikatan Kovalen, dan Ikatan Logam. Hal tersebut sesuai SK 1 dan KD 1.3 berikut:
1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia
1.3. Membandingkan proses pembentukan ikatan ion, ikatan kovalen, ikatan kovalen koordinasi, dan ikatan logam serta hubungannya dengan sifat fisik senyawa yang terbentuk
Untuk struktur dari grafena yang berbentuk planar dengan hibridisasi sp2 dapat dikaitkan untuk menjelaskan materi ikatan kimia di kelas XI, yaitu tentang hibridisasi. Sedangkan dalam proses pembuatan grafena secara sederhana dengan teknik selotip, dapat dikaitkan untuk menjelaskan materi tentang gaya antar molekul. Hal tersebut berkesesuaian dengan SK 1 dan KD 1.2 serta 1.3 berikut:
1. Memahami struktur atom untuk meramalkan sifat-sifat periodik unsur, struktur molekul, dan sifat-sifat senyawa
1.2. Menjelaskan teori jumlah pasangan elektron di sekitar inti atom dan teori hibridisasi untuk meramalkan bentuk molekul
1.3. Menjelaskan interaksi antar molekul (gaya antar molekul) dengan sifatnya F. Materi Ikatan Kimia
Hampir semua atom membentuk ikatan dengan atom-atom lain. Tetapi ada enam unsur lain yang tidak bersifat demikian, yaitu unsur-unsur gas mulia yang terdiri dari: helium (2He), neon (10Ne), argon (18Ar), krypton (36Kr), xenon (54Xe), dan
radon (86Rn). Unsur-unsur gas mulia hampir tidak membentuk ikatan dengan atom
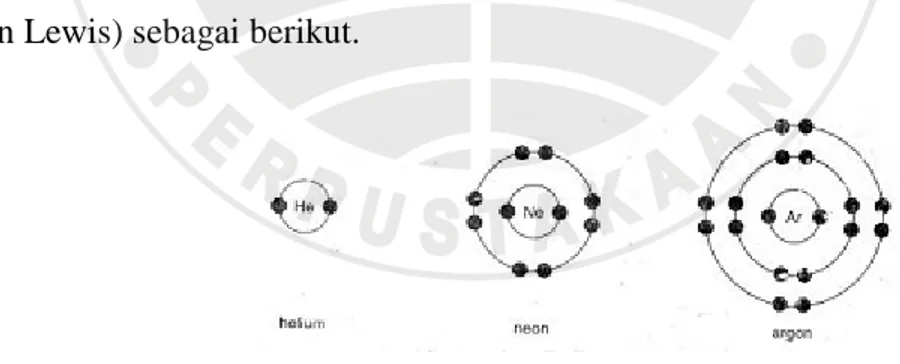
lain dan karena tidak reaktifnya maka sering disebut gas inert. Gas mulia yang paling dikenal adalah helium, neon, dan argon dengan struktur elektron (disebut rumus titik elektron Lewis) sebagai berikut.
Gambar 2.5. Struktur Elektron Helium, Neon, dan Argon
Kecuali helium yang memiliki 2 elektron (duplet), semua gas mulia memiliki 8 elektron (oktet) pada kulit terluarnya. Susunan yang demikian menurut Kossel dan Lewis sangat stabil, sehingga atom-atom gas mulia tidak menerima elektron atau pun
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
melepaskan elektron terluarnya. Hal inilah yang menyebabkan mengapa gas mulia sangat stabil.
Tabel 2.1 Konfigurasi Elektron Unsur-Unsur Gas Mulia
Dengan demikian, dapat disimpulkan bahwa suatu atom yang memiliki konfigurasi elektron serupa dengan gas mulia akan stabil. Dengan kata lain, unsur-unsur yang memiliki konfigurasi elektron tidak mirip dengan konfigurasi elektron gas mulia tidak stabil. Berdasarkan hal itu, Lewis menyatakan bahwa unsur-unsur selain gas mulia dapat mencapai stabil dengan cara bersenyawa dengan unsur lain atau unsur yang sama agar konfigurasi elektron dari setiap atom itu menyerupai konfigurasi elektron gas mulia. Suatu atom dapat mencapai konfigurasi elektron gas mulia dengan cara melepaskan elektron valensi, menangkap elektron, atau menggunakan bersama elektron valensi membentuk pasangan elektron.
1. Ikatan Ion
Senyawa yang dibentuk akibat ikatan ion dinamakan senyawa ion. Ikatan ion biasanya terbentuk akibat adanya serah-terima elektron di antara atom-atom yang berikatan, sehingga konfigurasi elektron dari atom-atom itu menyerupai konfigurasi
elektron gas mulia. Adanya serah-terima elektron menghasilkan atom-atom bermuatan listrik yang berlawanan sehingga terjadi gaya tarik-menarik elektrostatik. Gaya tarik-menarik inilah yang disebut ikatan ion. Atom-atom yang melepaskan elektron valensinya sehingga bermuatan positif disebut kation. Adapun atom-atomyang menangkap elektron sehimgga bermuatan negatif disebut anion.
2. Ikatan Kovalen
Unsur-unsur logam dan bukan logam cenderung membentuk senyawa ion untuk mencapai keadaan stabil. Di alam, banyak senyawa yang terbentuk dari unsur-unsur bukan logam seperti gas oksigen (O2), nitrogen (N2), dan metana (CH4).
Menurut Lewis, atom-atom bukan logam dapat membentuk ikatan dengan atom-atom bukan logam melalui penggunaan bersama pasangan elektron valensinya. Atom-atom bukan logam umumnya berada pada golongan VA–VIIA, artinya atom-atom tersebut memiliki elektron valensi banyak (5–7). Untuk mencapai konfigurasi elektron seperti gas mulia, atom-atom cenderung mengadakan saham (saling menyumbang), setiap atom menyumbang elektron valensi untuk digunakan bersama.
Ikatan yang terbentuk melalui penggunaan bersama pasangan elektron valensi dinamakan ikatan kovalen. Senyawa yang dibentuk dinamakan senyawa kovalen. Untuk menyatakan elektron valensi dalam ikatan kovalen, Lewis menggunakan rumus titik elektron.
2.1. Ikatan KovalenTunggal
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
sepasang elektron (setiap atom memberikan saham satu elektron untuk digunakan bersama).
Contoh:
Atom H dapat berikatan kovalen dengan Cl membentuk HCl. Perhatikan konfigurasi elektron atom H dan Cl berikut.
1H = 1 17Cl = 2 8 7
Agar elektron valensi atom H mirip dengan atom He (2) maka diperlukan satu elektron. Demikian pula atom Cl, agar mirip dengan konfigurasi elektron atom Ar (2 8 8), diperlukan satu elektron. Oleh karena kedua atom tersebut masing-masing memerlukan satu elektron maka cara yang paling mungkin adalah setiap atom memberikan satu elektron valensi untuk membentuk sepasang elektron ikatan. Perhatikan Gambar di bawah ini!
Gambar 2.6 Ikatan antara H dengan Cl
berikut:
Gambar 2.7 Proses Pembentukan Ikatan antara Atom C dan H
Pada CH4, setiap atom H memiliki 2 elektron valensi (seperti He) dan atom
C memiliki 8 elektron valensi (seperti Ne). Dalam molekul CH4 terdapat 4 pasang
elektron ikatan atau 4 ikatan kovalen tunggal. 2.2. Ikatan Kovalen Rangkap
Dalam ikatan kovalen, selain ikatan kovalen tunggal juga terdapat ikatan kovalen rangkap dua dan rangkap tiga. Ikatan kovalen rangkap dua terbentuk dari dua elektron valensi yang disahamkan oleh setiap atom, misalnya pada molekul O2.
Ikatan kovalen rangkap tiga terbentuk dari tiga elektron valensi yang disahamkan oleh setiap atom, misalnya dalam molekul N2.
Konfigurasi elektron atom 8O= 2 6. Atom O akan stabil jika konfigurasi
elektronnya serupa dengan 10Ne=2 8. Agar stabil maka atom O memerlukan 2
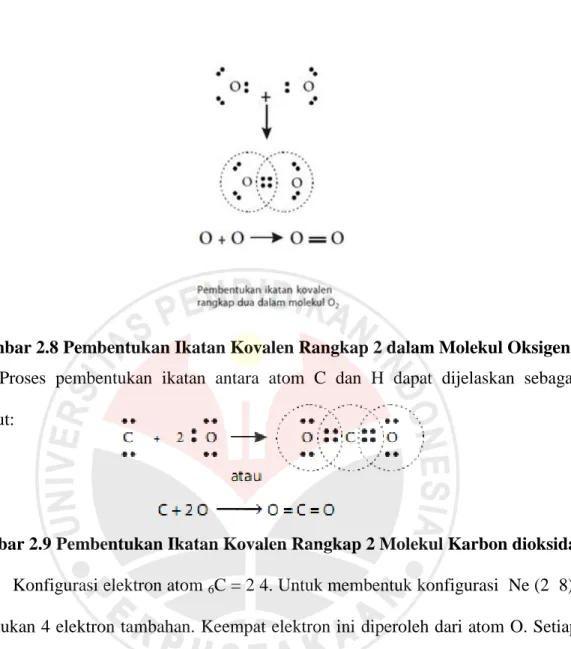
elektron tambahan. Kedua elektron ini diperoleh dengan cara patungan 2 elektron valensi dari masing- masing atom O membentuk ikatan kovalen rangkap dua seperti berikut:
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
Gambar 2.8 Pembentukan Ikatan Kovalen Rangkap 2 dalam Molekul Oksigen Proses pembentukan ikatan antara atom C dan H dapat dijelaskan sebagai berikut:
Gambar 2.9 Pembentukan Ikatan Kovalen Rangkap 2 Molekul Karbon dioksida Konfigurasi elektron atom 6C = 2 4. Untuk membentuk konfigurasi Ne (2 8),
diperlukan 4 elektron tambahan. Keempat elektron ini diperoleh dari atom O. Setiap atom O menyumbang 2 elektron valensisehingga membentuk dua buah ikatan kovalen rangkap dua.
3. Ikatan pada Logam
Ikatan pada logam berbeda dengan ikatan kimia lainnya sebab elektron-elektron dalam kristal logam bergerak bebas. Terdapat beberapa teori yang menerangkan ikatan pada logam, di antaranya adalah teori lautan elektron dan teori
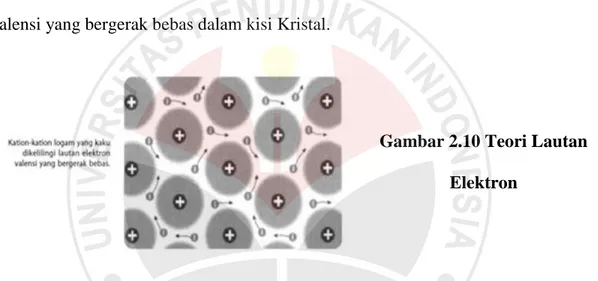
pita. Khusus untuk teori pita tidak dibahas di sini sebab memerlukan pengetahuan tentang ikatan kovalen dengan pendekatan teori Mekanika Kuantum. Teori ikatan logam kali pertama dikembangkan oleh Drude 1902), kemudian diuraikan oleh Lorentz (1916) sehingga dikenal dengan teori elektron bebas atau teori lautan elektron dari Drude-Lorentz. Menurut teori ini, kristal logam tersusun atas kation-kation logam yang terpateri di tempat (tidak bergerak) dikelilingi oleh lautan elektron valensi yang bergerak bebas dalam kisi Kristal.
Elektron-elektron valensi logam bergerak bebas dan mengisi ruang- ruang di antara kisi-kisi kation logam yang bermuatan positif. Oleh karena bergerak bebas, elektron-elektron valensi dapat berpindah jika dipengaruhi oleh medan listrik atau panas. Menurut teori Drude-Lorentz, jika cahaya tampak (visible) jatuh pada permukaan logam, sebagian elektron valensi logam akan tereksitasi. Ketika elektron yang tereksitasi itu kembali ke keadaan dasar akan disertai pembebasan energi dalam bentuk cahaya atau kilap. Peristiwa ini menimbulkan sifat mengkilap pada permukaan logam.
Gambar 2.10 Teori Lautan Elektron
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
Daya hantar listrik pada logam disebabkan oleh adanya elektron valensi yang bergerak bebas dalam kristal logam. Jika listrik dialirkan melalui logam, elektron-elektron valensi logam akan membawa muatan listrik ke seluruh logam dan bergerak menuju potensial yang lebih rendah sehingga terjadi aliran listrik dalam logam.
Jika sejumlah kalor (panas) diserap oleh logam, elektron-elektron valensi logam akan bergerak lebih cepat dan elektron-elektron tersebut membawa sejumlah kalor yang diserap. Akibatnya, kalor dapat didistribusikan oleh logam ke seluruh kristal logam sehingga logam menjadi panas.
Logam memiliki sifat lentur (mudah ditempa, dibengkokkan, tetapi tidak mudah patah). Bagaimana fakta ini dapat dijelaskan? Kisi-kisi kation bersifat kaku (tetap di tempat), sedangkan elektron valensi logam bergerak bebas. Jika logam ditempa atau dibengkokkan terjadi pergeseran kation-kation, tetapi pergeseran ini tidak menyebab- kan patah karena selalu dikelilingi oleh lautan elektron (Sunarya, 2009).
4. Teori Ikatan Valensi dan Hibridisasi 4.1. Prinsip Umum Teori Ikatan Valensi
Menurut teori ikatan valensi, ikatan akan terbentuk antara dua atom jika memenuhi syarat sebagai berikut.
1) Ketika membentuk ikatan, orbital-orbital pada atom pusat mengadakan restrukturisasi melalui proses hibridisasi membentuk orbital hibrida.
Selanjutnya, orbital hibrida ini berikatan dengan orbital atom lain.
2) Orbital-orbital yang berikatan harus bertumpang tindih (overlapping) satu sama lain.
3) Jumlah elektron dalam orbital ikatan yang bertumpang tindih maksimal dua elektron dengan spin berlawanan.
4) Kekuatan ikatan bergantung pada derajat tumpang tindih. Semakin besar daerah tumpang tindih, semakin kuat ikatan yang terbentuk.
5) Orbital-orbital atom selain orbital-s dalam berikatan memiliki arah tertentu sesuai orientasi orbital atom yang berikatan.
4.2. Hibridisasi Orbital Atom
Hibridisasi adalah proses pencampuran orbital-orbital atom membentuk orbital baru dengan tingkat energi berada di antara orbital-orbital yang dicampurkan. Orbital hasil pencampuran dinamakan orbital hibrida.
5. Gaya Antar Molekul
Gaya antarmolekul adalah gaya aksi di antara molekul-molekul yang menimbulkan tarikan antarmolekul dengan berbagai tingkat kekuatan. Pada suhu tertentu, kekuatan tarikan antarmolekul menentukan wujud zat, yaitu gas, cair, atau padat. Kekuatan gaya antarmolekul lebih lemah dibandingkan ikatan kovalen maupun ikatan ion. Ikatan kimia dan gaya antarmolekul memiliki perbedaan. Ikatan kimia merupakan gaya tarik menarik di antara atom-atom yang berikatan, sedangkan gaya antarmolekul merupakan gaya tarik-menarik di antara molekul.
Andri Rahadiandyah, 2012
Multimedia Pembelajaran Ikatan Kimia MenggunakanKonteks Sain Dan Teknologi Nani Material Grafena Untuk Meningkatkan Literasi Sains Siswa SMA
Universitas Pendidikan Indonesia | repository.upi.edu
Ada tiga jenis gaya antarmolekul, yaitu gaya dipol-dipol, gaya London, dan ikatan hidrogen. Gaya dipol-dipol dan gaya London dapat dianggap sebagai satu jenis gaya, yaitu gaya Van der Waals.
5.1. Gaya Dipol-Dipol
Gaya dipol-dipol adalah gaya yang terjadi di antara molekul-molekul yang memiliki sebaran muatan tidak homogen, yakni molekul-molekul dipol atau molekul polar. Molekul-molekul polar memiliki dua kutub muatan yang berlawanan. Oleh karena itu, di antara molekul-molekulnyaakan terjadi antaraksi yang disebabkan kedua kutub muatan yang dimilikinya.
5.2. Gaya London
Gaya London adalah gaya yang terjadi pada atom atau molekul, baik polar maupun nonpolar. Gaya London atau disebut juga gaya dispersi, yaitu gaya yang timbul akibat dari pergeseran sementara (dipol sementara) muatan elektron dalam molekul homogen. Dalam ungkapan lain, dapat dikatakan bahwa gaya London terjadi akibat kebolehpolaran atau distorsi “awan elektron” dari suatu molekul membentuk dipol sementara (molekul polar bersifat dipol permanen).
5.3. Ikatan Hidrogen
Ikatan hidrogen terbentuk pada senyawa-senyawa polar yang mengandung atom H dan atom yang memiliki keelektronegatifan tinggi, seperti F, O, N, dan Cl. Atom-atom yang memiliki keelektronegatifan tinggi akan menarik pasangan elektron
ikatan lebih kuat sehingga kulit valensi elektron pada atom hidrogen seperti terkelupas, dan inti atom hydrogen yang bermuatan positif seolah-olah berada di permukaan molekul. Semakin tinggi skala keelektronegatifan atom yang mengikat atom hidrogen, semakin besar peluangnya untuk membentuk ikatan hidrogen.