BAB 2 TINJAUAN PUSTAKA
2.1 Pengertian Baterai
Baterai adalah komponen dari perangkat elektronik yang berperan sebagai perangkat penyimpanan energi yang dapat mengkonversikan energi kimia menjadi energi listrik. Baterai terdiri dari beberapa sel elektrokimia dan setiap sel mengandung elektroda negatif (anoda), elektroda positif (katoda), dan elektrolit (Mahmoud & Xu, 2011). Secara garis besar baterai terdiri dari dua macam yaitu baterai primer dan baterai sekunder.
2.1.1 Jenis-jenisBaterai 1. Baterai Primer
Baterai primer adalah baterai yang hanya bisa sekali pakai, dalam baterai primer ini energi kimia yang tersimpan dalam sel disusun sedemikian rupa sehingga hanya dapat digunakan sekali untuk menghasilkan energi listrik, dimana setelah kapasitasnya habis maka tidak bisa digunakan lagi (Aifantis et al., 2010). Keuntungan umum baterai primer adalah waktu hidup baik, densitas energi yang tinggi pada laju discharge
rendah, dan mudah digunakan (Linden, 2002). 2. Baterai Sekunder
2.2 Baterai Ion Lithium
Lithium adalah logam paling ringan dan memiliki potensi elektrokimia yang tinggi. Sifat ini memungkinkan logam lithium untuk mencapai densitas energi dan densitas power yang tingi dan menjadi bahan yang menjanjikan di pasar produksi baterai (Mahmoud & Xu, 2011). Baterai ion lithium adalah baterai yang digerakkan oleh ion lithium. Baterai ion lithium pertama kali dikomersialisasikan pada tahun 1990 oleh Sony Corp untuk ponsel Kyocera. Sejak diperkenalkan, pasar ion lithium telah berkembang menjadi sekitar $4 miliar pada tahun 2005 (Yoshio et al., 2009).
Baterai ion lithium memiliki banyak keunggulan dibandingkan dengan baterai sekunder lainnya yaitu ringan, densitas energinya tinggi, tidak memiliki memori effect, dapat diisi ulang (rechargeable), tahan lama, tegangannya tinggi (4V), ramah lingkungan dan penurunan kapasitas baterai ion lithium rendah sekitar 5% per bulan. Namun, baterai ion lithium masih memiliki kekurangan diantaranya sangat sensitif terhadap suhu tinggi dan biayanya lebih tinggi dibandingkan dengan baterai yang sudah ada (Oswal et al., 2010).
2.3 Karakteristik Baterai Ion Lithium
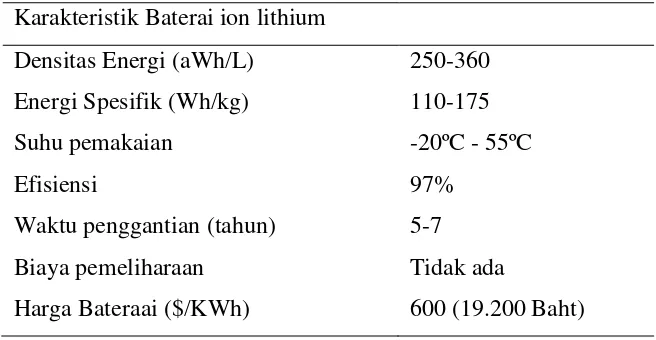
Lithium ion adalah salah satu jenis baterai yang paling populer dan dapat di apikasikan dalam berbagai hal. Oleh sebab itu kita harus mengetahui karakteristik yang ada pada baterai ion lithium, pada Tabel 1 menampilkan karakteristik dari baterai ion lithium.
Tabel 1. Karakteristik Baterai Ion Lithium Karakteristik Baterai ion lithium
2.3.1 Energi Densitas
Densitas Energi adalah penyimpanan energi per satuan berat atau per satuan volume dalam baterai. Perbandingan densitas energi dalam empat baterai ini populer dapat diamati dengan jelas pada Gambar 2 (Mahmoud & Xu, 2011).
Baterai ion lithium juga memiliki sifat utama yaitu nilai spesifik energi secara grafimetrik maupun volumetrik jauh lebih unggul dibandingkan dengan baterai sekunder lain (Kawamoto, 2010).
Gambar 2. Perbandingan Baterai Ion Lithium dengan Baterai Sekunder Lainnya
Penjelasan pada Gambar 2 dapat dilihat perbandingan antara baterai ion lithium dengan baterai sekunder lainnya pada Tabel 2 dibawah ini.
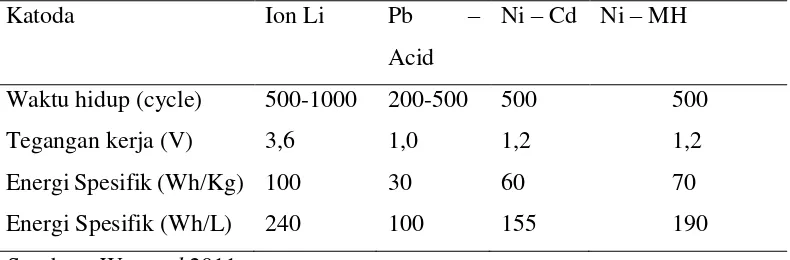
Tabel 2. Perbandingan Baterai Ion Lithium dengan Baterai Sekunder Lainnya
Katoda Ion Li Pb –
Acid
Ni – Cd Ni – MH
Waktu hidup (cycle) 500-1000 200-500 500 500 Tegangan kerja (V) 3,6 1,0 1,2 1,2
Energi Spesifik (Wh/Kg) 100 30 60 70
Energi Spesifik (Wh/L) 240 100 155 190
2.3.2 Waktu Hidup
Definisi waktu hidup adalah jumlah lengkap dari proses charge-discharge
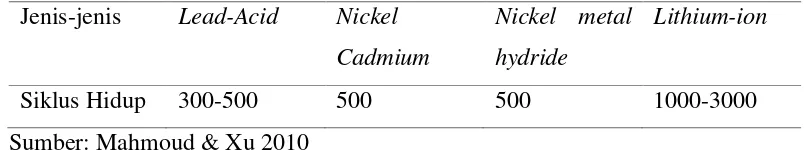
yang dilakukan oleh baterai. Saat kapasitas turun menjadi 80% dari nilai kapasitas awal, kehidupan baterai ini berakhir. Biasanya, mekanisme penuaan (aging) mengakibatkan hilangnya kapasitas setelah digunakan berulang-ulang, yang mempengaruhi siklus hidup baterai. Siklus hidup dari berbagai baterai sekunder ditunjukkan pada Tabel 3.
Tabel 3. Siklus Waktu Hidup dari Berbagai Jenis Baterai Jenis-jenis Lead-Acid Nickel terendah, yang juga merupakan sampel yang digunakan di laboratorium. Namun, kapasitas baterai Li-ion yang diperlukan. Walaupun biaya produksi baterai Li Ion adalah sekitar 100 dolar, hal ini dapat diterima karena baterai Li-ion memliki energi spesifik lebih tinggi dibandingkan baterai sekunder lainnya yaitu 90 Wh kg-1 yang dapat meningkatkan waktu hidup dari sistem baterai seperti yang diharapkan.
2.4 Bahan Dalam Baterai Ion Lithium
Untuk penggunaan akhir, mungkin kadang-kadang tampak seperti hanya ada satu jenis baterai baterai ion lithium, tetapi kenyataannya ada beberapa jenis sel kimia yang berbeda dari sel ion lithium. Anoda standar di sebagian besar sel komersial saat ini adalah grafit. Namun, bahan katoda dan elektrolit bervariasi secara substansial dalam sel, bersama-sama dengan formulasi komposit elektroda, ukuran partikel bahan aktif, dan lain-lain (Nordh,2013).
2.4.1 Material Anoda
yang sering digunakan sebagai komponen sel baterai lithium rechargeable adalah grafit/karbon dan logam lithium. Kedua material tersebut memenuhi syarat sebagai suatu material untuk proses interkalasi. Adapun tiga syarat utama yang harus dimiliki material anoda pada baterai ion lithium yaitu sebagai berikut : 1. Potensial penyisipan dan pelepasan ion lithium pada anoda harus sekecil mungkin. 2. Banyaknya ion lithium yang dapat dimuat oleh material anoda harus besar untuk mencapai kapasitas spesifik yang besar. 3. Host pada anoda harus menahan penyisipan dan pelepasan ion lithium yang berulang–ulang tanpa kerusakan strukturnya untuk memperoleh siklus hidup yang panjang (Yao, 2003). Anoda dipilih dengan mempertimbangkan: efisiensi sebagai reduktor, hasil keluaran coulomb tinggi (Ah/g), konduktivitas yang baik, stabilitas baik, kemudahan fabrikasi, dan biaya yang murah. (Linden, 2002).
2.4.2 Material Katoda
Katoda atau elektroda positif sebagai pengoksidasi elektroda yang menerima elektron dari sirkuit eksternal dan reduksi selama reaksi elektrokimia. katoda harus menjadi oksidator yang baik, stabil ketika berhubungan dengan elektrolit, dan memiliki tegangan kerja yang dapat digunakan dengan baik (Linden, 2002).
2.4.3 Elektrolit
Elektrolit adalah bahan yang memberikan konduktivitas ionik murni antara elektroda positif dan negatif dari sel (Winter & Brodd, 2004). Penambahan bahan ion biasanya dalam bentuk larutan air, cair, atau padat (Aifantis et al., 2010). Elektrolit
aqueous tidak dapat digunakan dalam baterai ion lithium, jadi garam anorganik terlarut dalam pelarut organik yang dapat digunakan sebagai elektrolit. Bahan elektrolit yang sempurna harus memiliki konduktivitas ionik yang tinggi, stabilitas yang baik dan keamanan yang sangat baik. LiPF6 adalah elektrolit yang paling umum di pasar saat ini (Mahmoud & Xu, 2011).
2.4.4 Separator
nantinya diisi dengan elektrolit. Separator harus berpori antara ion dan inert dalam lingkungan baterai (Winter & Brodd, 2004).
2.5 Pengoperasian Baterai
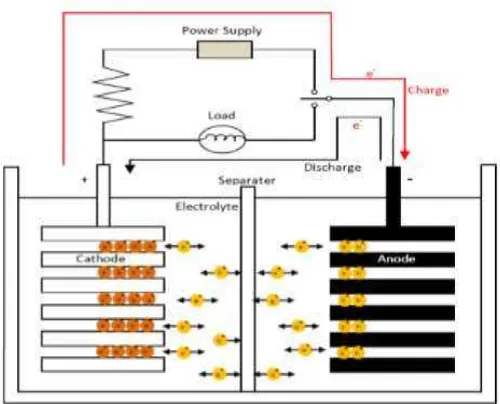
Bahan dengan potensi reduksi standar positif yang lebih rendah disebut elektroda negatif atau anoda pada discharge (karena memberikan elektron), sedangkan bahan dengan pengurangan standar positif yang lebih tinggi disebut elektroda positif atau katoda pada discharge (karena menerima elektron) (Aifantis et al., 2010). Prinsip baterai Li-ion ditunjukkan pada Gambar 3.
Gambar 3. Prinsip Kerja Baterai Ion Lithium
Pada umumnya anoda baterai ion lithium adalah karbon (grafit), sedangkan katoda dibuat dari kobalt dioksida lithium (LiCoO2) dan elektrolit adalah non-aqueous
pelarut organik termasuk garam lithium (LiPF6). Reaksi setengah sel pada elektroda positif adalah:
xLi+ + xe- +
Li1-x CoO2 LiCoO2 (1)
Reaksi di elektroda negatif adalah sebagai berikut:
LixC xLi+xe-+ C (2)
discharge
charge
discharge
Reaksi totalnya adalah:
Li1-xCoO2 + LixC LiCoO2 + C (3)
Baterai Ion Lithium bergantung pada proses interkalasi. Ion lithium dimasukkan kedalam kisi dari elektroda tanpa mengubah struktur kristal (Mahmoud & Xu, 2011). Selama proses charge baterai, terjadi pergerakan ion lithium dari elektroda positif (katoda) melalui seperator dan elektrolit ke elektroda negatif (anoda). Elektron cenderung mengalir ke arah yang berlawanan di sekitar sirkuit luar. Ketika semua ion berhenti mengalir, baterai seharusnya terisi penuh dan siap untuk digunakan. Baterai menyimpan energi selama proses ini (Oswal et al., 2010).
Selama discharge, ion lithium bergerak dari elektroda negatif (anoda) ke elektroda positif (katoda) melalui seperator dan elektrolit, menghasilkan densitas daya pada baterai. Elektron cenderung mengalir sebaliknya melalui sirkuit luar (Oswal et al., 2010). Ion lithium dipisahkan bermigrasi melewati elektrolit dan masuk ke dalam struktur karbon. Pada saat yang sama elektron mengalir ke sirkuit luar sebagai kompensasinya. Karena reaksi ini adalah reveversibel, ion lithium lolos kembali dan balik antara elektroda saat pengisian dan pemakaian. Baterai Li-Ion juga mengalami mekanisme penuaan (aging), yang meningkatkan resistansi internal, menyebabkan kerugian kapasitas dan memperpendek siklus hidup (Mahmoud &Xu, 2011).
Dalam sel baterai, site reduksi disebut katoda dan site oksidasi disebut anoda. Elektroda yang bertindak sebagai anoda dan yang bertindak sebagai katoda ditentukan oleh bagaimana potensial reduksi standar berhubungan satu sama lain, dan dengan demikian yang lainnya lebih mudah teroksidasi. Elektroda dengan potensial standar yang lebih tinggi akan bertindak sebagai katoda, dan potensial rendah sebagai anoda (Nordh, 2013).
2.6 Komponen dalam Lembaran Elektroda
Lembaran elektroda dalam baterai sering digabungkan dari beberapa bahan. Tiga komponen utama komponen yaitu bahan aktif, konduktor elektronik dan pengikat. Bahan aktif adalah bahan yang berperan dalam reaksi redoks yang
discharge
menghasilkan arus dalam baterai. Bahan aktif memiliki konduksi elektronik yang rendah, dan karena itu konduktor elektronik perlu ditambahkan. Karena bahan aktif dan ditambah konduktif dan dicampur dalam bentuk bubuk, pengikatnya ditambahkan untuk membuat pegangan elektroda bersama-sama. Campuran elektoda ini dilapiskan ke current colector dalam proses manufaktur dan karena itu tidak dapat dipisahkan lagi (Nordh,2013).
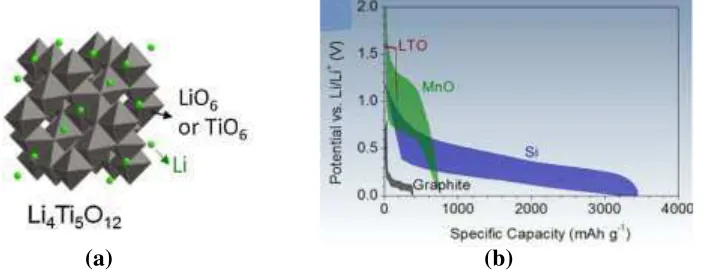
2.6.1 Material Aktif (LTO)
(a) (b)
Gambar 4. (a) Struktur LTO (Li4Ti5O12), (b) Charge-Discharge pada Kondisi Low Rates
Li4Ti5O12 atau LTO merupakan material anoda yang dapat digunakan sebagai pengganti grafit dalam baterai ion lithium sekunder (Sibiryakov, 2013). Pada Gambar 4 (a) memperlihatkan struktur kristal dari LTO. LTO telah berhasil dikomersialkan karena memungkinkan kombinasi stabilitas termal yang superior, high rate, kapasitas volumetrik yang relatif tinggi, dan siklus hidup yang panjang. Meskipun biaya yang lebih mahal dari Ti, tegangan sel berkurang dan kapasitas yang lebih rendah. LTO dianggap “zero strain” karena perubahan fasa yang disebabkan oleh
lithiation/delithiation hanya menghasilkan sedikit perubahan volume (0,2 %). Secara elektrokimia, pada saat tegangan kecil tegangan hysteresis ditunjukkan dalam kondisi
terbentuk, kurangnya perubahan volume meningkatkan stabilitas SEI karena impedanssi SEI tidak menjadi masalah, nano partikel LTO dapat digunakan, yang mirip dengan interkalasi bahan katoda, dan mengakibatkan kinerja lebih tinggi pada penurunan volumetrik dengan kapasitas yang lebih rendah (Nitta et al., 2014). Namun, LTO juga memiliki kelemahan yang cukup besar, seperti koefisien konduktivitas dan lithium difusi spesifik yang rendah. kelemahan ini dapat dihilangkan dengan cara yang berbeda, misalnya, dengan penciptaan struktur cacat, pengurangan ukuran partikel, lapisan permukaan partikel dengan karbon, dan doping dengan logam (tembaga, timah, perak). Reduksi ukuran partikel dapat memperpendek jarak difusi ion lithium dalam fase padat dan meningkatkan permukaan kontak dengan elektrolit (Sibiryakov et al., 2013).
2.6.2 Konduktor Elektronik (AB)
Karbon hitam telah banyak digunakan sebagai filler dalam industri polimer karena sifat yang sangat baik seperti panas, kimiawi dan tahan cuaca, sangat ringan,
electroconductivity, dan suhu ekspansi rendah. Khususnya, elektrik komposit konduktif disiapkan melalui penggabungan konduktif acetylene black (AB). AB memiliki diameter partikel rata-rata adalah 36 nm dan luas permukaan adalah 65 m2 /g. Meskipun AB pada dasarnya sama dengan karbon hitam lainnya, tapi jauh berbeda bahwa partikel didalamnya berbentuk rantai, dan memiliki grafitisasi yang sangat canggih (Lee et al., 2010).
2.6.3 Binder PTFE (Polytetrafluoroethylene)
Binder atau pengikat dapat digunakan untuk mempertahankan integritas struktural dari partikel aktif dan membantu bahan elektroda ke arus kolektor (Zhong
sebagai aditif untuk meningkatkan ketahanan aus atau properti gesekan dari bahan lain (Teng, 2012). PTFE memiliki ketahanan kimia yang luar biasa, ketahanan panas dan dingin yang tinggi, bersifat isolasi, tahan terhadap sinar UV (ultra violet), ketahanan cuaca yang baik, koefisien gesek yang rendah, anti-patah, lentur, ketahanan tinggi terhadap api dan penyerapan air yang sangat rendah (Biron, 2007). PTFE sangat dikenal dengan manfaat seperti ketahanan kimia yang sangat baik, anti-perekat permukaan yang baik, resistansi UV dan dapat digunakan lebih dari satu jarak temperatur yang luas (Bruemmer & Schnabel, 1999).
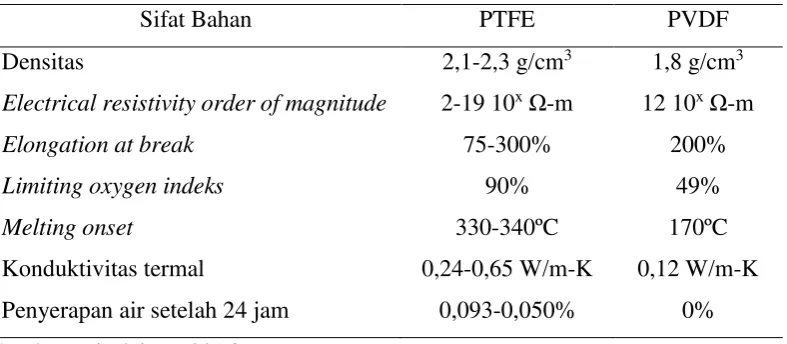
PTFE adalah hydrophobic dan secara kimia tahan terhadap semua pelarut, asam, dan basa. Hindari suhu di atas 300 ° C karena bahan dapat mencair. Hindari dekomposisi yang berbahaya, seperti: karbon monoksida, karbon dioksida, styrene, akrilonitril, hidrokarbon, sianida. Dari informasi toksikologi, tidak ada data yang tersedia (MSDS-PTFE, 2008). Berikut ini perbandingan sifat bahan pengikat antara PTFE dan PVDF ditunjukkan dalam Tabel 4 yang menunjukkan perbedaan yang mendasar.
Tabel 4. Perbandingan Sifat Bahan PTFE dan PVDF
Sifat Bahan PTFE PVDF
Densitas 2,1-2,3 g/cm3 1,8 g/cm3
Electrical resistivity order of magnitude 2-19 10xΩ-m 12 10xΩ-m
Elongation at break 75-300% 200%
Limiting oxygen indeks 90% 49%
Melting onset 330-340ºC 170ºC
Konduktivitas termal 0,24-0,65 W/m-K 0,12 W/m-K
Penyerapan air setelah 24 jam 0,093-0,050% 0%
Sumber: Disclaimer 2016
2.7 Karakterisasi Material 2.7.1 FTIR
dari bahan organik, khususnya polimer. Spektroskopi FTIR didasarkan pada interaksi cahaya inframerah dengan molekul. Energi absorbsi dari ikatan kimia menciptakan spektrum FTlR. Energi dari cahaya berbanding lurus dengan bilangan gelombang:
E = hcW (4)
Dimana E dan W mewakili energi dan bilangan gelombang, masing-masing. Dan lain keduanya konstan: h adalah konstanta Planck (6,63x10-34 J/s) dan C adalah kecepatan cahaya. spektrometer FTIR terdiri dari sumber cahaya inframerah, detektor, sumber sinar laser, cermin geser dan cermin tetap. Bagian-bagian spektrometer FTIR ditunjukkan pada Gambar 5.
Gambar 5. Bagian-Bagian Spektrometer FTIR
2.7.2 XRD
X-Ray Diffraction (XRD) adalah suatu metode analisis dalam kristalografi. Pada umumnya, itu dimulai sebagai cara untuk menentukan struktur atom dari kristal, tapi sekarang dapat digunakan untuk menentukan informasi lebih banyak, misalnya: sebagai parameter sel, distorsi, ketegangan dan ukuran kristal sekarang informasi dapat diperoleh (Nordh, 2013). Untuk menghitung parameter kisi dengan strutur kristal kubik, maka kita dapat menggunakan Persamaan 5.
a = (5)
Dimana a adalah parameter kisi (A0), λ adalah panjang gelombang radiasi dari Cu Kα = 1,54 A0, θ (theta) adalah sudut yang terbentuk dan h,k,l adalah bidang kristal dari suatu material. Kisi Bravais dapat diidentifikasi dengan mencatat keberadaan sistematis (atau ketiadaan) refleksi dalam pola difraksi. Nilai h2+ k2+ l2
λ
untuk kisi kubik yang berbeda mengikuti urutan sesuai yang ditunjukkan pada Tabel 5.
Tabel 5. Nilai h2+ k2+ l2 untuk Kisi Kubik
Untuk menghitung jarak bidang kristal kubik maka dapat digunakan Persamaan 6.
a
(h2+ k2+ l2)1/2 (6)
Dimana d adalah jarak bidang kristal, a adalah parameter kisi dan h,k,l adalah bidang kristal suatu material. Ketika sinar X dikirim ke dalam sampel, sinar akan dihamburkan oleh atom nya dan menyebar ke segala arah. Sinar yang tersebar dari atom yang berbeda tetapi dalam arah yang sama akan membuat jarak yang berbeda dan karena itu akan keluar dari fase satu sama lain ketika mencapai titik yang ditetapkan, misalnya detektor. Prinsip kerja XRD ditunjukkan pada Gambar 6.
Gambar 6. Prinsip kerja alat X-ray diffraction
Primitive 1,2,3,4,5,6,7,8,9,10,11,12,131,14....
Body-centered 2,4,6,8,10,12,14,16...
Face-centered 3,4,8,11,12,16,19,20,24,27,32....
Gambar 6 memperlihatkan hukum Bragg terpenuhi ketika D sama dengan seluruh jumlah panjang gelombang, maka semua sinar terdifraksi akan memiliki fase satu sama lain (Nordh, 2013).
2.7.3 CV
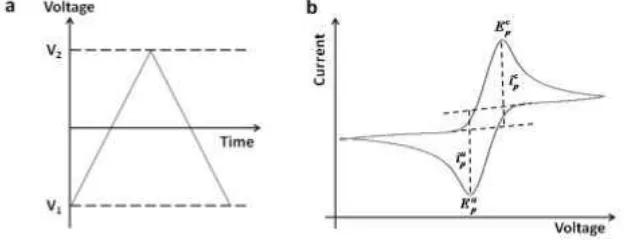
CV (Cyclic Voltammetry) adalah jenis pengukuran elektrokimia potensio dinamik,dan merupakan salah satu metode elektrokimia yang paling sering digunakan karena relatif sederhana dan isi informasi yang tinggi. Selama pengujian CV, pada Gambar 7 (a) potensi linear pemindaian siklik (yaitu, elektroda potensial landai linear terhadap waktu) dikenakan ke elektroda dan arus yang dihasilkan dicatat.
Gambar 7. Tipikal Cyclic Voltammogram untuk Proses Redoks Reversibel
= � ²
(2,69)2 .1010 4/3�2 2 (7)
Dimana, n merupakan bilangan elektron, A luas permukaan elektroda (cm2),C merupakan konsentrasi ion lithium di dalam padatan (4,37 x 10-3 mol/cm-3 ), v merupakan kecepatan scan rate (0,1 mV/sec). Untuk mencari daya makan dapat menggunakan rumus sebagai berikut:
�( ) = ������� �� (8)
Dimana, Voksidasi merupakan tegangan maksimum dari puncak sampel dan Ip merupakan arus polarisasi (mA).
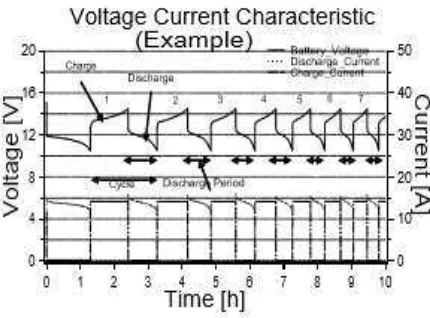
2.7.4 CD
CD (Charge-discharge) adalah teknik elektrokimia yang paling umum digunakan untuk karakterisasi perangkat penyimpanan energi. Dalam pengujian ini sebuah sel diisi dan dikosongkan dengan menggunakan arus konstan di antara tegangan atas dan tegangan bawah (Li, 2012). Karakterisasi ini dibuat untuk mengevaluasi kerusakan baterai. Pada Gambar 8 dijelaskan bahwa ketika charging, tegangan meningkat, sedangkan bila discharging dimulai, tegangan menurun.
2.7.5 DTA/TGA
Thermal analysis merupakan teknik untuk mengkarakterisasi sifat material yang dipelajari berdasarkan respon material tersebut terhadap temperatur. Untuk menentukan sifat termo-fisiknya metode yang biasa digunakan salah satunya adalah
differential thermal analysis (DTA). Dalam bidang metalurgi dan ilmu material kegunaan dari DTA ini adalah untuk mempelajari transisi fasa yang terjadi dibawah pengaruh atmosfer, temperatur, laju pemanasan atau pendinginan. DTA adalah analisis termal yang menggunakan referensi sebagai acuan perbandingan hasilnya, material referensi ini biasanya material inert. Sampel dan material referensi dipanaskan secara bersamaan dalam satu tempat. Perbedaan temperatur sampel dengan temperatur material referensi dicatat selama siklus pemanasan dan pendinginan (Klancnik et al., 2009).