commit to user
TOKSISITAS 4-VYNILCYCLOHEXENE DIEPOXIDE (VCD)
TERHADAP STROMA OVARIUM
Studi pada tikus galur Wistar ( Rattus Novergicus Lam )
(Studi Pendahuluan)
TESIS
Disusun untuk Memenuhi Sebagian Persyaratan
Mencapai Derajat Magister Kesehatan
Program Studi Magister Kedokteran Keluarga
Minat Utama Ilmu Biomedik
Oleh:
Arif Dharmawan
S500907009
PROGRAM PASCASARJANA UNIVERSITAS SEBELAS MARET
commit to user
ii
Halaman Pengesahan Tesis
TOKSISITAS 4-VYNILCYCLOHEXENE DIEPOXIDE (VCD) TERHADAP STROMA OVARIUM
Disusun Oleh:
Arif Dharmawan
S500907009
Telah Disetujui oleh Tim Pembimbing untuk
Komisi
Pembimbing Nama Tanda Tangan Tanggal
Pembimbing I Dr.Sri Sulistyowati, dr., Sp.OG (K)
NIP. 196208221989122001
…………. ………
Pembimbing II Prof.Dr.J.B.Dalono , dr., Sp.OG (K)
NIP. 194105041970041001
.………… ………
Ketua Program Studi
Magister Kedokteran Keluarga
Dr. Hari Wujoso, dr.,SpF,M.M
commit to user
iii
TOKSISITAS 4-VYNILCYCLOHEXENEDIEPOXIDE (VCD) TERHADAP STROMA OVARIUM
Studi Pendahuluan pada tikus galur Wistar ( Rattus Novergicus Lam )
Disusun Oleh:
Arif Dharmawan
S500907009
Telah Disetujui oleh Tim Penguji
Pada hari :
Tanggal :
Jabatan Nama Tanda Tangan
Ketua Dr. Hari Wujoso, dr.,SpF,M.M
NIP. 196210221995031001
Sekretaris Prof. Dr. Harsono Salimo, dr.,SpA NIP. 19483131976101001
Anggota Penguji 1. Dr. Sri Sulistyowati, dr., Sp.OG(K)
commit to user
iv
PERNYATAAN
Nama : Arif Dharmawan
NIM : S500907009
Menyatakan dengan sesungguhnya bahwa tesis berjudul Toksisitas
4-Vynilcyclohexene Diepoxide (VCD) Terhadap Stroma Ovarium adalah
betul-betul karya sendiri. Hal-hal yang bukan karya saya, dalam tesis tersebut diberi
tanda citasi dan ditunjukkan dalam daftar pustaka.
Apabila di kemudian hari terbukti pernyataan saya tidak benar, maka saya
bersedia menerima sanksi akademik berupa pencabutan tesis dan gelar yang saya
peroleh dari tesis tersebut.
Surakarta, Juni 2012
Yang membuat pernyataan
commit to user
v
KATA PENGANTAR
Assalamualaikum Wr. Wb.
Alhamdulillahirobbilalamin Yaa Allah, segala puji dan syukur saya
panjatkan kehadirat Allah SWT yang telah melimpahkan Rahmat, Taufik dan
Hidayah Nya sehingga saya dapat menyelesaikan tesis ini yang disusun untuk
memenuhi persyaratan dalam mengikuti Program Studi Dokter Spesialis I di
Fakultas Kedokteran Universitas Sebelas Maret serta untuk memenuhi persyaratan
mencapai derajat Magister Kesehatan di Program Studi Magister Kesehatan
Universitas Sebelas Maret Surakarta dengan judul “Toksisitas
4-VynilcyclohexeneDiepoxide (VCD) Terhadap Stroma Ovarium ”.
Terimakasih yang tak terhingga dan penghargaan yang sebesar-besarnya
saya sampaikan kepada Dr.Hj. Sri Sulistyowati, dr., Sp.OG(K) sebagai
pembimbing I yang dengan penuh perhatian dan kesabaran telah memberikan
dorongan, bimbingan, dan saran di tengah kesibukan beliau yang begitu padat
masih berkenan meluangkan waktu untuk memberi petunjuk, dalam proses
penyelesaian tesis ini.
Terimakasih yang tak terhingga dan penghargaan yang sebesar-besarnya
juga saya sampaikan kepada Prof. Dr. JB Dalono, dr., Sp.OG (K) dan A Laqif,
dr SpOG (K) sebagai pembimbing II yang dengan penuh perhatian dan kesabaran
telah memberikan dorongan, bimbingan, dan saran serta arahan, memecahkan
masalah yang timbul dan ikut membantu dalam proses penyelesaian tesis ini.
Terimakasih yang tak terhingga dan penghargaan yang sebesar-besarnya
juga saya sampaikan kepada Dr. Abkar Raden, dr., Sp.OG (K) sebagai
koordinator tesis yang telah memberikan dorongan, waktu dan kesempatan yang
seluas-luasnya dalam proses penyelesaian tesis ini.
Terimakasih yang tak terhingga dan penghargaan yang sebesar-besarnya
juga saya sampaikan kepada tim penguji, yang telah berkenan memberikan waktu
commit to user
vi
Dengan selesainya tesis ini, perkenankanlah pada kesempatan ini saya
mengucapkan terima kasih yang sebesar-besarnya dan rasa hormat
setinggi-tingginya kepada yang terhormat:
1. Prof. Dr. Ravik Karsidi, M.Si., sebagai Rektor Universitas Sebelas
Maret Surakarta.
2. Prof. Dr. Ir. Ahmad Yunus, MS sebagai Direktur Pascasarjana
Universitas Sebelas Maret Surakarta.
3. Dr. Hari Wujoso, dr.,SpF,M.M, sebagai Ketua Program Studi Magister
Kedokteran Keluarga Universitas Sebelas Maret Surakarta.
4. Prof. Dr. Zainal Arifin Adnan, dr., Sp.PD-KR., sebagai Dekan
Fakultas Kedokteran Universitas Sebelas Maret Surakarta.
5. Basoeki Sutardjo, drg., MMR., sebagai Direktur RSUD Dr. Moewardi
Surakarta.
6. Dr. Supriyadi Hari R, dr., Sp.OG., sebagai Ka. Bag SMF Obgin
Fakultas Kedokteran Universitas Sebelas Maret Surakarta.
7. Dr. Sri Sulistyowati, dr., Sp.OG (K)., sebagai KPS SMF Obgin
Fakultas Kedokteran Universitas Sebelas Maret Surakarta.
8. Affi Agelia dr.SpOG. Mkes., sebagai SPS SMF Obgin Fakultas
Kedokteran Universitas Sebelas Maret Surakarta.
9. Seluruh Staff PPDS I Bagian Obgin Fakultas Kedokteran Universitas
Sebelas Maret Surakarta. Prof. Dr. JB Dalono, dr., Sp.OG (K)., Dr.
commit to user
vii
10. Saya juga mengucapkan banyak terima kasih kepada H. Rusbandi, dr.
SpOG Kepala Bagian Obstetri dan Ginekologi RSU Sragen, Nugroho Adiwarso, dr SpOG Kepala Bagian Obstetri dan ginekologi RSU Blora, Eka Budi W, dr. MKes., SpOG Kepala Bagian Obstetri dan Ginekologi
RSU Wonogiri, H. Suroso, dr. SpOG Kepala Bagian Obstetri dan
Ginekologi RSU Kebumen, H. Suwaryo Madsukadi, dr. SpOG Kepala
Bagian Obstetri dan Ginekologi RSU Cepu, L Budiadi, dr SpOG
Kepala bagian Obstetri dan Ginekologi RSU Pandanarang Boyolali yang
selalu memberikan bimbingan dan memberi kesempatan kami untuk
belajar dan menimba pengalaman di rumah sakit jejaring tersebut.
11. Prof.Kuniarsih, drh, MVSc., PhD , Kepala Bagian Patologi Fakultas
Kedokteran Hewan Universitas Gadjah Mada Yogyakarta beserta semua
staf dan tenaga tehnis atas izin dan kesempatan yang diberikan untuk
menggunakan fasilitas laboratorium dalam penelitian tesis ini.
12. Semua rekan residen PPDS I Obgin Fakultas Kedokteran Universitas
Sebelas Maret Surakarta yang banyak membantu dalam pelaksanaan tesis
ini. Kepada para dokter muda/co-asisten , bidan dan paramedik saya
ucapkan terima kasih atas kerjasamanya yang baik selama masa
pendidikan ini.
13. Ayahanda H.Untung Hadi Purwanto (Alm) dan ibunda Hj.Itje
Mariam BSA, yang telah membesarkan saya, mengasuh, membimbing
dan mendidik disiplin kepada saya dengan penuh kasih sayang,
memberikan dorongan, fasilitas serta mendoakan kelancaran selesainya
pendidikan dan tesis ini.
14. Ayah dan ibu mertua, keluarga H.Zuhri Amin,SH, (Alm) dan
Hj Endang Pertiwi serta Kakek dan nenek ,H Ali Murtadho dan
Hj.Siti Nur Halimah yang telah banyak membantu, memberikan
dorongan, serta mendoakan kelancaran selesainya pendidikan dan tesis
commit to user
viii
15. Istri saya tercinta, dr.Nur Aeni Mulyaningsih yang telah banyak
berkorban selama saya mengikuti pendidikan PPDS I Obgin,dan tetap
mendorong, mendoakan, dan memberikan semangat sampai saya dapat
menyelesaikan pendidikan dan tesis ini.
16. Anak saya, Fairuz Zahiya Meuthia Dharmawan yang dapat menerima
dan memahami kesibukan saya dan juga mendorong semangat saya untuk
menyelesaikan pendidikan dan tugas tesis ini.
17. Saudaruku dr.Prima Isnaeni sekeluarga, Khusnul Laela,ST serta
saudara-saudara iparku, Nur Farida Yuliastuti,ST sekeluarga, Nur
Indah Tri Setyowati,SPsi sekeluarga, drg Nur Solecha Wahyu Lestari sekeluarga, Nur Zulaicha Soraya S.Ked, Nur Fatmawati K,SKG. yang telah banyak membantu serta mendorong semangat saya
untuk menyelesaikan pendidikan tugas tesis ini.
18. Semua pihak yang tidak dapat saya sebutkan satu persatu yang telah
banyak membantu saya dalam penyelesaian tesis ini.
Akhir kata semoga tesis ini bermanfaat bagi kemajuan ilmu pengetahuan,
dan semoga Allah SWT melimpahkan rahmat dan karuniaNya kepada kita semua.
Amin Yaa Robbal Alamin.
Wassalamualaikum Wr Wb.
commit to user
ix DAFTAR ISI
Halaman
HALAMAN JUDUL...……….…... i
HALAMAN PENGESAHAN PEMBIMBING... ii
HALAMAN PENGESAHAN PENGUJI TESIS...………… iii
PERNYATAAN ... iv
KATA PENGANTAR ... v
DAFTAR ISI………... ix
DAFTAR GAMBAR……….... xii
DAFTAR TABEL... xiii
DAFTAR SINGKATAN………... xiv
ABSTRAK... xv
BAB.I. PENDAHULUAN ... 1
A. Latar belakang ... 1
B. Rumusan Masalah ... 3
C. Tujuan penelitian ... 3
D. Manfaat penelitian ... 3
BAB. II. TINJAUAN PUSTAKA... 4
A. Stroma Ovarium... 4
1. Endokrinologi Ovarium ... 5
commit to user
x
3. Pertumbuhan Folikel ... 11
4. Peran Stroma pada Fungsi Ovarium ... 13
5. Kategori Kerusakan Ovarium ... 15
B. 4-Vynilcyclohexene Diepoxide (VCD) ... 18
1. Definisi ... 18
2. Mekanisme Seluler Ovotoksisitas ... 18
3. Mekanisme Molekuler Ovotoksisitas .. ... 20
4. Apoptosis pada Ovarium oleh Pengaruh VCD .. ... 23
5. Premature Ovarian Failure ….. ... 26
C. Kerangka Konseptual ... 32
Keterangan Kerangka Konsep ... 33
D. Hipotesis ... 34
BAB III. METODE PENELITIAN ... 35
A. Jenis dan Rancangan Penelitian ... 35
B. Lokasi dan Waktu Penelitian ... 36
C. Subjek Penelitian ... 36
D. Besar sampel .. ... 36
E. Varibel Penelitian .. ... 38
F. Definisi Operasional .. ... 38
G. Prosedur Penelitian yang Dilakukan .. ... 38
H. Alat dan Bahan Penelitian ... 39
I. Cara Kerja .. ... 40
commit to user
xi
BAB IV. HASIL DAN ANALISA PENELITIAN ... 44
A. Hasil Penelitian ... 44
B. Analisis Data Penelitian ... 44
BAB V. PEMBAHASAN ... 49
BAB VI. KESIMPULAN DAN SARAN ... 51
A. KESIMPULAN ... 51
B. SARAN ... 51
commit to user
xii
DAFTAR GAMBAR
Halaman
Gambar 1. Regulasi Saluran Reproduksi Wanita... 6
Gambar 2. Skematik Perkembangan Ovarium pada Fetus dan Dewasa .. ... 8
Gambar 3. Oogenesis dan folikulogenesis pada tikus ... 11
Gambar 4. Aktivitas sekresi faktor pertumbuhan. ... 14
Gambar 5. Penyempitan pembuluh darah Ovarium ... 17
Gambar 6. Sruktur kimia 4- vynilcyclohexene dan 4-vynilcyclohexene
diepoxide ... 18
Gambar 7. Kerangka Konsep ... 32
commit to user
xiii
DAFTAR TABEL
Halaman
Tabel 2.1. Etiologi terjadinya Premature Ovarian Failure ... 27
Tabel 4.1. Resume hasil pemeriksaan kerusakan stroma ovarium. ... 44
Tabel 4.2. Hasil uji Chi Kuadrat tentang perbedaan kerusakan stroma
ovarium menurut pemberian VCD pada hari ke 0 ... 45
Tabel 4.3. Hasil uji Chi Kuadrat tentang perbedaan kerusakan stroma
ovarium menurut pemberian VCD pada hari ke 5 ... 46
Tabel 4.4. Hasil uji Chi Kuadrat tentang perbedaan kerusakan stroma
ovarium menurut pemberian VCD pada hari ke 10 ... 47
Tabel 4.5. Hasil uji Chi Kuadrat tentang perbedaan kerusakan stroma
ovarium menurut pemberian VCD pada hari ke 15 ... 48
Tabel 4.6. Hasil uji McNemar tentang perubahan kerusakan stroma
ovarium pada hari ke 5, hari ke 10, dan hari ke 15
commit to user
xiv
DAFTAR SINGKATAN
Cu : Cuprum
DNA : Deoxyribonucleic Acid
FSH : Follicle Stimulating Hormone
GnRH : Gonadotropine Releasing Hormone
IGF : Insulin Growth Factor
IL : Interleukin
LH : Luteinisation Hormone
mRNA : Mutation Ribonucleic Acid
POF : Premature Ovarian Failure
SOD : Superoxide Dismutase
TNFα : Tumor Necrosing Factor α
VCD : 4-Vinylcyclohexane Diepoxide
VCH : 4-Vinylcyclohexene
commit to user
xv
Arif Dharmawan. 2012. Toksisitas 4-Vynilcyclohexene Diepoxide (VCD) terhadap Stroma Ovarium. TESIS. Pembimbing I: Dr.Sri Sulistyowati, dr.,
Sp.OG (K), II: Prof.Dr.J.B.Dalono , dr., Sp.OG (K). Program Studi Kedokteran Keluarga, Program Pascasarjana, Universitas Sebelas Maret Surakarta.
ABSTRAK
Latar Belakang: Sistem reproduksi wanita terdiri dari ovarium, tuba
uterina, uterus, vagina, dan genitalia eksterna. Sebagian besar ovarium berada intraperitoneal dan tidak dilapisi oleh peritoneum. Sebagian besar dari ovarium, baik korteks maupun medula, terdiri dari stroma. Stroma ovarium terdiri dari sel-sel yang berbentuk spindel yang mirip dengan fibroblas dan tersusun dalam suatu bentukan yang khas. Tidak seperti jaringan ikat pada umumnya, stroma ovarium tersusun dari banyak sel dengan serat yang menyokongnya (baik serat retikuler maupun jaringan kolagen biasa). Sel-sel terdiri atas cytoplasmic lipid dan dikelilingi oleh suatu serat retikulin. Beberapa sel menyerupai gambaran seperti miofibroblastik dan immunoreaktif dengan smooth muscle actin (SMA) dan desmin. Sel-sel stroma ovarium berhubungan dengan pematangan folikel, yang juga berkaitan erat dengan fungsi endokrin dan sekresi estrogen.
Pada studi ini peneliti mencoba merancang suatu hewan model untuk menyerupai kondisi alami proses menopause pada wanita. Penelitian dilakukan dengan menginduksikan agen kimia yang bersifat ovotoksik, 4-vinylcyclohexane
diepoxide (VCD) pada tikus galur Wistar untuk mempelajari proses kerusakan
pada ovarium. Telah diketahui bahwa VCD dapat menyebabkan terjadinya POF pada folikel ovarium hewan uji tikus. Namun masih belum diketahui pengaruhnya terhadap stroma ovarium yang merupakan jaringan penyangga dari ovarium. Penelitian ini dilakukan untuk mengetahui adanya pengaruh VCD terhadap stroma ovarium.
Tujuan: Untuk melihat efek toksisitas VCD terhadap stroma ovarium pada
tikus .
Metode penelitian: Penelitian dilakukan di laboratorium Patologi Fakultas
Kedokteran Hewan Universitas Gadjah Mada, merupakan penelitian obervasional laboratorium dengan pendekatan pretest -postest control group design. Variabel independen: dosis VCD, variabel dependen: Stroma ovarium pada Premature
Ovarian Failure. Jumlah sampel 60, dibagi dalam 3 grup (kontrol, perlakuan 80
mg/KgBB, dan perlakuan 160 mg/KgBB), Purposive Random Sampling. Analisis data dengan uji chi Square, menggunakan SPSS versi 17.00 for Windows.
Hasil Penelitian: Hasil studi menunjukkan bahwa tidak didapatkan
perbedaan yang signifikan antara kelompok kontrol dengan kelompok perlakuan. Hal ini menunjukkan bahwa pemberian VCD dengan dosis 80 mg/KgBB dan 160 mg/KgBB selama 15 hari, yang merupakan dosis yang telah menyebabkan terjadinya kerusakan folikel ovarium yang menyerupai POF, tidak menyebabkan terjadinya kerusakan stroma ovarium.
commit to user
xvi
Arif Dharmawan. 2012. Toxicity of 4-Vynilcyclohexene Diepoxide (VCD) through the Ovarin Stroma. DISSERTATION. Supervisor I: Dr.Sri
Sulistyowati, dr., Sp.OG (K), II: Prof.Dr.J.B.Dalono , dr., Sp.OG (K). Program Study of Medical Family, Post-graduate Program of Sebelas Maret University Surakarta.
ABSTRACT
Background: Women reproduction system is consist of ovary, uterine
tube, uterus, vagina, and external genitalia. Most of ovary, both cortex and medulla, consist of stroma. Ovarian stromas are spindle formed cells, looks like fibroblast and also lapped on typical form. Ovarian stroma has different form, it lapped on many cells with fibers that contributing on these cells (reticular fibers and collagen tissue). Cells are consist of cytoplasmic lipid and rounded by reticulin fibers. Some cells have form like miofibroblastic and immunoreactive with smooth muscle actin (SMA) and desmin. Ovarian stromal cells are related to follicle maturity, that also thightly related to endocrine function and estrogen secretion.
. In this study, observer is trying to stake out an animal model to become resemble of natural condition of menopause that happen in women. This study is done by inducted ovotoxic substance, 4-vinylcyclohexane diepoxide (VCD),in the wistar mices to examine the prosses of damage thata happen on ovary. It is known that VCD can cause POF on ovarian follicle on mice’s ovary. But, there is still unknown the effect of this substance on ovarian stroma. Ovarian stroma is a supporting tissue for ovary. This study is done for knowing the effect of VCD to the ovarian stroma.
Objectives: to examine the toxicity effect ofVCD through ovarian stroma of mice.
Methods: Research is done in Laboratory of Patology, Animal Medicine
Faculty, Gadjah Mada University. It is an observational laboratory research with pretest-posttest controlled group design. Independent variable is dose of VCD, dependent variable is ovarian stroma on Premature Ovarian Failure. We used 60 samples, devided inti 3 groups (control, treatment 80 mg/KgBW, and treatment 160 mg/KgBW), Purposive random sampling. Data analysis with Chi Square
examination, using SPSS version 17.0 for Windows.
Result: The result of this study shows that there is no significant differences between control group and treatment groups. It shows that induction of VCD on dose of 80 mg/KgBW and 160 mg/KgBW as long as 15 days, that is the dose to make the damages to ovarian follicle that resemble to POF, does not cause of damaging the ovarian stroma.
commit to user BAB I
PENDAHULUAN
A. Latar Belakang
Perindustrian membawa dampak positif dan negatif pada kehidupan
manusia. Salah satu dampak negatif industri pada kesehatan wanita adalah
kegagalan ovarium dini akibat paparan kronis zat ovotoksik. Ovotoksisitas
merupakan salah satu penyebab kegagalan ovarium dini (premature ovarian
failure). Premature ovarian failure ditandai dengan amenore, hipoestrogen
dan peningkatan kadar hormon gonadotropin yang menetap sebelum usia 40
tahun. Wanita yang menderita premature ovarian failure akan mengalami
gejala-gejala menopause (Shelling, 2010; Shuster et al, 2010). Menopause
berkaitan erat dengan berbagai masalah kesehatan (Hu, et al., 2001).
Premature ovarian failure (POF) atau menopause dini adalah suatu
keadaan dimana terjadi amenorhea yang disebabkan oleh berhentinya fungsi
ovarium sebelum usia 40 tahun. Wanita dengan POF mengalami anovulasi
dan hipoestrogenisme dengan adanya amenorhea primer atau sekunder,
infertilitas, defisiensi hormon steroid sex, dan peningkatan gonadotropin
(Conway, 2000). Rata-rata usia menopause wanita eropa adalah sekitar 51
tahun. Namun, 1-3% dari seluruh wanita mengalami POF, termasuk di
dalamnya 10-28% dari wanita dengan amenorhea primer dan 4-18% dari
wanita yang mengalami amenorhea sekunder (Lanying, 2001). Sebagian
commit to user
Beberapa agen kimia bersifat toksik terhadap ovarium yang dapat
menginduksi kerusakan folikel dan mengakibatkan kegagalan ovarium dini.
Paparan agen ovotoksik ini bermanifestasi pada risiko jangka panjang terkait
kegagalan ovarium dini pada wanita (Hu et al., 2001). Pada studi ini peneliti
mencoba merancang suatu hewan model untuk menyerupai kondisi alami
proses menopause pada wanita. Peneliti melakukan induksi agen kimia yang
bersifat ovotoksik, 4-vinylcyclohexane diepoxide (VCD) pada tikus galur
Wistar untuk mempelajari proses kerusakan pada ovarium. VCD merupakan
hasil metabolit dari 4-vinylcyclohexane (VCH) yang didapatkan sebagai agen
hasil manufaktur pada pembuatan pestisida, bahan berbasis karet, dan plastik.
Agen kimia ini mempunyai selektifitas untuk merusak folikel primordial dan
primer pada ovarium melalui proses induksi atresia secara alami (Hoyer dan
Sipes, 2007).
Tikus betina galur Wistar yang diinduksi dengan VCD secara
intraperitoneal dapat digunakan untuk mengetahui proses kegagalan ovarium
melalui atresia. Pada studi ini dilakukan evaluasi kadar estrogen, gambaran
morfologis folikel ovarium beserta stroma ovariumnya, ekspresi estrogen
reseptor alfa dan caspase 3 secara imunohistokimia.
Pada studi ini peneliti mencoba meneliti toksisitas 4-vynilcyclohexene
diepoxide (VCD) terhadap stroma untuk merancang suatu hewan model
untuk menyerupai kondisi alami proses menopause, sehingga dapat
commit to user B. Rumusan Masalah
Berdasar uraian diatas dapat dirumuskan untuk masalah penelitian
yaitu: Apakah 4-vynilcyclohexene diepoxide (VCD) dosis 80 mg/KgBB dan
160 mg/KgBB menyebabkan kerusakan stroma ovarium?
C. Tujuan penelitian
1. Tujuan Umum
Untuk melihat efek toksisitas 4-vynilcyclohexene diepoxide (VCD)
terhadap stroma ovarium pada tikus.
2. Tujuan Khusus
Mengetahui toksisitas 4-vynilcyclohexene diepoxide (VCD) terhadap
stroma ovarium.
D. Manfaat Penelitian
1. Manfaat teoritis
Memberikan pengetahuan tentang pengaruh 4-vynilcyclohexene
diepoxide (VCD) terhadap jaringan stroma yang dapat digunakan untuk
memperkaya khasanah keilmuan.
2. Manfaat Klinis
Menambah pengetahuan tentang pemeriksaan laboratorium
biomolekuler gambaran jaringan stroma ovarium akibat paparan
4-vynilcyclohexene diepoxide (VCD) sehingga dapat digunakan untuk
commit to user BAB II
TINJAUAN PUSTAKA
A.Stroma Ovarium
Sistem reproduksi wanita terdiri dari ovarium, tuba uterina, uterus,
vagina, dan genitalia eksterna. Ovarium berwarna putih dan terdiri dari
jaringan fibrosa yang tebal yang menjadi tempat melekatnya ovum. Ovarium
pada wanita dewasa berukuran panjang kira – kira 4 cm, lebar dan tebal kurang
lebih 1,5 cm (Sarwono, 2008).
Ovarium terletak pada lapisan belakang ligamentum latum. Sebagian
besar ovarium berada intraperitoneal dan tidak dilapisi oleh peritoneum.
Ovarium terhubung ke uterus dengan ligamentum ovarii propium. Dan
pembuluh darah ke ovarium melalui ligamentum suspensorium ovarii.
Ovarium merupakan tempat berkembangnya folikel-folikel hingga menjadi
folikel de Graaf, yang akhirnya akan melepaskan ovum saat wanita mengalami
ovulasi. Ovarium diliputi oleh epitel coelom yang dapat berubah menjadi epitel
torak berambut getar, yang memproduksi cairan jernih seperti ditemukan
dalam tuba atau epitel tidak berambut getar yang memproduksi musin seperti
pada endometrium (Bychkov, 2002).
Sebagian besar dari ovarium, baik korteks maupun medula, terdiri dari
stroma. Stroma ovarium terdiri dari sel-sel yang berbentuk spindel yang mirip
dengan fibroblas dan tersusun dalam suatu bentukan yang khas. Tidak seperti
commit to user
serat yang menyokongnya (baik serat retikuler maupun jaringan kolagen biasa).
Sel-sel terdiri atas cytoplasmic lipid dan dikelilingi oleh suatu serat retikulin.
Beberapa sel menyerupai gambaran seperti miofibroblastik dan immunoreaktif
dengan smooth muscle actin (SMA) dan desmin. Sel-sel stroma ovarium
berhubungan dengan pematangan folikel, yang juga berkaitan erat dengan
fungsi endokrin dan sekresi estrogen (Ganong, 2005).
1. Endokrinologi ovarium
Dalam endokrinologi reproduksi wanita, ovarium memiliki dua fungsi
utama, yaitu fungsi proliferatif dan fungsi sekretorik. Sebagai fungsi
proliferatif (generatif), ovarium merupakan sumber ovum selama masa
reproduksi. Di dalam ovarium terjadi petumbuhan folikel primer, folikel de
Graaf, peristiwa ovulasi, serta pembentukan corpus luteum. Sedangkan
sebagai fungsi sekretorik (vegetatif), ovarium merupakan tempat
pembentukan dan pengeluaran hormon steroid yaitu hormon estrogen,
progesteron, dan androgen (Sarwono, 2008).
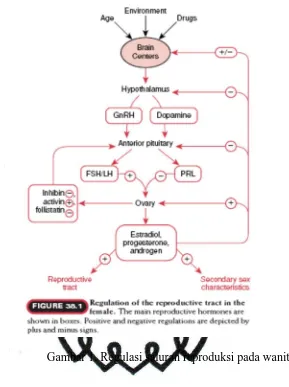
Pandangan umum dari interaksi faktor-faktor hormon pada sistem
reproduksi wanita ditunjukkan pada gambar 1. Sistem hormon wanita terdiri
dari otak, hipofise, ovarium, dan organ reproduksi ( tuba, uterus, cerviks dan
vagina). Didalam otak, hipotalamus menghasilkan gonadotropin releasing
hormone (GnRH) yang mengatur sekresi luteinizing hormone (LH) dan
commit to user
Gambar 1. Regulasi saluran reproduksi pada wanita
Ovarium matur mempunyai dua fungsi utama yaitu, maturasi sel
germinal ( folikulogenesis) dan steroidogenesis. Tiap sel germinal pada
akhirnya berkembang didalam folikel, yang merupakan sumber utama
penghasil hormone steroid selama siklus menstruasi. Saat ovulasi, ovum
dilepaskan dan folikel yang pecah berubah menjadi korpus luteum, yang
mensekresi progesteron. FSH terutama berperan pada stimulasi
perkembangan folikel ovarium, sedangkan LH memicu terjadinya ovulasi.
FSH dan LH mengatur steroidogenesis di folikel dan sekresi androgen dan
commit to user
ovarium akan menghambat sekresi LH dan FSH kecuali pada saat akan terjadi
ovulasi ( midcycle), estradiol menyebabkan umpan balik positif pada aksis
hipotalalamus- hipofisis dan secara bermakna memicu peningkatan sekresi
GnRH, LH dan FSH. Ovarium juga menghasilkan tiga hormone polipeptida
yaitu inhibin yang menekan sekresi FSH, activin (activin-binding protein)
meningkatkan sekresi FSH, dan follistatin (activin-binding protein) yang
menurunkan sekresi FSH (Speroff, 2005; Hutt et al, 2005).
2. Folikulogenesis
a. Ovarium Dewasa
Ovarium berisi tiga bagian yaitu korteks luar, medulla di sentral
dan pintu ovarium (hillus). Hillus berisi pembuluh syaraf, pembuluh
darah dan sel hillus yang menjadi aktif dalam proses steroidogenesis atau
mampu membentuk tumor. Sel ini sangat mirip dengan sel leydig di testis
yang memproduksi testosteron. Bagian korteks yang paling luar disebut
tunika albuginea, yang bagian atasnya ditutupi oleh satu lapis sel kuboid.
Oosit berhubungan dengan kompleks yang disebut folikel. Bagian dalam
korteks tertanam dekat dengan jaringan stroma. Jaringan stroma terdiri
atas jaringan penunjang dan sel interstitial yang berasal dari sel
mesenkim dan mempunyai kemampuan untuk berespon terhadap
luteinizing hormone (LH ) atau human chorionic gonadotropin ( hCG )
dan produksi androgen. Daerah tengah medulla dari ovarium sebagian
commit to user
Gambar 2. Skematik Masa Perkembangan Ovarium pada Fetus dan Dewasa
commit to user b. Ovarium tikus
Pada masa perkembangan ovarium tikus dari lahir hingga dewasa,
terjadi perubahan dari organ simpel menjadi organ yang multiform. Dalam
perkembangannya, pada ovarium terjadi pertumbuhan, differensiasi, serta
degenerasi.
Ovarium pada waktu tikus lahir terdiri dari 2 tipe sel utama, yaitu
oosit dan sel stroma multipotensial. Disebut multipotensial karena secara
morfologi, sel ini akan berdifferensiasi menjadi berbagai sel penyokong
antara lain sel granulosa, sel teka baik interna maupun eksterna, sel lutein,
serta bentuk sel yang lain (Schwiebert, 2007).
Pada saat lahir, ovarium tikus merupakan organ solid yang berisi
penuh dengan sel germinal dan sel stroma. Organ ini dilapisi oleh adanya
sel-sel epitel yang disebut sebagai epitel germinal walaupun sebenarnya
epitel ini bukan merupakan bagian dari sel germinal. Oosit mengisi
sebagian besar organ, kecuali bagian tengah dari pusat stroma.
Usia pubertas tikus bervariasi tergantung pada jenis tikus, status
nutrisi, serta adanya pengaruh lingkungan, namun secara umum pubertas
tikus terjadi pada usia antara 28 hingga 49 hari. Tanda-tanda terjadinya
pubertas pada tikus betina adalah adanya pembukaan vagina dan
munculnya sel epitel terkornifikasi pada vaginal smear. Fertilitas pada
tikus betina paling banyak terjadi pada usia 75 hingga 300 hari.
Tikus merupakan organisme yang polyestrous. Tikus betina akan
commit to user
biasanya terjadi pada malam hari. Ovulasi terjadi secara spontan, biasanya
terjadi 8-11 jam setelah onset estrus, namun ovulasi tidak selalu terjadi
pada setiap siklus estrus. Pap vagina digunakan untuk menentukan tahap
siklus estrus. Kopulasi pada tikus biasanya terjadi pada malam hari dan
dapat dikonfirmasi dengan adanya plug senggama di vagina selama 12-24
jam pasca kopulasi (Schwiebert, 2007).
Sel-sel germinal folikel primordial akan berproliferasi dan migrasi
ke dalam gonad yang belum berdiferensiasi. Pada periode post natal,
sel-sel germinal akan terpecah dan menjadi folikel primordial yang terus
berkembang menjadi folikel primer. Estrogen (E2) menghambat sel
germinal menjadi folikel primordial. Pada tikus yang kekurangan
faktor-faktor transkripsi oosit seperti NOBOX, SOHLH1, SOHLH2, and LHX8,
maka akan terjadi kematian folikel, baik folikel primordial maupun folikel
primer. Kematian dapat pula terjadi bahkan sebelum terbentuk folikel
primordial (Richards dan Pangas, 2010).
Secara morfologi, pembentukan ovarium pada tikus betina tidak
aktif, namun kejadian di tingkat molekuler paling banyak terjadi pada
tahap gonadogenesis. Terdapat lebih dari 1200 ekspresi gen yang mengatur
perkembangan gonad tikus betina pada hari ke-10 sampai hari ke-13 post
koital. Periode tersebut menentukan diferensiasi jenis kelamin gonadal
tikus. Peningkatan ekspresi penghambat siklus sel (seperti inhibitor
cyclin-dependen kinase) dan beberapa gen penanda meiosis terjadi pada gonad
commit to user
proliferasi sel somatik dihambat ketika se-sel germinal ovarium memasuki
tahap meiosis (Uzumchu dan Zachow, 2007).
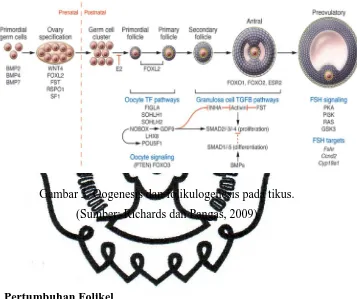
Gambar 3. Oogenesis dan folikulogenesis pada tikus.
(Sumber: Richards dan Pangas, 2009)
3. Pertumbuhan Folikel
Seperti pada masa pubertas, pada ovarium dewasa terjadi stadium
pembentukan folikel yang akan terus berulang. Pada awalnya oosit akan
membesar dan sel granulosa berproliferasi. Pada sat ini oosit berbentuk
masa bulat yang solid. Teka interna akan terbentuk pada stadium awal.
Zona pellucida mulai terbentuk (Calvanesea, et al, 2005).
Sekarang diketahui bahwa proses pembentukan folikel primer
sampai ovulasi berlangsung selama 85 hari. Pada masa ini tidak tergantung
gonadotropin sehingga kemudian mencapai keadaan yang siap untuk
commit to user
peningkatan gonadotropin seperti yang terlihat pada awal siklus haid, akan
terlihat pematangan folikel yang tergantung pada FSH. Jumlah folikel
yang matur tergantung pada jumlah FSH dan sensitifitas folikel terhadap
gonadotropin. Ekspresi reseptor FSH paling banyak pada sel granulosa,
namun bisa juga dijumpai pada epitel di permukaan ovarium dan epitel
tuba fallopii, yang fungsinya belum diketahui, tapi diduga berperan pada
tumor epitelial (Gosden, et al, 2009).
Pertama kali antrum terlihat sebagai sejumlah kavum intragranulosa
yang disebut badan cell – exner yang digambarkan oleh Emma Call dan
Siegmund Exner di Vienna pada tahun 1875. Pada satu titik saat
pembentukan ini, folikel akan terhenti dan mengalami proses apoptosis
yang dikenal sebagai atresia. Pada awalnya, komponen sel granulosa mulai
mengalami perpecahan. Kavum antral akan diserap dan kavum akan
kolaps dan mengalami obliterasi. Oosit akan berdegenerasi in situ.
Akhirnya, jaringan parut yang berbentuk pita yang berada disekitar sel
teka akan terlihat. Terkadang masa sel teka akan mengalami kehilangan
lipid dan sulit dibedakan dengan massa stroma yang sedang tumbuh. Oleh
karena itu, proses apoptosis akan berlanjut pada granulosa dan lapisan teka
merupakan bagian terbesar dari jaringan interstitial. Sebelum mengalami
regresi, folikel kistik akan berada di korteks untuk beberapa saat. (Speroff,
commit to user 4. Peran Stroma pada Fungsi Ovarium
Sebagian besar dari ovarium, baik korteks maupun medula,
terdiri dari stroma. Stroma ovarium terdiri dari sel-sel yang berbentuk
spindel yang mirip dengan fibroblas dan tersusun dalam suatu
bentukan yang khas. Tidak seperti jaringan ikat pada umumnya,
stroma ovarium tersusun dari banyak sel dengan serat yang
menyokongnya (baik serat retikuler maupun jaringan kolagen biasa).
Sel-sel terdiri atas cytoplasmic lipid dan dikelilingi oleh suatu serat
retikulin. Beberapa sel menyerupai gambaran seperti miofibroblastik
dan immunoreaktif dengan smooth muscle actin (SMA) dan desmin.
Sel-sel stroma ovarium berhubungan dengan pematangan folikel, yang
juga berkaitan erat dengan fungsi endokrin dan sekresi estrogen.
Selama perkembangan folikel, stroma ovarium yang
mengelilingi folikel tersebut akan berdiferensiasi menjadi teka interna
dan teka eksterna. Proses ini mulai berlangsung pada saat janin dalam
kandungan dan berakhir setelah menopause. Teka interna biasanya
terdiri dari tiga atau empat lapisan yang berbatasan dengan struktur
granulosa. Sedangkan struktur stroma yang lain dengan batas yang
kurang begitu jelas diantara folikel disebut sebagai teka eksterna (Hall
& Guyton, 2006).
Teka interna pada folikel yang berkembang merupakan jaringan
yang kaya akan vaskularisasi terdiri dari kapiler-kapiler yang dilatasi
commit to user
bentuk yang bervariasi dari bulat hingga berbentuk poligonal, dengan
diameter antara 12-20 um, berwarna kemerahan dan bersitoplasma
jernih dengan adanya vakuola dan nukleus di bagian sentral.
Teka interna merupakan jaringan yang menyokong
perkembangan folikel karena merupakan tempat terjadinya
steroidogenesis. Namun, fungsi endokrin dari sel teka eksterna masih
belum diketahui secara pasti. Sel teka interna pada folikel adalah
sumber utama estrogen dalam darah dimana terdiri dari tetesan lipid,
retikulum endoplasma yang halus dan luas, dan mitokondria yang
memiliki krista tubuler. Androgen dari sel teka diproses menjadi
estrogen dalam sel granuloma. Estrogen yang dihasilkan dari
granuloma ini kemudian memasuki sirkulasi (Ganong, 2005).
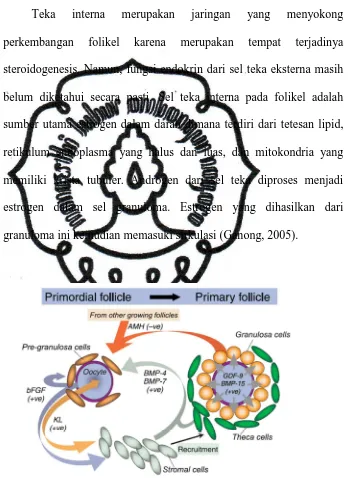
Gambar 4. Aktivitas sekresi faktor pertumbuhan.
commit to user 5. Kategori Kerusakan Stroma Ovarium
Stroma ovarium merupakan jaringan penyokong yang
memungkinkan ovarium untuk menjalankan fungsi normalnya. Kerusakan
yang terjadi pada stroma dapat berpengaruh pada fungsi ovarium. Pada
Premature Ovarian Failure (POF), kerusakan folikel terjadi karena adanya
proses apoptosis folikel itu sendiri. Tidak terjadi kerusakan pada jaringan
penyokong ovarium (stroma). Akan tetapi kerusakan pada stroma dapat
pula menyebabkan terjadinya keadaan yang mirip dengan POF, yaitu
terjadinya kerusakan folikel.
Perubahan-perubahan yang dapat terjadi pada kerusakan stroma
antara lain adalah terjadinya pembesaran fibroblas, hyalinisasi yang
prominen, dan terjadinya penyempitan pembuluh darah.
a. Fibrotik
Salah satu kemungkinan kerusakan yang dapat terjadi pada stroma
ovarium adalah terjadinya proses hyalinisasi yang prominen dan
berakhir pada proses fibrotik. Proses ini dikaitkan dengan adanya
inflamasi, nekrosis lemak, histosit yang berbusa, pembentukan plak
kolesterol, serta pembentukan makrofag hemosiderin.
Pada beberapa keadaan misalnya pemberian kemoterapi pada
pasien kanker, agen kemoterapi yang diberikan dapat berpengaruh pada
jaringan ovarium yang dapat menimbulkan terjadinya respon inflamasi
jaringan. Akibatnya inti sel membengkak, pleomorfik, dan
commit to user
Sitoplasma sel menjadi granular, bervakuola, dan terjadi dilatasi serta
kerusakan pada pada organela sitoplasma yang dihubungkan dengan
terjadinya destruksi lisosom (Chew et al., 2009).
b. Kekosongan area stroma
Kerusakan pada stroma ovarium dapat menyebabkan penurunan
fungsi jaringan stroma. Penurunan ini terutama terjadi jika didapatkan
adanya perubahan morfologi jaringan stroma. Penelitian yang dilakukan
pada domba dan kambing mengenai kerusakan folikel dan stroma
menunjukkan beberapa perubahan yang terjadi pada kerusakan stroma
ovarium. Diantara perubahan itu adalah terjadinya lisis membran sel
stroma, nekrosis stroma yang dikaitkan dengan adanya kekosongan area
jaringan stroma, serta terjadinya penurunan densitas kolagen dan fibrin
pada jaringan ovairum karena terjadinya kerusakan pada struktur
folikuler (Faustino et al., 2010).
c. Penyempitan pembuluh darah
Suplai darah ke ovarium merupakan suatu sistem end artery, yaitu
tidak didapatkan adanya sistem anastomose. Karena keadaan ini,
apabila terjadi penyempitan atau penyumbatan pembuluh darah akan
mengakibatkan hilangnya aliran darah ke ovarium. Kurangnya suplai
darah ini akan menyebabkan terjadinya fokal fibrosis. Selain itu,
kurangnya suplai darah ke ovarium akan menyebabkan penurunan
jumlah folikel premordial ovarium yang tampak terutama pada daerah
commit to user
Kerusakan dan obstruksi pembuluh darah ovarium dapat
menyebabkan terjadinya iskemia lokal yang berefek pada penghancuran
segmental pada korteks ovarium normal serta terjadinya penurunan
jumlah folikel premordial yang signifikan. Korteks ovarium yang rusak
tersebut akan digantikan oleh jaringan fibrotik dengan disertai
hilangnya fungsi normal ovarium. Apabila keadaan ini terjadi pada
seluruh korteks ovarium, maka akan dimungkinkan ovarium untuk
kehilangan seluruh cadangan folikel premordial yang dimilikinya dan
seluruh jaringan korteks ovarium akan digantikan dengan jaringan
parut. Keadaan ini merupakan suatu kerusakan ovarium total yang
permanen (Meirow, et al., 2007).
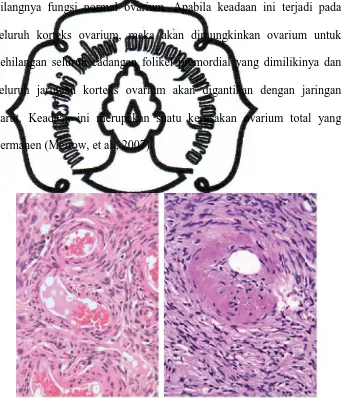
Gambar 5. penyempitan pembuluh darah yang terjadi pada pembuluh darah
ovarium (kiri), dan gambaran pembuluh darah ovarium normal (kanan).
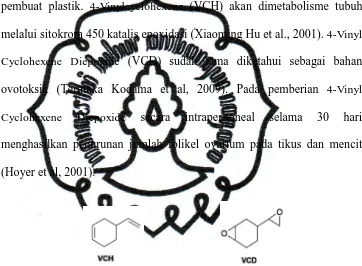
commit to user B. 4- VynilcyclohexeneDiepoxide (VCD)
1. Definisi
4-Vinyl Cyclohexene Diepoxide (VCD) adalah hasil metabolisme
dari 4-Vinylcyclohexene (VCH). 4-Vinylcyclohexene (VCH) terbentuk dari
dimerisasi dari 1,3-butadin pada perusahaan karet sintetis, insektisida,
pembuat plastik. 4-Vinylcyclohexene (VCH) akan dimetabolisme tubuh
melalui sitokrom 450 katalis epoxidasi (Xiaoming Hu et al., 2001). 4-Vinyl
Cyclohexene Diepoxide (VCD) sudah lama diketahui sebagai bahan
ovotoksik (Terutaka Kodama et al, 2009). Pada pemberian 4-Vinyl
Cyclohexene Diepoxide secara intraperitoneal selama 30 hari
menghasilkan penurunan jumlah folikel ovarium pada tikus dan mencit
(Hoyer et al, 2001).
VCH: Rumus kimia= C8H12, Berat molekul= 108,18
VCD: Rumus kimia= C8H12O2, Berat molekul= 140,18
Gambar 6. Sruktur kimia 4- vynilcyclohexene dan 4-vynilcyclohexene diepoxide.
(Sumber: Keating et al, 2008)
2. Mekanisme Seluler Ovotoksisitas
Peran VCD dalam menghasilkan kerusakan luas pada folikel telah
lama diidentifikasi. Pemberian VCD secara langsung akan merusak folikel
commit to user
menyebabkan penurunan jumlah folikel secara signifikan (Hoyer dan
Sipes, 2007). Pada ovarium mamalia, jumlah folikel primordial yang dapat
berkembang sampai ovulasi jumlahnya kecil, karena kebanyakan dari sel
tersebut akan mengalami atresia, kematian sel ini disebut apoptosis yang
terjadi secara fisiologis dan berbeda dengan nekrosis yang merupakan
respon terhadap jejas atau inflamasi. Apoptosis dan nekrosis berbeda
dalam karakteristik morfologi. Perbandingan perubahan ultrastruktur pada
folikel preantral kontrol dan yang diberi VCD menunjukan bahwa
gambaran oosit dalam folikel yang tidak sehat pada kedua kelompok sama.
Termasuk gangguan organela, peningkatan jumlah vakuola, akumulasi
komponen membran, dan segmentasi abnormal (cleavage). Gambaran
morfologi degenerasi selama atresia, tidak berubah pada pemberian VCD
tetapi VCD meningkatkan proses ini dan atresia terjadi dalam frekuensi
yang lebih tinggi (Hoyer et al, 2001).
Meskipun karakteristik morfologi merupakan metode yang paling
reliabel untuk membedakan antara apoptosis dan nekrosis, juga dapat
dibedakan dengan petanda biokimia dan molekuler. Salah satu gen pada
mamalia yang berkaitan secara spesifik dengan apoptosis adalah Bcl-2
yang bersifat proto-onkogen. Bcl-2 telah diidentifikasi pada membran luar
mitokondria, retikulum endoplasma, membran inti, dan berhubungan
dengan lamanya sel bertahan hidup. Gen lain dari famili Bcl-2 adalah Bax
yang rangkaiannya homolog. Rasio protein Bax terhadap Bcl-2 dalam sel
commit to user
akan bertahan hidup (rasio menurun) (Hsu dan Hsueh, 2000). Pengamatan
terhadap jumlah protein bax pada mRNA yang mengkode kematian sel
menunjukan terdapat peningkatan signifikan jumlah protein Bax
dibandingkan dengan kontrol (sebanyak 72 %, p < 0.005) pada 10 hari
pemberian VCD. Hal ini memberikan bukti keterlibatan bax protein dalam
ovotoksisitas yang diinduksi oleh VCD dan mendukung hipotesis kematian
sel yang disebabkan oleh VCD terjadi melalui apoptosis (Hoyer et al,
2001).
3. Mekanisme Molekuler Ovotoksisitas
Ovarium mengandung berbagai macam enzim yang bertugas untuk
melakukan biotransformasi dan detoksifikasi berbagai bahan ovotoksik.
Enzim tersebut diantaranya epoxidehydrolase, glutathione S-transferases,
dan cytochrome P-450 (Johnson et al., 2004). Mekanisme enzimatik utama
detoksifikasi adalah hidrasi untuk membentuk diol (yang dikatalisis oleh
microsomalepoxidehydrolase) dan konjugasi dengan gluttion (yang
dikatalisis oleh glutathione S-transferase). Pada studi isolasi in vitro folikel
ovarium diketahui bahwa folikel ovarium dapat mengubah secara langsung
VCD menjadi bentuk inaktif tetrol yaitu 4-(1,2- dihydroxy)
ethyl-1,2-dihydroxycyclohexane. Namun jika dibandingkan dengan folikel ovarium
dengan ukuran lebih besar, folikel ovarium kecil menunjukan kapasitas
paling rendah dalam detoksifikasi VCD, sehingga hal ini membuat folikel
preantral kecil sebagai target utama ovotksisitas VCD (Muhammad et al.,
commit to user
Antioksidan secara alami terdapat dalam sel, termasuk ovarium
seperti glutathione peroxidase, superoxide dismutase (SOD), dan katalase.
Antioksidan ini berfungsi sebagai enzim yang berespon terhadap stress
oksidatif karena melindungi sel dari efek merusak dari reactive oxygen
species dan apoptosis. Terdapat 3 isoform Superoxide Dismutase, yaitu
Manganese Superoxide Dismutase yang terdapat pada mitochondria,
copper/zinc Superoxide Dismutase yang terdapat pada sitosol, dan secreted
Superoxide Dismutase yang disekresikan ke ruang ektstraseluler.
Peningkatan masing-masing isoform ini memberi petunjuk terhadap
komponen molekuler yang terlibat.
Pemberian VCD meningkatkan level mRNA Manganese Superoxide
Dismutase folikel kecil 148 %, sedangkan peningkatan pada Cu
Superoxide Dismutase dan Zn Superoxide Dismutase sekresi tidak
meningkat secara bermakna. Sebaliknya pada folikel besar, tidak terjadi
efek, hal ini disebabkan tidak terjadi proses stress oksidatif pada folikel
besar. Hal ini memberikan bukti bahwa ovotoksisitas yang disebabkan
VCD pada folikel kecil terjadi pada mitokondria. Pada kondisi apoptosis,
Manganese Superoxide Dismutase juga meningkat secara signifikan,
sehingga memberi bukti tambahan bahwa proses ovotoksisitas VCD
terhadap ovarium menyerupai menopause (Haas et al., 2007).
Pada mitokondria, juga ada bax protein yang terdapat dalam
membran mitokondria. Bax protein terlibat dalam meningkatkan apoptosis
commit to user
pada folikel kecil didapatkan peningkatan ekspresi mRNA bax protein. Hal
ini juga memberikan bukti tambahan keterlibatan mitokondria intraseluler
terhadap apoptosis yang diinduksi oleh VCD. Kerusakan membran
mitokondria yang diinduksi oleh bax protein mengakibatkan kerusakan sel
yang dapat menyebabkan kebocoran sitokrom c protein dari mitokondria
ke sitosol. Pada sebuah studi, dimana dilakukan pengamatan dan analisis
ovarium yang telah diinduksi VCD menggunakan mikroskop confocal
dengan imuniohistokimia, didapatkan penurunan jumlah folikel, pada
pewarnaan khusus yang berikatan dengan sitokrom c protein mitokondria,
juga didapatkan peningkatan dan terlihat difus. Pada kondisi normal,
sitokrom c protein terlihat fokus dengan intensitas lebih tinggi namun
terlokalisasi pada mitokondria, sedangkan gambaran difus terjadi karena
sitokrom c protein menyebar ke sitoplasma (Mayer et al., 2002).
Pada apoptosis terjadi aktivasi dari enzim proteolitik caspase 3,
demikian juga pada induksi VCD pada ovarium. Aktivasi caspase 3 terjadi
pada sitosol selama induksi apoptosis, namun aktivasi caspase 3 juga dapat
disebabkan oleh kejadian lain, salah satunya adalah pecahnya mitokondria.
Inisiasi ini oleh sitokrom c protein yang dilepaskan mitokondria. Hal ini
dibuktikan oleh penelitian dimana didapatkan peningkatan aktivitas
caspase 3 pada folikel ovarium kecil dibandingkan kontrol dan folikel
ovarium besar (Takai, 2003).
Dari paparan diatas dapat disimpulkan bahwa target dari
commit to user
ovarium kecil. Dan induksi VCD menyebabkan aktivasi mekanisme
apoptosis yang terlihat pada Manganese Superoxide Dismutase, bax
protein, sitokrom c protein, dan caspase 3.
4. Apoptosis pada Ovarium oleh Pengaruh VCD
Ovarium mengandung berbagai macam enzim yang bertugas untuk
melakukan biotransformasi dan detoksifikasi berbagai bahan ovotoksik.
Enzim tersebut diantaranya epoxidehydrolase, glutathione S-transferases,
dan cytochrome P-450. Mekanisme enzimatik utama detoksifikasi adalah
hidrasi untuk membentuk diol (yang dikatalisis oleh
microsomalepoxidehydrolase) dan konjugasi dengan gluttion (yang
dikatalisis oleh glutathione S-transferase). Pada studi isolasi in vitro folikel
ovarium diketahui bahwa folikel ovarium pada dapat mengubah secara
langsung VCD menjadi bentuk inaktif tetrol yaitu 4-(1,2- dihydroxy)
ethyl-1,2-dihydroxycyclohexane. Namun jika dibandingkan dengan folikel
ovarium dengan ukuran lebih besar, folikel ovarium kecil menunjukan
kapasitas paling rendah dalam detoksifikasi VCD, sehingga hal ini
membuat folikel preantral kecil sebagai target utama ovotksisitas VCD
(Devine et al., 2004).
Antioksidan secara alami terdapat dalam sel, termasuk ovarium
seperti glutathione peroxidase, superoxide dismutase (SOD), dan katalase.
Antioksidan ini berfungsi sebagai enzim yang berespon terhadap stress
commit to user
species dan apoptosis. Terdapat 3 isoform Superoxide Dismutase, yaitu
Manganese Superoxide Dismutase yang terdapat pada mitochondria,
copper/zinc Superoxide Dismutase yang terdapat pada sitosol, dan secreted
Superoxide Dismutase yang disekresikan ke ruang ektstraseluler.
Peningkatan masing-masing isoform ini member petunjuk terhadap
komponen molekuler yang terlibat (Forabosco dan Sforza, 2007).
Pemberian VCD meningkatkan level mRNA Manganese Superoxide
Dismutase folikel kecil 148 %, sedangkan peningkatan pada Cu/Zn
Superoxide Dismutase dan Superoxide Dismutase sekresi tidak meningkat
secara bermakna. Sebaliknya pada foikel besar, tidak terjadi efek, hal ini
disebabkan tidak terjadi proses stress oksidatif pada folikel besar. Hal ini
memberikan bukti bahwa ovotoksisitas yang disebabkan VCD pada folikel
kecil terjadi pada mitokondria. Pada kondisi apoptosis, Manganese
Superoxide Dismutase juga meningkat secara signifikan, sehingga member
bukti tambahan bahwa proses ovotoksisitas VCD terhadap ovarium
menyerupai menopause (Di Pasquale, et al., 2004).
Pada mitokondria, juga ada bax protein yang terdapat dalam
membrane mitokondria. Bax protein terlibat dalam meningkatkan
apoptosis melalui interaksi dengan membrane mitokondria. Pada
pemberian VCD, pada folikel kecil didapatkan peningkatan ekspresi
mRNA bax protein. Hal ini juga memberikan bukti tambahan keterlibatan
mitokondria intraseluler terhadap apoptosis yang diinduksi oleh VCD.
commit to user
mengakibatkan kerusakan sel yang dapat menyebabkan kebocoran
sitokrom c protein dari mitokondria ke sitosol. Pada sebuah studi, dimana
dilakukan pengamatan dan analisis ovarium yang telah diinduksi VCD
menggunakan mikroskop confocal dengan imuniohistokimia, didapatkan
penurunan jumlah folikel, pada pewarnaan khusus yang berikatan dengan
sitokrom c protein mitokondria, juga didapatkan peningkatan dan terlihat
difus. Pada kondisi normal, sitokrom c protein terlihat focus dengan
intensitas lebih tinggi namun terlokalisasi pada mitokondria, sedangkan
gambaran difus terjadi karena sitokrom c protein menyebar ke sitoplasma
(Falcone, et al., 2004).
Pada apoptosis terjadi aktivasi dari enzim proteolitik caspase 3,
demikian juga pada induksi VCD pada ovarium. Aktivasi caspase 3 terjadi
pada sitosol selama induksi apoptosis, namun aktivasi caspase 3 juga dapat
disebabkan oleh kejadian lain, salah satunya adalah pecahnya mitokondria.
Inisiasi ini oleh sitokrom c protin yang dilepaskan mitokondria. Hal ini
dibuktikan oleh studi dimana didapatkan peningkatan aktivitas caspase 3
pada folikel ovarium kecil dibandingkan control dan folikel ovarium besar.
Dari paparan diatas dapat disimpulkan bahwa target dari pada
ovotoksisitas yang induksi VCD adalah mitokondria, terutama pada folikel
ovarium kecil. Dan induksi VCD menyebabkan aktivasi mekanisme
apoptosis yang terlihat pada Manganese Superoxide Dismutase, bax
commit to user
Ketika terjadi deplesi folikel primordial pada ovarium, maka akan
terjadi menopause pada wanita. Karena ovarium mengandung oosit dalam
jumlah yang terbatas ketika lahir, maka paparan bahan kimia lingkungan
dapat menghancurkan folikel primordial sehingga dapat menimbulkan
menopause lebih dini.
5. Premature Ovarian Failure (POF)
a. Definisi dan Epidemiologi
Premature ovarian failure (POF) atau dapat disebut pula
menopause dini adalah suatu keadaan dimana terjadi amenorhea yang
disebabkan oleh berhentinya fungsi ovarium sebelum usia 40 tahun.
Wanita dengan POF mengalami anovulasi dan hipoestrogenisme dengan
adanya amenorhea primer atau sekunder, infertilitas, defisiensi hormon
steroid sex, dan peningkatan gonadotropin (Conway, 2000). Rata-rata
usia menopause wanita eropa adalah sekitar 51 tahun. Namun, 1-3% dari
seluruh wanita mengalami POF, termasuk di dalamnya 10-28% dari
wanita dengan amenorhea primer dan 4-18% dari wanita yang
mengalami amenorhea sekunder (Lanying, 2001).
Menopause dini ditunjukkan dengan amenorhea dan peningkatan
hormon gonadotropin yang disebabkan oleh penurunan jumlah total oosit
dalam ovarium, dan oleh karenanya, kemungkinan untuk kembalinya
fungsi ovarium seperti sebelumnya menjadi tidak ada (Dixit et al., 2004).
commit to user
follicle stimulating hormone (FSH) di atas 40 IU/L menunjukkan suatu
penurunan fungsi dan jumlah folikel ovarium yang permanen
(Letur-Konirsch, 2003). Namun pada beberapa penelitian selanjutnya ditemukan
peningkatan fungsi ovarium yang intermitten, bahkan hingga mengalami
kehamilan pada wanita yang telah didiagnosis POF (Akbari, 2011).
b. Etiologi
Sebagian besar kasus POF merupakan keadaan idiopatik. Meskipun
telah dilakukan berbagai penelitian namun sebagian besar kasus masih
belum didapatkan penyebab pastinya (Pal dan Santoro, 2002).
Sebelumnya, didapatkan anggapan bahwa terjadi deplesi pada folikel
ovarium pada semua kasus POF. Namun pada penelitian selanjutnya
diketahui bahwa tidak semua kasus POF terjadi deplesi folikel ovarium
(Hoyer, 2005). Beberapa kasus POF tidak terjadi deplesi folikel ovarium,
folikel tersebut masih ada, namun tidak responsif terhadap stimulasi
dengan meningkatkan hormon gonadotropin dalam sirkulasi (van
Kasteren, 2001). Secara umum, etiologi POF dapat dibagi menjadi dua
kelompok, yaitu hilangnya fungsi ovarium karena deplesi folikel, dan
hilangnya fungsi ovarium karena disfungsi folikel dalam ovarium.
Penyebab secara lebih rinci dapat dilihat pada tabel 1 berikut.
Tabel 1. Etiologi terjadinya Premature ovarian Failure (POF)
Folicle depletion
Chromosomal Abnormalities X Chromosome
commit to user
germinal bergerak keluar dari tabung urogenital menuju ke ovarium
primitif yang kemudian berproliferasi sehingga membentuk 3,5 juta oosit
tiap ovarium. Sebagian besar dari sel germinal ini hancur karena proses
apoptosis (Pru dan Tilly, 2001). Ovarium biasanya memiliki jumlah
commit to user
tiap ovarium. Jumlah ini akan terus berkurang selama hidup karena
adanya atresia dan terjadinya ovulasi (Forges et al., 2004). Tidak lebih
dari 500 oosit (0,007%) yang dikeluarkan melalui ovulasi selama masa
reproduktif seorang wanita (Conway, 2000).
Pada POF idiopatik, terjadi suatu mekanisme yang belum diketahui
secara pasti yang menyebabkan terjadinya peningkatan apoptosis oosit.
Hal ini dapat mendorong terjadinya penurunan komplemen oosit dalam
ovarium pada saat lahir, atau dapat mempercepat terjadinya atresia (Laml
et al., 2002).
d. Apoptosis
Apoptosis merupakan suatu komponen yang normal pada
perkembangan dan pemeliharaan kesehatan pada organisme multiseluler.
Sel yang mati ini merupakan respon terhadap berbagai stimulus dan
selama apoptosis sel ini dikontrol dan diregulasi, sel yang mati kemudian
difagosit oleh makrofag. Apoptosis berbeda dengan nekrosis, pada
nekrosis terjadi kematian sel tidak terkontrol. Sel yang mati pada
nekrosis akan membesar dan kemudian hancur dan lisis pada satu daerah
yang merupakan respon terhadap inflamasi (Abir, et al. 2004).
Pada apoptosis sel-sel yang mati memberikan sinyal yang
diperantarai oleh beberapa gen yang mengkode protein untuk enzym
pencernaan yang disebut dengan caspase. Gen caspase ini merupakan
bagian dari cystein protease yang akan aktif pada perkembangan sel
commit to user
Kematian sel melalui apoptosis merupakan fenomena yang normal, yaitu
terjadi eliminasi sel yang tidak diperlukan lagi. Proses apoptosis secara
fisiologis diperlukan untuk (Hoyer, 2005):
i. Terminasi sel
Apoptosis dapat terjadi pada sel yang mengalami kerusakan
yang tidak bisa di repair,infeksi virus, keadaan yang mengakibatkan
stress pada sel . Kerusakan DNA akibat ionisasi radiasi maupun bahan
kimia toxic juga dapat mencetuskan apoptosis melalui aktivasi tumor
supresor gen p53. Keputusan untuk apoptosis dapat berasal dari sel itu
sendiri, dari jaringan disekitarnya ataupun dari sel yang termasuk
dalam sisem imun.
ii. Mempertahankan homeostasis
Pada organisme dewasa, jumlah sel dalam suatu organ atau
jaringan harus berada dalam keadaan yang relatif konstan. Proses
keseimbangan ini termasuk dalam homeostasis yang dibutuhkan oleh
makhluk hidup untuk mempertahankan lingkungan internalnya.
Keseimbangan (homeostasis) ini dapat tercapai bila kecepatan mitosis
pada jaringan seimbang dengan kematian sel.
iii. Perkembangan embryonal
Kematian sel yang terprogram merupakan bagian dari
perkembangan jaringan. Pada masa embryo , perkembangan suatu
jaringan atau organ didahului oleh pembelahan sel dan diferensiasi sel
commit to user iv. Interaksi limfosit
Perkembangan limfosit B dan Limfosit T pada tubuh manusia
merupakan suatu proses yang kompleks , yang akan membuang sel-sel
yang berpotensi menjadi rusak. Cytotoksik T sel dapat secara
langsung menginduksi apoptosis pada sel melalui terbukanya suatu
celah pada target membran dan pelepasan zat-zat kimia untuk
mengawali proses apoptosis. Celah ini dapat terjadi melalui adanya
sekresi perforin, granul yang berisi granzyme B, serine protease yang
dapat mengaktivasi caspase melalui pemecahan residu aspartat.
v. Involusi hormonal
Apoptosis dapat terjadi misalnya pada pelepasan sel
endometrium selama siklus menstruasi, regresi pada payudara setelah
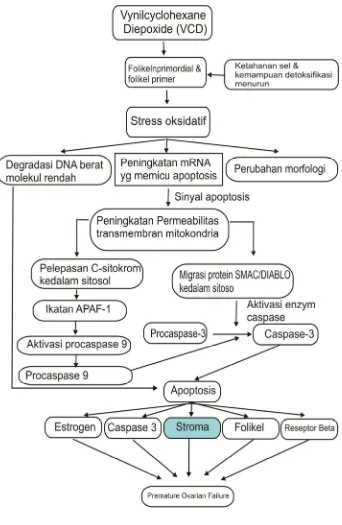
commit to user D. KERANGKA KONSEPTUAL
commit to user Keterangan Kerangka Konsep
4-Vinyl Cyclohexene Diepoxide (VCD) yang merupakan hasil
metabolisme dari 4-Vinylcyclohexene (VCH) adalah senyawa yang toksik
terhadap folikel ovarium. Pada folikel ovarium stadium antral, terjadi proses
detoksifikasi oleh enzim-enzim pelindung ovarium seperti epoxidehydrolase,
glutathione S-transferases, dan cytochrome P-450, yang dapat mengubah
VCD menjadi metabolit inaktif 4-(1,2- dihydroxy)
ethyl-1,2-dihydroxycyclohexane melalui proses hidrasi yang dikatalisasi oleh
microsomalepoxidehydrolase, dan konjugasi yang dikatalisis oleh glutathione
S-transferase).
Pada folikel yang lebih kecil, aktivitas enzim epoxidehydrolase,
glutathione S-transferases, dan cytochrome P-450 tidak sebesar aktivitasnya
pada folikel yang besar. Aktivitas yang lebih kecil ini tidak mampu untuk
mendetoksifikasi semua VCD menjadi bentuk metabolit yang inaktif. Adanya
VCD yang masih aktif pada folikel yang kecil mengakibatkan terjadinya stres
oksodatif pada folikel tersebut. Keadaan stres oksidatif ini akan mendorong
peningkatan produksi antioksidan alami dalam ovarium seperti glutathione
peroxidase, superoxide dismutase (SOD), dan katalase. Antioksidan ini akan
bekerja untuk melindungi sel dari kerusakan akibat efek reactive oxygen
species dan apoptosis yang disebabkan oleh proses stres oksidatif.
Antioksidan ini banyak mengalami peningkatan terutama pada folikel-folikel
commit to user
pada folikel besar hampir semua VCD diubah menjadi bentuk inaktif
sehingga tidak menimbulkan stres oksidatif.
Ketidakseimbangan jumlah antioksidan dan stres oksidatif yang terus
timbul menyebabkan ketidakmampuan sel dalam mempertahankan hidupnya.
Hal ini menebabkan terjadinya perubahan-perubahan dalam sel berupa
perubahan morfologi sel, degradasi DNA, serta akan menghasilkan sinyal
apoptosis sel. Sinyal apoptosis ini didapatkan dari peningkatan ekspresi
mRNA bax protein. Ekspresi mRNA bax protein ini akan menyebabkan
kerusakan membran mitokondria yang dapat menimbulkan kebocoran
sitokrom c protein dari mitokondria ke sitosol. Kebocoran sitokrom c ini akan
meyebabkan aktivasi apoptosome caspase-9, yang pada akhirnya akan
mendorong kematian sel karena proses apoptosis.
4-vynilcyclohexene diepoxide (VCD) merupakan zat kimia yang
merusak folikel primordial dan folikel primer ovarium secara selektif dengan
cara mempercepat proses alamaiah terjadinya atresia. Karena kerusakan yang
terjadi secara selektif, maka tikus akan mengalami kegagalan ovarium secara
bertahap, sampai akhirnya hanya tersisa jaringan stroma ovarium, sehingga
fungsi steroidogenesis dan folikulogenesis hilang.
E. Hipotesis
4-vinylcyclohexane diepoxide ( VCD ) dosis 80 mg/KgBB dan
commit to user BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian.
1. Jenis Penelitian
Penelitian ini secara eksperimental laboratorium.
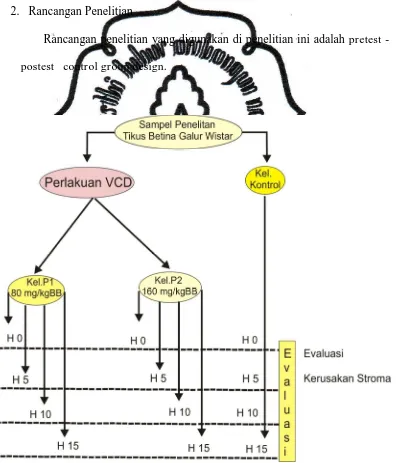
2. Rancangan Penelitian
Rancangan penelitian yang digunakan di penelitian ini adalah pretest
-postest control group design.
commit to user B. Lokasi dan Waktu Penelitian
Penelitian dilakukan mulai bulan April 2012 sampai dengan bulan Mei
2012, di lembaga pengembagan penelitian terpadu (LPPT) dan laboratorium
Patologi Anatomi Kedokteran Hewan Universitas Gadjah Mada, Yogyakarta.
C. Subjek Penelitian.
Subjek pada penelitian ini adalah hewan coba tikus betina galur Wistar
dengan kreteria inklusi tikus sehat, berumur 2.5 bulan ,berat badan 170 gr,
makan dan minum disamakan, suhu ruangan sama . Kreteria eksklusi tikus
sakit,gerak tidak aktif,warna bulu kusam dan atau rontok.
D. Besar sampel
Perhitungan jumlah sampel minimum yaitu dengan menggunakan
rumus sebagai berikut:
潐 2� 1 � � �� 1 � � 1 �
(Murti, 2010)
Keterangan:
n = ukuran sampel masing-masing dari 2 kelompok sampel
P = perkiraan proporsi (prevalensi) variable dependen pada populasi
� = (P1+P2)/2
Z1-α= statisitik Z
α = kesalahan tipe I
commit to user
Untuk perhitungan ukuran sampel digunakan software OpenEpi®, maka
didapatkan hasil di bawah ini:
Sample Size for Frequency in a Population
Population size(for finite population correction factor or fpc)(N): 1000000 Hypothesized % frequency of outcome factor in the population (p): 50%+/-23 Confidence limits as % of 100(absolute +/- %)(d): 23% Design effect (for cluster surveys-DEFF): 1
Sample Size(n) for Various Confidence Levels
Confidence Level(%) Sample Size
Results from OpenEpi, Version 2, open source calculator--SSPropor
Jadi dalam penelitian ini secara membutuhkan 60 sampel dengan perincian
20 tikus pada kelompok kontrol dan 40 tikus pada kelompok paparan VCD 80
mg/kgBB dan VCD 160 mg/kgBB (masing-masing kelompok sebanyak 20 tikus).
Sampel penelitian dibagi dalam tiga kelompok yaitu: Kelompok Kontrol
sebanyak 20 ekor yaitu tikus yang tidak mendapatkan perlakuan dengan VCD;
commit to user
dengan VCD 80mg/kgBB; Kelompok Perlakuan II sebanyak 20 ekor yaitu tikus
yang mendapat perlakuan dengan VCD 160mg/kgBB.
E. Variabel Penelitian.
1. Variabel bebas.
Kadar 4-vynilcyclohexene diepoxide (VCD).
2. Variabel terikat.
Kerusakan stroma ovarium.
F. Definisi Operasional.
1. 4-Vinyl Cyclohexene Diepoxide (VCD) adalah hasil metabolisme dari
4-Vinylcyclohexene (VCH). Yang diencerkan dan di beri emulgator sesame
oil yang telah disesuaikan dengan berat badan tikus dan di suntikkan
secara intraperitonial.
2. Stroma ovarium merupakan jaringan penyokong dari proses hormonal dan
fertilitas tikus pada usia reproduksi
3. Kerusakan stroma ovarium adalah adanya suatu kerusakan pada jaringan
stroma ovarium yang dapat berupa fibrotik, kekosongan area stroma,
penyempitan pembuluh darah, iskemia, atau nekrosis.
G. Prosedur penelitian yang dilakukan
1. Pemilihan mencit
2. Penimbangan mencit
3. Pemberian tanda
4. Pengelompokan mencit
commit to user 6. Pembedahan abdomen mencit
7. Pengambilan ovarium mencit
8. Pemeriksaan histopatologi ovarium
H. Alat dan Bahan Penelitian
Pembuatan Slide jaringan
a. Alat:
- Cassette tissue - Beaker glass
- Mikrotom - Poly L-Lysine slides
- Deckglass - Humidity chamber vertical
- Humidity chamber horisontal - Mikro pipet 10 µl
- Mikro pipet 100 µl - Mikro pipet 1000 µl
- PCR tube - Shaker
b. Bahan
- Formalin buffer 10% - Alkohol 100%, 95%, 80%, 70%.
- Xylol - Parafin
- Aquadest - Buffer sitrat pH 6
- PBS pH 7,2 - 7,4 - Metanol H2O2 0,3%
- Bloking serum - Streptavidin
-Substrat enzim peroksidase: DAB - Hematoxylin
- Canada balsam - Kapas atau tissue
c. Reagen: