BAB 2
TINJAUAN PUSTAKA
2.1. Karet Alam
Karet alam (Natural Rubber/NR), merupakan produk metabolit sekunder yang
dihasilkan oleh lebih dari 2000 jenis spesies tumbuhan. Pada umumnya karet alam komersial yang dikenal diperoleh dengan penyadapan tumbuhan Hevea Brasiliensis dan sisanya berasal dari tumbuhan semak dan tumbuhan kecil: milkweed (Asclepias spp.), dandelion (Taraxacum spp.) dan Guayule (Andrew Ciesielski, 1999).
Tumbuhan Hevea Brasiliensis telah dikenal oleh bangsa Maya di Amerika Selatan selama berabad-abad lamanya dengan sebutan Cautchou, pohon menangis. Kemudian pada 1770 oleh Joseph Priestley menciptakan istilah baru yaitu rubber (penghapus), karena Cautchouc bisa dipakai sebagai penghapus tulisan pensil, to rub out. Senyawa isoprena merupakan produk degradasi utama karet alam, yang
diidentifikasi pada tahun 1860 seperti yang dipublikasikan oleh J.C.F. Williams pada tahun 1862 di Journal Of Chem. Soc. 15 Part 10 (Stevents, M. P., 2001).
Karet alam dalam bentuk lateks yang diperoleh dari hasil penyadapan merupakan dispersi koloidal dengan massa jenis 0,975 -0,980 g/mL dan pH 6,5 -7, yang terdiri dari komponen karet dan non-karet, seperti protein, lipida, karbohidrat, asam dan beberapa senyawa anorganik. Komposisi ini sangat bervariasi tergantung pada tumbuhan karet sumbernya, seperti pada Tabel 2.1 (Flint, C. F., 1938).
angka mengacu pada kandungan maksimum pengotor yang terdapat dalam produk (Thio Goan Loo, 1980).
(a) (b)
Gambar 2.1. Pohon karet alam Hevea Brasiliensis (a) dan lateks karet alam (b)
Tabel 2.1 Komposisi lateks karet alam (Ceylon rubber latex)
No Komponen Persentase (%)
1 Kandungan karet kering 41,29
2 Protein 2,18
3 Karbohidrat 0,36
4 Senyawa anorganik 0,41
5 Air 55,15
Tabel 2.2. Standar Indonesian Rubber (SIR)
No Uraian SIR 5 SIR 10 SIR 20 SIR 50
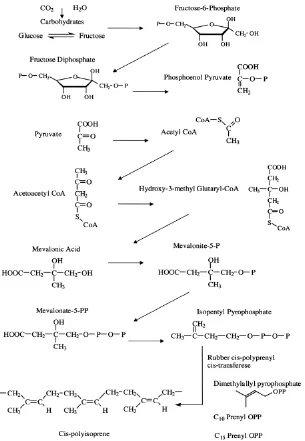
Secara kimia, karet alam merupakan senyawa poliisoprena, polimer rantai panjang
linier dengan unit berulang (monomer) isoprena, C5H8 yang terdiri atas 95% (w/w)
cis-1,4-poliisoprena, dengan berat molekul rata-rata 1.000.000. Disamping itu ada jenis lain tetapi dalam jumlah sedikit, yaitu karet alam yang disebut getah perca (gutta percha) merupakan trans-1,4-poliisoprena (Flint, C. F., 1938).
(a) (b)
Gambar 2.3. Rumus kimia cis-1,4-poliisoprena (a) dan trans-1,4-poliisoprena (b)
Pemanfaatan karet alam secara langsung sangat terbatas oleh karena sifatnya yang tidak tahan terhadap panas, oksigen, ozon, radiasi, sinar matahari dan kelarutannya dalam pelarut-pelarut hidrokarbon. Keterbatasan ini diakibatkan oleh terdapatnya ikatan rangkap dua karbon-karbon pada struktur kimia cis-1,4-poliisoprena.
Karet alam pada suhu 0°C sampai 10°C bersifat rapuh, gampang rusak, kabur/gelap. Diatas 20°C lembut, melenting dan diatas 60°C plastis dan lengket. Karet alam tidak larut dalam air, alkohol dan aseton, tetapi larut dalam bensin, benzen, kloroform, karbon tetraklorida, karbon disulfida serta sedikit larut dalam eter (William Klingensmit dan Brendan Rodgers, 2004).
Karet alam saat ini telah diolah menghasilkan beberapa material yang digunakan dalam kehidupan sehari-hari seperti ban, balon, sarung tangan karet, benang karet, tabung/pipa/selang, belt conveyor/transmission, seal, kondom, perekat (adhesive), pengikat (binder) dan lain-lain (William Klingensmit dan Brendan Rodgers, 2004).
2.2. Modifikasi kimia karet alam
Pemakaian karet alam secara langsung dalam kehidupan manusia sangat terbatas oleh karena sifat-sifat karet yang tidak stabil. Untuk meningkatkan pemakaian produk karet alam dalam bidang yang lebih luas maka perlu dilakukan modifikasi kimia terhadap struktur kimia poliisoprena. Modifikasi kimia karet alam yang paling utama adalah terkait dengan ikatan rangkap dua karbon-karbon dan introduksi gugus pemodifikasi (modifier) pada rantai karbon polimer cis-1,4-poliisoprena yang bertujuan untuk mendapatkan sifat-sifat dan stabilitas karet alam tertentu sehingga dapat diaplikasikan dalam bidang yang lebih luas.
Lee D.F., 1963 ; Mirzataheri, 2000 dan Riyajan dkk., 2006), depolimerisasi (Hussin Mohd. Nor dan John R. Ebdon, 1998) dan pencangkokan/grafting (Charmondusit K. dkk., 1998; Nakason, C. dkk. 2004; Eddyanto, 2007; Hinchiranan, N. dkk., 2007 dan Suwadee dkk., 2008 ). Modifikasi karet alam dengan epoksidasi, depolimerisasi dan siklisasi bahkan berhasil diproduksi secara komersial.
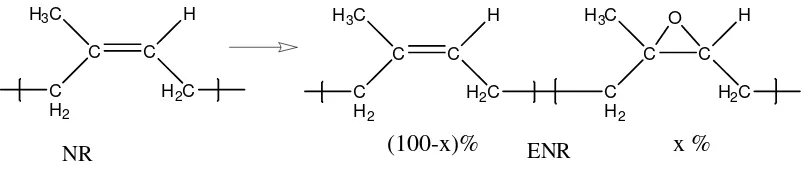
Epoksidasi karet alam menghasilkan karet alam epoksidasi/Epoxidized Natural Rubber (ENR), penelitian tentang karet alam epoksidasi bermula pada tahun 1920-an, seperti yang dipublikasikan tahun 1922 oleh R. Pummerer dan P.A. Burkard pada Uber Kautschuk, Ber. Dtsch. Chem. Ges. 55, 3458 (Si Dong Li dkk., 1997). Tetapi penelitian epoksidasi karet alam berkembang baru pada dua dekade terakhir dan berhasil diproduksi secara komersial dengan nama 25, 50 dan ENR-75, dimana bilangan mengacu pada derajat epoksidasi yaitu 25%, 50% dan 75%.
Epoksidasi karet alam menghasilkan produk yang memiliki gugus epoksi (oxirane) secara acak pada posisi ikatan rangkap poliisoprena. Epoksidasi dapat dilakukan dalam fase larutan (karet lateks) dengan pereaksi asam perptalat,
perbenzoat dan perasetat (Takayuki S. dkk., 2007).
Gambar 2.5. Reaksi epoksidasi karet alam
Perbedaan pereaksi yang digunakan menghasilkan produk akhir yang berbeda sifatnya dan banyaknya gugus epoksi yang terbentuk sangat bervariasi yang tergantung pada kondisi reaksi. Pereaksi yang banyak digunakan adalah perasam (peracid) menggunakan asam formiat dan hidrogen peroksida pada lateks karet
(Chonlada A. dkk., 2008; Heping Yu, dkk., 2008). Produk karet alam epoksidasi dikenal dengan karet yang tahan terhadap minyak. Sifat produk ini dibanding karet alam adalah memiliki ketahanan minyak (oil resistance) lebih baik, permeabilitas gas rendah, suhu transisi gelas (Tg) lebih tinggi dan stabilitas termal yang lebih baik (Seng Neon Gan dan Z.A. Hamid, 1997).
Karet epoksidasi juga meningkat kepolarannya sehingga memiliki kompatibilitas yang baik dengan polimer PVC (Chantara T. R. dan Khairul Zaman,
1999), nylon (Maswanee N. Dkk., 2012) dan karet nitril karboksilasi (Seng Neon Gan dan Z.A. Hamid, 1997).
Modifikasi karet alam juga dapat menghasilkan karet alam cair (Liquid Natural Rubber/LNR), yaitu produk karet alam yang diperoleh dengan proses depolimerisasi menghasilkan oligomer karet alam dengan berat molekul lebih rendah dari polimernya. Karet alam cair merupakan bentuk karet alam yang sudah lama dikenal yaitu pada tahun 1923 ketika pertama kali diproduksi secara komersial dengan nama dagang DPR oleh Hardman (Hussin Mohd. Nor dan John R. Ebdon, 1998).
Secara umum LNR diproduksi dengan cara pemutusan rantai poliisoprena
secara oksidatif. Pada awalnya metode yang digunakan untuk membuat LNR adalah dengan mengolah karet alam pada suhu 0-80oC dengan kehadiran garam logam berat yang larut dalam minyak, seperti kobal linoleat atau naftalena sehingga karet alam terdegradasi. Kemudian produk degradasi dilarutkan dalam petroleum eter dengan konsentrasi 20% dan viscositas sekitar 3000 poise pada suhu 25oC. LNR ini agak kental berwarna jingga sampai kuning dan mengandung 10% oksigen (Hussin Mohd. Nor dan John R. Ebdon, 1998).
Berdasarkan analisis LNR mengandung 0,001%-0,6% hidroperoksida, 0,3% carboxyl, 0,6% - l,5% ester, 3,3% - 4,0% aldehida dan 6,0% C=O (gugus fungsi keton). LNR dapat dibuat menjadi padat dengan pemanasan pada suhu 100 oC diudara terbuka. Metode pembuatan LNR dikembangkan selanjutnya dengan degradasi karet alam pada suhu 110-140 oC beberapa jam atau dengan suhu 250-300 oC dengan waktu yang lebih singkat dengan penambahan plastisizer seperti mercaptobenzthiazole (MBT). LNR yang diperoleh dengan metode ini memiliki berat molekul 2000, viskositas 5000-25000 Poise pada 20°C dan mengandung sekitar 1% oksigen (Hussin Mohd. Nor dan John R. Ebdon, 1998).
dapat dengan mudah dicampurkan tanpa konsumsi banyak energi sehingga lebih murah prosesnya dibandingkan karet alam. Pengembangan selanjutnya terhadap pembuatan LNR adalah penggunaan zat tambahan (ingredient) baru seperti p-quinone dioxime sebagai curing agent, Pb-peroksida sebagai pengisi dan amina sebagai akselerator. Zat-zat tambahan ini mempermudah kerja penanganannya, mengurangi kelengketan dan tahan lama dan yang paling penting adalah bahwa produk ini dapat divulkanisasi pada suhu ruang (Hussin Mohd. Nor dan John R. Ebdon, 1998).
Secara kimiawi degradasi polimer dapat terjadi dengan bantuan senyawa pemutus rantai molekul polimer. Penambahan senyawa pemutus rantai molekul
sistem redoks, campuran hidrogen peroksida dengan natrium hipoklorit, dikombinasikan dengan hidroksilamin netral sulfat akan menghasilkan lateks dengan viskositas Mooney rendah dan memiliki daya rekat baik. Secara garis besar depolimerisasi dapat dilakukan dengan mastikasi, pirolisis, fotolisis, dekomposisi kimia (Tanaka, Yasuyuki dkk, 1996).
Depolimerisasi menghasilkan karet dengan viskositas rendah, berat molekul rendah antara 40.000 - 50.000. Pada suhu kamar bentuk cairan sehingga memudahkan dalam proses pengolahan/pencampuran sampai proses akhir pengolahan. Karet alam cair sekaligus dapat berperan seperti plastisizer yang menurunkan waktu dan konsumsi energi pada proses pengolahan produk campurannya. Selanjutnya dapat mengalami ikat silang (cure) dengan mekanisme yang sama seperti karet alam (William Klingensmit dan Brendan Rodgers, 2004).
Produk ini biasanya diaplikasikan sebagai campuran material ban, keramik, modifier pelumas, bahan dasar polimer pembalut alat elektrik (electrical encapsulants), bahan seal (sealant) dan pemodifikasi aspal (modifier asphalt). Produk
2.3. Siklisasi Karet Alam
Siklisasi karet alam merupakan reaksi pembentukan cincin enam karbon intramolekuler cis-1,4-poliisoprena menghasilkan karet alam siklis (Cyclized Natural Rubber/CNR), yang dapat terjadi dengan melibatkan senyawa asam atau katalis Friedel-Craft. Perubahan karet alam menjadi resin/resinifikasi merupakan reaksi dimana terjadi pengurangan jumlah ikatan rangkap poliisoprena yang diikuti dengan pembentukan struktur siklis dan tidak terjadi perubahan rumus empiris karet, C5H8.
Sementara itu berat molekul tetap tinggi dan tetap larut dalam pelarut karet yang menunjukkan tidak terjadi ikat silang (cross link). Karet kehilangan sifat elastisitasnya dan berubah menjadi material yang keras dan rapuh. Pengurangan
jumlah ikatan rangkat yang terjadi dalam reaksi siklisasi bervariasi sekitar 40-90%. Beberapa peneliti sepakat dengan struktur karet alam siklis seperti gambar 2.4.(Lee, 1963)
Gambar 2.6. Struktur siklik karet alam siklis
Beberapa peneliti telah berhasil membuat karet alam siklis melibatkan katalis yang berbeda seperti asam p-toluena sulfonat (Janssen, 1954), P2O5 (Tumorsski,
1961), SnCl4 ( Lee, D.F., 1963 dan Mirzataheri, 2000) dan H2SO4 (Riyajan, 2006)
karet alam lateks non-protein/deproteinized natural rubber (DPNR) dengan yield 86%.
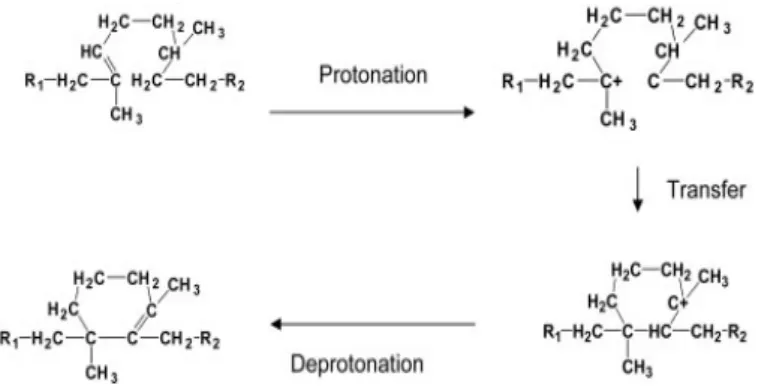
Ikatan rangkap bersifat labil dan mudah dipengaruhi oleh katalis. Reaksi siklisasi dapat terjadi jika ada dua unit ikatan rangkap yang berdekatan bereaksi menghasilkan struktur siklis dengan hadirnya pereaksi/katalis yang sesuai. Siklisasi karet alam disepakati secara umum sebagai tipe reaksi polimerisasi ionik, dimana terjadi protonasi pada ikatan rangkap yang diikuti oleh tahapan propagasi pembentukan struktur siklis dan diakhiri dengan deprotonasi (Lee, 1963). Telah diusulkan mekanisme reaksi molekul-molekul poliisoprena dalam pembentukan cincin enam karbon sebagai mekanisme ion karbonium. Reaksi ini dapat terjadi
sepanjang rantai poliisopren pada karet untuk menghasilkan struktur polisiklik (Mirzataheri, 2000).
Gambar 2.7. Mekanisme reaksi siklisasi karet alam (Riyajan dkk., 2006)
Rata-rata ukuran struktur siklis yang terbentuk selama proses siklisasi ditemukan bahwa tidak tergantung pada konsentrasi karet dan katalisnya tetapi ditentukan oleh temperatur reaksi siklisasi. Ikatan rangkap yang masih terdapat pada produk karet alam siklis lebih kecil dari 20% (Lee, D.F., 1963).
n p q
Karet Alam Karet Alam Siklis/ CNR
< 20 % 80%
Gambar 2.8. Reaksi siklisasi karet alam menghasilkan karet alam siklis
2.4. Pencangkokan
Pencangkokan (grafting) merupakan teknik yang secara luas dilakukan untuk memodifikasi bahan polimer dengan tujuan mendapatkan sifat-sifat tertentu polimer yang diinginkan. Pada reaksi pencangkokan terbentuk ikatan kovalen antar monomer
dengan rantai polimer. Teknik pencangkokan telah dilakukan dengan menggunakan inisiator panas (Zhen Yao dkk., 1998), bahan kimia, radiasi, fotokimia, induksi plasma dan enzimatik (A. Bhattacharya dan B. N. Misra, 2004).
2.4.1. Pencangkokan dengan inisiasi panas
2.4.2. Pencangkokan dengan inisiasi bahan kimia
Secara garis besar, pencangkokan dengan inisiasi bahan kimia ada dua yaitu mekanisme radikal bebas dan mekanisme ionik. Peranan inisiator sangat penting dalam proses kimia dan menentukan jalur dalam proses pencangkokan.
2.4.2.1. Pencangkokan mekanisme radikal bebas
Radikal bebas dihasilkan dari inisiator dengan pengaruh panas. Kemudian radikal selanjutnya mengabtraksi atom hidrogen polimer subtrat, sehingga terbentuk radikal pada molekul polimer. Selanjutnya monomer bertindak sebagai akseptor radikal membentuk kopolimer cangkok. Kemudian radikal monomer menjadi donor radikal
pada monomer tetangganya, begitu seterusnya, seperti mekanisme di bawah ini.
Gambar 2.9. Mekanisme reaksi kopolimerisasi cangkok dengan inisiator radikal bebas (A. Bhattacharya dan B. N. Misra, 2004).
2.4.2.2. Pencangkokan mekanisme ionik
Pencangkokan juga dapat dilakukan dengan model ionik. Suspensi logam alkali
dalam larutan basa Lewis, senyawa organologam dan naftalinida sangat berguna sebagai inisitor untuk tujuan ini. Alkil aluminium (R3Al) dan polimer induk dalam
bentuk halide (ACL) berinteraksi untuk membentuk ion karbonium sepanjang rantai polimer, yang membentuk kopolimer. Reaksi ini berlangsung melalui mekanisme kationik.
ACl + R3Al → A +
R3AlCl
Pencangkokan juga dapat melalui mekanisme anionik. Sodium-ammonia atau metoksida dari logam alkali membentuk alkoksida dari polimer (PO-Na+), yang bereaksi dengan monomer membentuk kopolimer cangkok.
P-OH + NaOR → PO
-Na+ + ROH PO-+M → POM
--M → kopolimer cangkok
2.4.3. Pencangkokan dengan inisiasi radiasi
Pencangkokan radiasi dapat berlangsung denga model ionik dimana terbentuknya ion dengan adanya irradisi berenergi tinggi, yang dapat dibedakan menjadi dua jenis
yaitu: kationik dan anionik. Polimer diirradiasi untuk membentuk ion yang kemudian bereaksi dengan monomer membentuk kopolimer cangkok atau bisa juga dengan cara dimana monomer diirradiasi untuk membentuk ion yang kemudian bereaksi dengan polimer membentuk kopolimer cangkok. Mekanisme dengan analogi yang sama dapat terjadi pada pencangkokan radiasi anionik.
2.4.4. Pencangkokan dengan inisiasi fotokimia
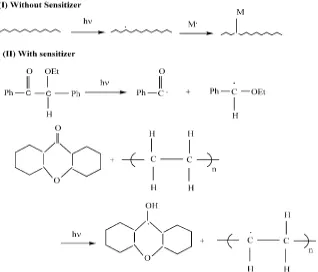
Ketika kromofor yang terdapat pada makromolekul menyerap cahaya akan terjadi eksitasi yang mungkin berdisosiasi membentuk radikal bebas reaktif yang akan menginisiasi reaksi. Jika absorbsi tidak menghasilkan radikal bebas melalui pemecahan ikatan, proses ini dapat dilakukan dengan penambahan fotosintetizer seperti benzofenon, xanthone, Na-2,7-antraquinon sulfonat. Jadi, proses ini dapat berlangsung dengan menggunakan atau tanpa fotosintetizer.
Mekanisme tanpa sensitizer melibatkan terbentuknya radikalbebas pada rantai polimer yang bereaksi dengan monomer membentuk kopolimer cangkok. Pada bagian lain, mekanisme dengan sensitizer terjadi dengan terbentuknya radikal oleh sensitizer
yang kemudian mengabstraksi atom hidrogen polimer untuk menghasilkan gugus radikal yang dibutuhkan pada proses pencangkokan.
2.4.5. Pencangkokan dengan inisiasi induksi plasma
Proses utama dalam plasma adalah eksitasi elektron terinduksi, ionisasi dan disossiasi. Kemudian elektron tereksitasi dari plasma memiliki energi yang cukup untuk menginduksi pembelahan dari ikatan kimia dalam struktur polimer membentuk radikal makromolekul kemudian menginisiasi kopolimer cangkok.
2.4.6. Pencangkokan dengan inisiasi enzimatik
Metode ini merupakan metode yang cukup baru. Prinsipnya enzim menginisiasi reaksi grafting kimia/elektrokimia. Contohnya, tirosin dapat mengkonversi fenol menjadi o-kuinon yang reaktif. Kemudian mengalami reaksi non-enzimatik dengan
kitosan (Bhattacharya, A. dan B. N. Misra, 2004).
2.5.Pencangkokan monomer Anhidrida Maleat
Anhidrida Maleat (AM) merupakan salah satu monomer polifungsional yang banyak digunakan memodifikasi material polimer untuk menghasilkan material teknik, bioteknik (bioengineering) dan nanoteknik (nanoengineering) berkinerja tinggi (high performance), baik polimer alam maupun sintesis. Penggunaan Anhidrida Maleat telah berhasil memperbaiki sifat-sifat kopolimer cangkok (graft copolymerization) polimer thermoplastik seperti poliolefin, polistiren, poliamida dan juga biopolimer dapat terdegradasi (biodegradable polymers), polisakarida dan karet alam dan sintesis (Zakir M. O. Rzayev, 2011).
Introduksi molekul Anhidrida maleat pada molekul nonpolar senyawa poliolefin dan karet mengatasi kelemahan akan rendahnya energi permukaan polimer ini, meningkatkan hidrofilitas permukaannya sehingga bermanfaat pada aplikasi di bidang pelapisan (coating) dan tinta cetak (printing ink) dan adhesinya terhadap polimer bersifat polar (poliamida), logam dan serat kaca (glass fiber) (Zakir M. O. Rzayev, 2011).
teknik berkemampuan tinggi (high performance engineering materials) dan nanokomposit dengan menggunakan sistim pereaksi reaktif (reactive extruder systems) dan in situ kompatibelisasi campuran polimer telah sangat berkembang,
bahkan beberapa berhasil secara komersial.
Sejarah pencangkokan Anhidrida maleat pada polyolefin khususnya polipropilen (pp) telah dimulai pada tahun 1969, dan berkembang sampai saat ini baik dalam fase larutan, cairan (molten process) dan padatan (solid phase grafting process). Ide dan Hasegawa telah melakukan pencangkokan Anhidrida maleat pada
polipropilen dalam fase cair menggunakan benzoil peroksida sebagai inisiator dan plastograph Brabender menghasilkan kopolimer cangkok yang kemudian digunakan
dalam campuran poliamida dan polipropilen (pp) sebagai pencampuran reaktif (Zakir M. O. Rzayev, 2011).
Untuk mempelajari mekanisme pencangkokan, fungsionalisasi pp dengan Anhidrida maleat telah diakukan penelitian dalam fase larutan (S. N. Sathe dkk., 1994; J. L. White, A. Sasaki, 2003) dan fase leleh (N. G. Gaylord, R. Mehta, 1988; Simmons, W. E. Baker, 1989) menggunakan berbagai jenis sistem ekstruder. Dengan pertimbangan biaya yang lebih rendah dan peralatan maka dipilih metode dengan fase leleh melalui proses reaktif.
Pencangkokan Anhidrida maleat pada low density polietilena (LDPE) dengan kehadiran dikumil peroksida dalam fase cair menghasilkan produk yang kemudian digunakan sebagai kompatibeliser pada campuran polietilen dengan poliamida 66. Juga dilaporkan bahwa reaksi berlangsung dalam pencampur internal dan ekstruder ganda (twin-extruder) dan disampaikan kinetika reaksi pencangkokannya (J. Cha, J. L. White, 2001).
Penelitian yang penting terkait pencangkokan Anhidrida maleat pada pp adalah penggunaan berbagai jenis ekstruder dan pencampur. Kemudian, fungsionalisasi Anhidrida maleat pada pp dalam fase leleh telah diteliti oleh Gaylord dan Mishra, 1983 dan Ho dkk., 1993 dimana reaksinya berlangsung di dalam pencampur internal Brabender Plasticorder. Konsenrasi AM dan inisiator peroksida berpengaruh terhadap jumlah kopolimer cangkok.
Penelitian pencangkokan AM pada pp menggunakan proses reaktif di dalam Haake torque rheometer diperoleh kesimpulan bahwa meningkatnya konsentrasi monomer Anhidrida maleat, inisiator, kecepatan rotor dan waktu reaksi mengakibatkan naiknya drajat grafting AM pada pp ( Bettini dan Agnelli, 1999).
Peranan stirena pada pencangkokan AM pada PP sangat nyata meningkatkan derajat grafting yang diperoleh pada perbandingan mol AM dan stirena 1:1. Stirena sebagai monomer electron donor, dapat berinteraksi dengan AM melalui kompleks bermuatan membentuk kopolimer stirena-AM yang selanjutnya dapat beraksi menghasilkan kopolimer cangkok AM-g-PP (Dong and Liu, 2003).
Penambahan stirena sebagai monomer kedua dalam sistim pencampuran fase leleh dapat membantu meningkatkan derajat grafting AM pada PP. Monomer stirena dapat menjembatani jarak antara makroradikal PP dan monomer AM, dimana stirena terlebih dahulu bereaksi dengan makroradikal PP membentuk makroradikal stirena yang lebih stabil untuk selanjutnya bereaksi dengan AM membentuk kopolimer AM-g-PP (Li dkk., 2001).
Pencangkokan AM pada karet alam dapat meningkatkan kompatibilitas antara karet alam dengan elastomer polar dan plastic seperti poliamida.Belakangan ini pencangkokan AM pada karet alam banyak dilakukan dalam fase lelh menggunakan pencampur seperti roll mill dan pencampur internal/internal mixer ( J. Saelao, P. Phinyocheep, 2005; Demin Jia, 2000).
diakibatkan oleh terjadinya interaksi intermolekuler antara gugus ujung poliamida atau gugus hidroksil dari makromolekul cassava starch (Nakason, C. dkk., 2001; M. Sclavons dkk., 1996).
2.6.Anhidrida Maleat
Anhidrida Maleat juga dikenal dengan nama lain yaitu: cis-butenadioat Anhidridaa, Anhidridaa toksilat dan dihidro-2,5-dioksofuran. Merupakan senyawa organik yang memiliki rumus molekul C4H2O3. Anhidrida Maleat merupakan padatan tidak
berwarna atau berwarna putih dan memiliki bau yang tajam. Anhidrida Maleat adalah senyawa vinil tidak jenuh, merupakan bahan baku pada sintesa resin poliester,
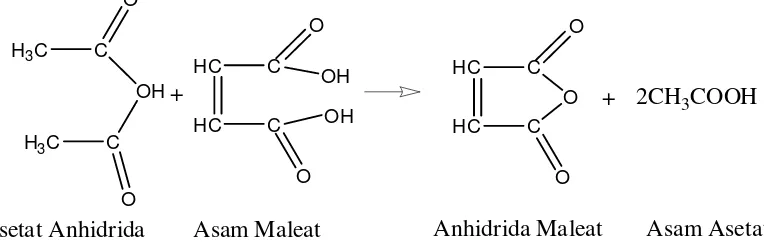
pelapisan permukaan karet, deterjen, bahan aditif dan minyak pelumas, plastisizer dan kopolimer. Anhidrida Maleat mempunyai sifat kimia khas yaitu adanya ikatan etilenik dengan gugus karbonil di dalamnya, yang berfungsi dalam reaksi adisi. Anhidrida Maleat diproduksi secara komersial dengan reaksi oksidasi benzena atau senyawa aromatik lainnya. Anhidrida Maleat dapat dibuat seperti reaksi di bawah ini.
H3C C
Gambar 2.12. Reaksi pembentukan Anhidrida Maleat
Anhidrida Maleat mempunyai sifat kimia khas yaitu adanya ikatan etilenik dengan gugus karbonil di dalamnya ,yang berfungsi dalam reaksi adisi. Anhidrida maleat dapat mengalami reaksi sebagai berikut:
a. hidrolisis menghasilkan asam maleat, cis HO2CCH = CHCO2H.
c. Anhidrida Maleat merupakan dienofil dalam reaksi Diels-Alder.
d. Anhidrida Maleat merupakan dieno Anhidrida Maleat (AM) dapat berfungsi sebagai ligan yang baik untuk kompleks logam bervalensi rendah, misalnya Pt(PPh3)2(MA) dan Fe(CO)4(MA).
Anhidrida Maleat dan senyawa isostruktur analognya secara luas digunakan pada reaksi pembentukan makromolekul dengan struktur linier, bercabang dan penataan ulang untuk menghasilkan material kinerja tinggi, bioteknik dan nano teknik.
Tabel 2.3. Sifat-sifat Anhidrida Maleat (HSDB, 1995)
No Sifat Keterangan
1 Deskripsi Tak berwarna atau padatan putih 2 Rumus Molekul C4H2O3
3 Berat Molekul 98,06 g/mol 4 Titik Didih 202 oC 5 Titik Leleh 52,8 oC
6 Kelarutan Larut dalam air, eter, asetat, kloroform, dioksan, aseton, benzen, toluen dan o-xylen
2.7.Inisiator
Selain teknik pencangkokan dengan panas dan radiasi, semua reaksi pencangkokan pada proses grafting dimana konsentrasi inisiator mempengaruhi laju reaksi grafting. Ada berbagai ketergantungan hubungan secara empiris dari efisiensi grafting terhadap konsentrasi inisiator. Jelas bahwa sekali konsentrasi tertentu inisiator terpenuhi, peningkatan jumlah inisiator tidak serta merta meningkatkan konversi dari monomer tercangkok (Krump, H., P. 2005).
Homolisis ikatan peroksida yang lemah membentuk radikal yang sangat reaktif. Inisiator peroksida cukup sering digunakan dalam proses grafting secara kimia. Berikut beberapa alasan menggunakan peroksida sebagai inisiator yaitu :
1. Kecepatan dekomposisi peroksida, proses awal dekomposisi untuk menghasilkan radikal bebas sangat bergantung pada kondisi reaksi dan variabel proses.
2. Reaktifitas radikal yang dihasilkan melalui pemindahan atom hidrogen dari polimer.
3. Inisiasi radikal terhadap monomer mengarah pada homopolimerisasi. Homopolimerisasi dari monomer reaktif meningkat bersamaan dengan meningkatnya reaktifitas inisiator untuk berpolimerisasi menghasilkan tingkatan rendah dari radikal bebas.
4. Waktu paruh (t1/2) peroksida, hal ini menunjukan laju dekomposisi peroksida
dibawah kondisi reaksi yang khusus termasuk temperatur, sifat fisik dari polimer diantara faktor lainnya.
5. Sifat fisik peroksida, sifat fisik (cair, padat, terserap dalam pembawa padat) dapat menjadi penting untuk pengiriman dan pencampuran termasuk karakteristik fisik lainnya seperti volatilitas, kelarutan, bau dan toksisitasnya (Eddyanto, 2007).
2.8.Benzoil Peroksida
Kebanyakan pemicu yang digunakan secara luas adalah radikal bebas yang dihasilkan dari peruraian peroksida. Benzoil peroksida C14H10O4 mempunyai berat molekul
larut dalam benzene, eter, aseton, kloroform, titik leleh 104,5 oC (220,1 F); titik dekomposisi 106-108 oC (223-226 F); tekanan uap <1 mmHg pada 20oC; gravitasi spesifik (air=1) 1,3340 pada 25 oC; kelarutan dalam air <1%. Peroksida organik seperti benzoil peroksida merupakan sumber radikal bebas yang kuat. Digunakan sebagai inisiator polimerisasi, katalis dan agen vulkanisir (HSBD, 1995).
O
O O
O
Gambar 2.14. Struktur Benzoil Peroksida
2.9. Ekstrusi menggunakan peralatan Brabender Olasticorder
Ekstruder (extruder) yang digunakan dalam studi ini adalah extruder Brabender Plasticorder Model PL 2000. Brabender Plasticorder (torque rheometer) telah secara
luas digunakan untuk menentukan sifat-sifat pemrosesan bahan polimer, reologi lelehan polimer pencampuran polimer dan lain-lain. Torque rheometer merupakan peralatan penting untuk mengukur toque secara umum. Torque rheometer merupakan suatu alat dengan ruang pencampuran berjaket yang volumenya sekitar 50 cm3. Pencampuran material dalam ruang pencampuran dilakukan oleh dua pencampur (rotor) horisontal yang memiliki tonjolan. Hambatan oleh material bahan uji terhadap rotor berputar dalam ruang pencampuran diketahui dengan bantuan keseimbangan dinamometer.
temperatur. Berbagai jenis rotor dapat dengan mudah dipasang dan turun karena pengikat dan kopling sistem yang sederhana. Setelah kondisi pengujian (tipe rotor, rpm dan suhu ) diatur, waktu yang cukup diberikan untuk suhu untuk mencapai nilai yang ditetapkan dan menjadi stabil. Selanjutnya bahan dimasukkan ke ruang pencampuran untuk mendapatkan waktu kurva torsi atau plastogram.
Gambar 2.15. Internal Mixer Brabender Plasticorder Model PLE 331
2.10. Karakterisasi 2.10.1.Softening Point
2.10.2.Viskositas
Viskositas merupakan ukuran kekentalan suatu fluida yang menunjukkan besar kecilnya gesekan internal fluida. Viskositas fluida berhubungan dengan gaya gesek antarlapisan fluida ketika satu lapisan bergerak melewati lapisan yang lain. Pada zat cair, viskositas disebabkan terutama oleh gaya kohesi antar molekul. Setiap fluida memiliki besaran viskositas yang berbeda yang dinyatakan dengan massa per volume. Viskositas dapat dengan mudah dipahami dengan meninjau satu lapisan tipis fluida yang ditempatkan di antara dua lempeng logam yang rata. Satu lempeng bergerak (lempeng atas) dan lempeng yang lain diam (lempeng bawah). Fluida yang bersentuhan dengan lempeng ditahan oleh gaya adhesi antara molekul fluida dan
molekul lempeng. Dengan demikian, lapisan fluida yang bersentuhan dengan lempeng yang bergerak akan ikut bergerak, sedangkan lapisan fluida yang bersentuhan dengan lempeng diam akan tetap diam. Lapisan fluida yang bergerak mempunyai kelajuan sama dengan kelajuan lempeng yang bergerak, yaitu sebesar v. lapisan fluida yang diam akan menahan lapisan fluida di atasnya karena adanya gaya kohesi. Lapisan yang ditahan itu menahan lapisan di atasnya lagi dan seterusnya sehingga kelajuan setiap lapisan fluida bervariasi dari nol sampai v. Untuk menggerakkan lempeng diperlukan gaya. Untuk membuktikannya, dapat dicoba dengan menggerakan sebuah potongan kaca di atas tumpahan sirup. Semakin kental fluida, semakin besar gaya yang diperlukan untuk mendorong. Pada penelitian ini penentuan viskositas dilakukan dengan metode (Ford 4CCup) In Toluene.
2.10.3.Massa Jenis
ρ = m / V
Dalam sistem Satuan Internasional (SI), satuan massa jenis dinyatakan dengan kilogram per meter kubik (kg/m3), sedangkan dalam sistem cgs satuan massa jenis adalah gram per sentimeter kubik (g/cm3). Jika dikonversikan, kesetaraan kedua satuan ini adalah 1.000 g/cm3 = 1 kg/m3).
2.10.4.Warna
Warna adalah berwarna Pada penelitian ini penentuan warna dilakukan dengan metode Gadner Scale 1963, in
60% TL.
2.10.5.Spektrofotometri Infra Merah
Spektrofotometri infra merah/Infra Red (IR) merupakan teknik yang umum digunakan untuk memperoleh informasi struktur molekul suatu senyawa. Daerah serapan inframerah terletak antara daerah tampak dan panjang gelombang mikro, pada kisaran panjang gelombang 0,5-200 µm. Daerah 0,8-2,5 µm disebut inframerah dekat dan daerah 15-200 µm disebut inframerah jauh. Molekul-molekul suatu senyawa mempunyai frekuensi vibrasi yang khas. Gugus fungsional ini mengabsorbsi radiasi infra merah dan menjadi energi vibrasi molekular.
intensitas. Oleh karena masing-masing frekuensi radiasi berkaitan dengan gerakan spesifik, maka jenis gerakan molekul yang dimiliki oleh sampel dapat dilihat dengan mengukur spektrum infra merahnya. Gugus fungsional yang ada dalam molekul dapat ditentukan dengan menginterpretasikan spektrum inframerah (F.W. Fifield dan D. Kealey, 2000).
Informasi mengenai struktur suatu senyawa dapat diperoleh dengan mempelajari daerah terjadinya absorbsi gugus fungsional. Daerah yang paling berguna untuk mengenal struktur senyawa adalah daerah 4000-1500 cm-1. Serapan setiap tipe ikatan (N-H, C-H, O-H, C-X, C=O, C-C, C=C, C=N, dan sebagainya) hanya diperoleh dalam bagian-bagian kecil tertentu dari daerah vibrasi inframerah.
Kisaran serapan yang kecil dapat digunakan untuk menentukan setiap tipe ikatan. Daerah 4000-2500 cm-1 merupakan absorbsi yang disebabkan oleh regangan ikatan N-H, C-H, O-H, serta gerakan kontraksi. Ikatan O-H dan N-H menyerap pada daerah 3600-3300 cm-1 dan regangan ikatan C-H terjadi dekat 3000 cm-1 Daerah antara 2500-2000 cm-1 adalah daerah tempat regangan ikatan rangkap tiga, untuk itu baik nitril ( R-C=N) maupun alkuna keduanya menunjukkan puncak di daerah ini. Daerah dari 2000-1500 cm-1 mengandung serapan ikatan rangkap dua, ikatan C=O, C=N, C=C, menunjukkan serapan di daerah ini. Produk hasil sintesis diharapkan mempunyai serapan C=O, C=C, OH, dan serapan aromatis (Da-Wen Sun, 2009).
Pada dasarnya spektrofotometri FT-IR (Fourier Trasform Infra Red) adalah sama dengan spektrofotometri IR dispersi, yang membedakannya adalah pengembangan pada sistim optiknya sebelum berkas sinar infra-merah melewati contoh.
2.10.6.Analisa Thermal
penguapan, pirolisis, interaksi padat-padat dan kemurnian. Data semacam ini berguna untuk karakterisasi senyawa yang memandang kesesuaian, stabilitas, kemasan dan pengawasan kualitas. Pengukuran dalam analisis termal meliputi suhu transisi, termogravimetri dan analisis cemaran.
Gambar 2.16. Peralatan Spektrofotometri Infra Merah Model GALAXY 5000
Karakteristik termal memegang peranan penting terhadap sifat suatu bahan karena berkaitan erat dengan struktur dalam bahan itu sendiri. Suatu bahan bila dipanaskan akan terjadi perubahan struktur yang mengakibatkan adanya perubahan dalam kapasitas panas atau energi termal bahan tersebut. Teknik analisa termal
suatu bahan yang ditunjukkan dengan penyerapan panas (endotermik) dan pengeluaran panas (eksotermik). Proses termal meliputi antara lain proses perubahan fase (transisi gelas), pelunakan, pelelehan, oksidasi, dan dekomposisi (F.W. Fifield dan D. Kealey, 2000).
Dalam kaitannya dengan industri, teknik analisa termal digunakan untuk penentuan kontrol kualitas suatu produk/bahan khususnya polimer. Tanpa adanya pengetahuan data-data termal, pemrosesan suatu bahan akan sangat sulit dilakukan. Sifat termal suatu bahan menggambarkan kelakuan dari bahan tersebut jika dikenakan perlakuan termal (dipanaskan/didinginkan). Dengan demikian pengetahuan tentang sifat termal suatu bahan menjadi sangat penting dalam kaitannya dengan pemrosesan
bahan menjadi barang jadi maupun untuk control kualitas.
Dua jenis teknik analisa termal yang utama adalah Analisa Termogravimetrik /Thermographymetric Analysis (TGA), yang secara otomatis merekam perubahan berat sampel sebagai fungsi dari suhu maupun waktu dan Kalorimetri Pemindaian Differensial/Differential Scanning Chalorimetry (DSC) yang mengukur perbedaan suhu, T, antara sampel dengan material referensi yang inert sebagai fungsi dari suhu.
2.10.6.1. Analisa Thermogravimetri
Analisa Thermogravimetri atau Thermographymetric Analysis (TGA) adalah teknik untuk mengukur perubahan berat dari suatu senyawa sebagai fungsi suhu ataupun waktu. Hasilnya biasanya berupa rekaman diagram yang kontinu, reaksi dekomposisi satu tahap yang skematik diperlihatkan pada Gambar 1. sampel yang digunakan, dengan berat beberapa miligram, dipanaskan pada laju konstan, berkisar antara 1 – 20 0C /menit, mempertahan berat awalnya , Wi, sampai mulai terdekomposisi pada suhu Ti. Pada kondisi pemanasan dinamis, dekomposisi biasanya berlangsung pada range suhu tertentu, Ti – Tf, dan daerah konstan kedua teramati pada suhu diatas Tf, yang
Gambar 2.17. Skema thermogram reaksi dekomposisi satu atap
Gambar 2.18. Peralatan Thermographymetric Analysis (TGA)
Bertolak belakang dengan berat, harga Ti dan Tf, merupakan harga yang
bergantung pada beragam variabel, seperti laju pemanasan, sifat dari padatan (ukurannya) dan atmosfer di atas sampel. Efek dari atmosfer ini dapat sangat
kondisi eksperimen, karenanya tidak mewakili suhu-suhu dekomposisi pada equilibrium.
Gambar 2.19. Dekomposisi CaCO3 pada atmosfer yang berbeda
2.10.6.2. Differential Scanning Calorimetry (DSC)
Analisa termal diferensial adalah teknik dimana suhu sampel dibandingkan dengan material referen inert selama perubahan suhu terprogram. Suhu sampel dan referensi akan sama apabila tidak terjadi perubahan, namun pada saat terjadinya beberapa peristiwa termal, seperti pelelehan, dekomposisi atau perubahan struktur kristal pada sampel, suhu dari sampel dapat berada di bawah (apabila perubahannya bersifat endotermik) ataupun di atas (apabila perubahan bersifat eksotermik) suhu referensi.
Prinsip DSC tidak jauh berbeda dengan prinsip kalorimetri biasa, hanya dalam hal ini digunakan sampel dari polimer yang agak jauh lebih kecil (maksimum 50 mg , misalnya 10 mg ) dan peralatan kalor lebih teliti. Berbeda dengan dengan teknik TGA, teknik DSC menggunakan teknik pemanas individual masing-masing untuk sampel dan pembanding seperti diperlihatkan pada Gambar 2.13 (David I. bower, 2002).
terjadi perubahan kapasitas kalor sampel selama kenaikan suhu, pemanas sampel berusaha mengatur banyaknya kalor yang diberikan. Perbedaan tenaga listrik yang dibutuhkan antara pemanas sampel dan pemanas pembanding ini berbanding langsung dengan perubahan entalpi proses yang dialami sampel.
Gambar 2.20. Perlatan Differential scanning calorimetry (DSC) TA INSTRUMENTS Q2000
Gambar 2.21. Skematik pengujian dengan DSC
termogram DSC, yakni plot perubahan entalpi (ΔH) terhadap kenaikan suhu, proses eksotermis dinyatakan sebagai – ΔH dan proses endotermis sebagai + ΔH, (Basuki Wirjosentono, 1995). Karakterisasi sifat thermal dalam penelitian ini menggunakan alat DSC TA INSTRUMENTS Q2000.