BAB I PENDAHULUAN
A. Latar Belakang Masalah
Indonesia merupakan negara agraris, dimana sebagian besar penduduknya
bekerja di bidang pertanian. Salah satu produk utama pertanian di Indonesia
adalah padi. Hal ini tidak terlepas dari kenyataan bahwa beras yang termasuk hasil
olahan dari padi merupakan bahan makanan pokok masyarakat Indonesia,
sehingga sumber bahan makanan ini dapat dijumpai di mana saja. Berdasarkan
data Badan Pusat Statistik (BPS), pada tahun 2014 produksi padi di Indonesia
sebanyak 70,85 juta ton gabah kering giling (GKG). Produksi padi tahun 2015
diperkirakan sebanyak 75,55 juta ton GKG atau mengalami kenaikan sebanyak
4,70 juta ton (6,64 persen) dibandingkan tahun 2014 (Badan Pusat Statistik,
2015). Sementara itu, hasil samping pengolahan padi serta limbahnya belum
dimanfaatkan secara maksimal, seperti sekam padi dan jerami.
Sekam padi merupakan limbah dari proses penggilingan padi yang
memiliki berat 20-22% dari bobot padi (Linda Trivana, Sri Sugiarti, dan Eti
Rohaeti, 2015). Oleh karena itu, salah satu limbah pertanian yang paling
melimpah adalah sekam padi. Pemanfaatan sekam padi secara umum masih relatif
rendah dan belum optimal. Hal ini karena karakteristik sekam padi yang bersifat
kasar, bernilai gizi rendah, memiliki kerapatan yang rendah, dan kandungan abu
yang cukup tinggi (Houston, 1972). Selama ini, sekam padi hanya digunakan
sebagai alas pakan ternak, media bercocok tanam, bahan bakar pada proses
keramik, atau dibuang begitu saja. Padahal, abu sekam padi memiliki kandungan
silika (SiO2) yang cukup tinggi, yaitu sebesar 85-97% (A. M. Fuadi dkk, 2012).
Tingginya kandungan silika ini merupakan potensi besar yang dapat digunakan
sebagai bahan baku pengganti sumber silika lain yang lebih mahal dan sekaligus
mampu meningkatkan kualitas dan nilai ekonomis sekam padi.
Silika yang terdapat di dalam sekam padi bersifat amorf sehingga untuk
peleburan abu sekam padi tidak memerlukan waktu yang lama dan temperatur
tinggi (Linda Trivana, Sri Sugiarti, dan Eti Rohaeti, 2015). Dengan demikian, abu
sekam padi dapat digunakan sebagai sumber silika dalam pembuatan zeolit, baik
melalui proses alkali hidrotermal maupun sintesis pada temperatur kamar. Dewasa
ini, telah banyak dilakukan penelitian sintesis zeolit dengan memanfaatkan abu
sekam padi sebagai sumber silika antara lain zeolit A oleh Sinung Kurny Hadi
(1993), Suharno (1994), dan Nur (2001); zeolit Y oleh Didi Dwi Anggoro,
Muhamad Amri Fauzan, dan Nanda Dharmaparayana (2007); dan nanozeolit NaA
oleh Ghasemi dan Younesi (2011).
Zeolit merupakan kristal aluminosilikat terhidrasi yang mengandung kation
alkali maupun alkali tanah. Struktur zeolit berupa kerangka tiga dimensi terbuka
yang dibangun oleh tetrahedral-tetrahedral SiO44- dan AlO45− yang saling
berhubungan melalui atom O membentuk rongga-rongga intrakristalin dan
saluran-saluran teratur. Dalam struktur tersebut, Si4+ dapat digantikan dengan Al3+
sehingga terbentuk muatan negatif berlebih pada ion Al. Muatan negatif ini akan
dinetralkan oleh kation-kation (Barrer, 1982). Zeolit dapat digunakan dalam
katalis sehingga zeolit sintetis ini dapat dikembangkan untuk keperluan alternatif
pengolah limbah.
Pada penelitian yang dilakukan oleh A.M. Fuadi, dkk (2012) mengenai
pembuatan zeolit sintetis dari sekam padi menghasilkan fakta bahwa temperatur
dan lamanya waktu sintesis dapat berpengaruh terhadap kristalinitas zeolit yang
dihasilkan. Pada penelitian yang dilakukan oleh Ghasemi dan Younesi (2011)
mengenai preparasi dan karakterisasi nanozeolit NaA dari abu sekam padi pada
temperatur kamar tanpa menambahkan aditif organik diperoleh hasil bahwa
alkalinitas, perbandingan Na2O/SiO2, dan waktu kristalisasi berpengaruh pada
karakteristik produk yang dihasilkan. Pada penelitian yang dilakukan oleh
Jumaeri, Widi Astuti, dan Wahyu Tutik Puji Lestari (2007) tentang sintesis zeolit
dari abu layang batubara diketahui bahwa konsentrasi NaOH, waktu, dan
temperatur proses hidrotermal berpengaruh pula terhadap karakteristik produk
yang dihasilkan.
Berdasarkan latar belakang tersebut, mendorong penulis untuk melakukan
penelitian menggunakan abu sekam padi sebagai sumber silika dalam sintesis
zeolit yang dilakukan pada suhu kamar dengan berbagai variasi waktu aging.
Sintesis pada suhu kamar didasarkan pada prinsip Green Chemistry yang
memperhitungkan sumber daya yang digunakan serta penggunaan energi yang
diminimalkan. Pada penelitian ini akan dilakukan karakterisasi pada zeolit hasil
sintesis dengan menggunakan Difraksi Sinar-X (XRD) untuk mengetahui struktur
kristal (kristalinitas) zeolit yang dihasilkan dan Spektroskopi Inframerah (FTIR)
B. Identifikasi Masalah
Berdasarkan latar belakang masalah yang telah diuraikan di atas,
permasalahan yang dapat diidentifikasi adalah sebagai berikut.
1. Sumber silika yang digunakan dalam proses sintesis zeolit.
2. Temperatur yang digunakan pada proses sintesis zeolit.
3. Waktu aging yang digunakan pada sintesis zeolit.
4. Karakterisasi senyawa zeolit hasil sintesis.
C. Pembatasan Masalah
Berdasarkan berbagai identifikasi masalah di atas, maka dalam penelitian
ini masalah dibatasi sebagai berikut.
1. Sumber silika yang digunakan adalah abu sekam padi yang diperoleh dari
tempat pembuatan batu bata di dusun Ngampon, Sitimulyo, Piyungan, Bantul,
Yogyakarta yang diabukan dalam tungku pembakar.
2. Temperatur yang digunakan pada proses sintesis zeolit adalah temperatur
kamar (T= 25 ± 2°C).
3. Waktu aging yang digunakan pada sintesis zeolit yaitu 24 , 48, dan 72 jam.
4. Karakterisasi senyawa zeolit hasil sintesis meliputi struktur kristal
(kristalinitas) dengan menggunakan Difraksi Sinar-X (XRD) dan analisis
gugus fungsi yang ditentukan dengan Spektroskopi Inframerah (FTIR).
D. Perumusan Masalah
Berdasarkan batasan masalah di atas, permasalahan dalam penelitian ini
1. Berapakah waktu aging optimal pada sintesis zeolit dari abu sekam padi pada
temperatur kamar?
2. Bagaimana pengaruh waktu aging terhadap karakter zeolit hasil sintesis dari
abu sekam padi?
E. Tujuan Penelitian
Penelitian ini dilaksanakan dengan tujuan sebagai berikut.
1. Menentukan waktu aging optimal pada sintesis zeolit dari abu sekam padi
pada temperatur kamar.
2. Mengetahui pengaruh waktu aging terhadap karakter zeolit hasil sintesis dari
abu sekam padi.
F. Manfaat Penelitian
Manfaat yang diperoleh dari penelitian ini adalah sebagai berikut.
1. Memberikan informasi mengenai waktu aging optimal pada sintesis zeolit dari
abu sekam padi dengan menggunakan temperatur kamar.
2. Memberikan pengetahuan tentang pengaruh waktu aging pada sintesis zeolit
dari abu sekam padi sehingga terhadap karakter hasil sintesis.
3. Memberikan pengetahuan tentang cara pengolahan limbah sekam padi yang
mudah dan tidak memerlukan biaya yang banyak.
BAB II
KAJIAN PUSTAKA
A. Deskripsi Teori 1. Sekam Padi
Padi merupakan komoditas pangan utama di Indonesia. Tingkat produksi
maupun konsumsi padi selalu menempati urutan pertama dibandingkan dengan
komoditas tanaman pangan lainnya. Konsumsi padi dari tahun ke tahun selalu
mengalami peningkatan seiring dengan pertambahan penduduk. Demikian juga
dengan produksi maupun produktivitas padi semakin meningkat seiring dengan
penggunaan varietas unggul dan teknik budidaya yang intensif (Yudhi Mahmud
dan Sulistyo Sidik Purnomo, 2014).
Tanaman padi merupakan sejenis tumbuhan semusim yang sangat mudah
ditemukan, terutama di daerah pedesaan. Tanaman padi termasuk tanaman yang
berumur pendek. Biasanya hanya berumur kurang dari satu tahun dan berproduksi
satu kali. Setelah tanaman padi itu berbuah dan dipanen, padi tidak akan tumbuh
seperti semula lagi, tetapi akan mati. Pada dasarnya, tanaman padi dibagi menjadi
dua bagian, yaitu bagian vegetatif dan bagian generatif. Bagian vegetatif terdiri
atas akar, batang, anakan, dan daun, sedangkan bagian generatif terdiri atas malai
dan buah padi (AAK, 1990).
Sekam padi adalah bagian terluar dari butir padi. Sekam padi merupakan
produk samping yang melimpah dalam proses penggilingan padi, yaitu sekitar
20% dari bobot gabah. Sekam padi terdiri dari senyawa organik dan senyawa
lemak, serat, pentosa, selulosa, hemiselulosa, dan lignin. Sedangkan komposisi
senyawa anorganik biasanya terdapat dalam abunya. Komposisi sekam padi dapat
dilihat pada Tabel 1.
Tabel 1. Komposisi Kimia Sekam Padi
No. Komponen % Berat
1. H2O 2,4 - 11,35
2. Crude Protein 1,7 - 7,26
3. Crude Fat 0,38 - 2,98
4. Ekstrak Nitrogen Bebas 24,7 - 38,79
5. Crude Fiber 31,37 - 49,92
6. Abu 13,16 - 29,04
7. Pentosa 16,94 - 21,95
8. Selulosa 34,34 - 43,80
9. Lignin 21,40 – 46,97
(Sumber : Houston, 1972)
Penggunaan sekam padi antarnegara atau daerah berbeda-beda, tergantung
pada sistem penggilingan padi. Pertimbangan penggunaannya akan dipengaruhi
oleh suplai di suatu daerah, penyimpanan, teknologi yang ada, dan yang penting
adalah pertimbangan ekonomi. Diperkirakan saat ini, hampir seluruh sekam tidak
dipakai atau dibuang begitu saja. Sebenarnya, sekam padi bisa digunakan untuk
berbagai keperluan, akan tetapi penggunaannya di Indonesia masih terbatas pada
beberapa hal, seperti litter untuk ternak dan bahan bakar untuk pembakaran tanah
liat (Edi Soenarjo, Djoko S. Damardjati, dan Mahyuddin Syam, 1991).
Menurut Joddy Arya Laksmono dan Nova Ardiyanto (1999), sekam padi
sebagai limbah pertama dari penggilingan padi memiliki potensi cukup besar
1. Sumber Silika
Silika dapat diperoleh dengan membakar sekam pada suhu tertentu
sehingga dihasilkan abu yang berwarna keputih-putihan yang mengandung silika
sebagai komponen utamanya.
2. Penghasil pelarut berupa minyak
Pemasakan sekam dengan adanya larutan asam dalam proses destilasi uap
akan menghasilkan minyak yang berfungsi sebagai pelarut. Juga sebagai bahan
baku industri kimia, terutama kandungan zat kimia furfural.
3. Bahan Bangunan
Sekam digunakan pada bahan bangunan terutama kandungan silika (SiO2)
untuk campuran pada pembuatan semen portland, bahan isolasi, husk-board dan
campuran pada industri bata merah, seperti cetakan batu bata, batu bata tulis. Hal
ini penting untuk membuat batu bata dan beton lebih ringan. Sekam padi juga
dapat digunakan untuk membuat papan kedap air bagi bangunan.
4. Bahan Bakar
Sekam dipakai untuk menggerakkan mesin di dalam penggilingan padi.
Selain itu dipakai untuk memanaskan udara dalam pengeringan padi. Sumber
energi panas karena kadar selulosanya cukup tinggi sehingga dapat memberikan
pembakaran yang merata dan stabil. Jika diinginkan tidak ada asap dan
pemanasan lebih lama, maka sekam digunakan dalam bentuk briket arang sekam.
5. Bahan Pengampelas
Kandungan silika yang sangat tinggi pada bagian luar sekam
mengakibatkan kekerasan yang tinggi pada sekam. Hal tersebut membuat sekam
mempunyai sifat abrasive (sifat keras) sehingga dapat digunakan sebagai
2. Abu Sekam Padi
Abu sekam padi merupakan limbah yang diperoleh dari hasil pembakaran
sekam padi. Pada pembakaran sekam padi, semua komponen organik diubah
menjadi gas karbondioksida (CO2) dan air (H2O) dan tinggal abu yang merupakan
komponen anorganik (Amaria, 2012). Sekam padi apabila dibakar secara
terkontrol pada suhu tinggi (500-600ºC) akan menghasilkan abu silika yang dapat
dimanfaatkan untuk berbagai proses kimia (Andhi Laksono Putro dan Didik
Prasetyoko, 2007). Sebagian besar abu tersebut mengandung silika, sedikit logam
oksida, dan karbon residu yang diperoleh dari pembakaran terbuka. Komposisi
kimia abu sekam padi dapat dilihat pada Tabel 2.
Tabel 2. Komposisi Abu dari Sekam Padi. Komponen % Berat Kering
SiO2 86,9 - 97,3
K2O 0,58 – 2,50
Na2O 0,0 – 1,75
CaO 0,20 – 1,50
MgO 0,12 – 1,96
Fe2O3 trace – 0,54
P2O5 0,20 – 2,85
SO3 0,10 – 1,13
Cl trace – 0,42
(Sumber: Houston dalam Edi Soenarjo, Djoko S. Damardjati, dan Mahyuddin Syam, 1991).
Berdasarkan literatur lain dijelaskan bahwa sekam padi yang dibakar pada
suhu antara 500-700ºC akan menghasilkan struktur abu sekam padi yang amorf
(Ngatijo, Faizar Faried, dan Intan Lestari, 2011). Pembakaran sekam dapat
menghasilkan silika dalam berbagai bentuk tergantung pada kebutuhan industri
tertentu dengan mengatur suhu pembakaran. Silika dalam bentuk amorf sangat
abu silika bentuk amorf dan biasanya mengandung 86,9–97,80% silika dan 10–
15% karbon (Dardjo Sumaatmadja, 1985).
3. Senyawa SiO2
Silika adalah senyawa hasil polimerisasi asam silikat, yang tersusun dari
rantai satuan SiO4 tetrahedral dengan formula umum SiO2. Di alam, senyawa
silika ditemukan dalam beberapa bahan alam, seperti pasir, kuarsa, gelas, dan
sebagainya. Silika sebagai senyawa yang terdapat di alam berstruktur kristalin,
sedangkan sebagai senyawa sintetis adalah amorf. Secara sintetis senyawa silika
dapat dibuat dari larutan silikat atau dari pereaksi silan (Siti Sulastri dan Susila
Kristianingrum, 2010).
Silika merupakan mineral yang banyak terdapat di alam dalam keadaan
bebas maupun sebagai campuran dengan mineral lainnya membentuk mineral
silikat. Senyawa silikat yang paling sederhana mengandung ion SiO − dan dikenal
sebagai ortosilikat. Dalam spesies SiO −, atom Si merupakan atom pusat dari
sebuah tetrahedron yang keempat sudutnya ditempati oleh atom oksigen (O)
(Kristian H. Sugiyarto, 2004). Kerangka struktur SiO − dapat dilihat seperti pada
Gambar 1.
Gambar 1. Struktur SiO −
Menurut Kristian Handoyo (1996), silika dibagi menjadi 2 macam. 1. Silika amorf
Silika amorf terbentuk ketika silikon teroksidasi secara termal. Silika amorf
terdapat dalam beberapa bentuk yang tersusun dari partikel-partikel kecil yang
kemungkinan ikut tergabung. Biasanya silika amorf mempunyai kerapatan
2,21g/cm3.
2. Silika kristal
Silika kristal terdiri dari bermacam-macam jenis, seperti kwarsa, tridimit,
dan kristobalit yang merupakan akibat dari modifikasi temperatur dari rendah ke
tinggi yang merubah simetri kristal dan kerapatannya.
Silika merupakan bahan kimia yang pemanfaatan dan aplikasinya sangat
luas, mulai bidang elektronik, mekanik, medis, seni hingga bidang-bidang lainnya.
Salah satu pemanfaatan serbuk silika yang cukup luas adalah sebagai penyerap
kadar air di udara sehingga memperpanjang masa simpan bahan dan sebagai
bahan campuran untuk membuat keramik seni (Islam dan Ani, 2000).
4. Zeolit
Zeolit pertama kali ditemukan pada tahun 1756 oleh Cronstedt, seorang ahli
mineralogi Swedia. Nama zeolit berasal dari dua kata dalam bahasa Yunani, yaitu
“zein” berarti “mendidih” dan “lithos” artinya “batuan". Disebut demikian karena
mineral ini mempunyai sifat mendidih/mengembang apabila dipanaskan (M.
Arifin dan Uun Bisri, 1995).
Zeolit merupakan mineral yang terdiri dari kristal aluminosilikat terhidrasi
yang mengandung kation alkali atau alkali tanah dalam kerangka tiga dimensinya.
dan dapat menyerap air secara reversibel (Mursi Sutarti dan Minta Rachmawati,
1994).
Struktur zeolit berupa kerangka tiga dimensi terbuka yang dibangun oleh
tetrahedral-tetrahedral SiO44- dan AlO4− yang saling berhubungan melalui atom O
membentuk rongga-rongga intrakristalin dan saluran-saluran yang teratur. Dalam
struktur tersebut, Si4+ dapat digantikan dengan Al3+ sehingga terbentuk muatan
negatif berlebih pada ion Al. Muatan negatif ini akan dinetralkan oleh
kation-kation (Barrer, 1982).
Kerangka tetrahedral alumina dan silikat yang membentuk struktur zeolit
dapat dilihat pada Gambar 2.
Gambar 2. Tetrahedral Alumina dan Silikat pada Struktur Zeolit
(Sumber: Barrer, 1982).
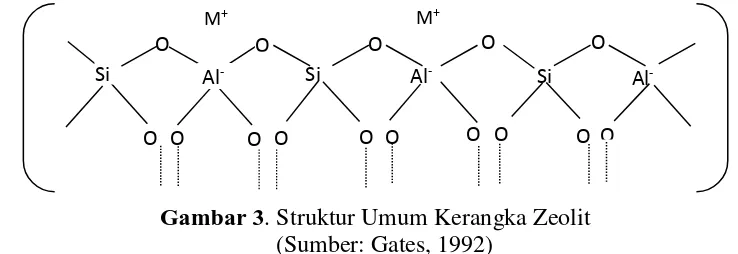
Struktur umum penyusun kerangka zeolit dapat dilihat pada Gambar 3
berikut ini:
Gambar 3. Struktur Umum Kerangka Zeolit
(Sumber: Gates, 1992)
Al -O
O O
Si O
O O
Si Al-
O
O O O
O O O O
M+ M+
O
Si Al-
O O O O O O O
Rumus struktur zeolit menurut Georgiev et al. (2009) dapat dituliskan
sebagai berikut.
Mx/n [(AlO2)x.(SiO2)y] . wH2O
Keterangan: M = kation alkali atau alkali tanah
n = valensi dari kation M
w = jumlah molekul air per satu unit sel
x,y = total jumlah tetrahedral per satu unit sel
[ ] = struktur kerangka alumina silikat
Jadi zeolit terdiri dari 3 komponen, yaitu kation yang dipertukarkan,
kerangka aluminosilikat, dan fase air. Ikatan ion Al-Si-O membentuk struktur
kristal, sedangkan logam alkali merupakan sumber kation yang mudah
dipertukarkan (Mursi Sutarti dan Minta Rachmawati, 1994).
Menurut Mursi Sutarti dan Minta Rachmawati (1994), zeolit mempunyai
beberapa sifat, diantaranya adalah sebagai berikut.
1. Dehidrasi
Sifat dehidrasi zeolit berpengaruh terhadap sifat adsorbsinya. Zeolit dapat
melepaskan molekul air dari dalam rongga permukaan yang menyebabkan medan
listrik meluas ke dalam rongga utama dan akan efektif terinteraksi dengan
molekul yang akan diadsorbsi.
2. Adsorbsi
Dalam keadaan normal ruang hampa dalam kristal zeolit terisi oleh molekul
air bebas yang berada di sekitar kation. Bila kristal zeolit dipanaskan pada suhu
300–400ºC maka air tersebut akan keluar sehingga zeolit dapat berfungsi sebagai
3. Penukar ion
Ion-ion pada rongga atau kerangka elektrolit berguna untuk menjaga
kenetralan zeolit. Ion-ion ini dapat bergerak bebas sehingga pertukaran ion yang
terjadi tergantung dari ukuran dan muatan maupun jenis zeolitnya. Sifat sebagai
penukar ion dari zeolit antara lain tergantung dari sifat kation, suhu dan jenis
anion.
4. Katalis
Ciri paling khusus dari zeolit yang secara praktis akan menentukan sifat
khusus mineral ini adalah adanya ruang kosong yang akan membentuk saluran di
dalam strukturnya. Bila zeolit digunakan pada proses penyerapan atau katalitis
maka akan terjadi difusi molekul ke dalam ruang bebas di antara kristal. Dengan
demikian dimensi serta lokasi saluran sangat penting. Reaksi kimia juga terjadi
dipermukaan saluran tersebut. Zeolit merupakan katalisator yang baik karena
mempunyai pori-pori yang besar dengan permukaan maksimum.
5. Penyaring/pemisah
Zeolit sebagai penyaring molekul maupun pemisah didasarkan atas
perbedaan bentuk dan ukuran. Molekul yang berukuran lebih kecil dapat melintas
sedangkan yang berukuran lebih besar dari ruang hampa akan tertahan atau
ditolak.
Menurut proses pembentukannya, zeolit dapat digolongkan menjadi dua
kelompok, yaitu zeolit alam dan zeolit sintetis. Zeolit alam terbentuk karena
adanya proses perubahan alam (zeolitisasi) dari batuan vulkanik tuf. Sedangkan
zeolit sintetis dibuat dari gel alumio silikat dengan meniru proses hidrotermal
silikat, dan natrium hidroksida (M. Arifin dan Uun Bisri, 1995). Menurut
Auerbach dkk dalam A.M. Fuadi, dkk (2012), zeolit sintetis memiliki karakteristik
yang berbeda dengan zeolit alam. Jika karakteristik zeolit alam tergantung dengan
kondisi geologis dan geografis alam, maka karakteristik zeolit sintetis hanya
dipengaruhi oleh teknik sintesis, kondisi proses pembuatan serta komposisi bahan
baku. Dewasa ini telah dikenal beragam jenis zeolit sintetis, beberapa diantaranya
dapat dilihat pada Tabel 3.
Tabel 3. Rumus Oksida Beberapa Jenis Zeolit Sintetis
Zeolit Rumus Oksida
Zeolit A Na2O.Al2O3.2SiO2.4,5H2O
Zeolit N-A (Na,TMA)2O.Al2O3.4,8SiO2.7H2O; TMA – (CH3)4N+
Zeolit H K2O.Al2O3.2SiO2.4H2O
Zeolit L (K2Na2)O.Al2O3.6SiO2.5H2O
Zeolit X Na2O.Al2O3.2,5SiO2.6H2O
Zeolit Y Na2O.Al2O3.4,8SiO2.8,9H2O
Zeolit P Na2O.Al2O3.2-5SiO2.5H2O
Zeolit O (Na2,K2,TMA2)O.Al2O3.7SiO2.3,5H2O; TMA – (CH3)4N+ Zeolit Ω (Na,TMA)2O.Al2O3.7SiO2.5H2O; TMA – (CH3)4N+
Zeolit ZK-4 0,85Na2O.0,15(TMA)2O.Al2O3.3,3SiO2.6H2O
Zeolit ZK-5 (R,Na2)O.Al2O3.4-6SiO2.6H2O
(Sumber: Georgiev et al., 2009)
Sifat zeolit sangat tergantung dari jumlah komponen Al dan Si dari zeolit
tersebut. Oleh sebab itu, maka zeolit sintetis menurut Mursi Sutarti dan Minta
Rachmawati (1994) dikelompokkan sesuai dengan perbandingan kadar komponen
Al dan Si dalam zeolit menjadi:
1. Zeolit kadar Si rendah (kaya Al)
Zeolit jenis ini banyak mengandung Al, berpori, mempunyai nilai ekonomi
dapat mencapai 0,5 cm3 tiap cm3 volum zeolit. Contoh zeolit Si rendah yaitu zeolit
A dan X.
2. Zeolit kadar Si sedang
Jenis zeolit modernit mempunyai perbandingan Si/Al = 5 sangat stabil,
maka diusahakan membuat zeolit dengan kadar Si yang lebih tinggi dari 1 yang
kemudian diperoleh zeolit Y dengan perbandingan kadar Si/Al = 1-3. Contoh
zeolit sintetis jenis ini adalah zeolit Omega.
3. Zeolit kadar Si tinggi
Zeolit ini mempunyai perbandingan kadar Si/Al antara 10-100 bahkan lebih
dan mempunyai sifat permukaan yang kadang-kadang tidak dapat diperkirakan
sebelumnya. Sifatnya sangat hidrofilik dan akan menyerap molekul yang tidak
polar dan baik digunakan sebagai katalisator asam untuk hidrokarbon. Contoh
zeolit jenis ini adalah zeolit ZSM-5, ZSM-11, ZSM-21, ZSM-24.
4. Zeolit Si
Kalau zeolit Si tinggi masih mengandung Al meskipun hanya sedikit, tetapi
zeolit Si ini tidak mengandung Al sama sekali atau tidak mempunyai sisi kation
sama sekali. Sifat zeolit jenis ini adalah sangat hidrofilik-hidrofobik sehingga
dapat mengeluarkan atau memisahkan suatu molekul organik dari suatu campuran
air. Contoh zeolit silika adalah silikalit.
5. Sintesis Zeolit
Menurut Mursi Sutarti dan Minta Rachmawati (1994), zeolit sintetis dapat
diproduksi dengan cara hidrotermal dan kebanyakan diproduksi di bawah kondisi
tidak seimbang, akibatnya zeolit yang dihasilkan merupakan bahan metastabil
Teknik hidrotermal merupakan teknik preparasi zeolit sintetis yang paling
umum digunakan. Meskipun relatif sederhana dan tidak memerlukan peralatan
yang khusus, namun teknik ini memiliki kelemahan, yaitu memerlukan waktu
yang lama dan banyak bahan kimia yang terbuang. Sehingga pada tahap terapan,
metode ini menjadi tidak ekonomis (A.M. Fuadi dkk, 2012). Bahan utama
pembentuk zeolit dalam kondisi hidrotermal adalah aluminat silikat (gel) dan
berbagai logam sebagai kation. Komposisi gel, sifat fisik dan kimia reaktan, serta
jenis kation dan kondisi kristalisasi sangat menentukan struktur yang diperoleh.
Menurut Mursi Sutarti dan Minta Rachmawati (1994), beberapa proses
untuk menghasilkan zeolit yang mempunyai nilai ekonomi dapat dibagi menjadi
3 kelompok berikut.
1) Proses hidrogel
Bahan dasar awal terdiri dari larutan Na silikat, Na aluminat, dan NaOH. Gel
dikristalisasikan dalam sistem hidrotermal tertutup pada suhu yang bervariasi
antara suhu kamar sampai 200ºC. Waktu yang diperlukan untuk kristalisasi
adalah antara beberapa jam sampai beberapa hari. Bahan lain yang diperlukan
adalah metal alkali dari hidroksida yang larut, aluminat dan silikat.
2) Konversi dari mineral kapur
Bahan dasar awal untuk proses ini adalah kaolin, yang biasanya harus
didehidroksilasi menjadi meta-kaolin dengan jalan kalsinasi. Pada suhu antara
500-600ºC terbentuk meta-kaolin, diikuti terbentuknya mulit pada suhu antara
3) Bahan dasar yang ada di alam
Bahan yang ada di alam antara lain kerak geotermal, abu terbang dan limbah
cair dari industri aluminium. Kerak geotermal yang mengandung 92% SiO2
dan 1,1 Al2O3 ditambah dengan Na aluminat dan NaOH sehingga campuran
mempunyai komposisi Na2O/SiO2 = 1,1; SiO2/Al2O3 = 2 dan H2O/Na2O = 60
dipanaskan pada suhu 90-95ºC selama 4 jam akan menghasilkan zeolit A
dengan kadar 88%.
Kapasitas air murni sebagai pelarut pada temperatur yang tinggi seringkali
tidak mampu untuk melarutkan zat dalam proses pengkristalan, oleh karena itu
perlu ditambahkan mineralizer. Mineralizer adalah suatu senyawa yang
ditambahkan pada larutan yang encer untuk mempercepat proses kristalisasi
dengan cara meningkatkan kemampuan melarutnya, sehingga yang biasanya tidak
dapat larut dalam air dengan ditambahkannya mineralizer dapat menjadi larut.
Mineralizer yang khas adalah suatu hidroksida dari logam alkali, khususnya
amfoter dan oksida asam. Mineralizer yang digunakan untuk SiO2 adalah NaOH,
KOH, Na2CO3 atau NaF (Jumaeri, Widi Astuti, dan Wahyu Tutik Puji Lestari,
2007).
6. Difraksi Sinar-X (XRD)
Difraksi sinar-X merupakan suatu metode analisis yang didasarkan pada
interaksi antara materi dengan radiasi elektromagnetik sinar-X (mempunyai λ =
0,5-2,5 Å dan energi ± 107 eV), yaitu pengukuran radiasi sinar-X yang terdifraksi
oleh bidang kristal. Penghamburan sinar-X oleh unit-unit padatan kristalin, akan
menghasilkan pola-pola difraksi yang digunakan untuk menentukan susunan
Dasar dari penggunaan difraksi sinar-X untuk mempelajari kisi kristal
adalah persamaan Bragg. Menurut Chorkendroff dan Niemantsverdiet (2003),
persamaan Bragg ditunjukkan pada persamaan berikut.
n.λ = 2 d sinθ
Keterangan: n : bilangan bulat orde refleksi/ pembiasan (1,2,3, dst....)
λ : panjang gelombang sinar-X yang digunakan (Å)
d : jarak antara dua bidang kisi (Å)
θ : sudut antara sinar datang dengan bidang normal (º)
Pola difraksi sinar-X memberikan data berupa jarak interplanar (d spacing),
sudut difraksi (2θ), intensitan relative (I/I0), indeks miller (dhkl), lebar puncak,
parameter unit sel (a, b, c, a, b dan g). Analisis kualitatif maupun kuantitatif data
tersebut memberikan informasi tentang kemurnian mineral, identifikasi jenis
mineral dengan membandingkan data d yang diperoleh dengan data d dari Joint
Comitte of Powder Diffraction Standart (JCPDS) dan diperjelas dengan XRD
Simulated Pattern (Udaibah dalam Dania Kurniawati, 2010).
Pola difraktogram yang dihasilkan berupa deretan puncak-puncak difraksi
dengan intensitas relatif bervariasi sepanjang nilai 2θ tertentu. Besarnya intensitas
relatif dari deretan puncak-puncak tersebut bergantung pada jumlah atom atau ion
yang ada dan distribusinya di dalam sel satuan material tersebut. Tiap puncak
yang muncul pada pola XRD mewakili satu bidang kristal yang memiliki orientasi
tertentu dalam sumbu tiga dimensi. Pola difraksi setiap padatan kristalin yang
yang digunakan. Dengan demikian, sangat kecil kemungkinan dihasilkan difraksi
yang sama untuk suatu padatan kristalin yang berbeda (Warren, 1990).
Secara umum, difraksi serbuk sinar-X digunakan untuk mengidentifikasi
bahan yang tidak diketahui, menentukan kemurnian sampel, dan menentukan
ukuran kristal. Banyak data difraksi serbuk sinar-X yang dikumpulkan dari
senyawa anorganik, organologam, dan organik telah disusun menjadi Joint
Committee on Powder Diffraction Standards (JCPDS). Standar ini digunakan
untuk mengidentifikasi bahan yang tidak diketahui (Weller, 2006).
Aplikasi sinar-X pada zeolit dapat ditentukan dengan membandingkan pada
pola difraksi standar JCPDS. Puncak karakteristik zeolit X sesuai pola difraksi
standar JCPDS No. 01-073-9586 Quality: B dapat dilihat pada Tabel 4.
Tabel 4. Puncak Karakteristik Zeolit X pada Standar JCPDS
No. 2θ d Irel h k l
1. 6,11 14,452 100,0 1 1 1
2. 9,99 8,850 19,8 2 2 0
3. 11,72 7,547 6,5 3 1 1
4. 15,42 5,743 8,1 3 3 1
5. 23,28 3,817 7,9 5 3 3
6. 26,63 3,345 6,6 2 4 6
7. 30,91 2,890 7,9 1 5 7
7. Spektroskopi Inframerah (FTIR)
Spektroskopi inframerah merupakan metode analisis yang didasarkan pada
penyerapan (adsorbsi) energi pada suatu molekul cuplikan yang dilewatkan radiasi
inframerah. Pengadsorbsian energi pada berbagai frekuensi dapat dideteksi oleh
spektrofotometer inframerah, yang memplot jumlah radiasi inframerah yang
diteruskan melalui cuplikan sebagai fungsi frekuensi (panjang gelombang) radiasi
yang lain, maka molekul akan tereksitasi ke tingkatan energi yang lebih tinggi bila
mereka menyerap radiasi inframerah. Hanya frekuensi (energi) tertentu dari
radiasi inframerah yang akan terserap oleh molekul (Hardjono Sastrohamidjojo,
1992).
Hampir setiap senyawa yang memiliki ikatan kovalen, baik senyawa
organik atau anorganik, menyerap berbagai frekuensi radiasi elektromagnetik
dalam daerah spektrum inframerah. Kegunaan utama dari spektrofotometri
inframerah adalah untuk memperoleh keterangan tentang struktur karena setiap
frekuensi radiasi yang berbeda berpengaruh terhadap molekul dengan cara yang
berbeda. Oleh sebab itu, perlu memperhatikan prosedur penyiapan cuplikan
mengingat senyawa yang akan dianalisis dapat berupa padatan, cairan, dan gas
yang memerlukan penanganan yang berbeda pula (Hardjono Sastrohamidjojo,
1992).
Spektrofotometer inframerah adalah suatu instrumen yang digunakan untuk
mengukur serapan radiasi inframerah pada berbagai panjang gelombang antara
300–4000 cm-1. Spektrum inframerah tengah yang terletak pada daerah panjang
gelombang 300-1300 cm-1 merupakan alat yang sensitif untuk menunjukkan sifat
struktur dari kerangka zeolit. Frekuensi vibrasi pada daerah tersebut menyediakan
informasi mengenai komposisi dan cara setiap tetrahedral SiO4 dan AlO4 terikat
satu sama lain (Flanigen, dan Khatami, 1974).
Serapan-serapan di atas 1300 cm-1 bukan merupakan serapan karakteristik
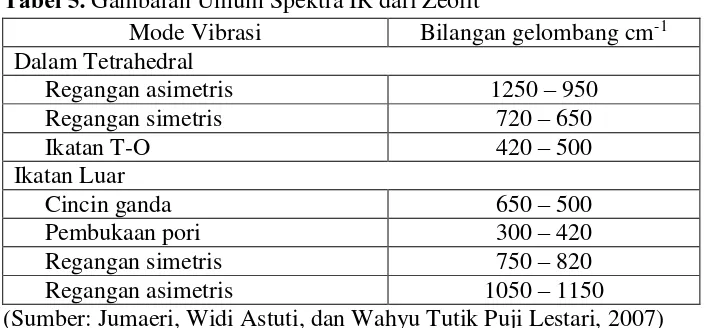
dari zeolit. Gambaran umum mengenai spektra IR dari zeolit ditunjukkan seperti
Tabel 5. Gambaran Umum Spektra IR dari Zeolit
Mode Vibrasi Bilangan gelombang cm-1
Dalam Tetrahedral
Regangan asimetris 1250 – 950
Regangan simetris 720 – 650
Ikatan T-O 420 – 500
Ikatan Luar
Cincin ganda 650 – 500
Pembukaan pori 300 – 420
Regangan simetris 750 – 820
Regangan asimetris 1050 – 1150
(Sumber: Jumaeri, Widi Astuti, dan Wahyu Tutik Puji Lestari, 2007)
B. Penelitian yang Relevan
Jumaeri, Widi Astuti, dan Wahyu Tutik Puji Lestari (2007) telah
melakukan penelitian mengenai preparasi zeolit dari abu layang batubara secara
alkali hidrotermal dengan menggunakan autoclave stainless-steel. Abu layang
batubara tersebut digunakan sebagai sumber SiO2 dan Al2O3. Dalam penelitian ini
diperoleh hasil bahwa aktivasi abu layang dengan proses alkali hidrotermal dapat
menghasilkan material zeolit (zeolit-like) yang mengandung mineral sodalit,
mullit, dan zeolit P. Karakteristik zeolit yang dihasilkan sangat dipengaruhi oleh
konsentrasi NaOH dan temperatur pada proses hidrotermal. Pada konsentrasi
NaOH dan temperatur yang lebih tinggi terjadi peningkatan kristalinitas produk.
Proses alkali hidrotermal pada temperatur 160ºC, konsentrasi NaOH 2M dan
waktu 72 jam dihasilkan zeolit dengan intensitas fasa kristalin tertinggi. Perlakuan
awal dengan larutan HCl 1M juga dapat meningkatkan kristalinitas produk yang
dihasilkan.
Penelitian lainnya memanfaatkan abu sekam padi sebagai sumber silika
Penelitian ini dilakukan pada suhu kamar tanpa menggunakan bahan organik.
Nanokristal zeolit NaA dengan ukuran kristal 50-120 nm berhasil disintesis pada
temperatur kamar dengan waktu kristalisasi selama 3 hari dan perbandingan
Na2O/SiO2 = 6. Hasil penelitian menunjukkan bahwa waktu reaksi, perbandingan
Na2O/SiO2, dan alkalinitas sangat berpengaruh pada sifat struktural produk yang
dihasilkan.
Penelitian lainnya yang juga memanfaatkan abu sekam padi sebagai sumber
silika untuk pembuatan zeolit dilakukan oleh A.M. Fuadi, dkk (2012). Pembuatan
zeolit sintetis dilakukan dengan menggunakan microwave pada berbagai variasi
suhu dan waktu. Pada penelitian ini, sintesis dengan microwave yang dilakukan
pada suhu rendah dapat menghasilkan kristal zeolit sintetis setelah 60 menit, pada
kondisi med low kristal zeolit diperoleh setelah proses 20 menit, dan pada suhu
sedang kristal zeolit sudah terbentuk meskipun proses baru berjalan 5 menit.
Kesimpulan yang diperoleh yaitu suhu dan waktu reaksi berpengaruh pada proses
pembuatan zeolit sintetis. Semakin besar suhu yang digunakan, maka akan
semakin cepat kristal zeolit sintetis tersebut terbentuk sehingga lebih efisien
waktu.
C. Kerangka Berpikir
Padi merupakan produk utama pertanian di berbagai negara agraris, seperti
Indonesia. Sekam padi merupakan salah satu hasil samping dari proses
penggilingan padi yang selama ini hanya dianggap sebagai limbah. Pada proses
pembakaran sekam padi, semua komponen organik diubah menjadi gas
kandungan silika (SiO2) yang cukup besar, yaitu berkisar antara 86,9-97,3%.
Kandugan silika yang tinggi tersebut memungkinkan dimanfaatkan sebagai
sumber silika untuk menggantikan sumber lain yang lebih mahal.
Penelitian ini mencoba memanfaatkan abu sekam padi sebagai sumber
silika pada pembuatan zeolit sintesis dengan menerapkan prinsip Green Chemistry
yang memperhitungkan sumber daya yang digunakan serta penggunaan energi
yang diminimalkan. Penelitian ini menggunakan temperatur kamar (T= 25 ± 2°C)
sebagai temperatur sintesis dengan berbagai variasi waktu aging.
Sintesis zeolit dimulai dengan peleburan abu sekam padi menggunakan
larutan natrium hidroksida (NaOH) akan membentuk larutan natrium silikat
(Na2SiO3) yang larut dalam air. Kemudian membuat larutan natrium aluminat
dengan mencampurkan larutan NaOH dengan Al2O3. Proses sintesis dilakukan
dengan menambahkan larutan natrium aluminat secara perlahan-lahan ke dalam
larutan natrium silikat disertai pengadukan hingga homogen. Pengadukan
dilanjutkan dengan periode aging pada suhu kamar (T= 25 ± 2ºC) dengan
berbagai variasi waktu aging, yaitu 24, 48, dan 72 jam.
Serbuk yang dihasilkan dari proses sintesis selanjutnya dikarakterisasi
secara kualitatif. Karakterisasi serbuk dilakukan dengan menggunakan difraksi
sinar-X untuk mengetahui struktur kristal (kristalinitas) zeolit yang dihasilkan dan
spektroskopi inframerah untuk mengetahui perubahan gugus fungsi. Hasil
karakterisasi tersebut diharapkan sama dengan standar difraksi sinar-X (JCPDS)
BAB III
METODE PENELITIAN
A. Subjek dan Objek Penelitian 1. Subjek Penelitian
Subjek penelitian ini adalah senyawa zeolit dari abu sekam padi.
2. Objek Penelitian
Objek penelitian ini adalah karakter zeolit dari abu sekam padi.
B. Variabel Penelitian 1. Variabel Bebas
Variabel bebas dalam penelitian ini adalah variasi waktu aging yaitu 24; 48;
dan 72 jam.
2. Variabel Terikat
Variabel terikat dalam penelitian ini adalah suhu reaksi, massa abu sekam
padi, dan waktu kalsinasi.
C. Alat dan Bahan Penelitian 1. Alat
Alat-alat yang digunakan dalam penelitian ini adalah sebagai berikut:
a. Spektrofotometer FTIR Shimadzu 8201 PC
b. Difraktometer Sinar-X (XRD) merkRigaku MiniFlex 600
c. Oven pemanas
d. Muffle Furnace
e. Desikator
g. Timbangan analitik merk Ohaus Explorer
h. Magnetic stirrer merk Cimarec 2 thermolyne
i. Labu Erlenmeyer
j. Pipet tetes
k. Kaca arloji
l. Cawan porselin
m. Kertas saring
n. pH meter
2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah sebagai berikut:
a. Sekam padi yang diperoleh dari tempat pembuatan batu bata di dusun
Ngampon, Sitimulyo, Piyungan, Bantul, Yogyakarta
b. NaOH (p.a. Merck), kadar 97 %
c. Al2O3 (p.a. Merck), kadar 97 %
d. Akuades
D. Prosedur Penelitian
1. Proses Pengabuan Sekam Padi
Sampel sekam padi diperoleh dari tempat pembuatan batu bata di dusun
Ngampon, Sitimulyo, Piyungan, Bantul, Yogyakarta. Sekam padi dibersihkan dari
batu, tanah, kerikil, daun, batang, dan kotoran lainnya. Sekam padi yang sudah
bersih dicuci dengan air bersih, kemudian dijemur di bawah sinar matahari hingga
kering. Sekam padi yang telah kering dan bersih dibakar dengan menggunakan
diabukan dalam tungku pembakar (muffle furnace) pada temperatur 600ºC selama
8 jam. Setelah didinginkan, abu sekam padi yang diperoleh digerus dan diayak
dengan menggunakan ayakan ukuran 200 mesh.
2. Pembuatan Larutan Natrium Silikat
Sebanyak 1,26 gram abu sekam padi hasil ayakan dicampur dengan NaOH
sebanyak 3,895 gram dan 24,93 gram akuades di dalam labu erlenmeyer.
Pencampuran tersebut disertai pengadukan dengan magnetic stirrer pada skala 6-8
selama 1 jam. Hasil pengadukan ini merupakan larutan yang akan digunakan
sebagai bahan sintesis zeolit pada temperatur kamar.
3. Pembuatan Larutan Natrium Aluminat
Larutan natrium aluminat dibuat dengan melarutkan 3,895 gram NaOH
dalam 24,93 gram akuades. Ke dalam larutan tersebut dimasukkan 2,04 gram
Al2O3 sambil dipanaskan pada suhu 50oC selama 1 jam disertai pengadukan
dengan magnetic stirrer pada skala 6-8. Larutan hasil pencampuran ini akan
digunakan sebagai bahan sintesis zeolit pada temperatur kamar.
4. Sintesis Zeolit
Proses sintesis zeolit dilakukan dengan menambahkan larutan natrium
aluminat secara perlahan-lahan ke dalam larutan natrium silikat dari abu sekam
padi disertai dengan pengadukan dengan kecepatan skala 2 selama 1 jam.
Kemudian pengadukan dilanjutkan dengan periode aging pada suhu kamar (T= 25
± 2oC) dengan variasi waktu aging 24, 48, dan 72 jam. Serbuk yang diperoleh
dicuci dengan akuades hingga mencapai pH 8, lalu dikeringkan dalam oven pada
suhu 110oC. Serbuk yang dihasilkan selanjutnya diuji secara kualitatif dengan
5. Karakterisasi Serbuk Hasil Sintesis a. Difraksi Sinar-X (XRD)
Serbuk ditempatkan pada plat kaca yang kemudian dimasukkan dalam
tempat sampel. Sampel disinari sinar-X pada pola daerah sudut difraksi 2θ(2-80º),
interval 0,02 dan laju 10 dengan menggunakan Difraktometer Sinar-X merk
Rigaku MiniFlex 600.
b. Spektroskopi Inframerah (FTIR)
Serbuk yang dihasilkan dari proses sintesis sebanyak ujung spatula
dicampur dengan KBr, selanjutnya dibuat pelet kemudian dimasukkan dalam
tempat sampel. Perekaman dilakukan menggunakan Spektrofotometer FTIR
Shimadzu 8201 PCpada daerah bilangan gelombang 300-4000 cm-1.
E. Teknik Pengumpulan Data
Data yang diperoleh pada penelitian ini berupa data yang diuji
menggunakan alat Difraktometer Sinar-X merk Rigaku MiniFlex 600 dan
Spektrofotometer FTIR Shimadzu 8201 PC untuk mengetahui struktur kristal
(kristalinitas) zeolit yang dihasilkan dan mengetahui perubahan gugus fungsional.
F. Teknik Analisis Data
Data yang diperoleh pada penelitian ini dianalisis secara kualitatif. Analisis
struktur kristal (kristalinitas) zeolit yang terbentuk dilakukan dengan
menggunakan Difraktometer Sinar-X merk Rigaku MiniFlex 600 pada pola
daerah sudut difraksi 2θ antara 2-80º. Selanjutnya nilai 2θ dalam difraktogram
hasil sintesis dibandingkan dengan standar difraksi sinar-X (JCPDS) No.
analisis gugus fungsional dari kristal zeolit hasil sintesis dilakukan dengan
menggunakan Spektrofotometer FTIR Shimadzu 8201 PC pada bilangan
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Hasil Penelitian
Penelitian yang telah dilakukan bertujuan untuk menentukan waktu aging
optimal pada sintesis zeolit dari abu sekam padi pada temperatur kamar dan
mengetahui pengaruh waktu aging terhadap karakter zeolit hasil sintesis dari abu
sekam padi.
Penelitian ini terdiri atas beberapa proses, yakni proses pengabuan sekam
padi, sintesis zeolit dan karakterisasi serbuk hasil sintesis. Hasil dari
masing-masing proses dan data yang dihasilkan dijabarkan sebagai berikut.
1. Pengabuan Sekam Padi
Sekam padi yang digunakan berasal dari tempat pembuatan batu bata di
dusun Ngampon, Sitimulyo, Piyungan, Bantul, Yogyakarta. Hasil yang diperoleh
dalam proses pengabuan sekam padi adalah abu sekam yang berwarna putih dan
bercampur sedikit warna hitam. Selanjutnya abu sekam yang berwarna putih
dipisahkan secara manual, kemudian digerus dan diayak dengan ayakan 200 mesh,
sehingga diperoleh abu sekam padi berwarna putih dan halus.
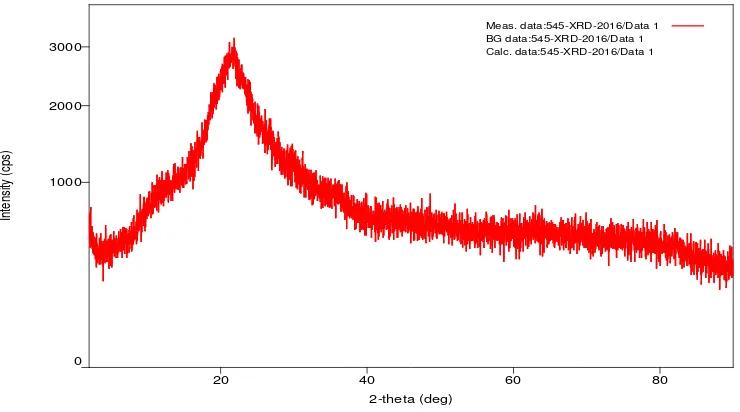
Hasil analisa silika dari abu sekam padi menggunakan XRD ditunjukkan
Gambar 4. Difraktogram Abu Sekam Padi
Pola difraktogram pada Gambar 4 menunjukkan bahwa abu sekam padi
yang dihasilkan bersifat amorf dengan satu puncak tajam pada sudut 2θ: 21,16°.
2. Sintesis Zeolit
Sintesis zeolit dilakukan dengan mereaksikan larutan natrium silikat dari
abu sekam padi dan larutan natrium aluminat. Hasil dari sintesis tersebut berupa
serbuk berwarna putih. Reaksi pembentukan larutan natrium silikat dan larutan
natrium aluminat menurut Widi Astuti dan Indah Nurul Izzati (2015) adalah
sebagai berikut.
SiO2 (abu sekam padi) + 2 NaOH (aq) Na2SiO3 (aq)
Al2O3 (s) + 2 NaOH (aq) 2 NaAl(OH)4 (aq)
Reaksi kimia proses pembentukan zeolit adalah sebagai berikut.
Na2Al(OH)4(aq) + Na2SiO3(aq) Nax [(AlO2)x(SiO2)y] . wH2O Meas. data:545-XRD-2016/Data 1
BG data:545-XRD-2016/Data 1 Calc. data:545-XRD-2016/Data 1
2-theta (deg)
Intensity (cps)
20 40 60 80
0 1000 2000 3000
3. Karakterisasi Serbuk Hasil Sintesis
Karakterisasi serbuk hasil sintesis pada penelitian ini dilakukan dengan
menggunakan difraksi sinar-x (XRD) dan spektroskopi inframerah (FTIR). Hasil
karakterisasi serbuk hasil sintesis dijabarkan sebagai berikut.
a. Difraksi Sinar-X (XRD)
Karakterisasi dengan difraksi sinar-x (XRD) digunakan untuk mengetahui
struktur kristal (kristalinitas) serbuk hasil sintesis. Karakterisasi ini menggunakan
alat Difraktometer Sinar-X (XRD) merk Rigaku miniFlex 600 dengan pola sudut
difraksi 2θ(2-80º). Data yang diperoleh dari karakterisasi ini disebut difraktogram.
Pola difraktogram hasil sintesis dengan berbagai variasi waktu aging
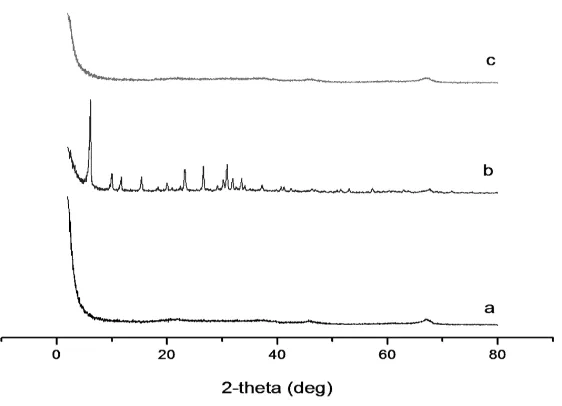
[image:32.595.185.466.404.607.2]ditunjukkan pada Gambar 5.
Gambar 5. Difraktogram Serbuk Hasil Sintesis dengan Variasi Waktu Aging
a) 24 Jam, b) 48 Jam, dan c) 72 Jam
Gambar 5a menunjukkan sintesis zeolit yang dilakukan pada temperatur
struktur amorf. Gambar 5b menunjukkan sintesis zeolit yang dilakukan pada
temperatur kamar dengan variasi waktu aging 48 jam menghasilkan serbuk yang
bersifat kristalin dan memiliki kristalinitas tinggi. Dalam difraktogram tersebut
muncul puncak-puncak yang jelas dan memiliki intensitas ketajaman puncaknya
tinggi, diantaranya pada sudut 2θ: 6,133º; 10,011º; 11,741º; 15,435º; 23,279º;
26,638º; dan 30,917º. Gambar 5c menunjukkan sintesis zeolit yang dilakukan
pada temperatur kamar dengan variasi waktu aging 72 jam menghasilkan serbuk
yang memiliki struktur amorf.
b. Spektroskopi Inframerah (FTIR)
Karakterisasi dengan spektroskopi inframerah (FTIR) digunakan untuk
mengetahui gugus fungsi yang terkandung dalam serbuk hasil sintesis.
Karakterisasi ini menggunakan alat Spektrofotometer FTIR Shimadzu 8201 PC
pada daerah bilangan gelombang 300-4000 cm-1. Data yang diperoleh dari
karakterisasi ini disebut spektrum inframerah.
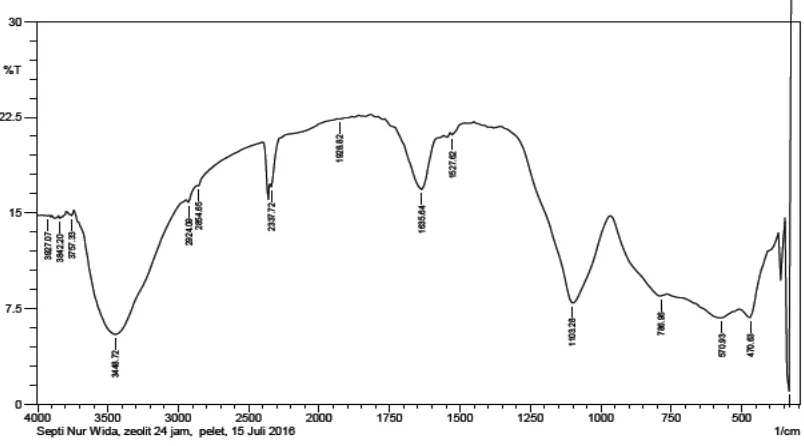
Spektrum inframerah serbuk yang dihasilkan dari sintesis pada temperatur
Gambar 6. Spektrum Inframerah Serbuk Hasil Sintesis pada Waktu Aging 24 Jam
Pada Gambar 6 dapat dilihat adanya beberapa serapan lemah yang muncul,
diantaranya pada bilangan gelombang 3448,72 cm-1; 1635,64 cm-1; 1103,28 cm-1;
786,96 cm-1; 570,93 cm-1; dan 470,63 cm-1.
Spektrum inframerah serbuk yang dihasilkan dari sintesis pada temperatur
Gambar 7. Spektrum Inframerah Serbuk Hasil Sintesis pada Waktu Aging 48 Jam
Pada Gambar 7 dapat dilihat adanya beberapa puncak tajam yang muncul,
diantaranya pada bilangan gelombang 3448,72 cm-1; 1635,64 cm-1; 972,12 cm-1;
740,12 cm-1; 563,21 cm-1; dan 462,92 cm-1.
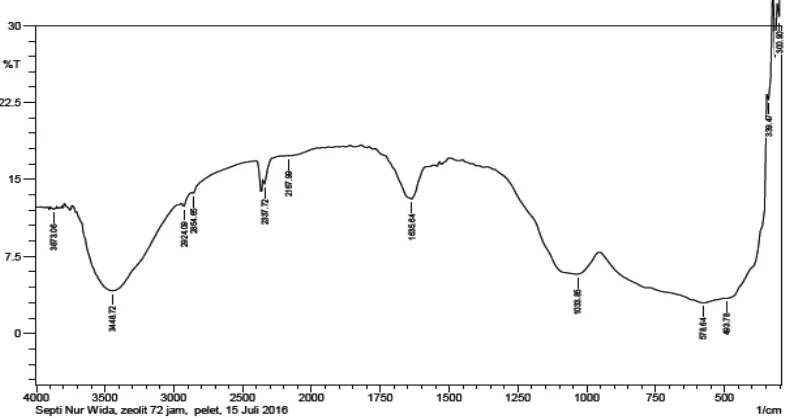
Spektrum inframerah serbuk yang dihasilkan dari sintesis pada temperatur
Gambar 8. Spektrum Inframerah Serbuk Hasil Sintesis pada Waktu Aging 72 Jam
Pada Gambar 8 dapat dilihat adanya beberapa serapan lemah yang muncul,
diantaranya pada bilangan gelombang 3448,72 cm-1; 1635,64 cm-1; 1033,85 cm-1;
578,64 cm-1; dan 493,78 cm-1.
B. Pembahasan
Pembahasan hasil penelitian ini terdiri atas beberapa proses, diantaranya
pengabuan sekam padi, sintesis zeolit, dan karakterisasi zeolit hasil sintesis. Hasil
dan uraian masing-masing proses dijabarkan sebagai berikut.
1. Pengabuan Sekam Padi
Proses pengabuan sekam padi dalam penelitian ini diawali dengan
pengambilan sampel sekam padi. Sekam padi dibersihkan dari pengotor padat dan
dijemur di bawah sinar matahari hingga kering. Sekam padi yang telah kering dan
bersih dibakar hingga menjadi arang berwarna hitam terlebih dahulu, dengan
sempurna sehingga diperoleh kemurnian abu yang tinggi. Kemudian arang
diabukan dalam muffle furnace pada temperatur 600ºC selama 8 jam.
Hasil yang diperoleh dari proses pengabuan sekam padi adalah abu yang
berwarna putih dan bercampur sedikit warna hitam. Abu yang berwarna putih
menunjukkan bahwa abu tersebut mengandung silika sebagai komponen
utamanya, sedangkan warna hitam masih mengandung senyawa karbon yang
belum terdekomposisi dan teroksidasi secara sempurna. Abu yang berwarna putih
dipisahkan secara manual, kemudian digerus dan diayak dengan ukuran 200 mesh.
Penggerusan dan pengayakan dilakukan untuk menghomogenkan ukuran dan
memperluas permukaan abu sekam padi sehingga mempercepat adanya interaksi
antarmolekul saat pembentukan natrium silikat.
Pada pola difraktogram Gambar 4 dapat dilihat bahwa abu sekam padi yang
dihasilkan memiliki kristalinitas rendah (bersifat amorf) dengan satu puncak tajam
pada sudut 2θ = 21,16º. Menurut Kalapathy, Proctor, dan Shultz (2002), puncak
tersebut merupakan puncak khas dari silika. Data hasil perbandingan antara abu
sekam padi yang dihasilkan dengan data difraktogram silika dapat ditunjukkan
pada Tabel 6.
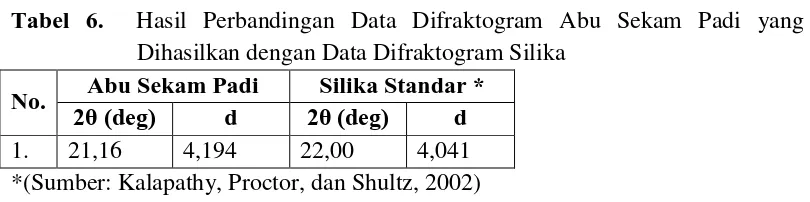
Tabel 6. Hasil Perbandingan Data Difraktogram Abu Sekam Padi yang
Dihasilkan dengan Data Difraktogram Silika
No. Abu Sekam Padi Silika Standar *
2θ (deg) d 2θ (deg) d
1. 21,16 4,194 22,00 4,041
*(Sumber: Kalapathy, Proctor, dan Shultz, 2002)
Berdasarkan data di atas dapat disimpulkan bahwa abu sekam padi yang
[image:37.595.108.513.551.652.2]dalam Sholeh Nura Aditama (2015), silika amorf memiliki susunan atom dan
molekul berbentuk pola acak dan tidak beraturan, sehingga dalam berbagai
kondisi silika ini lebih reaktif daripada silika kristalin. Maka dari itu, abu sekam
tersebut efektif digunakan untuk pembuatan natrium silikat.
2. Sintesis Zeolit
Pada penelitian ini, sintesis zeolit dilakukan dengan mereaksikan larutan
natrium silikat dengan larutan natrium aluminat. Larutan natrium silikat dibuat
dengan melarutkan NaOH dengan akuades, kemudian ditambahkan dengan abu
sekam padi yang telah diayak. Pencampuran disertai dengan pengadukan
menggunakan magnetic stirrer selama 1 jam pada skala 6-8. Hal tersebut
dimaksudkan untuk mempercepat reaksi antara larutan NaOH dengan silika yang
terkandung dalam abu sekam padi sehingga diperkirakan silika dapat terlarut
secara sempurna membentuk larutan natrium silikat. Sedangkan larutan natrium
aluminat dibuat dengan melarutkan NaOH ke dalam akuades, ditambahkan Al2O3
dan dilarutkan dengan pemanasan disertai pengadukan pada skala 6-8 selama 1
jam. Pemanasan dan pengadukan dilakukan agar kristal Al2O3 dapat melarut
sempurna dalam larutan NaOHmembentuk larutan natrium aluminat.
Proses sintesis zeolit dilakukan dengan mencampurkan larutan natrium
silikat dan larutan natrium aluminat disertai dengan pengadukan pada skala 2
selama 1 jam dan dilakukan pada keadaan basa. Keadaan basa tersebut dapat
menyebabkan silikat dan aluminat berinteraksi sehingga terjadi polimerisasi
dengan variasi waktu aging 24, 48, dan 72 jam pada suhu kamar (T= 25±2oC)
membentuk serbuk berwarna putih.
Pada proses pencampuran natrium silikat dan natrium aluminat terbentuk
dua fasa, yaitu fasa padat sebagai gel amorf dan fasa larutan sebagai larutan lewat
jenuh. Pembentukan zeolit terjadi pada saat kedua fasa tersebut berada pada
keadaan setimbang (Sriyatun, 2004). Serbuk yang dihasilkan selanjutnya dicuci
menggunakan akuades hingga filtrat mencapai pH 8. Proses pencucian ini
bertujuan untuk mengurangi kandungan NaOH serta mineral-mineral sisa dari
sintesis yang bukan menjadi bagian dari struktur zeolit. Kemudian serbuk
dikeringkan dan selanjutnya dikarakterisasi menggunakan difraksi sinar-X (XRD)
dan spektroskopi inframerah (FTIR).
3. Karakterisasi Serbuk Hasil Sintesis
Serbuk yang diperoleh dari hasil sintesis selanjutnya dikarakterisasi secara
kualitatif. Karakterisasi dilakukan dengan menggunakan difraksi sinar-X (XRD)
dan spektrofotometer inframerah (FTIR). Hasil analisis dari masing-masing
karakterisasi dijabarkan sebagai berikut.
a. Analisis Difraktogram Hasil Sintesis
Difraksi sinar-X (XRD) merupakan metode analisis kualitatif yang
digunakan untuk mengidentifikasi struktur kristal (kristalinitas) hasil sintesis.
Struktur zeolit merupakan salah satu karakteristik penting dari zeolit (A.M. Fuadi
dkk, 2012). Hasil yang diperoleh dari karakterisasi menggunakan difraksi sinar-X
disebut difraktogram. Pola difraktogram yang dihasilkan berupa deretan
puncak-puncak difraksi dengan intensitas yang bervariasi sepanjang nilai 2θ tertentu. Tiap
tertentu dalam sumbu tiga dimensi. Puncak-puncak yang diperoleh dari data
pengukuran ini kemudian dicocokkan dengan standar difraksi sinar-X, yaitu
JCPDS (Joint Committee on Powder Diffraction Standards).
Gambar 5a menunjukkan bahwa sintesis zeolit pada temperatur kamar
dengan lama waktu aging 24 jam belum menghasilkan zeolit. Hal tersebut
nampak pada pola difraktogram dimana serbuk tersebut memiliki struktur amorf
dan kristalinitas rendah. Tidak terbentuknya zeolit terjadi karena waktu aging
yang terlalu singkat menyebabkan proses pembentukan inti kristal dan penataan
strukturnya menjadi belum sempurna.
Gambar 5b menunjukkan puncak-puncak yang jelas dengan intensitas
ketajaman puncaknya tinggi dan tajam pada beberapa nilai sudut 2θ.
Puncak-puncak dari difraktogram hasil sintesis memiliki kemiripan dengan difraktogram
standar difraksi sinar-X (JCPDS), yaitu PDF card No. 01-073-9586 Quality: B
seperti yang ditunjukkan pada Tabel 7.
Tabel 7. Hasil Perbandingan Data Difraktogram Hasil Sintesis dan Zeolit Standar No. Hasil Sintesis Zeolit Standar
2θ (deg) d 2θ (deg) d
1. 6,133 14,400 6,11 14,452
2. 10,011 8,829 9,99 8,850
3. 11,741 7,531 11,72 7,547
4. 15,435 5,736 15,42 5,743
5. 23,279 3,818 23,28 3,817
6. 26,638 3,343 26,63 3,345
7. 30,917 2,890 30,91 2,890
Berdasarkan hasil di atas menunjukkan bahwa puncak-puncak pada
difraktogram hasil sintesis tersebut merupakan puncak spesifik untuk senyawa
pada temperatur kamar dengan waktu aging 48 jam telah berhasil membentuk
senyawa zeolit X (Na). Hal tersebut terjadi karena dua fasa, yaitu fasa padat
sebagai gel amorf dan fasa larutan sebagai larutan lewat jenuh yang terbentuk
pada proses pencampuran natrium silikat dan natrium aluminat telah berada pada
keadaan setimbang.
Gambar 5c menunjukkan bahwa sintesis zeolit pada temperatur kamar
dengan lama waktu aging 72 jam memiliki struktur amorf dan kristalinitas rendah.
Dalam penelitian ini, sintesis dilakukan secara paralel dengan sampel yang
berbeda untuk masing-masing variasi waktu aging. Data yang diperoleh dari
sintesis ini hanya terdapat satu data, sehingga data tersebut tidak dapat digunakan
untuk mengambil kesimpulan pada waktu aging 72 jam.
Dari hasil analisis difraktogram di atas dapat dilihat bahwa waktu optimal
yang diperlukan dalam sintesis zeolit pada temperatur kamar terjadi pada sintesis
dengan lama waktu aging 48 jam. Hal ini terjadi karena pada hasil sintesis
tersebut telah membentuk zeolit dengan tipe zeolit X (Na) dan memiliki
kristalinitas yang paling tinggi dibandingkan dengan hasil sintesis yang lain.
b. Analisis Spektrum Inframerah Hasil Sintesis
Karakterisasi susunan gugus fungsional dilakukan dengan menggunakan
spektroskopi inframerah (FTIR). Pola serapan inframerah yang digunakan dalam
penelitian ini dilakukan pada daerah bilangan gelombang 300-4000 cm-1.
Spektrum inframerah serbuk yang dihasilkan pada penelitian ini ditunjukkan pada
Gambar 6 untuk variasi waktu aging 24 jam, Gambar 7 untuk variasi waktu aging
Spektrum masing-masing variasi waktu aging diinterpretasikan dengan
membandingkan antara spektrum hasil sintesis dan hasil interpretasi kerangka
struktur zeolit X pada penelitian yang dilakukan oleh Sholeh Nura Aditama
(2015). Interpretasi masing-masing spektrum inframerah hasil sintesis dapat
[image:42.595.118.518.230.430.2]dilihat pada Tabel 8.
Tabel 8. Interpretasi Spektrum Inframerah Hasil Sintesis No.
Bilangan Gelombang (cm-1)
Interpretasi Variasi
24 jam
Variasi 48 jam
Variasi
72 jam Zeolit X*
1. 3448,72 3448,72 3448,72 3448 Gugus –OH
2. 1635,64 1635,64 1635,64 1637 Tekukan H-O-H
3. 1103,28 972,12 1033,85 1017 Regangan asimetri T-O internal (T = Si atau Al)
4. 786,96 740,67 - 773 Regangan simetri T-O internal (T = Si atau Al)
5. 570,93 563,21 578,64 570 Cincin ganda
6. 470,63 462,92 493,78 463 Tekukan O-T-O (T= Si atau Al) *(Sumber: Sholeh Nura Aditama, 2015)
Berdasarkan hasil analisis spektroskopi inframerah tersebut dapat dilihat
bahwa hasil sintesis pada temperatur kamar dengan variasi waktu aging 48 jam
memiliki kemiripan susunan gugus fungsi yang dimiliki oleh zeolit X. Sehingga
dapat disimpulkan bahwa hasil sintesis dengan variasi waktu aging 48 jam
mengandung gugus fungsi penyusun zeolit X. Perbedaan intensitas serapan
puncak-puncak menunjukkan adanya perbedaan dari pembentukan zeolit.
Semakin tajam intensitas serapan menunjukkan semakin tinggi struktur atau
gugus fungsi yang terbentuk (Purbaningtias dan Prasetyoko dalam Sholeh Nura
48 jam memiliki puncak-puncak yang lemah karena pada hasil sintesis tersebut
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Bedasarkan penelitian yang telah dilakukan dan uraian pembahasan dapat
diambil kesimpulan sebagai berikut :
1. Senyawa zeolit X (Na) berhasil disintesis dari abu sekam padi pada temperatur kamar dengan waktu aging optimal 48 jam sesuai dengan JCPDS No.
01-073-9586 Quality: B.
2. Sintesis dengan waktu aging 24 menghasilkan senyawa amorf, waktu aging
48 jam kristalin, dan waktu aging 72 jam belum dapat digunakan untuk
mengambil kesimpulan.
B. Saran
Berdasarkan hasil penelitian yang telah dilakukan, maka saran yang dapat
diberikan sebagai pengembangan penelitian yang akan datang adalah:
1. Perlu dilakukan modifikasi lanjut mengenai sintesis zeolit dari subjek dan
objek serta sumber yang lain.
2. Perlu dilakukan analisis uji karakter yang lain agar diperoleh informasi yang
lebih lengkap.
3. Perlu dibuat rancangan percobaan dengan ulangan yang cukup untuk dapat
DAFTAR PUSTAKA
AAK. (1990). Budidaya Tanaman Padi. Yogyakarta: Kanisius.
A.M. Fuadi, Malik Musthofa, Kun Harismah, Haryanto, dan Nur Hidayati. (2012). Pembuatan Zeolit Sintetis dari Abu Sekam Padi. Simposium Nasional RAPI XI FT UMS-2K012. ISSN : 1412-9612. 55-62.
Amaria. (2012). Adsorpsi Ion Sianida dalam Larutan Menggunakan Adsorben Hibrida Aminopropil Silika Gel dari Sekam Padi Terimpregnasi Aluminium (Adsorption of Cyanide Ions in Solution Using a Hybrid Adsorbent Aminopropyl Silica Gel from Rice Husks of Impregnated With Aluminum). Jurnal Manusia dan Lingkungan. 19, 1. 56-65.
Andhi Laksono Putro dan Didik Prasetyoko. (2007). Abu Sekam Padi Sebagai Sumber Silika pada Sintesis Zeolit ZSM-5 Tanpa Menggunakan Templat Organik ‡. Jurnal Akta Kimindo. 3, 1. 33-36.
Badan Pusat Statistik. (2015). Produksi Padi Tahun 2015 Diperkirakan Naik 6,64%. Diakses dari http://www.bps.go.id/brs/view/id/1157 pada tanggal 27
Januari 2016, Jam 19.22 WIB.
Barrer, R.M. (1982). Hydrothermal Chemistry of Zeolites. London: Academic
Press.
Chang, Raymond. (1998). Chemistry sixth edition. Boston: McGraw-Hill.
Chorkendroff, I dan Niemantsverdiet, J. W. (2003). Concepts of Modern Catalysis and Kinetics. New York: Wliey-VCH GmbH&Co. 145-147.
Dania Kurniawati. (2010). Sintesis Zeolit dari Abu Layang Batubara secara Hidrotermal Melalui Proses Peleburan dan Aplikasinya untuk Penurunan Logam Cr dalamLimbah Industri Penyamakan Kulit. Skripsi. Semarang:
Universitas Negeri Semarang.
Dardjo Sumaatmadja. (1985). Sekam Gabah Sebagai Bahan Industri. Makasar:
Balai Penelitian dan Pengembangan Industri Banjar Baru.
Didi Dwi Anggoro, Muhamad Amri Fauzan, dan Nanda Dharmaparayana. (2007). Pengaruh Kandungan Silikat dan Aluminat dalam Pembuatan Zeolit Sintesis Y dari Abu Sekam Padi. Seminar Nasional Teknik Kimia “Kejuangan”,
UPN Veteran, Yogyakarta. 1-6.
Edi Soenarjo, Djoko S. Damardjati, dan Mahyuddin Syam. (1991). Padi Buku 3.
Flanigen, Edith M., dan Khatami, Hasan. (1974). Infrared Structural Studies of Zeolite Frameworks. In Molecular Sieve Zeolites-I. American Chemical
Society: Washington.
Gates, Bruce C. (1992). Catalytic Chemistry. Singapore: John Wiley and Sons
Inc.
Georgiev, Dimitar; Bogdanov, Bogdan; Angelova, Krasimira; Markovska, Irena; dan Hristov, Yancho. (2009). Synthetic Zeolites - Structure, Clasification, Current Trends in Zeolite Synthesis. International Science conference.VII.
1-5.
Ghasemi, Zahra dan Younesi, Habibollah. (2011). Preparation and Characterization of Nanozeolite NaA from Rice Husk at Room Temperature without Organic Additives. Journal of Nanomaterials, 2011, Article ID
858961. 1-8.
Hardjono Sastrohamidjojo. (1992). Spektroskopi Inframerah. Yogyakarta:
Liberty.
Houston, D. F. (1972). Rice Chemistry and Technology. American Association of
Cereal Chemist, Inc., St. Paul, Minnesota, USA, IV.
Islam, M. N. dan Ani, F. N. (2000). Techno-Economics of Rice Husk Pyrolysis, Conversion with Catalytic Treatment to Produce Liquid Fuel. Journal Bioresource Technology 75. 67-75.
Joddy Arya Laksmono dan Nova Ardiyanto. (1999). Pengambilan SiO2 dari Abu
Sekam Padi dengan Proses Leaching. Semarang: Laporan Penelitian,
Jurusan Kimia UNDIP.
Jumaeri, Widi Astuti, dan Wahyu Tutik Puji Lestari. (2007). Preparasi dan Karakterisasi Zeolit dari Abu Layang Batubara Secara Alkali Hidrotermal.
Jurnal Reaktor, 11, 1, Juni. 38-44.
Kalapathy, U., Proctor, A., dan Shultz, J. (2000). A Simple Method for Production of Pure Silica from Rice Hull Ash. Journal Bioresource Technology, 73.
257-262.
Kristian Handoyo. (1996). Kimia Anorganik. Yogyakarta: Gadjah Mada
University Press.
Kristian H. Sugiyarto. (2004). Kimia Anorganik I. Yogyakarta: FMIPA UNY.
Linda Trivana, Sri Sugiarti, dan Eti Rohaeti. (2015). Sintesis dan Karakterisasi Natrium Silikat (Na2SiO3) dari Sekam Padi. Jurnal Sains dan Teknologi
M. Arifin dan Uun Bisri. (1995). Bahan Galian Industri Zeolit. Bandung: Pusat
Penelitian dan Pengembangan Teknologi Mineral.
Mursi Sutarti dan Minta Rachmawati. (1994). Zeolit Tinjauan Literatur. Jakarta:
Pusat Dokumentasi dan Informasi Ilmiah LIPI.
Ngatijo, Faizar Faried, dan Intan Lestari. (2011). Pemanfaatan Abu Sekam Padi (ASP) Payo dari Kerinci Sebagai Sumber Silika dan Aplikasinya dalam Ekstraksi Fasa Padat Ion Tembaga (II). Jurnal Penelitian Universitas Jambi Seri Sains. ISSN 0852-8349, 13, 2. 47-52.
Nur, Hadi. (2001). Direct Synthesis of NaA Zeolite from Rice Husk and Carbonaceous Rice Husk Ash. Indonesian Journal of Agricultural Sciences,
1, 40-45.
Sholeh Nura Aditama. (2015). Sintesis dan Karakterisasi Zeolit X dari Abu Vulkanik Gunung Kelud dengan Variasi Suhu Hidrotermal Menggunakan Metode Sol-Gel. Skripsi. Malang: UIN Maulana Malik Ibrahim.
Sinung Kurny Hadi. (1993). Pembuatan dan Karakterisasi Zeolit A dari Sekam Padi. Skripsi. Yogyakarta: FMIPA UGM.
Siti Sulastri dan Susila Kristianingrum. (2010). Berbagai Macam Senyawa Silika: Sintesis, Karakterisasi dan Pemanfaatan. Prosiding seminar Nasional Penelitian, Pendidikan dan Penerapan MIPA. 211-216.
Sriyatun. (2004). Sintesis Zeolit A dan Kemungkinan Penggunaannya Sebagai Penukar Kation. Jurnal Kimia Sains dan Aplikasi. VII. 3. Desember. 66-72.
Suharno. (1994). Sintesis, Karakterisasi dan Substitusi Isomorfis Atom Fosfor ke Dalam Struktur Zeolit A yang Dihasilkan dari Limbah Sekam Padi. Skripsi.
Yogyakarta: FMIPA UGM.
Warren, Bertram Eugene, (1990). XRay Diffraction. New York: Dover
Publications.
Weller, Mark T. (2006). Inorganic Materials Chemistry. New York: Oxford
University Press.
Widi Astuti dan Indah Nurul Izzati. (2015). Granulasi Abu Layang Batubara Menggunakan Karagenan dan Aplikasinya Sebagai Adsorben Pb(II). Jurnal Bahan Alam Terbarukan. 4 (2). 55-60.
Lampiran 1.
Diagram Kerja
Limbah sekam padi hasil penggilingan
Sekam padi bersih dan kering
Dibakar dan diabukan pada temperatur 600°C selama 8 jam
Abu sekam padi putih
Abu sekam padi halus dan putih
- Dibersihkan - Dicuci dan
dijemur
Digerus dan diayak (200 mesh)
Pembuatan Larutan Natrium Silikat
Pembuatan Larutan Natrium Aluminat
1,26 g abu sekam padi + 3, 895 g NaOH + 24,93 g akuades
2,04 g Al2O3
+ 3,895 g NaOH + 24,93 g akuades
disertai pengadukan dengan
magnetic stirrer (skala 6-8)
selama 1 jam
Dipanaskan pada suhu 50°C selama 1 jam disertai pengadukan dengan magnetic stirrer (skala 6-8)
Pengadukan dengan skala 2 selama 1 jam
Sintesis pada suhu kamar (T=25±2°C) disertai pengadukan, dilanjutkan periode aging 24, 48, dan 72 jam
dicuci hingga pH8, dikeringkan dengan
Oven (T=110°C)
Hasil Sintesis
Lampiran 2.
Difraktogram Abu Sekam Padi
No. 2-theta
(deg) d (ang.) Height (cps) FWHM (deg) Int. I (cps deg) Int. W (deg) Asym. factor
1 21.16(6) 4.194(12
) 1587(115) 8.69(13) 26511(386) 16.7(15) 0.75(3)
Meas. data:545-XRD-2016/Data 1 BG data:545-XRD-2016/Data 1 Calc. data:545-XRD-2016/Data 1
2-theta (deg)
Intensity (cps)
20 40 60 80
Lampiran 3.
Difraktogram Serbuk Hasil Sintesis dengan Waktu Aging 24 Jam
No. 2-theta(deg) d(ang.) Height (cps)
FWHM(deg) Int. I (cps deg)
Int. W(deg) Asym. factor
1 45.84(15) 1.978(6) 224(43) 2.06(17) 622(39) 2.8(7) 0.7(2)
2 67.23(7) 1.3913(13
) 426(60) 3.71(12) 2912(50) 6.8(11) 2.8(3)
Meas. data:Zeolit 24 Jam/Data 1
2-theta (deg)
Intensity (cps)
20 40 60
Lampiran 4.
Difraktogram Serbuk Hasil Sintesis dengan Waktu Aging 48 Jam
No. 2-theta
(deg) D (ang.) Height (cps) FWHM(deg) Int. I (cps deg) Int. W(deg) Asym. factor
1 6.133(7) 14.400(17) 11359(308
)
0.261(11) 5054(69) 0.445(18) 2.0(3) 2 10.011(13) 8.829(11) 1806(123) 0.303(11) 605(26) 0.34(4) 2.2(4)
3 11.741(13) 7.