PEMANFAATAN LIMBAH AMPAS SUSU KEDELAI SEBAGAI BAHAN PELINDUNG
PROBIOTIK L. acidophillus FNCC 0051 SELAMA DI SALURAN CERNA IN VITRO
I.B. AGUNG YOGESWARA1, N, W, NURSINI1., I.G.A. WITA KUSUMAWATI1
1
.FAKULTAS ILMU KESEHATAN, SAINS DAN TEKNOLOGI UNIVERSITAS DHYANA PURA, TEGAL JAYA, DALUNG, BALI
EMAIL : ibayogeswara@yahoo.com, nursini_2811@yahoo.com, wita_kusumawati@yahoo.co.id
Proses pembuatan susu kedelai menghasilkan limbah padat berupa ampas kedelai. Ampas kedelai (okara) masih memiliki sifat fungsional seperti aktivitas antioksidan yang tinggi, kaya akan protein dan serat serta bersifat sebagai prebiotik. Dalam pengembangan pangan probiotik, pemilihan bahan pelindung untuk mempertahankan viabilitas sel probiotik selama di saluran cerna sangat penting. Tujuan dari penelitian ini adalah untuk memanfaatkan limbah ampas susu kedelai untuk mempertahankan viabilitas probiotik L.
acidophillus FNCC 0051 selama di saluran cerna in vitro dan diamati viabilitasnya selama penyimpanan
35 hari pada suhu 50 C. Penelitian ini menggunakan rancangan acak kelompok (RAK) dengan tiga kali pengulangan dengan variasi konsentrasi 1%, 3%, 5% dan kontrol. Hasil dari penelitian ini adalah, L.
acidophillus FNCC 0051 memiliki viabilitas 9 log cfu/ml selama 35 hari penyimpanan. Konsentrasi okara
1% dan 3% memiliki ketahanan yang lebih baik dibanding 5% dengan viabilitas 0,48 log cfu/ml – 1,49 log cfu/ml selama 35 hari penyimpanan. Hal ini menunjukkan bahwa okara dapat dimanfaatkan sebagai bahan pelindung dan mampu mempertahankan viabilitas probiotik L. acidophillus FNCC 0051 selama di saluran cerna.
Kata kunci : limbah ampas susu kedelai, probiotik, saluran cerna in vitro
1. Pendahuluan
Susu kedelai merupakan salah satu pangan fungsional yang sangat digemari oleh masyarakat Indonesia. Susu kedelai dan produk berbasis kedelai lainnya merupakan sumber protein nabati yang baik, serat pangan, kandungan oligosakarida yang tinggi, memiliki kandungan vitamin dan mineral serta mampu menurunkan resiko penyakit jantung koroner, diabetes tipe 2, menurunkan resiko karsinogenesis, mengurangi gejala – gejala negatif akibat menopause dan meningkatkan kesehatan tulang ( Bedani et al.,2006; Chen et
al., 2010). Penggunaan proses fermentasi pada
susu kedelai oleh bakteri asam laktat akan meningkatkan rasa, tekstur dan efek kesehatan dari susu kedelai tersebut. Proses fermentasi susu kedelai juga mengurangi bau tengik dari
sari kedelai dan mengurangi flatulensi serta gangguan perut yang diakibatkan oleh oligosakarida (stakiosa dan raffinosa) yang terdapat pada susu kedelai (Saad et al., 2013).
Proses pembuatan susu kedelai menghasilkan limbah padat berupa ampas kedelai yang jarang dikonsumsi oleh manusia sehingga memiliki nilai ekonomis yang rendah. Ampas kedelai atau disebut okara masih memiliki nilai gizi yang tinggi seperti kandungan protein, lemak, serat pangan, mineral, monosakarida dan oligosakarida. Okara mentah memiliki kandungan isoflavone sebesar 22% , sumber antioksidan yang potensial, bersifat prebiotik, menurunkan kadar kolesterol dan gula darah (Marazza et al.,2013; Fei lu et
Menurut WHO (2001) probiotik adalah sel hidup yang dikonsumsi dalam jumlah tepat dapat memberikan efek kesehatan bagi inang. Bakteri probiotik mempunyai mekanisme untuk memperbaiki mikroflora saluran pencernaan sehingga dapat mengatasi masalah gangguan pencernaan. Untuk dapat berfungsi sebagai probiotik, bakteri probiotik harus memenuhi persyaratan antara lain; berasal dari manusia, tidak bersifat patogen, toleran terhadap asam lambung dan garam empedu dan kemampuan untuk menempel dan mengkoloni usus minimal dalam jangka waktu pendek juga merupakan salah satu syarat dari galur probiotik untuk dapat memberikan manfaat sepenuhnya (Shortt, 1999). Pemilihan carier pada pengembangan produk probiotik sangat penting karena media carier tersebut akan mempengaruhi viabilitas bakteri probiotik selama di saluran pencernaan dan proses penyimpanan. Beberapa upaya dapat dilakukan untuk mempertahankan viabilitas probiotik selama di saluran cerna seperti penambahan prebiotik, penambahan strain yeast yang dapat bersinergi dengan probiotik atau dengan penambahan matriks pangan (Su et al., 2007).
Agar dapat dikonsumsi dalam waktu yang cukup lama maka probiotik harus memiliki viabilitas dan stabilitas yang tinggi selama penyimpanan dan di saluran cerna. Proses penyimpanan atau lama penyimpanan akan mempengaruhi viabilitas probiotik selama di saluran cerna. Pada penelitian sebelumnya (Yogeswara et al., 2013), bakteri probiotik L.
acidophillus FNCC 0051 di dalam susu kedelai
fermentasi menunjukkan penurunan sebesar 3 log cycle terhadap simulated gastric juice (pH 2,0 dan pepsin) selama 10 hari penyimpanan dengan suhu penyimpanan 50 C, sedangkan pada fase simulated intestinal juice (pH 8,0 dan garam empedu 1%) probiotik L. acidophillus
mengalami penurunan 2 log cycle pada hari ke 10 penyimpanan. Sedangkan pada suhu penyimpanan 250 C kultur L. acidophillus FNCC 0051 tidak dapat bertahan pada simulated gastric
juice dan simulated intestinal juice pada lama
penyimpanan 10 hari. Penggunaan okara dan inulin yang dilakukan oleh Bedani et al., (2013) melaporkan bahwa penambahan okara (5 g/100 ml) dan inulin (3 g/100 ml) di dalam susu kedelai fermentasi dapat mempertahankan viabilitas dan stabilitas bakteri L. acidophillus dan Bifidobacterium animalis pada simulated
gastrointestinal juice dan selama 28 hari
penyimpanan. Informasi mengenai pemanfaatan okara serta konsentrasi okara yang digunakan pada susu kedelai fermentasi masih terbatas di Indonesia, oleh karena itu masih perlu dilakukan penelitian untuk mengetahui potensi okara untuk mempertahankan viabilitas dan stabilitas bakteri probiotik selama penyimpanan dan di saluran pencernaan. Penelitian ini bertujuan untuk mengetahui pengaruh penambahan okara dengan berbagai konsentrasi pada susu kedelai fermentasi terhadap viabilitas bakteri L. acidophillus FNCC 0051 terhadap simulated gastrointestinal juice selama penyimpanan 35
2. Bahan dan metode 2.1 Bahan
Bahan yang digunakan adalah kacang kedelai diperoleh dari pasar Badung, kultur L.
acidophillus FNCC 0051 yang diperoleh dari
PSPG UGM, NaCl 0,85% (Merck), de Man Ragosa Sharp broth (Oxoid), MRS Agar (Oxoid), pepsin (porcine gastric mucosa, sigma), garam empedu (oxoid), larutan saline 5%, susu skim, HCl 5 M, NaOH 1 M.
2.2 Preparasi kultur bakteri L. acidophillus FNCC 0051
Kultur bakteri diambil dengan jarum ose (1 kali) lalu dimasukkan ke dalam tabung reaksi (pyrex) yang telah berisi 10 ml MRS dan diinkubasi pada suhu 370 C selama 16-18 jam. Kultur bakteri dimasukkan ke dalam tabung mikro eppendorf, kemudian disentrifuse selama 20 menit dengan kecepatan 3500 rpm lalu dicuci dengan larutan fisiologis (NaCl 0,85%) setelah itu disentrifuse lagi, diresuspensi dengan larutan fisiologis dengan volume yang sama sebanyak 100 ml, kemudian divortex (Thermolyne) dan siap digunakan. Kultur yang siap digunakan kemudian diinokulasikan ke dalam sari kedelei terfermentasi. Sari kedelei kemudian difermentasi selama 10 jam pada suhu 430 C.
2.3 Pembuatan susu kedelai dan fermentasi susu kedelai
Kedelai direndam selama 4 jam sampai kulit ari kedelai terlepas dari bijinya.
Selanjutnya kedelai ditiriskan dan dimasukkan ke dalam air mendidih dan direbus selama 10 menit, kemudian ditiriskan kembali. Kedelai dihancurkan dalam blender sambil ditambah air hangat (70 – 800 C) dengan perbandingan 1 : 6. Penggilingan dilakukan selama 5 menit dengan kecepatan tinggi. Bubur tersebut diaduk dan disaring untuk diambil filtratnya. filtrat yang diperoleh kemudian digunakan untuk pembuatan tepung okara.
Proses pembuatan susu kedelai fermentasi mengikuti metode yang dilakukan oleh Jenie et al., (1996) dengan sedikit modifikasi. Kedalam susu kedelai ditambahkan tepung okara sebanyak 3 %, 5% dan 10% serta sukrosa 3%. Campuran diaduk merata, dipanaskan pada suhu 800 C selama 5 menit, kemudian ditambahkan gelatin sebanyak 0,3% w/v dan didinginkan hingga suhu mencapai 370 C. susu kedelai selanjutnya diinokulasi dengan kultur L. acidophillus FNCC 0051 sebanyak 10% kemudian diinkubasi pada suhu 370 C selama 24 jam. Susu kedelai yang sudah selesai difermentasi kemudian dilanjutkan dengan penyimpanan pada suhu 50 C. Penyimpanan dilakukan selama 35 hari dan analisa mikrobiologi dilakukan pada hari ke 0, 7, 14, 21, 28 dan 35 hari. Analisa yang dilakukan adalah total bakteri asam laktat selama penyimpanan, ketahanan terhadap simulated gastrointenal juice yang meliputi ketahanan terhadap simulated
gastric juice pH 2,0 selama 90 menit inkubasi,
8,0 selama 60 menit inkubasi dan pH susu kedelai fermentasi selama penyimpanan.
2.4 Pembuatan tepung okara
Pembuatan tepung okara mengikuti metode yang dilakukan oleh Bedani et al., (2013). Filtrat atau ampas yang diperoleh dari pembuatan susu kedelai dikeringkan dengan menggunakan oven pada suhu 550 C selama 48 jam. Setelah kering, tepung okara kemudian dihaluskan menggunakan blender (Phillips) dan dilanjutkan dengan pengayakan (ukuran 60 mesh) sampai memperoleh butiran tepung okara yang halus. Tepung okara yang diperoleh kemudian ditambahkan pada susu kedelai fermentasi dengan berbagai konsentrasi (1%, 3%, 5%).
2.5 Ketahanan terhadap Simulated Gastric Juice dan Simulated Intestinal Juice (Lian et al., 2003; Krasaekoopt et al., 2004)
Uji ketahanan terhadap simulated gastric juice dilakukan dengan metode plate
count. Ketahanan dilakukan dalam larutan saline 5% yang ditambahkan pepsin (3 g/l), 1, 25 M KCl, 0, 45 M NaHCO3, kemudian pH diatur
menggunakan HCl 5 M sehingga pH media diperoleh 2,0. Kultur segar diinokulasi ke dalam
simulated gastric juice (SGJ), selanjutnya
diinkubasi pada suhu 370 C selama 90 menit. Setelah pengujian di SGJ kultur selanjutnya diuji secara berkesinambungan terhadap simulated intestinal juice. Uji ketahanan terhadap SIJ menggunakan
konsentrasi garam empedu yang terbuat dari larutan KH2PO4 0,05 M dengan pH 8,2 ditambah
garam empedu sebesar 0,5% dan pankreatin (1 mg/ml). Kultur bakteri asam laktat yang telah diinokulasikan ke dalam 10 ml SGJ steril kemudian diambil 1 ml dan diinokulasikan kembali ke 10 ml larutan SIJ steril yang memiliki konsentrasi 0,5%. Selanjutnya diinkubasi pada suhu 370 C selama 1 jam. Jumlah bakteri yang tumbuh dihitung menggunakan Quebec Colony Counter (Quebec)
2.5 Penentuan total bakteri asam laktat dan pH susu kedelai fermentasi
Penentuan total bakteri asam laktat selama penyimpanan dilakukan menggunakan metode sebar pada media MRS agar. Dari setiap tiga seri tingkat pengenceran terakhir diambil 0,1 ml dan dimasukkan ke dalam cawan petri steril (dilakukan duplo). Setelah media memadat, cawan dibalik dan diinkubasi pada suhu 370 C selama 24 – 48 jam. Jumlah bakteri dihitung dengan menggunakan Quebec Colony
Counter. pH susu kedelai fermentasi dilakukan
menggunakan pH meter yang telah dikalibrasi dengan buffer pH 4,0 dan pH 7,0. Nilai pH diukur sebanyak 3 kali ulangan.
2.6 Rancangan percobaan
Rancangan percobaan yang digunakan dalam penelitian ini adalah rancangan acak kelompok (RAK) dengan tiga kali ulangan. Data yang diperoleh dianalisa menggunakan analisis varian
3.1 Total bakteri asam laktat dan pH susu kedelai fermentasi
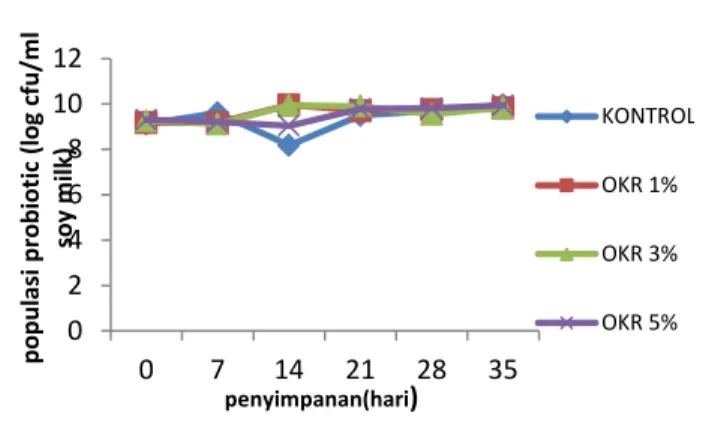
Jumlah bakteri asam laktat pada susu kedelai fermentasi tidak mengalami penurunan selama penyimpanan sampai hari ke -21 dengan suhu penyimpanan 50 C. Pada awal penyimpanan jumlah bakteri asam laktat adalah 9,11-9,30 log cfu/ml dan pada akhir penyimpanan 9,50-9,77 log cfu/ml untuk semua perlakuan. Jumlah tersebut sudah memenuhi syarat sebagai probiotik, dimana jumlah minimal yang bakteri asam laktat pada susu terfermentasi adalah 106 -108 cfu/ml (Tamime and Robinson, 2002). Gambar total bakteri asam laktat dapat dilihat pada Gambar 1.
Gambar 1. Total probiotik L. acidophillus FNCC 0051 selama 35 hari penyimpanan
Dari gambar diatas dapat dilihat bahwa jumlah bakteri asam laktat pada susu kedelai fermentasi tanpa okara dan dengan penambahan okara tidak menunjukkan penurunan selama penyimpanan pada suhu 50 C sampai hari ke -21. Hal ini disebabkan bakteri asam laktat sudah mencapai fase statis selama penyimpanan. Penambahan
okara juga memberikan viabilitas terhadap bakteri asam laktat selama penyimpanan. Bedani
et al., (2013) melaporkan bahwa keberadaan
komponen prebiotik inulin dan okara pada susu kedelai fermentasi dapat mempertahankan viabilitas probiotik B. animalis dan L.
acidophillus selama penyimpanan.Viabilitas
probiotik selama penyimpanan juga dapat ditingkatkan dengan penambahan prebiotik FOS sebanyak 1,5% pada yogurt dan dapat memperbaiki viabilitas probiotik sebesar 1,42 log cfu/ml selama empat minggu penyimpanan pada suhu 40 C (Capela et al., 2006).
Beberapa studi melaporkan bahwa penggunaan kedelai dan produk kedelai dapat mempertahankan viabilitas probiotik. Donkor et
al ., (2007) melaporkan bahwa viabilitas
probiotik L. acidophillus L10, B. animalis subsp
lactis B94 dan L. casei L26 diatas 8 log
cfu/ml.Lebih lanjut dilaporkan bahwa suplementasi 2% inulin dan 1% raffinosa + 1% glukosa mampu meningkatkan viabilitasnya selama penyimpanan dan fermentasi susu kedelai. Hal ini membuktikan bahwa tepung okara dapat berfungsi sebagai prebiotik dan sinbiotik pada susu kedelai fermentasi berdasarkan populasi bakteri asam laktat yang tinggi selama 35 hari penyimpanan.
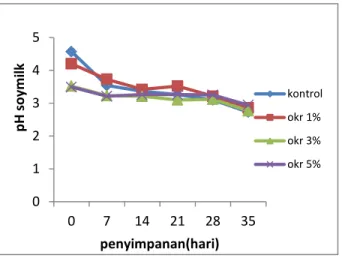
pH susu kedelai fermentasi selama penyimpanan dapat dilihat pada Gambar 2. pH susu kedelai fermentasi mengalami penurunan selama 35 hari pada penyimpanan 50 C. pH susu kedelai fermentasi mencapai 2,73 – 2,94 di akhir periode penyimpanan . 0 2 4 6 8 10 12 0 7 14 21 28 35 p o p u lasi p ro b io ti c (l o g c fu /ml so y mi lk) penyimpanan(hari) KONTROL OKR 1% OKR 3% OKR 5%
Gambar 2. pH susu kedelai fermentasi selama penyimpanan
Penurunan pH susu kedelai fermentasi dikarenakan bakteri asam laktat menghasilkan asam – asam organik yang dihasilkan dari degradasi karbohidrat selama proses fermentasi. Bakteri asam laktat mampu menghidrolisa gula raffinosa dan stakiosa yang terdapat pada susu kedelai (Wang et al., 2009). Menurut Wang et
al., (2009) pH susu kedelai fermentasi
mengalami penurunan karena susu kedelai memiliki kemampuan buffer yang rendah yang disebabkan oleh sifat fisikokimia dan komposisi dari protein kedelai. Penurunan pH susu kedelai fermentasi diduga karena pengaruh penambahan tepung okara. Okara merupakan media pertumbuhan yang baik bagi beberapa strain bakteri asam laktat karena mengandung gula stakiosa dan raffinosa. Beberapa strain dari L.
acidophillus dilaporkan memiliki kemampuan
untuk memetabolisme oligosakarida selama fermentasi susu kedelai (Donkor et al., 2007). Hasil serupa dilaporkan oleh Bedani et al.,( 2013), suplementasi inulin dan okara pada susu
kedelai fermentasi memberikan penurunan pH selama penyimpanan dingin mencapai 4,46 selama 28 hari penyimpanan.
3.2 Ketahanan terhadap saluran cerna in vitro
Salah satu syarat bakteri asam laktat sebagai probiotik adalah mampu bertahan pada pH rendah di lambung. Dalam hal ini adalah pengujian bakteri asam laktat selama di saluran cerna dilakukan 2 fase yaitu terhadap simulated
gastric juice pH 2.0 secara in vitro dan Simulated intestinal juice. Pengujian pada SGJ
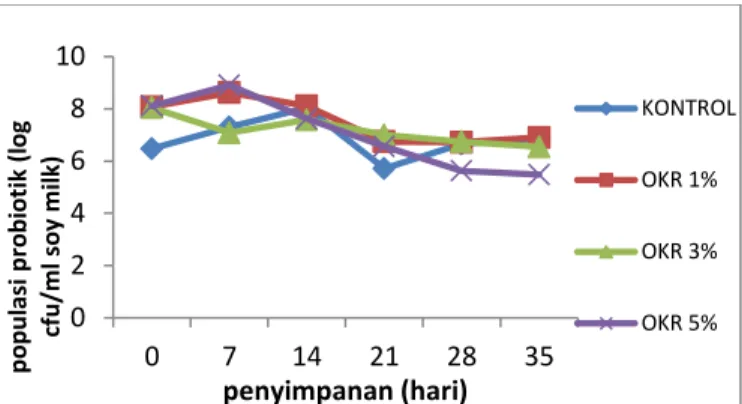
dilakukan selama 90 menit, pemilihan waktu tersebut berdasarkan lama transit minuman di lambung. Ketahanan bakteri asam laktat terhadap SGJ selama penyimpanan dapat dilihat pada Gambar 3.
Gambar 3. Ketahanan probiotik L. acidophillus FNCC 0051 terhadap SGJ selama penyimpanan.
Data diperoleh setelah 90 menit inkubasi pada suhu 370 C selama 24 jam
Pada gambar diatas dapat dilihat bahwa viabilitas sel bakteri asam laktat terhadap SGJ selama penyimpanan mengalami penurunan 2
0 1 2 3 4 5 0 7 14 21 28 35 p H soymi lk penyimpanan(hari) kontrol okr 1% okr 3% okr 5% 0 2 4 6 8 10 0 7 14 21 28 35 p o p u lasi p ro b io tik (l o g cfu/ m l so y m ilk) penyimpanan(hari) KONTROL OKR 1% OKR 3% OKR 5%
log cfu/ml pada sampel kontrol dan pada susu kedelai fermentasi okara mengalami penurunan 0,33 – 0,96 log cfu/ml sampai hari ke -21 penyimpanan. Secara keseluruhan ketahanan bakteri asam laktat terhadap SGJ relatif baik selama penyimpanan pada sampel kontrol maupun pada susu kedelai fermentasi okara. Hal ini menunjukkan bahwa penambahan okara dapat melindungi sel bakteri asam laktat terhadap paparan pH rendah di lambung. Keberadaan komponen prebiotik pada makanan dapat mempertahankan atau meningkatkan viabilitas probiotik selama di saluran cerna sehingga akan memberikan efek kesehatan (Moustafa., et al 2010). Hal tersebut didukung oleh Moustafa et al.,(2010) yang melaporkan bahwa penambahan prebiotik inulin pada sirup maple dapat mempertahankan viabilitas probiotik B. lactis Bb12 dan L. rhamnosus GG sebesar 107 – 108 cfu/ml selama di simulasi cairan cerna dan penyimpanan pada suhu 40 C.
Ketahanan terhadap garam empedu merupakan salah satu syarat penting untuk bakteri asam laktat yang akan digunakan sebagai probiotik. Asam empedu merupakan racun bagi sel hidup, oleh karena itu mikroba pada saluran pencernaan harus mempunyai suatu mekanisme pertahanan untuk melindungi diri dari aktivitas racun tersebut. Pengujian pada SIJ dilakukan selama 60 menit inkubasi dengan konsentrasi garam empedu 0,5%. Ketahanan bakteri asam laktat terhadap garam empedu dapat dilihat pada Gambar 4.
Gambar 4. Ketahanan probiotik L. acidophillus FNCC 0051 terhadap SGJ selama penyimpanan.
Data diperoleh setelah 60 menit inkubasi pada suhu 370 C selama 24 jam
Pada gambar diatas, penambahan tepung okara pada susu kedelai fermentasi dapat mempertahankan viabilitas probiotik L. acidophillus FNCC 0051 pada hari ke 0, 7 dan
14. Akan tetapi pada hari ke 21 sampai hari ke 35 populasi L. acidophillus FNCC 0051 menunjukkan penurunan 1,60 – 2,60 log cfu/ml. penurunan populasi ini masih dalam batas minimal yang dianjurkan untuk probiotik mencapai kolon (jumlah minimal probiotik adalah 106 cfu/ml). Menurut Antara (2009) enzim BSH merupakan enzim yang dihasilkan oleh bakteri asam laktat yang mampu menghidrolisa garam empedu dan mengubah kemampuan fisikokimia yang dimiliki garam empedu, sehingga tidak toksik bagi bakteri tersebut.
4. Kesimpulan
Kesimpulan dari penelitian ini adalah, penambahan tepung okara pada susu kedelai fermentasi mampu mempertahankan viabilitas probiotik L. acidophillus FNCC0051 selama
0 2 4 6 8 10 0 7 14 21 28 35 p o p u lasi p ro b io ti k (l o g cf u /ml so y mi lk) penyimpanan (hari) KONTROL OKR 1% OKR 3% OKR 5%
penyimpanan dingin. Viabilitas L. acidophillus FNCC 0051 diatas 8 log cfu/ml dan populasi tersebut tidak dipengaruhi dengan penurunan pH dari susu kedelai fermentasi yang mencapai 3,70 – 2,94. Pada fase pengujian di simulated gastric
juice pH 2,0 jumlah rata - rata populasi probiotik L. acidophillus FNCC 0051 adalah 7 log cfu/ml
dan fase simulated intestinal juice diatas 6 log cfu/ml. Penelitian ini menunjukkan bahwa ampas susu kedelai (okara) memiliki potensi yang baik sebagai bahan pelindung pangan probiotik sehingga akan meningkatkan nilai ekonomis dari okara tersebut. Perlu dilakukan penelitian lebih lanjut mengenai nilai gizi dan uji sensoris dari susu kedelai fermentasi yang disuplementasi oleh tepung okara.
5. Daftar pustaka
Antara, N.S, I Nyoman Dibia, W.R Aryanta. 2009 Karakterisasi Bakteri Asam Laktat yang Diisolasi dari Susu Kuda Bima.Agritech. Vol 29 :1-8
Bedani, R., Rossi, A, E., Saad, S, M, I. 2013. Impact of inulin and okara on Lactobacillus
acidophillus La-5 and Bifidobacterium
animalis Bb-12 viability in a fermented soy
product and probiotic survival under in vitro simulated gastrointestinal conditions. Food
Microbiology. 34 : 382 – 389.
Capela P, Hay TKC, Shah NP. 2006. Effect of cryoprotectants, prebiotics and microencapsulation on survival of probiotic organism in yogurt and freeze dried yogurt.
Food Res Int. 39 : 203 - 211
Chen, H., Li- jun, Z., Bo, X., Rui, L., 2010. Effect of soybean oligosaccharides on blood lipid, glucose levels and antioxidant enzymes
activity in high fat rats. Food Chemistry. 119: 1633-1636
Donkor, O, N., Henriksson, A., Vasiljevic, T., Shah, N, P., 2007. Alpha galactosidase and proteolytic activities of selected probiotic and dairy cultures in fermented soymilk. Food
Chemistry. 104, 10 – 20
Fei Lu., Yang Liu., Bo Li., 2013. Okara dietary fiber and hypoglycemic effect of okara foods.
Bioactive Carbohydrate and Dietary Fibre.
2, 126 – 132
Jenie, B. S. L., Candrasari, E. Y., dan Lilis nuraida. 1996. Aktivitas antimiikroba dari susu kedelai yang difermentasi oleh
Lactobacillus casei. Jurnal Ilmu dan
Teknologi Pangan. 1 : 16 – 26
Krasaekoopt, W., Bhandari, B., and Deeth, H., 2004. The influence of coating materials on some properties of alginate beads and survivability of microencapsulated probiotic bacteria. International Dairy Journal 14, 737 : 743
Lian, Wen-Chian., Hung-Chi Hsiao, and Cheng-Chun Chou. 2003. Viability of microencapsulation bifidobacteria in simulated gastric juice and bile solution. Int.
J. Food. Microbiol,86 : 293-301.
Marazza, J, A., LeBlanc, G, J., de Giori, G, S., Garro, M, S., 2013. Soymilk fermented with
Lactobacillus rhamnosus CRL981
ameliorates hypergycemia, lipid profiles and increases antioxidant enzyme activities in diabetic mice. J. Functional Foods. Article in Press
Moustafa Khalf., Dabour, N., Kheadr, E., and Fliss I., 2010. Viability of probiotic bacteria in maple sap products under storage and gastrointestinal conditions. Bioresource Technology. 101 : 7966 – 7972
Saad, S, M., Rossi, E, A., Vieira, D, S., Bedani, R., 2013. Tropical fruit pulps decreased
probiotic survival to in vitro gastrointestinal stress in synbiotic soy yoghurt with okara during storage. LWT- Food Science and
Technology. 1 – 8
Su, P., Henriksson, A., Mitchell, H., 2007. Prebiotic enhances survival and prolong the retention period of specific probiotic inocula in an in vivo murine model. Journal of
Applied Microbiology. 106, 2393 – 2400
Shortt, C. 1999. The probiotic century : historical and current perspective. Review Trends Food Science and Tech. 10 : 411 – 417
Tamime, A.Y. dan R.K. Robinson. 2002. Yogurt
Science and Technology. New York. CRC
Press. p: 1-9.
Yogeswara, I, B, A., Wita, K, I, G, A., Nursini, N, W. 2013. Viabilitas probiotik
Lactobacillus acidophillus FNCC 0051 pada
susu kedelai terfermentasi selama proses penyimpanan. Hibah Penelitian Dosen Pemula
Wang, J., Guo, Z., Zhang, Q., Yan, L., Chen, W., Liu, X.M., Zhang, H.P., 2009. Fermentation characteristics and transit tolerance of probiotic L. casei Zhang in soymilk and bovine milk during storage. J.