SISTEM PENGHANTARAN OBAT SISTEM PENGHANTARAN OBAT
MIKROENKAPSULASI MIKROENKAPSULASI
ditulis untuk memenuhi tugas mata kuliah si
ditulis untuk memenuhi tugas mata kuliah sistem penghantaran obat baru padastem penghantaran obat baru pada semester 7 tahun ajaran 2017/20
semester 7 tahun ajaran 2017/201818
Disusun oleh : Disusun oleh :
Tri
Tri Nenci Nenci S S Puri Puri 260110140115260110140115 Siti
Siti Sofiatul Sofiatul Jannah Jannah 260110140126011014011616 Anggun
Anggun Putri Putri Perwira Perwira 260110140126011014011717
FAKULTAS FARMASI FAKULTAS FARMASI UNIVERSITAS PADJADJARAN UNIVERSITAS PADJADJARAN JATINANGOR JATINANGOR 2017 2017
PEMBAHASAN PEMBAHASAN
I.
I. PendahuluanPendahuluan
Enkapsulasi merupakan teknik penyalutan suatu bahan sehingga bahan Enkapsulasi merupakan teknik penyalutan suatu bahan sehingga bahan yang disalut dapat dilindungi dari pengaruh lingkungan. Bahan penyalut disebut yang disalut dapat dilindungi dari pengaruh lingkungan. Bahan penyalut disebut enkapsulan sedangkan yang disalut/dilindungi disebut
enkapsulan sedangkan yang disalut/dilindungi disebut corecore. Enkapsulasi pada. Enkapsulasi pada bakteri
bakteri dapat dapat memberikan memberikan kondisi kondisi yang yang mampu mampu melindungi melindungi mikroba mikroba daridari pengaruh lingkungan
pengaruh lingkungan yang tidak yang tidak menguntungkan, seperti menguntungkan, seperti panas panas dan dan bahan bahan kimia.kimia. Sedangkan mikroenkapsulasi adalah proses fisik dimana bahan aktif (bahan inti), Sedangkan mikroenkapsulasi adalah proses fisik dimana bahan aktif (bahan inti), seperti partikel padatan, tetesan air ataupun gas, dikemas dalam bahan sekunder seperti partikel padatan, tetesan air ataupun gas, dikemas dalam bahan sekunder (dinding), berupa lapisan film tipis. Proses ini digunakan untuk melindungi suatu (dinding), berupa lapisan film tipis. Proses ini digunakan untuk melindungi suatu zat agar tetap tersimpan dalam keadaan baik dan untuk melepaskan zat tersebut zat agar tetap tersimpan dalam keadaan baik dan untuk melepaskan zat tersebut pada kondisi tertentu saat digunakan (Paramita, 2010).
pada kondisi tertentu saat digunakan (Paramita, 2010).
Mikroenkapsulasi adalah salah satu teknik yang dapat digunakan untuk Mikroenkapsulasi adalah salah satu teknik yang dapat digunakan untuk pembuatan
pembuatan sediaan sediaan lepas lepas terkendali. terkendali. Mikroenkapsulasi Mikroenkapsulasi merupakan merupakan suatu suatu prosesproses penyalutan
penyalutan secara secara tipis tipis partikel partikel padat, padat, tetesan tetesan cairan cairan dan dan dispersi dispersi zat zat cair cair oleholeh bahan
bahan penyalut. penyalut. Mikrokapsul Mikrokapsul sebagai sebagai hasil hasil dari dari proses proses mikroenkapsulasimikroenkapsulasi mempunyai ukuran antara 1-5.000 µm, memiliki kelarutan dan stabilitas yang mempunyai ukuran antara 1-5.000 µm, memiliki kelarutan dan stabilitas yang baik. Keunikan
baik. Keunikan dari dari mikrokapsul adalah mikrokapsul adalah kecilnya partikel kecilnya partikel yang tersalut yang tersalut dan dapatdan dapat digunakan lebih lanjut terhadap berbagai bentuk sediaan farmasi (Lachman, 1994; digunakan lebih lanjut terhadap berbagai bentuk sediaan farmasi (Lachman, 1994; Wang
Wang et al et al ., 2006).., 2006).
Beberapa alasan utama dalam pembuatan mikroenkapsulasi adalah sebagai Beberapa alasan utama dalam pembuatan mikroenkapsulasi adalah sebagai berikut :
berikut : a.
a. Untuk melindungi produk dari kondisi lingkungan, seperti suhu,Untuk melindungi produk dari kondisi lingkungan, seperti suhu, kelembapan, radiasi sinar UV, dan adanya interaksi dengan zat lain). kelembapan, radiasi sinar UV, dan adanya interaksi dengan zat lain). b.
b. Untuk menjaga lingkungan dari bahaya atau toksisitas obat, sehinggaUntuk menjaga lingkungan dari bahaya atau toksisitas obat, sehingga penanganan bahan bisa menjadi lebih aman.
c.
c. Mengurangi evaporasi atau perpindahan laju bahan inti ke lingkunganMengurangi evaporasi atau perpindahan laju bahan inti ke lingkungan luar,
luar, d.
d. Mengkonversi bentuk cairan atau semisolid ke dalam bentuk serbukMengkonversi bentuk cairan atau semisolid ke dalam bentuk serbuk yang kering sehingga memudahkan proses penampuran dan
yang kering sehingga memudahkan proses penampuran dan mencegahmencegah lumping
lumping (Re, 1998). (Re, 1998).
Ide dasar mikroenkapsulasi berasal dari sel, yaitu permeabilitas selektif Ide dasar mikroenkapsulasi berasal dari sel, yaitu permeabilitas selektif membran sel memberikan perlindungan terhadap inti sel dari kondisi lingkungan membran sel memberikan perlindungan terhadap inti sel dari kondisi lingkungan yang berubah-ubah dan berperan dalam pengaturan metabolisme sel. yang berubah-ubah dan berperan dalam pengaturan metabolisme sel. Mikroenkapsulasi yang berkembang saat ini menggunakan prinsip yang sama Mikroenkapsulasi yang berkembang saat ini menggunakan prinsip yang sama untuk melindungi bahan aktif dari kondisi lingkungan yang tidak mendukung. untuk melindungi bahan aktif dari kondisi lingkungan yang tidak mendukung. Tujuan utama umum mikroenkapsulasi adalah untuk membuat bahan cairan Tujuan utama umum mikroenkapsulasi adalah untuk membuat bahan cairan bersifat
bersifat seperti seperti padatan. padatan. Hal Hal ini ini menyebabkan menyebabkan beberapa beberapa sifat sifat bahan bahan inti inti menjadimenjadi berubah,
berubah, misalnya misalnya sifat sifat aliran aliran bahan bahan dan dan penangan penangan bahan bahan menjadi menjadi lebih lebih mudahmudah dalam bentuk padatan (Paramita, 2010).
dalam bentuk padatan (Paramita, 2010).
Mikrokapsul dengan bentuk berupa bola, persegi panjang ataupun tak Mikrokapsul dengan bentuk berupa bola, persegi panjang ataupun tak beraturan. Struktur utama dari mi
beraturan. Struktur utama dari mikrokapsul terdiri dari inti krokapsul terdiri dari inti dan pelapis. Bahan intidan pelapis. Bahan inti merupakan bahan yang ada di dalam mikrokapsul yang sering disebut materi inti, merupakan bahan yang ada di dalam mikrokapsul yang sering disebut materi inti, bahan
bahan aktif, aktif, pengisi, pengisi, dan dan fasa fasa internal. internal. Bahan Bahan pelapis pelapis merupakan merupakan bahan bahan yangyang melapisi bagian inti sering disebut pelapis, kulit, membran, dinding bahan, fase melapisi bagian inti sering disebut pelapis, kulit, membran, dinding bahan, fase luar atau matriks (Zuidam and Shimoni, 2010).
luar atau matriks (Zuidam and Shimoni, 2010).
Tipe mikroenkapsulasi secara umum ada dua yaitu satu inti (
Tipe mikroenkapsulasi secara umum ada dua yaitu satu inti ( single single corecore)) dan banyak inti (
dan banyak inti (multiple coremultiple core) pada bagian dindingnya. Mikrokapsul dengan) pada bagian dindingnya. Mikrokapsul dengan banyak
banyak inti inti memiliki memiliki inti inti yang yang tersebar tersebar secara secara merata merata di di bagian bagian dinding dinding dandan bagian
bagian tengah tengah mikrokapsul mikrokapsul biasanya biasanya berupa berupa rongga rongga kosong kosong yang yang dihasilkan dihasilkan daridari pemuaian selaa
pemuaian selaa tahap pengeringan akhir tahap pengeringan akhir (Jafari(Jafari et al et al ., 2008). Mikrokapsul dengan., 2008). Mikrokapsul dengan satu inti biasanya memiliki muatan inti yang tinggi, misalnya 90% dari total berat satu inti biasanya memiliki muatan inti yang tinggi, misalnya 90% dari total berat mikrokapsul. Sedangkan mikrokapsul dengan struktur banyak inti biasanya mikrokapsul. Sedangkan mikrokapsul dengan struktur banyak inti biasanya memiliki persentase pelapis hingga 70% dari berat mikrokapsul. Bahan pelapis ini memiliki persentase pelapis hingga 70% dari berat mikrokapsul. Bahan pelapis ini akan rusak secara mekanik (pengunyahan, pemanasan, dan pelarut), perubahan akan rusak secara mekanik (pengunyahan, pemanasan, dan pelarut), perubahan
pH, enzim, serta sifat fisik dan kimia dari bahan inti (kelarutan, difusivitas, tekanan uap, dan koefisien partisi) dan pelapis (ketebalan, porositas, dan kemampuan bereaksi) sehingga bahan inti akan terlepas).
Gambar 1 Tipe Mikrokapsul (Jafari et al ., 2008)
Gambar 2 perbedaan struktur mikrokapsul dan microsphere (Singh et al , 2010).
Keberhasilan melakukan proses mikroenkapsulasi menurut Deasy (1987) terdiri dari:
a. Bentuk bahan inti yang dikapsul (padat, cair, gas) b. Stabilitas terhadap suhu dan pH
c. Jenis bahan pelapis yang digunakan
d. Sifat fisikokimia (solubilitas, hidrofobik atau hidrofilik)
f. Prinsip mikroenkapsulasi yang digunakan (fisik atau kimia) g. Ukuran mikroenkapsulasi yang dibuat
Bahan-bahan pelapis yang dapat digunakan dalam proses mikroenkapsulasi harus memiliki syarat yang diantaranya: dapat memberikan lapisan tipis yang bersifat kohesif dengan bahan inti, stabilitas pada bahan inti, tidak higroskopis dan tidak bereaksi dengan bahan inti, mampu melapisi bahan inti secara kuat, keras dan fleksibel, mampu terlepas dibawah kondisi tertentu, dan ekonomis (Agnihotri et al ., 2012). Bahan-bahan pelapis sudah banyak digunakan yaitu: gum (gum arab, sodium aglinat, karagenan), karbohidrat (pati, dekstrin, sukrosa), selulosa (metilselulosa, karbonsimetilselulosa), lemak (parafin, asam stearat, pospolipid) dan protein (gelatin, albumin).
II. Keuntungan dan Kerugian Mikroenkapsulasi
Menurut Agnihotri et al . (2012), mikroenkapsulasi memiliki keuntungan dan kerugian sebagai berikut:
Tabel 1. Keuntungan dan Kerugian Mikroenkapsulasi
No. Keuntungan Kerugian
1. Mampu mengatur bahan inti
(mengubah bahan inti cair menjadi padat, sehingga lebih mudah
penangannya dan memiliki bau yang lebih netral)
Perubahan stabilitas pengkapsulan selama proses produksi dan
penyimpanan
2. Melindungi bahan inti (mencegah perubahan dan pengurangan kadar bahan inti)
Ketidakpuasan konsumen terhadap kualitasnya
3. Meningkatkan kestabilan bahan inti selama proses produksi sampai produk akhir (mengurangi
penguapan bahan aktif, reaksi dengan udara, air dan bahan lain, serta proses degradasi)
Meningkatkan kekompleksan proses produksi
4. Mengontrol proses pelepasan bahan inti
Penambahan cost
III. Teknik Pembuatan
Ada beberapa teknik yang digunakan dalam mikroenkapsulasi. Pemilihan proses berdasarkan pada sensitivitas bahan aktif, sifat fisik dan kimia baik bahan
aktif maupun lapisan kulit, ukuran mikrokapsul yang diinginkan, tujuan aplikasi bahan, mekanisme pelepasan bahan aktif, dan alasan ekonomi.
Metode fisik dari mikroenkapsulasi meliputi spray drying , spray cooling/chilling , freeze drying , spinning disk , fluidized bed , extrusion dan co-crystallization. Proses mikroenkapsulasi secara kimia adalah interfacial polymerization dan solvent evaporation and extraction. Proses mikroenkapsulasi baik secara fisik maupun kimia diantaranya coaservation/fase pemisahan, enkapsulasi molekular, dan liposome entrapment . Alur proses mikroenkapsulasi dapat dilihat pada Gambar 3.
1.
Spray drying
Teknik spray drying mengubah bahan yang awalnya berupa bahan cair menjadi materi padat. Pada proses spray drying , bahan yang akan dikeringkan disemprotkan dalam bentuk kabut. Luas permukaan bahan yang kontak langsung dengan media pengering dapat lebih besar sehingga menyebabkan penguapan berlangsung lebih baik. Faktor yang mempengaruhi spray drying adalah bentuk penyemprot, kecepatan alir produk dan sifat produk (Paramita, 2010).
Penggunaan spray drying tidak terbatas pada bahan makanan saja, tetapi juga pada makhluk hidup bersel tunggal, misalnya bakteri. Mikroenkapsulasi menggunakan spray dyring paling banyak digunakan dalam industri karena biayanya relatif lebih rendah. Di bidang farmasi, mikroenkapsulasi banyak digunakan terutama pada drying process, grranulasi, preparasi disperse padat, alterasi polimorfisme obat, preparasi serbuk kering untuk sediaan aerosol, pembuatan sediaan lepas terkendali, dan proses penyalutan obat untuk memperbaiki rasa atau melindungi zat aktif dari proses oksidasi (Yeo et al , 2001).
Proses mikroenkapsulasi fleksibel, dapat digunakan untuk variasi bahan dalam mikroenkapsulasi karena peralatannya mudah diterapkan dalam pengolahan bermacam bahan dan menghasilkan partikel-partikel yang berkualitas baik dengan distribusi ukuran partikel yang konsisten. Bahan yang dikemas dengan cara ini meliputi lemak, minyak, dan penyedap rasa. Pelapisnya dapat berupa karbohidrat, seperti dekstrin, gula, pati, dan gum, atau protein, seperti gelatin dan protein kedelai. Proses mikroenkapsulasi meliputi pembentukan emulsi atau suspensi antara bahan aktif dan pelapis, dan pengkabutan emulsi ke sirkulasi udara kering panas dalam ruang pengering menggunakan atomizer ataupun nozzle. Kadar air
dalam droplet emulsi diuapkan akibat kontak dengan udara panas. Padatan yang tersisa dari bahan pelapis menjebak bahan inti (Paramita, 2010).
Spray drying berguna untuk bahan yang sensitif terhadap panas karena proses pengeringan berlangsung sangat cepat. Pada proses spray drying , bahan yang akan dikeringkan disemprotkan dalam bentuk kabut. Luas permukaan bahan yang kontak langsung dengan media pengering dapat lebih besar sehingga menyebabkan penguapan berlangsung lebih baik. Faktor yang mempengaruhi spray drying adalah bentuk penyemprot, kecepatan alir produk dan sifat produk.
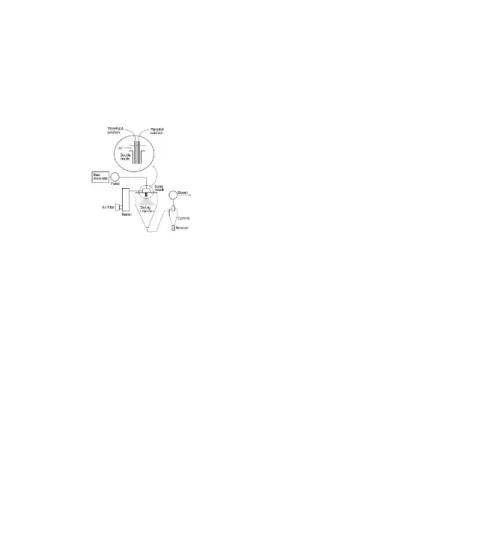
Polimer hidrofilik maupun hidrofobik dilarutkan dalam pelarut yang sesuai (pada umumnya pelarut organik). Zat aktif obat dapat dilarutkan maupun disuspensikan ke dalam pelarut. Selain itu, larutan yang berisi zat aktif dapat diemulsifikasikan ke dalam larutan polimer. Campuran ini kemudian di
semprotkan melalui nozzle dari bagian spray dryer sehingga akan menghasilkan mikrosper solid yang akan terpresipitasi ke dalam kolektor di bagian bawah. Beberapa proses terkadang menggunakan plasticizer untuk membentuk mikrokapsul dengan permukaan yang halus dengan mengurangi rigiditas rantai polimer (Yeo et al , 2001).
Gambar 2. Skema/diagram proses penggunaan spray dryer untuk preparasi mikropartikel PGLA
Penggunaan metode spray drying terbilang cukup mudah, cepat, dan sederhana untuk proses scale-up sehingga banyak digunakan sebagai alternative dari metode konvensional, seperti koaservasi dan metode eulsi untuk obat berupa protein (Yeo et al , 2001). Teknik spray drying digunakan dalam produksi mikropartikel PGLA yang mengandung thyrotropin releasing hormone (TRH). TRH dalam air dan PGLA dalam asetonitril dicampur untuk membentuk larutan yang jernih kemudian disemprotkan. Karena produksi mikropartikel ini sering
menimbulkan aglomerasi dan menempel pada dinding chamber , alat didesain menggunakan sistem nozzle ganda dengan penambahan larutan mannitol sebagai anti-adherent secara simultan. Proses ini menghasilkan partikel dengan ukuran 20 µm dengan pelepasan obat TRH pada orde nol dengan penggunaan selama satu bulan dari dosis awal (Takada et al , 1995).
Kelebihan: keanekaragaman dan ketersediaan mesin, kualitas mikrokapsul yang tetap baik, berbagai ukuran partikel yang dapat diproduksi, dan kemampuan dispersibilitas yang baik dalam media berair, produk akan menjadi kering tanpa menyentuh permukaan logam yang panas, temperatur produk akhir rendah walaupun temperatur pengering relatif tinggi, waktu pengeringan singkat dan produk akhir berupa bubuk stabil yang memudahkan penanganan dan transportasi
(Paramita, 2010).
Kekurangan: kehilangan bahan aktif dengan titik didih rendah, adanya proses oksidasi dalam senyawa penyedap rasa, dan keterbatasan pada pilihan bahan dinding, dimana bahan dinding harus dapat larut pada air dengan jumlah
2.
F reeze drying
Merupakan metode mikroenkapsulasi yang digunakan dalam proses pengeringan pada hampir semua bahan yang sensitif terhadap panas dan aroma. Telah digunakan untuk mengkapsul essence yang larut dalam air dan aroma alami (Gouin, 2004). Menurut Zuidam and Shimoni (2010), pada tahap pertama, sampel dibekukan dalam suhu antara −90 dan −40°C, kemudian pengeringan dengan sublimasi langsung dibawah tekanan rendah sehingga suhunya menurun antara −90 dan −20°C. Setelah pengeringan sampel yang terbentuk dapat dihancurkan dalam bentuk yang lebih kecil, apabila perlu dapat melakukan proses penghancuran melalui grinding. Kerugian utama metode freeze draying adalah penggunaan energi yang tinggi, prosesnya yang lama dan struktur pori yang terbuka yang mana secara umum kurang bagusnya ikatan yang mengelilingi bahan aktif. Dibandingkan dengan spray drying , metode freeze drying 30 – 50 kali lebih mahal (Gharsallaoui et al ., 2007).
3.
Spinning disk
Merupakan modifikasi proses dari spray cooling/chilling dengan menggunakan metode atomisasi (Paramita, 2010). Spray chilling (congealing) merupakan metode alternative dari metode spray drying, meliputi proses disolusi atau disperse zat aktif ke dalam pembawa yang meleleh tanpa adanya pelarut (Yeo et al , 2001). Prinsip dari spray cooling/chilling mirip dengan spray drying , namun menggunakan udara dingin dalam proses pengeringannya. Spinning disk melibatkan pembentukan inti suatu suspensi di lapisan cairan dan suspensi ini terletak di atas disk yang berputar dalam kondisi yang mengakibatkan lapisan film jauh lebih tipis daripada ukuran partikel inti. Pemakaian proses ini meningkat dengan cepat sejak tahun 2000 karena memberikan hasil yang seimbang atau bahkan lebih baik daripada spray drying atau spray cooling/chilling dengan biaya proses yang tidak berbeda (Paramita, 2010).
4.
F lui dized bed coating
Merupakan teknik yang digunakan dalam mengkapsul bubuk dengan peralatan yang diset dalam proses kontinyu atau tidak. Bubuk dibentuk oleh udara yang ekstrim dengan temperatur yang spesifik kemudian dispray dengan atomisas i untuk membuat bahan pelapis. Sehingga secara berangsur-angsur bahan aktif akan tertutup oleh pelapis pada saat dispray. Bahan pelapis harus memiliki sifat viskositas cocok sehingga dapat dipompa dan diatomisasi, harus stabil dalam kondisi panas dan seharusnya dapat membentuk lapisan film sebagai bahan pelapis (Zuidam and Shimoni, 2010). Keterbatasan penggunaan teknologi ini adalah hanya dapat digunakan untuk mengkapsul partikel padat dan ukuran produk yang terbentuk tidak dapat kurang dari 10 μm (Gouin, 2004).
5. Teknik
coacervation
Merupakan pemisahan fase cair/cair secara spontan yang terjadi ketika dua polimer yang bermuatan berlawanan (misalnya protein dan polisakarida) dicampur dalam media berair kemudian mengarah ke pemisahan menjadi dua fase. Fase yang lebih rendah disebut (kompleks) coacervate dan memiliki konsentrasi yang tinggi dari kedua polimer. Fase atas disebut sebagai supernatan atau fase kesetimbangan, yang merupakan larutan polimer encer. Coacervate digunakan sebagai bahan makanan, misalnya pengganti lemak atau memberi rasa yang mirip daging dan biomaterial, seperti lapisan tipis ( film) yang dapat dimakan dan kemasan. Metode ini sangat efisien dan menghasilkan mikrokapsul dengan ukuran yang lebih bervariarif daripada teknik mikroenkapsulasi yang lain (Paramita, 2010).
Proses ini meliputi tiga tahap, pertama, mecampur tiga fase yang saling tidak melarutkan (fase kontinyu atau air, bahan aktif yang akan dimikroenkapsulasi dan bahan pelapis). Kedua, bahan pelapis membentuk lapisan pada bahan inti. Hal ini dicapai dengan merubah pH, suhu atau kekuatan ion yang menghasilkan pemisahan fase (coacervation) dari pelapis dan sebaran inti yang terjebak.
Terakhir, bahan pelapis memadat karena adanya panas, crosslinking (hubungan silang) dan teknik desolvasi. Mikrokapsul yang dihasilkan dari pemisahan fase encer memiliki dinding yang larut air dan bahan aktif yang bersifat menjauhi air (hidrofobik), seperti minyak sayur, penyedap rasa, dan vitamin yang larut dalam minyak (Paramita, 2010).
Gambar 4. Diagram proses pembentukan mikrokapsul menggunakan teknik koaservasi
Teknik penyiapan fase dapat diklasifikasikan berdasarkan metode untuk menginduksi fase pemisahannya, yaitu penambahan non-solvent, perubahan suhu, penambahan polimer inkompatibel atau penambahan garam, dan interaksi polimer-polimer (Yeo et al , 2001).
a. Penambahan Non-solvent
Zat polimer yang akan disalut dilarutkan terlebih dahulu ke dalam pelarut yang sesuai, kemudian zat aktif obat akan dilarutkan atau disuspensikan ke dalam larutan polimer. Selanjutnya nonsolvent atau coacervating agent pertama yang dapat tercampur baik dengan pelarut namun tidak terlarut dengan polimer ditambahkan secara perlahan ke dalam sistem larutan polimer-zat aktif. Polimer tersebut kemudian akan terkonsentrasi karena pelarut perlahan-lahan akan terestraksi ke dalam
larutan non-solvent, kemudian diinduksi ke fase pemisahan dan membentuk droplet koaservat yang mengandung obat.Ukuran droplet obat dapat disesuaikan dengan kecepatan pemutaran/pengadukan. Droplet kemudian dipindahkan ke dalam non-solvent kedua atau hardening agent yang akan mengeras menjadi mikropartikel.
Contoh non-solvent yang digunakan memiliki berat molekul kecil, seperti polybutadiene, polimer methacrylic cair, minyak silicon, minyaak dari sayuran, dan paraffin cair BM rendah. Sementara untuk non-solvent kedua digunakan hidrokarbon alifatik seperti heptane, heksan, dan lain-lain.
b. Perubahan suhu
Jika suhu menurun di bawah area kurva, fase pemisahan polimer terlarut akan terjadi membentuk cairan tidak tercampurkan dan polimer akan memepel di sekitar partikel obat membentuk mikrokapsul.
c. Penambahan polimer inkompatibel
Ketika dua jenis polimer yang berbeda secara kimia dalam suatu pelarut tidak tercampurkan/inkompatibel, maka fase pemisahan akan terjadi dalam sistem mikrokapsul. Obat akan terdispersi ke dalam salah satu larutan polimer dan ditambahkan polimer yang lain, ketika mencapai titik jenuh dengan penambahan polimer lain tersebut, terjasi fase pemisahan dan pembentukan droplet yang mengandung zat aktif dan mengalami coalescing membentuk mikrokapsul. Pada kondisi yang sama, garam inorganik juga dapat ditambahkan ke dalam larutan yang berisi polimer larut air untuk membentuk fase pemisahan.
d. Interaksi polimer-polimer (complex coacervation)
Interaksi polielektrolit yang berbeda muatan akan menghasilkan pembentukan kompleks dengan mengurangi solubilitas kemudian terjadi fase pemisahan. Pada umumnya gelatin digunakan sebagai polimer
kationik pada pH dibawah isoelektrik, kemudian direaksikan dengan polimer anionic seperti gom arab pada pH 4.5 dan suhu 40-45°C membentuk kompleks koaservat dalam larutan akuos. Ketika terjadi fase pemisahan, larutan bahan inti berisi zat aktif yang tidak larut air ditambahkan dan diemulifikasi untuk membentuk ukuran droplet yang diinginkan.
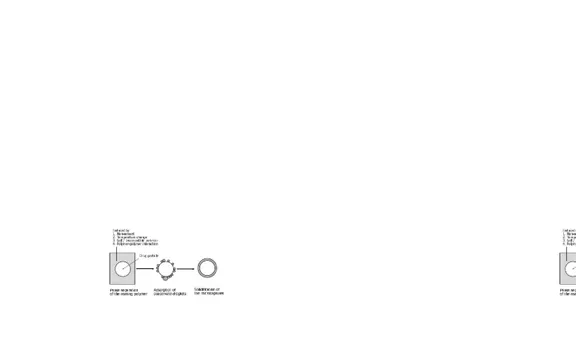
Berikut diagram proses pada berbagai metode untuk membentuk fase pemisahan dapat dilihat pada gambar 5.
Gambar 5. Diagram fase pemisahan secara umum pada teknik koaservasi berdasarkan pelarut (A), suhu (B), polimer inkompatibel (C), dan interaksi
Kelebihan: memiliki payload yang sangat tinggi yaitu >99%, kemudahan dalam mengontrol lepasnya bahan inti dari pelapis (Gouin, 2004).
Kekurangan: Biaya proses produksi yang tinggi dan pembatasan yang kompleks apabila ingin digunakan secara komersial (Madene et al ., 2006).
6. Enkapsulasi molekuler/pemasukan kompleksasi
Proses ini menggunakan cyclodextrin untuk membuat kompleks dan imobilisasi molekul. Cyclodextrin digunakan untuk menstabilkan emulsi dan melindungi bahan makanan yang sensitif dari cahaya, panas, dan oksigen. Siklodextrin dapat meningkatkan kelarutan bahan yang bersifat hidrofobik, mengurangi penguapan dari penyedap rasa pada makanan, dan menutupi rasa, aroma, atau warna makanan yang tidak diinginkan (Paramita, 2010).
Reaksi umum dalam enkapsulasi molekuler menggunakan prinsip “host- guest ”. Kemampuan cyclodextrin untuk membentuk pemasukan kompleksasi dengan molekul tamu memiliki dua faktor kunci. Yang pertama adalah tergantung pada ukuran relatif cyclodextrin dengan ukuran molekul tamu atau kunci tertentu di dalam kelompok-kelompok fungsional tamu. Jika ukuran tamu salah maka tidak akan sesuai untuk masuk ke dalam rongga cyclodextrin. Faktor kritis kedua adalah termodinamik interaksi antara berbagai komponen dari sistem (cyclodextrin, tamu, pelarut). Diperlukan adanya daya dorong dari molekul tamu ataupun daya tarik dari cyclodextrin yang menguntungkan. Dalam hal ini, cyclodextrin memiliki sifat fungsional hidrofilik (mendekati air) pada bagian bawah dan atas strukturnya yang seperti donat dan bersifat hidrofobik (menjauhi air) pada bagian tengah karena terhubung dengan jembatan glikosidik oksigen. Senyawa yang dapat membetuk kompleks dengan cyclodextrinadalah senyawa yang bersifat hidrofobik atau memiliki bagian yang hidrofobik. Bagian hidrofobik
dari molekul tamu membentuk interaksi yang stabil nonkovalen dengan bagian tengah cyclodextrin (Paramita, 2010).
7. Liposom entrapment
Liposom terbentuk dari dua lapis membran yang mana terdiri dari molekul lipid seperti fosfolipid (lecithin) dan kolesterol. Mereka terbentuk ketika lipid terpisah pada media cair dan terekspos sebagai potongan yang menggunakan microfluidization atau penggilingan koloid. Mekanisme utama dalam pembentukan liposom adalah interaksi hidrofilik dan hidrofobik antara fospolipid dan molekul air. Bahan aktif dapat ditangkap dengan bahan cair dari liposom atau dengan menangkap dengan membran. Ukuran partikel antara 30 nm atau beberapa dalam bentuk mikron. Penyimpanan menyebabkan ukuran menjadi lebih besar sehingga perlu dijaga dengan electrostatic repulsion (seperti dengan penambahan lipid pada membran pelapis (Zuidam and Shimoni, 2010). Menurut Madene et al . (2006), kerugian metode ini adalah kestabilannya hanya dalam waktu yang pendek, susah dalam proses scale up dan susah dalam proses kapsul karena bahan
membutuhkan kondisi kering.
Tabel 2. Ringkasan Proses Mikroenkapsulasi (Zuidam and Shimoni, 2010)
Teknologi Alur Proses Bentuk Muatan
(%)
Partikel (µm) Freeze drying 1. Penyebaran bahan aktif dengan
bahan pelapis pada air 2. Pembekuan sampel
3. Pengeringan dalam temperatur yang rendah
4. Proses pengecilan produk
Matrix Berbagai macam
20-5.000
Spray drying 1. Penyebaran bahan aktif pada pelapis cair
2. Atomisasi 3. Pengeringan Spray
chilling/cooling
1. Penyebaran bahan aktif pada pelapis tipis 2. Atomisasi 3. Pendinginan Matrix 10-20 20-200 Fluid bed coating
1. Pembentukan bubuk aktif 2. Pelapisan secara semprot 3. Pengeringan atau pendinginan
Reservoir 5-50 5-5.000
Coacervation 1. Mempersiapkan pencampuran bahan aktif pada fase cair
2. Pencampuran dengan menggunakan turbulen 3. Pendinginan Reservoir 40-90 10-800 Liposome entrapment
1. Penyebaran bahan aktif pada lemak
2. Pengurangan ukuran
Berbagai macam
5-50 10-1.000
IV. Evaluasi Sediaan Mikrokapsul
a. Analisis spektroskopi IR (Weiss et al ., 2007)
Mikrokapsul glikuidon dalam bentuk serbuk, diukur serapan inframerahnya dengan menggunakan alat Fourier Transform Infrared (FT-IR). Mikrokapsul glikuidon diletakkan di atas transparent disk kemudian dilakukan pembacaan (scan) oleh alat FT-IR.
b. Berat mikrokapsul yang diperoleh
Berat mikrokapsul yang diperoleh ditimbang dengan timbangan analitik. c. Distribusi ukuran partikel (Halim, 1995; Voigt, 1994)
Mikroskop sebelum digunakan dikalibrasi terlebih dahulu dengan menggunakan mikrometer pentas. Lalu sejumlah mikrokapsul didispersikan dalam parafin cair dan diteteskan pada kaca objek. Kemudian letakkan di bawah mikroskop, amati ukuran partikel serbuk dan hitung jumlah partikelnya (300 partikel).
d. Penetapan kandungan air (Rajesh et al ., 2011)
Mikrokapsul diukur kadar airnya menggunakan alat pengukur kadar lembab (moisture balance).
e. Penetapan kandungan glikuidon dalam mikrokapsul
Mikrokapsul glikuidon dari masing-masing formula ditimbang 50 mg. Lalu dimasukan ke dalam labu ukur 50 mL dan dilarutkan dengan metanol sampai tanda batas, kemudian dikocok dan disonikasi selama 1 jam. Setelah itu dipipet 5 mL filtrat ke dalam labu ukur 25 mL, lalu diencerkan dengan metanol sampai tanda batas. Lakukan pengenceran hingga 3 kali dan ukur serapan pada panjang gelombang serapan maksimum glikuidon dengan spektrofotometer UV. Konsentrasi zat aktif dapat ditentukan dengan menggunakan kurva kalibrasi. Masingmasing formula dilakukan pengulangan 3 kali.
f. Penentuan loading obat, efisiensi enkapsulasi, dan hasil mikrokapsul (Khamanga et al ., 2009)
Dari penentuan kandungan obat dalam mikrokapsul yang diperoleh dapat dihitung persentase zat aktif yang tersalut dengan menggunakan rumus:
%Loading = berat zat aktif
berat mikrokapsul× 100% Persentase microcapsule yield dihitung menggunakan rumus:
% =
× 100% Keterangan:
Mo = Berat awal
=
× 100% Setiap pengujian dilakukan sebanyak tiga kali pengulangan.
g. Scanning Electron Microscopy (Khamanga et al ., 2009; Rajesh et al ., 2011) Sampel diletakkan pada sampel holder aluminium dengan ketebalan 10 nm. Sampel kemudian diamati berbagai perbesaran alat SEM. Voltase diatur pada 5 kV dan arus 12 mA.
h. Profil disolusi (Ahad et al ., 2010)
Mikrokapsul didisolusi dengan metode dayung pada kecepatan 50 rpm. Labu diisi dengan medium disolusi dapar fosfat pH 7,4 sebanyak 900 mL pada suhu 37±0,5oC. Setelah suhu tersebut tercapai, dimasukkan mikrokapsul yang setara dengan 30 mg mikrokapsul ke dalam wadah disolusi. Pada menit ke 10, 20, 30, 45, 60, 120, 240, dan 360 dipipet larutan sebanyak 5 mL. Pada setiap pemipetan, larutan di dalam labu diganti dengan medium disolusi dengan volume dan suhu yang sama.
Lalu dilakukan pengukuran absorban dengan menggunakan spektrofotometer UV pada pajang gelombang maksimum zat aktif. Kadar zat aktif pada masing-masing waktu pemipetan dapat ditentukan dengan bantuan kurva kalibrasi. Pengujian ini dilakukan sebanyak tiga kali dengan mengambil sampel yang sama pada tiap formula.
V. Aplikasi Mikroenkapsulasi
Teknologi mikrokapsul yang bayak digunakan di bidang farmasi salah satunya dalam pembuatan sediaan obat lepas terkendali (controlled release). Berbagai macam teknik telah banyak dikembangkan untuk memodifikasi pelepasan zat aktif, seperti transport agen terapeutik secara selektif ke target obat
untuk mengoptimasi respon biologis yang diinginkan atau mengatur pelepasan obat pada target selektif dengan laju yang diinginkan. Laju pelepasan obat dapat disesuaikan dengan pengaturan sistem yang akan menghasilkan konsentras obat dalam plasma yang konstan di antara batas efisiensi dan batas toksisitas obat (Porte dan Courarraze, 1994). Beberapa aplikasi mikroenkapsulasi dalam bidang farmasi di antaranya :
1. Mikroenkapsulasi Vitamin C
Uddin dkk. (2001) mempelajari pengaruh variabel proses pada asam askorbat karakteristik. Mereka memilih empat teknik enkapsulasi yang berbeda yaitu : pemisahan fase termal, dispersi leleh, penguapan pelarut dan pengeringan semprot. Pada fase teknik pemisahan termal digunakan etil selulosa sebagai bahan pembentuk dinding. Berat molekulnya bervariasi dan parameter lainnya tetap sama. Diketahui bahwa produk mikroenkapsulasi akan menurun seiring kenaikan berat molekul. Alasan yang paling mungkin diberikan adalah penurunan agregasi dari mikrokapsul sebagai berat molekul etil selulosa meningkat. Mereka juga mempelajari tingkat pelepasan asam askorbat, yang didefinisikan sebagai rasio asam askorbat dilepaskan ke solusi untuk berat yang dienkapsulasi awal. Ini ditentukan dengan mensuspensikan 200 mg mikrokapsul dalam 1000 ml air dan terus menerus digetarkan pada 30oC.
Jumlah Asam askorbat yang dilepaskan diukur dengan menggunakan Spektrofotometer UV Hasil menunjukkan bahwa ada perbedaan yang signifikan dalam rasio rilis dengan berat molekul etil selulosa yang berbeda. Semakin tinggi berat molekulnya, semakin rendah tingkat pelepasannya. Tingkat molekuler bukanlah faktor pelepasan lengkap karena berat molekul tinggi atau rendah memberikan pelepasan tingkat ~ 1,0 dalam 20 menit. Ini lebih baik dibandingkan dengan asam askorbat bebas, yang mencapai rasio pelepasan 1,0 setelah hanya 20 detik pembubaran. Lilin Carnauba digunakan dalam metode dispersi melelehkan mikroenkapsulasi. Hasil menunjukkan mikrokapsul sferikel berukuran kira-kira 50μm. Rasio pelepasan hampir 0,6 setelah 120 menit yang secara substansial lebih
rendah dan lebih lambat daripada menggunakan etil selulosa dalam pemisahan fasa. Ini menunjukkan Karnauba membuat asam askorbat lebih stabil.
Teknik penguapan pelarut digunakan untuk menyelidiki efek dari berbagai suhu, rasio inti kedinding dan adanya peliat plastik (trietil sitrat) pada asam askorbat mikroenkapsul. Hasil penelitian menunjukkan bahwa kehadiran plasticiser menurunkan laju pelepasan. Dua rasio inti-ke-dinding yang digunakan adalah 1: 1 dan 3: 1. Tidak ada efek signifikan yang ditemukan. Demikian pula, kedua suhu tersebut digunakan untuk penguapan pelarut 28oC dan 55o C, tidak menunjukkan pengaruh yang signifikan terhadap laju pelepasan. Teknik pengeringan semprot menggunakan empat bahan pelapis polimer yang berbeda, baik sendiri maupun sebagai campuran.
Hasil penelitian menunjukkan bahwa kehilangan asam askorbat selama pengeringan semprot hanya 20% yang dianggap rendah. Masing-masing dari berbagai bahan pelapis dihasilkan dalam ukuran kapsul kebanyakan antara 90-280om fraksi. Namun, rasio asam askorbat yang dienkapsulasi tidak terlalu tinggi, kurang dari 50%. Ini berarti bahwa kurang dari 50% asam askorbat yang digunakan dalam teknik ini sebenarnya mikroenkapsulasi. Sementara pengeringan semprot adalah metode enkapsulasi murah dan ekonomis, nilai ini tidak terlalu tinggi. Rasio yang dienkapsulasi sedikit lebih tinggi bila β-siklodekstrin digunakan. Meskipun nilai rasio yang lebih rendah, asam askorbat telah memperbaiki sifat seperti tidak ada perubahan warna setelah terpapar udara selama satu bulan. Percobaan penyimpanan dilakukan pada suhu 38oC dan 84% kelembaban. Asam askorbat mikroenkapsulasi menunjukkan degradasi yang lebih lambat dari pada kristal asam askorbat.
Studi tersebut menyimpulkan bahwa:
1. Asam askorbat mikroenkapsulasi dapat mencegah perubahan warna asam askorbat dengan menjadi sangat stabil, dapat menghambat laju pelepasan inti dan umumnya menutupi rasa asam.
2. Menggunakan lilin karnauba bukan etil Selulosa memberikan rasio pelepasan yang sangat berkurang yang ideal.
3. Pati dan β-siklodekstrin menunda degradasi asam askorbat bila disimpan pada suhu 38oC dan kelembaban relatif 84%.
2. Mikroenkapsulasi Mikroorganisme
Telah banyak digunakan untuk enkapsulasi dan imobilisasi mikroorganisme (Prakash, 2011). Enkapsulasi sel bakteri adalah proses yang dapat terjadi secara alami saat bakteri berkembang biak dan menghasilkan exopolysaccharides, polimer dengan berat molekul tinggi yang tersusun dari residu gula. Struktur exopolysaccharide dapat bertindak sebagai kapsul pelindung dan mengurangi permeabilitas dan paparan bakteri terhadap faktor lingkungan yang merugikan.
Penelitian awal menggunakan mikroenkapsulasi untuk imobilisasi sel bakteri pada industri makanan dan susu, seperti yang dibahas dalam ulasan lain (Lacroix, 2005).
Dalam beberapa tahun terakhir, mikroenkapsulasi sel probiotik, "mikroorganisme hidup, yang bila diberikan dalam jumlah yang cukup, memberi manfaat kesehatan pada tuan rumah," mendapat perhatian untuk pengobatan sejumlah gangguan pencernaan dan kesehatan lainnya (FAO dan WHO, 2001). Namun, sel probiotik yang dikirim secara lisan harus dikirim dan tetap bertahan melalui kondisi keras GIT bagian atas. Oleh karena itu, mikroenkapsulasi dapat digunakan sebagai perlindungan untuk pengiriman sel. Penelitian difokuskan pada mikroenkapsulasi probiotik telah terbukti berhasil dalam konteks gagal ginjal, penyakit kardiovaskular, dan pada kelainan usus besar, seperti yang dijelaskan
kemudian.
Penelitian awal di bidang mikroorganisme mikroenkapsulasi dilakukan, oleh Prakash dan Chang, menggunakan strain Escherichia coli yang dimodifikasi secara genetik (DH5) yang mengandung gen urease dari aeronel Klebsiella (Prakash, 1995). Enkapsulasi dilakukan dengan gelasi alginat dalam kalsium klorida, diikuti oleh tahap pelapisan dengan polietin dan alginat, untuk menghasilkan mikrokapsul alginate-polylysine-alginate (APA) yang mengandung sel E. coli. Bila diberikan secara oral ke tikus uremik, E. coli yang dienkapsulasi berhasil menurunkan kadar urea plasma dan amonia kembali ke tingkat normal, serta memodulasi banyak penanda gagal ginjal. Ini adalah laporan pertama yang mencatat penggunaan sel buatan membran polimer untuk pengiriman oral organisme rekayasa genetika. Penelitian ini juga menyoroti mikroenkapsulasi sebagai metode untuk mengisolasi mikroorganisme yang dikirim melalui transit GIT sampai ekskresi, menghilangkan masalah keselamatan yang terkait dengan penyaluran mikroorganisme. Penelitian juga dilakukan, secara in vitro, dengan E. coli yang sama namun menggunakan mikrokapsul polivinil alkohol yang memiliki kekuatan mekanik jauh lebih tinggi daripada mikrokapsul APA (Gao, 2004). Penelitian tambahan juga dilakukan dengan Lactobacillus delbrueckii yang mampu mengeluarkan urea, untuk menanggapi kekhawatiran toksisitas terkait dengan penggunaan strain E. coli yang direkayasa secara genetika.
Penelitian oleh Prakash et al . memberikan penelitian pertama yang menyelidiki penggunaan sel ragi mikroenkapsulasi, Saccharomyces cerevisiae, pada gagal ginjal. Kelompok penelitian menyelidiki pemberian oral sel ragi hidup pada mikrokapsul APA pada model tikus uremia gagal ginjal. Studi ini menunjukkan bahwa sel ragi mikroenkapsulasi ditahan di mikrokapsul melalui transit GIT namun memungkinkan urea menyebar melalui membran semipermeabel mikrokapsul dan ditindaklanjuti oleh urease ragi. Yang lebih penting lagi, penurunan 18% yang signifikan dicatat untuk tingkat urea selama periode perawatan 8 minggu, menunjukkan keefektifan formulasi sebagai terapi untuk menghilangkan tingkat metabolit yang meningkat yang ada pada gagal ginjal.
Microenkapsulasi Mikroba dalam Hiperkolesterolemia dan Penyakit
Kardiovaskular
Mikroenkapsulasi sel bakteri baru-baru ini mendapat perhatian untuk pengobatan dan pencegahan hiperkolesterolemia. Pekerjaan awal oleh Garofalo dkk. menyelidiki penggunaan Pseudomonas pictorum mikroenkapsulasi dengan alginat-polietfin dan pori agar terbuka. Pasteurum mikroenkapsulasi ditunjukkan pada aktivitas penipisan kolesterol yang signifikan, dengan aktivitas tertinggi
dengan formulasi mikrokapsul pori agar terbuka (Garofalo, 1989).
Melanjutkan jenis pekerjaan yang sama, Jones et al . menyelidiki APA microencapsulated Lactobacillus plantarum 80 (pCBH1) yang dimodifikasi secara mikroenkapsulasi yang dimodifikasi secara genetik (BSH-) aktif untuk menghancurkan dan menghilangkan asam empedu (Jones, 2012). Penelitian ini menetapkan penggunaan organisme mikroenkapsulasi BSH untuk menurunkan kolesterol serum darah.
Setelah karya ini, Martoni dkk. menunjukkan bahwa APA mikroenkapsulasi secara alami BSH-active Lactobacillus reuteri dapat berhasil dikirim ke usus besar dan tetap aktif secara enzimatik, dengan menggunakan model gastrointestinal manusia yang disimulasikan (Martoni, 2008). Formulasi probiotik ini dapat memberi kontribusi pada penurunan kolesterol yang signifikan pada penyakit kardiovaskular, dengan berkontribusi pada dekonjugasi garam
empedu di usus.
Penelitian lebih lanjut oleh Jones et al . menunjukkan penggunaan APA microencapsulated BSH-active L. reuteri dalam studi klinis manusia, diberikan sebagai formulasi yogurt. Perumusan tersebut ditunjukkan untuk mengurangi kolesterol LDL, kolesterol total, kolesterol apolipoprotein B-100 (apoB-100), dan kolesterol non-high-density lipoprotein (HDL) pada pasien hiperkolesterolemia lebih efisien daripada terapi probiotik tradisional dan lainnya. bahan penurun kolesterol (Jones, 2012).
Lactobacilli yang dienkapsulasi mikrokapsul dalam Penyakit Colon
Mikroba yang tersirkulasi mikro juga mendapat perhatian untuk modulasi peradangan kolon, khususnya yang berkaitan dengan kanker usus besar, namun berpotensi untuk gangguan inflamasi kolon lainnya, seperti sindroma radang usus besar (IBS) dan penyakit radang usus (IBR). Urbanska dkk. menyelidiki sifat antitumorigenik dari APA yang dilumasi mikroplaktin Lactobacillus acidophilus pada tikus Min (multiple intestinal neoplasia) yang membawa mutasi Germline Apc yang secara spontan mengembangkan banyak neoplasma usus pretumorik (Urbanska, 2009). Administrasi probiotik menyebabkan penurunan yang signifikan dalam jumlah adenoma dan neoplasia gastrointestinal pada hewan yang diobati, menunjukkan bahwa bakteri mikroenkapsulasi dapat berperan dalam pengembangan kanker usus besar yang berhasil terapeutik.
Penelitian lebih lanjut menyelidiki kemampuan APA micr oencapsulated L. acidophilus untuk menekan radang usus pada tikus, untuk aplikasi potensial pada penyakit peradangan kronis seperti IBS dan IBD. Pemberian formulasi mikroenkapsulasi menyebabkan penurunan kadar sitokin proinflamasi yang signifikan. Penanda yang terkait dengan kelangsungan hidup sel epitel kolon juga meningkat dengan formulasi L. acidophilus mikroenkapsulasi. Studi yang telah disebutkan sebelumnya, berkaitan dengan mikroba mikroba terserap FAE, telah menunjukkan sifat antioksidan yang signifikan, yang juga dapat terbukti bermanfaat untuk gangguan peradangan usus besar (Urbanska, 2009).
3. Mikropartikel obat NSAID untuk penyakit arthritis
NSAID merupakan jenis obat analgesic yang paling umum digunakan untuk mengobati nyeri pada arthritis, namun kebanyakan obat golongan ni memiliki efek samping terutama pada saluran gastrointestinal. Salah satu upaya untuk mengurangi efek samping obat ini adalah dengan formulasi sediaan lepas terkendali untuk mengoptimasi pelepasan obat dengan dosis yang konstan menggunakan teknologi mikrokapsul (Abadi et al , 2016).
DAFTAR PUSTAKA
A. M. Urbanska, J. Bhathena, C. Martoni, and S. Prakash. 2009. Estimation of the potential antitumor activity of microencapsulated Lactobacillus acidophilus
yogurt formulation in the attenuation of tumorigenesis in Mice. Digestive Diseases and Sciences, vol. 54, no. 2, pp. 264 – 273.
Abadi, S.S., Moin A., Veerabhadrappa G.H. 2016. Review Article: Fabricated Microparticles: An Innovative Method to Minimize the Side Effects of NSAIDs in Arthritis. Crit Rev Ther Drug Carrier Syst. 2016;33(5):433-488. Agnihotri N., R. Mishra, C. Goda, and M. Arora.. 2012. Microencapsulation-A novel approach in drug delivery: a review. Indo GlobalJ of Phram Sci. 2 (1): 1-20.
Ahad, H. A., Kumar, C. S., Reddy, K. K., Kumar, A., Sekhar, C., Sushma, K., et al . 2010. Preparation and Evaluation of Sustained Release Matrix Tablets of Gliquidone Based on Combination of Natural and Synthetic Polymers. Journal of Advanced Pharmaceutical Research, 1(2): 108-114.
C. Lacroix, F. Grattepanche, Y. Doleyres, and D. Bergmaier. 2005. Immobilised cell technologies for the dairy industry, in Applications of Cell Immobilisation Biotechnology, chapter 18. Netherlands : Springer.
C. Martoni, J. Bhathena, A. M. Urbanska, and S. Prakash. 2008. Microencapsulated bile salt hydrolase producing Lactobacillus reuteri for oral targeted delivery in the gastrointestinal tract. Applied Microbiology and Biotechnology, vol. 81, no. 2, pp. 225 – 233.
Deasy P. 1987. Microencapsulation and Related Drugs Process. London (UK): Marcel Dekker.
F. A. Garofalo, M. Eng, and T. M. S. Chang. 1989. Immobilization of P. Pictorum in open pore agar, alginate and polylysine-alginate microcapsules
for serum cholesterol depletion. Biomaterials, Artificial Cells, and Artificial Organs, vol. 17, no. 3, pp. 271 – 289.
FAO and WHO. 2001. Health and Nutritional Properties of Probiotics in Food Including Powder Milk with Live Lactic Acid Bacteria.
Gharsallaoui A, G. Roudaut, O. Chambin, A. Voilley, and R. Saurel. 2007. Applications of spray-drying in microencapsulation of food ingredients: an overview. J Food Res Intern. 40: 1107 – 1121.
Gouin S. 2004. Microencapsulation: industrial appraisal of existing technologies and trends. J Food Sci and Tech. 15: 330-347.
H. Gao, Y. Yu, B. Cai, and M. Wang. 2004. Preparation and properties of microencapsulated genetically engineered bacteria cells for oral therapy of uremia. Chinese Science Bulletin, vol. 49, no. 11, pp. 1117 – 1121.
Halim, A. 1995. Teknologi Partikel . Padang: Universitas Andalas.
Jafari S. M., E. Assadpoor, Y. He, and B. Bhandari. 2008. Encapsulation Efficiency of Food Flavours and Oils during Spray Drying. J Drying Tech. 26: 816-835.
Khamanga, S. M., Parfitt, N., Tsitsi Nyamuzhiwa, Haidula, H., & Walker1, R. B. 2009. The Evaluation of Eudragit Microcapsules Manufactured by Solvent Evaporation Using USP Apparatus 1. Dissolution Technologies.
Lachman, L., Lieberman, H. A., & Kanig, J.L. 1994. Teori dan Praktek Farmasi Industri. Jakarta: Universitas Indonesia Press.
M. I Ré. 1998. Microencapsulation By Spray Drying, Drying Technology: An International Journal, 16:6, 1195-1236.
M. L. Jones, C. J. Martoni, M. Parent, and S. Prakash. 2012. Cholesterol-lowering efficacy of a microencapsulated bile salt hydrolase-active Lactobacillus
reuteri NCIMB, 30243 yoghurt formulation in hypercholesterolaemic adults. The British Journal of Nutrition, vol. 107, no. 10, pp. 1505 – 1513.
Madene A., M. Jacquot, J. Scher, and S. Desobry. 2006. Flavour encapsulation and controlled release – a review. J Food Sci and Tech. 41: 1-21.
Paramita V. 2010. Mikroenkapsulasi dalam industri pangan. IPTEK Inovasi 16: 22.
Rajesh, Narayananan, & chacko, A. 2011. Formulation and Evaluation of Mucoadhesive Microcapsules of Aceclofenac Using HPMC and SCMC as Mucoadhesive Polymers. Journal of Pharmacy Research,Vol.4 (issue 12), 4558-4561.
S. Prakash and T. M. S. Chang. 1995. Preparation and in vitro analysis of microencapsulated genetically engineered E. coli DH5 cells for urea and ammonia removal. Biotechnology and Bioengineering , vol. 46, no. 6, pp. 621 – 626.
S. Prakash, M. Malhotra, W. Shao, C. Tomaro-Duchesneau, and S. Abbasi. 2011. Polymeric nanohybrids and functionalized carbon nanotubes as drug delivery carriers for cancer therapy. Advanced Drug Delivery Reviews, vol. 63, no. 14-15, pp. 1340 – 1351.
Singh, M. N., Hemant, K. S. Y., Ram, M., & Shivakumar, H. G. 2010. Microencapsulation: A promising technique for controlled drug delivery. Research in Pharmaceutical Sciences, 5(2), 65 – 77.
Uddin, M. S., Hawlader, M. N. A. and Zhu, H. J. 2001. Microencapsulation of ascorbic acid: effect of process variables on product characteristics. Journal of Microencapsulation, 18 (2): 199-209.
Voigt, R. 1994. Buku Pelajaran Teknologi Farmasi. Edisi 5. Yogyakarta: UGM Press.