KADAR FENOLIK TOTAL DAN AKTIVITAS
ANTIOKSIDAN DARI ASAM FENOLAT AMPAS TEH HIJAU
Yohanes Martono, Maria Gunawan, Lusiawati Dewi Prodi Kimia Fakultas Sains dan Matematika
Universitas Kristen Satya Wacana Jl. Diponegoro 52 – 60 Salatiga e-mail: [email protected]
ABSTRAK
Ampas teh hijau yang digunakan untuk memproduksi minuman teh di industri ternyata masih mengandung senyawa fenolik dan mempunyai aktivitas antioksidan. Tujuan dari penelitian ini adalah untuk memperoleh asam fenolat bebas (AFB), ikatan ester (AFE), dan ikatan glikosida (AFG) dari ekstrak kasar (EK) ampas teh hijau, menentukan kadar fenolik total, aktivitas antikosidan, dan melakukan identifikasi senyawa asam galat, kafein, dan epigalokatekin galat (EGCG) EK, AFB, AFE, dan AFG pada ampas teh hijau. Pengukuran kadar fenolik total dilakukan dengan metode Folin Ciocalteu dan pengukuran aktivitas antioksidan dilakukan dengan metode kemampuan mereduksi. Identifikasi asam galat, kafein, dan EGCG dilakukan dengan menggunakan Kromatografi Cair Kinerja Tinggi (KCKT). Data kadar fenolik total dan aktivitas antioksidan yang diperoleh dari penelitian dianalisa dengan menggunakan Rancangan Acak Kelompok (RAK) terdiri dari 4 perlakuan dan 6 kali ulangan dan uji Beda Nyata Jujur (BNJ) dengan tingkat kebermaknaan 5%. Hasil penelitian ini menunjukkan bahwa kadar fenolik total ampas teh hijau berturut-turut adalah EK > AFB > AFE = AFG. Aktivitas antioksidan ampas teh hijau berturut-turut adalah AFB > EK > AFE > AFG. Kandungan asam galat, kafein, dan EGCG tertinggi terdapat pada ekstrak kasar ampas teh hijau.
Keywords: fenolik total, aktivitas antioksidan, asam fenotat, teh hijau
PENDAHULUAN
Teh (Camellia sinensis) merupakan minuman penyegar yang sudah dikenal dengan luas di Indonesia dan di dunia. Aromanya yang harum serta rasanya yang khas membuat minuman ini banyak dikonsumsi. Teh merupakan minuman yang sangat bermanfaat bagi kesehatan tubuh. Teh akan meningkatkan sistem pertahanan biologis tubuh terhadap kanker, membantu penyembuhan penyakit (misalnya mencegah peningkatan kolesterol darah), dapat mengatur gerak fisik tubuh dengan mengaktifkan sistem saraf karena kandungan kafeinnya dan menghambat proses penuaan karena adanya senyawa katekin yang merupakan antioksidan kuat (Bambang, 2006).
Prospek ekonomi dari produk teh sangat besar untuk dikembangkan pada tahun-tahun mendatang karena Indonesia merupakan salah satu negara penghasil teh. Sebagai salah satu negara produsen, banyak perkebunan dan pabrik minuman teh yang ada di Indonesia. Di samping sebagai negara produsen teh, tentu negara ini juga menghasilkan limbah atau ampas teh baik dari produksi dan konsumsi teh itu sendiri. Dengan makin banyaknya produksi dan konsumsi teh di Indonesia, maka makin banyak pula limbah atau ampas teh yang dihasilkan. Selama ini, pemanfaatan ampas teh hanya digunakan sebagai pupuk kompos (Yuwono, 2009).
bahwa ampas teh masih mempunyai aktivitas antioksidan yang tinggi (Daniells, 2005). Hal tersebut menunjukkan bahwa ampas teh masih mengandung senyawa polifenol yang berpotensi untuk diolah menjadi sumber antioksidan alami. Dalam penelitian Zadernowski dkk. (2002), dengan metode fraksinasi asam fenolat senyawa polifenol dapat difraksinasi menjadi tiga fraksi asam fenolat yaitu asam fenolat bebas, asam fenolat ikatan ester, dan asam fenolat ikatan glikosida. Maka perlu adanya penelitian lebih lanjut untuk meneliti tentang kadar fenolik total dan aktivitas antioksidan dari tiga fraksi asam fenolat pada senyawa polifenol dalam ampas teh hijau, yaitu pada fraksi asam fenolat bebas, fraksi asam fenolat ikatan ester, dan fraksi asam fenolat ikatan glikosida.
BAHAN DAN METODE Bahan
Sampel yang digunakan adalah ampas teh hijau yang diperoleh dari PT. Coca-Cola Bottling Indonesia, Bawen, Jawa Tengah. Bahan-bahan kimia yang digunakan di antaranya adalah etanol 96%, Na2SO4, aquades, NaOH, HCl pekat, buffer fosfat, K4Fe(CN)6 (Merck), TCA, FeCl3, folin (100%, Merck), Na2CO3, asam galat (98+%, Sigma-Aldrich), eter, dan gas N2, NaHCO3,
Piranti
Piranti yang digunakan adalah neraca analitis (Mettler H80), oven, cawan petri, waterbath (Memmert), rotary evaporator (Buchi R-114), spektrofotometer UV-VIS (Shimadzu 1240), shaker (Kika Labortechnik KS501 digital), swing type centrifuge (Tomy Seiko Co., Ltd. model C-40N), piranti gelas, corong pisah, kertas saring, kertas tisu, aluminium foil, dan botol sampel.
Metoda
Ekstraksi sampel
25 gram sampel ampas teh hijau dimaserasi dengan pelarut etanol 50 % secara bertingkat (5 x 100 mL). Kemudian hasil maserasi disaring. Filtrat adalah ekstrak kasar dari ampas teh hijau.
Fraksinasi asam fenolat ekstrak kasar ampas teh hijau (Zadernowski dkk., 2002)
100 mL ekstrak kasar diasamkan dengan HCl 6 N hingga larutan pH 2. Larutan tersebut diekstraksi lima kali dengan dietil eter 1 : 1 (v/v) pada suhu ruang dengan corong pisah. Lapisan atas merupakan fraksi eter (Lapisan A), sedangkan lapisan bawah merupakan fraksi air (Lapisan B). Lapisan A digunakan untuk fraksi asam fenolat bebas. Lapisan B digunakan untuk fraksi asam fenolat ikatan ester dan asam fenolat ikatan glikosida.
Asam fenolat bebas
Lapisan A (fraksi eter) ditambahkan Na2SO4. Filtrat dipekatkan dengan rotary evaporator. diekstrak dengan dietil eter sebanyak 5 x 100 mL. Lapisan atas diambil dan diberi drying agent (Na2SO4). Filtrat dipekatkan dengan rotary evaporator. Lapisan bawah (lapisan C) adalah fraksi air digunakan untuk fraksinasi asam fenolat ikatan glikosida.
Asam fenolat ikatan glikosida
dietil eter sebanyak 5 x 100 mL. Lapisan atas diambil dan ditampung, kemudian diberi drying agent (Na2SO4). Filtrat dipekatkan dengan rotary evaporator.
Pemurnian asam fenolat (Zadernowski dkk., 2002)
Untuk pemurnian, fraksi asam fenolat bebas, asam fenolat ikatan ester, asam fenolat ikatan glikosida dilarutkan dalam 50 mL NaHCO3 5% (pH = 8), kemudian diekstrak dengan dietil eter sebanyak lima kali. Lapisan bawah (fraksi air) diasamkan dengan HCl 6 N hingga pH 2. Larutan tersebut diekstraksi lagi dengan dietil eter sebanyak lima kali. Lapisan atas (fraksi eter) diambil dan diuapkan dengan rotary evaporator sampai kering. Residu tersebut dilarutkan dengan etanol 50% dan digenapkan dengan labu takar 10 mL hingga garis tera (untuk sampel uji).
Pengukuran kadar fenolik total (Povilaityte and Venskutonis, 2000 dalam Lestario dkk, 2005)
1 mL sampel / ekstrak dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan 2 mL folin 10% dan 2,5 mL Na2CO3 7,5% ke dalam tabung tersebut, dan didiamkan selama 30 menit. Absorbansi dari masing-masing larutan diukur dengan menggunakan spektrofotometer UV-VIS pada panjang gelombang 765 nm Pengukuran absorbansi sampel dilakukan secara triplo. Sebagai blanko digunakan pelarut sampel untuk pengganti ekstrak, sedangkan sebagai standar digunakan larutan asam galat dengan berbagai konsentrasi.
Pengukuran aktivitas antioksidan metode kemampuan mereduksi (Lim dkk., 2006 yang dimodifikasi)
1 mL sampel / ekstrak dimasukkan ke dalam tabung reaksi, ditambah 2,5 mL buffer fosfat 0,2 M pH 6,6 dan 2,5 mL K3Fe(CN)6 1%. Campuran larutan diinkubasi pada suhu 50oC dalam waterbath selama 20 menit. Selanjutnya, larutan ditambah 2,5 mL TCA 10%. Kemudian, 2,5 mL dari bagian atas larutan atau supernatan diambil dan ditambah dengan
Analisa Kuantitatif Asam Galat, Kafein, dan EGCG (Martono, 2008)
Ekstrak kering dari ekstrak kasar, asam fenolat bebas, asam fenolat ester, dan asam fenolat glikosida ampas teh hijau dilarutkan ke dalam 5 mL pelarut (H3PO4 : H2O : asetonitril : metanol = 14 : 7 : 3 : 1 v/v/v/v). Kemudian masing-masing larutan disaring dengan filter 0,45 m. Sejumlah 60 L diinjeksikan ke dalam sistem KCKT. Kadar asam galat, kafein, dan EGCG ditentukan berdasarkan kurva baku yang didapat dari konsentrasi versus luas kromatogram. Kondisi Operasional KCKT adalah sebagai berikut :
Instrumen = KCKT Knaver GmBH – Model Smart Line Series
digunakan Beda Nyata Jujur (BNJ) dengan tingkat kebermaknaan 5%. Untuk KCKT (Kromatografi Cair Kinerja Tinggi) akan dianalisa secara deskriptif.
HASIL DAN DISKUSI
Kadar fenolik Total Fraksi fenolik Ampas Teh Hijau
Hasil penelitian Agustianingrum (2009) menunjukkan bahwa ampas teh masih mengandung polifenol. Dalam polifenol tumbuh-tumbuhan, terdapat asam fenolat baik dalam bentuk bebas maupun terikat. Dalam penelitian Zadernowski, dkk. (2002), dengan metode fraksinasi, asam fenolat senyawa polifenol dapat difraksinasi menjadi tiga fraksi asam fenolat yaitu asam fenolat bebas, asam fenolat ikatan ester, dan asam fenolat ikatan glikosida. Data asam fenolat yang diperoleh dari ekstrak kasar ampas teh hijau dengan cara difraksinasi dalam bentuk bebas dan terikat sesuai dengan prosedur dalam penelitian Zadernowski, dkk. (2002) dapat dilihat pada Tabel 1.
Tabel 1. Kadar fenolik Total (mg asam galat/g) dalam Berbagai Fraksi Fenolik Ampas Teh Hijau
Keterangan : AFG = Asam fenolat ikatan Glikosida AFE = Asam fenolat ikatan Ester AFB = Asam fenolat Bebas EK = Ekstrak kasar
Angka-angka yang diikuti oleh huruf yang sama menunjukkan antar perlakuan tidak berbeda nyata, sedangkan angka yang diikuti oleh huruf yang berbeda menunjukkan antar perlakuan berbeda nyata
Berdasarkan Tabel1. dapat diketahui bahwa kadar fenolik total tertinggi terdapat pada ekstrak kasar ampas teh hijau. Walaupun, kadar fenolik total pada AFB lebih rendah dari EK, tetapi lebih tinggi dari AFE dan AFG. Sedangkan, kadar fenolik total AFE sama dengan AFG. EK memiliki kadar fenolik total tertinggi karena polifenol dalam ampas teh hijau terekstrak dengan optimal pada pelarut etanol 50%. Dalam penelitian Agustianingrum (2009), ampas teh yang diekstraksi dengan pelarut etanol 50% menghasilkan kadar fenolik total tertinggi. AFB memiliki kadar fenolik total yang lebih tinggi dibanding AFE dan AFG karena dalam fraksi asam fenolat jumlah AFB secara alami lebih dominan (Zadernowski dkk., 2002). Kadar fenolik total AFE sama dengan AFG dimungkinkan karena keduanya memiliki komponen glikon yang sulit dilepaskan dari gugus glikosidanya.
Aktivitas Antioksidan Fraksi fenolik Ampas Teh Hijau
Data hasil pengukuran aktivitas antioksidan disajikan pada Tabel 2. Berdasarkan
Tabel2. dapat diketahui bahwa aktivitas antioksidan tertinggi terdapat pada AFB. Aktivitas antioksidan pada EK lebih rendah dari AFB, tetapi lebih tinggi dari AFE dan AFG. Data
Kadar fenolik Total
AFG AFE AFB EK
purata 2,9857 3,1744 4,6106 6,3036
± SE 0,2379 0,3054 0,4181 0,3423
BNJ 5% a a b c
hasil pengukuran juga menunjukkan bahwa aktivitas antioksidan AFE lebih tinggi daripada AFG.
Tabel 2. Aktivitas Antioksidan (mek/gram) dalam Berbagai Fraksi Fenolik Ampas Teh Hijau
Keterangan : sama dengan Tabel 1.
Walaupun kadar fenolik total EK lebih tinggi dibanding AFB, tetapi aktivitas antioksidan AFB lebih tinggi dibanding EK. Pada proses fraksinasi AFB, komponen utama yang terekstraksi adalah komponen aglikon (flavonoid yang tidak terikat dengan gula) yang memiliki aktivitas antioksidan lebih tinggi dibandingkan komponen glikon (flavonoid yang terikat dengan gula) (Fleury dkk., 1992 dalam Huang dkk.,1992) sehingga aktivitas antioksidan AFB lebih tinggi dibanding fraksi fenolik lainnya. Hal ini menunjukkan bahwa aktivitas antioksidan tidak selalu bergantung pada kadar fenolik total, jenis komponen kimia pun dapat mempengaruhi besar aktivitas antioksidan suatu senyawa. EK memiliki aktivitas antioksidan lebih tinggi dibanding AFE dan AFG karena jumlah komponen glikon EK lebih tinggi dari dua asam fenolat tersebut. Aktivitas antioksidan pada AFG paling rendah karena AFG merupakan flavonoid yang terikat dengan gula yang kekurangan 3 hidroksil bebas pada cincin C (karbon) sehingga kemampuan untuk mendonorkan atom hidrogennya berkurang (Sibuea, 2004).
Identifikasi Kuantitatif Asam Galat, Kafein, dan EGCG Fraksi fenolik Ampas Teh hijau dengan Metode KCKT
Dari penelitian ini diperoleh hasil bahwa kadar fenolik total tertinggi terdapat pada fraksi ekstrak kasar, sedangkan aktivitas antioksidan tertinggi terdapat pada fraksi asam fenolat bebas. Hasil pengukuran kadar asam galat, kafein, dan EGCG pada ekstrak kasar (EK), asam fenolat bebas (AFB), asam fenolat ikatan ester (AFE), asam fenolat ikatan glikosida (AFG) ampas teh hijau dengan metode Kromatografi Cair Kinerja Tinggi (KCKT) dapat dilihat pada Tabel 3.
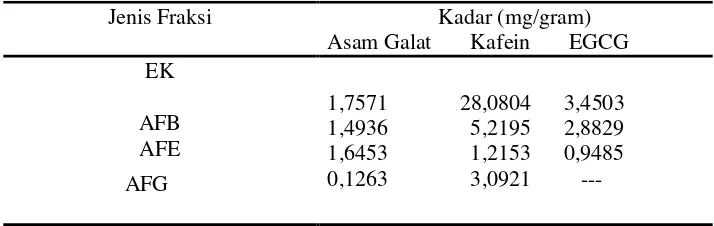
Tabel 3. Hasil Uji Kadar Asam Galat, Kafein, EGCG (mg/gram) dengan KCKT
Pada Tabel 3. terlihat bahwa kandungan asam galat, kafein, dan EGCG tertinggi terdapat pada EK ampas teh hijau. Pada AFB, kandungan EGCG lebih besar dibanding
Aktivitas antioksidan
AFG AFE EK AFB
purata 0,3518 0,4308 0,7708 0,8812
± SE 0,0273 0,0404 0,0357 0,0566
BNJ 5% a b c d
W = 0,0685
Jenis Fraksi Kadar (mg/gram)
Asam Galat Kafein EGCG EK
1,7571 28,0804 3,4503 1,4936 5,2195 2,8829 1,6453 1,2153 0,9485 0,1263 3,0921 --- AFB
AFE
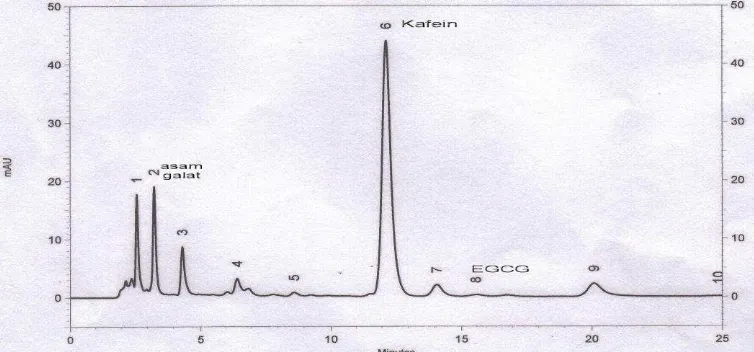
asam galat. Pada AFE, kandungan asam galat lebih besar dibanding EGCG. Sedangkan pada AFG hanya terdapat asam galat dan kafein. Kadar kafein menurun setelah EK difraksinasi dikarenakan kafein terbuang bersama lemak pada saat pemurnian AFB, AFE, dan AFG. Selain kromatogram asam galat, EGCG, dan kafein ternyata pada fraksi EK, AFB, AFE, dan AFG terdapat kromatogram senyawa lainnya yang belum diidentifikasi. Di bawah ini terdapat gambar hasil uji identifikasi asam galat, kafein, dan EGCG pada EK, AFB, AFE, dan AFG.
Gambar 6. Kromatogram hasil identifikasi senyawa asam galat, kafein dan epigalokatekin galat dalam EK
KESIMPULAN
Berdasarkan hasil penelitian, dapat disimpulkan bahwa kadar fenolik total ampas teh hijau mengikuti urutan sebagai berikut EK tertinggi diikuti AFB, sedangkan AFE sama dengan AFG. Aktivitas antioksidan ampas teh hijau mengikuti urutan sebagai berikut AFB tertinggi diikuti EK, AFE, lalu AFG. Hasil identifikasi menunjukkan bahwa baik EK, AFB, maupun AFE mengandung senyawa asam galat, kafein, dan EGCG dimana kandungan terbesar senyawa-senyawa tersebut terdapat pada EK. Sebaliknya, AFG hanya mengandung senyawa asam galat dan kafein.
DAFTAR PUSTAKA
Agustianingrum, N., 2009. Aktivitas Antioksidan, Kadar fenolik Total dan Epigalokatekin Galat Pada Ampas Teh dari Industri Teh di Daerah Ungaran. Skripsi Program Studi Kimia Fakultas Sains dan Matematika. Universitas Kristen Satya Wacana, Salatiga. Anonim, 2008. Poliphenols. http://www.alexis-biochemicals.com (12/4/10)
Bambang, Kustamiyanti, 2006. Prospek Teh Indonesia Sebagai Minuman Fungsional. http://www.ipard.com/art_perkebun/Aug02-06_kb.asp (18/7/09)
Daniells, S., 2005. Tea Waste Rich With Extractable Antioxidants.
http://www.nutraingredients.com/news/ng.asp?id=64274-green-tea-antioxidant-black-tea (5/12/08)
Huang, M. T., C. T. Ho., dan C. Y. Lee. 1992. Phenolic Compounds In Food And Their Effects On Health II : Antioxidants and Cancer Prevention. American Chemical Society Symposium Series 507 : Washington D.C.
Lim Y. Y., T. T. Lim, dan J. J. Tee, 2006. Antioxidant Properties of Guava Fruit : Comparison With Some Local Fruits. Sunway Academic Journal 3 : 9 – 20.
Lestario, L.N., Pudji Hastuti, Sri Raharjo, dan Tranggono, 2005. Sifat Antioksidatif Ekstrak Buah Duwet (Syzygium cumini). Agritech 25 (1) : 24 - 31.
Martono, Y. 2008. Validasi Metode Kromatografi Cair Kinerja Tinggi Untuk Penetapan Kadar Asam Galat, Kafein, dan Epigalokatekin Galat Pada Berbagai Produk Teh Celup. Thesis. Universitas Gajah Mada, Yogyakarta.
Sibuea, Posman, 2004. Kuersetin.
http://kulinerkita.multiply.com/reviews/item/886 (12/4/10) Yuwono, Rony, 2009. Ampas Teh pun Bisa Menjadi Kompos.
http://suaramerdeka.com/v1/index.php/read/cetak/2009/07/11/71948/Ampas.Teh.pun.Bis a.Menjadi.Kompos (18/7/09)
Zadernowski, R., M. Naczk, and H. Nowak-Polakowska, 2002. Phenolic Acids of Borage
(Borago officinalis L.) and Evening Primrose (Oenothera biennis L.). Paper no. J10057