DENSITY FUNCTIONAL THEORY UNTUK PENENTUAN
GEOMETRI DAN KARAKTERISTIK IKATAN DARI
KOMPLEKS Ni(II)-DIBUTILDITIOKARBAMAT
DAN Co(II)-DIBUTILDITIOKARBAMAT
Pongajow, N.T.,
1Juliandri
2dan Hastiawan, I.
31Pascasarjana Unpad, Jl. Dipati Ukur No 35, Bandung , 40132
2Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Padjadjaran,
Jl. Raya Bandung – Sumedang Km.21 Jatinagor e-mail : nicolinpongajow@yahoo.com
ABSTRAK
DENSITY FUNCTIONAL THEORY UNTUK PENETUAN GEOMETRI DAN
KARAKTERISTIK IKATAN DARI KOMPLEKS Ni(II)-DIBUTILDITIOKARBAMAT DAN Co(II)-DIBUTILDITIOKARBAMAT.DFT merupakan salah satu metode komputasi yang digunakan untuk perhitungan kimia.Metode ini memudahkan kimiawan untuk meramalkan struktur dan karakteristik dari suatu senyawa. Dalam penelitian ini akan ditentukan geometri dan karaktersitik ikatan dari senyawa kompleks Ni(II)-dibutilditiokarbamat dan Co(II)-dibutilditiokarbamat menggunakan metode DFT dengan fungsi B3LYP dan B3PW91. Basis set yang akan digunakan adalah LANL2DZ dan perangkat lunak Gaussian 03W.Hasil optimasi geometrimenunjukkan bentuk struktur yang sama dengan data pembanding Ni(II)-dietilditiokarbamat, yaitu persegi planar. Keterisian elektron pada ikatan Ni – S adalah 1,8873 elektron, yang merupakan 20,24 % elektron dari Ni dan 79,76 % dari S. Untuk ikatan Co – S, keterisian elektronnya adalah 1,8971 elektron dengan kontribusi elektron dari Co adalah 19,43% dan S adalah 80,57%. Bentuk geometri persergi planar dibuktikan dengan hasil analisis NBO yang menunjukkan hibridisasi Ni(II)-dibutilditiokarbamat adalah d1,05sp2.05dan Co(II)-dibutilditiokarbamat
adalah d1,04sp2,04.
Kata kunci: DFT,dibutilditiokarbamat, geometri, karakteristik ikatan, senyawa kompleks
ABSTRACT
DENSITY FUNCTIONAL THEORY FOR GEOMETRY CALCULATION AND BOND
CHARACTERIZATION OF Ni(II)-DIBUTYLDITHIOCARBAMATE AND
Co(II)-DIBUTYLDITHIOCARBAMATE.Density Functional Theory (DFT)is one of computational method that used for chemical calculation. This method helps chemist to predict structure and bonding characters of complex compounds. In this study the geometriesandbond charactersofNi(II)-dibutyldithiocarbamate and Co(II)-charactersofNi(II)-dibutyldithiocarbamate complex compoundswill be determined. The functions used in this study areB3LYPandB3PW9. All calculations were performed at LANL2DZlevel of
basis set as implemented in Gaussian03W.The geometries ofCo(II)-, and
Ni(II)-dibutyldithiocarbamateshow a similarity to theexperimentalsquare-planar Ni(II)-dietyldithiocarbamate. The electronic occupation of Ni–S molecular orbital is 1.8873 electrons, with 20.24% and 79.76% contribution from Ni and S respectively. For the Co–Smolecular orbital, the electronic occupation is 1.8971, with 19.43% and 80.57% contibution from Co and Srespectively. Square-planar geometrieswere proved by NBO analysis that produce the hybridization of Ni(II)-dibutyldithiocarbamateand Co(II)-dibutyldithiocarbamateared1.05sp2.05and d1.04sp2.04respectively.
1. PENDAHULUAN
Senyawa ditiokarbamat memiliki berbagai kegunaan baik dalam industri maupun di laboratorium. Salah satu kegunaan dari senyawa ini adalah bisa bereaksi sebagai ligan sehingga bisa digunakan dalam pemisahan suatu logam. Untuk mendapatkan hasil yang baik dalam pemisahan maka karakteristik dari ligan yang akan digunakan juga harus diketahui.
Perkembangan teori mekanika kuatum, telah memberi kemudahan bagi kimiawan untuk memprediksi sifat-sifat dari suatu senyawa dengan hasil yang akurat. Untuk melakukan prediksi terhadap suatu senyawa, saat ini telah berkembang suatu cabang baru dalam ilmu kimia yang dikenal dengan istilah kimia komputasi. Penggunaan kimia komputasi memberikan kemudahan kepada kimiawan karena bisa menghitung suatu senyawa yang bersifat kompleks dan meramalkan sifat dari senyawa tersebut.
Salah satu metode yang digunakan dalam perhitungan komputasi adalah metode Density Functional Theory (DFT). DFT adalah cara cerdas untuk menyelesaikan persamaan Schrodinger untuk sistem banyak-partikel [1]. Dasar pemikiran dari metode ini adalah energi dari suatu molekul dapat ditentukan dari kerapatan elektron dari molekul tersebut [2].Dalam metode ini tidak menghitung elektron secara keseluruhan karena cara perhitungannya berdasarkan kerapatan elektronnya. Penggunaan metode ini memberikan kemudahan karena bisa menghitung dengan hasil yang mendekati eksperimen dan tidak membutuhkan waktu yang cukup lama.
Beberapa penelitian terdahulu yang telah berhasil dengan penggunaan metode DFT diantaranya adalah : penentuan geometri pada senyawa Zn-dibutilditiokarbamat [3], penentuan distribusi muatan dan karakteristik ikatan pada senyawa kompleks Co-dietilditiokarbamat dan Ni-dietilditiokarbamat [4], serta memprediksi energi dan geometri senyawa [5].
Dalam penelitian ini, peneliti akan melakukan suatu kajian tentang senyawa kompleks Co-dibutilditiokarbamat dan Ni dibutilditiokarbamat dalam penentuan geometri dan karakterisasi yang dimiliki dari kedua kompleks ini. Keadaan geometri bisa mempengaruhi sifat-sifat fisis dan kimia dari suatu senyawa.
Diharapkan dengan adanya informasi tentang geometri dari senyawa Co-dibutilditiokarbamat dan Ni-dibutilditiokarbamat dapat membantu kimiawan
dalam penggunaan senyawa ini baik di laboratorium maupun dunia industri.
2. TEORI
Metode DFT umum digunakan untuk optimasi geometri dan stuktur elektron kompleks logam transisi. Metode ini cukup akurat, mudah digunakan, dan cukup cepat untuk mempelajari molekul yang relatif besar dari kompleks logam transisi. Keakuratan perhitungan DFT dapat diuji dengan cara mencocokkan data perhitungannya dengan data eksperimen, seperti data XRD, UV-Vis, FTIR, dan NMR [6]. Metode ini telah menjadi metode pilihan untuk senyawa logam transisi [7].
Dalam perhitungan komputasi dengan metode DFT diperlukan suatu fungsi/fungsional yang merupakan pendekatan dari beberapa teori dalam perhitungan komputasi. Beberapa fungsi yang sering digunakan dalam penelitian adalah B3LYP, B3PW91, BLYP, HFS, VWN, G96, P86, B96 dan B3P86 [2].
B3LYP dan B3PW91 disebut juga sebagai fungsi Hybrid karena merupakan hasil kombinasi perkiraan Hartree-Fock dengan pertukaran energi dan perkiraan DFT dengan pertukaran energi, semuanya dikombinasikan dalam fungsional yang meliputi korelasi elektron. Berikut ini adalah persamaan dari metode Hybrid B3LYP [8]:
(1) dengan a, b, dan c adalah konstanta semiempiris dengan nilai a = ~ 0,2; b = ~ 0,7 dan c = ~ 0,8. Fungsional B3PW91 menunjukkan penggunaan dari tiga-parameter, dan juga pertukaran GGA dan fungsi korelasi B dan PW91, dengan persamaan sebagai berikut [9] :
(2) dimana a, b, dan c masing-masing adalah 0,20; 0,72, dan 0,81.
Untuk perhitungan elektron, diperlukan adanya fungsi basis yang telah memiliki nilai koefisien di dalamnya. Dalam penelitian ini, LANL2DZ bisa digunakan sebagai fungsi basis untuk senyawa kompleks yang akan dikaji. LANL2DZ cocok digunakan untuk kompleks Ni-dibutilditiokarbamat dan Co-dibutilditiokarbamat karena termasuk kompleks
dengan sistem banyak-elektron. Fungsi basis LANL2DZ hanya akan menghitung elektron valensi dari masing-masing atom saja sehingga tidak memerlukan waktu komputasi yang lama tapi bisa memberikan hasil yang mendekati data percobaan.
3. TATA KERJA (BAHAN DAN METODE) Perangkat lunak yang akan digunakan yaitu Gaussian 03W [10] untuk melakukan optimasi geometri dan perhitungan frekuensi. Metode komputasi yang digunakan adalah DFT dengan fungsi B3LYP (Becke, 1993) dan B3PW91 pada basis set LANL2DZ [11]. B3LYP adalah Fungsional hybrid yang dikemukakan Becke. B3PW91 adalah fungsi hybrid tiga paramete Becke dan fungsi korelasi gradien terkoreksi PW91 [12]. Basis set LANL2DZ diaplikasikan untuk atom H, Li-La, Hf-Bi.
Tahapan percobaan meliputi : pemodelan struktur dengan perangkat lunak Gauss View, dibuat input pada Gaussian 03W dengan basis set LANL2DZ untuk masing-masing metode yaitu B3LYP dan B3PW91, proses perhitungan, diperoleh data hasil perhitungan, dibandingkan dengan data pembanding untuk analisis data. Data pembanding yang digunakan yaitu Ni(II)-dietilditiokarbamat [4]. Tujuannya untuk validasi metode yang digunakan. Untuk mendapatkan karakterisasi ikatan digunakan analisis Natural Bond Orbital [13].
4. HASIL DAN PEMBAHASAN 4.1 Molekul Ni(II)-dietilditiokarbamat
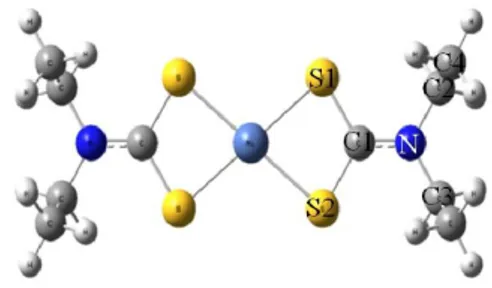
Untuk mendapatkan keakuratan hasil perhitungan dan validasi metode yang digunakan maka dibuat pemodelan untuk senyawa Ni(II)-dietilditiokarbamat guna dibandingkan dengan data ekperimen. Gambar 1. berikut ini adalah hasil optimasi geometri yang diperoleh dengan metode komputasi. Hasil optimasi geometri menunjukkan bentuk struktur senyawa Ni(II)-dietilditiokarbamat adalah persegi planar. Bentuk struktur ini sesuai dengan geometri pada data eksperimen yaitu persegi planar. Berikut ini adalah tabel perbandingan data hasil perhitungan secara ekperimen dengan komputasi. (Tabel 1.)
Perbandingan panjang ikatan Ni(II)-dietilditiokarbamat singlet secara komputasi dan ekperimen menunjukkan hasil yang baik dengan selisih panjang ikatan 0,1 Å dan sudut ikatan
sekitar 0,1 – 0,2 . Misalnya panjang ikatan Ni – S1 hasil perhitungan komputasi adalah 2.3194 Å (B3LYP); 2.3011 Å (B3PW91); dan2.3362 Å (BLYP) sedangkan data eksperimen adalah 2.2011 Å.
Gambar 1. Ni(II)-dietilditiokarbamatsinglet
Tabel 1. Panjang ikatan dan sudut ikatan dari Ni(II)-dietilditiokarbamat singlet Panjang Ikatan (Å) dan Sudut Ikatan (◦) Eksperimen Komputasi B3LYP B3PW91 Ni – S1 2,201 2,319 2,301 S2 – C1 1,723 1,787 1,779 C1 – N 1,318 1,346 1,343 N – C2 1,475 1,491 1,484 C2 – C4 1,512 1,542 1,536 S1–Ni–S2 79,55 79,48 79,81 Ni–S1–C1 85,33 84,21 84,03 S1–C1–N 124,9 123,9 123,9 C1–N–C2 121,2 120,9 120,7 C2–N–C3 117,4 118,1 118,6 C1–N–C3 121,3 120,9 120,7
Sudut ikatan S1–Ni–S2 dari data eksperimen adalah 79,55 sedangkan data perhitungan komputasi adalah 79,48 (B3LYP), 79,81 (B3PW91) dan 79,27 (BLYP). Adanya selisih panjang dan sudut ikatan ini diperkirakan karena perbedaan wujud zat dari senyawa kompleks yang disimulasi secara komputasi dengan eksperimen di laboratorium. Dalam simulasi komputasi, kompleks dianggap dalam wujud gas sedangkan dalam eksperimen laboratorium kompleks tersebut dalam bentuk padatan.
Selisih panjang dan sudut ikatan yang diperoleh tidak menunjukkan perbedaan yang signifikan sehingga bisa dikatakan metode DFT dengan fungsi B3LYP, B3PW91 dan BLYP bisa digunakan untuk optimasi geometri pada senyawa kompleks yang akan dikaji.
4.2 Geometri senyawa Ni(II)-dibutilditiokarbamat
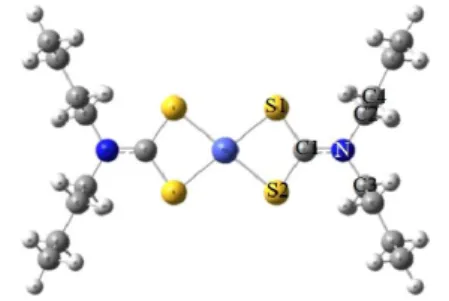
Bentuk geometri yang diperoleh untuk senyawa kompleks Ni(II)-dibutilditiokarbamat dalam keadaan singlet adalah persegi planar. Bentuk persegi planar menunjukkan bahwa orbital hibrida yang digunakan dalam pembentukan kompleks adalah dsp2.
Gambar 2. Ni(II)-dibutilditiokarbamatsinglet
Berikut ini adalah tabel hasil perhitungan panjang dan sudut ikatan dari kompleks ini.
Tabel 2. Panjang ikatan dan sudut ikatan dari Ni(II)-dibutilditiokarbamat singlet PanjangIkatan(Å) dan Sudut Ikatan (o) MetodeKomputasi B3LYP B3PW91 Ni – S1 2,319 2,300 S2 – C1 1,788 1,779 C1 – N 1,345 1,342 N – C2 1,489 1,482 C2 – C4 1,545 1,539 S1–Ni–S2 79,49 79,83 Ni–S1–C1 84,21 84,03 S1–C1–N 123,96 123,95 C1–N–C2 120,90 120,67 C2–N–C3 118,18 118,65 C1–N–C3 120,91 120,68
Hasil perhitungan komputasi untuk senyawa kompleks Ni(II)-dibutilditiokarbamat dengan Ni(II)-dietilditiokarbamat menunjukkan hasil yang hampir sama. Misalnya panjang ikatan Ni– S1 untuk kompleks Ni-dibutilditiokarbamat singlet dengan metode B3LYP diperoleh hasil 2,319 Å dan untuk Ni(II)-dietilditiokarbamat singlet adalah 2,319 Å. Sudut ikatan S1–Ni–S2 untuk Ni(II)-dibutilditiokarbamat singlet adalah 79,49 sedangkan untuk Ni(II)-dietilditiokarbamat singlet adalah 79,48 . Perbandingan dengan data eksperimen juga
tidak menunjukkan perbedaan yang signifikan meskipun rantai alkilnya berbeda tapi bentuk geometrinya sama yaitu persegi planar.
4.3 Geometri senyawa Co(II)-dibutilditiokarbamat
Hasil optimasi geometri menunjukkan bentuk struktur persegi planar untuk senyawa
kompleks
Co(II)-dibutilditiokarbamatdoublet.Orbital hibrida yang digunakan dalam pembentukan kompleks adalah dsp2. Dari hasil ini dapat diamati adanya
kesamaan bentuk geometri antara senyawa Co(II)-dibutilditiokarbamat dengan Ni(II)-dibutilditiokarbamat. Bentuk geometri yang sama ini diduga karena atom pusat Co dan Ni memiliki sifat yang sama. Hal ini dilatarbelakangi oleh bilangan oksidasi yang dimiliki atom Co dan Ni adalah sama-sama +2 dan +3 sehingga memungkinkan diperolehnya bentuk geometri yang sama.
Gambar 3. Co(II)-dibutilditiokarbamatdoublet Berikut ini adalah tabel hasil perhitungan panjang dan sudut ikatan untuk kompleks ini.
Tabel 3. Panjang ikatan dan sudut ikatan dari Co(II)-dibutilditiokarbamat doublet PanjangIkatan(Å), Sudut Ikatan (o) Komputasi B3LYP B3PW91 Co – S1 2,334 2,315 S2 – C1 1,789 1,781 C1 – N 1,346 1,343 N – C2 1,490 1,482 C2 – C4 1,545 1,539 S1 – Co – S2 79,03 79,36 Co – S1 – C1 84,37 84,21 S1 – C1 – N 123,88 123,89 C1 – N – C2 120,93 120,70 C2 – N – C3 118,13 118,59 C1 – N – C3 120,93 120,70
antara Co(II)-dibutilditiokarbamat dan Ni(II)-dibutilditiokarbamat menunjukkan hasil yang hampir sama baik metode B3LYP dan B3PW91. Hasil ini juga membuktikan akan kemiripan sifat yang dimiliki antara atom pusat Co dan Ni. 4.4 Karakteristik Ikatan
Keterisian elektron pada ikatan Ni-S senyawa kompleks Ni(II)-dibutilditiokarbamat (singlet) dianalisis dengan NBO (Natural Bond Orbital). Hasil analisis menunjukkan bahwa keterisian elektron dalam pada ikatan Ni – S adalah 1,8873 elektron dimana atom Ni menyumbangkan elektron sebesar 20,24 % dan atom S sebesar 79,76 % elektron. Untuk senyawa Co(II)-dibutilditiokarbamat, keterisian elektron pada ikatan Co – S adalah 1,8971 elektron dengan kontribusi elektron dari Co adalah 19,43% dan S adalah 80,57%.
Hasil analisis ini membuktikan bahwa atom pusat juga memiliki kontribusi dalam pembentukan kompleks. Elektron yang berikatan tidak hanya berasal dari ligan saja tetapi juga dari atom pusat. Adanya kontribusi dari atom pusat dalam pembentukan kompleks juga dibuktikan dengan perubahan muatan pada atom pusat dari Ni2+ menjadi Ni0,02+ dan untuk
Co2+ berubah menjadi Co0,01+.
Hasil analisis NBO juga membuktikan hibridisasi yang terjadi pada kompleks Ni(II)-dibutilditiokarbamat singlet adalah d1,05sp2,05 dan
untuk kompleks Co(II)-dibutilditiokarbamat singlet adalah d1,04sp2,04.
5. KESIMPULAN
Perhitungan komputasi dengan metode DFT telah berhasil digunakan dalam penentuan geometri dan karakteristik ikatan pada kompleks logam Ni(II)-dibutilditiokarbamat singlet dan Co(II)-dibutilditiokarbamat doublet. Hasil optimasi geometri menunjukkan bahwa kedua kompleks ini memiliki bentuk geometri persegi planar. Hibridisasi yang terbentuk adalah d1,05sp2.05 untuk Ni(II)-dibutilditiokarbamat dan
d1,04sp2.04 untuk Co(II)-dibutilditiokarbamat
yang juga dibuktikan dengan analisis NBO. Dalam pembentukkan kompleks, ternyata atom pusat juga memberikan kontribusi elektron ketika berikatan. Hal ini dibuktikan secara komputasi dengan perubahan muatan yang terjadi pada atom pusat.
6. DAFTAR PUSTAKA
1. FIOLHAIS, C.,NOGUEIRA, F. and MARQUES, M., A Primer in Density Functional Theory, Springer, Germany (2002).
2. YOUNG, D.C., Computational Chemistry : A Practical Guide for ApplyingTechniquesto Real-WorldProblems, Wiley & Sons, Inc. New York (2001).
3. KHOTIB, M., Tesis, Jurusan Kimia, Tesis, Institus Pertanian Bogor, Bogor (2010) 4. LEE, C.R., TAN, L.Y. dan WANG, Y.
Charge density distribution and bond characterization of metal dialkyldithiocarbamate complexes (M = Co,Ni). J.Phy.Chem.Solids 62.613-1628. (2001).
5. LI, QIAN-SHU., XU, XIU-DONG., ZHANG, S. Predicting energies and geometries for reactions involved in atmosphere chemistry: a comparison study between hybrid DFT methods. J. Chem.Phy Letters 384, 20-24. (2003).
6. SUNARTO, Y.N., Tesis, Jurusan Kimia, ITB, Bandung (2012)
7. TROMBA and HAMBLEY., Molecular Modeling of Inorganic Compounds, Wiley-VHC, Germany (2001).
8. JENSEN, F., Introduction to Computational Chemistry, Wiley& Sons , Chicester (2007).
9. Cramer, C. J., Essentials of Computational Chemistry, John Wiley and Sons, Chicester (2004).
10. FRISCH, M. J., G. W. TRUCKS, H. B. SCHLEGEL, G. E. SCUSERIA, M. A. ROBB, J. R. CHEESEMAN, V. G. ZAKREWSKI, J. A. MONTGOMERY, Jr., R. E. STARTMANN, J. C. BURATN, S. DAPPRICH, J. M. MILLAM, A. D. DANIELS, K. N. KUDIN, M. C. STRAIN, O. FARKAS, J. TOMASI, V. BARONE, M.COSSI, R. CAMMI, B. MENUCCI, C. POMELLI, C. ADAMO, S. CLIFFORD, J. OCHTERSKI, G. A. PETERSSON, P. Y. AYALA, Q. CUI, K. MOROKUMA, D. K. MALICK, A. D. RABUCK, K. RAGHAVACHARI, J. B. FORESMAN, J. CIOSLOWSKI, J. V. ORTIS, A. G. BABOUL, B. B. STEFANOV, G. LIU, A. LIASHENKO, P. PISKORZ, I. KOMAROMI, R. GOMPERTS, R. L. MARTIN, D. J. FOX, T. KEITH, M. Al-LAHAM, C. Y.
PENG, A. NAYAKKARA, C.
M. W. GILL, B. JOHNSON, W. CHEN, M. W. WONG, J. L. ANDREAS, C. GONZALES, M. HEAD-GORDON, E. S. REPLOGE and J. A. POPLE.Gausian 03Rev, E.01., Gausian, Inc., Pittsburgh (2003).
11. HAY, P. J andWADT, W. R. J. Chem. Phys.82, 270 (1985).
12. PERDEW, J. P., BURKE, K., andWANG, Y.,Phys. Rev. B54, 16533 (1996).
13. REED, A.E., CARPENTER, J.E., WEINHOLD, F., NBO version 3.1.
DISKUSI Aan Harvian:
Apa tidak lebih baik penggunaan XAR? Nicolin Tirza Pongajow: