III
BAHAN DAN METODE PENELITIAN
3.1 Bahan Penelitian
3.1.1 Bahan Pakan Biji Sorgum
Bahan pakan yang digunakan dalam penelitian ini adalah biji sorgum (Sorghum bicolor) dengan tipe grain sorghum sebanyak 5 kg dengan umur panen yang sama yaitu sekitar 4 bulan. Biji sorgum ini diperoleh dari PD. Mustofa. Pasar burung Sukahaji Los D No. 73-74,79-80 Jl. Peta Lingkar Selatan. Bandung.
3.1.2 Larutan NaOH
Larutan NaOH yang digunakan untuk merendam biji sorgum yaitu larutan NaOH 0,1 N. Larutan NaOH ini digunakan untuk merendam biji sorgum sesuai dengan konsentrasi yang telah ditentukan.
3.1.3 Cairan Rumen
Cairan rumen yang digunakan berasal dari rumen sapi perah dengan kisaran umur 10-12 bulan yang dipotong di rumah potong hewan Pangalengan, Bandung. Pengambilan cairan rumen dalam keadaan anaerob dengan suhu 39-40°C sampai pada saat perlakuan (in vitro).
3.1.4 Saliva Buatan
Larutan saliva digunakan sebagai medium buffer untuk menyesuaikan kondisi seperti dalam rumen yang sesungguhnya. Larutan ini digunakan sebagai media pertumbuhan dan perkembangan mikroba rumen (in vitro). Pembuatan larutan media mengacu pada metode Mc. Dougall (1948).
3.1.5 Gas karbondioksida (CO2)
Gas karbondioksida (CO2) digunakan saat campuran cairan rumen dan saliva buatan dimasukan ke dalam tabung fermentor. Pengunaan CO2 yaitu untuk membuat suasana dalam tabung fermentor menjadi anaerob.
3.1.6 Zat Kimia
Zat kimia yang digunakan terdiri atas dua macam berdasarkan kegunaan. Yakni mengukur produksi amonia (NH3 ) dan mengukur produksi Volatile Fatty
Acid (VFA).
1) Zat kimia untuk mengukur produksi dari amonia (NH3 ) antara lain: H2SO4 0,005 N; NaOH jenuh; dan asam borat.
2) Zat kimia untuk mengukur produksi Volatile Fatty Acid (VFA) antara lain: H2SO4 15%; HCL 0,5 N; dan indikator PP (Phenolpthalen).
3.1.7 Pembuatan larutan NaOH 0,1 N
1) Menghitung kebutuhan NaOH yang akan dilarutkan dengan rumus N =𝑚𝑎𝑠𝑠𝑎 𝑀𝑟 x 1000 𝑣𝑜𝑙𝑢𝑚𝑒 0,1=𝑚𝑎𝑠𝑠𝑎 40 x 1000 1000 Massa = 4 gram
2) Mentimbang NaOH sebanyak 40 gram kemudian masukan dalam gelas piala
3) larutkan dengan aquadest dan tunggu sampai dingin
4) memasukan larutan NaOH ke dalam labu takar ukuran 1000 ml dan tambahkan aquadest sampai tanda batas.
3.2 Peralatan Penelitian
3.2.1 Peralatan Pengolahan Biji Sorgum Secara Kimia
1) Cup plastik, digunakan sebagai tempat perendaman biji sorgum dengan NaOH.
2) Batang pengaduk, digunakan untuk mengaduk larutan NaOH dengan biji sorgum.
3.2.2 Peralatan Pengambilan Sampel
1) Timbangan digital merk sartorius dengan ketelitian 0,001; digunakan untuk menimbang berat sampel.
2) Plastik, digunakan untuk menyimpan sampel yang telah dikeringkan. 3) Label, digunakan untuk memberi nama atau menandai sampel.
3.2.3 Peralatan Pengambilan Cairan Rumen
1) Termos berisikan air hangat dengan suhu 39-40 °C, digunakan untuk mempertahankan kondisi hangat pada saat cairan rumen dimasukan ke dalam termos agar mikroba rumen dapat tetap hidup.
2) Corong, berfungsi untuk memudahkan dalam memasukan cairan rumen kedalam termos.
3) Kain saring jenis muslin, berfungsi untuk menyaring cairan rumen agar residu rumen tidak ikut terbawa.
3.2.4 Peralatan Untuk Uji in vitro
1) Tabung fermentor, berfungsi sebagai wadah untuk proses fermentasi. 2) Waterbath yang digunakan untuk inkubasi rumen dilengkapi termostat
3) Rak tabung, sebagai tempat penyimpanan tabung-tabung kimia.
4) Alat sentrifugasi, berfungsi untuk memisahkan antara residu dengan cairan rumen.
5) Tabung plastik kapasitas 30 ml, untuk menyimpan supernatan hasil dari sentrifugasi. Supernatan ini disiapkan untuk analisis NH3 dan VFA. 6) Corong, berfungsi untuk memudahkan dalam memasukan cairan rumen
kedalam tabung kimia.
7) Gas CO2, digunakan pada tabung fermentor agar kondisi didalam tabung tetap dipertahankan dalam kondisi anaerob.
3.2.5 Peralatan Untuk Analisis NH3
1) Pipet, berfungsi untuk mengambil supernatan yang akan dianalisis serta meneteskan larutan NaOH dan asam borat.
2) Cawan conway, berfungsi untuk mengukur konsentrasi NH3.
3) Buret, berfungsi sebagai sarana untuk mentitrasi hasil analisa pada cawan conway.
3.2.6 Peralatan Untuk Analisa VFA
1) Pipet, berfungsi untuk mengambil supernatan yang akan dianalisis serta meneteskan larutan indikator phenolplalen.
2) Seperangkat tabung destilasi sebagai tempat penyulingan uap dan sampel yang dianalisis. Kelengkapan alat tersebut meliputi tabung destilasi, pendingin, erlemeyer sebagai penampung uap dan NaOH, stireer sebagai pengaduk, serta kompor gas.
3.3 Metode Penelitian
3.3.1 Perendaman Biji Sorgum dengan NaOH
1) Menyiakan bahan dan peralatan yang akan digunakan. 2) Memasukan Sampel biji Sorgum kedalam cup plastik.
3) Memasukan larutan NaOH dengan dosis yang telah ditentukan.
4) Menunggu perendaman biji shorgum dengan larutan NaOH pada waktu yang telah ditentukan.
5) Membuang larutan NaOH pada biji sorgum yang terdapat pada cup plastik kemudian dibilas dengan air.
7) Mengeringkan biji sorgum. 3.3.2. Pengambilan Cairan Rumen
1) Termos yang diberi air panas disiapkan terlebih dahulu dengan suhu 39-40°C yang bertujuan untuk mempertahankan kondisi dalam termos agar saat mikroba rumen masuk tidak mati.
2) Saluran pencernaan sapi perah yang telah dipotong dikeluarkan, kemudian bagian rumennya dibelah.
3) Pengambilan cairan rumen segera dilakukan setelah ternak dipotong. 4) Air panas dalam termos dibuang terlebih dahulu. Corong diletakkan
dimulut termos, isi rumen diambil, kemudian diperas dan disaring menggunakan kain muslin.
5) Cairan rumen dimasukan kedalam termos hingga terisi penuh kemudian termos tertutup rapat. Hal ini dimaksudkan untuk menjaga cairan rumen tetap dalam keadaan anaerob.
6) Cairan rumen segera dibawa ke laboratorium dan keadaan anaerob tetap dipertahankan sampai percoban in vitro.
3.3.3. Pelaksanaan in vitro
Prosedur pelaksanaan in vitro mengacu pada metode Tilley dan Terry (1963). Tahapannya adalah sebagai berikut:
1) Semua peralatan yang akan digunakan dalam proses in vitro disiapkan terlebih dahulu.
2) Sampel bahan ditimbang sebanyak ± 1 gram kering udara untuk setiap tabung, kemudian sampel tersebut dimasukan kedalam tabung fermentor yang telah diberi label.
3) Saliva buatan sebanyak 40 mililiter dan cairan rumen sebanyak 10 mililiter dimasukan kedalam tabung fermentor yang telah diisi sampel.
4) Gas karbondioksida dialirkan kedalam tabung. Kemudian lubang fermentor tersebut ditutup dengan menggunakan tutup karet berventilasi. 5) Tabung fermentor dimasukan kedalam rak yang telah tersedia didalam
waterbath yang berisi air dengan pengaturan suhu 39-40 °C selama 3 jam sambil dilakukan pengocokan secara kontinyu setiap 30 menit sekali. 6) Setelah inkubasi selama 3 jam dalam keadaan anaerob, tutup karet dibuka
kemudian ditambahkan 2-3 tetes larutan HgCL2 jenuh untuk menghentikan aktivitas mikroba. Tabung fermentor dikocok secara perlahan agar larutan HgCL2 jenuh bercampur homogen dengan cairan fermentor.
7) Cairan fermentor dimasukan kedalam tabung sentrifugasi, kemudian diputar selama 15 menit dengan kecepatan 4500 putaran per menit (rpm) untuk mendapatkan supernatan yang akan dianalisis kandungan Volatile
3.4. Peubah Yang Diamati 3.4.1. Amonia (NH3)
Kadar NH3 ditentukan dengan teknik mikrodifusi conway (general laboratory procedure, 1966). Bibir cawan conway dan tutup diolesi dengan vaselin. Supernatan yang berasal dari proses fermentasi diambil 1 milimiter, kemudian ditempatkan pada salah satu ujung alur cawan conway. Larutan NaOH jenuh sebanyak 1 milimiter ditempatkan pada salah satu ujung conway yang bersebelahan dengan supernatan. Larutan asam borat berindikator metil red dan brom kressol green sebanyak 1 milimiter ditempatkan pada cawan kecil yang terletak ditengah cawan conway. Cawan conway yang sudah diolesi vaselin ditutup rapat hingga kedap udara, larutan NaOH dicampur dengan supernatan hingga merata dengan cara menggoyang-goyangkan dan memiringkan cawan tersebut. Setelah itu dibiarkan selama 24 jam dalam suhu kamar. Setelah 24 jam suhu kamaar dibuka, asam borat berindikator dititrasi dengan H2SO4 0,005 N sampai terjadi perubahan warna dari hitam menjadi merah muda. Kadar produksi NH3 dalam cairan rumen dapat dihitung dengan rumus sebagai berikut:
NH3 (mM) = (V H2SO4 X N H2SO4 X 1000) mM Keterangan :
V = Volume H2SO4 yang terpakai untuk titrasi N = Normalitas H2SO4
3.4.2. Volatile Fatty Acid (VFA)
Produksi VFA ditentukan dengan destilasi tekanan uap (general laboratory procedure, 1966). Sebanyak 5 milimiter supernatan dimasukan kedalam tabung destilasi yang dipanaskan dengan uap air. Tabung segera ditutup rapat setelah ditambahkan 1 milimiter H2SO4 15%. Tabung destilasi dihubungkan dengan labu yang berisi air mendidih dan dipanaskan terus menerus selama proses destilasi.
Uap panas akan mendesak VFA melewati tabung pendingin terkondensasi dan ditampung dengan erlenmeyer berisi 5 milimiter NaOH 0,5 N sampai mencapai volume sekitar 300 milimiter, selanjutnya ditambah indikator phenolptalen sebanyak 2-3 tetes dan dititrasi dengan HCL 0,5 N. Penetesan berakhir samapai didapatkan perubahan warna dari merah muda menjadi bening atau tidak berwarna. Dilakukan pula titrasi blangko terhadap 5 milimiter H2SO4. Kadar VFA dihitung dengan rumus:
VFA total (mM) =(𝑏−𝑠)𝑥 𝑁𝐻𝐶𝐿 𝑥 1000 𝑆
Keterangan:
B = volume titrasi blangko s = volume titrasi sample N = Normalitas larutan HCL 3.5.3. Analisis Statistik
Percobaan dilakukan secara eksperimental dengan menggunakan Percobaan Rancangan Acak Lengkap (RAL) pola tersarang. Perlakuan terdiri atas tiga tingkat dosis NaOH 0,1 N (D1= 10%, D2=15%, dan D3=20%) dan tiga tingkat waktu perendaman (W1=10 menit, W2=15 menit dan W3=20 menit) masing-masing diulang sebanyak tiga kali, sehingga menghasilkan keterangan sebagai berikut :
D1W1= Biji sorgum direndam pada larutan 10% NaOH 0,1 N dan waktu perendaman 10 menit.
D1W2= Biji sorgum direndam pada larutan 10% NaOH 0,1 N dan waktu perendaman 15 menit.
D1W3= Biji sorgum direndam pada larutan 10% NaOH 0,1 N dan waktu perendaman 20 menit.
D2W1= Biji sorgum direndam pada larutan 15% NaOH 0,1 N dan waktu perendaman 10 menit.
D2W2= Biji sorgum direndam pada larutan 15% NaOH 0,1 N dan waktu perendaman 15 menit.
D2W3= Biji sorgum direndam pada larutan 15% NaOH 0,1 N dan waktu perendaman 20 menit.
D3W1= Biji sorgum direndam pada larutan 20% NaOH 0,1 N dan waktu perendaman 10 menit.
D3W2= Biji sorgum direndam pada larutan 20% NaOH 0,1 N dan waktu perendaman 15 menit.
D3W3= Biji sorgum direndam pada larutan 20% NaOH 0,1 N dan waktu perendaman 20 menit.
Keterangan: D = Dosis W = Waktu
Percobaan ini terdapat 9 kombinasi perlakuan dengan 3 ulangan sehingga secara keseluruhan dihasilkan 27 unit percobaan. Data percobaan yang diperoleh selanjutnya dianalisis statistik menggunakan Analisis Ragam. Model matematik rancangan acak lengkap pola tersarang berdasarkan Montgomerry (1991) sebagai berikut :
Y(ijk) = µ + α(i) + βj(i) + є(ijk) keterangan:
Y(ijk) : Pengamatan dosis taraf ke-i, waktu dalam dosis taraf ke-j dan ulangan ke-k
µ : Rataan Umum
α(i) : Pengaruh dosis pada taraf ke-i
βj(i) : Pengaruh waktu dalam dosis pada taraf ke-j pada αi
є(ijk) : Pengaruh galat dosis taraf ke-i, waktu dalam dosis taraf ke-j dan Ulangan ke-k
i : Banyaknya perlakuan ke-i (i=1,2,3) j : Banyaknya perlakuan ke-j (j=1,2,3) k : Ulangan (1, 2, 3)
Hipotesis yang diuji :
H0 = α2 = 0
H1 = α2 ≠ 0
H0 = β22 = 0
H1 = β22 ≠ 0 Maka:
H0 = Tidak ada perbedaan pengaruh dosis NaOH dan waktu dalam dosis perendaman terhadap produksi VFA dan NH3 pada cairan rumen sapi perah FH (in vitro).
H1 = Ada pengaruh dosis NaOH dan waktu dalam dosis perendaman terhadap kenaikan produksi VFA pada cairan rumen sapi perah FH (in vitro).
H0 = Tidak ada perbedaan pengaruh dosis NaOH dan waktu dalam dosis perendaman terhadap produksi VFA dan NH3 pada cairan rumen sapi perah FH (in vitro).
H1 = Ada pengaruh dosis NaOH dan waktu dalam dosis perendaman terhadap penurunan produksi NH3 pada cairan rumen sapi perah FH (in vitro).
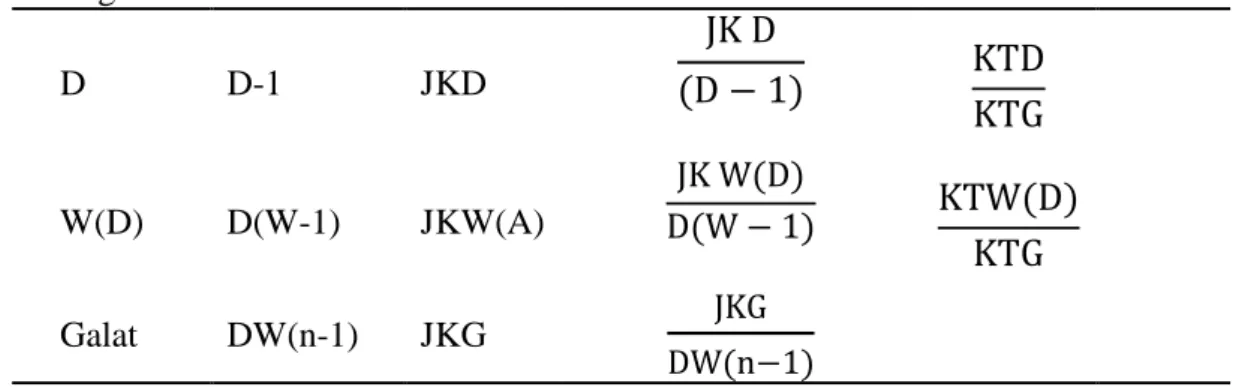
Tabel 1. Daftar Sidik Ragam Sumber Keragaman DB JK KT Fhit F0,05 D D-1 JKD JK D (D − 1) KTD KTG W(D) D(W-1) JKW(A) JK W(D) D(W − 1) KTW(D) KTG Galat DW(n-1) JKG JKG DW(n−1) Total DWn-1 JKT Keterangan: DB = Derajat Bebas JK = Jumlah Kuadrat KT = Kuadrat Tengah D = Faktor Dosis
W = Faktor waktu dalam dosis r = Ulangan
n = Jumlah data
Kaidah pengambilan keputusan:
(1) Bila Fhitung ≤ Ftabel; berbeda tidak nyata (non significant) atau terima H0. (2) Bila Fhitung > Ftabel; berbeda nyata (significant) atau tolak H0.
Jika H0 diterima, berarti tidak ada pengaruh perlakuan yang berbeda, oleh karena itu pengujian lanjutan tidak perlu dilakukan, tetapi apabila ditolak, berarti ada perlakuan yang berbeda, maka perlu dilakukan pengujian lanjut untuk mengetahui perbedaan diantara nilai tengah tersebut.
Selanjutnya untuk menguji perbedaan antar perlakuan digunakan uji Jarak Berganda Duncan : Sx = LSR α = SSRα . Sx Keterangan : Sx : Standard error
KT galat : Kuadrat Tengah Galat
SSR : Studentized Significant Range LSRα : Least Significant Range
r : Banyaknya Ulangan
Kaidah Keputusan :
Bila d ≤ LSR, terima H0 (tidak berbeda nyata) Bila d > LSR, tolak H0 (berbeda nyata)
Keterangan :
d = selisih antara dua beda nyata
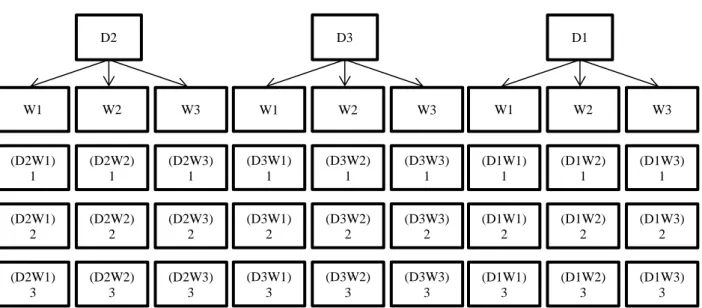
Penelitian dilakukan pengacakan setiap unit percobaan memiliki peluang yang sama pada kondisi pengambilan sampel terhadap perlakuan. Tata letak percobaan diperoleh dari hasil pengacakan, sebagai berikut:
Ilustrasi 3. Tata letak percobaan D2 W2 W3 W1 (D2W1) 1 (D2W1) 2 (D2W1) 3 (D2W2) 1 (D2W2) 2 (D2W2) 3 (D2W3) 1 (D2W3) 2 (D2W3) 3 D3 W2 W3 W1 (D3W1) 1 (D3W1) 2 (D3W1) 3 (D3W2) 1 (D3W2) 2 (D3W2) 3 (D3W3) 1 (D3W3) 2 (D3W3) 3 D1 W2 W3 W1 (D1W1) 1 (D1W1) 2 (D1W1) 3 (D1W2) 1 (D1W2) 2 (D1W2) 3 (D1W3) 1 (D1W3) 2 (D1W3) 3