KATA PENGANTAR
Puji dan syukur kami sampaikan kehadirat Tuhan Yang Maha Esa, karena berkat Karunia-Nya kami dapat menyelesaikan makalah ini.
Makalah ini kami buat dan kami susun dengan maksud untuk memenuhi tugas yang diberikan serta untuk menambah pengetahuan pembaca tentang Asam Karboksilat pada mata kuliah Kimia Organik.
Kami haturkan terima kasih kepada bapak Drs. Irdoni HS, MS. yang telah membimbing kami dalam mempelajari mata kuliah Kimia Organik, kemudian kepada teman-teman sejawat yang telah membantu kami dalam penyelesaian makalah ini.
Kami menyadari bahwa makalah ini masih banyak kekurangan. Tetapi kami berharap makalah ini dapat bermanfaat bagi siapapun yang membacanya.
Oleh karena itu, kami mohon maaf atas segala kekurangan dalam penyajian makalah ini, maka dari itu kritik dan saran sangat kami harapkan.
Pekanbaru, Maret 2010
Kelompok Daftar Isi
Kata Pengantar 2
Daftar Isi 3
Daftar Tabel
5
Daftar Flow Chart 6
BAB I PENDAHULUAN 7
I.1 Latar Belakang 7
I.2 Rumusan Masalah
7
I.3 Tujuan Penulisan
8
BAB II PEMBAHASAN 9
II.1 Definisi Asam Karboksilat 9
II.2 Penamaan Asam Karboksilat 9
II.3 Isomer Asam Karboksilat 12
II.4 Sifat-sifat Asam Karboksilat 13
II.4.1 Sifat Spektral Asam Karboksilat
15
II.4.2 Bagaimana Struktur Mempengaruhi Kuat Asam 17
II.5 Keasaman dan Ketetapan Keasaman 33
II.6 Reaksi-reaksi Pembuatan Asam Karboksilat 35
II.7 Reaksi-reaksi Senyawa Asam Karboksilat 43
II.7.1 Reaksi Asam Karboksilat dengan Basa
II.7.2 Estersifikasi Asam Karboksilat
II.7.3 Reduksi Asam Karboksilat
II.8 Kegunaan Asam Karboksilat 55
BAB III KESIMPULAN DAN SARAN 59
BAB IVPERTANYAAN
60
Daftar Pustaka 63
BAB I PENDAHULUAN
I.1 Latar Belakang Asam Karboksilat
Asam karboksilat disebut golongan asam alkanoat. Asam karboksilat merupakan senyawa karbon yang mempunyai gugus karboksil –COOH. Istilah karboksil berasal dari dua gugus, yaitu gugus karbonil (-CO-) dan gugus hidroksil (-OH). Asam karboksilat merupakan turunan dari alkana dimana sebuah atom H dari alkana diganti gugus –COOH. Rumus umum asam karboksilat adalah R-COOH atau CnH2nO2.
Asam karboksilat adalah suatu senyawa organik yang mengandung gugus karbonil (-COOH ), misalnya : asam formiat, asam asetat, asam propionnat, asam butirat, dan lain-lain. Asam asetat dapat dihasilkan dengan mereaksikan Na-asetat dengan K-hidrosulfat. Suatu ester karboksilat adalah suatu senyawa yang mengandung gugus -COOR dengan R yang berupa alkil atau aril. Ester ini dapat di bentuk dengan mereaksikan langsung suatu asam karboksilat dengan suatu alkohol. Reaksi ini di sebut reaksi esterifikasi, yang berkataliskan asam dan bersifat reversibel.
I.2 Rumusan Masalah Asam Karboksilat
Apa yang dimaksud dengan asam karboksilat ?
Bagaimana sifat fisik dan sifat kimia asam karboksilat ?
Bagaimana cara penulisan tata nama asam karboksilat ?
Bagaimana reaksi-reaksi pembuatan asam karboksilat ?
Apa saja reaksi-reaksi senyawa asam karboksilat ?
Apa saja kegunaan dari asam karboksilat ?
BAB II PEMBAHASAN II.1 DEFINISI ASAM KARBOKSILAT
Asam organic yang paling penting adalah asam-asam karboksilat. Gugus fungsinya adalah gugus karboksil. Kependekan dari dua bagian yaitu gugus karboksil dan hidroksil. Asam karboksilat juga merupakan senyawa karbon turunan alkana. Rumus umum asam karboksilat dapat dipanjangkan atau dipendekan seperti :
O O
–C-OH R – C – OH atau RCOOH atau RCO2H gugus karboksil tiga cara untuk menulis asam karboksilat
II.2 PENAMAAN ASAM KARBOKSILAT 1. Nama IUPAC
Pada system IUPAC nama asam diturunkan dari nama alkana, akhiran adiganti dengan oat di depannya ditambah kata asam, jadi senyawa ini disebut golongan asam alkanoat.
Untuk senyawa yang mempunyai isomer, tata namanya sama seperti pada aldehid karena gugus fungsinya sama-sama berada pada ujung rantai C. Cara penamannya sebagai berikut .
(a) Rantai pokok adalah rantai yang paling panjang yang mengandung gugus fungsi. Nama alkanoat sesuai nama rantai pokok diberi akhiran oat.
(b) Penomoran dimulai dari gugus fungsi
(c) Penulisan nama dimulai dengan nama cabang atau gugus lain yang diisusun menurut abjad kemudian nama rantai pokok. Karena gugus fungsi pasti nomor satu, jadi nomor gugus fungsi tidak perlu disebutkan.
Contoh :
CH3-CH-C-OH
CH3
Asam 2-metilpropanoat
O
Asam 2-amino-4-metilpentanoat
CH3 NH2 O
CH3-CH-CH2-CH-C-OH
Cl
O
Asam 3-klorobutanoat
CH3-CH-CH2-C-OH CH3-CH-CH2- C C-OH
Asam 4-hidroksi-2,2-dimetilpentanoat
CH3O
CH3 OH
Asam karboksilat yang mempunyai dua gugus fungsi disebut asam alkanadioat. Sedangkan, asam yang mempunyai tiga gugus fungsi disebut asam alkanatrioat.
Contoh :
Asam 1,2-etanadioat (asam oksalat)
HO-C-C-OH
O O
Asam 1,3-propanadioat (asam malonat)
HO-C-CH2-C-OH
O O
Asam 1,3,5-pentanatrioat (asam sitrat)
HC-C-OH H2C-C-OH
O O O
H2C-C-OH
Asam 2,2-dimetilpropanoat
CH3-C C-OH
CH3 O
CH3
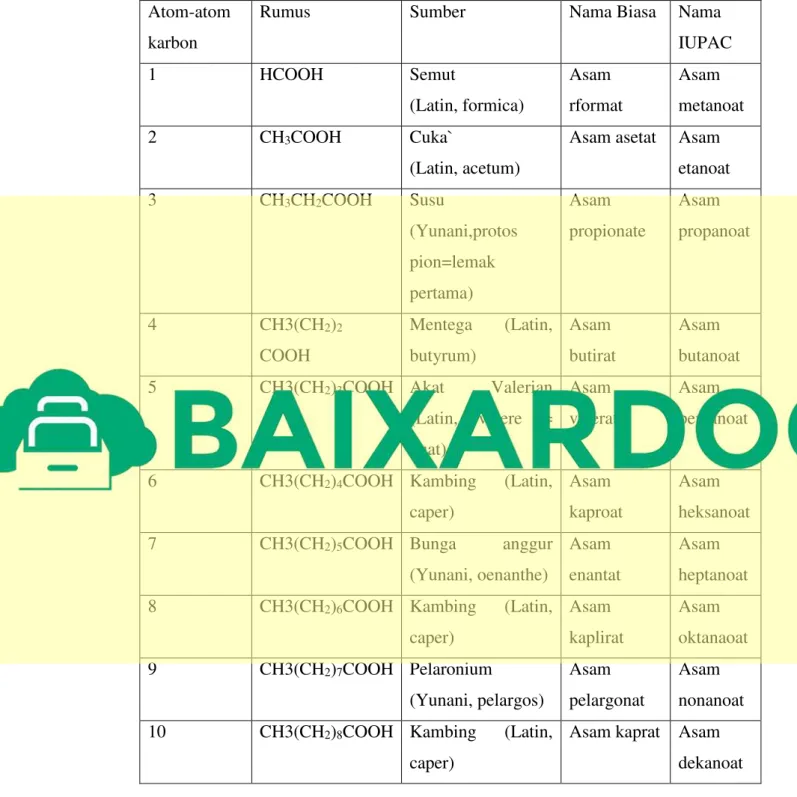
2. Nama Lazim ( Trivial)
Nama lazim asam karboksilat diambil dari nama asal asam tersebut di alam.
Tabel II.1 Asam-asam karboksilat alifatik Atom-atom
karbon
Rumus Sumber Nama Biasa Nama
IUPAC
1 HCOOH Semut
(Latin, formica)
Asam rformat
Asam metanoat
2 CH3COOH Cuka`
(Latin, acetum)
Asam asetat Asam etanoat
3 CH3CH2COOH Susu
(Yunani,protos pion=lemak pertama)
Asam propionate
Asam propanoat
4 CH3(CH2)2
COOH
Mentega (Latin, butyrum)
Asam butirat
Asam butanoat 5 CH3(CH2)3COOH Akat Valerian
(Latin, valere = kuat)
Asam valerat
Asam pentanoat
6 CH3(CH2)4COOH Kambing (Latin, caper)
Asam kaproat
Asam heksanoat 7 CH3(CH2)5COOH Bunga anggur
(Yunani, oenanthe)
Asam enantat
Asam heptanoat 8 CH3(CH2)6COOH Kambing (Latin,
caper)
Asam kaplirat
Asam oktanaoat 9 CH3(CH2)7COOH Pelaronium
(Yunani, pelargos)
Asam pelargonat
Asam nonanoat 10 CH3(CH2)8COOH Kambing (Latin,
caper)
Asam kaprat Asam dekanoat
II.3 ISOMER ASAM KARBOKSILAT
Seperti alkanal, asam karboksilat juga tidak mempunyai isomer posisi karena gugus fungsinya di ujung rantai C. Karena yang dapat berubah
hanya stuktur alkil maka isomernya adalah isomer struktur. Isomer struktur asam karboksilat dimulai dari asam butanoat.
Contoh :
O
1) Isomer struktur C4H9C – OH ada dua, yaitu :
CH3-CH2-CH2-C-OH
O
Asam Butanoat
O
CH3-CH2-CH-C-OH
CH3
Asam 2-metilbutanoat O
2) Isomer struktur C5H11-C-OH ada 4 (empat), yaitu :
CH3-CH2-CH-C-OH
O
CH3
Asam 2-metilbutanoat
CH3-CH-CH2-C-OH
O
CH3
Asam 3-metilbutanoat
Asam 2,2-dimetilpropanoat
CH3-C C-OH
CH3 O
CH3
II.4 SIFAT FISIS dan SIFAT KIMIA ASAM KARBOKSILAT
Anggota-anggota pertama dari asam karboksilat adalah cairan tak berwarna dengan bau yang menyengat. Cuka adalah larutan 4 atau 5%
asam asetat, baud an rasanya khas. Asam butirat berasal dari mentega tengik, asam-asam kaproat,kaprilat, dan kaprat berbau kambing.
Sebagaimana diramalkan dari strukturnya, asam karboksilat bersifat polar seperti halnya alcohol. Asam karboksilat membentuk ikatan hydrogen dengan sesamanya atau dengan molekul lain. Karena itu titik didihnya lebih tinggi dibandingkan dengan alcohol dengan bobot molekul yang hampir sama. Misalnya, asam asetat dan n-propil alcohol mempnuyai bobot molekul sama (60) tetapi titik didihnya berturut-turut 118⁰C dan 97⁰C. penetapan bobot molekul menunjukan bahwa asm-asam format dan asetat merupakan dimer dalam pelarut non polar, sekalipun dalam keadaan gasnya. Dua molekul saling berpegangan melalui ikatan hydrogen.
C R
Ikatan hidrogen
R C
H O
H O O
O
Ikatan hidrogen
Gambar 1. Ikatan hidrogen pada asam karboksilat
Ikatan hydrogen juga menjelaskan sifat-sifat kelarutan air pada asam-asam karboksilat berbobot molekul rendah.
Beberapa point tentang sifat fisis dan kimia asam karboksilat , diantaranya adalah
Mengandung gugus COOH yang terikat pada gugus alkil (R-COOH) maupun gugus aril (Ar-COOH)
Asam dengan jumlah C 1 – 4 : larut dalam air
Asam dengan jumlah C = 5 : sukar larut dalam air
Asam dengan jumlah C > 6 : tidak larut dalam air
Larut dalam pelarut organik seperti eter, alkohol, dan benzen
TD asam karboksilat > TD alkohol dengan jumlah C sama.
Suku-suku rendah mudah larut dalam air. Makin banyak atom C dalam molekul kelarutan akan semakin berkurang. Senyawa yang berwujud padat tidak larut dalam air.
Titik didih dan titik lelehnya tinggi, karena antara molekulnya terdapat ikatan hydrogen.
Merupakan asam lemah. Makin panjang rantai C makin lemah kekuatan asamnya.
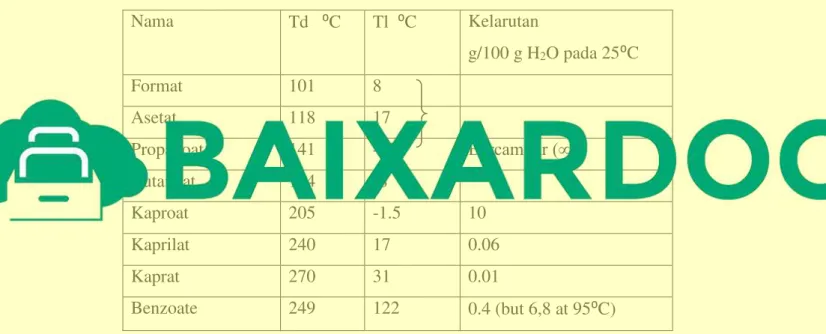
Contoh beberapa sifat fisis dari asam karboksilat diantaranya adalah
Tabel II.2 Sifat fisik beberapa asam karboksilat
Nama Td ⁰C Tl ⁰C Kelarutan
g/100 g H2O pada 25⁰C
Format 101 8
Asetat 118 17
Propanoat 141 -22 Bercampur (∞)
Butanoat 164 -8
Kaproat 205 -1.5 10
Kaprilat 240 17 0.06
Kaprat 270 31 0.01
Benzoate 249 122 0.4 (but 6,8 at 95⁰C)
II.4.1 Sifat Spektral Asam Karboksilat a. Spektra Inframerah
Asam karboksilat, baik sebagai cairan ataupun dalam larutan dengan konsentrasi di atas 0,01 M, berada terutama dalam bentuk dimer berikatan-hidrogen, bukannya dalam bentuk monomer diskrit (discrete).
Karena itu spectrum inframerah asam karboksilat adalah spectrum dari dinernya. Karena adanya ikatan hydrogen, resapan uluran OH (dari) asam- asam karboksilat sangat lebar dan intensif. Resapan OH ini mulai sekitar 3300 cm-1(3,0 µm) dan melandai ked lam daerah resapan karbon-hidrogen
dapat mengaburkan resapan CH aromatic dan alifatik, maupun resapan OH atau NH lainnya didalam spectrum itu.
Resapan karbonil dijumpai pada kira-kira 1700-1725 cm-1 (5,8-5,88 µm), dengan intensitas yang cukup kuat. Konjugasi menggeset resapan ini frekuensi yang lebih rendah: 1680-1700 cm-1 (5,9-5,95 µm).
Daerah sidik jari dalam spectrum inframerah suatu asam karboksilat seringkali menunjukan uluran C – O dan tekukan OH ( lihat table II.3). Getaran tekukan OH lainnya (dari) dimer itu menimbulkan resapan lebar di dekat 925 cm-1 (10,8 µm).
b. Spektra nmr
Dalam spectrum nmr, resapan proton asam (dari) suatu asam karboksilat nampak sebagai suatu singlet jauh dibawah medan (δ = 10-13 ppm), diuar skala dari rentang spectra yang biasa. Proton alfa hanya sedikit sekali dipengaruhi oleh gugus C=O; resapnnya sedikit dibawah medan (sekitar 2,2 ppm) karena efek induktif (dari) karbon karbonil yang positif parsial. Tidak terdapat pola penguraian yang unikk, yang dikaitkan dengan gugus asam karboksilat, karena proton karboksilat tidak mempunyai tetangga proton.
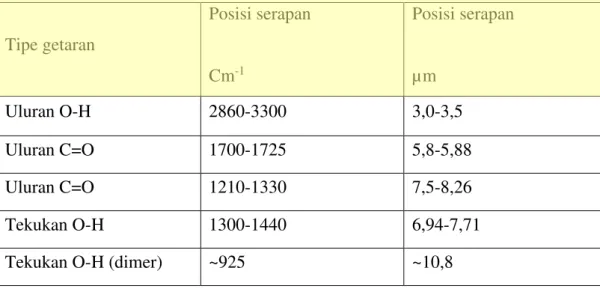
Tabel II.3 Resapan inframerah karakteristik untuk asam-asam karboksilat
Tipe getaran
Posisi serapan
Cm-1
Posisi serapan
µm
Uluran O-H 2860-3300 3,0-3,5
Uluran C=O 1700-1725 5,8-5,88
Uluran C=O 1210-1330 7,5-8,26
Tekukan O-H 1300-1440 6,94-7,71
Tekukan O-H (dimer) ~925 ~10,8