STUDI LITERATUR POTENSI INSTABILITAS DAN
INKOMPATIBILITAS PADA RESEP RACIKAN SEDIAAN KRIM YANG MENGANDUNG GENTAMISIN SULFAT DAN DESOKSIMETASON
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Junia Brigita Tamara NIM : 168114177
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
Halaman Judul
STUDI LITERATUR POTENSI INSTABILITAS DAN
INKOMPATIBILITAS PADA RESEP RACIKAN SEDIAAN KRIM YANG MENGANDUNG GENTAMISIN SULFAT DAN DESOKSIMETASON
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Junia Brigita Tamara NIM : 168114177
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
viii ABSTRAK
Peracikan obat masih sering dilakukan di Indonesia. Salah satunya adalah racikan sediaan krim yang dapat berpotensi mengalami instabilitas dan inkompatibilitas yang dapat menurunkan efikasi dan keamanan obat. Namun, obat racikan secara umum belum dinilai efikasi dan keamanannya dibandingkan dengan obat komersial. Maka dari itu, seorang apoteker memiliki peranan sangat penting untuk mengidentifikasi dan memastikan resep yang diberikan kepada pasien telah tepat untuk diracik dalam rangka mencapai tujuan terapi yang diharapkan. Tujuan dari penelitian ini adalah untuk mengetahui potensi instabilitas dan inkompatibilitas resep racikan krim yang mengandung Gentamisin Sulfat dan Desoksimetason. Penelitian ini dilakukan dengan metode kepustakaan. Pengkajian potensi dilakukan dengan cara studi literatur dari berbagai referensi seperti kompendial, artikel ilmiah dan database. Hasil dari studi kasus menunjukkan bahwa sediaan racikan krim gentamisin sulfat dan desoksimetason berpotensi mengalami instabilitas yang dipengaruhi oleh kelembapan. Namun, sediaan racikan tidak mengalami potensi inkompatibitas dalam peracikan.
Kata kunci : Peracikan obat, sediaan krim, gentamisin sulfat, desoksimetason, inkompatibilitas, instabilitas
ix ABSTRACT
Extemporaneous preparation still do in Indonesia. One of them is the creams extemporaneous preparation which potentially induce instability and incompatibilities due to decreased efficacy and safety of the drug. In general, quality and safety of extemporaneous preparation do not yet rated. Therefore a pharmacist plays an important role to identify and ensure whether the patients have received the appropriate prescribing of medications to achieve the expected therapeutic goal. This study aimed to find out the potential for instability and incompatibility of prescription creams containing gentamicin sulfate and desoxymetasone. The researcher used library research as a method to gather information. This study was carried out by studying literature from various references such as compendial, scientific articles, and databases. The results of this case study show that the extemporaneous prescription of gentamicin sulfate and dexamethasone creams have the potential to cause instability caused by humidity. The creams extemporaneous preparation doesn't have the potential for incompatibility.
Keywords : Drug compounding, cream, gentamicin sulphate, desoxymethasone, incompatibility, instability
x DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
PENGESAHAN SKRIPSI ... iii
PERNYATAAN KEASLIAN KARYA ... iv
LEMBAR PERNYATAAN PERSETUJUAN ... v
PRAKATA ... vi
ABSTRAK ... viii
ABSTRACT ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
PENDAHULUAN ... 1
METODE PENELITIAN ... 3
HASIL DAN PEMBAHASAN ... 5
KESIMPULAN ... 17
SARAN ... 17
DAFTAR PUSTAKA ... 18
xi
DAFTAR TABEL
Tabel I. Potensi Degradasi Gugus- Gugus Fungsional Gentamisin Sulfat ... 7 Tabel II. Potensi Degradasi Gugus- Gugus Fungsional
xii
DAFTAR GAMBAR
Gambar 1. Struktur Gentamisin Sulfat ... 5
Gambar 2. Reaksi Oksidasi pada Alkohol Sekunder ... 8
Gambar 3. Struktur Desoksimetason... 10
Gambar 4. Reaksi Pembentukan Hemiasetal ... 12
Gambar 5. Reaksi Oksidasi pada Alkohol Primer ... 12
Gambar 6. Mekanisme Pembentukan Degradasi Desoksimetason dalam Kondisi Basa ... 13
1 PENDAHULUAN
Peracikan obat merupakan pilihan terapi yang penting untuk dilakukan terutama dalam menangani pasien dengan kebutuhan medis khusus, saat suatu produk komersial yang dikehendaki tidak tersedia di pasaran atau untuk individualisasi dosis pasien (Gudeman et al., 2013, Guharoy et al., 2013). Namun, peracikan obat juga dapat menimbulkan beberapa masalah yang termasuk ke dalam medication error atau masalah kesehatan dalam pengobatan (Randell and Duffy, 2014). Kedua hal ini menyebabkan peracikan obat masih menjadi pro dan kontra di masyarakat serta tenaga kesehatan lainnya.
Menurut U.S Food & Drug Administration (2018), peracikan obat (compounding) adalah kegiatan yang dilakukan oleh seorang apoteker berlisensi atau seseorang dengan pengawasan apoteker berlisensi (asisten apoteker) yang mencampur atau mengubah bahan obat dan/atau obat jadi dari pabrik untuk membuat obat yang disesuaikan dengan kebutuhan pasien. Bahan yang digunakan dalam sediaan racikan harus kompatibel antara zat obat satu dengan zat obat lainnya dan dapat menyerupai formulasi yang dekat dengan produk komersial yang tersedia sehingga dapat menghasilkan produk obat yang stabil, berkhasiat dan aman (Minghetti et al, 2014; Pharmacy Board of Australia, 2017; Sellers and Utian, 2012).
Secara umum, obat racikan belum dinilai efikasi dan keamanannya. Hal ini dapat membahayakan pasien yang menggunakan obat tersebut (Kurniawan, 2013). Oleh karena itu, seorang apoteker memiliki peranan yang sangat penting untuk mengidentifikasi dan juga memastikan resep yang diberikan kepada pasien telah tepat untuk diracik dalam rangka mencapai tujuan terapi yang diharapkan. Salah satu bentuk sediaan racikan yang diresepkan dan diracik adalah sediaan semisolid dan bentuk sediaan semisolid dapat berpotensi mengalami medication error pada saat proses peracikan (Kristina et al, 2017). Salah satu medication error yang dapat terjadi adalah instabilitas dan inkompatibilitas obat yang dapat menurunkan bioavailabilitas, efikasi, dan keamanan obat (Bharate et al, 2010; Singh et al, 2000). Sebagai contoh hasil penelitian dari Makeen et al (2018), menunjukan bahwa sediaan racikan semisolid memiliki data stabilitas yang terbatas, dalam
2
penelitiannya peneliti mendapatkan bahwa salep methyl salicylate berpotensi mengalami degradasi yang cepat berupa penurunan konsentrasi obat pada kondisi temperatur tinggi.
Pada beberapa rumah sakit Indonesia masih banyak ditemukan penulisan resep racikan oleh dokter saat melakukan pelayanan kesehatan (Rochjana, 2019). Penggunaan antibakteri dan antiinflamasi sebagai pengobatan pada penyakit kulit dalam bentuk sediaan semisolid menjadi salah satu contoh obat racikan yang diresepkan di rumah sakit. Meskipun cukup banyak diresepkan, namun belum ada bukti yang pasti terkait penggunaan yang tepat pada kedua golongan obat ini secara bersamaan terutama mengenai efikasi dan keamanannya (Fleischer et al, 2017).
Salah satu formula racikan antibakteri dan antiinflamasi yang diresepkan di rumah sakit adalah resep racikan kombinasi yang mengandung gentamisin sulfat dan desoksimetason yang dibuat dalam bentuk sediaan krim. Dari 47 resep racikan topikal yang diresepkan disalah satu rumah sakit di Yogyakarta, resep racikan yang mengandung gentamisin sulfat dan desoksimetason diresepkan dengan frekuensi 32 kali pada periode bulan januari hingga april tahun 2019. Oleh karena itu, studi literatur terhadap sediaan obat racikan terutama sediaan racikan krim yang mengandung gentamisin sulfat dan desoksimetason perlu dilakukan untuk menilai efikasi dan keamanannya. Tujuan dari penulisan ini adalah untuk mengetahui potensi terjadinya instabilitas dan inkompatibilitas terhadap resep racikan krim yang mengandung gentamisin sulfat dan desoksimetason. Hasil dari penulisan skripsi ini diharapkan dapat digunakan sebagai referensi untuk proses edukasi bagi Apoteker, tenaga kefarmasian di instalasi farmasi dan tenaga medis lain di Rumah sakit dan dapat digunakan sebagai acuan mengenai keamanan terkait peresepan racikan krim kepada pasien.
3 METODE PENELITIAN
Jenis Penelitian
Penelitian yang digunakan dalam penulisan skripsi ini adalah studi kasus dengan metode kepustakaan. Metode kepustakaan adalah salah satu jenis metode penelitian kualitatif yang lokasi atau tempat penelitiannya dilakukan di pustaka, dokumen, arsip, dan lain sejenisnya (Zed, 2004). Kasus dalam penelitian ini yaitu resep racikan yang mengandung gentamisin sulfat dan desoksimetasondengan jumlah frekuensi peresepan sebanyak 32 resep pada periode bulan Januari hingga April 2019 dengan contoh resep yang mengandung formula tersebut adalah:
R/ Sagestam® cream 1 Topcort® cream 1 m.f. cream da in pot 1 S u e
Analisis Potensi Instabilitas dan Inkompatibilitas
Analisis potensi instabilitas dan inkompatibilitas dilakukan dengan mengumpulkan informasi umum, stabilitas dan inkompatibilitas gentamisin sulfat dan desoksimetason yang dapat digunakan dalam proses pengkajian potensi instabilitas dan inkompatibilitas sediaan racikan. Selain itu, dilakukan juga analisis gugus fungsional yang terkandung dalam senyawa obat dan potensi interaksi yang mempengaruhi stabilitas dan inkompatibilitas sediaan racikan. Pengumpulan informasi umum dilakukan dengan mengumpulkan informasi terkait rumus molekul, struktur kimia, bobot molekul, pemerian, kelarutan, titik leleh, nilai pKa, wadah dan penyimpanan, dan indikasi obat dari masing-masing senyawa obat. Pengumpulan informasi stabilitas dilakukan dengan mengumpulkan informasi terkait stabilitas dan instabilitas senyawa obat terhadap cahaya, suhu, kelembapan, pH, asam-basa, dan oksidator kuat. Informasi inkompatibilitas dilakukan dengan mengumpulkan informasi terkait kompatibilitas dan inkompatibilitas senyawa obat terhadap eksipien, terhadap senyawa obat lain serta terhadap wadah dan kemasan.
Analisis potensi instabilitas dan inkompatibilitas pada sediaan racikan dilakukan melalui studi literatur. Literatur yang digunakan dalam pengumpulan
4
informasi meliputi Farmakope Indonesia (FI) sebagai literatur utama, USP, database seperti Pubchem, buku, serta artikel ilmiah yang memuat informasi tentang obat yang dikaji. Kriteria artikel ilmiah yang dipakai yaitu diterbitkan oleh badan organisasi resmi (WHO dan FDA), jurnal bereputasi yang minimal sudah terindeks SINTA 2 secara nasional serta jurnal internasional terindeks DOAJ (Directory of Open Access Journals), Pubmed, dan lainnya. Cara mencari artikel ilmiah adalah dengan kata kunci pencarian di mesin pencari jurnal (google cendekia, Pubmed, Embase, dll). Contoh kata kunci yang digunakan yaitu the functional group of (nama obat), functional group analysis of (nama obat), incompatibility of (gugus fungsi obat), degradation of (gugus fungsi obat), stability of (nama obat), incompatibility of (nama obat), pharmaceutical drug interaction of (nama obat), degradation of (nama obat), dan sebagainya.
Interpretasi Hasil
Hasil dari penelitian terkait dengan kajian potensi instabilitas dan inkompatibilitas racikan krim yang mengandung Gentamisin Sulfat dan Desoksimetason dipaparkan secara deskriptif berdasarkan hasil dari penelusuran data dengan menjabarkan secara rinci studi literatur berkaitan dengan potensi terjadinya instabilitas dan inkompatibilitas senyawa-senyawa tersebut dalam bentuk paragraf.
5 HASIL DAN PEMBAHASAN
Informasi umum, Stabilitas dan Inkompatibilitas 1. Gentamisin Sulfat
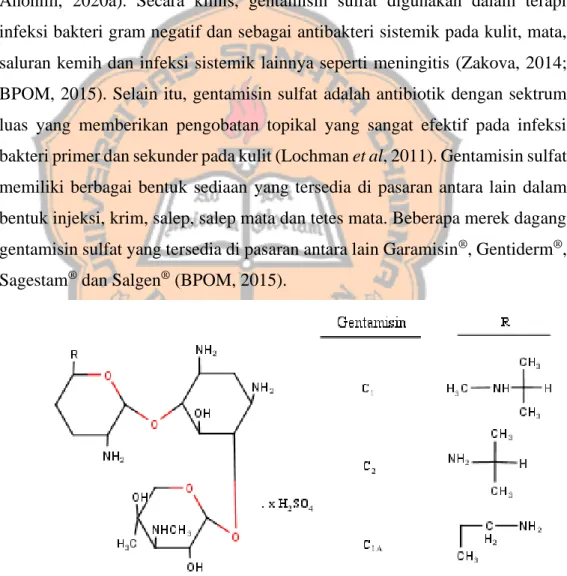
Gentamisin Sulfat merupakan antibakteri golongan aminoglikosida yang berupa garam sulfat atau campuran dari antibiotik yang dihasilkan oleh pembiakan Micromonospora purpurea (Kemenkes RI, 2014; Pennington et al, 1975). Gentamisin sulfat terdiri dari 3 komponen, yaitu gentamisin C1, C2 dan C1a yang setiap komponennya terdiri dari lima nitrogen basa (Grote et al, 2012; Anonim, 2020a). Secara klinis, gentamisin sulfat digunakan dalam terapi infeksi bakteri gram negatif dan sebagai antibakteri sistemik pada kulit, mata, saluran kemih dan infeksi sistemik lainnya seperti meningitis (Zakova, 2014; BPOM, 2015). Selain itu, gentamisin sulfat adalah antibiotik dengan sektrum luas yang memberikan pengobatan topikal yang sangat efektif pada infeksi bakteri primer dan sekunder pada kulit (Lochman et al, 2011). Gentamisin sulfat memiliki berbagai bentuk sediaan yang tersedia di pasaran antara lain dalam bentuk injeksi, krim, salep, salep mata dan tetes mata. Beberapa merek dagang gentamisin sulfat yang tersedia di pasaran antara lain Garamisin®, Gentiderm®, Sagestam® dan Salgen® (BPOM, 2015).
6
Gentamisin sulfat dengan rumus molekul C60H125N15O25S memiliki potensi setara dengan tidak kurang dari 590 μg per mg gentamisin, dihitung terhadap zat yang telah dikeringkan. Gentamisin sulfat yang berupa serbuk berwarna putih hingga kekuning-kuningan memiliki berat molekul 1488,8 g/mol. Gentamisin sulfat larut dalam air, tidak larut dalam etanol, aseton, kloroform,eter dan benzen (Kementerian Kesehatan RI, 2014 ; Pubchem, 2020). Gentamisin sulfat memiliki nilai pKa 12,55 dalam asam kuat dan 10,18 dalam basa kuat. Titik lebur gentamisin sulfat yaitu pada suhu 218-237oC (Anonim, 2020b). Pada larutan, gentamisin sulfat memiliki pH antara 3,5 dan 5,5 (Kementerian Kesehatan RI, 2014).
Berbagai bentuk sediaan gentamisin sulfat seperti krim, salep, dan salep mata mengandung gentamisin tidak kurang dari 90,0% dan tidak lebih dari 135,0% dari jumlah yang tertera pada etiket. Penyimpanan krim, salep, dan salep mata dalam tube yang dapat ditekan atau dalam wadah tertutup rapat. Penyimpanan dilakukan pada suhu 2oC - 30oC dan dihindarkan dari panas berlebih. Gentamisin sulfat juga tersedia dalam bentuk sediaan injeksi yang merupakan larutan steril dari gentamisin sulfat dalam air untuk injeksi dan mengandung tidak kurang dari 90,0% dan tidak lebih dari 125,0% gentamisin dari jumlah yang tertera pada etiket. Injeksi gentamisin sulfat berupa larutan jernih, agak kuning, dan berbau lemah. Selain itu, injeksi gentamisin sulfat memiliki pH antara 3,0 dan 5,5 dan disimpan dalam wadah dosis tunggal atau dosis ganda, sebaiknya wadah yang digunakan merupakan wadah kaca tipe I (Kementerian Kesehatan RI, 2014).
7
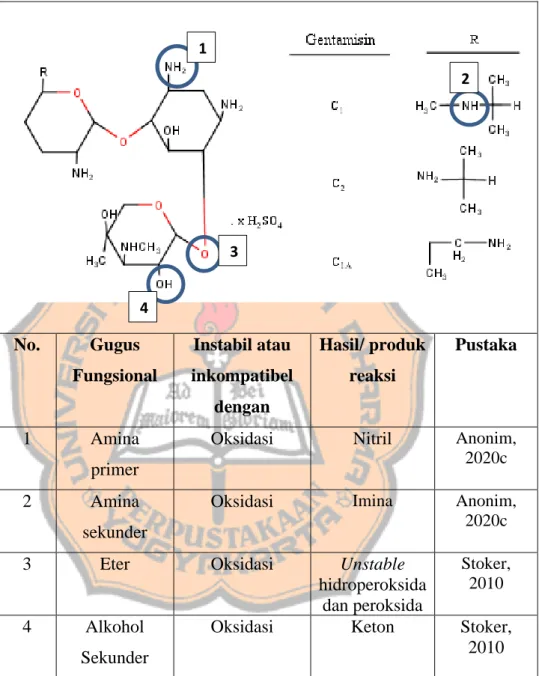
Tabel I. Potensi Degradasi Gugus- Gugus Fungsional Gentamisin Sulfat No. Gugus Fungsional Instabil atau inkompatibel dengan Hasil/ produk reaksi Pustaka 1 Amina primer
Oksidasi Nitril Anonim, 2020c
2 Amina sekunder
Oksidasi Imina Anonim, 2020c
3 Eter Oksidasi Unstable hidroperoksida dan peroksida Stoker, 2010 4 Alkohol Sekunder
Oksidasi Keton Stoker, 2010 Gentamisin sulfat memiliki 4 gugus fungsional yang berpotensi mengalami reaksi dengan senyawa lain yaitu amin primer, amin sekunder, eter, dan alkohol sekunder (Tabel I). Keempat gugus fungsional tersebut berpotensi mengalami reaksi oksidasi yang merupakan reaksi yang terjadi akibat adanya penambahan oksigen atau lepasnya hidrogen dari suatu molekul (Bharate, 2010; Stoker, 2010). Gugus amin primer akan teroksidasi dengan agen pengoksidasi ringan seperti NaOCl yang menghilangkan 4 atom hidrogen dari amin primer untuk membentuk
2 1
3 4
8
nitril (R-C≡N) (Anonim, 2020c). Amin sekunder juga mengalami oksidasi dengan bantuan reagen seperti MnO2 yang akan membentuk imina (R2CH―NHR′) (Anonim, 2020c). Gugus eter pada gentamisin sulfat bereaksi lambat dengan oksigen dari udara untuk membentuk hidroperoksida yang tidak stabil dan peroksida. Alkohol sekunder pada gentamisin sulfat juga berpotensi membentuk keton dengan reaksi oksidasi oleh agen pengksidator ringan seperti potassium permanganate (KMnO4), potassium dichromate (K2Cr2O7), dan chromic acid (H2CrO4) (Stoker, 2010).
Gambar 2. Reaksi Oksidasi pada Alkohol Sekunder (Stoker, 2010) Gentamisin sulfat cenderung stabil terhadap cahaya dan oksidator kuat. Gentamisin sulfat disimpan dengan dua kondisi paparan cahaya yang berbeda yaitu penerangan minim dengan menggunakan kantong foil terbuka pada suhu 20o C dan penerangan tinggi dengan menggunakan lampu neon. Pengaruh stabilitas gentamisin sulfat terhadap pengoksidator dilakukan dengan 30% hidrogen peroksida (H2O2) yang disimpan dalam gas nitrogen pada suhu 20o Cdan terlindung dari cahaya. Hasil yang didapat menunjukkan bahwa tidak terdapat degradasi yang terjadi pada gentamisin sulfat (Cote et al, 2010 ; Mullin et al, 2016 ; Akram et al, 2006).
Menurut penelitian Rizk et al (1995), suhu hanya memiliki pengaruh yang kecil untuk membentuk senyawa kompleks dan mempengaruhi stabilitas dari gentamisin sulfat. Gentamisin sulfat tidak menunjukkan adanya proses degradasi yang signifikan dalam penyimpanan pada suhu 4oC dan 60oC. Pengaruh gentamisin sulfat pada kondisi asam dan basa juga diuji dengan menggunakan asam klorida
9
(HCl) dan natrium hidroksida (NaOH). Hasil yang didapat tidak menunjukan adanya indikasi terjadi degradasi pada gentamisin sulfat (Mullin et al, 2016).
Studi stabilitas Gentamisin sulfat terkait kelembapan juga dilakukan oleh Freiess and Schlapp (2006) terhadap penyimpanan Gentamisin sulfat. Gentamisin sulfat disimpan dalam tiga kondisi berbeda yaitu pada 4oC/35% RH, 25oC/60% RH, dan 40oC/75% RH yang akan dievaluasi sebanyak tiga kali pada minggu ke 2.4 dan 12. Hasil yang didapat pada 4oC/35% RH adalah gentamisin sulfat tidak mengalami degradasi sampai minggu ke 12. Pada 25oC/60% RH, pada minggu ke 4 ditemukan adanya degradasi sebesar 5% dan pada 40oC/75% RH ditemukan juga adanya degradasi pada minggu ke 2 sebesar 5%, minggu ke 4 sebesar 67% dan minggu ke 12 sebesar 67%.
Penelitian Sombie et al (2014) menemukan penambahan gliseril monoleat pada gentamisin sulfat akan menyebabkan degradasi sebesar 11% setelah 6 bulan penyimpanan pada suhu 25oC. Gentamisin sulfat dengan penambahan gliseril monoeat juga menunjukkan perubahan warna sediaan menjadi kekuningan hingga kuning yang lebih gelap. Perubahan warna yang terjadi disebabkan oleh reaksi hidrolisis pada gliseril monoleat. Gentamisin sulfat juga akan mengalami degradasi jika dilarutkan dengan larutan dextrose 5% dengan pemanasan selama 5 hingga 27 menit dan tanpa dilakukan pemanasan dengan penyimpanan selama 3 minggu pada suhu ruangan. Hasil degradasi pada campuran obat dengan dilakukan pemanasan adalah 48% dan campuran yang tidak dilakukan pemanasan setelah 3 minggu akan mengalami degradasi sebesar 37%. Degradasi yang terjadi akan menurunkan potensi antimikroba pada gentamisin sulfat (Graham et al, 1997).
Gentamisin sulfat tidak kompatibel dengan obat-obat golongan penisilin, sefalosporin, heparin, furosemide dan natrium bikarbonat. Larutan gentamisin pH asam dapat melepaskan karbon dioksida. Interaksi pada preparasi pada pH basa dan obat-obat yang tidak stabil pada pH asam masih memungkinkan untuk dilakukan (Sweetman et al, 2009).
10 2. Desoksimetason
Desoksimetason adalah obat golongan kortikosteroid topikal turunan dari deksametason di mana gugus hidroksi pada posisi 17-alfa disubstitusi oleh hidrogen (Patwardan et al, 2015 ; Pubchem, 2020). Biasanya digunakan sebagai agen anti-inflamasi dan antipruritik. Selain itu, bisa digunakan untuk mengatasi psioriasis (Bagel and Nelson, 2018). Desoksimetason dibuat dalam berbagai bentuk sediaan semisolid yaitu krim dan salep dalam rentang konsentrasi 0,05% hingga 0,25% (Vladimirov et al, 1996). Beberapa merek dagang desoksimetason yang tersedia di pasaran antara lain Dercason®, Desomex®, Inerson®, dan Topcort® (BPOM, 2015).
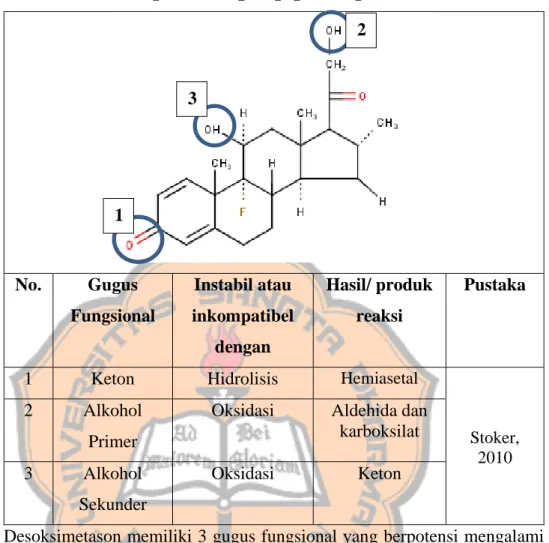
Gambar 3. Struktur Desoksimetason (Kementrian Kesehatan RI, 2014) Desoksimetason memiliki rumus molekul C22H29FO4 mengandung tidak kurang dari 97,0% dan tidak lebih dari 103,0% C22H29FO4, dihitung terhadap zat yang telah dikeringkan. Desoksimetason berupa serbuk hablur putih sampai praktis putih, dan tidak berbau dengan berat molekul 376,46 g/mol. Desoksimetason tidak larut dalam air, mudah larut dalam etanol, dalam aseton dan dalam kloroform (Kementerian Kesehatan RI, 2014). Desoksimetason memiliki nilai pKa 13,44 dalam asam kuat dan -3,3 dalam basa kuat (Anonim 2020d). Pada sediaan krim, desoksimetason memiliki pH antara 4,0 sampai 8,0 (USP, 2009). Titik leleh desoksimetason antara 206 o C dan 218o C. Penyimpanan desoskimetason dalam wadah tertutup baik (Kementerian Kesehatan RI, 2014).
11
Tabel II. Potensi Degradasi Gugus- gugus Fungsional Desoksimetason
No. Gugus Fungsional Instabil atau inkompatibel dengan Hasil/ produk reaksi Pustaka
1 Keton Hidrolisis Hemiasetal
Stoker, 2010
2 Alkohol Primer
Oksidasi Aldehida dan karboksilat 3 Alkohol
Sekunder
Oksidasi Keton
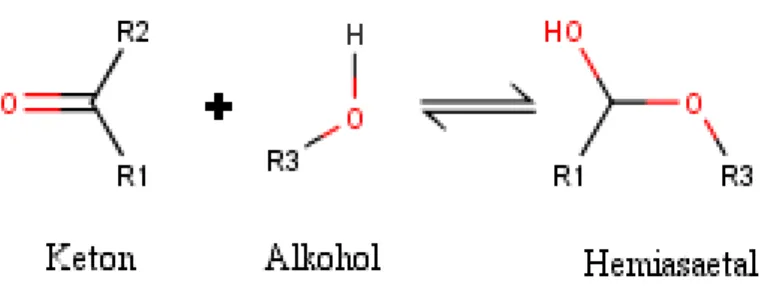
Desoksimetason memiliki 3 gugus fungsional yang berpotensi mengalami reaksi dengan senyawa lain yaitu keton, alkohol primer, dan alkohol sekunder (Tabel II). Gugus keton pada desoksimetason berpotensi mengalami reaksi hidrolisis yang merupakan reaksi kimia yang menguraikan air dengan melibatkan katalis asam atau basa (Wardiyah, 2016). Gugus keton akan berpotensi mengalami reaksi hidrolisis dengan adanya gugus alkohol yang akan menghasilkan senyawa hemiasetal. Hemiasetal adalah senyawa organik yang atom karbonnya berikatan dengan dua gugus sekaligus, yaitu hidroksi (-OH) dan alkoksi (-OR) (Stoker, 2010)
1
3
12
Gambar 4. Reaksi Pembentukan Hemiasetal (Stoker, 2010) Gugus alkohol primer dan alkohol sekunder juga berpotensi mengalami reaksi oksidasi. Alkohol primer akan teoksidasi menjadi aldehida dan jika aldehida dari hasil tersebut mengalami oksidasi lagi akan menjadi asam karboksilat. Alkohol sekunder akan teroksidasi menjadi keton (Gambar 2). Oksidasi yang terjadi dipicu oleh adanya agen pengoksidasi ringan seperti potassium permanganate (KMnO4), potassium dichromate (K2Cr2O7), dan chromic acid (H2CrO4) (Stoker, 2010).
Gambar 5. Reaksi Oksidasi pada Alkohol Primer (Stoker, 2010) Desoksimetason stabil terhadap cahaya dan panas. Menurut penelitian Srinivasu et al (2012), desoksimetason yang disimpan pada suhu 60o dalam oven kering dan dipaparkan oleh cahaya pada ruang stabilitas cahaya selama 10 hari tidak membentuk produk degradasi yang ditunjukkan dengan nilai kadar awal obat dari 99,5% menjadi 99,8%.
Srinivasu et al (2012) juga melakukan penelitian stabilitas desoksimetason terhadap hidrolisis asam dan oksidator kuat. Hidrolisis asam dilakukan menggunakan 1N HCl dan oksidator kuat menggunakan 5% H2O2 pada sampel obat selama 24 jam. Hasil yang didapatkan adalah tidak ditemukan produk degradasi yang terbentuk pada sampel obat. Pada hidrolisis asam, nilai kadar awal obat 99,2% menjadi 99,7% dan pada kondisi oksidator kuat nilai kadar awal obat 98,5%
13
menjadi 99,7%. Penelitian juga dilakukan terhadap ketsabilan obat terhadap air yang disimpan pada suhu ruangan selama 48 jam dan hasil yang didapatkan terbukti bahwa obat sangat stabil.
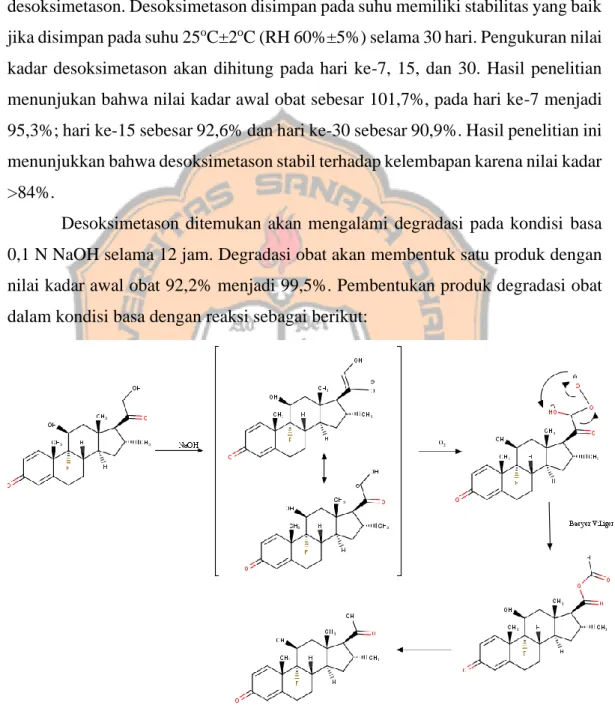
Frankel dan Patel (2012) melakukan penelitian terhadap kelembapan pada desoksimetason. Desoksimetason disimpan pada suhu memiliki stabilitas yang baik jika disimpan pada suhu 25oC±2oC (RH 60%±5%) selama 30 hari. Pengukuran nilai kadar desoksimetason akan dihitung pada hari ke-7, 15, dan 30. Hasil penelitian menunjukan bahwa nilai kadar awal obat sebesar 101,7%, pada hari ke-7 menjadi 95,3%; hari ke-15 sebesar 92,6% dan hari ke-30 sebesar 90,9%. Hasil penelitian ini menunjukkan bahwa desoksimetason stabil terhadap kelembapan karena nilai kadar >84%.
Desoksimetason ditemukan akan mengalami degradasi pada kondisi basa 0,1 N NaOH selama 12 jam. Degradasi obat akan membentuk satu produk dengan nilai kadar awal obat 92,2% menjadi 99,5%. Pembentukan produk degradasi obat dalam kondisi basa dengan reaksi sebagai berikut:
Gambar 6. Mekanisme Pembentukan Degradasi Desoksimetason dalam Kondisi Basa (Srinivasu et al, 2012).
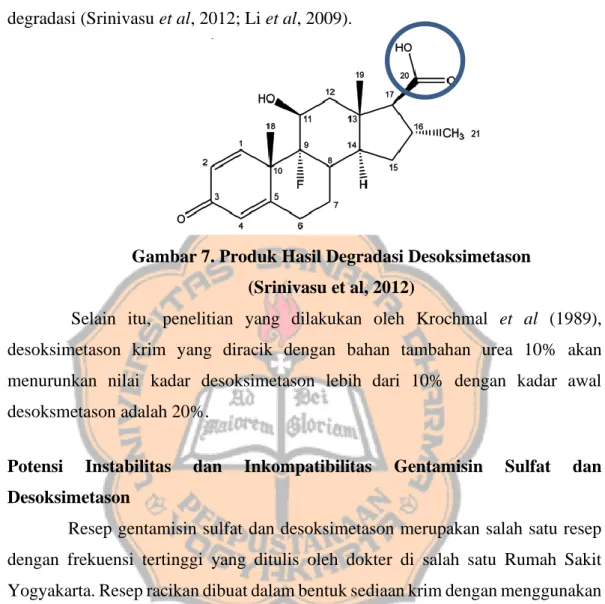
Hasil produk degradasi desoksimetason yang terbentuk adalah 9-alfa-fluoro-11-beta,20-dihidroksi-16alfa-metilpregna-1,4-diene-3,20dione. Reaksi
14
yang terlibat adalah reaksi oksidasi terutama pada rantai 20-keto-21-hidroksi yang akan membentuk gugus asam karboksilat pada rantai C17 pada hasil produk degradasi (Srinivasu et al, 2012; Li et al, 2009).
Gambar 7. Produk Hasil Degradasi Desoksimetason (Srinivasu et al, 2012)
Selain itu, penelitian yang dilakukan oleh Krochmal et al (1989), desoksimetason krim yang diracik dengan bahan tambahan urea 10% akan menurunkan nilai kadar desoksimetason lebih dari 10% dengan kadar awal desoksmetason adalah 20%.
Potensi Instabilitas dan Inkompatibilitas Gentamisin Sulfat dan Desoksimetason
Resep gentamisin sulfat dan desoksimetason merupakan salah satu resep dengan frekuensi tertinggi yang ditulis oleh dokter di salah satu Rumah Sakit Yogyakarta. Resep racikan dibuat dalam bentuk sediaan krim dengan menggunakan gentamisin sulfat krim dan desoksimetason krim. Resep dengan kedua obat tersebut biasanya diindikasikan sebagai terapi dalam penanganan dermatitis atopik (Keles dkk, 2016). Gentamisin sulfat dan desoksimetason juga dapat diresepkan untuk pasien yang menderita paronikia kronis (Ningtyas dan Sibero, 2019).
Berdasarkan hasil wawancara dengan Apoteker Penanggung Jawab, tahapan yang dilakukan pada saat melakukan peracikan kedua obat ini adalah mencampur langsung gentamisin sulfat krim dan desoksimetason krim ke dalam mortir yang tersedia. Pada proses peracikan obat ini, tidak dilakukan penambahan bahan tambahan lain dan tidak dilakukan pengenceran. Pengenceran sediaan krim
15
hanya dapat dilakukan jika sesuai pengenceran yang cocok dan harus dilakukan dengan teknik aseptis (Cartika, 2016). Jika dilakukan pengenceran pada peracikan obat ini akan memungkinkan terjadi potensi perubahan volume dan konsentrasi dari obat racikan. Gentamisin krim yang digunakan memiliki berat massa 10 g dan desoksimetason memiliki berat massa 10 g sehingga sediaan racikan kedua obat memiliki total berat massa 20 g. Berat massa yang semakin besar pada sediaan racikan akan memungkinkan untuk mempengaruhi penurunan konsentrasi dari sediaan racikan. Jika konsentrasi obat menurun, maka efikasi pada pasien dalam penggunaan sediaan racikan tersebut akan berpotensi menurun juga.
Penggunaan sediaan krim pada peracikan gentamisin sulfat dan desoksimetason akan lebih rentan untuk mengalami degradasi dan kontaminasi mikroba dikarenakan berdasarkan formulasinya sediaan krim mengandung air lebih banyak dibandingkan dengan sediaan ointment. Berdasarkan Farmakope Indonesia edisi III (1979), sediaan krim mengandung tidak kurang dari 60%. Degradasi obat dan kontaminasi mikroba merupakan salah satu bentuk dari instabilitas obat (Bajaj et al, 2012). Kontaminasi mikroba pada sediaan racikan dapat mempengaruhi sifat fisika dari sediaan serta mengubah sifat kandungan bahan aktif. Perubahan ini akan mempengaruhi potensi efikasi dan keamanan pada pasien (Heinrich, 2003).
Berdasarkan kondisi ruang peracikan yang digunakan untuk meracik sediaan gentamisin sulfat dan desoksimetason, apoteker penanggung jawab menyatakan bahwa ruang racikan terlindung dari paparan sinar matahari. Gentamisin sulfat dan desoksimetason merupakan senyawa yang stabil terhadap cahaya (Cote et al, 2010; Srinivasu, 2012). Hal ini menunjukkan bahwa potensi terjadinya instabilitas yang disebabkan oleh cahaya tidak dimungkinkan terjadi. Selain itu, gentamisin sulfat dan desoksimetason juga stabil terhadap suhu (Rizk et al, 1995; Srinivasu, 2012). Peracikan sediaan racikan gentamisin sulfat dan desoksimetason dilakukan di ruangan dengan suhu yang diatur pada 25oC. Rata-rata suhu udara di Kabupaten Sleman pada bulan Januari-April 2019 yaitu 26oC. Hal ini juga menunjukkan bahwa tidak ada potensi terjadinya instabilitas dari sediaan racikan yang mungkin terjadi.
16
Desoksimetason cenderung stabil ketika disimpan pada suhu 25oC±2oC dengan nilai kelembapan relatif 60%±5% (Frankel dan Patel, 2012). Berbeda dengan desoksimetason, gentamisin sulfat tidak stabil pada penyimpanan 40oC dengan nilai kelembapan relatif 70% dan akan mengalami degradasi sebesar 67% (Freiess and Schlapp, 2006). Kadar kelembaban relatif pada bulan Januari hingga April 2019 di Kabupaten Sleman, Yogyakarta berada pada rentang 84-88% (BMKG Stasiun Geofisika Yogyakarta, 2019). Hal ini menunjukkan adanya potensi degradasi gentamisin sulfat. Jika dilakukan peracikan antara gentamisin sulfat dan desoksimetason pada kelembapan tersebut maka akan sangat berpotensi untuk mempengaruhi stabilitas sediaan racikan. Namun, diperlukan penelitian lebih lanjut mengenai efek terapi akibat adanya degradasi gentamsin sulfat. Kelembapan juga dapat mempengaruhi tumbuhnya mikroba pada sediaan racikan. Hal ini didukung dengan bentuk sediaan krim yang memiliki kandungan air yang tinggi sehingga meningkatkan potensi terjadinya kontaminasi mikroba.
Sediaan racikan gentamisin sulfat dan desoksimetason tidak ditemukan adanya data yang menunjukkan terjadinya inkompatibilitas pada kedua obat. Salah satu basis krim yang digunakan pada gentamisin sulfat krim adalah propilen glikol (Gardezi et al, 2016). Basis krim yang digunakan dalam pembuatan desoksimetason krim adalah petrolatom putih, isopropil miristat, lanolin alkohol, mineral oil, dan ketostearil alkohol (Gad, 2008). Pada peracikan ini, basis krim pada masing-masing sediaan tidak ditemukan adanya instabilitas maupun inkompatibilitas satu dengan yang lainnya.
Sediaan racikan krim yang mengandung gentamisin sulfat dan desoksimetason menggunakan pot plastik transparan sebagai wadah tempat sediaan racikan. Namun, bahan pembuatan dari pot tersebut tidak diketahui. Gentamisin sulfat dan desoksimetason tidak ditemukan adanya inkompatibilitas tehadap pot plastik transparan yang digunakan. Hal ini menunjukkan bahwa penggunaan pot plastik transparan aman digunakan sebagai wadah sediaan racikan gentamisin sulfat dan desoksimetason.
17 KESIMPULAN
Dari penelitian ini dapat disimpulkan bahwa resep racikan sediaan krim yang mengandung gentamisin sulfat dan desoksimetason aman untuk dilakukan. Potensi instabilitas pada sediaan racikan diperkirakan dipengaruhi oleh kelembapan. Kelembapan juga dapat mempengaruhi peningkatan terjadinya kontaminasi mikroba pada sediaan racikan krim yang diracik. Namun, sediaan racikan ini tidak berpotensi mengalami inkompatibilitas.
SARAN
Peracikan sediaan krim gentamisin sulfat dan desoksimetason dapat dilakukan dengan memperhatikan kebersihan dari ruangan dan alat yang digunakan untuk memperkecil potensi terjadinya kontaminasi mikroba yang dapat mempengaruhi stabilitas sediaan krim. Jika diperlukan dapat ditambahkan bahan tambahan berupa pengawet pada sediaan krim. Meskipun demikian, potensi instabilitas dan inkompatibilitas yang ditemukan dalam studi ini masih berdasar pada studi literatur, sehingga perlu dilakukan penelitian eksperimental untuk mengetahui profil stabilitas dan kompatibilitas sediaan racikan krim yang mengandung gentamisin sulfat dan desoksimetason.
18
DAFTAR PUSTAKA
Akram, M., El-didanmony, A., Ghoinem A., et al, 2006. Indirect spectrophotometric determination of gentamicin and vancomycin antibiotics based on their oxidation by potassium permanganate, Central European Journal of Chemistry, Volume 4(4), 708-722.
Anonim, 2020a, Gentamicin Sulfate Salt, Merck, https://www.sigmaaldrich.com/catalog/product/sial/e003632?lang=en® ion=ID
Anonim, 2020b. Gentamicin [WWW Document]. Drugbank,. URL https://www.drugbank.ca/drugs/ DB00798
Anonim, 2020c. Reaction of Amine, Encyclopædia Britannica, Inc., https://www.britannica.com/science/amine/Reactions-of-amines
Anonim, 2020d. Desoximetasone [WWW Document]. Drugbank,. URL https://www.drugbank.ca/drugs/DB00547
Bagel, Jerry, and Nelson, Elise, 2018. An Open-label, Observational Study Evaluating Desoximetasone Topical Spray 0.25% in Patients with Scalp Psoriasis, J Clin Aesthet Dermatol, Volume 11(5), 27-29
Bajaj, S., Singla, D., and Sakhuja, N., 2012, Stability testing of pharmaceutical products, Journal of Applied Pharmaceutical Science, Volume 2 (3), 129-138.
Bharate, Sonali S., Bharate, Sandip B.,and Bajaj, Amrita N., 2010, Interactions and incompatibilities of pharmaceutical excipients with active pharmaceutical ingredients: A comprehensive review, Journal of Excipients and Food Chemicals, Volume 1 (3).
Black, J., et al., 1964, Pharmacology of Gentamicin, New Broad Spectrum Antibiotic in Sylvester, p.138-147.
BMKG Stasiun Geofisika Kelas I Yogyakarta, 2019. Prakiraan Cuaca DI Yogyakarta [WWW Document]. Badan Meteorologi, Klimatologi, dan
Geofisika,. URL
19
BPOM Republik Indonesia., 2019. Sagestam (online), http://pionas.pom.go.id/monografi/gentamisin 6 Mei 2020
BPOM Republik Indonesia., 2019. Sagestam (online), http://pionas.pom.go.id/obat/sagestam 8 Maret 2020.
BPOM Republik Indonesia., 2019. Topcort (online), http://pionas.pom.go.id/obat/topcort 15 Maret 2020.
Cartika, Harpolia, 2016. Kimia Farmasi Komprehensif
Cote, D., Lok, C., Battistella, M., et al., 2010. Stability of Trisodium Citrate and Gentamicin Solution for Catheter Locks after Storage in Plastic Syringes at Room Temperature, Can J Hoop Pharm, Volume 63(4), 304-311.
Fleischer, David M., et al., 2017. Atopic Dermatitis: Skin Care and Topical Therapies, Seminars in Cutaneous Medicine and Surgery, Volume 63 (176-187).
Frankel, A., Patel, B., 2012. Compatibility Study Examining the Physical and Chemical Stability of Calcipotriene Ointment 0.005% With Three Topical Corticosteroids: Clobetasol Ointment 0.05%, Desoximetasone Ointment 0.25%, and Desoximetasone Ointment 0.05%. Psoriasis Forum, 18(2), 72– 74
Friess, Wolfgang and Schlapp, Monica, 2006. Sterilization of gentamicin containing collagen/PLGA microparticle composites, European Journal of Pharmaceutics and Biopharmaceutics, Volume 36 (3)
Gad, Shayne Cox, 2008, Pharmaceutical Manufacturing Handbook
Gardezi, Ali I., Schlageter, Karen W., C., Foster Brad, et al, 2016. Erosion of the Silicone Peritoneal Dialysis Catheter with the Use of Gentamicin Cream at the Exit Site. Advances in Peritoneal Dialysis, Vol. 32
Graham, A.E., Speicher, E., and Williamson, B. 1997. Journal of Pharmaceutical and Biomedical Analysis, Vol. 15 (537-543).
Grote, Jonathan, Himmelsbach, Richard and Johnson, Don, 2012. Methodology for the rapid separation of gentamicin components and regiospecific synthesis of gentamicin conjugates. Vol. 53 (6751-6754).
20
Gudeman, J., Jozwiakowski, M., Chollet, J., and Randell M., 2013. Potential Risk of Pharmacy Compounding. Drug R D, 13, 1-8.
Guharoy, R., J. Noviasky, Z. Haydar., et al., 2013. Compounding pharmacy conundrum: "We cannot live without them but we cannot live with them" according to the present paradigm. Chest, Volume 143 (4), 896-900. Heinrich, J., 2003. State and Federal Oversight of Drug Compounding by
Pharmacies, United State : General Accounting Offive
Jao, Rodolfo L. and Jackson, George Gee, 1964, Gentamicin Sulfate, New Antibiotic Against Gram-Negative Bacilli, Jama, Volume 189 (11).
Keles, Flinka F., Pandaleke, Herry E.J., dan Mawu, Ferra O., 2016, Profil Dermatitis Atopik Pada Anak di Poliklinik Kulit Dan Kelamin RSUP Prof. Dr. R. D. Kandou Manado Periode Januari 2013 – Desember 2015. Jurnal E-Clinic, Vol. 4(2).
Kementrian Kesehatan Republik Indonesia. 2014. Farmakope Indonesia. Edisi V. Direktorat Jenderal Bina Kefarmasian dan Alat Kesehatan, Jakarta.
Kibbe, A.H., 2000, Pharmaceutical Excipients Third Edition. American Pharmaceutical Association, Washington, D.C.
Kristina, S.A., Chairun Wiedyaningsih, Niken Nur Widyakusuma, Hardika Aditama, 2017, Extemporaneous Compounding Practice by Pharmacists : A Systematic Review, International Journal of Pharmacy and Phamaceutical Sciences, Volume 9 (2).
Krochmal, Lincoln, Wang, Jonas C.T., Patel, B. et al, 1989. Topical corticosteroid compounding: Effects on physicochemical stability and skin penetration rate, Journal of the American Academy of Dermatology, Volume 21(5) 979-984.
Kurniawan, B. R., 2013. Stabilitas Resep Racikan yang Berpotensi Mengalami Inkompatibilitas Farmasetika yang Disimpan pada Wadah Tertutup Baik, Jurnal Ilmiah Mahasiswa Universitas Surabaya, Volume 2 (2).
Li, Min, Chen, Bin, Monteiro, Stephanie, et al., 2009. Mechanism of base-catalyzed autooxidation of corticosteroids containing 20-keto-21-hydroxyl side chain, Tetrahedron Letters, Vol. 50 (4574-4581).
21
Lochman, Petr, Paral, Jiri, and Koci, Jaromir, 2011. Gentamicin bound to the nanofibre microdispersed oxidized cellulose in the treatment of deep surgical site infections. Journal of Applied Biomedicine Vol. 9(143-149) Makeen HA., Pancholi SS., Alhazmi HA.,Ezzi AA., Hazzazi AJA., Meraya AM.,
2018, Stability Testing of Extemporaneous Preparation of Methyl Salicylate Ointment, Journal of Health Specialties, Volume 6 (2).
Martin, Sandra E., and Garrone, Analia, 2002. Efficient solvent-free iron(III) catalyzed oxidation of alcohols by hydrogen peroxide. Tetrahedron Letters, Vol. 44 (549-552).
McMurry, J., 2011. Fundamentals of Organic Chemistry, Seventh Edition. Cengange Learning, USA.
Minghetti, P., Pantano, D., C., Gennari, et al., 2014, Regulatory framework of pharmaceutical compounding and actual developments of legislation in Europe, Health Policy, Volume 117 (3), 328-333.
Mullin, N., Deadman, B., Moynihan, H., et al., 2016. The impact of storage
conditions upon gentamicin coated antimicrobial, Journal of
Pharmaceutical Analysis, Volume 6(6), 374-381.
Ningtyas, Nurma Retno dan Sibero, Hendra Tarigan, 2019. Penggunaan Antibiotik Kombinasi Antifungal Sistemik Dan Kortikosteroid Topikal Sebagai Tatalaksana Paronkia Kronik. Medical Journal of Lampung University, Vol. 8(2).
Patwardhan, N., A., De, Kulkarni, K., et al., 2017. Pharmacological Properties and Therapeutic Efficacy in the Treatment of Steroid Responsive Dermatoses, International Journal of Health Sciences & Research, Volume 7(12), 290-298.
Pennington, J. E., Dale, D. C., Reynolds, H. Y., MacLowry, J. D, 1975, Gentamicin sulfate pharmacokinetics: lower levels of gentamicin in blood during fever, Journal of Infectious Diseases, Volume 132(3), 270-275.
22
Pubchem. 2020. Gentamicin Sulfate.
https://pubchem.ncbi.nlm.nih.gov/compound/Gentamicin-sulphate diakses pada tanggal 5 Maret 2020
Pubchem. 2020. Desoxymethasone.
https://pubchem.ncbi.nlm.nih.gov/compound/Desoxymethasone diakses pada tanggal 7 April 2020
Randell, M. D., and Duffy, P. J., 2014. Risk and Liabilities of Prescribing Compounded Medication. Postgraduate Medicine, 126(4), 179.
Rizk, M., Zakhari, A., and Carreira, A., 1995. Fluorometric Determination of Aminoglycoside Antibiotics Using Lanthanide Probe Ion Spectroscopy, Elsevier Science, Volume 42, 1849-1856.
Rochjana et al, 2019. Masalah Farmasetika dan Interaksi Obat pada Resep Racikan Pasien Pediatri: Studi Retrospektif pada Salah Satu Rumah Sakit di Kabupaten Bogor, Jurnal Farmasi Klinik Indonesia, Volume 8 (1).
Sellers, S., and Utian, W., 2012. Pharmacy compounding primer for physicians: Prescriber beware, Journal of Drug, Volume 72 (16), 2043-2050.
Singh S., and Bakshi M., 2000, Guidance on conduct of stress test to determine inherent stability of drugs. Pharm Technol Asia, Special Issue, Sep./Oct. 24-36.
Sombié, Bavouma Charles, Yameogo, B Gérard Josias, Semdé, Rasmané, et al., 2014. Stability Study in Accelerated Conditions of Based Gel Used in the Treatment of Chronic Osteomyelitis, American Journal of Advanced Drug Delivery, Volume 2(2), 203-212.
Stoker, H.S., 2016. General, Organic and Biological Chemistry. USA: Cengange Learning. P.524.
Srinivasu, P., Sudhakarbabu, K., Sreeramulu, J., 2012. Identification,
characterization of degradation component in desoximetasone
pharmaceutical dosage forms and its quantification in the presence of process related impurities. Journal of Liquid Chromatography and Related Technologies, Volume 35 (8).
23
Sweetman, S.C. 2009. Martindale The Complete Drug Reference. Thirty sixth edition. London: Pharmaceutical Press.
United States Pharmacopeia 32, 2009. United States Pharmacopeia 32 NF 27. U.S Food & Drug Administration, 2018, Compounding and the FDS : Questions
and Answers(online),
https://www.fda.gov/drugs/human-drug-compounding/compounding-and-fda-questions-and-answers diakses pada 23 September 2019.
Vladimirov, Sote, Cudina, Olivera, Agbaba, Danica, et al, 1995. Spectrophotometric determination of desoximetasone in ointment using 1,4-dihydrazinophthalazine, Journal of Pharmaceutical and Biomedical Analysis. Vol. 14 (947-950).
Wardiyah, 2016. Kimia Organik
Watson, David G., Lin, Mei, Morton, Andrew et al, 2005. Compatibility and stability of dexamethasone sodium phosphate and ketamine hydrochloride subcutaneous infusions in polypropylene syringes, Journal of Pain and Symptom Management, Volume 30(1), 80-86.
Zakova, Maria, et al., Dose Derivation of Once-Daily Dosing Guidelines for Gentamicin in Critically Ill Pediatric Patients, The Drug Monitoring, Vol. 36 (233-294).
Zed, Mestika, 2004, Metode Penelitian Kepustakaan, Jakarta: Yayasan Obor Indonesia
24
BIOGRAFI PENULIS
Penulis naskah skripsi berjudul “Studi Literatur Potensi Instabilitas dan Inkompatibilitas Sediaan Racikan Krim yang Mengandung Gentamisin Sulfat dan Desoksimetason” bernama lengkap Junia Brigita Tamara, lahir di Pontianak pada tanggal 29 Juni 1998. Penulis merupakan anak pertama dari dua bersaudara dari pasangan Aiysong dan Noriana Naun. Penulis menempuh pendidikan formal di TK Swasta Suster Pontianak (2003-2004), SD Swasta Suster Pontianak (2004-2010), SMP Swasta Suster Pontianak (2010-2013), SMA Santu Petrus Pontianak (2013-2016) dan melanjutkan Pendidikan Sarjana di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta pada tahun 2016. Selama menempuh pendidikan di perguruan tinggi tersebut, penulis aktif di beberapa organisasi dan kepanitiaan. Penulis aktif dalam organisasi Jaringan Mahasiswa Kesehatan Indonesia komisariat Universitas Sanata Dharma pada periode 2017/2018 sebagai anggota divisi infokom dan Pengurus JMKI wilayah Yogyakarta 2018/2019 sebagai anggota departemen infokom. Penulis aktif dalam berbagai kepanitiaan seperti seperti Pharmalympic 2017 sebagai koordinator publikasi dan dokumentasi, Titrasi 2018 sebagai koordinator publikasi dan dokumentasi, dan Pharmacy Performance sebagai koordinator publikasi dan dokumentasi. Penulis juga pernah menjadi Asisten Praktikum Farmasi Fisika (2017/2018), Asisten Praktikum Biofarmasetika Farmakokinetika (2018/2019), Asisten Praktikum Formulasi dan Teknologi Sediaan Farmasi (2018/2019)