PENENTUAN KADAR BESI DENGAN METODA SPEKTROFOTOMETER MENGGUNAKAN SPEKTRONIC-20
LAPORAN PRAKTIKUM
disusun untuk memenuhi salah satu tugas praktikum mata kuliah Instrumentasi Analitik
Dosen Pembimbing: Ari Marlina, Dra., M.Si.
Oleh:
Kelompok 1 Kelas 1B - TK
Arya Wibisono NIM 161411033 Cahya Handayani NIM 161411034 Ditta Atsna Nuriya S NIM 161411035 Dwiki Abdurrahman NIM 161411036
PROGRAM STUDI D3-TEKNIK KIMIA JURUSAN TEKNIK KIMIA
POLITEKNIK NEGERI BANDUNG BANDUNG
Judul Percobaan : Penentuan Kadar Besi menggunakan Sp. Spektronic-20 Pembimbing : Ari Marlina, Dra., M.Si.
Tanggal Percobaan : 13 Maret 2017
I. TUJUAN PERCOBAAN
1. Untuk menentukan kadar besi total
2. Dapat mengoprasikan spektronic-20 dengan benar 3. membuat kurva kalibrasi Fedengan benar
II. DASAR TEORI
Spectronic-20 adalah spectrofotometer absorpsi sinar tampak berkas tunggal. Spektrofotometer merupakan alat yang digunakan untuk mengukur absorbansi dengan cara melewatkan cahaya dengan panjang gelombang tertentu pada suat objek/kuvet yang berisi larutan blanko/sampel.
Spektronik-20 merupakan spektrometer
visible yang susunannya menggunakan satu berkas tunggal (single beam). Spektrofotometer jenis ini memiliki susunan paling sederhana yang terdiri dari sumber sinar, monokromator, kisi difraksi dan sistem pembacaan secara langsung.
Dalam analisis dengan spektrofotometri digunakan suatu sumber radiasi pada daerah sinar tampak, yaitu pada panjang gelombang 380-750 nm. Spektrum yang diperoleh akan lebih ideal, yaitu dengan lebar pita kurang 1 nm. Hal ini dikarenakan instrument yang digunakan (spektrofotometer) dilengkapi dengan system optic (yang dapat menghasilkan sebaran/dispers radiasi elektromagnetik yang masuk) dan alat untuk mengukur intensitas radiasi yang diteruskan.
Panjang Gelombang (nm) Warna Warna Komplementer
400-435 Ungu Hijau kekuningan
435-480 Biru Kuning
480-490 Biru kehijauan Jingga 490-500 Hijau kebiruan Merah
560-580 Hijau kekuningan Ungu
595-610 Jingga Biru kehijauan
610-680 Merah Hijau kebiruan
680-700 Ungu kemerahan Hijau
Tabel 1. Hubungan Warna dengan Warna Komplementer
Cahaya putih dari lampu wolfram difokuskan oleh lensa A ke celah masuk; lensa B mengumpulkan cahaya dari celah masuk itu dan memfokuskan ke celah keluar setelah dipantulkan dan didespersikan oleh kisi difraksi untuk memperoleh berbagai panjang gelombang. Cahaya monokromatik yang menembus celah keluar melewati sampel yang akan diukur dan jatuh ke tabung foto.
Prinsip kerja spektrofotometri berdasarkan Hukum Lambert-Beer, bila cahaya monokromatik (I0) melalui suatu media (larutan), maka sebagian cahaya tersebut akan
diserap (Ia), sebagian dipantulkan (Ir), dan sebagian lagi diteruskan (It). Berdasarkan
hukum Lambert-Beer, rumus yang digunakan untuk menghitung banyaknya cahaya yang dihamburkan:
Dan absorbansi dinyatakan dengan rumus:
Dimana I0 merupakan intensitas cahaya datang dan It atau I1 adalah intensitas
cahaya setelah melewati sampel. Rumus yang diturunkan dari Hukum Beer dapat ditulis sebagai:
Dimana:
A= Absorbansi
c = Konsentrasi larutan yang diukur
ε = Tetapan absorbtivitas molar (jika konsentrasi larutan yang diukur dalam ppm) b = Tebal larutan (tebal kuvet diperhitungkan juga umumnya 1cm)
Dari persamaan Lambert-Beer di atas menunjukkan bahwa absorbansi (A) berbanding lurus dengan konsentrasi larutan (c). Jika dibuat suatu kurva antara absorbansi (A) lawan konsentrasi (c), maka akan diperoleh suatu kurva kalibrasi atau kurva standar, yang dapat digunakan untuk menentukan konsentrasi larutan uji (sampel) setelah absorbansi dari larutan uji tersebut diukur.
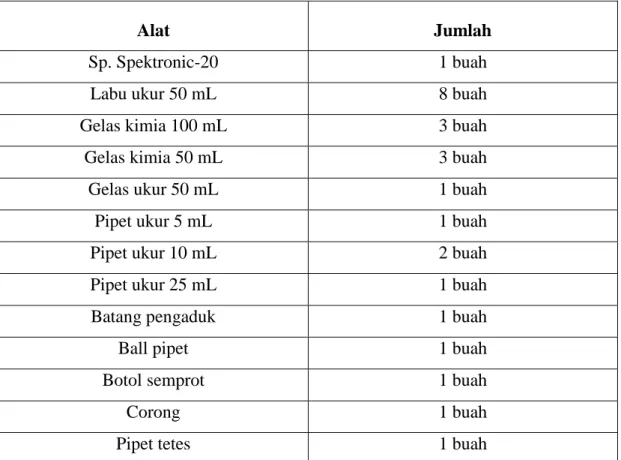
III. ALAT BAHAN
Alat Jumlah
Sp. Spektronic-20 1 buah
Labu ukur 50 mL 8 buah
Gelas kimia 100 mL 3 buah
Gelas kimia 50 mL 3 buah
Gelas ukur 50 mL 1 buah
Pipet ukur 5 mL 1 buah
Pipet ukur 10 mL 2 buah
Pipet ukur 25 mL 1 buah
Batang pengaduk 1 buah
Ball pipet 1 buah
Botol semprot 1 buah
Corong 1 buah
Pipet tetes 1 buah
Tabel 2. Alat yang digunakan
Bahan Jumlah
Larutan Hidroksilamin-HCl 10% 50 mL
Tabel 3. Bahan yang digunakan
IV. PROSEDUR KERJA A. Persiapan Larutan
1. Menyiapkan 8 buah labu takar 50 mL
2. Menambahkan larutan standar kedalam masing-masing labu (Fe3+ 100 ppm) sebanyak 0 mL; 0,5 mL; 1 mL; 1,5 mL; 2 mL; 2,5 mL; 3 mL; dan 3,5 mL 3. Menambahkan 0,5 mL larutan Hidroksilamin-HCl 10% , 5 mL larutan Na
asetat dan 5 mL larutan O-Fenantrolin ke dalam masing-masing labu 4. Mengencerkan hingga tanda batas dan menggojoknya (dihomogenkan)
No. Fe (II) 100 ppm (mL) Hidroksilamin - HCl 10% (mL) Na Asetat 10% (mL) O-Fenantrolin 0,1 % (mL) Aquadest hingga (mL) 1 0 0,5 5 5 50 2 0,5 0,5 5 5 50 3 1,0 0,5 5 5 50 4 1,5 0,5 5 5 50 5 2,0 0,5 5 5 50 6 2,5 0,5 5 5 50 7 3,0 0,5 5 5 50 8 3,5 0,5 5 5 50
Tabel 4. Pembuatan Larutan Deret Standar
Larutan baku Fe3+ 100 ppm 50 mL Larutan O-Fenantrolin 50 tetes
B. Pengukuran dengan Sp. Spektronic-20
a. Penentuan panjang gelombang maksimum
1. Menghubungkan alat dengan sumber listrik dan menyalakan alat dengan memutar (ke kanan) tombol yang terletak di bagian depan bawah sebelah kiri (dan memanaskannya selama 30 menit)
2. Mengatur skala pada posisi 0 dengan memutar tombol bagian depan bawah sebelah kiri
3. Mengatur panjang gelombang yang diinginkan
4. Memasukan kuvet atau sel yang berisi larutan blanko ke dalam alat 5. Mengatur skala %T pada posisi 100% dengan memutar tombol bagian
depan bawah, sebelah kanan
6. Mengganti larutan blanko dengan larutan standar yang berkonsentrasi sedang dan mengubah panjang gelombang sesuai dengan senyawa yang akan diukur
7. Mencatat nilai %T yang tertera pada alat
8. Mengulangi langkah 2, 3, 4, 5 dan 6 sampai diperoleh panjang gelombang maksimum
9. Membuat kurva antara panjang gelombang, lawan absorbsi, A (mengubah %T menjadi A) dan menentukan panjang gelombang maksimumnya
b. Penentuan kurva kalibrasi dan konsentrasi cuplikan
1. Mengulangi pengerjaan/langkah (a) ke 2, 3, 4 dan 5 (mengatur panjang gelombang pada panjang gelombang maksimum yang diperoleh dari percobaan sebelumnya)
2. Mengganti larutan blanko dengan larutan standar dari konsentrasi yang paling rendah dan mencatat nilai %T
3. Mengulangi pengerjaan no. 2 dengan mengganti larutan standar yang berbeda-beda konsentrasinya
5. Mengulangi pengerjaan no. 2 dengan mengganti larutan standar dengan larutan cuplikan (sampel) dan mencatat nilai %T
V. MSDS A. Fe (II)
Sifat Kimia dan Sifat Fisika
1. Nama Kimia : Fe atau Ferrum 2. Nomor Atom : 26
3. Warna : Logam berwarna perak abu-abu, yang bersifat reaktif dengan oksigen dan air,sehingga mudah membentuk karat. 4. Jumlah : Besi adalah elemen nomor 4 terbesar di
kerak bumi.
5. Sifat : Besi murni bersifat lunak( lebih lunak darialumunium), tetapi dapat diperkeras dan diperkuat dengan campuran lain seperti carbon dengan proses smelting. Bahaya Besi bagi Kesehatan
1. Besi adalah mineral yang diperlukan oleh tubuh manusia untuk pembentukan hemoglobin.
2. Besi dapat ditemukan di sumber makanan daging dan sayur-sayuran. 3. Besi dapat menimbulkan masalah kesehatan conjunctivitis, choroiditis,
retinitis jika kontak dan besi tetap permanen didalamnya.
4. Inhalasi kronik debu atau fume dari besi oksida bisa menimbulkan masalah kesehatan pneumoconiosis jinak yang dinamakan siderosis dan meningkatkan resiko kanker paru-paru.
5. LD 50 ( oral, rat ) : 30 gm/kg Bahaya Lingkungan Besi
Iron ( III )-O-arsenite, pentahydrate dapat berbahaya untuk lingkungan, terutama terhadap tumbuh-tumbuhan, air dan udara. Sangat direkomendasikan supaya lingkungan tidak tercemar oleh kimia ini. Aplikasi Kesehatan Kerja Besi
1. Pig iron untuk industri : kompor, pipa, radiator, rel kereta api. 2. Stainless steel untuk : alat rumah tangga, alat kesehatan.
B. Hikdrosilamin – HCl Sifat Kimia
1. Nama Kimia : Hydroxylamine Hydrochloride 2. Rumus Kimia : NH2OH.HCl
Identifikasi Bahaya
1. Mata : Menyebabkan iritasi pada mata, kerusakan pada mata, dan kebutaan
2. Kulit : Menyebabkan peradangan pada kulit dan menimbulkan kegatalan
3. Inhalasi : Menghirup debu akan menghasilkan iritasi pada saluran gastro-intestinal atau saluran pernapasan, yang ditandai dengan pembakaran, bersin dan batuk.
Pertolongan Pertama
1. Kontak Mata : Cek dan lepas jika menggukan kontak lensa. Bilas dengan air mengalir selama 15 menit. 2. Kulit : Bilas bagian kulit yang terkena zat dengan air
mengalir selama 15 menit. Lepas dan cuci pakaian yang terkena zat. Gunakan krim anti – bakterial bila diperlukan. Hubungi dokter apabila terjadi iritasi serius.
3. Inhalasi : Bawa korban ke udara segar, beri korban beberapagelas susu atau air. Bila diperlukan beri korban oksigen. Hubungi dokter.
Penanganan Kebakaran
1. Titik nyala : 152°C (305.6°F).
2. Media pemadam : Bila terjadi kebakaran kecil gunakan bubuk kimia kering. Apabila terjadi kebakaran besar gunakan semprotan air, kabut atau busa.
C. Na Asetat Sifat Kimia
1. Nama Kimia : Sodium acetate 2. Rumus Kimia : CH3COONa Identifikasi Bahaya
1. Mata : Menyebabkan iritasi pada mata, kerusakan pada mata, dan kebutaan
2. Kulit : Menyebabkan peradangan pada kulit dan menimbulkan kegatalan
saluran gastro-intestinal atau saluran pernapasan, yang ditandai dengan pembakaran, bersin dan batuk.
Pertolongan Pertama
1. Kontak mata : Periksa dan lepaskan lensa kontak. Dalam kasus kontak, segera basuh mata dengan banyak air selama minimal 15 menit. Air dingin dapat digunakan. Dapatkan bantuan medis jika terjadi iritasi.
2. Kontak Kulit : Cuci dengan sabun dan air. Tutupi kulit yang teriritasi dengan emolien. Dapatkan bantuan medis jika terjadi iritasi. Air dingin dapat digunakan.
3. Inhalasi : Jika terhirup, pindahkan ke udara segar. Jika tidak bernapas, berikan pernapasan buatan. Jika sulit bernapas, berikan oksigen. Dapatkan medis perhatian jika gejala muncul.
4. Proses menelan : Jangan memaksakan muntah kecuali diarahkan untuk melakukannya oleh tenaga medis. Tidak pernah memberikan apapun melalui mulut
kepada sadar
orang. Kendurkan pakaian ketat seperti kerah, dasi, ikat pinggang atau pinggang. Dapatkan bantuan medis jika gejala muncul.
D. O – Fenantrolin Sifat Kimia
1. Nama Produk : Phenanthroline monohydrate 2. Rumus Kimia : C12H8N2.H2O
Identifikasi Bahaya
Sangat berbahaya dalam kasus menelan. Berbahaya dalam kasus kontak kulit (iritan), kontak mata (iritan), inhalasi. Sedikit berbahaya dalam kasus kontak kulit (permeator). Parah over-exposure dapat mengakibatkan kematian.
Pertolongan Pertama
1. Kontak mata : Periksa dan lepaskan lensa kontak. segera siram mata dengan air yang mengalir sedikitnya 15 menit, dengan kelopak mata tetap dibuka. Air dingin dapat digunakan. Jangan gunakan salep mata. Mencari bantuan medis.
2. Kontak Kulit : Setelah kontak dengan kulit, segera cuci dengan banyak air. Lembut dan benar-benar mencuci kulit terkontaminasi dengan berjalan air dan sabun non-abrasif. Sangat berhati-hati untuk membersihkan lipatan, celah-celah, lipatan dan pangkal paha. Tutupi kulit yang teriritasi dengan yang melunakkan. Jika terjadi iritasi, mencari perhatian medis. Cuci pakaian yang terkontaminasi sebelum menggunakan kembali. Bila terjadi iritasi serius cuci dengan sabun desinfektan dan menutupi kulit terkontaminasi dengan krim anti-bakteri. Hubungi dokter. 3. Inhalasi : Biarkan korban untuk beristirahat di area yang
berventilasi. Mencaribantuan medis segera. Bila terjadi inhalasi serius evakuasi korban ke daerah yang aman secepatnya. Kendurkan pakaian ketat seperti kerah, dasi, ikat pinggang atau pinggang. Jika sulit bernafas, berikan oksigen. Jika korban tidak bernafas, melakukan mulut ke mulut. Hubungi dokter
4. Proses menelan : Jangan memaksakan muntah. Periksa bibir dan mulut untuk memastikan apakah jaringan yang rusak, indikasi kemungkinan bahwa bahan beracun tertelan; tidak adanya tanda-tanda seperti itu, bagaimanapun, tidak konklusif. Kendurkan pakaian ketat seperti leher, dasi, ikat pinggang atau pinggang. Jika korban tidak bernafas, melakukan mulut ke mulut. Mencari perhatian medis segera.
VI. DATA PENGAMATAN A.Pembuatan Larutan Deret Standar
Perlakuan Pengamatan
Pemipetan dari larutan induk
Larutan induk tidak berwarna sehingga pada saat pemipetan larutan induk kedalam labu ukur, larutan tidak berwarna
Penambahan Hidroksilamin - HCl 10%
Larutan tetap tidak ada perubahan warna
Penambahan Na Asetat 10% Larutan tetap tidak ada perubahan warna
Penambahan O-fenantrolin 0,1 %
Terjadi perubahan warna pada larutan yang mengadung Fe berwarna orange
Pengenceran dan Penandabatasan
Ketika ditambahkan aquadest dan ditanda bataskan
Tabel 5. Data Pengamatan Pembuatan Larutan Deret Standar
VII. DATA PERCOBAAN
Untuk mencari panjang gelombang maksimum digunakan larutan yang berkonsentrasi sedang yaitu 5 ppm dengan panjang gelombang yang diatur antara 400 – 520 nm. Berdasar hasil percobaan didapat data %T sebagai berikut.
Penentuan panjang gelombang
NO Panjang gelombang %T A
1 410 38 0,420
2 420 31,5 0,501
3 430 28 0,553
5 450 21,5 0,667 6 460 19 0,721 7 470 17 0,769 8 480 15,5 0,809 9 490 14,5 0,838 10 500 14 0,854 11 505 14 0,854 12 510 14 0,854 13 520 16 0,796 14 530 22 0,658 15 540 31,5 0,502 16 550 45,5 0,342
Tabel 6. Data Percobaan Penentuan Panjang Gelombang
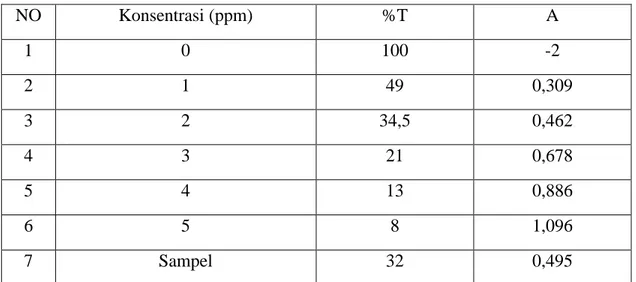
Penentuan kurva kalibrasi ( maks = 505 nm )
NO Konsentrasi (ppm) %T A 1 0 100 -2 2 1 49 0,309 3 2 34,5 0,462 4 3 21 0,678 5 4 13 0,886 6 5 8 1,096 7 Sampel 32 0,495
Kurva Panjang Gelombang Maksimum Fe (5 ppm) Kurva Kalibrasi 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 0 100 200 300 400 500 600 Ab so rb an si (A) Panjang gelombang (ʎ)
Kurva Penentuan Panjang Gelombang Maksimum Fe (5 ppm)
titik ekivalen y = 0.1998x + 0.0868 R² = 0.9968 0 0.2 0.4 0.6 0.8 1 1.2 0 1 2 3 4 5 6 Ab so rb an si (A) Konsentrasi (C)
VIII. PENGOLAHAN DATA
Pembuatan larutan baku Fe(II) 100 mL air dari garam Fe (NH4OH)2SO4
𝑀𝑟 𝑠𝑒𝑛𝑦𝑎𝑤𝑎 𝐴𝑟 𝐹𝑒 = 392 56 = 7 𝑔𝑟𝑎𝑚 𝑙𝑖𝑡𝑒𝑟 = 3,5 𝑔𝑟𝑎𝑚 500 𝑚𝑙 ⁄
Pembuatan O – Fenantrolin 0,1 % untuk 500 ml Artinya massa O – Fenantrolin = 0,1 𝑔𝑟𝑎𝑚⁄100 𝑚𝑙
Jadi untuk membuat 500 ml dibutuhkan o – fenantrolin sebanyak 0,5 gram
Pembuatan Na – Asetat 10 % untuk 500 ml Artinya massa Na – Asetat = 10 𝑔𝑟𝑎𝑚⁄100 𝑚𝑙
Jadi untuk membuat larutan 𝐶𝐻3𝐶𝑂𝑂𝑁𝑎 500 ml dibutuhkan Na – Asetat
sebanyak 50 gram
Pembuatan Hidroksilamin 10% untuk 250 ml Artinya massa Na – Asetat = 25 𝑔𝑟𝑎𝑚⁄100 𝑚𝑙
Jadi untuk membuat Hidroksilamin 250 ml dibutuhkan sebanyak 25 gram
Menghitung Konsentrasi (ppm) o Fe (II) 0 ml V1 x ppm1 = V2 x ppm2 0 x 100 = 50 x ppm2 ppm2 = 0 ppm o Fe (II) 0,5 ml V1 x ppm1 = V2 x ppm2 0,5 x 100 = 50 x ppm2 Ppm2 = 1 ppm o Fe (II) 1 ml V1 x ppm1 = V2 x ppm2 1 x 100 = 50 x ppm2 Ppm2 = 2 o Fe (II) 1,5 ml V1 x ppm1 = V2 x ppm2 1,5 x 100 = 50 x ppm2 Ppm2 = 3 ppm o Fe (II) 2 ml V1 x ppm1 = V2 x ppm2 2 x 100 = 50 x ppm2
Ppm2 = 4 ppm o Fe (II) 2,5 ml V1 x ppm1 = V2 x ppm2 2,5 x 100 = 50 x ppm2 Ppm2 = 5 ppm o Fe (II) 3 ml V1 x ppm1 = V2 x ppm2 3 x 100 = 50 x ppm2 Ppm2 = 6 ppm o Fe (II) 3,5 ml V1 x ppm1 = V2 x ppm2 3,5 x 100 = 50 x ppm2 Ppm2 = 7 ppm
Persamaan garis dari grafik: y = 0.1998x + 0.0868 Kadar sampel: Abs sampel: 0.495 y = 0.1998x + 0.0868 0.495 = 0.1998x + 0.0868 0.1998x = 0.495 – 0.0868 x = 0.4082/0.1998 x = 2.043 ppm IX. PEMBAHASAN
Menurut Arya Wibisono (161411033)
Pada percobaan kali ini, dilakukan analisis penentuan kadar besi Fe(III) dalam sampel air dengan teknik spektrofotometri UV-Vis. Spektrofotometri yang digunakan tepatnya adalah spektrofotometri cahaya tampak, karena logam besi mempunyai panjang gelombang lebih dari 400 nm, sehingga jika menggunakan spktrofotometri UV, logam besi dalam sampel tidak terdeteksi. Spektrofotometer adalah alat untuk mengukur transmitan atau absorban suatu sampel sebagai fungsi panjang gelombang. Syarat analisis menggunakan visibel adalah cuplikan yang dianalisis bersifat stabil membentuk kompleks dan larutan berwarna. Oleh karena itu, dalam penetuan kadar besi dalam air, perlu ditambahakan hidroksilamin-HCl 10% untuk mereduksi Fe3+
menjadi Fe2+. Besi dalam keadaan Fe2+ akan lebih stabil dibandingkan besi Fe3+. Dalam keadaan dasar, larutan besi tidak berwarna sehingga perlu ditambahkan larutan orto-fenantrolin agar membentuk kompleks larutan berwarna.
Reaksi antara besi dengan orto-fenantrolin merupakan reaksi kesetimbangan dan berlangsung pada pH 6 sampai 8. Karena alasan tersebut, pH larutan harus dijaga tetap dengan cara menambahkan garam natrium asetat. Penambahan larutan natrium asetat dilakukan sebelum penambahan orto-fenantrolin. Dalam penentuan kadar fe dalam sampel menggunakan spektrofotometri visibel perlu dibuat larutan standar. Tujuannya adalah untuk membuat kurva kalibrasi yang nantinya akan digunakan untuk menghitung kadar besi dalam sampel air.
Pada percobaan, mula-mula dilakukan penentuan panjang gelombang
maksimum dengan larutan yang mempunyai ppm sedang yaitu 5 ppm dan didapatkan panjang gelombang maksimum sebesar 505 nm, selanjutnya dilakukan penentuan %T pada larutan dengan konsentrasi yang bervariasi yaitu 0 ppm, 1 ppm, 2 ppm, 3 ppm, 4 ppm, 5 ppm didapatkan %T sebesar 100 %, 49 %, 34,5 %, 21 % , 13 %, 8 % maka didapatkan absorbansi (A) dari perhitungan A= log 1
𝑇 sebesar -2 A, 0,309 A,
0,462 A, 0,678 A ; 0,886 A 1,096 A dapat dilihat bahwa semakin tinggi konsentrasi absorbansinya semakin besar oleh karena itu absorbansi dipengaruhi oleh
konsentrasi,lalu dilanjutkan dengan penentuan konsentrasi sampel dari absorbansi 0,495 A didapatkan dari persamaan y = 0,9958x – 1,0063 maka konsentrasi sampel sebesar 1,5 ppm.
Menurut Cahya Handayani (161411034)
Pada praktikum kali ini bertujuan untuk menentukan konsentrasi Fe total, penentuan konsentrasi ini dilakukan dengan metode spektrofotometri. Sebelum menentukan konsentrasi Fe total dilakukan dulu penentuan panjang gelombang maksimum, dan didapat panjang gelombang maksimum Fe sebesar 505 nm.
Pada penentuan kurva kalibrasi larutan yang dicampur dengan Fe 0 ml didapat konsentrasi Fe sebesar 0 ppm dengan nilai absorbansi -2, larutan yang dicampur dengan Fe 0,5 ml didapat konsentrasi Fe sebesar 1 ppm dengan nilai absorbansi 0,309, larutan yang dicampur dengan 1 ml Fe didapat konsentrasi Fe 2 ppm dengan nilai absorbansi
0,462, larutan yang dicampur dengan 1,5 ml Fe didapat konsentrasi Fe sebesar 3 ppm dengan nilai absorbansi 0, 678, larutan yang dicampur dengan larutan Fe 2 ml didapat konsentrasi Fe sebesar 4 ppm dengan nilai absorbansi 0,886, larutan yang dicampur dengan larutan Fe 2,5 ml didapat konsentrasi Fe sebesar 5 ppm dengan nilai absorbansi 1, 096. Pada larutan terakhir nilai absorbansi melebihi 1 dikarenakan beberapa faktor seperti proses pengenceran dan kualitas larutan.
Lalu pada saat penentuan konsentrasi Fe dalam larutan sampel didapat nilai absorbansi sebesar 0,495 dan setelah dilakukan perhitungan didapat konsentrasi Fe dalam sampel sebesar 1,507 ppm
Menurut Ditta Atsna Nuriya Salsabila (161411035)
Pada percobaan ini, dilakukan analisis penentuan kadar besi dengan metoda spektrofotometri UV-Vis. Alat yang digunakan adalah spektrofotometer cahaya tampak,(spektrofotometer-20), karena logam besi mempunyai panjang gelombang berkisar antara 410-580nm.
Dalam penentuan kadar besi, pertama dilakukan pembuatan larutan dengan menambahkan beberapa larutan ke dalam larutan besi, diantaranya penambahan hidroksilamin-HCL, yang berfungsi untuk mereduksi Fe³⁺ menjadi Fe²⁺. Karena besi dengan ion 2+ akan lebih stabil. Lalu ditambahkan larutan natrium asetat agar pH larutan berada pada rentan 6-8. Sehingga dapat ditambahkan larutan orto-fenantrolin yang akan memberikan warna pada larutan agar dapat diukur absorbansinya, karena orto-fenantrolin dapat bereaksi dengan besi pada ph 6-8.
Pada penggunaan spektrofotometri UV-Vis digunakan larutan blanko untuk menstandarisasi. Larutan blanko berbeda dengan larutan sampel dan digunakan sebagai pembanding agar yang terukur hanya absorbansi atau penyerapan zat yang diinginkan. Lalu dilakukan penentuan panjang gelombang maksimum dari larutan standar yaitu larutan yang memiliki konsentrasi tengah (larutan 5) dengan mengganti larutan standar dan blanko diikuti dengan mengatur panjang gelombang. Dan didapat panjang gelombang maksimum sebesar 505nm. Lalu dilakukan pengukuran absorbansi dari larutan besi (II) dengan konsentrasi yang berbeda-beda untuk menentukan kurva larutan sstandarnya. Larutan yang digunakan yaitu larutan besi (II) dengan konsentrasi 1ppm, 2ppm, 3ppm, 4ppm dan 5ppm yang masing-masingnya sudah ditambahkan natrium asetat dan orto-fenantrolin. Lalu diukur dengan panjang gelombang 505nm
dan didapat absorbansi larutan besi (II) untuk masing-masing konsentrasi dari 1 ppm sampai 5 ppm yaitu 0.309 A, 0.462 A, 0.678 A, 0.886 A dan 1.096 A.
Setelah diketahui absorbansi dan panjang gelombangnya maka dilakukan pengukuran sampel dari campuran larutan standar dan didapat absorbansi sebesar 0.495 A. Kemudian untuk mengetahui kadar besi dalam sampel dapat dilakukan dengan membuat grafik hubungan antara absorbansi dengan konsentrasi dengan fungsi linear. Maka didapat y lalu lakukan perhitungan antara persamaan y dengan nilai absorbansi sampel sehingga didapat kadar Fe sebesar 2.043 ppm.
Menurut Dwiki Abdurrahman (161411036)
Praktikum Spektrofotometri kali ini bertujuan untuk menentukan kadar Fe (besi) dalam larutan sampel menggunakan spektrofotometer sp 20 dan menggunakan Spektrofotometer sp 20 dengan benar. Pada praktikum ini langkah pertama adalah mebuat 7 larutan yang mengandung kadar Fe yang berbeda-beda dimulai dari 0 ppm sampai 3,5 ppm yang kemudian dicampur dengan Hidroksilamin-HCl 10% sebanyak 0,5 ml untuk mereduksi Fe3+ menjadi Fe2+, Na Asetat (CH3COONa) sebanyak 5 ml,
dan O-Fenantrolin 10% sebanyak 5 ml agar membentuk kompleks larutan berwarna, yang kemudian diencerkan sampai 50 ml dengan aquades dalam labu takar.
Selanjutnya menentuan panjang gelombang maksimum pada larutan dengan kadar Fe 2ppm. Rentang panjang gelombang yang diuji adalah 410-550 nm. Dengan menggunakan spektrometer sp 20 angka yang terlihat adalah nilai %T yang kemudian harus dikonversikan ke nilai A (Absorbansi) menggunakan rumus A = log 1/T . Sebelum melakukan percobaan spektrofotometer harus dikalibarsi terlebih dahuli menggunakan larutan blanko. Fungsi dari blanko sendiri adalah mengukur serapan pereaksi yang digunakan untuk analisis kadar Fe sehingga jumlah serapan Fe sendiri adalah nilai absorbansi larutan standar atau sampel (mengandung pereaksi dan Fe) dikurangi serapan pereaksinya. Sehingga absorbansi yang didapat pada pengukuran ini adalah serapan untuk Fe dalam sampel, fungsi kalibrasi juga untuk menghilangkan efek refleksi akibat pancaran sinar radiasi menuju larutan.
Diketahui pada panjang gelombang 410 nm molekul-molekul dalam larutan mampu memperoleh absorbansi sebesar 0,42 atau cahaya yang diserap sebesar 42% pada panjang gelombang tersebut. Nilai absorbansi ini terus meningkat hingga pada panjang gelombang 510 nm dengan absorbansi 0,854 atau 85,4% cahaya diserap. Namun absorbansi mulai menurun dengan meningkatnya panjang gelombang. Hingga pada panjang gelombang 550 nm, nilai absorbansi yang didapat adalah 0,342. Dari
hasil percobaan ini dapat disimpulkan bahwa larutan tersebut menyerap cahaya secara maksimal pada panjang gelombang 510 nm.
Kemudian langkah selanjutnya yaitu menentukan kadar Fe dalam larutan sampel, larutan sampel dibuat dari campuran ketujuh larutan yang telah dibuat sebelumnya. Setelah diperiksa larutan sampel tersebut memiliki nilai absorbansi 0,495, sehingga bila digambar dengan kurva kadar Fe pada larutan sampel tersebut adalah 1,507 ppm.
X. KESIMPULAN
Berdasarkan hasil pengamatan dan pembahasan, dapat disimpulkan bahwa konsentrasi besi dalam larutan dapat ditentukan dengan mengukur spectrum serapan dari masing-masing larutan standar dengan menggunakan spektrofotometer UV-Vis dan membandingkan absorbansinya dengan larutan sampel yang akan ditentukan konsentrasi besinya. Kadar besi dalam sampel adalah 2.043 ppm.
XI. DAFTAR ISI
http://alfinasbahry.blogspot.co.id/2015/01/laporan-praktikum-spektrofotometri.html