Spektrofotometer
pektrofotometer merupakan alat yang digunakan untuk mengukur absorbansi dengan cara melewatkan cahaya dengan panjang gelombang tertentu pada suatu obyek kaca atau kuarsa yang disebut kuvet.Sebagian dari cahaya tersebut akan diserap dan sisanya akan dilewatkan. Nilai absorbansi dari cahaya yang dilewatkan akan sebanding dengan konsentrasi larutan di dalam kuvet.
S
Spektrofotometer adalah alat untuk mengukur transmitan atau absorban suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan gabungan dari alat optik dan elektronika serta sifat-sifat kimia fisiknya dimana detektor yang digunakan secara langsung dapat mengukur intensitas dari cahaya yang dipancarkan (It) dan secara tidak lansung cahaya yang diabsorbsi (Ia), jadi tergantung pada spektrum elektromagnetik yang diabsorb (serap) oleh benda. Tiap media akan menyerap cahaya pada panjang gelombang tertentu tergantung pada senyawaan atau warna terbentuk.
Jenis-jenis
Spektrofotometer dibagi menjadi dua jenis yaitu spektrofotometer single-beam dan spektrofotometer double-beam. Perbedaan kedua jenis spektrofotometer tersebut hanya pada pemberian cahaya, dimana pada single-beam, cahaya hanya melewati satu arah sehingga nilai yang diperoleh hanya nilai absorbansi dari larutan yang dimasukan. Berbeda dengan single-beam, pada spektrofotometer double-beam, nilai blanko dapat langsung diukur bersamaan dengan larutan yang diinginkan dalam satu kali proses yang sama. Prinsipnya adalah dengan adanya chopper yang akan membagi sinar menjadi dua, dimana salah satu melewati blanko (disebut juga reference beam) dan yang lainnya melewati larutan (disebut juga sample beam). Dari kedua jenis spektrofotometer tersebut, spektrofotometer double-beam memiliki keunggulan lebih dibanding single-beam, karena nilai absorbansi larutannya telah mengalami pengurangan terhadap nilai absorbansi blanko. Selain itu, pada single-beam, ditemukan juga beberapa kelemahan seperti perubahan intensitas cahaya akibat fluktuasi voltase.
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari spectrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang di transmisikan atau yang di absorpsi.
λ (nm) <400 400-450 450-500 500-570 570-590 590-620 620-750 >750 warna UV Violet Biru Hijau Kuning Jingga Merah Infra Merah
Penyerapan sinar uv dan sinar tampak o/ molekul, melalui 3 proses yaitu : Penyerapan o/ transisi electron ikatan dan electron anti ikatan.
Penyerapan o/ transisi electron d dan f dari molekul kompleks Penyerapan o/ perpindahan muatan.
Interaksi antara energy cahaya dan molekul dapat digambarkan sbb :
E = hv
Dimana , E = energy (joule/second) h = tetapan plank
v = frekuensi foton
Penyerapan sinar uv-vis dibatasi pd sejumlah gugus fungsional/gugus kromofor (gugus dengan ikatan tidak jenuh) yang mengandung electron valensi dengan tingkat eksitasi yang rendah. Dengan melibatkan 3 jenis electron yaitu : sigma, phi dan non bonding electron. Kromofor-kromofor organic seperti karbonil, alken, azo, nitrat dan karboksil mampu menyerap sinar ultraviolet dan sinar tampak. Panjang gelombang maksimalnya dapat berubah sesuai dengan pelarut yang digunakan. Auksokrom adalah gugus fungsional yang mempunyai elekron bebas, seperti hidroksil, metoksi dan amina. Terikatnya gugus auksokrom pada gugus kromofor akan mengakibatkan pergeseran pita absorpsi menuju ke panjang gelombang yang lebih besar (bathokromik) yang disertai dengan peningkatan intensitas (hyperkromik).
1. Suatu sumber energy cahaya yang berkesinambungan yang meliputi daerah spectrum dimana instrument itu dirancang untuk beroperasi.
2. Suatu monokromator, yakni suatu piranti untuk mengecilkan pita sempit panjang-panjang gelombang dari spectrum lebar yang dipancarkan oleh sumber cahaya. 3. Suatu wadah sampel (kuvet)
4. Suatu detector, yang berupa transduser yang mengubah energy cahaya menjadi suatu isyarat listrik.
5. Suatu pengganda (amplifier), dan rangkaian yang berkaitan membuat isyarat listrik itu memadai untuk di baca.
6. Suatu system baca (piranti pembaca) yang memperagakan besarnya isyarat listrik, menyatakan dalam bentuk % Transmitan (% T) maupun Adsorbansi (A).
Skema spektrofotometer ;
Sumber Cahaya..Monokromator….Sampel…Detektor….Amplifier..Piranti Pembaca/Penunjuk
Beberapa jenis spektrofotometer :
1. Spektrofotometer UV-Vis 2. Spektrofotometer Infra merah
3. Spektrofotometer Serapan Atom (SSA)
4. Spektrofotometer Resonansi Magnetik (NMR)
5. Spektrofotometer Pendar Molecular (pendar fluor/pendar fosfor)
6. Spektrofotometer dengan metode hamburan cahaya ( nefelometer, turbidimeter dan spektrofotometer Raman)
Panjang gelombang warna yang diserap warna komplementer 400-435 nm ungu (lembayung) hijau kekuningan
450-480 nm biru kuning
480-490 nm biru kehijauan orange 490-500 nm hijau kebiruan merah 500-560 nm hijau merah anggur
560-580 nm hijau kekuningan ungu (lembayung) 580-595 nm kuning biru
595-610 nm orange biru kekuningan 610-750 nm merah hijau kebiruan
Pergeseran-pergeseran :
1. Bathokromik, pergeseran ke panjang gelombang yang lebih tinggi dengan energy yang lebih rendah.
2. Hypsokromik(pergeseran biru), pergeseran ke panjang gelombang yang lebih pendek.
3. Hyperkromik, peningkatan absoritivitas molar. 4. Hypokromik, reduksi absortivitas molar.
Hukum Beer : Absorbans, log (Po/P), radiasi monokromatik berbanding lurus dengan konsentrasi sutu spesies penyerap dalam larutan.
Hukum Bouguer (Lambert) : Bayangkan suatu medium penyerap yang homogen dalam lapisan-lapisan yang sama tebal. Tiap lapisan menyerap radiasi monokromatik yang memasuki lapisan itu dalam fraksi yang sama seperti lapisan-lapisan lain. Dengan semuanya yang lain sama, maka absorbans itu berbanding lurus dengan panjang jalan yang melewati medium.
Gabungan Hukum Bouguer-Beer, sering di tuliskan sebagai
A = abc
atauA = εbc
Dengan A = absorbans
ε = absorpsivitas molar (jika konsentrasi dalam molar) dengan satuan M-1cm-1
a = absorpsivitas (jika konsentrasi dalam %b/v) dituliskan E1% 1cm
b = panjang jalan/kuvet
c = konsentrasi ( dalam molar atau %b/v)
Spektra absorpsi sering diyatakan dalam %T maupun dalam bentuk A (absorbansi) Maka, A = – log (%T)
A = log (Po/P), Po adalah daya cahaya masuk dan P adalah daya yang diteruskan
melewati sampel.
Metode analisa kuantitatip didasarkan pada absorpsi radiasi oleh suatu unsur yang mengabsorpsi dan melibatkan pengukuran intensitas cahaya atau kekuatan radiasi.Kita sekarang mempertimbangkan faktor yang mempengaruhi kekuatan radiasi dari cahaya yang dipancarkan melalui media absorsi.
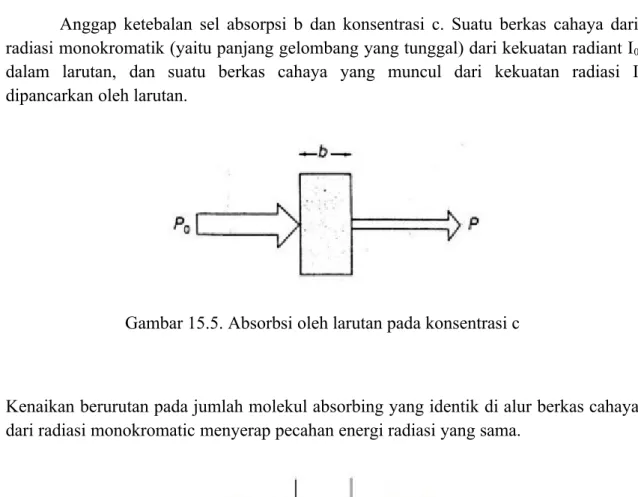
Anggap ketebalan sel absorpsi b dan konsentrasi c. Suatu berkas cahaya dari radiasi monokromatik (yaitu panjang gelombang yang tunggal) dari kekuatan radiant I0
dalam larutan, dan suatu berkas cahaya yang muncul dari kekuatan radiasi I dipancarkan oleh larutan.
Gambar 15.5. Absorbsi oleh larutan pada konsentrasi c
Kenaikan berurutan pada jumlah molekul absorbing yang identik di alur berkas cahaya dari radiasi monokromatic menyerap pecahan energi radiasi yang sama.
Gambar 15.6. Penurunan intensitas radiasi dengan bertambahnya ketebalan larutan
Jika penambahanketebalan dari alur adalah db dan penurunan kekuatan radiasi yang melewati ketebalan adalah dI maka :
yaitu dI = -kIdb
Integrasi dari total ketebalan b
yaitu ln I = -kb + w
sekarang jika : b = 0 , I = I 0
? w = ln I0
? ln I = – kb + ln I0
yaitu
Hukum ini dikenal sebagai Hukum Lambert dan menghubungkan ketebalan dari sel sampel (kuvet) pada perbandingan kekuatan radiasi berkas cahaya yang masuk dan berkas cahaya yang keluar, dan menyatakan :
“Ketika radiasi monokromatik lewat melalui suatu medium yang transparan yang berisi suatu unsur absorbing, tingkat penurunan kekuatan radiasi dengan ketebalan dari medium adalah setara dengan kekuatan radian dari suatu radiasi“ Dengan alasan yang sama, untuk perubahan penambahan konsentrasidari unsur absorbing, dc ,
Hukum ini disebut Hukum Lambert-Beer, dan berlaku untuk unsur yang menyerap cahaya dengan menghubungkan konsentrasi dari jenis absorbing pada perbandingan kekuatan radiant berkas cahaya yang masuk dan yang keluar :
“Ketika radiasi monokromatk lewat melalui suatu medium yang transparan yang berisi suatu unsur absorbing, tingkat penurunan kekuatan radian dengan konsentrasi jenis unsur absorbing adalah sebanding dengan kekuatan radian dari
suatu radiasi “
Hukum Lambert dan Hukum Lambert-Beer biasanya dikombinasikan dalam suatu hubungan tunggal sebagai dasar untuk semua penentuan kuantitatif.
Ini disebut Hukum Lambert-Beer. Hukum ini hanya berlaku untuk radiasi monokromatik.
Karena jumlah kekuatan radiant I0 dan I merupakan sebuah perbandingan, ada beberapa
unit yang mungkin digunakan. Jika ketebalan, yang disebut panjang sampel dalam bentuk centimeter dan konsentrasi, c dalam gram unsur absorbing per satu liter larutan, kemudian konstanta a disebut absorptivitas (kadang disebut koefisien ekstensi)
Biasanya, c ditetapkan dalam konsentrasi molar, dengan b dalam sentimeter. Dalam hal ini Hukum Lambert-Beer ditulis sebagai
dimana ? disebut absorptivitas molar (atau disebut koefisien ekstensi molar). Absorptivitas molar memiliki satuan L. mol-1.cm-1
Jumlah log (I0/I) didefinisikan sebagai absorbansi dan diberi simbol A, sehingga Hukum Lambert-Beer umumnya ditulis sebagai :
A = ε b c
Spektrofotometer modern dikalibrasi secara langsung dalam satuan absorbansi. Dalam beberapa buku lama log I0/I disebut densitas optik dan I digunakan sebagai ganti simbol
P)
Perbandingan I/I0 disebut transmitans (T) dan beberapa instrumen disajikan dalam % transmitans, ( I/I0 ) x 100. Sehingga hubungan absorbansi dan transmitans dapat ditulis
sebagai :
A = – log T
Dengan menggunakan beberapa instrumen, hasil pengukuran tercatat sebagai transmitans dan absorbansi dihitung dengan menggunakan rumus tersebut.
Dari pembahasan di atas dapat dikatakan bahwa konsentrasi dari suatu unsur berwarna harus sebanding dengan intensitas warna larutan. Ini adalah dasar pengukuran yang menggunakan pembanding visual di mana intensitas warna dari suatu larutan dari suatu unsur yang konsentrasinya tidak diketahui dibandingkan dengan intensitas warna dari sejumlah larutan yang diketahui konsentrasinya.
Beberapa Istilah Dalam Spektrofotometri
Absorbans (A) , A = log (Po/P)Absorptivitas (a), tetapan dalam Hukum Bouguer-Beer bila konsentrasi dinyatakan dalam %b/v dan tebal kuvet dalam cm. Dengan satuan liter per gram per sentimeter. Absorptivitas molar (ε), tetapan dalam Hukum Bouguer-Beer bila konsentrasi dinyatakan dalam molar dan tebal kuvet dalam cm. Dengan satuan liter per mol per sentimeter.
Transmitan (T), fraksi dari daya radiasi yang diteruskan oleh suatu sampel T = P/Po.
Sering dinyatakan sebagai suatu persentase : %T = (P/Po) x 100%.
Pengukuran Absorbansi beberapa Senyawa
Asam askorbat merupakan salah satu pereduksi yang dapat menghasilkan senyawa kompleks berwarna. Dalam metode asam askorbat, ammonium molibdat bereaksi dalam medium asam dengan fosfor membentuk kompleks fosfomolibdat
berwarna kuning yang akan direduksi menjadi kompleks biru-molibdem (molybdenum
blue) oleh asam askorbat yang mempunyai panjang gelombang absorbansi maksimum
880 nm.
Serapan vitamin larut air pada panjang gelombang 270, 275, dan 280 nm
No Vitamin Serapan pada Panjang
Gelombang
270 275 280
1 Asam askorbat 0,3542 0,2624 0,1755
2 Menadion natrium bisulfit 0,3540 0,2335 0,1245
3 Nikotinamida 0,2863 0,1097 0,0207 4 Asam folat 0,2346 0,2466 0,2437 5 Piridoksin hidroklorida 0,2272 0,3413 0,4666 6 Sianokobalamin 0,1191 0,1231 0,1180 7 Riboflavin 0,3376 0,2562 0,1839 8 Tiamin hidroklorida 0,2751 0,2009 0,1253
Bentuk kombinasi obat yang beredar di pasaran seringkali menimbulkan permasalahan dalam kontrol kualitasnya terutama dalam hal validitas analisis kuantitatifnya. Salah satu bentuk kombinasi tersebut adalah kombinasi asam askorbat dan α – tokoferol asetat dalam suplemen antioksidan. Untuk mengatasi permasalahan diatas maka penelitian terhadap campuran tersebut dilakukan dengan metode spektrofotometri UV-Vis Cara simultan. Pada penetapan kadar campuran zat secara simultan, tahap pertama menentukan panjang gelombang terpilih masing – masing komponen, kemudian menentukan serapan jenis masing – masing komponen.Dari tahap ini didapatkan panjang gelombang terpilih pada 245 nm untuk asam askorbat dan 265 nm α –
tokoferol asetat.
Penelitian ini menguji tingkat validitas penerapan metode spektrofotometri UV-Vis cara simultan dalam penentuan kadar campuran asam askorbat dan α – tokoferol asetat baik tanpa bahan tambahan maupun dengan bahan tambahan Pada pembuatan campuran asam askorbat danα – tokoferol asetat baik tanpa bahan tambahan maupun dengan bahan tambahan dalam berbagai perbandingan, perlu ditambahkan larutan standar a – tokoferol asetat sebanyak 50 ppm agar dapat masuk rentang pembacaan.
Hasil analisis data untuk linieritas, didapatkan koefisien relasi (r) hitung asam askorbat pada panjang gelombang 245 nm adalah 0,9999 dan pada 265 nm adalah 0,9996 lebih besar dari r tabel (0,878). Serta Vxo 0,62 % (245 nm) dan 1,17 % (265 nm). Sedangkan untuk α – tokoferol asetat pada panjang gelombang 245 nm adalah 0,9996 dan pada 265 nm adalah 0,9999 lebih besar dari r tabel (0,878), serta Vxo 1,70 % (245 nm) dan 0,09 % (265 nm) Dari data tersebut dapat disimpulkan ada hubungan yang Tinier antara kadar campuran asam askorbat dan a – tokoferol asetat dengan absorban.
Nilai serapan jenis yan& didapat untuk asam askorbat pada panjang gelombang 245 nm sebesar 4,9275.10" dan pada 265 nm sebesar 1,4597.10"2. Sedangkan serapan jenis untuk α – tokoferol asetat pada panjang gelombang 245 nm sebesar 1,5238. 10-3 dan pada 265 nm sebesar 1,4828.10"3.
Sumber :
http://id.wikipedia.org/wiki/Spektrofotometer http://www.chem-is- try.org/materi_kimia/instrumen_analisis/spektrum_serapan_ultraviolet-tampak__uv-vis_/kesalahan-dalam-analisis-spektrometri-kuantitatif/ http://www.chem-is-try.org/materi_kimia/instrumen_analisis/spektrum_serapan_ultr aviolet-tampak__uv-vis_/analisis-kuanitatif/ http://www.chem-is-try.org/materi_kimia/instrumen_analisis/spektrum_serapan_ultr aviolet-tampak__uv-vis_/penyimpangan-hukum-beer/ http://rgmaisyah.wordpress.com/2008/11/25/spektrofotometer/ http://catatankimia.com/catatan/kaliberasi-spektrofotometer-uv-vis.html http://210.57.222.58/go.php?id=gdlhub-gdl-s1-2008-pratokodwi-9085&node=642&start=6&PHPSESSID=fb688e772e96670b5ed82380bb2f43e 8