SINTESIS SENYAWA KALSIUM FOSFAT DENGAN TEKNIK
PRESIPITASI SINGLE DROP
IRMA PURNAMA RAMADHANI
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2012
Teknik Presipitasi Single Drop. Supervised by SETYANTO TRI WAHYUDI
dan SETIA UTAMI DEWI
.
The high damage of bone trigger a variety of research about bone biomaterial. So far,
compliance for this needed done import materials. The material which used for bone
biomaterial is calcium phosphate. In this research used synthesis of calcium phosphate.
Synthesis of calcium phosphate performed using precipitation method single drop and
wise drop at room temperature with sintering themperature 900
oC, themperature 70
oC
with sintering time variation (110
oC, 300
oC, 600
oC, and 900
oC). Results obtained from
sintering is fluffy white powder. Result from x-ray diffraction characteristic for all sample
with themperature sintering 900
oC show the phase formed is calcium pyrophosphate and
other phase from calcium phosphate that is hydroxyapatite, tricalcium phosphate,
octacalcium phosphate, carbonate apatite type-A and carbonated apatite type-B. The
longer stirring time so the phase of calcium pyrophosphate formed the less. Reaction
themperature is very effect in formation of phase calcium pyrophosphate, because
calcium pyrophosphate which the resulting in room themperature is more than in
themperature 70
oC. Beside that precursor compound that has not reacted in
themperature70
oC more less from room themperature, this is because precursor
compound is more faster when heated. In sintering variationthemperature 110
oC and
300
oC the precursor formed is more and the best sintering themperature is 900
oC.
Keywords: calcium pyrophosphate, calcium phosphate, hydroxyapatite, tricalcium
phosphate, octacalcium phosphate
ii
ABSTRAK
IRMA PURNAMARAMADHANI. Sintesis Senyawa Kalsium Fosfat dengan
Teknik Presipitasi Single Drop. Dibimbing oleh SETYANTO TRI WAHYUDI
dan SETIA UTAMI DEWI
.
Tingginya kerusakan tulang memicu adanya berbagai penelitian mengenai
biomaterial tulang. Sejauh ini, pemenuhan akan kebutuhan ini dilakukan dengan
bahan-bahan impor. Bahan yang digunakan untuk biomaterial tulang adalah
kalsium fosfat. Pada penelitian ini dilakukan sintesis kalsium fosfat. Sintesis
kalsium fosfat dilakukan dengan menggunakan metode presipitasi single drop
dan wise drop pada suhu ruang dengan suhu sintering 900
oC, pada suhu 70
oC
dengan suhu sintering 900
oC dan metode single drop pada suhu 70
oC dengan
variasi sintering (110
oC,300
oC,600
oC, 900
oC). Hasil yang diperoleh dari
sinteringberupa serbuk putih halus. Hasil dari karakterisasi x-ray diffractionuntuk
semua sampel hasil sintering 900
oCmenunjukkan fase yang terbentuk adalah
calcium pyrophosphate dan fase kalsium fosfat lainnya yaitu hydroxyapatite,
tricalcium phosphate, octacalcium phosphate, carbonate apatite type-A dan
carbonate apatite type-B. Semakin lama waktu stirring maka fase calcium
pyrophosphate yang terbentuk semakin sedikit. Suhu reaksi sangat berpengaruh
dalam terbentuknya fase calcium pyrophosphate, karena calcium pyrophosphate
yang dihasilkan pada suhu ruang lebih banyak dari suhu 70
oC. Namun senyawa
prekursor yang belum bereaksi pada suhu 70
oC lebih sedikit dari suhu ruang, hal
ini dikarenakan senyawa prekursor lebih cepat bereaksi bila dipanaskan. Pada
variasi suhu sintering 110
oC dan 300
oC prekursor yang terbentuk masih banyak
dan suhu sintering yang paling bagus adalah 900
oC.
Kata kunci: calcium pyrophosphate, kalsium fosfat, hydroxyapatite, tricalcium
phosphate, octacalcium phosphate.
SINTESIS SENYAWA KALSIUM FOSFAT DENGAN TEKNIK
PRESIPITASI SINGLE DROP
IRMA PURNAMA RAMADHANI
Skripsi
Sebagai salah satu syarat Sarjana Sains pada
DepartemenFisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
iv
LEMBAR PENGESAHAN
Judul : Sintesis Senyawa Kalsium Fosfat Dengan Teknik Presipitasi Single
Drop
Nama
: Irma Purnama Ramadhani
NIM : G74080042
Pembimbing 1
Pembimbing 2
Setyanto Tri Wahyudi, M.Si
Setia Utami Dewi, M.Si
Diketahui
Kepala Bagian Biofisika
Dr. Kiagus Dahlan
KATA PENGANTAR
Asslamu’alaikum Wr. Wb, ucapan terima kasih yang pertama penulis ucapkan
kehadirat Allah SWT karena dengan izin-Nya penulis dapat menyelesaikan penelitian ini
yang berjudul Sintesis Senyawa Kalsium Fosfat dengan dengan teknik presipitasi Single
Drop. Penelitian ini sebagai salah satu syarat kelulusan program sarjana di Departemen
Fisika Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor.
Ucapan terimakasih juga penulis ucapkan kepada pihak-pihak yang telah
membantu dalam penyelesaian skripsi ini:
1. Bapak dan Ibu serta kedua adik penulis Adi dan Geri dan keluarga besar di
Bandung yang selalu memberikan doa dan support selama penulis menempuh
pendidikan di IPB.
2. Bapak Setyanto Tri Wahyudi, M.Si selaku pembimbing pertama yang telah
memberikan banyak masukan, bimbingan, motivasi dan yang telah mendanai
penelitian ini.
3. Ibu Setia Utami Dewi, M.Si selaku pembimbing kedua yang telah memberikan
masukan, motivasi dan membantu dalam mempelajari biomaterial.
4. Seluruh dosen fisika yang telah memberikan ilmu selama penulis menempuh
pendidikan di IPB.
5. Pak Didikatas kerjasamanya selama karakterisasi XRD.
6. Dani Yosmanyang selalu memberikan support, do’a dan selalu membantu saat
suka dan duka.
7. Ajeng selaku rekan kerja penulis dalam penelitian ini serta towil yang selalu
menemani kita bermain uno.
8.
Seluruh teman-teman Fisika 45tiada kesan tanpa kebersamaan selama ini.
9.
Adik-adik angkatan 46 dan 47 yang selalu mendoakan penulis.
10.
Teman-teman lukita (Pingkan, Herni dan Aliya) yang selalu menemani di kosan
dikala malam datang.
11.
Teman-teman asrama212 (Muti, Rita dan Ratu) yang selalu hadir dalam canda
dan tawa.
12.
Mba aisyah yang selalu membantu dalam pengolahan data.
13.
Pak Jun yang selalu membantu dalam proses pemakaian laboratorium.
14.
Pak Firman yang selalu membantu dalam hal administrasi.
15.
Pak Indro selaku editor.
16.
Pak Faozan dan Pak Ardian selaku penguji.
Akhir kata, dengan adanya hasil penelitian ini diharapkan dapat memberikan
manfaat yang besar. Kritik dan saran yang membangun sangat diharapkan untuk
kemajuan dari penerapan biomaterial yang akan dilakukan penelitian saat ini.
vi
RIWAYAT HIDUP
Penulis dilahirkan di Bandung, Jawa Barat pada tanggal 15 April
1990 dari pasangan Abdul Firman dan Tetty Setyawati. Penulis
merupakan
anak
pertama
dari
tiga
bersaudara.
Penulis
menyelesaikan pendidikan di TK Ananda, SD Kartika XI-II, MTS
Zakaria, SMAN 12 Bandung dan melanjutkan ke perguruan tinggi
S1 di Departemen fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut
Pertanian Bogor melalui jalur USMI. Selama menempuh pendidikan penulis aktif dalam
bidang organisasi, penulis aktif sebagai anggota UKM Taekwondo IPB dan penulis pun
pernah menjabat sebagai sekretaris departemen kominfo BEM FMIPA Totalitas
Kebangkitan. Selain itu penulis juga aktif dalam acara kepanitiaan seperti panitia pesta
sains 2009 sebagai logstran, pesta sains 2010 sebagai kestari, panitia MPF sebagai MOD,
panitia G-Expo sebagai sekretaris, panitia seminar sains sebagai kestari. Penulis pun
pernah mendapat juara 3 dalam perlombaan atletik sprint putri dalam acara
SPIRIT-FMIPA.
DAFTAR ISI
Hal.
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
BAB I. PENDAHULUAN ... 1
1.1.
Latar Belakang ... 1
1.2.
Tujuan Penelitian ... 1
1.3.
Perumusan Masalah ... 1
1.4.
Hipotesis ... 1
2.1.
Senyawa Kalsium Fosfat ... 1
2.1.1.
Tricalcium Phosphate ... 2
2.1.2.
Hydroxyapatite... 2
2.1.3.
Octacalcium Phosphate ... 2
2.1.4.
Dicalcium Phosphate Dihydrate ... 2
2.1.5.
Calcium Pyrophosphate ... 3
2.2.
Difraksi sinar-X ... 3
BAB III. METODOLOGI PENELITIAN ... 4
3.1.
Tempat dan Waktu Penelitian ... 4
3.2.
Alat dan Bahan ... 4
3.3.
Prosedur Penelitian ... 4
3.3.1.
Persiapan Bahan ... 4
3.3.2.
Pembuatan kalsium fosfat pada suhu ruang ... 4
3.3.3.
Pembuatan kalsium fosfatpada suhu 70
oC ... 4
3.3.4.
Pembuatan kalsium fosfat metode single drop suhu 70
oC dengan variasi
sintering (110
oC, 300
oC, 600
oC, dan 900
oC) ... 5
3.3.5.
Karakterisasi XRD ... 5
BAB IV. HASIL DAN PEMBAHASAN ... 6
4.1.
Persiapan Bahan ... 6
4.2.
Hasil Kalsium Fosfat Pada Suhu Ruang ... 6
4.3.
Hasil Kalsium Fosfat Pada Suhu 70
oC. ... 6
4.4.
Hasil Kalsium Fosfat Metode Single Drop Pada Suhu 70
oC dengan Variasi
Sintering (110
oC, 300
oC, 600
oC, 900
oC) ... 7
viii
BAB V. KESIMPULAN DAN SARAN ... 15
5.1.
Kesimpulan ... 15
5.2.
Saran ... 15
DAFTAR PUSTAKA ... 16
DAFTAR TABEL
Hal.
1. Penamaan kode sampel kalsium fosfat……….…5
2. Efisiensi massa Ca dan fosfat pada suhu ruang ... 6
3. Efisiensi massa Ca dan fosfat pada suhu 70
oC ... 6
4. Efisiensi massa Ca dan fosfat pada suhu 70
oC dengan variasi sintering ... 6
5. Komposisi senyawa yang dihasilkan dari sintesis kalsium fosfat suhu ruang ... 9
6. Perhitungan parameter kisi dan persentase ketepatancalcium pyrophosphatepada suhu
ruang ... 10
7. Komposisi senyawa yang dihasilkan dari sintesis kalsium fosfat ... 11
8. Perhitungan parameter kisi dan persentase ketepatancalcium pyrophosphatepada suhu
70
oC ... 11
9. Komposisi senyawa yang dihasilkan dari sintesis kalsium fosfat ... 13
10. Perhitungan parameter kisi dan persentase ketepatanCa
2P
2O
7pada suhu 70
oC dengan
variasi sintering ... 14
x
DAFTAR GAMBAR
Hal.
1.
Struktur molekul TCP.
6... 2
2.
Struktur unit sel kristal HAp.
9... 3
3.
Struktur molekul OCP.
12... 3
4.
Struktur molekul DCPD.
13... 3
5.
Struktur molekul Ca
2P
2O
7.
14... 3
6.
Skema sinar datang dan sinar terdifraksi oleh kisi kristal.
15... 3
7.
Skema Difraktometer sinar-x.
15... 3
8.
Hasil XRDsampel denganmetode single drop dan wise drop pada suhu ruang
yang di-sintering 900
oC ... 8
9.
Hasil XRD sampel dengan metode single drop dan wise drop pada suhu 70
oyang
di-sintering 900
o. ... 11
10.
Hasil XRD sampel dengan metode single drop pada suhu 70
oC yang dengan
variasi suhu sintering. ... 13
DAFTAR LAMPIRAN
Hal
1.
Diagram alir penelitian……...………... 18
2.
Tabel JCPDS fasa HA…………...………...
19
3.
Tabel JCPDS fasa Octa-Calcium Phosphate………...
19
4.
Tabel JCPDS Type A Carbonated Apatite………...
20
5.
Tabel JCPDS fasa Type-B Carbonated Apatite………...
20
6.
Tabel JCPDS fasa TCP...
21
7.
Tabel JCPDS CaCl
2.………...
21
8.
Tabel JCPDS Na
2HPO
4………...
22
9.
Tabel JCPDS Ca
2P
2O
7………...
22
10. Foto Penelitian………...
23
11. Perhitungan komposisi senyawa yang dihasilkan………...
24
BAB I. PENDAHULUAN
1.1.
Latar Belakang
Tingginya kerusakan tulang memicu adanya berbagai penelitian mengenai biomaterial tulang. Sejauh ini, pemenuhan akan kebutuhan
ini dilakukan dengan bahan-bahan
impor.Biomaterial adalah suatu material alami maupun buatan (sintetis) yang dapat diimplantasikan ke dalam sistem atau jaringan hidup sebagai pengganti fungsi jaringan yang mengalami kerusakan. Material ini harus bersifat biokompatibel dengan tubuh manusia. Saat ini, biomaterial yang banyak dikembangkan adalah biomaterial subtitusi tulang.1Tulang merupakan jaringan keras dari tubuh manusia selain gigi. Tulang merupakan organ biologi dinamik yang tersusun oleh sel aktif metabiologi yang terintegrasi ke dalam rangka yang kaku.2
Secara umum penyusun dasar
komponen anorganik dalam jaringan keras khususnya tulang adalah kalsium fosfat. Kalsium fosfat terdapat dalam dua bentuk yaitu fase amorf dan fase kristal. Senyawa kalsium fosfat kristal sintetis mempunyai 4 fase yaitu CaHPO2 (dicalcium phosphate dehydrate /
DCPD), Ca8H2(PO4)6 octacalcium phosphate /
OCP), Ca3(PO4)2 (tricalcium phosphate/TCP),
dan Ca10(PO4)6(OH)2 (hydroxyapatite / HA). Hydroxyapatitemerupakan kristal paling stabil
dibandingkan 3 fase lainnya.4
Biomaterial pengganti tulang pada umumnya berasal dari senyawa kalsium fosfat diantaranyaHydroxyapatite (Ca10(PO4)6(OH)2)
dan tricalcium phosphate (Ca3(PO4)2 karena
kedua material ini memiliki komposisi kimia yang mendekati dengan komponen-komponen yang terdapat di dalam tulang. Hydroxyapatite (HA)merupakan senyawa kalsium fosfat yang paling stabil, tetapi tingkat kelarutannya paling rendah jika dibandingkan dengan tricalcium
phosphate (TCP). Salah satu polymorpf TCP
yang banyak digunakan untuk rekontruksi tulang yaitu β-TCP karena memiliki tingkat biodegradasi yang sesuai dengan laju pertumbuhan tulang dan memiliki sifat
osteoconductive.3
Pada penelitian ini dilakukan pembuatan kalsium fosfat dengan metode presipitasi secara
single drop dansebagai kontrolnya digunakan wise dropyang telah biasa dilakukan di Lab
Biofisika IPB. Metode single drop,
mencampurkan langsung larutan kimia
sedangkan wise drop mencampurkan larutan kimia tetes demi tetes. Bahan yang digunakan pada penelitian ini, adalah larutan kalsium klorida (CaCl2) dan dinatrium hidrogen fosfat
(Na2HPO4). Serbuk putih yang
dihasilkandianalisis menggunakan x-ray diffraction (XRD) untuk mengindentifikasi
kristal kalsium fosfat, parameter kisi dan ukuran kristal.
1.2.
Tujuan Penelitian
1. Melakukan sintesis senyawa kalsium fosfat
dengan metode single drop dan
membandingkan hasilnya dengan
metodewise drop.
2. Mempelajari pengaruh waktu stirring dan suhu reaksi pada proses single drop terhadap pembentukan kalsium fosfat. 3. Mempelajari variasi suhu sintering terhadap
pembentukan senyawa kalsium fosfat.
1.3. Perumusan Masalah
1. Bagaimana pengaruh suhu reaksi terhadap pembentukan kalsium fosfat pada metode
single drop dan wise drop?
2. Bagaimana pengaruh waktu stirring pada proses single dropterhadap pembentukan kalsium fosfat?
3. Bagaimana perbandingan kalsium fosfat yang terbentuk dari proses single drop dan
wise drop?
4. Bagaimana pengaruh suhu sintering pada kalsium fosfat yang terbentuk?
1.4.
Hipotesis
Senyawa kalsium fosfat yang dibuat dengan menggunakan metode single drop tidak akan berbeda dengan senyawa kalsium fosfat yang
dibuat dengan menggunakan metode
wisedroppada suhu yang sama. Namun
perbedaan suhu reaksi akan menghasilkan data yang berbeda.
BAB II. TINJAUAN PUSTAKA
2.1. Senyawa Kalsium Fosfat
Secara umum penyusun dasar komponen anorganik dalam jaringan keras khususnya tulang adalah kalsium fosfat. Kalsium fosfat terdapat dalam dua bentuk yaitu fase amorf dan fase kristal. Senyawa kalsium fosfat kristal sintetis mempunyai 4 fase yaitu CaHPO2
(dicalcium phosphate dehydrate / DCPD), Ca8H2(PO4)6 octacalcium phosphate/OCP),
Ca3(PO4)2 .
( tricalciumphosphate / TCP), dan Ca10(PO4)6(OH)2 Hydroxyapatite / HA).
Dalam proses pembuatan senyawa
biomaterial yang menyerupai jaringan keras, proses kristalisasi dapat ditingkatkan dengan
menaikkan aktivitas ion yang terlibat dengan cara meningkatkan laju pengadukan, menaikkan pH, menaikkan suhu atau menghilangkan penghambat.5
Sintesis senyawa kalsium fosfat dengan cara presipitasi pada umumya melalui amorf sebagai fase sementara. Fase amorf ini, sama halnya terjadi selama mineralisasi dalam jaringan keras. Senyawa kalsium fosfat amorf yang terbentuk masih mungkin tersusun oleh kristal yang mempunyai ukuran yang sangat kecil.4
2.1.1. Tricalcium Phosphate
Tricalcium phosphate (TCP) adalah material biokeramik yang dapat digunakan untuk rekontruksi tulang.6 Kombinasi TCP dari kalsium dan senyawa fosfat dengan rumus Ca3(PO4)2. TCP memiliki 4 polymorf yaitu α,
β, γ dan super α. Polymorf α teramati pada suhu 1120oC - 1500oC, polymorf β teramati sekitar suhu 1120oC, polymorf γ berada pada fase tekanan tinggi, dan polymorf super α teramati pada suhu diatas 1500oC.6 Struktur molekul TCP dapat dilihat pada Gambar 1.
2.1.2. Hydroxyapatite
Hydroxyapatite (HA) merupakan senyawa
kalsium fosfat yang merupakan komponen utama dari tulang dan gigi yang mempunyai sifat dapat berikatan dengan tulang natural.7 Hidroksiapatit merupakan senyawa mineral dan anggota kelompok mineral apatit dengan rumus kimia Ca10(PO4)6(OH)2 dan mempunyai
struktur heksagonal dengan parameter kisi a = 9,433Å danc = 6,875Å serta rasio Ca/P sekitar 1,67.7Struktur unit sel Kristal HA dapat dilihat pada Gambar 2.
Mineral HA dapat disintesis dengan mereaksikan senyawa kalsium(Ca) dan fosfor(P) pada suhu dan tekanan tertentu. Sintesis HA dapat dilakukan dengan beberapa metode, yaitu metode basah dan metode kering. Metode basah menggunakan prinsip presipitasi dan sol-gel sedangkan metode kering menggunakan prinsip pencampuran sumber senyawa Ca dan P pada suhu dan tekanan tinggi. Namun, metode yang sering digunakan dalam mensintesis HA adalah metode basah, yaitu dengan menggunakan metode presipitasi sebab metode ini menghasilkan HA yang memiliki kemurnian yang cukup tinggi (90%). Proses pada metode ini, HA disintesis dengan cara mentitrasi larutan yang mengandung Ca dengan larutan yang mengandung P. Nisbah Ca/P agar material HA terbentuk adalah 1,67. Perbedaan nisbah Ca/P akan menimbulkan hasil sintesis senyawa yang berbeda. Sintesis
apatit tidak hanya dipengaruhi oleh nisbah Ca/P tetapi juga sumber senyawa Ca dan P. Paduan Ca/P yang bersumber dari sumber Ca dan P yang berbeda tidak hanya menghasilkan HA tetapi juga senyawa-senyawa campurannya yang bergantung pada senyawa sumber Ca dan P tersebut. Misalnya, sumber Ca yang berasal dari CaCl2.2H2Oakan memiliki kemungkinan
menghasilkan apatit yang mengandung klorin.8
2.1.3. Octacalcium Phosphate
Octacalcium phosphate(OCP) adalah kalsium fosfat yang mempunyai rumus Ca8H2(PO4)6.5H2O. OCP dapat menjadi
prekursor dari pembuatan email gigi, dentin dan dan tulang dalam kehidupan organisme.10
OCP telah terbukti menjadi prekursor dari hidroksiapatit, yaitu biomineral anorganik yang sangat penting dalam pertumbuhan tulang. Determinasi dari struktur kristal OCP dan kristal apatit sehingga muncul menjadi prasyarat untuk mempelajari sifat pembentukan dan sifat kimia dari jaringan tulang.Suatu saat
OCP dapat menggantikan HAp dalam
pencangkokan tulang dan implant karena strukturnya mirip dengan struktur apatit.
Menurut Weissenberg OCP mempunyai
parameter kisi a = 19,7 Å, b = 9,59 Å, c = 6,87 Å, α = β = 90,7o dan γ = 71,8o.11Struktur OCP
dapat dilihat pada Gambar 3.
2.1.4. Dicalcium Phosphate Dihydrate
Dicalcium Phosphate Dihydrate (DCPD)
juga dikenal sebagai brushite, adalah mineral kalsium fosfat yang terhidrasi dengan komposisi CaHPO4.2H2O. Struktur DCPD
hampir identik dengan dimensi gipsum yang masing-masing unit selnya sangat mirip.Tulang punggung dari DCPD terdiri dari kalsium dan atom fosfor yang membentuk rantai melalui
berbagai oksigen (empat oksigen
fosfat).13Struktur DCPD dapat dilihat pada Gambar 4.
3
Gambar 2Struktur unit sel kristal HAp.9
Gambar 3Struktur molekul OCP.11
Gambar 4Struktur molekul DCPD.12
Gambar 5 Struktur kristalβ- Ca2P2O7 dan
α-Ca2P2O7.14
2.1.5. Calcium Pyrophosphate
Calcium pyrophosphate (CPP) yang
mempunyai rumus kimia Ca2P2O7adalah senyawa kimia yang dapat dibentuk oleh reaksi asam pirofosfat dan kalsium dengan cara memanaskan kalsium fosfat. Biasanya digunakan sebagai agen abrasif ringan dalam pasta gigi.13Ca2P2O7 memiliki tiga bentuk yaitu γ, β, dan α. Bentuk γ-Ca2P2O7 terbentuk pada suhu rendah, sedangkan β- Ca2P2O7 terbentuk pada suhu 750oC dan α-Ca2P2O7 terbentuk pada suhu 1171oC13. Struktur kristalβ- Ca2P2O7 dan α-Ca2P2O7dapat dilihat pada Gambar 5.
2.2. Difraksi sinar-X
Difraksi sinar-X yaitu metode yang digunakan untuk mengetahui nilai parameter kisi, struktur kristal, dan derajat kekristalan. Derajat kekristalan adalah besaran yang menyatakan banyaknya kandungan kristal dalam suatu materi dengan membandingkan luasan kurva puncak dengan total luasan amorf dan kristal.16
Difraksi sinar-X terjadi pada hamburan elastis foton-foton sinar-X oleh atom dalam sebuah kisi periodik yang dapat dilihat seperti
pada Gambar 5. Hamburan monokromatis sinar-X dalam fasa tersebut memberikan interferensi yang konstruktif. Dasar dari
penggunaan difraksi sinar-X untuk
mempelajari kisi kristal adalah berdasarkan persamaan Bragg :
..……...(1)
Dengan λ adalah panjang gelombang sinar-X yang digunakan, d adalah jarak antara dua bidang kisi, θ adalah sudut antara sinar datang dengan bidang normal, dan n adalah bilangan bulat yang disebut sebagai orde pembiasan.16
Berdasarkan persamaan Bragg, jika seberkas sinar-X di jatuhkan pada sampel kristal, maka bidang kristal itu akan membiaskan sinar-X yang memiliki panjang gelombang yang sama dengan jarak antar kisi dalam kristal tersebut. Sinar yang dibiaskan akan ditangkap oleh detektor kemudian diterjemahkan sebagai sebuah puncak difraksi. Makin banyak bidang kristal yang terdapat dalam sampel, makin kuat intensitas pembiasan yang dihasilkannya. Setiap puncak yang muncul pada pola XRD mewakili satu bidang kristal yang memiliki orientasi tertentu dalam sumbu tiga dimensi. Puncak-puncak yang didapatkan dari data pengukuran ini kemudian dicocokkan dengan standar difraksi snar-X untuk hampir semua jenis material. Standar ini disebut JCPDS.16
Gambar 6Skema sinar datang dan sinar terdifraksi oleh kisi kristal.15
Gambar 7 Skema Difraktometer sinar-x.16 Komponen difraktometer sinar-X: 17
1. Tabung sinar-X, merupakan tempat produk sinar-X, berisi katoda filament tungsten sebagai sumber elektron dan anoda yang berupa logam target.
2. Goniometer, merupakan unit dengan tempat sampel dan detektor yang bergerak
memutar selama alat dioperasikan. Sampel diisikan dalam lempeng logam atau plat kaca yang cekung atau diisikan dalam lubang yang berada ditengah. Sampel berputar bersama goniometer dan membentuk sudut terhadap sinar-X yang datang.
3. Tempat sampel, berupa lempengan logam atau plat kaca yang cekung atau berlubang ditengahnya, dimana sampel serbuk diisikan. Sampel akan berputar bersama goniometer dan membentuk sudut terhadap sinar-X yang datang.
4. Detektor gas, berisi gas yang sensitif terhadap sinar-X, katoda dan anoda. Atom-atom gas akan terionisasi saat dikenai sinar-X (yang terdifraksi oleh sampel). menuju anoda sehingga menghasilkan arus listrik. Arus listrik diubah menjadi pulsa yang akan dihitung oleh counter dan scaler.
5. Difraktometer (scaler and counter),
berfungsi mendeteksi posisi sudut difraksi dan intensitasnya terlihat seperti pada Gambar 6.
6. Rekorder, berfungsi menampilkan pola difraksi atau difraktogram. Posisi sudut difraksi menggambarkan jenis kristal. Intensitas dapat mewakili konsentrasi kristal maupun tingkat kekristalan suatu sampel. Sampel dengan kekristalan tinggi meskipun jumlahnya sedikit akan memberikan intensitas yang tinggi dan tajam.
BAB III. METODOLOGI
PENELITIAN
3.1.
Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Biofisika Material, Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor dari bulan November 2011 sampai dengan bulan Oktober 2012.
3.2. Alat dan Bahan
Alat yang digunakan pada penelitian ini ialah peralatan preparasi, neraca analitik, labu ukur 100 ml, labu ukur 500 ml, hotplate, kertas saring,corong, crussible, alat furnacedengan merk lamberthem dan alat karakterisasi XRD merk Shimadzu tipe XRD-6000.Bahan yang digunakan dalam penelitian ini adalah CaCl2
Merck kGaA dengan No. Produk
1.06580.0500, Na2HPO4 Merck kGaA dengan
No. Produk 1.02382.0500, alumunium foil dan aquades.
3.3. Prosedur Penelitian
3.3.1. Persiapan Bahan
Bahan yang digunakan pada penelitian ini berupa serbuk CaCl2 dan Na2HPO4 dengan
perbandingan konsentrasi molarnya sebesar 0,5 M CaCl2 dan 0,3M Na2HPO4. Kedua bahan
dihitung massanya sehingga didapatkan massa untuk CaCl2 sebesar 7,351 gram per 100 ml
dan massa untuk Na2HPO4 sebesar 5,339
grapm per 100 ml.
3.3.2. Pembuatan kalsium fosfat pada
suhu ruang
Sintesis kalsium fosfat pada suhu ruang menggunakan metode single drop dan wise
drop. Sintesis kalsium fosfat diawali dengan
pembuatan larutan 0,5M CaCl2 dan 0,3M
Na2HPO4. Pada metode single drop kedua
larutan tersebut dicampurkan langsung ke dalam labu erlenmeyer dan di-strirring dengan menggunakan variasi waktu 3 jam, 6 jam, 12 jam, 18 jam, dan 24 jam. Sintesis kalsium fosfat dengan menggunakan metode wise drop dilakukan dengan cara meneteskan larutan 0,5M CaCl2secara perlahan kedalam larutan
0,3M Na2HPO4sambil dilakukan stirring
selama 90 menit. Setelah kedua larutan tersebut tercampur,stirringdilanjutkan selama 1 jam.Kemudian larutan di-aging selama 12 jam
dan disaring menggunakan kertas
saring.Selanjutnya adalah proses pengeringan dengan menggunakan furnace pada suhu 110oC
dengan waktu penahanan5 jam dan
prosessintering pada suhu 900oC dengan waktu penahanan 5 jam. Sampel yang telah
di-sintering di timbang dan sampel siap untuk
dikarakterisasi.
3.3.3. Pembuatan kalsium fosfatpada
suhu 70
oC
Larutan 0,5M CaCl2 dan 0,3M Na2HPO4
yang telah dibuat dengan metode single
dropdicampurkan secara langsung. Larutan
CaCl2 dipanaskan dengan menggunakan hotplate pada suhu 70oC selama 1 jamdan dicampurkan dengan larutan Na2HPO4secara
langsung dan di stirringselama 3 jam menggunakanhotplatepada suhu 70oC. Pada
wise drop dengan cara meneteskan larutan
0,5M CaCl2 kedalam larutan0,3M
Na2HPO4.Larutan CaCl2 dipanaskan dengan
menggunakan hotplate pada suhu 70oC selama 1 jam dan dicampurkan dengan larutan Na2HPO4dengan cara diteteskan. Setelah
5
selesai diteteskan larutan di-stirring selama 1 jam. Larutan di aging selama 12 jam dan disaring menggunakan kertas saring. Selanjutnya adalah proses pengeringan dengan menggunakan furnace pada suhu 110oCdengan waktu penahanan 5 jam dan proses sintering pada suhu 900oCdengan waktu penahanan 5 jam. Timbang massa sampel yang sudah
di-sintering dan sampel siap untuk dikarakterisasi.
3.3.4. Pembuatan kalsium fosfat metode
single drop suhu 70
oC dengan
variasi sintering (110
oC, 300
oC,
600
oC, dan 900
oC)
Larutan 0,5M CaCl2 dan 0,3M Na2HPO4
yang telah dibuat dengan metode single
dropdicampurkan secara langsung. Larutan
CaCl2 dipanaskan dengan menggunakan hotplate pada suhu 70oC selama 1 jamdan dicampurkan dengan larutan Na2HPO4secara
langsung dan di stirringselama 3 jam menggunakan hotplatepada suhu 70oC. Larutan di-aging selama 12 jam dan disaring
menggunakan kertas saring. Selanjutnya adalah proses pengeringan dengan menggunakan
furnace pada suhu 110oCdengan waktu penahanan 5 jam dan proses sintering pada suhu 300oC, 600oC, dan 900oCdengan waktu penahanan masing-masing 5 jam. Timbang massa sampel yang sudah di-sintering dan sampel siap untuk dikarakterisasi. Penamaan sampel menggunakan kode yang dapat dilihat pada Tabel 1.
3.3.5.
Karakterisasi XRD
Setelah sampel selesai dibuat dengan menggunakan metode single drop dan wise
drop, kemudian sampel tersebut dikarakterisasi
menggunakan XRD yang bertujuan untuk mengetahui nilai parameter kisi, struktur kristal, dan derajat kekristalan. Sudut 2θ yang digunakan dalam pengujian fasa pada sampel antara 10o – 80o.
Tabel 1 Penamaan kode sampel kalsium fosfat
No Kode sampel Nama sampel
1 KF_SR(3) Kalsium Fosfat metode single drop variasi stirring 3 jam pada suhu ruang
2 KF_SR(6) Kalsium Fosfat metode single drop variasi stirring 6 jam pada suhu ruang
3 KF_SR(12) Kalsium Fosfat metode single drop variasi stirring 12 jam pada suhu ruang
4 KF_SR(18) Kalsium Fosfat metode single drop variasi stirring 18 jam pada suhu ruang
5 KF_SR(24) Kalsium Fosfat metode single drop variasi stirring 24 jam pada suhu ruang
6 KF_WR Kalsium Fosfat metode wise drop variasi stirring pada suhu ruang
7 KF_s70 Kalsium Fosfat metode single drop variasi stirring pada suhu 70oC
8 KF_W70 Kalsium Fosfat metode wise drop variasi stirring pada suhu 70oC
9 KF_s70(110) Kalsium Fosfat metode single drop variasi stirring pada suhu 70oC suhu
sintering 110
10 KF_s70(300) Kalsium Fosfat metode single drop variasi stirring pada suhu 70oC suhu
sintering 300
11 KF_s70(600) Kalsium Fosfat metode single drop variasi stirring pada suhu 70oC suhu
sintering 600
12 KF_s70(900) Kalsium Fosfat metode single drop variasi stirring pada suhu 70oC suhu
4.1. Persiapan Bahan
Pencampuran 0,5 M CaCl2 sebanyak 7,351
gram dan 0,3 M Na2HPO4 sebanyak 5,339
gram dalam aquades menghasilkan larutan kalsium fosfat 200 ml yang berwarna putih seperti susu.
4.2. Hasil Kalsium Fosfat Pada Suhu
Ruang
Hasil dari proses sintering 900oC selama 5 jam adalah kalsium fosfat berupa serbuk putih halus.Sintesis kalsium fosfat dilakukan dengan menggunakan metode presipitasi yaitu
single drop dan wise drop. Pada single drop
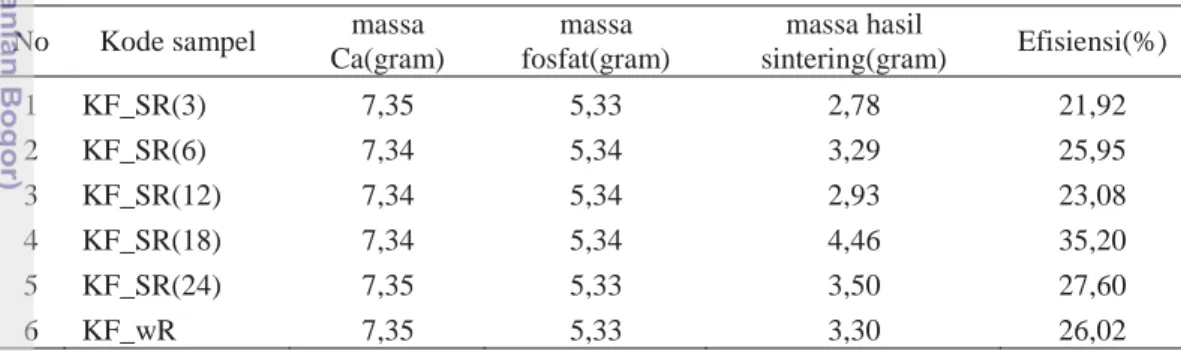
dilakukan variasi waktu stirring 3 jam, 6jam, 12 jam, 18 jam, dan 24 jam. Dari hasil sintesis kalsium fosfat didapatkan datamassa Ca dan fosfat sebelum dan sesudah sintering dan hasil tersebut dapat dilihat pada Tabel 2. Dari Tabel 2 dapat dilihat bahwa massa hasil sintering lebih kecil dari massa awal, hal ini dikarenakan
dimana m’ adalah massa hasil sintering, m1 adalah massa Ca dan m2 adalah massa fosfat.
4.3. Hasil Kalsium Fosfat Pada Suhu
70
oC
Hasil dari proses sintering 900oC selama 5 jam adalah kalsium fosfat berupa serbuk putih halus.Sintesis kalsium fosfat dilakukan dengan menggunakan metode presipitasi yaitu single
drop dan wise drop. Dari hasil sintesis kalsium
fosfatdidapatkan data massa Ca dan fosfat sebelum dan sesudah sintering dan hasil tersebut dapat dilihat pada Tabel 3. Dari Tabel 3 dapat dilihat bahwa massa hasil sintering lebih kecil dari massa awal, hal ini dikarenakan adanya pelepasan uap air selama proses
sintering berlangsung. Efisiensi pada Tabel 3
diperoleh dari persamaan 2.
Tabel 2 Efisiensi massa Ca dan fosfat pada suhu ruang
Tabel 3Efisiensi massa Ca dan fosfat pada suhu 70oC
No Kode sampel massa Ca (gram)
massa fosfat (gram)
massa hasil sintering (gram)
Efisiensi (%)
1 KF_S70 7,34 5,34 3,22 25,39
2 KF_W70 7,35 5,36 3,04 23,91
Tabel 4 Efisiensi massa Ca dan fosfat pada suhu 70oC dengan variasi sintering
No Kode sampel massa Ca (gram) massa fosfat (gram) massa hasil sintering(gram) Efisiensi (%) 1 KF_s70(110) 7,36 5,34 4,04 31,85 2 KF_s70(300) 7,36 5,34 3,96 31,18 3 KF_s70(600) 7,35 5,35 3,73 29,37 4 KF_s70(900) 7,35 5,35 2,74 21,57
No Kode sampel massa Ca(gram) massa fosfat(gram) massa hasil sintering(gram) Efisiensi(%) 1 KF_SR(3) 7,35 5,33 2,78 21,92 2 KF_SR(6) 7,34 5,34 3,29 25,95 3 KF_SR(12) 7,34 5,34 2,93 23,08 4 KF_SR(18) 7,34 5,34 4,46 35,20 5 KF_SR(24) 7,35 5,33 3,50 27,60 6 KF_wR 7,35 5,33 3,30 26,02
4.4. Hasil Kalsium Fosfat Metode Single
Drop Pada Suhu 70
oC dengan
Variasi Sintering (110
oC, 300
oC,
600
oC, 900
oC)
Hasil dari proses sintering110oC selama 5 jam adalah kalsium fosfat berupa serbuk putih namun tidak terlalu halus, sedangkan hasil dari proses sintering 300oCselama 5 jam adalah kalsium fosfat berupa serbuk putih yang sangat halus. Hasil dari proses sintering600oC selama 5 jam adalah berupa serbuk putih halus dan hasil dari prosessintering 900oC selama 5 jam adalah kalsium fosfat berupa serbuk putih halus. Dari hasil sintesis kalsium fosfatdidapatkan data massa Ca dan fosfat sebelum dan sesudah sintering dan hasil tersebut dapat dilihat pada Tabel 4. Dari Tabel 4 dapat dilihat bahwa massa hasil sintering lebih kecil dari massa awal, hal ini dikarenakan adanya pelepasan uap air selama proses
sintering berlangsung.Efisiensi pada Tabel 4
diperoleh dari persamaan 2.
4.5. Hasil Karakterisasi XRD
Hasil karakterisasi XRD pada sampel
KF_SR(3) Gambar 7 menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphate karena fase calcium pyrophosphate dapat terbentuk pada suhu sintering >1000oCnamun terdapat fase lain dari
kalsium fosfat yaitu hydroxyapatite, octacalcium phosphate, carbonate apatite type-A dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard (JCPDS) untuk Na2HPO4
No. 33-1247, TCP No. 0169, HA No. 09-0432, CAA dengan No. 35-0180, CAB dengan No. 19-0272 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 7 hasil XRD sampel KF_SR(3)
puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 29,58o, CAB 33,8o, CAA 39,68o, dan HA 41,7o.
Hasil karakterisasi XRD pada sampel
KF_SR(6) Gambar 8menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphate karena fase calcium pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite dan tricalcium phosphate. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard (JCPDS) untuk CaCl2
No.24-0223,Na2HPO4 No. 33-1247, TCP No.
09-0169, HA No. 09-0432 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 7 hasil XRD sampel KF_SR(6) puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 29,58o dan Na2HPO431,92
o
Gambar 8Hasil XRDsampel denganmetode single drop dan wise drop pada suhu ruang yang
9
Hasil karakterisasi XRD pada sampel
KF_SR(12) Gambar 8 menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphatekarena fase calcium pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate, carbonate apatite type-A dan carbonate apatite type-B.Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan dataJoint Committee on Powder Diffraction Standard
(JCPDS) untuk CaCl2 No.24-0223,Na2HPO4
No. 33-1247, TCP No. 0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180, CAB dengan No. 19-0272 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 7 hasil XRD sampel KF_SR(12) puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 29,6o, OCP 26,66o, HA 32,58o dan CAB 49,72o.
Hasil karakterisasi XRD pada sampel
KF_SR(18) Gambar 8menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphate karena fase calcium pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan dataJoint Committee on Powder Diffraction Standard (JCPDS) untuk Na2HPO4
No. 33-1247, TCP No. 0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180, CAB dengan No. 19-0272 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 7 hasil XRD sampel KF_SR(18) puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 29,6o, 32,54o, OCP 26,68o dan CAB 49,72o.
Hasil karakterisasi XRD pada sampel
KF_SR(24) Gambar 8menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphatekarena fase calcium pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan dataJoint Committee on Powder Diffraction Standard (JCPDS) untuk CaCl2
No.24-0223,Na2HPO4 No. 33-1247, TCP No.
09-0169, HA No. 09-0432, CAA dengan No. 35-0180dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 7hasil XRD sampel KF_SR(24) puncak tertinggi dengan nilai 2θCa2P2O7 29,62o, OCP 27,72o, HA 32,58o dan CAB 49, 52o.
Hasil karakterisasi XRD pada sampel
KF_WR Gambar 8menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphatekarena fase calcium pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan dataJoint Committee on Powder Diffraction Standard (JCPDS) untuk CaCl2
No.24-0223, Na2HPO4 No. 33-1247, TCP No.
09-0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 7puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 29,66o, OCP 28,98o, CaCl2 42,74
o
dan CAB 49,24o
Tabel 5Komposisi senyawa yang dihasilkan dari sintesis kalsium fosfat suhu ruang
No Kode sampel %
Ca2P2O7 HA TCP OCP Na2HPO4 CaCl2 CAA CAB
1 KF_SR(3) 77,39 6,02 3,15 - 2,64 - 1,89 8,92 2 KF_SR(6) 78,54 3,72 5,75 - 10,16 1,83 - - 3 KF_SR(12) 61,89 9,7 4,45 12,61 1,95 2,09 3,01 4,3 4 KF_SR(18) 58,71 10,33 5,66 7,82 8,97 3,25 - 5,26 5 KF_SR(24) 58,56 10,29 1,06 18,72 4,47 3,96 - 2,94 6 KF_WR 55,06 11,09 11,92 6,72 3,12 4,66 - 6,01
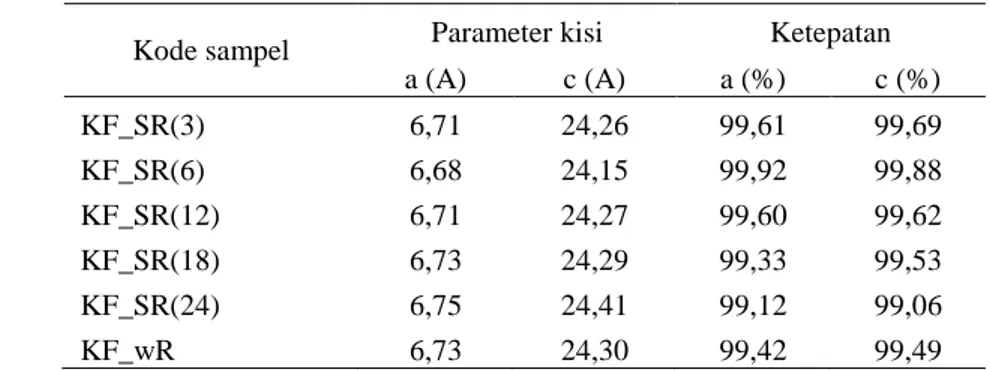
Tabel 6Perhitungan parameter kisi dan persentase ketepatancalcium pyrophosphatepada suhu ruang
Kode sampel Parameter kisi Ketepatan
a (A) c (A) a (%) c (%) KF_SR(3) 6,71 24,26 99,61 99,69 KF_SR(6) 6,68 24,15 99,92 99,88 KF_SR(12) 6,71 24,27 99,60 99,62 KF_SR(18) 6,73 24,29 99,33 99,53 KF_SR(24) 6,75 24,41 99,12 99,06 KF_wR 6,73 24,30 99,42 99,49
Komposisi senyawa yang dihasilkan dari sintesis senyawa kalsium fosfat dapat dilihat pada Tabel 5. Dari Tabel 5 dapat terlihat bahwa lamanya waktu stirring tidak terlalu berpengaruh dalam proses terbentuknya fase
calcium pyrophosphatekarena semakin lama
waktu stirring maka calcium pyrophosphate yang dihasilkan tidak semakin banyak. Disamping itu senyawa precursoryang larut lebih banyak pada waktu stirring 3 jam.
Perhitungan parameter kisi dan ukuran kristal dari metode single drop dan wise
droppada suhu ruang dapat diperoleh dari
analisis XRD dan parameter kisi dihitung dengan menggunakan metode Cramer. Hasil perhitungan parameter kisi dan persentase ketepatan parameter kisi sampel kalsium fosfat dari metode single drop dan wise drop pada suhu ruang dapat dilihat pada Tabel 6. Pada Tabel 6 dapat terlihat bahwa parameter kisi yang didapat hampir mendekati nilai JCPDS yaitu a = 6,688 Å dan c = 24,18 Å, hal ini terlihat pada sampel dengan variasi stirring 6 jam dengan nilai a = 6,68 Å dan c = 24,15 Å yang memiliki ketepatan 99,92% dan 99,98%.
Hasil XRD dari sampel KF_s70 Gambar 9menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium
pyrophosphate karena fase calcium
pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate,
carbonate apatite type-A dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard
(JCPDS)untuk CaCl2 No.24-0223, Na2HPO4
No. 33-1247, TCP No. 0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180, CAB dengan No. 19-0272 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 9 puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 28,96o, OCP27,68o , CAA 32,58o, Na2HPO440,58o,
HA 42,02o dan CAB 49,06o.
Hasil XRD dari sampel KF_W70Gambar 9menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium
pyrophosphatekarena fase calcium
pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate, carbonate apatite type-A dan carbonate apatite type-B.Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard
(JCPDS)untuk Na2HPO4 No. 33-1247, TCP
No. 09-0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180 dan Ca2P2O7 dengan No. 09-0346. Pada Gambar 8 puncak tertinggi dengan nilai 2θ untuk dan Ca2P2O7 29,58o, OCP 27,68o, HA 32,56o, CAA 39,74o dan CAB 49,12o.
11
Gambar 9HasilXRD sampel dengan metode single drop dan wise drop pada suhu 70
oyang di-sintering 900
o.
Tabel 7Komposisi senyawa yang dihasilkan dari sintesis kalsium fosfat
Tabel 8Hasil perhitungan parameter kisi menggunakan persamaan-persamaan pada lampiran 12 dan persentase ketepatancalcium pyrophosphatepada suhu 70oC
Komposisi senyawa yang dihasilkan dari sintesis senyawa kalsium fosfat dapat dilihat pada Tabel 7. Dari Tabel 7 dapat terlihat bahwa pada metode wise drop lebih banyak menghasilkan fase calcium pyrophosphate dan faselain dari kalsium fosfat yaitu hydroxyapatite dan tricalcium phosphate, disamping itu senyawa prekursornya sudah mulai bereaksi karena pada saat dipanaskan senyawa prekursorakan lebih cepat bereaksi. Pengaruh kenaikan suhu pada kelarutan zat
berbeda-beda antara yang satu dengan yang lainnya. Tetapi pada umumnya kelarutan zat padat dalam cairan bertambah dengan naiknya suhu, karena kebanyakan proses pembentuka larutan bersifat endoterm.18
Perhitungan parameter kisi dan ukuran kristal dari metode single drop dan wise
droppada suhu 70oC dapat diperoleh dari analisis XRD dan parameter kisi dihitung dengan menggunakan metode Cramer. Hasil perhitungan parameter kisi dan persentase ketepatan parameter kisi sampel kalsium fosfat dari metode single drop dan wise drop pada
No Kode sampel %
Ca2P2O7 HA TCP OCP Na2HPO4 CaCl2 CAA CAB
1 KF_s70 44,46 5,86 2,31 26,35 7,21 0,21 9,61 3,99
2 KF_W70 53,2 20,84 5,43 10,31 3,3 - 3,04 3,88
Kode sampel Parameter kisi Ketepatan
a (A) c (A) a (%) c (%)
KF_S70 6,72 24,29 99,57 99,54
suhu ruang dapat dilihat pada Tabel 8. Pada Tabel 8 dapat terlihat bahwa parameter kisi yang didapat hampir mendekati nilai JCPDS yaitu a = 6,688 Å dan c = 24,18 Å, hal ini terlihat pada sampel single drop dengan nilai a = 6,67 Å dan pada sampel wise drop dengan nilai c = 24,26 Å yang memiliki ketepatan 99,57% dan 99,66%.
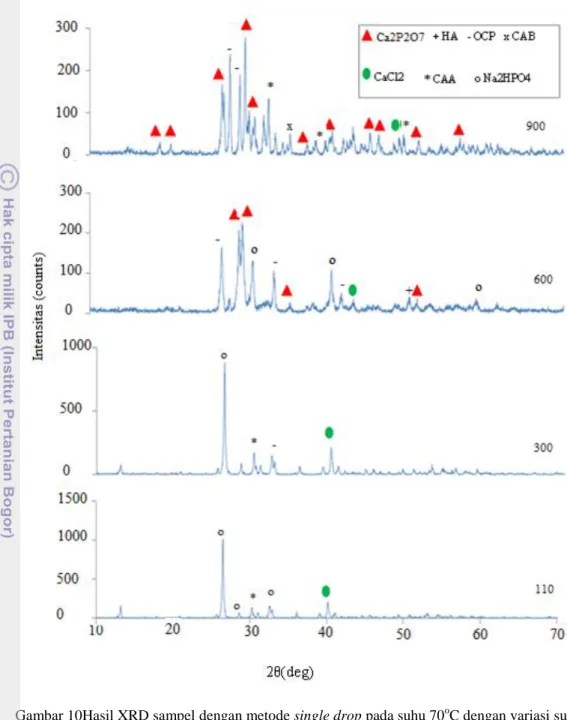
Hasil XRD sampel KF_s70(110) Gambar 10menunjukkan bahwa fase yang dominan terbentuk masih bahan prekursornya namun sudah terdapat fase lain dari kalsium fosfat yaitu fase hydroxyapatite dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard
(JCPDS)untukNa2HPO4 No. 33-1247, CAA
dengan No. 35-0180dan CaCl2 No.24-0223.
Pada Gambar 9 puncak tertinggi dengan nilai 2θ untukNa2HPO4 26,52o, CAA 32,58odan
CaCl240,04o.
Hasil XRD sampel KF_s70(300)Gambar 10menunjukkan bahwa fase yang dominan terbentuk masih bahan prekursornya namun sudah terdapat fase lain dari kalsium fosfat yaitu fase hydroxyapatite dan fase octacalcium phosphate. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard
(JCPDS)untukNa2HPO4 No. 33-1247, TCP No.
09-0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180 dan CaCl2
No.24-0223.Pada Gambar 9 puncak tertinggi dengan nilai 2θ untuk Na2HPO4 26,38
o
,OCP32,28o dan CaCl240,02o.
Hasil XRD sampel KF_s70(600) Gambar 10menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium pyrophosphate namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite dan
octacalcium phosphate. Identifikasi fase
kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard (JCPDS)untukNa2HPO4
No. 33-1247,TCP No. 0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180, CaCl2 No.24-0223 dan Ca2P2O7 dengan No. 09-0346.Pada gambar 17 puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 28,86o, CaCl228,9 o , OCP 26,66o, Na2HPO430,54 o dan HA 50,24o.
Hasil XRD sampel KF_s70(900)Gambar 10menunjukkan bahwa fase yang paling dominan terbentuk adalah fase calcium
pyrophosphatekarena fase calcium
pyrophosphate dapat terbentuk pada suhu sintering >1000oC namun terdapat fase lain dari kalsium fosfat yaitu hydroxyapatite, tricalcium phosphate, octacalcium phosphate, carbonate apatite type-A dan carbonate apatite type-B. Identifikasi fase kalsium fosfat yang dihasilkan dilakukan dengan mencocokan pola hasil karakterisasi XRD dengan data Joint Committee on Powder Diffraction Standard
(JCPDS)untukNa2HPO4 No. 33-1247, TCP No.
09-0169, HA No. 09-0432, OCP No. 44-0778, CAA dengan No. 35-0180, CaCl2
No.24-0223dan Ca2P2O7 dengan No. 09-0346.Pada Gambar 10 puncak tertinggi dengan nilai 2θ untuk Ca2P2O7 26,72
o
, CaCl2 29,66 o
, OCP 27,72o, CAA 32,62o dan CAB 35,3o.
13
Gambar 10Hasil XRD sampel dengan metode single drop pada suhu 70oC dengan variasi suhu
sintering.
Tabel 9Komposisi senyawa yang dihasilkan dari sintesis kalsium fosfat
No Kode sampel %
Ca2P2O7 HA TCP OCP Na2HPO4 CaCl2 CAA CAB
1 KF_s70(110) - 5,61 - - 72,96 10,72 - 1,9
2 KF_s70(300) - 14,28 - 8,79 49,72 15,61 11,6 -
3 KF_s70(600) 8,33 4,98 - 23,28 22,73 40,68 - -
Tabel 10Perhitungan parameter kisi dan persentase ketepatanCa2P2O7 pada suhu 70oC dengan
variasi sintering
Tabel 11Hasil pengukuran derajat kristalinitas pada suhu 70oC dengan variasi sintering
Komposisi senyawa yang dihasilkan dari sintesis senyawa kalsium fosfat dapat dilihat pada Tabel 9. Dari Tabel 9 dapat terlihat bahwa suhu sintering sangat berpengaruh karena pada saat sintering suhu 110oC senyawa prekursor masih belum bereaksi dengan sempurna sedangkan pada saat sintering suhu 900oC senyawa prekursor sudah bereaksi dan membentuk fase hydroxyapatite, tricalcium
phosphate dan octacalcium phosphate.
Disamping itu fase calcium pyrophosphate yang terbentuk lebih banyak.
Perhitungan parameter kisi dan ukuran kristal dari metode single drop variasi sintering dapat diperoleh dari analisis XRD dan parameter kisi dihitung dengan menggunakan metode Cramer. Hasil perhitungan parameter kisi dan persentase ketepatan parameter kisi sampel kalsium fosfat dari metode single
dropsuhu 70oC variasi sinteringdapat dilihat pada Tabel 10.Pada Tabel 10 dapat terlihat
bahwa parameter kisi yang didapat hampir mendekati nilai JCPDS yaitu a = 6,688 Å dan c = 24,18 Å, hal ini terlihat pada sampel dengan variasi sintering900oC dengan nilai a = 6,68 Å dan c = 24,16 Å yang memiliki ketepatan 99,88% dan 98,90%.
Pengukuran derajat kristalinitas dapat diperoleh langsung dari program karakterisasi XRD. Hasil pengukuran derajat kristalinitas dapat dilihat pada Tabel 11. Pada Tabel 11 derajat kristalinitas yang paling tinggi terdapat pada sampel KF_S70(900)hal ini menunjukan bahwa pada suhu sintering 900oC kristal yang terbentuk lebih banyak bila dibandingkan dengan suhu sintering lainnya, karena semakin besar suhu sinteringmaka kristal yang terbentuk akan semakin banyak sehingga proses sinteringakan berpengaruh cukup besar dalam proses pembentukan fase kristal suatu bahan.19
Kode sampel Parameter kisi Ketepatan
a (A) c (A) a (%) c (%)
KF_S70(600) 6,73 24,41 99,45 99,05
KF_S70(900) 6,68 24,16 99,88 99,90
Kode sampel Derajat kristalinitas KF_S70(110) 77,53 KF_S70(300) 87,86 KF_S70(600) 67,12 KF_S70(900) 92,12
BAB V. KESIMPULAN DAN
SARAN
5.1.
Kesimpulan
Sintesis senyawa kalsium fosfat yang dihasilkan dari pencampuran larutan 0,5 M CaCl2 dan larutan 0,3 M Na2HPO4 berupa
larutan putih seperti susu. Hasil dari sintering pada suhu 900oC berupa serbuk putih halus.
Sintesis senyawa kalsium fosfat dengan menggunakan metode single drop telah dilakukan dan hasil yang diperoleh membentuk fase kalsium fosfat yaitu hydroxyapatite,
tricalcium phosphate dan octacalcium phosphate sama dengan hasil dari metode wise drop namun komposisi yang dihasilkan
berbeda.
Hasil difraktogramX-Ray antara single drop pada suhu ruang dan suhu 70oC menunjukkan tidak adanya perbedaan yang signifikan.Pada suhu 70oC senyawa prekursornya semakin bereaksi dan bertransformasi menjadi
hydroxyapatite, tricalcium phosphate dan octacalcium phosphate.Hasil yang berbeda
ditunjukan pada hasil variasi sintering yang berbeda pada suhu yang berbeda.Pada suhu 110oC dan 300oC senyawa prekursor yang terbentuk masih belum bereaksi, sedangkan pada suhu 600oC dan 900oC senyawa
prekursornya telah bereaksi dan
bertransformasi menjadi calcium
pyrophosphate,hydroxyapatite, tricalcium phosphate dan octacalcium phosphate. Namun
yang paling dominan adalah fase calcium
pyrophosphate.Sintering terbaik untuk single dropdan wise dropdilakukan pada suhu 900oC. Proses sinteringakan berpengaruh cukup besar dalam pembentukan fase kristal suatu bahan.
Parameter kisi yang dihasilkan dari seluruh sampel mencapai nilai diatas 90%baik disintesis dengan single drop maupun wise
drop. Pada sampel kalsium fosfat pada suhu
ruang dengan variasi stirring 6 jam mempunyai ketepatan paling tinggi sebesar 99,92% dan 99,98%.
5.2. Saran
Untuk penelitian lebih lanjut dapat ditambahkan N2 pada saat proses sintesis
kalsium fosfat sehingga tidak ada udara luar yang masuk ke dalam larutan agar pada saat dikarakterisasi tidak terdapat karbonat di dalam sampel,dapat juga mengurangi konsentasi Molarnya agar larutan yang dibuat tidak terlalu
jenuh sehingga dapat menghasilkan kalsium fosfat yang sempurna khususnya HAp ataupun TCP yang murni. Disamping itu dapat juga membuat kalsium fosfat dengan suhu 700C dengan waktustiring diatas 3 jam.
Characterization of hydroxyapatit Porous Scaffolds for Tissue Engineering, Material
Science and Engineering C,
doi:10.1016/j.msec.2008.09.052, hal. 1. 2. Kalfas, Ian , H. (2001). principles of bone
healing. Neurosurg. Focus. Vol 10.
3. Krishna D.S.R., Siddharthan A, Seshadri SK, Kumar TSS.(2007). A Novel Route for Synthesis of Nanocrystalline Hydroxyapatite from Eggshell Waste.
Material Medicine 18:1735-1743.
4. Elliott, J.C. (1973). The Problem og
Composition and Structure of the Mineral Component of The Hard Tissues.
5. Soejoko, D.S.,Wahyuni, S. (2002). Spektroskopi Inframerah Senyawa Kalsium Fosfat Hasil Presipitasi. Makara
seri Sains 6 (No.3):117-120.
6. Shi, D. (2003). Biomaterial and Tissue Engineering. New York:Springer.
7. Aoki, H. (1991).Science and Medical
Application of Hydroxyapatite. Tokyo:
Tokyo Medical and Dental University. 8. Hanson, B. (2005). 150000000:1 Model of
Hydroxyapatite.
9. Boanini. E. et al. (2008).
Alendronate-hydroxyapatite nanocomposites and theirs interaction with osteoclasts and osteoblast-like cells.
10. Reacquel, Z.L. (1985). "Preparation of octacalcium phosphate (OCP): A direct fast method", Journal Calcified Tissue International, Volume 37, Number 2. 11. Brown, W. E., Lehr, J. R.. Smith, J. P.,
Frazier, A. W., J. (1957). Am. Chem. Soc.79 (19), 5318.
12. Anonim. (2012).dicalcium phosphate dehydrate. http://www. dailymed.nlm.nih.
[16 September 2012]
13. F.H. Lin, J.R. Liaw, M.H. Hon, C.Y. Wang, Mater. Chem. Phys. 41(1995) 110. 14. L.M. Grover, U. Gbureck, A.J. Wright,
and J. E. Barrale. (2005). Cement
formulations in the calcium phosphateH2O – H3PO4 – H4P2O7
systems. J. Am. Ceram. Soc. 88(11), 3096 – 3103.
15. Eby. G. N. (2004). Principles of Enviromental Geochemistry.
16. Cullity, B.D. and Stock, S.R., 2001, Elements of X-Ray Diffraction, Third Edition, Addison-Wesley, 664 p.
17. James R. Connolly. (2007). Introduction to X-Ray Powder Diffraction.