i
ISOLASI, IDENTIFIKASI DAN UJI AKTIVITAS ANTIOKSIDAN SENYAWA FLAVONOID FRAKSI METANOL DAN FRAKSI ASETON
DAUN TANAMAN ADAM HAWA (Rhoeo discolor (L'Hér.) Hance) DENGAN METODE 2,2-diphenyl-1-picrylhidrazyl (DPPH)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Deriven Samurai Teweng NIM : 138114046
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
iv
HALAMAN PERSEMBAHAN
ix
DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... vii
PERNYATAAN PERSETUJUAN PUBLIKASI ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
ABSTRAK ... xiii
ABSTRACT ... xiv
PENDAHULUAN ... 1
METODE PENELITIAN ... 2
HASIL DAN PEMBAHASAN ... 5
KESIMPULAN ... 13
DAFTAR PUSTAKA ... 14
LAMPIRAN ... 16
x
DAFTAR TABEL
Tabel I. Nilai Rf yang dihasilkan pada KLTP... ...7
Tabel II. Identifikasi Senyawa Flavonoid Isolat Fraksi Metanol... ...8
Tabel III. Identifikasi Senyawa Flavonoid Isolat Fraksi Aseton... ...8
xi
DAFTAR GAMBAR
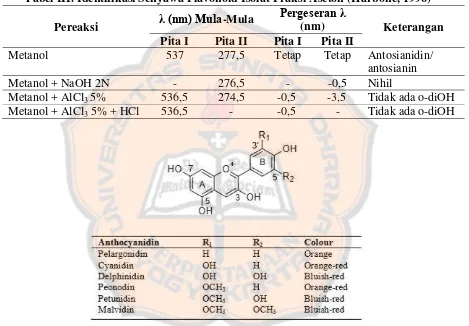
Gambar 1. Struktur Dasar Antosianidin...8
Gambar 2. Struktur Antosianidin Memiliki Aktivitas Antioksidan...9
Gambar 3. Reaksi antara Senyawa Antosianidin dan DPPH...9
Gambar 4. Grafik Konsentrasi Rutin terhadap Persen Hambat (%IC)...10
Gambar 5. Grafik Konsentrasi Fraksi Metanol terhadap Persen Hambat (%IC) ..11
xii
DAFTAR LAMPIRAN
Lampiran 1.Tanaman Adam Hawa ... ...16
Lampiran 2.Determinasi Tanaman Adam Hawa ... ...17
Lampiran 3.Sampel Daun Adam Hawa ... ...18
Lampiran 4.Ekstrasi dan Fraksinasi ... ...18
Lampiran 5.Isolasi dan Identifikasi Senyawa Flavonoid ... ...20
Lampiran 6.Uji Aktivitas Antioksidan (DPPH) ... ...23
Lampiran 7.Hasil Uji Statistik... ...35
xiii
Abstrak
Senyawa antioksidan adalah senyawa yang dapat menstabilkan radikal bebas. Daun adam hawa (Rhoeo discolor (L'Her.) Hance.) yang berwarna ungu diduga mengandung senyawa flavonoid yaitu antosianidin sebagai senyawa antioksidan. Penelitian ini bertujuan mengetahui jenis antosianidin dan aktivitas antioksidan yang dinyatakan sebagai nilai IC50 pada fraksi metanol dan aseton ekstrak etanol 96% daun adam hawa. Serbuk simplisia daun adam hawa dimaserasi dengan etanol 96% dan diremaserasi hingga hasil filtrat jernih. Ekstrak etanol 96% difraksinasi dengan metode dekantasi menggunakan pelarut n-heksan, aseton dan metanol. Fraksi aseton dan metanol yang diperoleh diisolasi dengan KLT preparatif dengan fase diam silika gel 60 F254 dan fase gerak n-butanol: asam asetat : air (4:1:5). Isolat diidentifikasi senyawa antosianidin dengan pereaksi geser dan diuji aktivitas antioksidan untuk mendapatkan nilai IC50 fraksi dengan metode 2,2-diphenyl-1-picrylhidrazyl (DPPH). Fraksi metanol diduga terdapat senyawa antosianidin yaitu malvidin dengan nilai IC50 yaitu 827,805 ± 32,710 µg/mL sedangkan fraksi aseton diduga terdapat senyawa antosianidin yaitu pelargonidin/peonidin dengan nilai IC50 yaitu 790,159 ± 29,623 µg/mL. Hasil yang diperoleh menunjukkan bahwa fraksi metanol dan aseton ekstrak etanol 96% daun adam hawa mengandung senyawa antosianidin dan memiliki aktivitas antioksidan.
xiv Abstract
1
PENDAHULUAN
Perubahan yang terjadi pada kondisi lingkungan dan pola hidup masyarakat, terutama pola makan dan kebiasaan buruk di kota-kota besar pada negara berkembang seperti Indonesia menjadikan tubuh lebih mudah terkena berbagai jenis penyakit, khususnya penyakit yang disebabkan oleh radikal bebas. Radikal bebas tersebut dapat menyebabkan timbulnya penyakit degenertif seperti kanker, penyakit kardiovaskular, kerusakan hati dan penuaan dini (Musaforah, 2015).
Senyawa yang dapat menstabilkan radikal bebas tersebut ialah senyawa antioksidan. Salah satu tanaman yang dapat digunakan sebagai sumber antioksidan ialah adam hawa (Rhoeo discolor (L'Hér.) Hance). Adam hawa termasuk dalam famili Commelinaceae dan suku gawar-gawaran yang berasal dari Meksiko dan Hindia Barat.
Tanaman ini sering ditanam sebagai tanaman hias karena daunnya yang berwarna keunguan dan dikenal juga digunakan sebagai etnobotani, yang mungkin dikaitkan dengan antibakteri dan antioksidan (Tan et al.,2014).
Berdasarkan penelitian Avila et al. (2003), melakukan uji aktivitas antioksidan DPPH ekstrak etanol 96% daun adam hawa dengan konsentrasi 1, 10, dan 100 µg/mL dengan masing-masing persen hambat yaitu 67, 68, dan 79%. Penelitian Sitorus et al. (2012) melakukan isolasi dengan KLT preparatif dan identifikasi senyawa flavonoid pada ekstrak etanol 95% daun adam hawa serta senyawa flavonoid yang diperoleh adalah antosianidin. Antosianidin merupakan aglikon antosianin yang terbentuk bila antosianin dihidrolisis dengan asam. Antosianidin ini larut dalam metanol, etanol, aseton, atau kloroform (Harborne, 1996).
2
METODE PENELITIAN
Bahan yang digunakan dalam penelitian ini adalah daun adam hawa (CV. Merapi Farma Herbal) diambil pada bulan Agustus 2016 sebagai bahan utama, metanol pro analisis (E.Merck), AlCl3 5% (E.Merck), NaOH 2M (E.Merck), dan HCl (E.Merck), etanol 96% (CV. General Labora), n-heksan teknis (CV. General Labora), aseton teknis (CV. General Labora), alumunium foil, DPPH (Aldrich), lempeng KLT Silika Gel 60 F254 (E.Merck), rutin (Sigma), n-butanol (E.Merck), asam asetat (E.Merck), dan aquadest (CV. General Labora).
Alat yang digunakan meliputi Shaker (Innova TM 2100), vortex (Janke & Kunkel), spektrofotometer UV-Vis (Shimadzu UVmini-1240 single beam A10935105039 CD, mikropipet (20-200) µL (Acura 825, Socorex), UV cabinet (CAMAG), timbangan analitik METTLER TOLEDO (max 3100 g, min 0,5 g), timbangan analitik OHAUS (max 210 g, min 0,0001 g), vakum penguap putar (vaccum rotary evaporator) (Buchi R-210,Jerman), Oven (Memmert 30-1060), ayakan no. mesh 40, blender, sentrifugator (PLC-03), waterbath, peralatan gelas.
Determinasi Tanaman
Determinasi tanaman adam hawa menggunakan seluruh bagian tanaman (daun, batang, akar, bunga dan buah) yang dilakukan secara benar berdasarkan buku acuan Flora Untuk Sekolah di Indonesia Tahun 1992 yang terdapat di Laboratorium Kebun Obat Fakultas Farmasi Universitas Sanata Dharma Yogyakarta, untuk proses determinasi dibantu oleh tenaga ahli (determinator).
Pengumpulan Bahan Uji
Bahan uji yang digunakan adalah daun tanaman adam hawa yang diperoleh dari CV. Merapi Farma, Yogyakarta. Daun yang diambil yaitu daun tua (bukan daun kuning). Daun dipetik satu persatu secara manual. Kriteria daun yang digunakan yaitu daun utuh, segar, berbentuk pedang dengan panjang 15 - 30 cm dan lebar 2,5 - 5,5 cm, ujung daun runcing, permukaan daun gundul serta warna daun di permukaan atas hijau dan di bagian bawah berwarna merah ungu.
Pembuatan Simplisia
3
dikeringkan dalam oven dengan bantuan blower pada suhu 40ºC. Daun adam hawa dikatakan kering jika daun dapat hancur ketika diremas dengan tangan. Daun adam hawa yang telah dikeringkan kemudian diserbuk menggunakan blender, lalu diayak menggunakan ayakan nomor mesh 40.
Ekstraksi Daun Tanaman Adam Hawa
Serbuk kering daun adam hawa ditimbang kurang lebih 50 g kemudian dimaserasi dengan pelarut etanol 96% sebanyak 250 mL. Maserasi meliputi pengadukan selama 6 jam dengan shaker, kemudian didiamkan selama 18 jam. Hasil maserat dan sisa serbuk dipisahkan. Sisa serbuk dimaserasi kembali dengan pelarut etanol 96% hingga filtrat hasil maserasi jernih. Hasil maserat digabung dan dipekatkan dengan vaccum rotary evaporator pada suhu kurang lebih 40ºC. Kemudian ekstrak dipekatkan kembali dengan waterbath hingga bobot tetap sehingga diperoleh ekstrak kental etanol 96% dan dihitung rendemennya.
Fraksinasi Ekstrak Daun Tanaman Adam Hawa
Ekstrak etanol 96% kental ditimbang kurang lebih 5 g, ekstrak dibagi menjadi dua dan masing-masing 2,5 g ekstrak ditambahkan dengan n-heksan sebanyak 50 mL, kemudian dipisahkan antara yang larut dan tidak larut dalam n-heksan. Ekstrak yang tidak larut dalam n-heksan ditambahkan 50 mL pelarut aseton, dipisahkan antara yang larut dan tidak larut dalam aseton. Ekstrak yang larut dalam aseton disebut fraksi aseton. Ekstrak yang tidak larut dalam aseton ditambahkan 50 mL metanol, dipisahkan antara yang larut dan tidak larut dalam metanol. Ekstrak yang larut dalam metanol disebut fraksi metanol. Masing-masing hasil fraksi aseton dan metanol digabung dan dipekatkan dengan vaccum rotary evaporator pada suhu kurang lebih 40oC. Kemudian tiap fraksi dipekatkan kembali dengan waterbath hingga bobot tetap dan dihitung rendemennya.
Isolasi Fraksi
4
254 nm dan 366 nm. Pita-pita yang diperoleh dari hasil KLT preparatif dikerok pada fase diam yang telah dielusikan, lalu serbuk dilarutkan dengan metanol p.a. sebanyak 10 mL dan disentrifugasi selama 15 menit dengan kecepatan 5000 rpm untuk mengendapkan fase diamnya (silika gel), lalu supernatannya diambil sebagai isolat.
Identifikasi Senyawa Flavonoid Isolat
Isolat yang didapatkan dari masing-masing fraksi aseton dan fraksi metanol diidentifikasi dengan spektrofotometer UV-Vis. Setiap isolat dari fraksi aseton dan fraksi metanol diambil 1 - 2 mL, kemudian diukur pada panjang gelombang dengan rentang 200-600 nm. Bila spektrum panjang gelombang menunjukkan spektrum khas flavonoid pada pita II (240-285) nm dan pita I (300-550) nm (Harbone,1996), isolat ditambahkan larutan pereaksi geser seperti AlCl3 5% (6 tetes)/HCl (3 tetes) dan NaOH 2M (3 tetes) secara
bergantian kemudian diukur panjang gelombangnya (λ).
Uji Aktivitas Antioksidan
Uji pendahuluan (penentuan panjang gelombang DPPH dan operating time (OT))
Larutan DPPH dibuat dengan konsentrasi 40 µg/mL, kemudian larutan DPPH diukur spektrum serapan menggunakan spektrofotometer UV/Vis pada panjang gelombang
400 nm hingga 600 nm dan ditentukan panjang gelombang maksimalnya (λmaks).
Setelah didapatkan λmaks, larutan DPPH 3,8 mL dimasukkan dalam tabung
ditambah 0,2 ml larutan standar rutin dengan masing-masing pada tiga tingkat konsentrasi yaitu tinggi, sedang dan rendah yaitu 10 ; 30 ; 50 µg/mL pada titik waktu 0; 5; 10; 15; 20; 25; 30; 35; 40; 45; 50; 55 dan 60 menit pada panjang gelombang maksimum yang telah diperoleh serta ditentukan operating time yang menunjukkan penurunan absorbansi yang tidak signifikan (stabil).
Uji Aktivitas Antioksidan Fraksi Metanol, Fraksi Aseton dan Rutin
5
Rutin digunakan sebagai baku pembanding, rutin ditimbang 10,0 mg dan dilarutkan dalam 10 mL metanol p.a hingga homogen (konsentrasi 1.000 µg/mL). Larutan rutin diambil masing-masing 0,2; 0,4; 0,6; 1; 1,4 mL, kemudian dimasukkan kedalam labu ukur 10 mL dan ditambahkan volumenya dengan metanol p.a hingga batas tanda (konsentrasi 20; 40; 60; 80; dan 100 µg/mL). Dari masing-masing konsentrasi larutan uji tiap fraksi diambil 0,2 mL dimasukkan kedalam tabung reaksi, ditambahkan 3,8 mL DPPH 0,02 mg/mL, divortex hingga homogen, didiamkan selama OT dan diukur serapannya pada panjang gelombang yang telah ditentukan. Pembanding rutin dilakukan pengujian yang sama seperti pada fraksi. Dilakukan replikasi tiga kali.
Tata Cara Analisis Hasil
Hasil Uji Aktivitas Antioksidan
Untuk mendapatkan nilai IC50 berdasarkan presentase hambat terhadap radikal DPPH dari masing-masing konsentrasi larutan sampel dengan rumus :
% hambat = ((abs kontrol – abs sampel) / abs kontrol) x 100%
(Marinova and Batchvarov, 2011). Keterangan :
Abs kontrol : absorbansi larutan kontrol
Abs sampel : absorbansi larutan uji fraksi atau absorbansi rutin
Kemudian nilai IC50 yang didapat akan dilakukan uji normalitas Shapiro-wilk taraf kepercayaan 95% dan uji T tidak berpasangan (terdistribusi normal) menggunakan aplikasi R 3.2.4 untuk menentukan signifikansi perbedaan nilai IC50 fraksi metanol dan fraksi aseton daun adam hawa yang diperoleh.
HASIL DAN PEMBAHASAN
6
hari menggunakan oven dengan bantuan blower untuk mengoptimalkan proses pengeringan.
Setelah kering, daun adam hawa diserbuk dengan blender untuk memperkecil ukuran serbuk kemudian diayak dengan ayakan mesh no.40 untuk menghomogenkan ukuran serbuk. Dalam penelitian Sapri, Fitriani dan Narulita (2014), nomor mesh ayakan yang digunakan mempengaruhi rendemen ekstrak yang diperoleh. Serbuk simplisia yang diperoleh 49,49 g dengan rendemen sebesar 4,797 %b/b. Nilai rendemen serbuk kecil diduga karena kandungan air yang tinggi dalam daun adam hawa.
Maserasi merupakan metode ekstraksi/ penyarian tidak menggunakan pemanasan karena senyawa flavonoid tidak stabil pada suhu tinggi. Pelarut etanol 96% digunakan untuk maserasi karena pelarut ini bersifat semipolar dan senyawa flavonoid larut dalam etanol. Maserasi dibantu dengan shaker untuk meningkatkan kelarutan sehingga mengoptimalkan proses ekstraksi. Remaserasi dilakukan untuk mendapatkan rendemen ekstrak yang optimal. Maserat yang diperoleh dipekatkan dengan menggunakan vacuum rotary evaporator. Keuntungan dari alat ini yaitu dapat mempercepat proses pemekatan
dengan panas yang tidak terlalu tinggi sehingga memperkecil kemungkinan rusaknya senyawa flavonoid. Bobot ekstrak etanol 96% daun adam hawa yang diperoleh 7,7165 g dengan rendemen sebesar 15,6075 %b/b.
Metode yang digunakan untuk memfraksinasi ekstrak adalah partisi padat-cair (dekantasi). Prinsip metode dekantasi adalah pemisahan padatan dan cairan (pelarut) berdasarkan bobot jenis (Saifudin, 2014). Ekstrak kental etanol 96% daun adam hawa difraksinasi berturut-turut menggunakan pelarut berdasarkan tingkat kepolarannya yaitu n-heksan (non polar), aseton (semi polar) dan metanol (polar). N-n-heksan digunakan untuk menghilangkan senyawa-senyawa non polar seperti lemak dan klorofil. Pelarut aseton dan metanol dipilih karena senyawa flavonoid terutama antosianin/antosianidin larut dalam pelarut tersebut. Bobot fraksi metanol ekstrak etanol 96 % daun adam hawa dari dua kali fraksinasi diperoleh 1,0944 g dengan rendemen sebesar 21,8871 %b/b. Bobot fraksi aseton ekstrak etanol 96 % daun adam hawa dari dua kali fraksinasi diperoleh 0,3687 g dengan rendemen sebesar 7,3737 %b/b. Hasil rendemen fraksi aseton kurang dari 10% atau lebih kecil dari rendemen fraksi metanol diduga karena kemampuan aseton melarutkan ekstrak etanol 96% daun adam hawa lebih rendah dari metanol.
7
96% daun adam hawa. Fase diam yang digunakan ialah plat silika gel 60 F254 yang bersifat polar, sedangkan fase gerak yang digunakan n-butanol : asam asetat : air (4:1:5) sebagai fase gerak bersifat sangat polar karena mengandung air. Plat KLT silika gel 60 F254 diaktifasi dengan cara di oven pada suhu 100 ºC selama 1 jam untuk menghilangkan air yang terdapat pada plat KLT. Kepolaran fase diam dan fase gerak hampir sama, tetapi masih lebih polar fase gerak sehingga senyawa flavonoid yang dipisahkan terangkat mengikuti aliran fase gerak, karena senyawa flavonoid bersifat polar.
Fase gerak yang dipakai dalam KLT ialah fase gerak campuan n-butanol : asam asetat : air (BAA) (4:1:5) yang mampu memberikan pemisahan untuk senyawa flavonoid. Karena dari komposisinya, fase gerak tersebut bersifat sangat polar sehingga bisa memisahkan senyawa-senyawa flavonoid yang juga bersifat polar. Pemisahan senyawa ditandai dengan nilai Rf yang berbeda (Gandjar dan Rohman, 2007) dan berikut hasil KLT preparatif yang disajikan pada Tabel I.
Tabel I. Nilai Rf yang dihasilkan pada KLTP
Fraksi Nilai Rf Warna Pita dengan Sinar UV
*Ket : tanda “-“ menunjukkan pita tidak terlihat atau bukan pita
8
Tabel II. Identifikasi Senyawa Flavonoid Isolat Fraksi Metanol (Harbone, 1996)
Pereaksi
Tabel III. Identifikasi Senyawa Flavonoid Isolat Fraksi Aseton (Harbone, 1996)
Pereaksi λ (nm) Mula-Mula
Pergeseran λ
(nm) Keterangan Pita I Pita II Pita I Pita II
Metanol 537 277,5 Tetap Tetap Antosianidin/
antosianin
Metanol + NaOH 2N - 276,5 - -0,5 Nihil
Metanol + AlCl3 5% 536,5 274,5 -0,5 -3,5 Tidak ada o-diOH Metanol + AlCl3 5% + HCl 536,5 - -0,5 - Tidak ada o-diOH
Gambar 1. Struktur Dasar Antosianidin (Miguel, 2011)
9
warna pita berwarna biru (Aziz dan Djamil, 2013) dan tidak memiliki respon terhadap AlCl3 sedangkan fraksi aseton isolat 2 diduga merupakan senyawa peonidin/ pelargonidin karena warna pita berwarna merah lembayung dan tidak ada respon terhadap AlCl3 (Lestario et al. 2009).
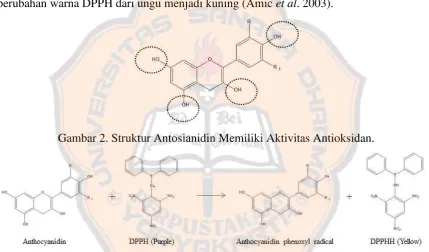
Uji aktivitas antioksidan menggunakan DPPH sebagai radikal bebas reaktif yang akan distabilkan oleh senyawa antioksidan dengan mendonorkan atom hidrogen. Senyawa flavonoid yaitu antosianidin memiliki aktivitas antioksidan karena memiliki gugus fenolik yang ditunjukkan pada Gambar 1. Senyawa antosianidin dapat mendonorkan atom hidrogen ketika bereaksi dengan DPPH sehingga DPPH menjadi stabil ditunjukkan pada Gambar 2. Aktivitas antioksidan senyawa flavonoid (antosianidin) ditandai dengan perubahan warna DPPH dari ungu menjadi kuning (Amic et al. 2003).
Gambar 2. Struktur Antosianidin Memiliki Aktivitas Antioksidan.
Gambar 3. Reaksi antara Senyawa Antosianidin dan DPPH.
Uji aktivitas antioksidan metode DPPH diawali dengan uji pendahuluan
10
ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan DPPH setelah bereaksi dengan rutin. Pengukuran dilakukan sebanyak tiga kali dengan konsentrasi rutin 10, 30 dan 50 µg/mL menggunakan λmaks yaitu 515 nm. Penggunaan tiga konsentrasi tersebut diharapkan dapat menggambarkan waktu operasional dari konsentrasi yang berbeda. Dari data waktu operasional yang diperoleh adalah 25 menit, yang berarti penurunan absorbansi optimal DPPH setelah bereaksi dengan rutin pada waktu 25 menit.
Rutin digunakan sebagai pembanding dalam uji aktivitas antioksidan karena rutin termasuk dalam golongan senyawa flavonoid yang mempunyai gugus fenolik yang telah terbukti memiliki aktivitas antioksidan sehingga dapat digunakan sebagai pembanding (kontrol positif) dalam uji aktivitas antioksidan (Lima et al., 2011). Alasan lain digunakan rutin adalah rutin lebih stabil dari antosianin/antosianidin (Herrero, Hernandez and Frutoz, 2015) dan antosianin/antosinidin memiliki banyak jenis di pasaran. Rutin, fraksi metanol dan fraksi aseton dibuat dengan menyiapkan lima konsentrasi sebagai seri dan dilakukan replikasi sebanyak tiga kali. Uji ini melihat kemampuan rutin, fraksi metanol dan aseton ekstrak etanol 96% daun adam hawa dapat menghambat aktivitas radikal bebas DPPH (aktivitas antioksidan) sehingga diperoleh persen hambat (%IC).
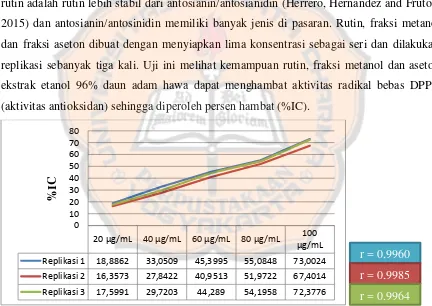
Gambar 4.Grafik Konsentrasi Rutin terhadap Persen Hambat (%IC). 20 µg/mL 40 µg/mL 60 µg/mL 80 µg/mL 100
µg/mL
Replikasi 1 18,8862 33,0509 45,3995 55,0848 73,0024
Replikasi 2 16,3573 27,8422 40,9513 51,9722 67,4014
11
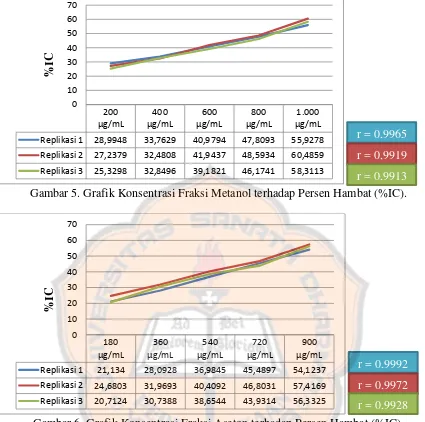
Gambar 5. Grafik Konsentrasi Fraksi Metanol terhadap Persen Hambat (%IC).
Gambar 6. Grafik Konsentrasi Fraksi Aseton terhadap Persen Hambat (%IC).
Pada Gambar grafik 1, 2 dan 3, dapat dilihat bahwa semakin tinggi konsentrasi yang digunakan, aktivitas antioksidan (%IC) yang ditimbulkan juga semakin besar. Hal ini disebabkan karena semakin banyak pula pendonor atom untuk radikal DPPH sehingga radikal DPPH menjadi lebih stabil.
200
Replikasi 1 28,9948 33,7629 40,9794 47,8093 55,9278
Replikasi 2 27,2379 32,4808 41,9437 48,5934 60,4859
Replikasi 3 25,3298 32,8496 39,1821 46,1741 58,3113 0
Replikasi 1 21,134 28,0928 36,9845 45,4897 54,1237
Replikasi 2 24,6803 31,9693 40,4092 46,8031 57,4169
12
Tabel IV. Nilai IC50 antara Rutin, Fraksi Aseton dan Fraksi Metanol
Rutin (Baku)
Dalam penelitian ini, uji aktivitas antioksidan dengan metode DPPH tidak dilakukan validasi metode karena menggunakan metode standar (baku) dari metode blois (Molyneux, 2004) sehingga hanya perlu verifikasi metode. Verifikasi metode dilakukan dengan menetapkan presisi. Presisi dapat dilakukan dengan replikasi yang bertujuan untuk melihat keterulangan hasil sehingga dapat menjamin mutu hasil uji (Gandjar dan Rohman, 2007). Nilai r menunjukan koefisien korelasi regresi linear antara konsentrasi dengan %IC, dapat dilihat bahwa hubungan antara konsentrasi dengan %IC korelasinya berbanding lurus, artinya semakin tinggi konsentrasi fraksi maupun baku maka %IC juga semakin besar. Dilihat Gambar grafik 1, 2 dan 3, nilai r rutin, fraksi aseton dan fraksi metanol mendekati 1, ini menunjukkan memiliki liniearitas yang baik. Persamaan regresi linear yang didapatkan digunakan untuk menghitung IC50 sebagai parameter aktivitas antioksidan.
13
menunjukkan bahwa fraksi metanol dan fraksi aseton memiliki aktivitas antioksidan lemah dibandingkan rutin.
Penelitian Avila et al. (2003) melakukan uji aktivitas antioksidan DPPH pada ekstrak etanol 96% daun adam hawa dengan konsentrasi 1, 10 dan 100 µg/mL dengan masing-masing persen hambat yaitu 67, 68 dan 79%. Persen hambat yang diperoleh dari fraksi metanol dan fraksi aseton lebih kecil dibandingkan ekstrak sehingga dapat dikatakan aktivitas antioksidan fraksi lebih rendah dari ekstrak. Ini mungkin disebabkan karena pada proses fraksinasi, senyawa antosianidin juga terlarut dalam pelarut non-polar (n-heksan) sehingga kandungan antosianidin sebagai senyawa antioksidan dalam fraksi metanol dan fraksi aseton sedikit.
Uji statistik dilakukan dengan aplikasi R 3.2.4 terhadap data yang diperoleh untuk memastikan perbedaan yang bermakna antara nilai IC50 rutin, fraksi metanol dan fraksi aseton ekstrak etanol 96% adam hawa. Pada uji normalitas, data yang didapatkan terbukti terdistribusi normal apabila p-value >0,05. Hasil nilai p yang diperoleh ialah 0,5313 (rutin), 0,1613 (fraksi metanol) dan 0,7642 (fraksi aseton) terlihat p-value > 0,05, ini menunjukkan bahwa rutin dan fraksi metanol, fraksi aseton ekstrak etanol 96% adam hawa memiliki data yang terdistribusi normal dan dapat dilanjutkan untuk uji parametrik.
Uji statistik kedua yaitu uji parametrik (uji t tidak berpasangan). Uji ini bertujuan untuk mengetahui apakah ada perbedaan antara IC50 rutin dan fraksi metanol, IC50 rutin dan fraksi aseton ekstrak etanol 96% adam hawa. Hasil p-value yang diperoleh yaitu 0,0005456 dan 0,0004805 dimana p-value <0,05 dengan taraf kepercayaan 95% sehingga dapat disimpulkan bahwa terdapat perbedaan yang signifikan antara nilai IC50 rutin dan fraksi metanol fraksi aseton ekstrak etanol 96% serta memiliki aktivitas antioksidan yang lebih kecil daripada rutin (baku) dengan perbedaan yang bermakna.
KESIMPULAN DAN SARAN
Fraksi metanol diduga mengandung senyawa antosianidin yaitu malvidin dan memiliki aktivitas antioksidan dengan nilai IC50 yaitu 827,805 ± 32,710 µg/mL sedangkan fraksi aseton diduga mengandung senyawa antosianidin yaitu pelargonidin/peonidin dan memiliki aktivitas antioksidan dengan nilai IC50 yaitu 790,159 ± 29,623 µg/mL.
14
DAFTAR PUSTAKA
Amic, D., Amic, D.D., Beslo D., Trinajstic, N., 2003. Structure-Radical Scavenging Activity Relationships of Flavonoids. Croatica Chemica Acta, 76 (1), 55-61.
Avilaa, M., Gonzalez, A., Arriaga, M., Garzaa, M., Carmen, M., 2003. Antigenotoxic, Antimutagenic and ROS Scavenging Activities Of A Rhoeo discolor Ethanolic Crude Extract. Toxicology in Vitro, 17, 77–83.
Aziz, Z., Djamil, R., 2013. Isolasi Dan Identifikasi Senyawa Flavonoid Dari Fase N-Butanol Daun Jeruk Purut (Citrus hystrix. DC). Seminar POKJANAS TOI ke-XLIV, Palembang.
Fidrianny, I., Darmawanti, A., Sukrasno, 2014. Antioxidant Capacities From Different Polarities Extracts of Cucurbitaceae Leaves Using Frap, DPPH Assays And Correlation With Phenolic, Flavonoid, Carotenoid Content. International Journal of Pharmacy nad Pharmaceutical Sciences, (6), 858-862.
Gandjar, I., G., Rohman, A., 2007. Kimia Farmasi Analisis. Pustaka Pelajar, Yogyakarta, 252-256, 324, 354, 359, 480.
Global Biodiversity Information Facility, 2013. Rhoeo discolor (L'Hér.) Hance. http://www.gbif.org/species/101345884, diakses pada tanggal 22 April 2016.
Harborne, J., 1996. Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan. Cetakan Ketiga, Penerjemah: Padmawinata, K. dan I. Soediro., Penerbit ITB, Bandung, 71-80.
Herrero, J.A., Hernández, Frutos, M.J., 2015. Influence Of Rutin and Ascorbic Acid in Colour, Plum Anthocyanins and Antioxidant Capacity Stability in Model Juices. Food Chemistry, 173, 495-500.
Indrayudha, P., Wiyarti, D., Munawaroh, R., 2013. Aktivitas Antibakteri Fraksi Metanol Ekstrak Etanol Daun Teh Hijau (Camellia Sinensis (L.) O.K) terhadap Streptococcus mutans dan Lactobacillus acidophilus serta Bioautografinya. Naskah Publikasi, Universitas Muhammadiyah Surakarta, Surakarta, 1-15.
Lestario, L.N., Lukito, D., Timotius, H., 2009. Kandungan Antosianin Dan Antosianidin Dari Jantung Pisang Klutuk (Musa brachycarpa Back) Dan Pisang Ambon (Musa acuminata Colla). J.Teknol dan Industri Pangan, 22 (2), 143-148.
Lima, A. D. J. B., Corrêa, A. D., Saczk, A. A., Martins, M. P., Castilho, R. O., 2011. Anthocyanins, Pigment Stability And Antioxidant Activity In Jabuticaba (Myrciaria cauliflora (Mart.) O. Berg). Rev. Bras. Frutic., Jaboticabal - SP, 33 (3), 877-887. Marinova, G. and Batchvarov, V., 2011. Evaluation Of The Methods For Determination Of
The Free Radical Scavenging Activity By DPPH. Bulgarian Journal of Agricultural Science, 17 (1), 11–24.
Miguel, M. G., 2011. Anthocyanins: Antioxidant and/or Anti-Inflammatory Activities. Journal of Applied Pharmaceutical Science, 01(06), 7-15.
Molyneux, P., 2004. The Use of The Stable Free Radical DPPH for Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol., 26 (2), 211-219.
Musarofah, 2015. Tumbuhan Antioksidan. Penerbit PT Remaja Rosdakarya, Bandung, 1 -21.
Saifudin, A., 2014. Senyawa Alam Metabolit Sekunder: Teori, Konsep, dan Teknik Pemurnian. Edisi 1, Deepublish, Yogyakarta, 35,49-50.
15
Sitorus, R. M. H., Wullur, A. C., Paulina, V.Y., Yam L., 2012. Isolasi Dan Identifikasi Senyawa Flavanoid Pada Daun Adam Hawa (Rhoe discolor). Pharmacon, 1(1), 53-57.
Steenis, V., Bloembergen, Eyma, P.J., 1992. FLORA Untuk Sekolah di Indonesia. Percetakan Penebar Swadaya, Jakarta, 43-51,136-138.
16
Lampiran 1. Tanaman Adam Hawa
Gambar Tanaman Adam Hawa untuk Deteminasi Tanaman
17
18
Lampiran 3. Sampel Daun Adam Hawa
Data Penimbangan
Serbuk Simplisia Daun Adam Hawa
Berat Wadah (g) Berat Wadah +
%rendemen = bobot serbuk daun adam ha a
bobot sampel daun adam ha a 00
%rendemen = 49,49 g
03 ,75 g x 100 % = 4,797 %b/b Lampiran 4. Maserasi dan Fraksinasi
Sampel : Serbuk digunakan dalam maserasi
Berat Wadah (g) Berat Wadah + Sampel : Ekstrak Etanol 96%
Bobot Ekstrak (g)
Wadah 65,1005
Wadah + isi 72,8170
Isi 7,7165
Rendemen Ekstrak
%rendemen = bobot ekstrak etanol 96 daun adam ha a
19 %rendemen = 7,7 65 g
49,44 g x 100 % = 15,6075 %b/b
Fraksinasi
Penimbangan ekstrak untuk fraksinasi
Wadah I
%rendemen = bobot fraksi ekstrak etanol 96 daun adam ha a
20
Lampiran 5. Isolasi dan Identifikasi Senyawa Flavonoid
Penimbangan Fraksi Metanol (100 mg)
Wadah (g) Wadah + Isi (g) Isi (g)
46,6766 46,7769 0,1003
Penimbangan Fraksi Aseton (100 mg)
Wadah (g) Wadah + Isi (g) Isi (g)
62,1265 65,2272 0,1007
Gambar Hasil elusi KLTP Fraksi Aseton Ekstrak Etanol 96% Daun Tanaman Adam Hawa pada UV 254 nm
21
Gambar Hasil elusi KLTP Fraksi Metanol Ekstrak Etanol 96% Daun Tanaman Adam Hawa pada UV 254 nm
Gambar Hasil elusi KLTP Fraksi Metanol Ekstrak Etanol 96% Daun Tanaman Adam Hawa pada UV 366 nm
22
Gambar Spektra Fraksi Metanol Isolat 1 dalam Metanol + NaOH 2N
Gambar Spektra Fraksi Metanol Isolat 1 dalam Metanol + AlCL3 5% + HCL
23
Gambar Spektra Fraksi Aseton Isolat 2 dalam Metanol + NaOH 2N
Gambar Spektra Fraksi Aseton Isolat 2 dalam Metanol + AlCL3 5% + HCL
Lampiran 6. Uji Aktivitas Antioksidan (DPPH)
Penimbangan DPPH (10 mg)
Replikasi Wadah (g) Wadah + Isi (g) Isi (g)
1 50,3486 50,3586 0,0100
2 50,0332 50,0434 0,0100
3 62,5513 62,5612 0,0099
4 62,5484 62,5584 0,0100
Pengenceran
- Replikasi 1
a. Konsentrasi Stok DPPH (100 µg/mL) 10 mg/ 100 mL = 0,1 mg/ mL = 100 µg/mL
b. Konsentrasi Seri DPPH (40 µg/mL) M1 x V1 = M2 x V2
24
- Replikasi 2
a. Konsentrasi Stok DPPH (100 µg/mL) 10 mg/ 100 mL = 0,1 mg/ mL = 100 µg/mL
b. Konsentrasi Seri DPPH (40 µg/mL) M1 x V1 = M2 x V2
100 µg/mL x V1 = 40 µg/mL x 100 mL V1 = 40 mL
-Replikasi 3
a. Konsentrasi Stok DPPH (99,0 µg/mL) 9,90 mg/ 100 mL = 0,0990 mg/ mL = 99,0 µg/mL
b. Konsentrasi Seri DPPH (40 µg/mL) M1 x V1 = M2 x V2
99 µg/mL x V1 = 40 µg/mL x 100 mL V1 = 40,40 mL
- Replikasi 4
a. Konsentrasi Stok DPPH (100 µg/mL) 10 mg/ 100 mL = 0,1 mg/ mL = 100 µg/mL
b. Konsentrasi Seri DPPH (40 µg/mL) M1 x V1 = M2 x V2
100 µg/mL x V1 = 40 µg/mL x 100 mL V1 = 40 mL
Penentuan Panjang Gelombang
Panjang gelombang maksimum yang didapat dengan konsentrasi DPPH 40 µg/mL adalah 515 nm
25
Konsentrasi Stok Rutin (1000 µg/mL) 10 mg/ 10 mL = 1 mg/ mL = 1000 µg/mL
b.Konsentrasi Seri Rutin - Konsentrasi Seri (10 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 10 µg/mL x 10 mL V1 = 0,1 mL
- Konsentrasi Seri (30 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 30 µg/mL x 10 mL V1 = 0,3 mL
- Konsentrasi Seri (50 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 50 µg/mL x 10 mL V1 = 0,5 mL
Penimbangan Rutin (10 mg)
Replikasi Wadah (g) Wadah + Isi (g) Isi (g)
a. Konsentrasi Stok Rutin (1000 µg/mL) 10 mg/ 10 mL = 1 mg/ mL = 1000 µg/mL
26 M1 x V1 = M2 x V2
1000 µg/mL x V1 = 20 µg/mL x 10 mL V1 = 0,2 mL
- Konsentrasi Seri (40 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 40 µg/mL x 10 mL V1 = 0,4 mL
- Konsentrasi Seri (60 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 60 µg/mL x 10 mL
V1 = 0,6 mL
- Konsentrasi Seri (80 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 80 µg/mL x 10 mL V1 = 0,8 mL
Konsentrasi Seri (100 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 100 µg/mL x 10 mL V1 = 1,0 mL
- Replikasi 2
a. Konsentrasi Stok Rutin (1000 µg/mL) 10 mg/ 10 mL = 1 mg/ mL = 1000 µg/mL
b.Konsentrasi Seri Rutin - Konsentrasi Seri (20 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 20 µg/mL x 10 mL V1 = 0,2 mL
- Konsentrasi Seri (40 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 40 µg/mL x 10 mL V1 = 0,4 mL
- Konsentrasi Seri (60 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 60 µg/mL x 10 mL V1 = 0,6 mL
- Konsentrasi Seri (80 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 80 µg/mL x 10 mL V1 = 0,8 mL
Konsentrasi Seri (100 µg/mL) M1 x V1 = M2 x V2
1000 µg/mL x V1 = 100 µg/mL x 10 mL V1 = 1,0 mL
- Replikasi 3
a. Konsentrasi Stok Rutin (1010 µg/mL) 10 mg/ 10 mL = 1 mg/ mL = 1010 µg/mL
27 1010 µg/mL x V1 = 20 µg/mL x 10 mL
V1 = 0,199 mL
- Konsentrasi Seri (40 µg/mL) M1 x V1 = M2 x V2
1010 µg/mL x V1 = 40 µg/mL x 10 mL V1 = 0,399 mL
- Konsentrasi Seri (60 µg/mL) M1 x V1 = M2 x V2
1010 µg/mL x V1 = 60 µg/mL x 10 mL
V1 = 0,599 mL
- Konsentrasi Seri (80 µg/mL) M1 x V1 = M2 x V2
1010 µg/mL x V1 = 80 µg/mL x 10 mL V1 = 0,799 mL
Konsentrasi Seri (100 µg/mL) M1 x V1 = M2 x V2
Grafik Replikasi 1 Konsentrasi Rutin Vs Absorbansi
28
Grafik Replikasi 1 Konsentrasi Rutin Vs %IC
Y-Values
Grafik Replikasi 2 Konsentrasi Rutin Vs Absorbansi
Y-Values
Linear (Y-Values) 80 55,0848
29
Grafik Replikasi 2 Konsentrasi Rutin Vs %IC
30
Grafik Replikasi 3 Konsentrasi Rutin Vs Absorbansi
Y-Values
Grafik Replikasi 3 Konsentrasi Rutin Vs %IC
31
Replikasi Nilai IC50 (µg/mL)
Uji Aktivitas Antioksidan Fraksi Peninbangan Fraksi
PenimbanganFraksi Metanol Replikasi (100 mg)
Replikasi Wadah (g) Wadah + Isi (g) Isi (g)
1 61,1018 61,2018 0,1000
2 63,1681 63,2681 0,1000
3 60,6083 60,7083 0,1000
PenimbanganFraksi Aseton Replikasi (60 mg)
32
Pengenceran Fraksi Metanol
*Untuk Replikasi 1,2 dan 3
a. Konsentrasi Stok Fraksi Metanol (10.000 µg/mL)
100 mg/ 10 mL = 10 mg/ mL = 10.000 µg/mL
b.Konsentrasi Fraksi Metanol - Konsentrasi Seri (200 µg/mL) M1 x V1 = M2 x V2
10.000 µg/mL x V1 = 200 µg/mL x 10 mL
V1 = 0,2 mL
- Konsentrasi Seri (400 µg/mL) M1 x V1 = M2 x V2
10.000 µg/mL x V1 = 400 µg/mL x 10 mL
V1 = 0,4 mL
- Konsentrasi Seri (600 µg/mL)
M1 x V1 = M2 x V2
10.000 µg/mL x V1 = 600 µg/mL x 10 mL
V1 = 0,6 mL
- Konsentrasi Seri (800 µg/mL) M1 x V1 = M2 x V2
10.000 µg/mL x V1 = 800 µg/mL x 10 mL
V1 = 0,8 mL
Konsentrasi Seri (1.000 µg/mL) M1 x V1 = M2 x V2
10.000 µg/mL x V1 = 1.000 µg/mL x 10 mL
33
Uji Aktivitas Antioksidan Fraksi Metanol
Diketahui :
Absorbansi %IC Persamaan regresi
Pengenceran Fraksi Aseton
*Untuk Replikasi 1,2 dan 3
a. Konsentrasi Fraksi Aseton(6.000 µg/mL)
60 mg/ 10 mL = 6,0 mg/ mL = 6.000 µg/mL
b.Konsentrasi Fraksi Aseton - Konsentrasi Seri (180 µg/mL)
M1 x V1 = M2 x V2
6.000 µg/mL x V1 = 180 µg/mL x 10 mL V1 = 0,3 mL
34 6.000 µg/mL x V1 = 360 µg/mL x 10 mL V1 = 0,6 mL
- Konsentrasi Seri (540 µg/mL) M1 x V1 = M2 x V2
6.000 µg/mL x V1 = 540 µg/mL x 10 mL V1 = 0,9 mL
- Konsentrasi Seri (720 µg/mL)
M1 x V1 = M2 x V2
6.000 µg/mL x V1 = 480 µg/mL x 10 mL V1 = 1,2 mL
Konsentrasi Seri (900 µg/mL) M1 x V1 = M2 x V2
6.000 µg/mL x V1 = 900 µg/mL x 10 mL V1 = 1,5 mL
Uji Aktivitas Antioksidan Fraksi Aseton
Diketahui :
35
Lampiran 7. Hasil Uji Statistik
38
BIOGRAFI PENULIS
Penulis skripsi yang berjudul “Isolasi, Identifikasi dan Uji Aktivitas Antioksidan Senyawa Flavonoid Fraksi Metanol Dan Fraksi Aseton Daun Tanaman Adam Hawa (Rhoeo discolor (L'Hér.) Hance) dengan Metode 2,2-diphenyl-1-picrylhidrazyl