ANALISIS CAMPURAN SIPROHEPTADIN HCl DAN KETOTIFEN FUMARAT DENGAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET (UV) APLIKASI DERIVATIF
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Progam Studi Ilmu Farmasi
KATA PENGANTAR
Oleh :
Maria Kartika Rachmawatie
NIM: 048114046
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2008
ii
ANALISIS CAMPURAN SIPROHEPTADIN HCl DAN KETOTIFEN FUMARAT DENGAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET (UV) APLIKASI DERIVATIF
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Progam Studi Ilmu Farmasi
KATA PENGANTAR
Oleh :
Maria Kartika Rachmawatie
NIM: 048114046
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2008
iii
Skripsi Berjudul
ANALISIS CAMPURAN SIPROHEPTADIN HCl DAN KETOTIFEN FUMARAT DENGAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET (UV) APLIKASI DERIVATIF
Yang disusun oleh:
Maria Kartika Rachmawatie
NIM: 048114046
telah disetujui oleh:
Pembimbing I
Christine Patramurti, M.Si., Apt.
Tanggal 27 Mei 2008
iv
Pengesahan Skripsi Berjudul
ANALISIS CAMPURAN SIPROHEPTADIN HCl DAN KETOTIFEN FUMARAT DENGAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET (UV) APLIKASI DERIVATIF
Oleh:
Maria Kartika Rachmawatie NIM: 048114046
v
BERDOA DAN BEKERJA
Kita tidak perlu khawatir akan masa depan...
Karena Tuhan akan memenuhi kebutuhan kita...
Bila kita bekerja keras tiap hari.
”
No
GAINS
without
PAINS
”
NO ONE IS INDISPENSABLE. NO ONE IS TOTALLY INDEPENDENT
Karya ini saya persembahkan untuk:
Orang tua, kakak, adek, keluarga besar, masku dan sahabat
Seluruh teman-teman angkatan 2004 dan satu kelompok penelitian khususnya,
Dan untuk almamater yang Tika cintai dan hormati
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Maria Kartika Rachmawatie NIM : 048114046
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
ANALISIS CAMPURAN SIPROHEPTADIN HCl DAN KETOTIFEN
FUMARAT DENGAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET (UV) APLIKASI DERIVATIF
Dengan demikian saya memberika kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikan ke internet atau media lain untuk kepentingan akademis tanpa meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal 26 Mei 2008
Yang menyatakan
Maria Kartika Rachmawatie
vii
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Kasih untuk rahmat-Nya
yang sangat besar sehingga penulis dapat menyelesaikan skripsi berjudul
”Analisis Campuran Siproheptadin HCl dan Ketotifen Fumarat dengan Metode Spektrofotometri Ultraviolet (UV) Aplikasi Derivatif”.
Skripsi ini dibuat untuk memenuhi salah satu syarat memperoleh gelar
Sarjana Farmasi (S. Farm.) program studi Farmasi Universitas Sanata Dharma
Yogyakarta.
Selama penyusunan skripsi ini, penulis banyak sekali mendapat banyak
bantuan dan dukungan dari berbagai pihak. Maka dalam kesempatan ini penulis
ingin mengucapkan banyak terima kasih kepada:
1. Ibu Rita Suhadi, M. Si., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Drama.
2. Ibu Christine Patramurti, M. Si., Apt. selaku dosen pembimbing yang
selalu sabar membimbing penelitian dan penyusunan skripsi.
3. Bapak Drs. Sulasmono, Apt. dan Ibu Lucia Wiwid Wijayanti, M. Si.
selaku dosen penguji untuk semua saran dan masukan yang telah
diberikan kepada penulis.
4. Pak Mukmin, Pak Prapto, Mas Sarwanto, Pak Parlan, Mas Kunto, Mas
Narto, Pak Tatmo, dan Mbak Sari untuk semua bantuannya.
viii
5. Mama, Papa, Mbak Mesya, Gilang, dan keluarga besar untuk dukungan
baik moril dan materil. Mas Stev buat pantun n joke-nya yang KATRO
abiezz
6. Yosef Bayu Adi yang selalu sabar ngadepin Tika, thanks buat dukungan
dan perhatiannya.
7. Sahabat-sahabat tersayang: Nono, Chika, Vinna, Yoana Rissa M,
S.Farm, Noer, Rintul, Nopheng, Thomas Arian Adrianto, S.Farm.
Thanks…
8. Sahabat-sahabat terbaik selama perjalanan: Rian “Ndoet” (untuk diskusi
n data), Nopheng, Ci Lyd, A Cin, dan Ismiyati “Reni”, semuanya
Thanks...!!!!
9. Teman-teman kelompok praktikum A dan B juga teman-teman angkatan
2004 (FST dan FKK), salam kompak selalu!!!!!
10.Teman-teman KKN: Dita, Yo2k, Tuti, Mami Sita, Dhiyan, Lupe, Teguh,
Donnie, dan Rian “Ndoet”.
Dan terima kasih pula kepada semua pihak yang telah membantu yang
tidak dapat penulis sebutkan satu persatu.
Penulis menyadari masih banyak kekurangan dalam penyelesaian skripsi
ini. Oleh karena itu, penulis menerima semua kritik dan saran yang membangun
demi kesempurnaan skripsi ini. Semoga skripsi ini bermanfaat bagi pembaca dan
bagi perkembangan ilmu pengetahuan.
Yogyakarta, Maret 2008
Penulis
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis
ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah
disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, Maret 2008
x
INTISARI
Siproheptadin HCl dan ketotifen fumarat merupakan obat antihistamin. Siproheptadin HCl dan ketotifen fumarat memiliki struktur kimia yang mirip dan keduanya larut dalam metanol, sehingga akan sulit dipisahkan secara konvensional, oleh karena itu kadar kedua senyawa dapat ditentukan secara simultan dengan metode spektrofotometri UV aplikasi derivatif. Tujuan dari penelitian untuk mengetahui akurasi, presisi, LOD dan LOQ dari metode yang digunakan.
Penelitian ini bersifat non-eksperimental deskriptif. Campuran siproheptadin HCl dan ketotifen fumarat dibuat dalam 2 seri perbandingan dengan 6 kali pengulangan yaitu 2:1 dan 1:1. Penelitian dilakukan dengan membuat spektra serapan, baik spektra normal maupun spektra derivat pertama. Spektra derivatif pertama merupakan plot dA/dλ lawan λ. Panjang gelombang zero
crossing siproheptadin HCl pada derivat pertama ada pada 287 nm, sedangkan panjang gelombang zero crossing ketotifen fumarat ada pada 297 nm. Persamaan kurva baku dibuat dengan persamaan regresi antara konsentrasi vs amplitudo.
Hasil yang diperoleh menunjukkan bahwa metode spektrofotometri UV dengan aplikasi derivatif terhadap campuran siproheptadin HCl dan ketotifen fumarat memiliki akurasi dan presisi yang baik. LOD dan LOQ untuk siproheptadin HCl sebesar 9,13 ppm dan 23,78 ppm, sedangkan untuk ketotifen fumarat sebesar 9,08 ppm dan 29,86 ppm.
Kata kunci : siproheptadin HCl, ketotifen fumarat, aplikasi derivatif
xi
ABSTRACT
Cyproheptadine HCl and ketotifen fumarate are antihistamine. Cyproheptadine HCl and ketotifen fumarate have similar chemical structure and both soluble in methanol. So, it will be very difficult to separate them conventionally. That’s why the dose from both substances can be conducted simultaneously by using derivative application with ultraviolet spectrophotometry method. This research was aimed to determine the accuracy, precision, LOD and LOQ of the method which is used.
This research was non-experimental descriptive. Cyproheptadine HCl and ketotifen fumarate was made in two comparison of series with six replication, they were 2:1 and 1:1. This research was done by make the absorbance spectra, both normal spectrum or first derivative spectrum. The first derivative spectrum is a plot of dA/dλ vs λ. Cyproheptadine HCl’s zero crossing was at 287 nm at first
derivative spectrum and ketotifen fumarate’s zero crossing was at 297 nm at first derivative. The standart equation curve was made by regression equation between concentration vs amplitude.
The result shows that determination using derivative application of ultraviolet spectrophotometry method towards the mixture of cyproheptadine HCl and ketotifen fumarate has good accuracy and precision. LOD and LOQ of cyproheptadine HCl are 9.13 ppm and 23.78 ppm respectively, while LOD and LOQ of ketotifen fumarate are 9.08 ppm and 29.86 ppm respectively.
Keywords: Cyproheptadine HCl, ketotifen fumarate, derivative application
xii
DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... . ... iv
HALAMAN PERSEMBAHAN ... v
PERNYATAAN PERSETUJUAN PUBLIKASI... vi
KATA PENGANTAR ...vii
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ...xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN...xviii
BAB I. PENDAHULUAN ... 1
A. Latar Belakang... 1
B. Permasalahan ... 3
C. Keaslian penelitian ... 3
D. Manfaat Penelitian ... 3
E. Tujuan Penelitian ... 4
BAB II. TINJAUAN PUSTAKA ... 5
A. Siproheptadin HCl ... 5
xiii
B. Ketotifen fumarat ... 6
C. Spektrofotometri Ultraviolet ... 7
D. Analisis multikomponen secara spektrofotometri UV ... 13
E. Spektrofotometri Derivatif………17
F. Parameter Validitas Metode ... 18
G. Keterangan Empiris ... 21
BAB III. METODOLOGI PENELITIAN ... 23
A. Jenis Rancangan Penelitian ... 23
B. Definisi Operasional ... 23
C. Bahan – bahan Penelitian... 24
D. Alat – alat Penelitian... 24
E. Tata Cara Penelitian... 24
1. Pembuatan larutan stok siproheptadin HCl dan ketotifen fumarat ... 24
2. Pembuatan seri larutan baku siproheptadin HCl dan ketotifen fumarat ... 25
3. Pengamatan spektra masing – masing senyawa ... 25
4. Penentuan zero crossing masing – masing senyawa ... 25
5. Pembuatan persamaan kurva baku... 25
6. Pengamatan amplitudo larutan sampel dan perhitungan kadar campuran siproheptadin HCl dan ketotifen fumarat (2:1) dan (1:1)... 26
F. Analisis Hasil ... 27
xiv
BAB IV. HASIL DAN PEMBAHASAN ... 29
A. Pembuatan Larutan Baku ... 29
B. Pengamatan Spektra masing – masing Senyawa... 30
C. Penentuan Zero Crossing masing – masing Senyawa ... 32
D. Pembuatan Persamaan Kurva Baku... 36
E. Penetapan Kadar Sampel dalam Campuran ... 40
BAB V. KESIMPULAN DAN SARAN …... 47
DAFTAR PUSTAKA ... 48
LAMPIRAN ... 51
BIOGRAFI PENULIS ... 66
xv
DAFTAR TABEL
Tabel I. Pelarut untuk daerah ultraviolet dan daerah tampak ... 11
Tabel II. Parameter validitas metode... 21
Tabel III. Data Kurva Baku Siproheptadin HCl ... 38
Tabel IV. Data Kurva Baku Ketotifen Fumarat... 39
Tabel V. Kadar siproheptadin HCl dan ketotifen fumarat dalam sampel 2:1 ... 43
Tabel VI. Kadar siproheptadin HCl dan ketotifen fumarat dalam sampel 1:1 ... 44
Tabel VII. LOD dan LOQ siproheptadin HCl dan Ketotifen fumarat... 45
xvi
DAFTAR GAMBAR
Gambar 1. Rumus Bangun Siproheptadin HCl ... 5
Gambar 2. Rumus Bangun Ketotifen Fumarat... ……... ...…. ...6
Gambar 3. Diagram tingkat energi elektronik... 8
Gambar 4. Sistem kromofor dari siproheptadin HCl... 10
Gambar 5. Sistem kromofor dan auksokrom dari ketotifen fumarat... 10
Gambar 6. Spektra serapan yang pada panjang gelombang terjadinya serapan maksimum masing-masing komponen tidak saling tumpang tindih... 14
Gambar 7. Spektra serapan tumpang tindih satu daerah... 15
Gambar 8. Spektra serapan tumpang tindih dua daerah ... 16
Gambar 9. Spektrogram derivatif pertama sampai keempat suatu pita gauss ... 18
Gambar 10. Spektra serapan normal dari tiga konsentrasi siproheptadin HCl ... 30
Gambar 11. Spektra serapan normal dari tiga konsentrasi ketotifen fumarat ... 31
Gambar 12. Spektra tumpang tindih dari siproheptadin HCl dan ketotifen fumarat... 32
Gambar 13. Spektra derivat pertama siproheptadin HCl delta panjang gelombang 1 nm dan 2 nm ... 33
xvii
Gambar 14. Spektra derivat pertama ketotifen fumarat delta panjang
gelombang 1 nm dan 2 nm ... 34
Gambar 15. Spektra gabungan derivat pertama siproheptadin HCl dan
ketotifen fumarat dengan delta panjang gelombang 1 nm ... 34
Gambar 16. Spektra gabungan derivat pertama siproheptadin HCl dan
ketotifen fumarat dengan delta panjang gelombang 2 nm ... 35
Gambar 17. Kurva baku siproheptadin HCl... 38
Gambar 18. Kurva baku ketotifen fumarat ... 39
Gambar 19. Spektra normal siproheptadin HCl, ketotifen fumarat dan
sampel 2:1... 41
Gambart 20. Spektra normal siproheptadin HCl, ketotifen fumarat dan
sampel 1:1... 41
Gambar 21. Spektra gabungan derivat pertama siproheptadin HCl,
ketotifen fumarat dan sampel 2:1 ... 42
Gambar 22. Spektra gabungan derivat pertama siproheptadin HCl,
ketotifen fumarat dan sampel 1:1 ... 42
xviii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis ketotifen fumarat ... 49
Lampiran 2. Sertifikat analisis siproheptadin HCl ... 50
Lampiran 3. Tabel penimbangan baku siproheptadin HCl dan contoh
perhitungan seri larutan baku siproheptadin HCl... 51
Lampiran 4. Tabel penimbangan baku siproheptadin HCl dan contoh
perhitungan seri larutan baku ketotifen fumarat ... 53
Lampiran 5. Data persamaan kurva baku Siproheptadin HCl... 55
Lampiran 6. Data persamaan kurva baku ketotifen fumarat ... 56
Lampiran 7. Tabel penimbangan baku siproheptadin HCl dan ketotifen
fumarat (2:1) dan contoh perhitungan konsentrasi sampel... 57
Lampiran 8. Tabel penimbangan baku siproheptadin HCl dan ketotifen
fumarat (1:1) dan contoh perhitungan konsentrasi sampel... 59
Lampiran 9. Contoh perhitungan kadar siproheptadin HCl dan ketotifen
fumarat dalam campuran 2:1... 61
Lampiran 10. Contoh perhitungan kadar siproheptadin HCl dan ketotifen
fumarat dalam campuran 1:1 ... 61
Lampiran 10. Contoh perhitungan kadar ,recovery, koevisien variansi
(KV) siproheptadin HCl dan ketotifen fumarat... 61
Lampiran 11. Hasil perhitungan kadar, recovery, KV dari sampel... 61
Lampiran 12. Penentuan zero crossing replikasi II ... 65
xix
Lampiran 13. Penentuan zero crossing replikasi III... 65
1
BAB I PENDAHULUAN
A. Latar Belakang
Saat ini patient safety merupakan isu kritis yang harus ditangani dengan
tepat karena menyangkut keselamatan pasien. Patient safety salah satunya
berkaitan dengan kesesuaian antara dosis, bentuk sediaan dan umur pasien. Pasien
anak umumnya sulit menerima sediaan dalam bentuk padat, sehingga lebih sering
diberikan dalam bentuk sirup atau pulveres. Sirup merupakan sediaan yang paling
cocok untuk pasien anak karena rasanya yang dapat diterima, tetapi tidak semua
obat dapat diberikan dalam bentuk sirup hal ini terkait dengan masalah stabilitas
dan kelarutannya dalam larutan. Hal ini dapat diatasi dengan pemberian obat
dalam bentuk pulveres yang lebih mudah ditelan daripada tablet.
Kelebihan bentuk sediaan pulveres yaitu dokter dapat
mengkombinasikan beberapa zat aktif menjadi satu untuk mencapai tujuan terapi.
Salah satu contoh bentuk kombinasi obat yang sering diberikan oleh Rumah Sakit
X di Yogyakarta untuk pengobatan asma pada pasien anak yaitu kombinasi antara
siproheptadin HCl dan ketotifen fumarat (2:1) sebagai obat anti-histamin.
Pulveres yang merupakan kombinasi dari siproheptadin HCl dan ketotifen
fumarat (2:1) dibuat dengan cara menggerus tablet kemudian dibagi secara visual
sesuai dengan dosis yang diinginkan dan dikemas. Pembagian obat secara visual
tidak menjamin adanya keseragaman dari sediaan.
2
Obat hasil racikan yang digunakan di Rumah Sakit X di Indonesia
umumnya tidak melalui pemeriksaan secara kualitatif maupun kuantitatif,
sehingga tidak ada jaminan keamanannya. Menurut KEPMENKES NO.
1197/MENKES/SK/X/2004 mengenai STANDAR PELAYANAN FARMASI DI
RUMAH SAKIT (Anonim, 2007) menyatakan bahwa standar pelayanan farmasi
harus sesuai dengan CPOB (Cara Pembuatan Obat yang Baik), sehingga obat jadi
hasil produksi suatu industri obat merupakan produk akhir dan tidak
diperkenankan mengalami formulasi ulang di dalam penggunaannya. Adanya
perubahan bentuk sediaan dari tablet menjadi pulveres di dalam produksinya akan
mempengaruhi stabilitas dari sediaan yang dibuat, baik stabilitas fisika maupun
stabilitas kimia. Stabilitas fisika dapat dilihat baik dari segi warna, bau, rasa, dan
bentuknya. Stabilitas kimia dapat dilihat dari kandungan zat aktif yang dapat
diketahui melalui pemerikasaan kuantitatif.
Metode analisis yang sesuai sangat dibutuhkan di dalam pemeriksaan
kuantitatif. Salah satu metode yang dapat digunakan untuk menganilisis suatu zat
dalam campuran yaitu secara spekrofotometri baik dengan teknik tunggal ataupun
simultan tergantung dari spektra masing-masing komponen. Siproheptadin HCl
dan ketotifen fumarat memiliki struktur kimia yang mirip dan keduanya larut
dalam alkohol sehingga sangat sulit dipisahkan secara konvensional, oleh karena
itu untuk penetapan kadarnya dapat dilakukan secara simultan. Salah satu teknik
penetapan kadar secara simultan dengan spektrofotometri yaitu metode derivatif.
Spektra derivat pertama merupakan plot dA/dλ lawan λ, sedangkan spektra
derivatif ke dua merupakan plot d2A/dλ2 lawan λ. Persamaan kurva baku dibuat
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
3
dengan persamaan regresi antara kadar vs amplitudo. Agar metode ini
memberikan hasil yang dapat dipertanggungjawabkan, perlu dilakukan validasi
metode. Suatu metode dikatakan memiliki validitas baik maka akurasi, presisi,
koefisien korelasi (r) harus memenuhi persyaratan validitas yang didukung oleh
LOD dan LOQ masing-masing senyawa.
1. Permasalahan
Bagaimanakah akurasi, presisi, linearitas, LOD dan LOQ dari metode
spektrofotometri ultraviolet (UV) dengan aplikasi derivatif untuk penetapan kadar
siproheptadin HCl dan ketotifen fumarat?
2.Keaslian Penelitian
Penetapan kadar campuran menggunakan spektrofotometri ultraviolet
(UV) dengan aplikasi derivatif sudah banyak dilakukan, akan tetapi, penetapan
kadar siproheptadin HCl dan ketotifen fumarat menggunakan spektrofotometri
ultraviolet (UV) aplikasi derivatif belum pernah dilakukan.
3. Manfaat Penelitian
a. Manfaat metodologis : Metode ini diharapkan dapat digunakan sebagai metode alternatif di dalam menetapkan kadar senyawa dalam campuran.
b. Manfaat praktis : Dengan adanya penelitian ini, penulis berharap memberikan solusi mengenai metode yang cepat dan praktis yang dapat
digunakan untuk penetapan kadar.
4
B. Tujuan
Untuk mengetahui akurasi, presisi, linearitas, LOD dan LOQ dari metode
spektrofotometri ultraviolet (UV) dengan aplikasi derivatif di dalam menetapkan
kadar siproheptadin HCl dan ketotifen fumarat dalam campuran.
5
BAB II
TINJAUAN PUSTAKA
A. Siproheptadin HCl
Siproheptadin HCl mengandung tidak kurang dari 98,5% dan tidak lebih
dari 100,5% C21H21N.HCl, dihitung terhadap zat yang telah dikeringkan.
Pemerian : serbuk hablur, putih sampai agak kuning; tidak berbau atau praktis
tidak berbau. Siproheptadin HCl sukar larut dalam air, mudah larut dalam
metanol, larut dalam kloroform, agak sukar larut dalam etanol, praktis tidak larut
dalam eter (Anonim, 1995). Siproheptadin HCl dapat ditetapkkan kadarnya
dengan metode spektrofotometri ultraviolet, didasarkan adanya serapan
siproheptadin HCl pada daerah ultraviolet. Hal ini dapat dilihat bahwa dalam
larutan asam, siproheptadin HCl memiliki panjang gelombang serapan maksimum
286 nm (Clarke, 1986).
N CH3 H Cl
C21H21N.HCl.11/2H2O; BM 350,89
Gambar 1. Rumus bangun Siproheptadin HCl (Anonim, 1995)
Siproheptadin HCl memiliki indikasi sebagai hay fever, migren dan
urtikaria. Efek samping dari penggunaan siproheptadin HCl antara lain mual,
6
muntah, anemia hemolitik, trombositopenia, leukopenia, agranulositosis. Dosis
siproheptadin HCl 4 mg 3-4 kali sehari, rentang dosis: 4-20 mg sehari maksimal
32 mg sehari; untuk anak dibawah 2 tahun tidak dianjurkan; anak 2-6 tahun 2 mg
2-3 kali sehari maksimal 12 mg sehari; anak 7-14 tahun 4 mg 2-3 kali sehari
maksimal 16 mg sehari. Dosis yang diberikan unutk migren adalah 4 mg diikuti 4
mg setelah 30 menit jika diperlukan; dosis penunjang 4 mg tiap 4-6 jam (Anonim,
2000).
B. Ketotifen fumarat
Ketotifen fumarat berbentuk serbuk kristal berwarna putih dengan titik
leleh antara 190˚ sampai dengan 196˚. Ketotifen larut dalam air, etanol, praktis
tidak larut dalam kloroform. Ketotifen fumarat dapat ditetapkan kadarnya dengan
metode spektrofotometri ultraviolet, didasarkan adanya serapan ketotifen fumarat
pada daerah ultraviolet. Hal ini dapat dilihat bahwa dalam larutan asam, ketotifen
fumarat memiliki panjang gelombang serapan maksimum 297 nm (Clarke, 1986).
S O
N
CH3
C19H19NOS; BM 309,43
Gambar 2. Rumus bangun Ketotifen Fumarat (Anonim, 1989)
Sebagai antihistamin, ketotifen fumarat dilaporkan tidak memiliki manfaat
klinis pada asma bronkial dan terbukti mengecewakan. Efek samping dari
7
penggunaan ketotifen fumarat antara lain mulut kering, mengantuk, pusing, dan
stimulasi susunan saraf pusat. Ketotifen diberikan dengan dosis 1 mg 2 kali sehari
waktu makan, jika perlu dosis dinaikkan 2 mg 2 kali sehari, sedangkan untuk anak
diatas 2 tahun dosis yang diberikan yaitu 1 mg 2 kali sehari (Anonim, 2000).
C. Spektrofotometri Ultraviolet (UV)
Spektrofotometer UV-Vis adalah anggota teknik analisis spektroskopik
yang memakai sumber radiasi elektromagnetik ultraviolet dekat (190-380 nm) dan
sinar tampak (380-780 nm) dengan memakai instrumen spektrofotometer (Mulja
dan Suharman, 1995). Spektrofotometer menghasilkan sinar dari spektra dengan
panjang gelombang tertentu, dan fotometer adalah alat pengukur intensitas cahaya
yang ditransmisikan yang diabsorpsi (Khopkar, 1990).
Prinsip kerja spektrofotometri berdasarkan atas interaksi yang terjadi
antara radiasi elektromagnetik dengan atom atau molekul (Mulya dan Suharman,
1995). Adanya interaksi tadi akan menyebabkan terjadinya perpindahan energi
dari sinar radiasi ke materi yang disebut absorpsi. Absorpsi oleh atom akan
menyebabkan terjadinya transisi elektronik, yaitu peningkatan energi elektron dari
tingkat dasar (ground state) ke tingkat yang lebih tinggi (excited state). Transisi
ini akan terjadi apabila energi yang diberikan oleh radiasi sama dengan energi
ynag dibutuhkan untuk melakukan transisi tersebut.
Transisi elektronik senyawa organik yang dapat terjadi yaitu transisi dari
orbital σ → σ*, π → π*, n → σ* dan n → π* yang ditunjukkan oleh gambar
berikut:
8
σ* Antibonding
π* Antibonding
E
n nonbonding
π Bonding
σ Bonding
Gambar 3. Diagram tingkat energi elektron molekul (Skoog, 1985) 1. Transisi elektron n →π*
Transisi jenis ini meliputi transisi elektron-elektron heteroatom tak
berikatan ke orbital antibonding π* seperti Nitrogen, Sulfur, Oksigen, dan
Halogen. Serapan ini terjadi pada panjang gelombang yang panjang dan
intensitasnya rendah (Sastrohamidjojo, 2001).
2. Transisi elektron n →σ*
Senyawa-senyawa jenuh yang mengandung heteroatom seperti Nitrogen,
Sulfur, Oksigen, dan Halogen yang memiliki nonbonding elektron (elektron yang
tidak berikatan) di samping elektron σ. Elektron nonbonding ini dapat
dipromosikan, pada panjang gelombang yang sangat pendek ke keadaan
antibonding σ*. Transisi ini terjadi panjang gelombang di bawah 200 nm
(Christian, 2003).
9
3. Transisi elektron π→π*
Transisi ini terjadi pada elektron di orbital π, yaitu pada ikatan rangkap
dua dan rangkap tiga. Eksitasi ini paling mudah terbaca dan bertanggung jawab
terhadap spektra elektronik dalam daerah UV dan tampak (Christian, 2003).
4. Transisi elektron σ→σ*
Transisi ini memberikan energi yang terbesar dan terjadi pada daerah
ultraviolet jauh yang diberikan oleh ikatan tunggal, sebagai contoh pada alkana. .
Tingkat energi yang dibutuhkan untuk eksitasi sangat besar (Mulja dan Suharman,
1995).
Transisi elektronik yang berguna dalam penelitian adalah transisi π → π*
dan n → π* karena memberikan spektra pada 200-700 nm. Kedua transisi ini
membutuhkan adanya kromofor dalam struktur molekulnya, yaitu suatu gugus
fungsional tidak jenuh yang meyediakan orbital π yang dapat meyerap pada
daerah ultraviolet (Skoog, 1985).
Selain kromofor, dikenal juga istilah auksokrom. Auksokrom merupakan
gugus jenuh yang bila terikat pada kromofor mengubah panjang gelombang dan
intensitas serapan maksimum, cirinya adalah heteroatom yang langsung terikat
pada kromofor (Sastrohamidjojo, 2001). Gugus auksokrom paling sedikit
memiliki sepasang elektron bebas yang dapat berinteraksi dengan elektron π,
misalnya -OH, -NH2 (Skoog, 1985).
10
Sistem kromofor siproheptadin HCl adalah sebagai berikut:
Gambar 4. Sistem kromofor dari siproheptadin HCl
Sistem kromofor dan auksokrom ketotifen fumarat adalah sebagai berikut:
Gambar 5. Sistem kromofor dan auksokrom dari ketotifen fumarat
Keterangan = --- dan ---: kromofor
--- : auksokrom
Spektrofotometri UV-Vis dapat melakukan penentuan terhadap sampel
yang berupa larutan, gas atau uap (Mulja dan Suharman, 1995). Pengaruh pelarut
dan substitusi gugus dapat menggeser intensitas dan panjang gelombang.
Pergeseran menuju panjang gelombang yang lebih panjang disebut sebagai
pergeseran batokromik, sedangkan pergeseran menuju panjang gelombang yang
lebih pendek disebut pergeseran hipsokromik. Pergeseran intensitas menuju
intensitas yang lebih besar disebut pergeseran hiperkromik, sedangkan pergeseran
menuju intensitas yang lebih kecil disebut hipokromik (Sastrohamidjojo, 2001).
11
Menurut Mulya dan Suharman, untuk sampel yang berupa larutan perlu
diperhatikan beberapa persyaratan pelarut yang dipakai, antara lain :
1. Pelarut yang dipakai tidak mengandung sistem ikatan rangkap terkonjugasi
pada struktur molekulnya dan tidak berwarna.
2. Tidak terjadi interaksi dengan molekul senyawa yang dianalisis.
3. Kemurniannya harus tinggi atau derajat unutk analisis.
Pelarut yang sering digunakan pada umumnya dalam analisis Spektrofotometri
UV-Vis adalah air, etanol, sikloheksan, dan isopropanol. Namun demikian perlu
diperhatikan serapan pelarut yang dipakai di daerah UV-Vis (penggal UV = UV
cut off) (Mulja dan Suharman, 1995).
Tabel 1. Pelarut untuk daerah ultraviolet dan daerah tampak (Day and Underwood, 1996)
Spektrofotometri dapat digunakan untuk analisis kualitatif dan kuantitatif.
Transisi elektron ditentukan oleh konfigurasi elektron dari molekul yang
bersangkutan, maka transisi ditentukan oleh struktur molekul. Sehingga molekul
yang berbeda struktur akan memiliki level energi yang berbeda dan setiap jenis
molekul menyerap radiasi pada daerah spektra tertentu. Hal inilah yang menjadi
dasar analisis kualitatif dengan metode spektrofotometri. Banyaknya cahaya yang
diserap pada panjang gelombang tertentu sesuai dengan jumlah molekul yang ada. Jenis pelarut UV cut off (nm) Jenis pelarut UV cut off (nm)
12
Hal inilah yang menjadi dasar analisis kuantitatif dengan metode spektrofotometri
(Willard, Merrit, Dean, Settle, 1988).
Analisis dengan spektrofotometri UV-Vis selalu melibatkan pembacaan
serapan radiasi elektromagnetik oleh molekul atau radiasi elektromagnetik yang
diteruskan. Keduanya dikenal sebagai serapan (A) tanpa satuan dan transmitan
dengan satuan persen (%T).
Apabila suatu suatu radiasi elektromagnetik dikenakan kepada suatu
larutan dengan intensitas radiasi yang datang (I0), maka sebagian radiasi tersebut
akan diteruskan (It), diapantulkan (Ir) dan diabsorpsi (Ia), sehingga :
I0 = Ir + Ia + It (1)
Harga Ir (± 4%) dengan demikian dapat diabaikan karena pengerjaan dengan
metode spektrofotometri UV-Vis dipakai larutan pembanding sehingga :
I0 = Ia + It (2)
Bouguer, Lambert dan Beer membuat formula secara matematik hubungan antara
transmitan (T) atau serapan (A) terhadap intensitas radiasi atau konsentrasi zat
yang dianalisis dan panjang sel. Bila konsentrasi (c) dinyatakan dalam mol/liter,
dan panjang sel (b) dinyatakan dalam cm, persamaan menjadi:
bc T
A=log 1 =!. . (3)
Istilah ! didefinisikan sebagai daya serap molar. Bila c dinyatakan dalam
gram/liter, persamaan menjadi:
c b a
A= . . (4)
(Mulja dan Suharman, 1995)
13
Serapan jenis didefinisikan sebagai serapan dari larutan 1% zat terlarut
dalam sel dengan ketebalan 1 cm dan diberi lambang A (1cm, 1%) (Anonim,
1995). Menurut Rohman (2007), hubungan antara ε denganE11%cm yaitu:
"= E11%cmxBM
10 (5)
Harga ε bergantung pada luas penampang senyawa yang terkena radiasi
(a) dan probabilitas terjadinya transisi energi yang diserap (p). Hubungan ε dan
variabel tersebut adalah sebagai berikut :
ε = k.p.a (5)
Keterangan :
ε = daya serap molar
k = suatu tetapan 1020 atau 8,7 !1019 p = probabilitas (0-1)
a = area molekul sasaran, untuk molekul zat organik (a = 10A2)
Transisi elektronik yang diperbolehkan (allowed transition) adalah transisi
elektronik yang memberikan harga ε > 104 atau harga p = 0,1–1. Sedangkan untuk
harga ε < 103 atau harga p < 0,01 merupakan transisi yang terlarang (for bidden
transition). Secara umum dapat dikatakan bahwa harga sangat mempengaruhi
puncak spektra suatu zat. Rincian harga ε terhadap puncak spektra adalah sebagai
berikut : 1-10 : sangat lemah; 10-102 : lemah; 102-103 : sedang; 103-104 : kuat;
104-105 : sangat kuat (Mulja dan Suharman, 1995).
D. Analisis Multikomponen secara Spektrofotometri Ultraviolet (UV)
Analisis kunatitatif multikomponen merupakan pengembangan analisis
komponen tunggalnya. Prinsipnya adalah mencari serapan atau beda serapan
tiap-tiap komponen yang memberikan korelasi yang linier terhadap konsentrasi,
14
sehingga dapat dihitung kadar-kadar masing-masing campuran zat secara serentak
atau salah satu komponen dalam campurannya dengan komponen lainnya (Mulja
dan Suharman, 1995). Pemilihan metode analisis multikomponen didasarkan pada
profil kurva serapan masing-masing komponen. Ada tiga kemungkinan profil
spektra serapan yang diperoleh dari suatu larutan yang mengandung dua
komponen penyerap.
1. Kemungkinan pertama
Spektra tidak saling tumpah tindih atau dimungkinkan untuk menemukan
panjang gelombang saat X menyerap dan Y tidak menyerap (λ1) serta panjang
gelombang saat Y menyerap dan X tidak (λ2). Oleh sebab itu, komponen X dan Y
masing-masing dapat diukur pada panjang gelombang tersebut (Day and
Underwood, 1996). Spektra ini terlihat pada gambar berikut:
X Y
S e r a p a n
λ1 λ2
Panjang gelombang
Gambar 6. Spektra serapan yang pada panjang gelombang terjadinya serapan maksimum masing-masing komponen tidak saling tumpang tindih
(Day and Underwood, 1996)
15
2. Kemungkinan kedua
Spektra yang tumpang tindih satu daerah, seperti pada gambar berikut:
S X Y
e r a p a n
λ1 λ2
Panjang gelombang
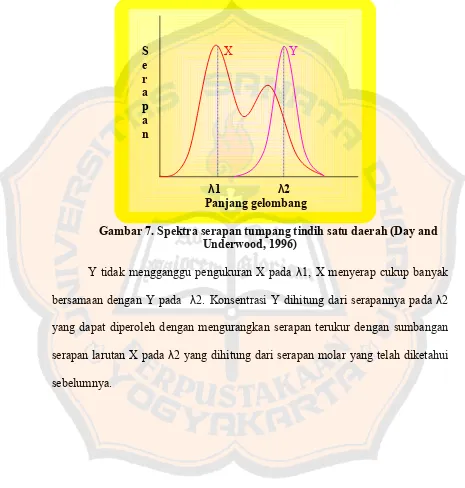
Gambar 7. Spektra serapan tumpang tindih satu daerah (Day and Underwood, 1996)
Y tidak mengganggu pengukuran X pada λ1, X menyerap cukup banyak
bersamaan dengan Y pada λ2. Konsentrasi Y dihitung dari serapannya pada λ2
yang dapat diperoleh dengan mengurangkan serapan terukur dengan sumbangan
serapan larutan X pada λ2 yang dihitung dari serapan molar yang telah diketahui
sebelumnya.
16
3. Kemungkinan ketiga
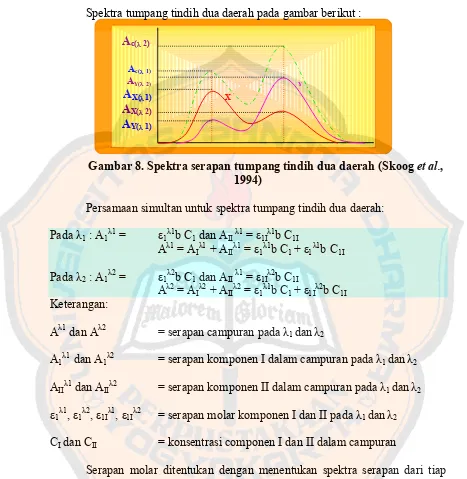
Spektra tumpang tindih dua daerah pada gambar berikut :
Ac(λ 2)
Gambar 8. Spektra serapan tumpang tindih dua daerah (Skoog et al., 1994)
Persamaan simultan untuk spektra tumpang tindih dua daerah:
Pada λ1 : A1λ1 = ε1λ1b C1 dan AIIλ1 = ε1Iλ1b C1I
CI dan CII = konsentrasi componen I dan II dalam campuran
Serapan molar ditentukan dengan menentukan spektra serapan dari tiap
komponen secara terpisah dalam larutan yang telah diketahui konsentrasinya.
Kemudian dua konsentrasi yang tidak diketahui ditetapkan dengan menyelesaikan
persamaan simultan yang diperoleh dari pengukuran serapan pada dua panjang
gelombang yang berbeda (Sastrohamidjojo, 2001).
17
E. Spektrofotometri Derivatif
Spektrofotometri derivatif merupakan metode manipulatif terhadap
spektra pada spektrofotometri ultraviolet dan tampak (Connors, 1982). Pada
spektrofotometri konvensional, spektra ini merupakan plot serapan, A, terhadap
panjang gelombang, λ. Pada metode derivatif, plot A vs λ, ini ditransformasikan
menjadi plot
! d dA
vs λ, untuk derivatif pertama, dan d2A/ dλ2 vs λ, untuk derivatif
kedua. Derivasi dapat dibuat yang lebih tinggi, dengan demikian spektrogram
akan bertambah dengan sejumlah pemecahan puncak-puncak yang lebih terinci,
dan puncak spektra yang melebar, terpecah menjadi dua. Metode ini dapat
digunakan untuk analisis campuran tanpa pemisahan terlebih dahulu (Willard et
al., 1988).
Analisis kuantitatif spektra derivatif dilakukan dengan jalan
menggambarkan selisih serapan (ΔA) dua panjang gelombang (ΔA = Aλ1 – Aλ2)
terhadap rata-rata dua panjang gelombang tersebut yang berderet teratur, yaitu :
!
(Mulja dan Suharman, 1995)
Profil penurunan spektra derivat dari spektra normal sampai derivat ke
empat tampak pada gambar berikut ini:
18
Gambar 9. Bentuk spektrogram derivatif pertama sampai keempat suatu pita Gauss (Rattenbury, 1981)
Berdasarkan gambar 9 dapat dibaca bahwa pada spektra derivat pertama,
garis akan melewati nol pada saat y = 0. Pada panjang gelombang zero crossing
suatu senyawa tidak mempunyai serapan atau =0
! d dA
. Derivatif yang lebih tinggi
dari serapan sering kali dimaksudkan untuk mendapatkan spektra yang lebih
spesifik. Dalam spektra derivatif, kemampuan unutk mendeteksi dan mengukur
gambaran spektra dinaikkan cukup besar. Bentuk spektra yang karakteristik ini
mampu membedakan antara spektra yang sangat mirip dalam sebuah
spektrogram. Lebih jauh spektra ini dapat digunakan unutk analisis kuantitatif,
untuk mengukur konsentrasi dari analit yang mempunyai puncak yang
tersembunyi, misalnya yang bertumpang tindih dengan puncak analit lain dalam
sampel (Willard et al. 1988)
F. Parameter Validitas Metode Analisis
19
Validitas metode analisis merupakan suatu ukuran untuk membuktikan
bahwa metode yang digunakan memberikan hasil seperti yang diharapkan dengan
ukuran akurasi serta presisi yang memadai (Mulja dan Suharman, 1995). Ada
berbagai parameter untuk menilai apakah suatu metode valid atau tidak,
diantaranya:
1. Akurasi atau kecermatan
Akurasi suatu metode adalah keterdekatan nilai pengukuran dengan nilai
sebenarnya dari analit dalam sampel. Indikasi yang paling umum untuk
menyatakan akurasi ysng tinggi adalah perolehan kembali (% recovery). Akurasi
bahan obat dengan kadar kecil yang masih dapat diterima adalah 90-110%,
akurasi untuk kadar yang lebih besar lagi yaitu 95-105%, akurasi untuk bahan
baku yaitu 80-120% (Mulja dan Hanwar, 2003).
2. Presisi atau ketelitian
Presisi suatu metode analisis yaitu sejumlah pancaran hasil yang
diperoleh dari analisis berulangkali pada suatu sampel homogen. Presisi biasanya
dinyatakan dengan Koefisien Variansi (KV). Suatu metode dikatakan memiliki
presisi yang bagus apabila memiliki nilai KV<2%, tetapi kriteria ini fleksibel
tergantung dari kondisi analit yang diperiksa, jumlah sampel dan kondisi
laboratorium. Untuk bioanalisis KV = 15-20% masih diterima (Mulja dan
Hanwar, 2003).
20
3. Linearitas
Linearitas dari suatu metode analisis merupakan kemampuan untuk
mendapatkan hasil uji yang secara langsung proporsional dengan konsentrasi
analit pada kisaran yang diberikan (Rohman, 2007). Data linearitas dapat diterima
jika memenuhi nilai koefisien korelasi (r) > 0,99 (Anonim, 2004).
4. Limit of Detection (LOD) dan Limit of Quantitation (LOQ)
Limit deteksi (Limit of Detection) adalah konsentrasi analit terendah
dalam sampel yang masih dapat dideteksi, meskipun tidak dapat dikuantitasi.
LOD seringkali diekspresikan sebagai suatu konsentrasi pada rasio signal
terhadap derau (signal to noise ratio) yang biasanya 2 atau 3:1 (Rohman, 2007).
Sedangakan limit kuantitasi (Limit of Quantitation) merupakan
konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi
dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan.
Rasio signal to noise LOQ umumnya 10:1 (Rohman, 2007).
5. Range
Range merupakan interval antara kadar terendah sampai dengan kadar
tertinggi dari suatu analit yang masih dapat diukur secara kuantitatif
menggunakan metode tertentu yang masih dapat menghasilkan akurasi serta
presisi yang memadai. Biasanya range memiliki satuan yang sama dengan satuan
yang digunakan pada metode analisis, misalnya persen atau ppm (Rohman, 2007;
Anonim, 2005).
21
Metode analisis dibedakan menjadi empat kategori menurut The United
States Pharmacopea (USP) (2005), yaitu:
1. Kategori I
Mencakup metode-metode analisis kuantitatif, untuk menetapkan
kadar komponen utama bahan obat atau zat aktif dalam sediaan farmasi.
2. Kategori II
Mencakup metode-metode analisis kualitatif dan kuantitatif yang
digunakan untuk menganalisis impurities (cemaran) ataupun degradation
compounds dalam sediaan farmasi.
3. Kategori III
Mencakup metode-metode analisis yang digunakan untuk menentukan
karakteristik penampilan suatu sediaan farmasi.
4. Kategori IV (tes identifikasi)
Tabel II. Parameter validitas metode yang dipersyaratkan untuk setiap kategori (Anonim, 2005)
Kategori 2 Parameter
analisis Kategori 1 Kuantitatif Kualitatif Kategori 3 Kategori 4
Akurasi Ya Ya * * Tidak
Presisi Ya Ya Tidak Ya Tidak
LOD Tidak Tidak Ya * Ya
LOQ Tidak Ya Tidak * Tidak
Linearitas Ya Ya Tidak * Tidak
Range Ya Ya * * Tidak
* = Mungkin tidak diperlukan (tergantung sifat spesifik tes)
G. Keterangan empiris
Siproheptadin HCl dan ketotifen fumarat masih digunakan sebagai obat
anti-histamin, keduanya dapat ditetapkan kadarnya menggunakan
spektrofotometri ultraviolet (UV). Baik siproheptadin HCl maupun ketotifen
22
fumarat larut dalam alkohol, sehingga akan sangat sulit dipisahkan secara
konvensional. Secara teoritis siproheptadin HCl memiliki serapan maksimum
pada panjang gelombang 286 nm, sedangkan ketotifen fumarat pada 297 nm.
Dengan adanya serapan maksimum pada panjang gelombang yang berdekatan
tersebut memungkinkan terjadinya spektra yang tumpang tindih. Sehingga untuk
penetapan kadar kedua senyawa dalam campuran dapat dilakukan secara
spektrofotometri ultraviolet (UV), salah satunya menggunakan aplikasi derivatif.
Validitas suatu metode dapat dilihat dari akurasi, presisi, linearitas, LOD
dan LOQ. Suatu metode dikatakan valid apabila menghasilkan akurasi pada
rentang 90-110% dan presisi kurang dari 2%
23
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan penelitian non-eksperimental deskriptif karena
tidak ada subjek uji yang dimanipulasi atau dikenai perlakuan.
B. Definisi Operasional
1. Spektrofotometri derivatif merupakan metode manipulatif terhadap spektra pada spektrofotometri ultraviolet dan tampak. Pada metode derivatif, plot
absorban versus panjang gelombang ditransformasikan menjadi plot
! d dA
vs λ
untuk derivat pertama, dan d2A/ dλ2 vs λuntuk derivat kedua.
2. Panjang gelombang zero crossing merupakan panjang gelombang yang memberikan amplitudo nol pada spektra derivatif.
3. Amplitudo merupakan laju perubahan serapan terhadap panjang gelombang (dnA/ dλn), diturunkan dari hukum Lambert-Beer, memiliki hubungan yang
linear terhadap konsentrasi.
4. Campuran siproheptadin HCl dan ketotifen fumarat yang digunakan memiliki perbandingan 2:1, seperti komposisi dalam pulveres yang diproduksi oleh
Rumah Sakit X di Yogyakarta. Kadar yang dipakai menggunakan satuan ppm.
5. Pengukuran siproheptadin HCl dilakukan pada zero crossing ketotifen fumarat dan pengukuran ketotifen fumarat dilakukan pada zero crossing siproheptadin
HCl
24
6. Parameter kesahihan metode analisis yang digunakan yaitu akurasi, presisi, LOD dan LOQ.
C. Bahan-bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah siproheptadin HCl
(Pharos), ketotifen fumarat (Dankos), metanol pro analisis (E.Merck).
D. Alat-alat Penelitian
Alat yang digunakan dalam penelitian ini adalah Genesis Spectrofotometer
10UV, kuvet Quartz, neraca analitik merk Scaltec, mikropipet Biohit, dan
seperangkat alat gelas.
E. Tatacara Penelitian 1. Pembuatan larutan stok
a. Pembuatan larutan stok Siproheptadin HCl 1000 ppm
Lebih kurang 10,0 mg baku siproheptadin HCl ditimbang seksama
kemudian dilarutkan dengan metanol pro analysis sampai volume 10,00 ml.
b. Pembuatan larutan stok ketotifen fumarat 1000 ppm
Lebih kurang 10,0 mg baku ketotifen fumarat ditimbang seksama kemudian
dilarutkan dengan metanol pro analysis sampai volume 10,00 ml.
25
2. Pembuatan seri larutan baku
a. Pembuatan seri larutan baku siproheptadin HCl
Larutan stok siproheptadin HCl dipipet 0,200; 0,250; 0,300; 0,350; 0,400;
0,450; 0,500 ml dimasukkan kedalam labu takar 10,00 ml, kemudian diencerkan
dengan metanol pro analysis hingga tanda sehingga didapat larutan siproheptadin
HCl dengan konsentrasi 20,00; 25,00; 30,00; 35,00; 40,00; 45,00; 50,00 ppm.
b. Pembuatan seri larutan baku ketotifen fumarat
Larutan stok ketotifen fumarat dipipet 0,200; 0,250; 0,300; 0,350; 0,400;
0,450; 0,500 ml dimasukkan kedalam labu takar 10,00 ml, kemudian diencerkan
dengan metanol pro analysis hingga tanda sehingga didapat larutan ketotifen
fumarat dengan konsentrasi 20,00; 25,00; 30,00; 35,00; 40,00; 45,00; 50,00 ppm.
3. Pengamatan spektra masing-masing senyawa
Diambil 1 seri konsentrasi larutan terbesar, kemudian dibaca serapannya
pada rentang panjang gelombang 240-380 nm, kemudian dibuat spektra serapan
normal (panjang gelombang vs absorbansi), spektra derivat pertama (
!
d dA
vs
panjang gelombang).
4. Penentuan zero crossing masing-masing senyawa
Dari spektra derivat pertama masing-masing senyawa, ditentukan panjang
gelombang amplitudonya
[
(
)
]
2
memiliki harga nol.
5. Pembuatan persamaan kurva baku
Dibuat kurva baku antara amplitudo terhadap konsentrasi senyawa dari
derivat pertama untuk larutan baku siproheptadin HCl dan ketotifen fumarat.
26
Pengukuran amplitudo siproheptadin HCl dibaca pada zero crossing ketotifen
fumarat, sedangkan amplitudo ketotifen fumarat dibaca pada zero crossing
siproheptadin HCl. Dengan persamaan regresi, akan diperoleh persamaan kurva
baku untuk masing-masing senyawa.
6. Pengamatan amplitudo larutan sampel dan perhitungan kadar campuran siproheptadin HCl dan ketotifen fumarat (2:1) dan (1:1)
a. Pembuatan sampel campuran siproheptadin HCl dan ketotifen fumarat Lebih kurang 20 mg siproheptadin HCl dan 10 mg ketotifen fumarat (2:1)
yang ditimbang seksama dilarutkan dalam metanol sampai 10,00 ml. Sebanyak
0,220 ml larutan tersebut diencerkan dengan metanol sampai 10,00 ml. Setelah itu
larutan sampel dibaca serapannya pada panjang gelombang 240-380 nm. Dari
serapan normal dibuat derivat pertama (
!
d dA
).
Lebih kurang 10 mg siproheptadin HCl dan 10 mg ketotifen fumarat (1:1)
yang ditimbang seksama dilarutkan dalam metanol sampai 10,00 ml. Sebanyak
0,350 ml larutan tersebut diencerkan dengan metanol sampai 10,00 ml. Setelah itu
larutan sampel dibaca serapannya pada panjang gelombang 240-380 nm. Dari
serapan normal dibuat derivat pertama (
!
d dA
).
b. Penentuan kadar masing-masing senyawa campuran
Dari spektra derivat pertama sampel, amplitudo sampel dibaca pada zero
crossing yang telah ditetntukan sebelumnya, dimasukkan ke dalam persamaan
kurva baku masing-masing senyawa. Persamaan kurva baku y = bx + a, dimana y
27
adalah amplitudo, b adalah koefisien regresi, x adalah kadar senyawa (ppm) dan a
adalah konstanta.
F. Analisis Hasil
Validitas dari metode yang digunakan dalam penetapan kadar
siproheptadin HCl dan ketotifen fumarat dalam campuran secara spektrofotometri
ultraviolet dengan aplikasi metode derivatif dapat ditentukan berdasarkan
parameter berikut:
1. Akurasi
Akurasi metode analisis dinyatakan dengan recovery yang dihitung
dengan cara berikut:
recovery= kadar terukur kadar diketahuix
100%
Jika nilai recovery berada pada rentang 90-110%, maka metode ini dinilai
memiliki akurasi yang baik.
2. Presisi
Presisis metode analisis dinyatakan dengan koefisien variasi (KV) yang
dihitung dengan cara berikut:
100% kur
kadar teru rerata
SE =
KV x
Jika nilai koefisien variasi kurang dari sama dengan 2%, maka metode ini dinilai
memiliki presisi yang baik (Mulja dan Suharman, 1995).
28
3. Linearitas
Linearitas dilihat dari harga r (koefisien korelasi) dari pengukuran seri
baku pada panjang gelombang zero crossing masing-masing senyawa.
4. LOD dan LOQ
LOD dihitung dari :
Y-Yb = 3Sb
LOQ dihitung dari :
Y-Yb = 10 Sb
Dimana Y merupakan absorban pada panjang gelombang spektra normal,
Yb merupakan intersep dari pengukuran seri larutan baku pada panjang
gelombang spektra normal dan Sb merupakan Sx/y. Y dari masing-masing
senyawa pada panjang gelombang spektra normal dirata-rata kemudian
dimasukkan kedalam persamaan garis panjang gelombang zero crossing
masing-masing senyawa.
29
BAB IV
HASIL DAN PEMBAHASAN
A. Pembuatan Larutan Baku
Siproheptadin HCl memiliki kelarutan dalam metanol (Anonim, 1995)
sedangkan ketotifen fumarat memiliki kelarutan dalam etanol (Clarke, 1986),
tetapi dalam penelitian pelarut yang digunakan adalah metanol. Hal ini
dikarenakan siproheptadin HCl sukar larut dalam etanol (Anonim, 1995),
sedangkan ketotifen fumarat memiliki kelarutan yang cukup baik dalam metanol.
Metanol yang digunakan sebagai pelarut memiliki kualitas pro analysis,
diperlukan kemurnian cukup tinggi sehingga hasil yang diperoleh diharapkan
cukup akurat.
Larutan baku dari masing-masing senyawa dibuat dalam 7 seri kadar.
Larutan baku siproheptadin HCl dibuat dengan konsentrasi 20,00; 25,00; 30,00;
35,00; 40,00; 45,00 dan 50,00 ppm. Larutan baku ketotifen fumarat dibuat dengan
konsentrasi yang sama dengan ketotifen fumarat yaitu 20,00; 25,00; 30,00; 35,00;
40,00; 45,00 dan 50,00 ppm. Pembuatan seri kadar larutan baku dibuat dalam
rentang yang cukup besar, yaitu 20,00-50,00 ppm baik untuk siproheptadin HCl
maupun ketotifen fumarat, dengan tujuan untuk mendapatkan nilai amplitudo
serapan yang cukup besar, sehingga dapat terlihat jelas kenaikan amplitudo
tersebut. Harga amplitudo (dnA/ dλn) sangat bergantung pada beda serapan (dA)
karena dλ bernilai tetap. Sehingga untuk mendapatkan nilai beda serapan yang
cukup signifikan maka konsentrasi larutan diperbesar.
30
B. Pengamatan Spektra masing-masing Senyawa
Menurut Day dan Underwood (1996) metanol memiliki UV cut off pada
panjang gelombang 210 nm sehingga metanol memiliki kemampuan untuk
meneruskan sinar pada panjang gelombang lebih panjang dari 210 nm, oleh
karena itu penentuan spektra masing-masing senyawa dilakukan pada panjang
gelombang 220 – 380 nm agar pada saat pengukuran serapan tidak dipengaruhi
oleh metanol.
Penentuan spektra normal untuk masing-masing senyawa dilakukan pada
penelitian ini untuk melihat apakah terjadi spektra yang tumpang tindih antara
siproheptadin HCl dengan ketotifen fumarat sehingga dapat dikuantifikasi
menggunakan derivatif, dengan menghubungkan serapan sebagai fungsi panjang
gelombang akan diperoleh spektra serapan normal dari masing-masing senyawa.
Penentuan spektra normal dilakukan menggunakan tiga seri konsentrasi yang
berbeda untuk memastikan reprodusibilitas dari data yang dihasilkan.
Gambar 10. Spektra serapan normal tiga konsentrasi siproheptadin HCl
31
Berdasarkan spektra serapan normal siproheptadin HCl pada gambar 10
dapat dilihat bahwa bentuk spektranya stabil walaupun siproheptadin HCl yang
digunakan hanya memiliki kualitas working standart. Puncak serapan maksimum
siproheptadin HCl ada pada panjang gelombang 286 nm. Menurut Clarke (1986),
serapan maksimum siproheptadin HCl ada pada panjang gelombang 286 nm. Hal
ini berarti panjang gelombang yang didapatkan dari penelitian sesuai dengan teori.
Gambar 11. Spektra serapan normal tiga konsentrasi ketotifen fumarat
Berdasarkan spektra serapan normal ketotifen fumarat pada gambar 11
dapat dilihat bahwa bentuk spektranya stabil walaupun ketotifen fumarat yang
digunakan hanya memiliki kualitas working standart. Puncak serapan maksimum
ketotifen fumarat ada pada panjang gelombang 298 nm. Menurut Clarke (1986),
serapan maksimum ketotifen fumarat ada pada panjang gelombang 297 nm,
meskipun panjang gelombang maksimum lebih panjang 1 nm dari teoritis tetapi
masih memenuhi persyaratan Farmakope Indonesia IV (1995) bahwa panjang
gelombang serapan maksimum yang boleh digunakan adalah ± 2 nm.
Penggabungan antara spektra normal siproheptadin HCl dengan ketotifen
fumarat akan terlihat seperti gambar berikut ini:
32
Gambar 12. Spektra tumpang tindih antara siproheptadin HCl dan ketotifen fumarat. (a) spektra siproheptadin HCl (λmax 286 nm); (b) spektra
ketotifen fumarat (λmax 298 nm)
Berdasarkan spektra gabungan di atas dapat dilihat tumpang tindih spektra
siproheptadin HCl dan ketotifen fumarat terjadi pada panjang gelombang 220-380
nm.
C. Penentuan Zero Crossing masing-masing Senyawa
Spektrofotometri derivatif merupakan metode manipulatif terhadap
spektra pada spektrofotometri ultraviolet dan tampak (Connors, 1982). Pada
spektrofotometri konvensional, spektra merupakan plot antara serapan, A, dengan
panjang gelombang, λ. Pada spektrofotometri derivatif, plot A vs λ
ditransformasikan menjadi plot
!
d dA
vs λ, untuk derivatif pertama, dan d2A/dλ2 vs
λ, untuk derivatif kedua. Pembacaan serapan suatu senyawa dilakukan pada
panjang gelombang zero crossing yang sudah ditetapkan sebelumnya. Panjang
33
gelombang zero crossing suatu senyawa merupakan panjang gelombang saat
senyawa tersebut tidak memberikan sinyal atau amplitudonya bernilai nol tetapi
senyawa lain memberikan sinyal.
Berdasarkan spektra normal, dibuat spektra derivat pertama, yaitu dengan
memplotkan amplitudo dA/dλ vs λ. Penentuan amplitudo dA/dλ dilakukan
dengan cara selisih serapan (ΔA = Aλ1 – Aλ2) yang berderet teratur dibagi dengan
delta panjang gelombang. Penggunaan delta panjang gelombang yang optimum
akan meminimalkan pengaruh derau atau noise sehingga pengaruhnya tidak
terlalu besar terhadap bentuk spektra dan juga dapat menunjukkan kejelasan dari
bentuk spektra suatu senyawa.
Spektra derivat pertama dari siproheptadin HCl dengan menggunakan
delta panjang gelombang 1 nm dan 2 nm tampak pada gambar berikut ini:
-0.14
220 225 230 235 240 245 250 255 260 265 270 275 280 285 290 295 300 305 310 315 320 325
Panjang gelombang (nm)
Delta panjang gelom bang 2 nm Delta panjang gelom bang 1 nm
Gambar 13. Spektra derivat pertama siproheptadin HCl delta panjang gelombang 1 nm dan 2 nm
Berdasarkan gambar 13, pengukuran siproheptadin HCl dengan
menggunakan delta panjang gelombang 1 nm masih banyak terdapat peak jika
dibandingkan spektra derivat dengan delta panjang gelombang 2 nm yang lebih
halus.
34
Spektra derivat pertama dari ketotifen fumarat dengan delta panjang
gelombang 1 nm dan 2 nm tampak pada gambar berikut ini:
-0.14
220 225 230 235 240 245 250 255 260 265 270 275 280 285 290 295 300 305 310 315 320 325
Panjang gelombang (nm)
Delta panjang gelom bang 2 nm Delta panjang gelom bang 1 nm
Gambar 14.Spektra derivat pertama ketotifen fumarat delta panjang gelombang 1 nm dan 2nm
Berdasarkan gambar 14, pengukuran ketotifen fumarat dengan
menggunakan delta panjang gelombang 1 nm masih banyak terdapat peak jika
dibandingkan spektra derivat dengan delta panjang gelombang 2 nm yang lebih
halus.
Spektra gabungan akan diperoleh jika kedua spektra derivat pertama
masing-masing senyawa dengan delta panjang gelombang 1 nm digabungkan
menjadi satu seperti gambar berikut ini:
-0.14
220 225 230 235 240 245 250 255 260 265 270 275 280 285 290 295 300 305 310 315 320 325
Panjang gelombang (nm)
Gambar 15. Spektra gabungan derivat pertama siproheptadin HCl dan
35
ketotifen fumarat dengan delta panjang gelombang 1 nm
Pembacaan spektra dengan menggunakan delta panjang gelombang 1 nm
belum menghasilkan pemisahan spektra yang jelas seperti terlihat pada gambar
15, hal ini dapat mengakibatkan terjadinya kesalahan dalam menentukan panjang
gelombang zero crossing yang akan digunakan untuk mengukur senyawa.
Spektra gabungan akan diperoleh jika kedua spektra derivat pertama
masing-masing senyawa dengan delta panjang gelombang 2 nm digabungkan
menjadi satu seperti yang terlihat pada gambar berikut ini:
-0.14
220 225 230 235 240 245 250 255 260 265 270 275 280 285 290 295 300 305 310 315 320 325
Panjang gelombang (nm)
Siproheptadin HCl Ketotifen fum arat
Gambar 16. Spektra gabungan derivat pertama siproheptadin HCl dan ketotifen fumarat dengan delta panjang gelombang 2 nm
Berdasarkan gambar 16, jika menggunakan delta panjang gelombang 2 nm
untuk pembacaan serapan lebih menghasilkan pemisahan spektra yang jelas,
sehingga delta panjang gelombang 2 nm merupakan delta panjang gelombang
yang optimum untuk pengukuran. Selain itu terdapat titik potong terhadap
absisnya yang disebut dengan zero crossing. Pada panjang gelombang zero
crossing tersebut spektra derivatnya menunjukkan amplitudo bernilai nol. Apabila
kedua spektra digabungkan, dapat dilihat bahwa pada zero crossing suatu
36
senyawa, senyawa tersebut tidak memberikan sinyal sedangakan senyawa yang
lain memberikan sinyal.
Spektra derivat pertama siproheptadin HCl dan ketotifen fumarat sudah
menunjukkan pemisahan yang jelas seperti tampak pada gambar 16. Maka untuk
menentukan zero crossing siproheptadin HCl dan ketotifen fumarat dapat
langsung menggunakan spektra derivat pertama selain itu pita serapan untuk
masing-masing senyawa tidak memiliki panjang gelombang yang hampir sama.
Zero crossing siproheptadin HCl ada pada 265 nm dan 287 nm.
Sedangkan zero crossing ketotifen fumarat ada pada 257 nm dan 297 nm. Panjang
gelombang yang digunakan dalam penelitian ini yaitu 287 nm dan 297 nm. Pada
panjang gelombang 287 nm ketotifen fumarat memberikan sinyal sedangkan
siproheptadin HCl tidak memberikan sinyal, karena amplitudonya bernilai nol
maka pengukuran ketotifen fumarat pada panjang gelombang zero crossing
siproheptadin HCl sehingga tidak akan terganggu siproheptadin HCl dan begitu
juga sebaliknya. Siproheptadin HCl diukur pada panjang gelombang zero crossing
ketotifen fumarat yaitu pada 297 nm.
D. Pembuatan Persamaan Kurva Baku
Berdasarkan panjang gelombang zero crossing yang telah ditetapkan, seri
kadar larutan baku siproheptadin HCl dan ketotifen fumarat yang telah dibuat
diukur amplitudo serapan derivat pertamanya pada panjang gelombang tersebut.
Pengukuran seri larutan baku dilakukan sebanyak tiga kali, tetapi hanya satu
persamaan kurva baku yang akan digunakan untuk penetapan kadar siproheptadin
37
HCl dan ketotifen fumarat. Konsentrasi larutan dan amplitudo masing-masing
senyawa dimasukkan ke dalam persamaan regresi linier sehingga diperoleh
persamaan kurva baku, yaitu sebagai berikut ini:
Y = b X + a
Di mana y = amplitudo (dA/dλ), b = koefisien regresi,
x = konsentrasi, dan a = konstanta.
Persamaan tersebut analog dengan hukum Lambert-Beer, di mana semakin
besar konsentrasi maka semakin besar pula harga amplitudo, sehingga ada
hubungan yang linier antara konsentrasi dengan amplitudo (dA/dλ). Parameter
linearitas dilihat dari harga koefisien korelasi (r). Persamaan kurva baku dikatakan
memiliki linearitas yang baik bila harga koefisien korelasinya melebihi r tabel
pada derajat bebas dan tingkat signifikansi tertentu. Dari setiap pengulangan yang
dilakukan, diperoleh harga r yang melebihi harga r tabel yaitu 0,874 dengan df 5
dan tingkat signifikansi 99%.
Selain berdasarkan r tabel, pemilihan persamaan kurva baku juga
didasarkan pada harga r yang mendekati 1. Harga koefisien korelasi yang
mendekati satu menunjukkan hubungan yang linier antara konsentrasi dengan
amplitudo, sehingga persamaan Lambert-Beer dapat terpenuhi. Berikut ini
merupakan hasil pengukuran amplitudo dan perhitungan koefisien korelasi
masing-masing senyawa.
38
Tabel III. Data kurva baku siproheptadin HCl pada 297 nm
Replikasi I Replikasi II Replikasi III
Konsentrasi (ppm)
Amplitudo Konsentrasi (ppm)
Amplitudo Konsentrasi (ppm)
Amplitudo
20,20 - 0,0130 20,20 - 0,0120 20,04 - 0,0140 25,25 - 0,0175 25,25 - 0,0155 25,05 - 0,0190 30,30 - 0,0195 30,30 - 0,0185 30,06 - 0,0210 35,35 - 0,0280 35,35 - 0,0230 35,07 - 0,0270 40,40 - 0,0290 40,40 - 0,0260 40,08 - 0,0300 45,45 - 0,0300 45,45 - 0,0285 45,09 - 0,0315 50,50 - 0,0400 50,50 - 0,0330 50,01 - 0,0355
r 0,971 r 0,998* r 0,991
B -8,168.10-4 B -6,825.10-4* B -7,036.10-4
A 3,589.10-3 A - 1,768.10-3* A -7,631.10-4
Berdasarkan tabel III, masing-masing replikasi menghasilkan harga r
yang melebihi r tabel. Persamaan kurva baku dikatakan memiliki linearitas yang
baik selain memiliki harga r yang mendekati 1 juga > 0,99 (Anonim, 2004),
karena menandakan adanya korelsi yang baik antara konsentrasi dengan
amplitudo. Replikasi kedua memiliki harga r yang telah memenuhi persyaratan
linearitas. Didapatkan persamaan kurva baku siproheptadin HCl :
Y = -6,825.10-4 X – 1,768.10-3
Gambar 17. Kurva baku siproheptadin HCl
39
Tabel IV. Data kurva baku ketotifen fumarat pada 287 nm
Replikasi I Replikasi II Replikasi III
Konsentrasi (ppm)
Amplitudo Konsentrasi (ppm)
Amplitudo Konsentrasi (ppm)
Amplitudo
20,06 0,0125 20,02 0,0130 20,20 0,0130 25,08 0,0160 25,02 0,0170 25,25 0,0180 30,09 0,0210 30,03 0,0205 30,30 0,0210 35,11 0,0230 35,04 0,0230 35,35 0,0230 40,12 0,0270 40,14 0,0280 40,40 0,0275 45,14 0,0285 45,04 0,0290 45,45 0,0295 50,15 0,0335 50,05 0,0340 50,50 0,0340
r 0,993 r 0,995* r 0,994
B 6,694.10-4 B 6,740.10-4* B 6,542.10-4
A - 4,296.10-4 A - 1,227.10-4* A 5,893.10-4
Berdasarkan tabel IV, masing-masing replikasi menghasilkan harga r yang
melebihi r tabel. Persamaan kurva baku dikatakan memiliki linearitas yang baik
selain memiliki harga r yang mendekati 1 juga > 0,99 (Anonim, 2004), karena
menandakan adanya korelsi yang baik antara konsentrasi dengan amplitudo.
Replikasi kedua memiliki harga r yang telah memenuhi persyaratan linearitas.
Didapatkan persamaan kurva baku ketotifen fumarat:
Y = 6,740.10-4 X - 1,227.10-4
Gambar 18. Kurva baku ketotifen fumarat