1
dalam Larutan NaCl 1%
Ni Ketut Ketis1), Deana Wahyuningrum2), Sadijah Achmad2) dan Bunbun Bundjali3)
1)Guru Kimia, SMA Negeri 3 Palu, Palu
2)Kelompok Keilmuan Kimia Organik, Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Bandung, Bandung
3)Kelompok Keilmuan Kimia Anorganik dan Fisik, Program Studi Kimia, Fakultas Matematika dan Ilmu
Pengetahuan Alam, Institut Teknologi Bandung, Bandung e-mail: deana@chem.itb.ac.id
Diterima 13 Juli 2009, disetujui untuk dipublikasikan 23 Maret 2010
Abstrak
Korosi pada permukaan bagian dalam pipa merupakan masalah pelik dalam pertambangan minyak dan gas bumi. Salah satu solusinya adalah penggunaan inhibitor korosi organik. Asam amino dan turunannya berpotensi sebagai inhibitor korosi, diantaranya yang dipelajari dalam studi ini adalah asam glutamat. Efektivitas asam glutamat sebagai inhibitor korosi pada baja karbon dalam larutan NaCl 1% (w/v) jenuh CO2 telah ditentukan menggunakan metode Tafel dengan optimasi konsentrasi asam glutamat, pH, dan suhu media uji. Asam glutamat memberikan efisiensi inhibisi korosi paling baik pada suhu kamar (26oC) dengan konsentrasi 8 ppm dalam larutan NaCl 1% da pH media uji 6,5, yaitu 48,19%. Adanya larutan buffer asetat dalam media uji dan pada kondisi di atas suhu kamar menyebabkan asam glutamat 8 ppm menjadi tidak efektif lagi digunakan sebagai inhibitor korosi.
Kata kunci: Inhibitor korosi, Baja karbon, Asam glutamat, Metode tafel
Abstract
Corrosion towards the inner parts of oilfield pipelines is one of most disturbing problems in oil and gas industries. Amino acid and its derivatives have potent as corrosion inhibitor, including glutamic acid, which has been studied within this research project. The effectivity of glutamic acid as corrosion inhibitor towards carbon steel in 1% (w/v) NaCl solution saturated by CO2 has been determined utilizing Tafel method with the optimization of glutamic acid concentration, pH, and temperature of tested medium. Glutamic acid showed the highest corrosion inhibition efficiency at room temperature (26oC), which is 48.19% at the concentration of 8 ppm in 1% NaCl solution and pH 6.5. The presence of acetate buffer solution in the medium that was being tested and at the temperature higher than room temperature has caused glutamic acid at the concentration of 8 ppm became ineffective to be applied as corrosion inhibitor.
Keywords: Corrosion inhibitor, Carbon steel, Glutamic acid, Tafel method
Pendahuluan
Korosi merupakan masalah rumit dalam pertambangan minyak dan gas bumi. Selain mengandung air, minyak mentah dan gas alam juga dapat mengandung CO2, asam organik, misalnya
asam asetat, serta senyawa sulfida dan garam-garam klorida yang bersifat korosif terhadap bagian dalam pipa baja pengalirnya (Hong and Jepson 2001; Cruz dkk., 2005). Korosi baja karbon bergantung pada komposisi anion-anion dalam larutan elektrolit. Dalam larutan yang mengandung ion Cl– (klorida)
dan CO2 terlarut, perilaku korosi baja karbon
dipengaruhi oleh pH, konsentrasi ion dan suhu yang dapat mempengaruhi potensial korosi (Jones 1992; Kuznetsov 2002; Perez 2004). Korosi pada permukaan luar pipa dapat dihambat dengan pengecatan dan perlindungan katoda, tetapi korosi pada permukaan bagian dalam pipa hanya dapat dilakukan menggunakan inhibitor korosi. Ada dua macam inhibitor korosi, yaitu inhibitor anorganik dan
organik. Inhibitor anorganik memiliki inhibisi yang baik terhadap laju korosi namun menimbulkan masalah bagi lingkungan bila terakumulasi, sehingga penggunaan inhibitor organik menjadi pilihan alternatif karena lebih ramah lingkungan (Bentiss dkk., 2004; Lopez dkk., 2004). Senyawa organik yang mengandung satu atau lebih atom nitrogen, oksigen, sulfur, fosfor, ikatan rangkap atau cincin aromatik pada molekulnya dapat digunakan sebagai inhibitor korosi, karena dapat teradsorpsi dengan baik pada permukaan logam. Senyawa organik yang mengandung gugus amina dan karboksilat seperti asam amino juga dapat digunakan sebagai inhibitor korosi (Srhiri dkk., 1996; Heeg dkk., 1998; Rajendran dkk., 2001; Stupnisek-Lisac dkk., 2002). Hal ini disebabkan oleh adanya gugus amina, gugus karboksilat, dan gugus samping yang mengandung gugus fungsi belerang, senyawa aromatik dan heterosiklik nitrogen, yang berpotensi untuk dapat berinteraksi dengan permukaan logam dan membentuk lapisan pelindung terhadap lingkungan
yang korosif. Dengan adanya gugus-gugus tersebut maka dapat diasumsikan senyawa asam amino dan turunannya merupakan kandidat yang potensial sebagai inhibitor korosi. Beberapa penelitian telah melibatkan beberapa asam amino sebagai inhibitor korosi, diantaranya adalah asam amino histidin (Wahyuningrum, 2004, 2006; Mateo dkk., 2003), sistein (Brolo dkk., 2002; Matos, 2004), dan triptofan (El-Shafei dkk., 2004). Asam amino lain dan turunannya yang sudah diteliti memberikan efisiensi inhibisi (EI) yang baik tetapi secara ekonomi masih belum menguntungkan (Rajendran dkk., 2001; Stupnisek-Lisac dkk., 2002). Asam glutamat adalah asam amino yang memiliki dua gugus karboksilat dan satu gugus amina yang diharapkan dapat menginhibisi korosi dengan cara teradsorpsi pada permukaan baja karbon. Asam glutamat merupakan senyawa antara dalam pembuatan mono sodium glutamat (MSG) yang relatif murah di pasaran, sehingga apabila asam glutamat terbukti berpotensi sebagai inhibitor korosi, maka secara otomatis asam glutamat menjadi suatu kandidat inhibitor korosi yang secara ekonomi relatif murah dan meningkatkan nilai ekonomis pada produksi MSG secara umum.
Penelitian ini bertujuan untuk mengetahui efektivitas asam glutamat sebagai inhibitor korosi pada baja karbon dalam larutan NaCl 1% jenuh CO2,
dengan optimasi konsentrasi asam glutamat, pH dan suhu media uji dengan menggunakan metode Tafel. Manfaat yang diharapkan dari penelitian ini yaitu memperkaya khazanah keilmuan mengenai inhibitor korosi organik, khususnya untuk menghambat peristiwa korosi pada baja karbon yang biasa digunakan pada pipa pertambangan minyak dan gas bumi.
2. Metodologi
Pengukuran laju korosi menggunakan alat Voltalab® potensiostat PGZ 301 dengan metode
Tafel. Secara umum prosedur pengukuran korosi baja karbon dalam larutan uji, baik tanpa inhibitor (blanko) maupun dengan inhibitor sebagai berikut: ke dalam sel elektrokimia yang dilengkapi pengaduk magnet dituangkan 100 mL larutan uji, lalu ketiga elektroda dipasang. Ketiga elektroda tersebut adalah elektroda kerja (baja karbon), elektroda bantu (platina) dan elektroda pembanding (elektroda kalomel jenuh, SCE). Elektroda kerja (baja karbon) yang telah dipoles basah dengan ampelas silikon karbida (SiC) 1000 grit hingga halus dan rata kemudian dicuci dengan aquadest, disemprot dengan gas nitrogen dan dicuci dengan aseton. Selanjutnya ketiga elektroda dihubungkan dengan potensiostat
PGZ 301, pengaduk magnet dijalankan, gas CO2
dialirkan secara bubbling selama 20 menit untuk mendesak gas oksigen keluar dari sistem, dan setelah 20 menit potensiostat dijalankan. Pasangan elektroda kerja dan elektroda pembanding mengukur potensial sel, pada saat bersamaan pasangan elektroda kerja dan elektroda bantu mengukur arus korosi. Data yang
dihasilkan dari pengukuran setelah 15 menit potensiostat dijalankan dan diproses oleh komputer menggunakan program Voltamaster®. Dengan
menggunakan metode ini data yang langsung diperoleh adalah nilai potensial korosi, Ekor, tahanan
polarisasi, Rp, tetapan Tafelanoda, βa, tetapan Tafel
katoda, βk, nilai kerapatan arus korosi, ikor (µA/cm2),
dan laju korosi, vkor (µm/thn). Penggambaran
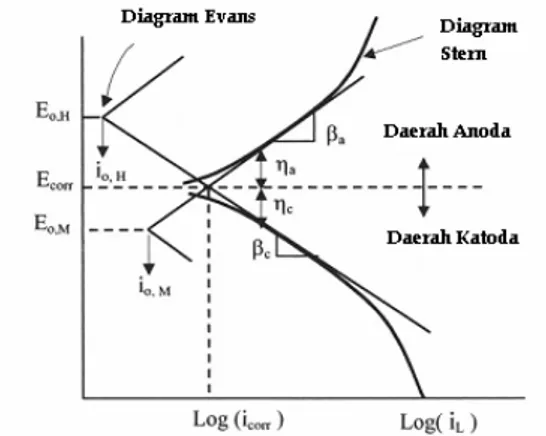
polarisasi Tafel dapat dipelajari dari kurva polarisasi ekstrapolasi Tafel yang dikemukakan oleh Evans dan Stern dalam bentuk diagram Evans dan Stern seperti pada Gambar 1 berikut (Perez, 2004).
Gambar 1. Kurva ekstrapolasi polarisasi Tafel
(modifikasi dari Perez, 2004).
Gambar 1 menunjukkan polarisasi Tafel dengan Eo,H dan Eo,M adalah potensial sirkuit terbuka
untuk hidrogen dan logam M, io,H dan io,M merupakan
perubahan kerapatan arus untuk hidrogen dan logam M, dan iL adalah limit kerapatan arus. Di sisi lain,
Gambar 1 menunjukkan kebolehjadian elektrokimia yang didominasi oleh daerah katoda dan daerah anoda. Kurva tegas putus-putus yang digambarkan dipengaruhi oleh kemurnian logam dan paduan logam dimana Ecorr (atau Ekor) adalah potensial korosi
dan icorr (atau ikor) adalah kerapatan arus korosi.
Kedua kurva polarisasi menghasilkan bagian linier yang disebut sebagai garis Tafel. Garis Tafel ini digunakan untuk menentukan kemiringan/tetapan Tafel anoda (βa) dan kemiringan/tetapan Tafel katoda
(βc). Kurva ekstrapolasi akan berpotongan dan
membentuk garis lurus yang menunjukkan telah dicapai harga Ekor x ikor (Perez, 2004).
Efisiensi inhibisi korosi ditentukan dengan membandingkan selisih kerapatan arus korosi logam dalam larutan blanko dan sampel terhadap kerapatan arus korosi logam dalam larutan blanko menggunakan Persamaan (2-1). Efisiensi inhibitor dapat diungkapkan sebagai suatu ukuran untuk menunjukkan penurunan laju korosi sebagai berikut (Kuznetsov, 2002):
( - )
Efisiensi Inhibisi (% EI) = 100 x kor kor
kor blanko sampel blanko i i i (2-1) Dalam persamaan tersebut, ikor blanko adalah
(larutan NaCl 1%); sedangkan ikor sampel adalah
kerapatan arus korosi logam pada larutan sampel. Penentuan efisiensi inhibisi korosi asam glutamat dilakukan dalam larutan NaCl 1% (w/v) jenuh CO2 dengan optimasi konsentrasi asam
glutamat, pH dan suhu media uji. Optimasi pH dan suhu dilakukan pada konsentrasi asam glutamat yang memberikan %EI maksimum. Asam glutamat yang digunakan berupa kristal putih kualitas pro analisis (p.a). Elektroda kerja merupakan baja karbon produksi Krakatau Steel dengan komposisi sebagai berikut (dalam persen, %): Fe (99,5756); C (0,05991); Si (0,02986); S (0,00731); P (0,0123); Mn (0,22984); Ni (0,0046); Cr (0,01895); V (0,00291); Cu (0,0066); W (0,00009); Ti (0,00252); Sn (0,00136); Al (0,04752); Pb (0,0022); Nb (0,00117); Zn (0,00237).
3. Hasil dan Pembahasan
3.1 Optimasi konsentrasi asam glutamat dalam larutan NaCl 1%
Pengukuran efisiensi inhibisi korosi asam glutamat terhadap baja karbon dilakukan pada konsentrasi 5, 8 10, 15, 20 dan 25 ppm. Untuk memperoleh konsentrasi ini dibuat larutan induk asam glutamat 200 ppm yang diencerkan dengan larutan NaCl 1% (w/v). Data yang diperoleh ditampilkan pada Tabel 1 dan Gambar 2 yang menunjukkan kurva hubungan antara potensial korosi dan kerapatan arus korosi hasil uji korosi logam baja karbon dalam larutan blanko (NaCl 1%) dan larutan asam glutamat pada variasi konsentrasi dalam larutan NaCl 1%.
Penambahan asam glutamat ke dalam larutan blanko (larutan NaCl 1% w/v) menyebabkan potensial korosi, Ekor, bergeser ke arah yang positif
seperti ditampilkan pada Tabel 1. Spesi-spesi dalam media yang dapat mempolarisasi baja karbon ke arah anoda (positif) adalah yang bermuatan negatif atau bermuatan parsial negatif. Molekul asam glutamat memiliki dua gugus bermuatan negatif yaitu gugus karboksilat dari gugus pokok asam amino dan rantai sampingnya. Hal ini menyebabkan kerapatan arus pada proses anoda (iFe⎜Fe2+) berkurang, yang juga
berdampak pada penurunan kerapatan arus korosi,
ikor. Oleh karena permukaan baja karbon terpolarisasi
secara anoda dan laju korosi baja karbon diinhibisi oleh asam glutamat, maka asam glutamat dikategorikan sebagai inhibitor jenis anoda, yaitu inhibitor yang menginhibisi pelarutan ion-ion Fe2+
dengan cara menurunkan kerapatan arus pada proses anoda. -750 -730 -710 -690 -670 -650 -630 -610 -590 -570 -0.5 0 0.5 1 1.5 2 2.5 3
Kerapatan Arus Korosi, ikor (mA/cm2)
P o te n s ia l K o ro s i, E ko r (m V ) Blank 5 ppm 8 ppm 10 ppm 15 ppm 20 ppm 25 ppm
Gambar 2. Kurva polarisasi Tafel untuk perilaku
korosi baja karbon dalam larutan blanko (NaCl 1%) dan larutan asam glutamat pada variasi konsentrasi dalam larutan NaCl 1% pada 26oC.
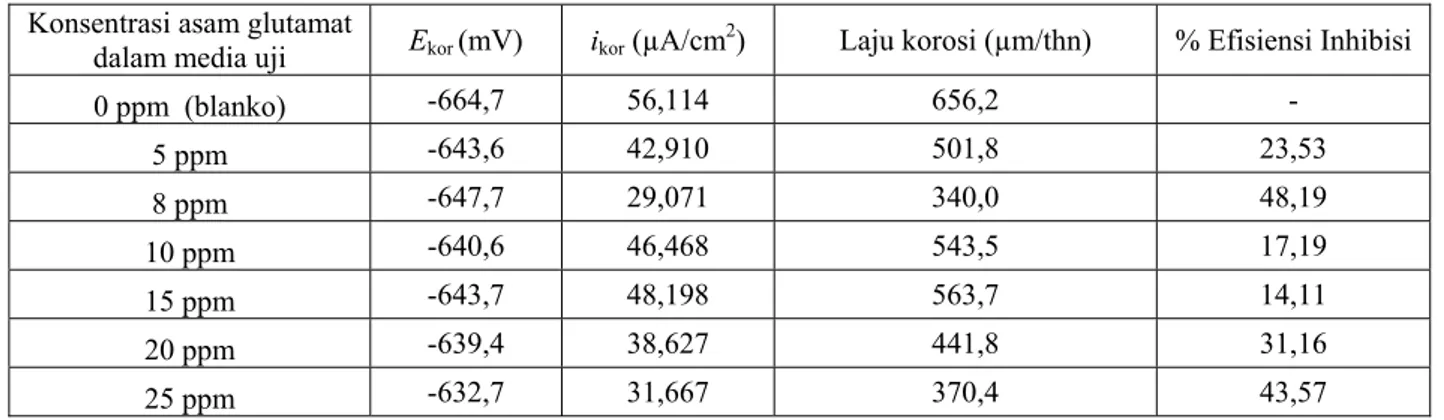
Tabel 1. Pengaruh konsentrasi asam glutamat terhadap korosi baja karbon dalam larutan NaCl 1 % jenuh CO2 pada
suhu 26oC
Konsentrasi asam glutamat
dalam media uji Ekor (mV) ikor (µA/cm2) Laju korosi (µm/thn) % Efisiensi Inhibisi
0 ppm (blanko) -664,7 56,114 656,2 - 5 ppm -643,6 42,910 501,8 23,53 8 ppm -647,7 29,071 340,0 48,19 10 ppm -640,6 46,468 543,5 17,19 15 ppm -643,7 48,198 563,7 14,11 20 ppm -639,4 38,627 441,8 31,16 25 ppm -632,7 31,667 370,4 43,57
Konsentrasi asam glutamat yang memberikan kerapatan arus korosi dan laju korosi paling kecil memberikan daya inhibisi paling besar, yaitu pada konsentrasi 8 ppm sebesar 48,19%. Polarisasi permukaan baja karbon ke arah lebih positif akibat terpolarisasi oleh gugus fungsi amina sangat kecil, sebab gugus tersebut dalam media uji berada dalam
keadaan terprotonasi sebagai gugus amonium, – NH3+. Hal ini berdasarkan nilai pKa1, pKa2, pKa3 dan
pI asam glutamat adalah, secara berturut-turut, 2,2; 9,7; 4,3; dan 3,2 (Solomon dan Fryhle, 2008), sehingga pada kondisi pengukuran dalam larutan NaCl 1% yang dijenuhkan oleh gas CO2, yaitu pada
berada dalam bentuk monoanionnya, dimana gugus α-amina terprotonasi (Gambar 2). Gugus –NH3+
cenderung mempolarisasi permukaan baja karbon ke arah lebih negatif. Dengan demikian, polarisasi permukaan baja karbon ke arah lebih positif disebabkan oleh kedua gugus karboksilat yang bermuatan negatif (–COO–), dengan gugus –COO–
rantai samping memegang peran yang lebih besar. Hal ini didukung oleh data hasil uji efisiensi inhibisi korosi asam amino glutamin pada konsentrasi yang sama (8 ppm dalam larutan NaCl 1%) yang memberikan efisiensi inhibisi korosi jauh lebih kecil (hanya 8,19%) daripada asam glutamat 8 ppm. Pada glutamin, nilai pKa1, pKa2 dan pI adalah, secara
berturut-turut, 2,2; 9,1 dan 5,7 (Solomon and Fryhle, 2008), sehingga pada pH media uji, yaitu 6,5, glutamin berada dalam bentuk zwitter ion-nya (Gambar 3). Dalam bentuk ini, glutamin hanya memiliki satu gugus –COO– yang dapat teradsorpsi
pada permukaan baja karbon, sedangkan gugus – NH3+ pada glutamin memberikan efek sebaliknya
yang menyebabkan efisiensi inhibisi korosi glutamin terhadap baja karbon menjadi kecil.
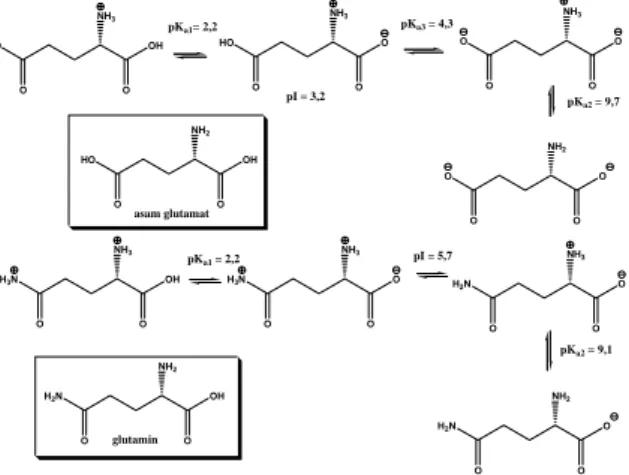
asam glutamat NH3 O HO O OH NH3 O HO O O NH3 O O O O NH2 O O O O NH2 O HO O OH pKa1= 2,2 pI = 3,2 pKa3 = 4,3 pKa2 = 9,7 a. glutamin NH3 O H3N O OH NH3 O H3N O O NH3 O H2N O O NH2 O H2N O OH pKa1 = 2,2 pI = 5,7 NH2 O H2N O O pKa2 = 9,1 b.
Gambar 3. Struktur spesi-spesi asam glutamat dan
glutamin pada berbagai kondisi pH
Sifat adsorpsi asam glutamat pada baja karbon adalah merupakan adsorpsi fisik, hal ini ditunjukkan oleh kecilnya nilai ∆G0
ads asam glutamat yang
ditentukan menggunakan Persamaan (3-1), (3-2) dan (3-3). Derajat penutupan permukaan (θ, degree of
surface coverage) dapat dihitung dari data kerapatan
arus korosi berdasarkan metode Tafel, sebagaimana dinyatakan oleh persamaan berikut (Khaled, 2003; Morad dan Kamal El-Dean, 2006)
1 inh uninh i i θ= − ⎜⎛ ⎞⎟ ⎝ ⎠ (3-1)
dengan iinh dan iuninh adalah kerapatan arus korosi
(dalam mA/cm2), secara berturut-turut, larutan
sampel dengan dan tanpa inhibitor korosi. Ternyata data yang dianalisis bersesuaian dengan isoterm adsorpsi Langmuir dalam bentuk yang paling sederhana, yaitu grafik linier hubungan antara konsentrasi sampel inhibitor korosi (Cinh) dengan
Cinh/ θ, sesuai persamaan berikut (Bentiss dkk., 2004; Morad dan Kamal El-Dean, 2006), sebagaimana ditunjukkan pada Gambar 4.
C 1 C inh inh b b θ= + (3-2)
dengan θ adalah derajat penutupan permukaan dan b adalah nilai koefisien adsorpsi, yang juga merupakan nilai tetapan kesetimbangan adsorpsi (Kads) untuk
asam glutamat, yang mengikuti hubungan linier isoterm adsorpsi Langmuir dalam bentuk senderhana (Persamaan 3-2). Nilai energi bebas adsorpsi (∆G0
ads,
dalam kJ/mol) dapat ditentukan melalui persamaan berikut (Morad dan Kamal El-Dean, 2006; Refaey
dkk., 2006; Fouda dkk., 2007): 0 1 exp 55,55 ads ads G K RT ⎛ ∆ ⎞ = ⎜− ⎟ ⎝ ⎠ (3-3)
dengan R = tetapan gas ideal = 8,314 J/mol.K, nilai 55,55 adalah konsentrasi air (H2O) dalam larutan
(dalam satuan mol), dan T adalah suhu dalam K. Berdasarkan ketiga persamaan tersebut diperoleh nilai koefisien adsorpsi, b, adalah 9465,4 M-1 dan
energi bebas adsorpsi, ∆G0
ads adalah −32,85 kJ/mol.
Nilai ∆G0
ads sampai dengan – 20 kJ/mol konsisten
dengan adanya adsorpsi fisik (fisiosorpsi), sedangkan untuk nilai ∆G0
ads di atas – 40 kJ/mol konsisten
dengan adanya adsorpsi kimia (kemisorpsi) (Migahed
dkk., 2003; Morad dan Kamal El-Dean, 2006).
Dengan demikian asam glutamat termasuk mengalami interaksi adsorpsi secara fisik (fisiosorpsi) pada permukaan baja karbon.
y = 2.437x + 1E-05 R2 = 0.8233 0.00E+00 5.00E-05 1.00E-04 1.50E-04 2.00E-04 2.50E-04 3.00E-04 3.50E-04 4.00E-04 4.50E-04 5.00E-04 0 0.00005 0.0001 0.00015 0.0002 C (dalam M) C/ θ
Gambar 4. Hubungan linier antara Cinh/θ dengan
konsentrasi asam glutamat (dalam satuan M) yang menunjukkan adanya adsorpsi pada permukaan logam berdasarkan persamaan isoterm adsorpsi Langmuir
Proses adsorpsi molekul-molekul asam glutamat pada permukaan baja karbon diasumsikan membentuk lapis lindung yang diilustrasikan pada Gambar 5 dengan menggunakan software
Gambar 5. Model ilustrasi adsorpsi molekul asam
glutamat pada permukaan baja karbon dengan menggunakan software Chemoffice® 3D ver 8.1.
3.2 Pengaruh pH larutan asam glutamat 8 ppm dalam Larutan Buffer Asetat
Uji korosi terhadap logam baja karbon dalam media uji larutan asam glutamat 8 ppm diukur pada pH 3, 4, 5, dan 6 menggunakan larutan buffer asetat. Larutan buffer asetat dibuat dengan konsentrasi natrium asetat tetap dan konsentrasi asam asetat yang bervariasi. Larutan buffer asetat digunakan sebagai pelarut larutan induk asam glutamat 200 ppm, yang kemudian diencerkan menjadi 8 ppm, dan sebagai pelarut NaCl agar konsentrasinya tetap 1%. Perlakuan secara rinci adalah sebagai berikut: sebanyak 4 mL larutan asam glutamat 200 ppm ditambahkan dengan 1 gram NaCl dan larutan buffer asetat hingga volume 100 mL, selanjutnya diukur efisiensi inhibisi korosinya terhadap logam baja karbon. Data yang diperoleh ditampilkan pada Tabel 2.
Peningkatan pH larutan uji menggeser potensial korosi ke arah lebih negatif, baik tanpa inhibitor maupun dengan inhibitor seperti ditampilkan pada Tabel 2. Nilai persen efisiensi inhibisi yang negatif menunjukkan bahwa logam baja karbon menjadi semakin terkorosi dalam media uji yang mengandung asam glutamat 8 ppm dalam larutan buffer asetat. Perubahan potensial ke arah yang lebih negatif menunjukkan pertukaran kerapatan arus pada proses katoda menurun yang disebabkan oleh berkurangnya konsentrasi H+ pada larutan,
sehingga potensial korosi, Ekor menurun. Sebenarnya,
pada pH yang lebih tinggi, berdasarkan nilai pKa1,
pKa2, pKa3 dan pI asam glutamat, seharusnya asam
glutamat dalam bentuk monoanionnya dapat meningkatkan efisiensi inhibisi korosinya. Namun dalam hal ini, proses korosi pada semua pH dalam media larutan uji dikendalikan oleh adanya ion asetat, CH3COO–, yang berasal dari larutan natrium asetat
dengan jumlah sama pada setiap pH media larutan uji. Hadirnya ion asetat dan asam asetat dalam media uji mengakibatkan kepolaran larutan uji meningkat yang berdampak pada adanya interaksi antara asam glutamat yang sudah maupun yang belum teradsorpsi pada permukaan baja karbon dengan ion asetat dan asam asetat tersebut secara reaksi asam-basa biasa. Akibatnya, distribusi asam glutamat yang teradsorpsi pada permukaan baja karbon menjadi berkurang karena lebih cenderung berada dalam fasa larutannya, sehingga permukaan baja karbon menjadi kurang terlindungi dari proses reaksi oksidasi-reduksi dengan lingkungannya yang cenderung korosif. Hal ini didukung oleh fakta bahwa laju korosi baja karbon dalam larutan CH3COOH 0,1M lebih rendah daripada
dalam larutan buffer asetat pH 3, bahkan laju korosi baja karbon makin lambat dengan meningkatnya konsentrasi CH3COOH tetapi makin cepat jika
konsentrasi ion CH3COO– diperbesar (Sunarya,
2008). Kenyataan ini diperkuat dengan pernyataan bahwa produk korosi dalam media yang mengandung asam asetat dan ion asetat (larutan buffer asetat) berupa selaput pasif yang kurang berpori (Bundjali, 2005). Selaput yang terbentuk di atas permukaan baja karbon pada konsentrasi asam asetat yang lebih tinggi bersifat lebih protektif karena menghasilkan produk korosi berupa partikel-partikel berukuran butir sangat halus, yaitu senyawa FeCO3.CH3COO– yang semakin
banyak terbentuk pada pH yang rendah (Bundjali, 2005). Pada pH yang semakin tinggi (pH 6), molekul asam glutamat yang bermuatan –1 semakin banyak, artinya asam glutamat dalam bentuk monoanionnya,
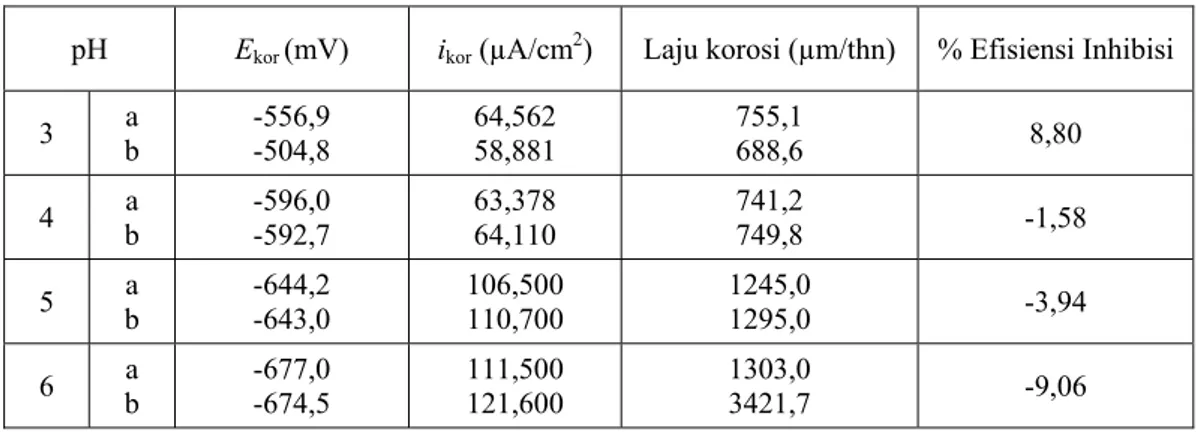
Tabel 2. Pengaruh pH terhadap efisiensi inhibisi korosi asam glutamat terhadap baja karbon dalam larutan NaCl 1%
jenuh CO2 pada suhu 26oC
pH Ekor (mV) ikor (µA/cm2) Laju korosi (µm/thn) % Efisiensi Inhibisi
3 b a -556,9 -504,8 64,562 58,881 755,1 688,6 8,80 4 b a -596,0 -592,7 63,378 64,110 741,2 749,8 -1,58 5 b a -644,2 -643,0 106,500 110,700 1245,0 1295,0 -3,94 6 b a -677,0 -674,5 111,500 121,600 1303,0 3421,7 -9,06
disamping adanya ion asetat dalam media uji dengan konsentrasi tetap, dengan demikian, secara keseluruhan dalam larutan media uji terdapat lebih banyak spesi anion. Pada permukaan logam terjadi arus reduksi membentuk spesi-spesi bermuatan negatif sehingga terjadi tolak menolak dengan seluruh spesi anion dalam larutan media uji, akibatnya kerapatan arus korosi dengan adanya ion asetat dalam media uji semakin tinggi pada pH yang semakin besar. Hal ini membuat asam glutamat menjadi tidak efektif lagi sebagai inhibitor korosi jika berada dalam media yang mengandung asam asetat dan garam asetat (larutan buffer asetat).
3.3 Pengaruh suhu terhadap efisiensi inhibisi korosi asam glutamat 8 ppm
Uji korosi terhadap logam baja karbon dilakukan pula dalam media uji larutan asam glutamat 8 ppm pada suhu 40oC, 55oC, 70oC, dan
85oC dalam larutan NaCl 1% jenuh CO
2. Data yang
diperoleh ditampilkan pada Tabel 3. Pada tabel tersebut, semakin tinggi suhu, potensial korosi bergeser ke arah lebih positif, baik pada larutan uji tanpa inhibitor maupun dengan penambahan inhibitor. Nilai persen efisiensi inhibisi yang negatif menunjukkan bahwa logam baja karbon menjadi semakin terkorosi dalam media uji yang mengandung asam glutamat 8 ppm pada suhu di atas suhu kamar. Peningkatan suhu menurunkan tahanan polarisasi pada antarmuka elektroda dan larutan uji, akibatnya zona serangan pada permukaan baja karbon makin luas (Bundjali, 2005; Sunarya, 2008). Pada suhu yang semakin tinggi, besi karbonat, FeCO3, sebagai
hasil reaksi Fe2+ dengan CO
32– teradsorpsi dengan
baik pada permukaan baja karbon, tetapi dengan adanya ion-ion Cl– kenaikan suhu dapat
meningkatkan serangan ion-ion Cl– terhadap lapisan
pasif FeCO3 sehingga terurai menjadi ion-ion Fe2+,
akibatnya arus korosi dan laju korosi semakin besar (Bundjali, 2005; Sunarya, 2008).
Kenaikan suhu cenderung menurunkan kekuatan interaksi antara atom-atom besi dengan gugus fungsi karboksilat dan amina dalam asam glutamat, sehingga kemampuan inhibisi asam glutamat pada korosi baja karbon cenderung menurun bahkan bersifat korosif pada suhu yang lebih tinggi. Sifat korosif ini disebabkan oleh karena pada suhu yang lebih tinggi asam glutamat terurai menjadi ion glutamat dan melepas ion H+ yang membuat larutan
uji semakin korosif. Selain itu, ion-ion korosif seperti ion Cl– dalam larutan uji semakin agresif pada suhu
yang semakin tinggi dan asam glutamat tidak mampu teradsorpsi pada permukaan baja karbon seperti pada suhu kamar. Ini berakibat pada bagian anoda yang tidak seluruhnya ditutupi oleh asam glutamat, sehingga akan memperluas daerah katoda. Dengan perbedaan luas ini intensitas serangan ion klorida pada baja karbon sangat meningkat pada daerah anoda yang sempit tetapi masih terbuka, sehingga laju korosi menjadi lebih besar (Supardi, 2002). Hal ini sejalan pula dengan sifat proses adsorpsi asam glutamat pada permukaan baja karbon yang bersifat fisiosorpsi, artinya interaksi antara gugus-gugus karboksilat pada asam glutamat dengan permukaan logam baja karbon berupa interaksi fisik dipol-dipol yang relatif lemah, sehingga naiknya suhu justru cenderung menginisiasi pemutusan interaksi tersebut dan menyebabkan permukaan baja karbon kurang tertutupi oleh asam glutamat. Akibatnya, logam baja karbon menjadi semakin terbuka kepada lingkungannya yang semakin korosif. Dengan demikian asam glutamat pada suhu yang semakin tinggi (di atas suhu kamar) tidak dapat digunakan sebagai inhibitor korosi karena pada kondisi tersebut justru menjadi korosif. Data energi pengaktifan (Ea)
proses inhibisi korosi asam glutamat terhadap logam baja karbon dalam larutan NaCl 1% (w/v) dapat diperoleh dengan mengalurkan ke dalam bentuk grafik hubungan antara logaritma kerapatan arus (log
icor) terhadap suhu (dalam 1000/T). Kemiringan
Tabel 3. Pengaruh suhu terhadap efisiensi inhibisi korosi asam glutamat 8 ppm pada korosi baja karbon dalam
larutan NaCl 1% jenuh CO2
Suhu (oC) E
kor (mV) ikor (µA/cm2) Laju korosi (µm/thn) % Efisiensi Inhibisi
40 a b -720,7 -724,4 145,068 134,596 1696,4 1518,0 7,22 55 a b -719,0 -720,5 172,073 172,466 2012,2 2015,0 -0,23 70 a b -716,6 -718,4 209,500 230,450 2449,9 2695,0 -10,00 85 a b -709,5 -709,8 231,750 259,800 2710,1 3038,0 -12,10 Keterangan: a = blanko ; b = sampel
grafik linier log icor terhadap 1000/T merupakan nilai
yang sebanding dengan nilai energi pengaktifan, Ea,
dibagi dengan tetapan gas ideal, R (dalam 8,314 KJ/mol.K). Berdasarkan data ini, energi pengaktifan proses inhibisi korosi senyawa turunan imidazol dapat ditentukan, sesuai persamaan berikut (Morad dan Kamal El-Dean, 2006).
exp cor a E i A RT = − (3-4)
dimana icor adalah kerapatan arus korosi (dalam
mA/cm2), A adalah faktor pre-eksponensial (tetapan
Arrhenius), Ea adalah energi pengaktifan proses
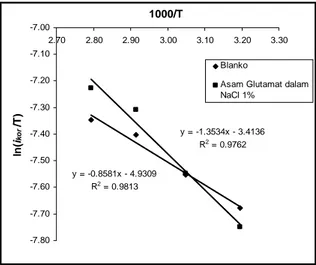
korosi (dalam kJ/mol), R adalah tetapan gas ideal (yaitu 8,314 kJ/mol.K) dan T adalah suhu (dalam K). Berdasarkan Gambar 6 dan Persamaan (3-4) diperoleh bahwa nilai energi pengaktifan, Ea, untuk
proses inhibisi korosi oleh asam glutamat adalah 25,91 kJ/mol sedangkan energi pengaktifan, Ea,
untuk larutan blanko adalah 16,43 kJ/mol. Hal ini menunjukkan bahwa proses korosi baja karbon dalam larutan asam glutamat 8 ppm tetap relatif lebih lambat terjadi dibandingkan dalam larutan blanko. Jadi, walaupun efisiensi inhibisi korosi asam glutamat pada konsentrasi 8 ppm kurang efektif dan cenderung korosif pada suhu di atas suhu kamar, namun masih memiliki potensi untuk menghambat laju korosi logam baja karbon dalam larutan NaCl 1%. Sehingga dapat disimpulkan bahwa kondisi optimum penggunaan asam glutamat sebagai kandidat inhibitor korosi adalah pada suhu kamar dengan konsentrasi 8 ppm dalam larutan NaCl 1% yang memiliki pH larutan 6,5.
y = -0.8581x - 4.9309 R2 = 0.9813 y = -1.3534x - 3.4136 R2 = 0.9762 -7.80 -7.70 -7.60 -7.50 -7.40 -7.30 -7.20 -7.10 -7.00 2.70 2.80 2.90 3.00 3.10 3.20 3.30 1000/T ln (i ko r /T ) Blanko
Asam Glutamat dalam NaCl 1%
Gambar 6. Aluran hubungan antara logaritma
kerapatan arus korosi (log icor, dalam mA/cm2) logam
baja karbon dalam larutan blanko dan larutan asam glutamat 8 ppm dalam NaCl 1% terhadap 1000/T (T adalah suhu dalam K)
4. Kesimpulan
Asam glutamat memberikan efisiensi inhibisi korosi paling efektif pada suhu kamar (26oC) dengan
konsentrasi 8 ppm dalam larutan NaCl 1% pada pH 6,5, yaitu sebesar 48,19%. Nilai efisiensi inhibisi
korosi ini relatif tidak begitu tinggi, namun dalam penggunaannya dapat ditingkatkan potensi efisiensi inhibisi korosinya dengan formulasi yang sesuai maupun dengan modifikasi gugus-gugus fungsi pada asam glutamat, yang dapat dijadikan suatu kajian penelitian lanjutan. Adanya spesi asam asetat dan natrium asetat sebagai larutan buffer dalam media uji serta kondisi media uji di atas suhu kamar menyebabkan potensi asam glutamat 8 ppm dalam larutan NaCl 1% sebagai inhibitor korosi menjadi sangat berkurang, bahkan korosif pada pH dalam sistem buffer asetat dan suhu yang lebih tinggi sehingga pada kondisi tersebut tidak efektif digunakan sebagai inhibitor korosi.
5. Ucapan Terima Kasih
Penelitian ini didanai oleh Hibah Riset Insentif Dasar Kemenristek RI kepada penulis kedua dan ketiga, dengan nomor Surat Perjanjian Kerja No. 0062i/K01.20/SPK-LPPM/PL2.1.5/I/2009, 23 Januari 2009.
Daftar Pustaka
Bentiss, F., M. Traisnel, H. Vezin, H. F. Hildebrand and M. Lagrenee, 2004, 2,5-Bis(4-dimethylaminophenyl)-1,3,4-oxadiazole and 2,5-bis(4-dimethylaminophenyl)-1,3,4-thiadiazole as Corrosion Inhibitors for Mild Steel in Acidic Media, Corros. Sci., 46, 2781-2792.
Brolo, A.G., P. Germain, and G. Hager, 2002, Investigation of The Adsorption of L-cysteine on a Polycrystalline Silver Electrode by Surface-Enhanced Raman Scattering (SERS) and Surface-Enhanced second harmonic generation (SESHG), J.
Phys. Chem. B, 106, p:5982–87.
Bundjali, B., 2005, Perilaku dan Inhibisi Korosi Baja
Karbon dalam Larutan Buffer Asetat, Bikarbonat-CO2, Disertasi Program Doktor, Institut Teknologi Bandung.
Cruz, J., T. Pandiyan and E. Garcı´a-Ochoa, 2005, A New Inhibitor for Mild Carbon Steel: Electrochemical and DFT Studies, J.
Electroanal Chem., 583, 8-16.
El-Shafei, A. A., S. A. Abd El-Maksoud, A. S. Fouda, 2004, The Role of Indole and Its Derivatives in The Pitting Corrosion of Al in Neutral Chloride Solution, Corros. Sci., 46, 579–590.
Heeg, B., D. Klenerman and T. Moros, 1998, Persistency of Corrosion Inhibitor Films on C-Steel under Multiphase Flow Conditions: Part I: The Jet-Cylinder Arrangement,
Corros. Sci., 40:8, 1303-1311.
Hong, T. and W. P. Jepson, 2001, Corrosion Inhibitor Studies in Large Flow Loop at High Temperature and High Pressure, Corros.
Jones, D. A., 1992, Principles and Prevention of
Corrosion. Singapore, Macmillan Publishing
Company.
Kadirgan, F. and S. Suzer, 2001, Electrochemical and XPS studies of corrosion behaviour of a low carbon steel in the presence ofFT2000 inhibitor, J. Electron. Spectrosc., 114, 597-601.
Kalman, E., J. Telegdi and T. Rigo, 2004, Nanolayer Barriers for Inhibition of Copper Corrosion.
Corrosion Engineering, Science and Technology, 39:1, 65-70.
Kuznetsov, Y. I., 2002, Current State of the Theory of Metal Corrosion Inhibition, Prot. Met+.,
38:2, 103-111.
Lopez, D. A., W. H. Schreiner, S. R. de Sanchez and S. N. Simison, 2004, The Influence of Inhibitors Molecular Structure and Steel Microstructure on Corrosion Layers in CO2
Corrosion: An XPS and SEM Characterization, Appl. Surf. Sci., 236, 77-97.
Mateo, E. Marti, Ch. Methivier, P. Dubot, and C. M. Pradier, 2003, Adsorption of (S)-Histidine on Cu(110) and Oxygen-Covered Cu(110), a Combined Fourier Transform Reflection Absorption Infrared Spectroscopy and Force Field Calculation Study, J. Phys. Chem. B,
107, 10785-10792
Matos, J.B , L. P. Pereira, S. M. L. Agostinho, O. E. Barcia, G. G. O. Cordeiro, and E. D’Elia, 2004, Effect of Cysteine on The Anodic Dissolution of Copper in Sulfuric Acid Medium, J. Electroanal. Chem., 570, 91–94. Migahed, M. A., H. M. Mohamed, 2003, Corrosion
Inhibition of H-11 Type Carbon Steel in 1 M Hydrochloric Acid Solution by N-Propyl Amino Lauryl Amide and Its Ethoxylated Derivatives, Mater. Chem. Phys., 80, 169-175.
Morad, M. S. and A. M. Kamal El-Dean, 2006, 2,2'-Dithiois(3-cyano-4,6-dimethylpyridine): A New Class of Acid Corrosion Inhibitors for Mild Steel, Corros. Sci., 48:11, 3398-3412. Perez, N., 2004, Electrochemistry and Corrosion
Science. New York, Boston, Dordrecht,
London, Moscow, Kluwer Academic Publishers.
Rajendran, S., B. V. Apparao, N. Palaniswamy, V. Periasamy and G. Karthikeyan, 2001, Corrosion Inhibition by Strainless Complexes, Corros. Sci., 43, 1345-1354. Refaey, S. A. M., F. Taha and A. M. A. El-Malak,
2006, Corrosion and Inhibition of 316L
Stainless Steel in Neutral Medium by 2-Mercaptobenzimidazole. Int. J. Electrochem.
Sci., 1, 80-91.
Srhiri, A., M. Etman and F. Dabosi, 1996, Electro and Physicochemical Study of Corrosion Inhibition of Carbon Steel in 3% NaCl by Alkylimidazoles Electrochim. Acta, 41:3, 429 - 437.
Solomon, T. W. G, and C. B. Fryhle, 2008, Organic
Chemistry, 9th ed., John Wiley & Sons Inc.,
Asia.
Stupnisek-Lisac, E., A. Gazivoda and M. Madzarac, 2002, Evaluation of Non-Toxic Corrosion Inhibitors for Copper in Sulphuric Acid.
Electrochim. Acta, 47, 4189-4194.
Sunarya, Y., 2008, Mekanisme dan Efisiensi Inhibisi
Sistein pada Korosi Baja Karbon dalam Larutan Elektrolit Jenuh Karbon Dioksida,
Disertasi Program Doktor, Institut Teknologi Bandung.
Supardi, R., 2002, Korosi dan Kegagalan Yang Terjadi Pada Pengecatan Otomotif. Bandung, Balai Besar Penelitian dan Pengembangan Industri Logam dan Mesin; Departemen Perindustrian dan Perdagangan. Veawab, A., P. Tontiwachwuthikul, and S.D. Bhole,
1997, Studies of Corrosion and Corrosion Control in a CO2
--2-Amino-2-methyl-1-propanol (AMP) Environment. Ind. Eng.
Chem. Res., 36, 264-269.
Wahyuningrum, D., Achmad, S., Nugraha, A. dan Damanik, R., (2004), Sintesis Senyawa Ester
Histidin dan Aplikasinya sebagai Inhibitor Korosi, Proceeding Seminar MIPA IV, ISSN
979-368-8-02-5
Wahyuningrum, D., R. Brahma, S. Achmad, dan B. Ariwahjoedi, 2005, The Synthesis of Some
Histidine Derivative Compounds Containing Imidazole Ring Framework and the Investigation of Their Inhibitor Activity towards Carbon Steel in 1% NaCl Solution,
The 6th ITB- UKM Joint Seminar on
Chemistry, Bali, Indonesia, JSChem ITB 2005, ISBN: 979-9299-16-0-540.
Wahyuningrum, D., A. Shobarudin, R. Brahma, S. Achmad, B. Ariwahjoedi, Ciptati, 2006, The
Synthesis of Some Acetyl Substituted Histidine Compounds Containing Imidazole Ring Framework and The Investigation of Their Inhibitor Activity towards Carbon Steel in 1% NaCl Solution, Proceeding of
Indonesian Symposium on Science and Technology on Chemistry (ISSToC), Serpong, Indonesia, ISSN: 1907-1485.