Pengaruh salinitas berbeda terhadap kelangsungan hidup dan pertumbuhan benih ikan nila (Oreochromis niloticus)
Desra Irawan1, Elfrida2, Dahnil Aswad2
1)
Mahasiswa Jurusan Budidaya Perairan E-mail : [email protected]
2)
Dosen Fakultas Perikanan Dan Ilmu Kelautan
Jurusan Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan Abstract
The purpose of this research was to find out and to determine the optimal salinity on survival (survival rate) and Tilapia seeds growth (Oreochromis niloticus). This research was take place on integrated laboratory fisheries and marine science faculty. It was chosen by using a completely randomized design, by using 4 treatments and 3 replicates. This research doing around 45 days, from march 5 until April 18 2014. A Treatment medium salinity 0-6 (fresh water) ppt, B treatment (medium salinity 15 ppt), C Treatment (medium salinity 20 ppt), D Treatment (medium salinity 25 ppt). The sample of this research was Tilapia fish (Oreochromis niloticus) with size was 1-2 cm, old 37 days, the total of sample was 300 fish. The container that was used 12 aquarium with size 40 x 35 x 20, each aquarium filled 25 Tilapia. The result of this research shows that the effect of different salinity towards highest survival on A Treatment (medium salinity fres water ) 92 %, whereas the best growth on C Treatment (medium salinity 25 ppt) weight average was 2,83 mg/tail and the best length on C Treatment (medium salinity 25 ppt)34.20 mm/tail.
Key words : Tilapia, Salinity, Oreochromis niloticus, Survival, Growth.
PENDAHULUAAN
Ikan Nila merupakan salah satu komoditas penting perikanan budidaya air tawar di Indonesia. Ikan ini disenangi tidak hanya karena rasa dagingnya yang khas, tetapi juga karena laju pertumbuhan dan perkembangbiakkannya yang cepat. sehingga, dikalangan peternak ikan, ikan Nila dijadikan komoniti unggulan.
Ikan Nila merupakan ikan yang memiliki daya tahan tubuh dan adaptasi yang baik. Salah satu adaptasi yang dapat dilakukan oleh ikan Nila adalah adaptasi fisiologis terhadap rentang salinitas yang tinggi karena ikan Nila tergolong ikan eurihaline dan
memiliki potensi untuk menyesuaikan diri pada salinitas air laut (± 35 ppt).
Mengingat bahwa ikan Nila cukup banyak diminati masyarakat dan memiliki batas toleransi terhadap salinitas yang cukup luas yaitu antara 0–35 ppt maka Ikan Nila berpotensi untuk dibudidayakan di daerah pantai dengan perairan payau. Salinitas merupakan salah satu faktor fisiologis yang berpengaruh terhadap pemanfaatan pakan pertumbuhan ikan. Pengaruh salinitas melalui tekanan osmotiknya terhadap pertumbuhan dapat terjadi baik secara langsung maupun tidak langsung. Pengaruh langsung salinitas yaitu efek osmotiknya terhadap osmoregulasi dan pengaruh secara tidak langsung salinitas mempengaruhi
organisme akuatik melalui perubahan kualitas air.
Penelitian ini telah pernah dilakukan Junius
Akbar (2012), dengan mengunakan ikan
betok sebagai ikan uji dan mendapatkan salinitas terbaik untuk pertumbuhan mutlak dan pertumbuhan relatif individu tertinggi terjadi pada media salinitas 0 ppt, sedangkan tingkat kelangsungan hidup tertinggi pada perlakuan salinitas 20 ppt.
Berdasarkan hal tersebut penulis tertarik untuk melakukan penelitiaan tentang pengaruh salinitas terhadap kelangsungan hidup dan pertumbuhan benih ikan Nila (Oreochromis niloticus) pada salinitas yang berbeda.
Penelitian ini bertujuan untuk mengetahui dan menentukan salinitas yang optimal terhadap kelangsungan hidup (survival rate) dan pertumbuhan benih ikan Nila (Oreochromis niloticus) .
Manfaat penelitian
Penelitian ini diharapkan dapat bermanfaat bagi informasi ilmiah kepada masyarakat pembudidaya tentang salinitas yang optimal bagi pertumbuhan dan kelangsungan hidup (survival rate) bagi benih ikan Nila
(Oreochromis niloticus)
MATERI DAN METODE PENELITIAN Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Terpadu Fakultas Perikanan Dan Ilmu Kelautan, dilaksanakan selama 45 hari, yang dimulai dari tanggal 5 Maret – 18 April 2014
Bahan dan Alat Bahan
• Ikan Uji
Ikan uji yang dipakai dalam penelitian ini adalah benih Nila (Oreochromis niloticus) dengan ukuran 1 – 2 cm yang berumur 37 hari, sebanyak 300 ekor benih ikan nila, benih tersebut diperoleh dari pemijahan sepasang induk di Laboratorium Terpadu, Fakultas Perikanan dan ilmu Kelautan Universitas Bung Hatta.
• Air Media Penelitian
Air yang digunakan sebagai media penelitian adalah air yang bersalinitas tawar, 15 ppt, 20 ppt, dan 25 ppt (sebagai perlakuan) dengan volume 10 liter setiap akuarium percobaan. Adapun rumus yang digunakan untuk mendapatkan salinitas yang sesuai dengan masing-masing perlakuan, dilakukan dengan cara mencampurkan antara air laut dan air tawar, dengan rumus sebagai berikut :
V1N1 = V2N2
Keterangan :
V1 = Volume air laut yang dipakai
N1 = Salinitas air laut yang dipakai
V2 = Volume air yang akan dibuat
N2 = Salinitas air yang akan dibuat
• Pakan
Pakan yang digunakan dalam penelitian ini adalah pakan berupa PM 500 yang diberikan secara adlibitum.
Alat Yang Digunakan Refraktometer DO Meter pH Universal Timbangan Termometer Aquarium Aerator Pengukur Salinitas Pengukur O2 Terlarut Pengukur pH
Alat Penimbang Berat Ikan Pengukur suhu
Wadah Pemeliharaan
Penyuplai O2
Metode Penelitian
Perlakuan dan Rancangan Percobaan
Rancangan yang digunakan adalah rancangan acak lengkap (RAL) dengan empat perlakuan dan tiga ulangan, yang mengacu pada rumus Steel dan Torrie
(1989).
Yji = µ + i + Σ ij
Ket :
Yij = Nilai pengamatan ke-i dan ulangan ke-j.
µ = Nilai tengah pengamatan i = Pengaruh perlakuan i
Σij = Pengaruh galat perlakuan ke I ulangan ke j
Adapun perlakuan yang digunakan adalah Perlakuan A = Media pemeliharaan bersalinitas 0 – 6 (tawar) ppt.
Perlakuan B = Media pemeliharaan bersalinitas 15 ppt.
Perlakuan C = Media pemeliharaan bersalinitas 20 ppt.
Perlakuan D = Media pemeliharaan bersalinitas 25 ppt.
Hipotesis dan Asumsi
Ho : Tidak ada pengaruh salinitas terhadap
kelangsungan hidup dan pertumbuhan ikan Nila (Oreochromis niloticus) pada salinitas yang berbeda.
H1 : Ada pengaruh salinitas terhadap
kelangsungan hidup dan pertumbuhan ikan Nila (Oreochromis niloticus) pada salinitas yang berbeda.
Asumsi yang dikemukakan:
• Pengaruh genetik dianggap sama.
• Penanganan selama penelitian dianggap sama.
Prosedur Penelitian Persiapan Wadah
• Persiapan akuarium sebagai tempat pemeliharaan sebanyak 12 buah yang berukuran 40 x 35 x 20,dan sebelumnya disterilkan dengan menggunakan PK , kemudian persiapan media bersalinitas tawar, 15, 20, dan 25 ppt.
• Wadah penelitian disusun secara acak sehingga diperoleh, pengaruh lingkungan dan proses pengangan yang sama.
• Pengisian wadah dengan media bersalinitas yang berbeda yaitu tawar (0 – 6 ppt), 15 ppt, 20 ppt, dan 25 ppt dengan volume air 18 l/akuarium.
Persiapan Ikan Uji
• Pengambilan embrio dari induk betina Induk betina ditangkap dan dipaksa
mengeluarkan (memuntahkan) telur sebelum menetas dan berkembang menjadi larva. Telur ini ditetaskan dan
dirawat dalam wadah khusus (inkubator).
• Pemeliharaan larva ikan Nila
Setelah kuning telur habis, larva ikan Nila diberi makan berupa Moina sp sampai ikan bisa memakan makan pakan butan berupa pellet.
Proses Adaptasi
Sebelum perlakuan, ikan uji ditempatkan dalam suatu wadah berupa akuarium yang kemudiaan diadaptasikan secara berlahan dengan air laut, yang dialirkan menggunakan infus secara bertahap, setelah ikan uji beradaptasi dengan salinitas 15 ppt maka selanjutnya ikan uji dipisahkan 75 ekor kewadah yang telah disediakan untuk perlakuan 15 ppt (Perlakuan B), sementara itu ikan uji yang berada pada aquarium utama masih diadaptasikan, setelah mencapai salinitas 20 ppt (Perlakuan C) ikan uji dipisahkan kembali 75 ekor untuk perlakuan 20 ppt , kemudian ikan yang tersisa pada aquarium utama diadaptasikan hingga salinitas mencapai 25 ppt (Perlakuan D), setelah itu baru dilakukaan pengamatan.
Pelaksanaan Penelitian
• Pada ikan dalam wadah masing – masing perlakuan dilakukan pemberian pakan berupa pellet PM 500 adlibitum. • Pengamatan awal dengan menimbang
berat dan mengukur panjang ikan. • Pengamatan kelangsungan hidup ikan
dilakukan setiap hari.
• Pengamatan panjang dan berat dilakukan 15 hari sekali, yang dilakukan selama 45 hari.
Paramater Uji. Kelangsungan Hidup
Kelangsungan hidup ikan dapat dihitung menggunakan rumus ( Effendie, 1978): Kelangsungan Hidup (SR) = No Nt x 100% Keterangan :
SR = kelangsungan hidup ikan Nila (%) Nt = jumlah ikan Nila yang hidup sampai
akhir penelitian
No = jumlah ikan Nila awal penelitian.
Laju Pertumbuhan bobot mutlak
Laju pertumbuhan bobot mutlak individu dinyatakan sebangai pertambahan bobot benih selama penelitian berlangsung dengan memakai rumus Effendi (1979) yaitu :
W = Wt - Wo
Keterangan :
W = laju Berat Mutlak
Wt = bobot benih pada waktu t (gr)
Wo = bobot benih ikan pada awal percobaan
Laju Pertumbuhan Panjang Mutlak
Menurut Effendie (1978) laju pertumbuhan panjang mutlak dapat dihitung dengan rumus :
Lm = Lt – Lo
Keterangan :
Lm = Laju pertumbuhan mutlak (mm) Lt = Pertumbuhan panjang mutlak /45 hari (mm)
Lo = Panjang awal (ekor)
Pengamatan Kualitas Air
Pengamatan kualitas air dilakukan 2 kali selama penelitian, yaitu pada awal dan akhir penelitian. Kualitas air yang diukur adalah untuk perikanan meliputi suhu, pH, DO.
Analisa Data
Semua data yang diperoleh dari hasil penelitian terlebih dahulu dilakukan uji statistik. Apabilah hasil analisis menunjukan
bahwa F hitung < F tabel pada taraf 95% berarti tidak ada pengaruh salinitas berbeda terhadap laju sintasan dan pertumbuhan larva ikan Nila, H0 diterima dan Hi ditolak. Jika F hitung > F tabel pada taraf 95% berarti ada pengaruh salinitas berbeda terhadap laju sintasan dan pertumbuhan larva ikan Nila H0 ditolak dan H1 diterima. Untuk melihat adanya pengaruh pelakuan dilakukan uji duncan’s (DMNRT).
HASIL DAN PEMBAHASAN
Kelangsungan Hidup Benih Ikan Nila (Oreochromis niloticus SP)
Data kelangsungan hidup benih ikan Nila yang dipelihara pada media bersalinitas yang berbeda yaitu tawar (kontrol), 15 ppt, 20 ppt, dan 25 ppt, dapat dilihat pada Lampiran 4, sedangkan rata – rata dari setiap perlakuan dapat dilihat pada Tabel 1
Tabel 1. Rata – rata kelangsungan hidup (%) benih ikan Nila selama penelitian
Perlakuan Kelangsungan Hidup
A B C D 92,00 ± 10,58 a 82,67 ± 10,07 a 86,67 ± 09,24 a 84,67 ± 05,03 a
Ket : A = Media pemeliharaan bersalinitas 0 – 6 (air tawar) ppt. B = Media pemeliharaan bersalinitas 15 ppt.
C = Media pemeliharaan bersalinitas 20 ppt. D = Media pemeliharaan bersalinitas 25 ppt Dari Tabel 1 dan Grafik 1 terlihat bahwa kelangsungan hidup tertinggi terdapat pada perlakuan A media pemeliharaan bersalinitas 0 – 6 ppt (air tawar), yaitu 92 % dan diikuti perlakuan C (media pemeliharaan bersalinitas 20 ppt) yaitu 86.67 % dan perlakuan D (media pemeliharaan bersalinitas 25 ppt) yaitu 85.33 %, sedangkan kelangsungan hidup
yang terendah terdapat pada perlakuan B (media pemeliharaan bersalinitas 15 ppt ) yaitu 82.67 %
Dari hasil analisis varian Lempira 4 terlihat bahwa pemeliharaan benih ikan Nila dengan salinitas yang berbeda, tidak terdapat pengaruh yang berbeda nyata terhadap kelangsungan hidup benih ikan Nila (P < 0,05).
Salinitas pembenih dibudiday Hapher menyebu Nila dap tinggi. kelangsun oleh kem Holliday kemampu bersalinit ikan untu mampu osmotik Kemungk mempuny tubuh yan dari ikan utama ya adaptasi terhadap Pangasiu Slembro Berdasark hidup be nyata pa menunjuk Gambar 2 air berpera han ikan. yakan di dan Prugin utkan bahwa at beradapta Pada ngan hidup mampuan osm y (1996)
uan ikan unt tas tergantun uk mengatur mempertaha yang kinan, ikan yai kemam ng lebih bai n uji merup ang menduku ikan – ika perlakuan us jambal (L uch et al., 2 kan analisa enih ikan N ada keempa kan bahwa 0 20 40 60 80 100 kelangsungan hidup % 2. Rata – rata an cukup p Ikan Nila perairan nin dalam F a beberapa s asi pada sa media ikan Nila moregulasi menyataka tuk bertahan ng kepada r cairan tubu ankan tingk mendekati n yang l mpuan meng ik. Kesempu pakan salah ung keberha an uji yang yang diberi Legendre et 003) statistik ke Nila tidak b at perlakua peningkata 0 0 0 0 0 0 A a kelangsung enting pada a biasanya bersalinitas Fitria (2012) spesies ikan alinitas yang bersalinitas, dipengaruhi an bahwa n pada media kemampuan uh, sehingga kat tekanan normal. ebih besar gatur cairan urnaan organ satu faktor asilan dalam g digunakan ikan kepada t al., dalam elangsungan berpengaruh an. Hal ini an salinitas B gan hidup (% a a . ) n g , i a a n a n . r n n r m n a m n h i s dari mem ikan hidu niilo terse bers (199 Dari hasi pada 15 p amo Tab yang mau men pera osm sehi men amo med amo C (m deng dala med B Perlakuan %) benih ika tawar mpengaruhi n Nila, ting up benih oticus) pada ebut, menu sifat euryha 96) i penelitian l rendahnya a perlakuan ppt, diduga oniak yang el 4 yang g tidak term upun dari has nyebabkan airan dika motik dalam ngga met nyebabkan fe oniak tinggi. dia salinitas t oniak yang d media salini gan salinita am tubuh ik dia tempat h C an Nila selam sampai 2 kelangsung gginya tingk ikan Nila a berbagai m unjukkan ba aline Lim n yang dila a tingkat kel B dengan m karena ting mencapai disebabkan makan oleh sil metabolis amoniak m arenakan k tubuh ikan tabolisme eses banyak . Namun se tidak mempe dapat diliha itas 20 ppt. as 20 ppt t an hampir s hidup (isoosm D ma penelitian 25 ppt, gan hidup b kat kelangsu a (Oreochr media bersal ahwa ikan dalam ba akukan dipe langsungan h media bersal gginya kandu 0,44 mg/l oleh sisa p benih ikan smee (feses) meningkat d karena tek kurang seim terganggu dan pembua emakin ting engruhi ting at pada perla ) Hal ini k tekanan osm seimbang de mostik) seh n tidak benih ungan romis linitas Nila astian eroleh hidup linitas ungan pada pakan Nila, yang dalam kanan mbang dan angan ginya ginya akuan karena motik engan ingga
energi dibutuhkan lebih kecil dan secara otomatis akan berpengaruh pada efesiensi pemanfaatan pakan, sehingga feses berkurang dan menyebabkan amoniak sedikit.
Tinggi amoniak di dalam perairan akan menyebabkan penurunan kualitas air dan rendahnya kandungan oksigen terlarut yang menyebabkan kematian benih ikan lebih tinggi. Dalam PP No. 82 tahun 2001, standar baku mutu kadar amoniak dalam usaha budidaya perikanan yaitu 0.02 ppm. Sedangkan mengapa perlakuan A (media bersalinitas tawar) didapat kelangsungan hidup tertinggi dikarenakan ikan Nila berasal dari habitat tersebut, sedangkan mengapa perlakuan C (media bersalinitas 20 ppt) tertinggi dikarenakan pada media tersebut adalah dengan batas optimum terbaik bagi ikan Nila. Hal ini terbukti pada perlakuan D (media salinitas 25 ppt) kelangsungan hidup ikan Nila menurun.
Effendi dalam Azka (2012), menyatakan
bahwa sumber amoniak dalam perairan berasal dari bahan organik (protein dan urea), feses maupun ekskresi biota akuatik yang merupakan limbah dari aktifitas metabolismee yang menghasilkan amoniak. Peningkatan kadar amoniak berkaitan erat dengan masuknya bahan organik (protein) yang mudah terurai di dalam perairan.
Salinitas memegang peranan penting dalam proses fisiologis ikan. Dalam menghadapi salinitas yang lebih tinggi maka konsentrasi garam dalam tubuh lebih tinggi dari pada konsentrasi garam pada lingkungan di luar tubuh atau lingkungan perairan, ikan – ikan air tawar cenderung mengekskresikan air lewat selaput keluar untuk mencapai homeostasis (Nybakken dalam Agustin
2001). Dengan adanya peningkatan salinitas
media, kondisi hipertonik antara cairan tubuh ikan dengan lingkungan perairan berkurang sehingga proses osmoregulasi yang terjadi juga berkurang
Osmoregulasi bagi ikan adalah merupakan upaya ikan untuk mengontrol keseimbangan air dan ion – ion antara didalam tubuh dan lingkungan melalui mekanisme pengaturan tekanan osmotik. Ginjal akan memompakan keluar kelebihan air tersebut sebagai air seni. Ginjal mempunyai glomeruli dalam jumlah yang banyak dengan diameter yang besar. Hal ini bertujuan untuk menahan garam-garam tubuh agar tidak keluar dan sekaligus memompa air seni sebanyak-banyaknya. Air seni yang keluar dari tubuh ikan sangat encer dan mengandung sejumlah kecil senyawa nitrogen. Proses osmoregulasi juga menghasilkan produk buangan seperti feses dan amoniak, sehingga media pemeliharaan akan berwarna keruh sebagai akibat banyaknya feses yang dikeluarkan ikan. Dampak dari ekskresi nitrogen tersebut akan mempengaruhi kehidupan ikan di dalamnya yaitu terhadap kondisi ambien, yang pada akhirnya berpengaruh terhadap pertahanan tubuhnya. Setelah melewati batas toleransi, maka ikan tersebut mengalami kematian. Mengingat tidak semua ikan mengalami kematian, maka dapat dipastikan bahwa daya toleransi pada populasi ikan dalam wadah berbeda-beda. Hal ini diduga karena perbedaan kondisi tubuh saat sebelum dimasukkan dalam media termasuk intensitas parasit, tingkat stress dan lain-lain. Untuk air tawar, organ yang terlibat dalam osmoregulasi antara lain insang, usus dan ginjal (Marshall, et al, 2006).
Hepher dan Priguinin (1981) menyatakan
pada media bersalinitas tinggi, karena kemampuan osmoregulasinya cukup baik. Perbedaan tingkat kelulus hidupan menunjukkan bahwa benih ikan Nila yang dipelihara pada media bersalinitas 0-25 ‰ bagus dalam memanfaatkan sumber energi pakannya dan diduga pada media 0-25 ‰ kondisi tekanan osmotik media mendekati tekanan osmotik benih ikan Nila, atau disebut isoosmotik.
Untuk organisme akuatik, proses tersebut digunakan sebagai langkah untuk menyeimbangkan tekanan osmose antara substansi dalam tubuhnya dengan lingkungan melalui sel yang permeabel. Dengan demikian, semakin jauh perbedaan tekanan osmotik antara tubuh dan lingkungan, semakin banyak energi metabolisme yang dibutuhkan untuk melakukan osmoregulasi sebagai upaya adaptasi, hingga batas toleransi yang dimilikinya.
Regulasi ion dan air pada ikan terjadi hipertonik, hipotonik atau isotonik tergantung pada perbedaan (lebih tinggi, lebih rendah atau sama) konsentrasi cairan tubuh dengan konsentrasi media. Perbedaan ini dapat dijadikan sebagai strategi dalam menangani komposisi cairan ekstrasellular dalam tubuh ikan.
Untuk ikan-ikan potadrom yang bersifat hiperosmotik terhadap lingkungannya dalam proses osmoregulasi, air bergerak ke dalam tubuh dan ion-ion keluar ke lingkungannya dengan cara difusi. Keseimbangan cairan tubuhnya dapat terjadi dengan cara meminum sedikit air atau bahkan tidak minum sama sekali. Kelebihan air dalam
tubuhnya dapat dikurangi dengan cara membuangnya dalam bentuk urin.
Untuk ikan-ikan oseanodrom yang bersifat hipoosmotik terhadap lingkungannya, air mengalir secara osmose dari dalam tubuhnya melalui ginjal, insang, dan kulit ke lingkungannya, sedangkan ion-ion masuk ke dalam tubuhnya secara difusi.
Sedangkan untuk ikan-ikan eurihalin, memiliki kemampuan yang cepat menyeimbangkan tekanan osmotik dalam tubuhnya dengan media (isoosmotik), namun karena kondisi lingkungan perairan tidak selalu tetap, maka proses osmoregulasi seperti halnya pada kedua jenis ikan di atas tetap terjadi Marshall, et al (2006).
Perubahan kadar salinitas mempengaruhi tekanan osmotik cairan tubuh ikan, sehingga ikan melakukan penyesuaian atau pengaturan kerja osmotik internalnya agar proses fisiologis di dalam tubuhnya dapat bekerja secara normal kembali. Apabila salinitas semakin tinggi ikan berupaya terus agar kondisi homeostasis dalam tubuhnya tercapai hingga pada batas toleransi yang dimilikinya. Kerja osmotik memerlukan energi yang lebih tinggi pula. Hal tersebut juga berpengaruh kepada waktu kenyang (satiation time) dari ikan tersebut (Conides,
et al.,2004).
Proses osmoregulasi juga menghasilkan produk buangan seperti feses dan amoniak, sehingga media pemeliharaan akan berwarna keruh sebagai akibat banyaknya feses yang dikeluarkan ikan. Dampak dari ekskresi nitrogen tersebut akan mempengaruhi kehidupan ikan di dalamnya yaitu terhadap kondisi ambient, yang pada akhirnya
berpengaruh terhadap pertahanan tubuhnya. Setelah melewati batas
Untuk air tawar , organ yang terlibat dalam osmoregulasi antara lain insang, usus dan ginjal. Sel-sel yang berperan dalam organ insang untuk proses tersebut adalah mitokondria-rich dan role of pavement (Marshall, et al, 2006).
Struktur insang memiliki hubungan dengan kemampuan toleransi terhadap kisaran salinitas. Hal ini dapat ditunjukkan dengan histology dari struktur insang Caprella (Amphipoda: caprellidea) yang dikumpulkan dari komunitas Sargassum di timur laut Jepang dan diamati di bawah mikroskop elektron. Epitel sel insang dari ikan-ikan tersebut terdiri dari perkembangan
apical infolding system (AIS) dan basolateral infolding system (BIS) yang dihubungkan dengan mitokondria. Percobaan tentang toleransi terhadap salinitas dari 4 spesies Caprella mengindikasikan bahwa konsentrasi median letalnya pada 20
o
C berkisar antara 12,97- 18,84 practical salinity unit (p.s.u) dengan kelangsungan hidup 80% pada kondisi salinitas di atas 25,37 p.s.u bahkan selama 5 hari. Karakteristik insang dan lebarnya rentang toleransi salinitas pada Caprella spp, menunjukkan bahwa Caprella spp yang menghuni komunitas Sargassum merupakan organisme yang eurihalin (Takeuchi, et
al.,2003). Laju Pertumbuhan Bobot Mutlak Benih
Ikan Nila (Oreochromis niloticus)
Dari hasil pengamatan pertumbuhan bobot ikan uji setiap perlakuan dan ulangan selama
penelitian dapat dilihat pada Lampiran 5 Rata – rata pertumbuhan bobot setiap perlakuan dan ulangan disajikan pada Tabel 3 berikut
Tabel 2. Laju pertumbuhan rata - rata bobot mutlak benih ikan Nila (Oreochromis niloticus)
Perlakuan Kelangsungan Hidup (SD)
A B C D 2,19 ± 0,72a 2,14 ± 0,33 a 2,83 ± 0,16 a 2,56 ± 0,41 a
Ket : A = Media pemeliharaan bersalinitas 0 – 6 (air tawar) ppt. B = Media pemeliharaan bersalinitas 15 ppt.
C = Media pemeliharaan bersalinitas 20 ppt. D = Media pemeliharaan bersalinitas 25 ppt Dari Tabel 2 terlihat bahwa data laju pertumbuhan tertinggi terdapat pada perlakuan C (Media pemeliharaan bersalinitas 20 ppt) yaitu 2.83 gr dan diikuti perlakuan D (Media pemeliharaan bersalinitas 25 ppt) yaitu 2.56 gr dan perlakuan A Media pemeliharaan bersalinitas 0 – 6 (air tawar) yaitu 2.20 gr, sedangkan pertumbuhan bobot yang
terendah pada perlakuan B (Media pemeliharaan bersalinitas 15 ppt ) yaitu 2,14 gr .
Dari hasil analisis varian (Lampiran 5) terlihat bahwa pemeliharaaan benih ikan Nila dengan salinitas yang berbeda, tidak terdapat perbedaan yang nyata terhadap pertumbuhan bobot ikan Nila (P < 0,05).
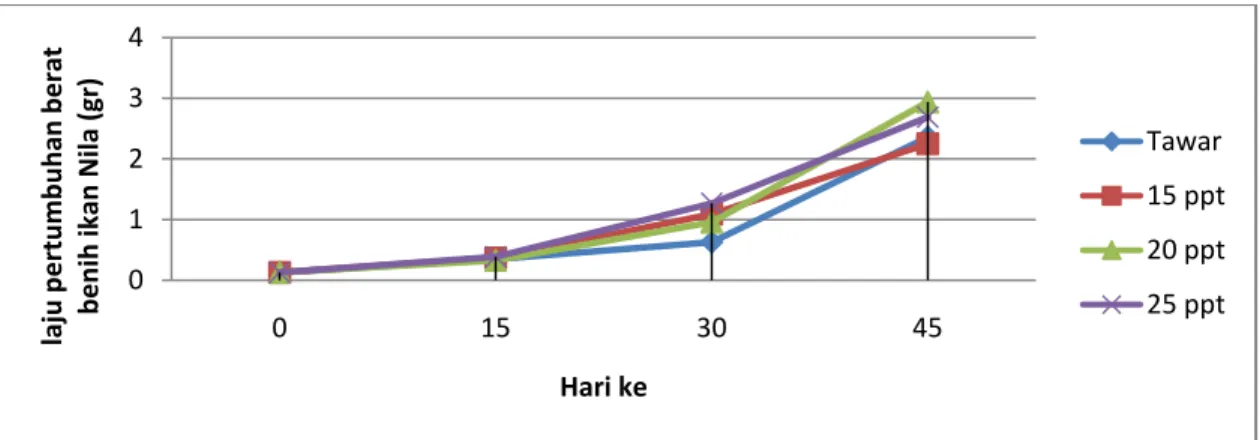
Gambar 3. Laju pertumbuhan rata - rata bobot benih ikan Nila (Oreochromis niloticus) per 15 hari
Dilihat dari diagram di atas dapat dilihat laju pertumbuhan bobot relatif dari setiap perlakuan per 15 hari. Dimana pertambahan berat rata – rata ikan Nila yang diperoleh dari grafik pertumbuhan yang cenderung meningkat pada stiap pengukuran pengamatan sampai akhir penelitian.
Peningkatan salinitas menyebabkan meningkatnya tekan osmotik perairan
(Boyd, 1982). Diduga tekanan osmotik
media bersalinitas 20 ppt paling mendekati tekanan osmotik darah benih ikan Nila. Pada kondisi isomotik kandungan ionik media mendekati konsentrasi ionik darah ikan, sehingga energi untuk kebutuhan osmoregulasi lebih kecil, serta energi untuk pertumbuhan tersedia pada jumlah yang lebih besar (Stickney ,1979)
Laju pertumbuhan ikan Nila juga dipengaruhi oleh konsentrasi amoniak.
Konsentrasi amoniak pada media bersalinitas 20 ppt relatif lebih rendah dibandingkan dari salinitas 15 ppt dan 25 ppt terlihat pada Tabel 4. Konsentrasi amoniak yang relatif rendah diduga menyebabkan laju pertumbuhan benih ikan lebih baik pada perlakuan tersebut. Konsentrasi amoniak yang besar akan menyebabkan pertumbuhan ikan menurun
(Boyd 1990).
Tingginya konsentrasi amoniak di perairan dapat mempengaruhi permeabilitas ikan oleh air dan mengurangi konsentrasi ion internal yang selanjutnya meningkatkan kerusakan insang dan konsumsi oksigen oleh jaringan, kerusakan insang dan mengurangi kemampuan darah mengangkut oksigen
(Schwedler et al, dalam Boyd, 1990) 0 1 2 3 4 0 15 30 45 laju pertumbuhan berat benih ikan Nila (gr) Hari ke Tawar 15 ppt 20 ppt 25 ppt
Pertumbuhan Panjang Mutlak Benih Ikan Nila (Oreochromis niloticus)
Tabel 3. Laju Pertumbuhan Rata - rata Panjang Mutlak Benih Ikan Nila (Oreochromis niloticus)
Perlakuan Kelangsungan Hidup (SD)
A B C D 56,67 ± 35,57a 54,67 ± 38,22 a 56,47 ± 40,29 a 55,58 ± 40,25a
Ket : A = Media pemeliharaan bersalinitas 0 – 6 (air tawar) ppt. B = Media pemeliharaan bersalinitas 15 ppt.
C = Media pemeliharaan bersalinitas 20 ppt. D = Media pemeliharaan bersalinitas 25 ppt Dari hasil pengamatan pertumbuhan panjang ikan uji setiap perlakuan dan ulangan selama penelitian dapat dilihat pada Lampiran 6 Rata – rata pertumbuhan bobot setiap perlakuan dan ulangan.
Dari Tabel 3, di atas terlihat bahwa pertumbuhan panjang mutlak yang tertinggi terdapat pada perlakuan C (media bersalinitas 20 ppt) yaitu 34,20 mm dan di ikuti perlakuan D (media bersalinitas 25 ppt selama 45 hari) yaitu 34,03 mm dan perlakuan B (media bersalinitas 15 ppt) yaitu 32,83 mm, sedangkan pertambahan
panjang yang terendah pada perlakuan A ( media bersalinitas air tawar) yaitu 32,53 mm.
Untuk mendapatkan gambaran yang jelas tentang pertumbuhan panjang benih ikan Nila selama penelitian, maka data dapat disajikan dalam bentuk gambar atau grafik berikut.
Hasil analisi varians untuk data pertambahan panjang individu ikan Nila menunjukan bahwa pengaruh salinitas yang berbeda tidak memberikan pengaruh nyata (P < 0,05)
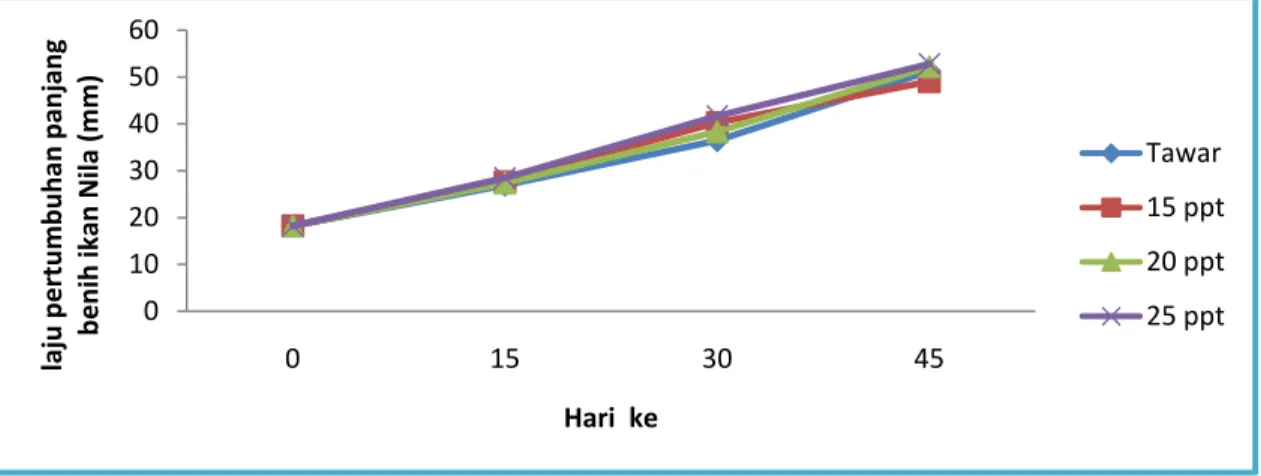
Gambar 4. Pertambahan Panjang Benih Ikan Nila (Oreochromis niloticus) per 15 hari
Berdasarkan dari diagram di atas dapat dilihat bahwa pertumbuhan panjang tertinggi terdapat pada perlakuan C (media
salinitas 20 ppt) dan terendah pada perlakuan A media bersalinitas 0-6 (tawar) disebabkan karena faktor lingkungan, 0 10 20 30 40 50 60 0 15 30 45 laju pertumbuhan panjang benih ikan Nila (mm) Hari ke Tawar 15 ppt 20 ppt 25 ppt
akibat dapat menyebabkan metabolisme tidak berjalan dengan baik sehingga pakan yang dimakan tidak termanfaatkan dengan baik.
Pada kondisi yang kurang tepat, suatu jenis ikan pertumbuhannya akan lambat dibandingkan dengan kondisi yang optimal, demikian juga didaerah yang beriklim panas pertumbuhan ikan akan lebih cepat dibandingkan daerah dingin (Efendie
dalam Erlinda, 2006).
Menurut Anderson dan Gureutur dalam
Erlinda (2006), kecepatan pertumbuhan
panjang individu dan distribusi frekuensi panjang merupakan sifat populasi ikan. Ikan secara umumnya mempunyai pertumbuhan yang tidak menentu, semua umur dan ukuran tidak dapat dipisahkan dengan pertumbuhan.
4.4. Pengamatan Kualitas Air
Data kualitas air selama penelitian dapat dilihat pada Tabel 4.
Tabel 4. Parameter kualitas air media pemeliharaan benih ikan Nila
(Oreochromis niliticus) selama penelitian
Parameter Kualitas Air
Awal Penelitian Akhir Penelitian
A B C D A B C D Suhu (0C) 26 26 26 26 27 27 27 27 DO (ppm) CO2 (ppm) 6,5 5,0 4,4 4,4 4.8 15 4.8 40 4.8 19 4.8 23 pH Amonia (ppm) 7 7,5 7,5 7,5 7 0.10 7,5 0.44 7,5 0.28 7.5 0.30
Effendi (1979), mengungkapkan bahwa
pertumbuhan merupakan parameter penting, dimana laju pertumbuhan dipengaruhi oleh faktor internal dan faktor eksternal. Faktor internal meliputi keturunan, umur dan ketahanan terhadap penyakit. Sedangkan faktor eksternal meliputi suhu perairan, oksigen terlarut, ukuran ikan, padat tebar serta jumlah mutu pakan. Parameter kualitas air yang diamati setiap perlakuan selama penelitian dapat dilihat pada Tabel 4
Suhu air selama penelitian berkisar antara
26-27 oC yang dianggap masih layak untuk
kehidupan ikan Nila (Oreochromis sp). Menurut Amri dan Khairun (2003), yang menyatakan suhu sesuai untuk ikan Nila
berkisar antara 14 – 35 oC.
DO (Dissolved Oxygen) merupakan kadar oksigen yang terlarut didalam air, kandungan oksigen terlarut (DO) selama penelitian nilai oksigen terlarut dalam air media penelitian berkisar antara 4,4 – 6,5 ppm masih dalam kisaran yang layak, karena dalam media penelitian diterapkan aerasi yang bertujuan untuk terjadinya proses diffusi oksigen di perairan. Oksigen sebanyak 4-6 ppm yang terlarut di dalam air dianggap paling ideal untuk tumbuh dan berkembang ikan. Bila keadaan kurang memungkinkan sehingga kandungan oksigen terlarut dalam air hanya 2 ppm, maka air tersebut masih memungkinkan dijadikan sumber air kolam. Tentunya air dengan kandungan oksigen yang rendah ini perlu dilakukan penanganan agak khusus,
misalnya dibuat air terjun yang masuk ke dalam kolam, sehingga terjadi diffusi oksigen dari udara bebas ke dalam air. Selain itu, permukaan air dalam kolam yang agak luas diharapkan juga mengakibatkan diffusi oksigen, (Susanto, 1991).
Karbondioksida (CO2) dalam perairan
dipengaruhi beberapa faktor terutama pengurai bahan – bahan organik, respirasi organisme air, serta diffusi dari udara. Dari hasil pengukuran kadar karbondioksida selama penelitian berkisar antara 20 – 40
mg/l. Kadar CO2 terlarut lebih dapat
ditoleransi oleh ikan dibandingkan dengan amoniak, bahkan banyak ikan yang hidup
pada air yang mengandung CO2
lebih besar dari 60 mg/l (Boyd, 1990). Selanjutnya Boyd (1982) meyatakan ikan mempunyai toleransi yang cukup besar
terhadap karbondioksida bebas jika kadar O2
cukup tinggi.
Nilai pH sangat penting dalam budidaya ikan Nila, sebab pH air merupakan faktor pembatas pada kehidupan ikan dan jasad renik lainya (Cahyono, 2001). pH air yang baik untuk kehidupan ikan adalah netral sampai sedikit alkali 7 - 8. Hal tersebut sesuai dengan kondisi pH air selama penelitian yaitu 7-7,5 yang sesuai untuk digunakan.
Abbas (2002) mengemukakan bahwa kadar
amoniak yang terkandung dalam air sebaiknya tidak lebih dari 1 ppm, apabila kadar amoniak lebih dari 0,5 ppt, maka dalam jangka waktu yang tidak lama ikan akan stress, sakit dan pertumbuhannya berkurang. Dari hasil penelitian terlihat kadar amoniak yang diperoleh berkisar antara 0.10 – 0.44 mg/l, maka masih dikategorikan layak untuk usaha budidaya.
KESIMPULAN DAN SARAN KESIMPULAN
Dari hasil penelitian yang telah dilakukan dapat disimpulkan.
1. Pada media pemeliharaan dengan salinitas yang berbeda memberikan pengaruh yang tidak berbeda nyata terhadap kelangsungan hidup dan pertumbuhan benih ikan Nila (Oreochromis niloticus) antar setiap perlakuan, dimana kelangsungan hidup tertinggi terdapat pada perlakuan A (media bersalinitas air tawar) yaitu 92 % 2. Pertumbuhan terbaik diperoleh pada
perlakuan C (media bersalinitas 25 ppt) dengan bobot ikan rata - rata 2.83 mg/ekor dan pertambahan panjang terbaik pada perlakuan C (media bersalinitas 25 ppt) yaitu 34.20 mm/ekor.
SARAN
Diharapkan adanya penelitian lanjutan untuk pemeliharaan ikan Nila dengan media salinitas dengan “range” yang lebih sempit untuk mendapatkan hasil yang lebih optimal.
DAFTAR PUSTAKA
Abbas S.D. 2002. Budidaya Nila GIT secara intensif. Kanisius. Yogyakarta
Akbar, J. 2012. Pertumbuhan dan Kelangsungan Hidup Ikan Betok (Anabas testudineus) Yang Dipelihara Pada Salinitas Berbeda. Fakultas Perikanan. Unlam.
Agustin, Y.2001. Pengaruh salinitas dan kesadahan terhadap kelangsungan hidup dan pertumbuhan ikan hias Sumatra (Barbus tetrazona Bleeker). Skripsi fakultas perikanan dan ilmu kelautan. Intitut Pertanian Bogor. Amri, k dan khairukman. 2003.. budidaya
ikan Nila secara intensif. Agromedia. Jakarta.
Aska. 2012. Pemberian vitazym dalam pakan terhadap kelangsungan hidup dan pertumbuhan larva ikan lele (Clarias batracus). Skripsi fakultas perikanan dan ilmu kelautan. Universitas Bung Hatta.
Boyd, C.E. & Lichtkoppler. 1982. Water quality management in pond fish culture. Auburn University. Auburn Alabama.
---. 1990 water quality management for pond fish culture. Elsevier scientific publishing company. New York.
Cahyono, B. 2001. Budidaya Ikan di Perairan Umum. Penerbit Kanisius, Yogyakarta.
Conides, A.J., Glamuzina, B., and Papaconstantinou, C. 2004. Laboratory Simulation of The Effects of Environmental Salinity on Wild Caught Juveniles of European Sea Bass Dicentrarchus Labrax and Gilthead Seabream, Sparusaurata.
Effendie. M. I. 1978. Biologi Perikanan. Fakultas Perikanan Institut Pertanian Bogor.
Efendie, M.I. 1979. Metode Biologi Perikanan. Penerbit Dwi Sri Bogor. Hepher, B. & Y. Priguinin. 1981.
Commercial Fish Farming with Special Reference to Fish Culture in Israel. John Willey and Sons Inc., New York.
Holliday, F.G.T. 1969. The Effects of salinity on the eggs and larvae of teleosts. In. hoar, W.S. & Randall, D.J. (Eds), Fish Physiology.
Lee, K.M, Kaneko, T., and Aida, K. 2005. Low Salinity Tolerance of Juvenile Fugu Takifugu Rupripes. Fisheries Science. Vol.71, pp.1324-1331
Marshall,C & Rossman. 2005. Designing Quyalitative Reseach London. Sage Publication. Marshall,C & Rossman. 2005. Designing Quyalitative Reseach London. Sage Publication.
Marshall, W.S., and Grosell, M. 2006. Ion Transport, Osmoregulation, and Acid- Base Balance. In the Physiology of Fishes. Evans, D.H and Claiborne, J.B. (eds). Taylor and Francis Group. pp 601.
Susanto, 1991, “Membuat Kolam Ikan Penebar Swadaya”, Jakarta
Slembrouch et al, J., et al. 2003. Larva biology. In slembrouck, J. et al.. technical manual for artificial propagation of the Indonesia catfist,
Pangasius djambal. Karya Pratama, Jakarta.
Stickney, R.R. 1979. Principle of Warmwater Aquaculture. John Willey and Sons Inc., New York.
Suyanto, R. 1994. Nila. Penerbit penebar Swadaya, jakarta.