LAPORAN PENELITIAN MANDIRI
EVALUASI KANDUNGAN GINGEROL PADA EKSTRAK RIMPANG JAHE (Zingiber officinale Roscoe.) DARI BOGOR
SEBAGAI BAHAN BAKU OBAT TRADISIONAL
Tim Pengusul
Ketua Peneliti
(
Hariyanti, M.Si., Apt.)Anggota Peneliti (Ni Putu Ermi Hikmawanti, M.Farm.)
PROGRAM STUDI FARMASI FAKULTAS FARMASI DAN SAINS
UNIVERSITAS MUHAMMADIYAH PROF. DR. HAMKA 2019
ABSTRAK
Jahe gajah atau jahe putih (Zingiber officinale Roscoe.) adalah salah satu tanaman obat yang diketahui dan dikenal sebagai obat herbal yang banyak khasiatnya. Salah satu kandungan kimia yang terkandung dalam jahe putih yaitu gingerol.Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan. Penelitian ini bertujuan mengetahui kandungan gingerol pada ekstrak rimpang jahe putih. Rimpang jahe putih diekstraksi menggunakan metode maserasi dengan pelarut etanol 70% dan aseton.
Identifikasi komponen senyawa gingerol dilakukan secara kualitatif menggunakan Gas Chromatography - Mass Spectrometer (GC-MS). Penetapan kadar fenolik total ekstrak rimpang jahe putih menggunakan Spektrofotometer UV – Vis pada panjang gelombang 764 nm. Hasil analisis GC-MS menunjukkan bahwa baik ekstrak etanol 70% maupun ekstrak aseton rimpang jahe putih memiliki kandungan gingerol dengan persentase kadar relatifnya masing – masing sebesar 2,60% ± 1,34 dan 5,94% ± 0,13. Kadar fenolik total ekstrak etanol 70% rimpang jahe putih sebesar 45,5788 ± 7,61 mgGAE/g sedangkan ekstrak aseton rimpang jahe putih sebesar 46,3655 ± 8,77 mgGAE/g.
Kata kunci: Aseton, etanol 70%, gingerol, GC-MS, jahe putih, Zingiber officinale var.
Roscoe.
DAFTAR ISI
HALAMAN PENGESAHAN ABSTRAK
DAFTAR ISI DAFTAR TABEL
DAFTAR GAMBAR
BAB 1. PENDAHULUAN Latar Belakang Masalah Masalah Penelitian Tujuan Penelitian
BAB 2. TINJAUAN PUSTAKA Roadmap penelitian
BAB 3. METODE PENELITIAN Alur Penelitian
Lokasi Penelitian Alat dan Bahan Prosedur kerja Analisis Data
BAB 4. HASIL DAN PEMBAHASAN BAB 5. SIMPULAN
DAFTAR PUSTAKA
DAFTAR TABEL
Halaman Tabel 1. Hasil Ekstraksi Rimpang Jahe Putih Menggunakan Metode
Maserasi dengan Pelarut Etanol 70% dan Aseton
18 Tabel 2. Hasil Pemeriksaan Organoleptis Ekstrak Jahe Putih 18 Tabel 3. Hasil penetapan Kadar air pada ekstrak
Tabel 4. Hasil penetapan kadar abu total pada ekstrak
Tabel 5. Hasil penetapan kadar abu tidak larut asam pada ekstrak Tabel 6. Hasil penetapan bobot jenis pada ekstrak
Tabel 7 Hasil penetapan cemaran logam berat pada ekstrak
Tabel 8 Hasil Penapisan Fitkomia Ekstrak Rimpang Jahe Putih 19 Tabel 9. Hasil Pengukuran Absorbansi Larutan Seri Konsentrasi
Asam Galat
21 Tabel 10. Hasil Analisis Profil Senyawa Gingerol Ekstrak Etanol 70%
Rimpang Jahe Putih
24 Tabel 11. Hasil Analisis Profil Senyawa Gingerol Ekstrak Aseton
Rimpang Jahe Putih
24 Tabel 12. Identifikasi Spektrum Massa Senyawa Gingerol Dengan
Menggunakan GC-MS
26
DAFTAR GAMBAR
Halaman Gambar 1. Grafik Hubungan Konsentrasi (ppm) Asam Galat terhadap
Absorbansinya
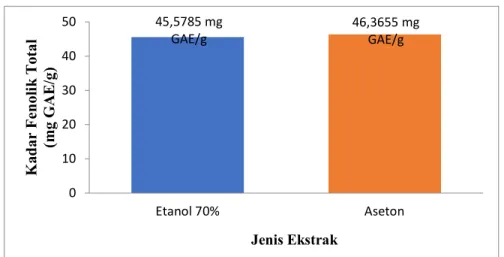
4 Gambar 2. Perbandingan Kadar Fenolik Total antara Ekstrak Etanol
70% dengan Ekstrak Aseton Rimpang Jahe Putih
5 Gambar 3. Pola Fragmentasi Gingerol Menggunakan Teknik Ionisasi
Elektron
21
BAB 1. PENDAHULUAN A. Latar Belakang Masalah
Jahe (Zingiber officinale) merupakan salah satu rempah dalam suku temu-temuan (Zingiberaceae). Tanaman ini se-famili dengan temu-temuan lainnya seperti temulawak (Curcuma xanthorrizha), temu hitam (Curcuma aeruginosa), kunyit (Curcuma domestica), kencur (Kaempferia galanga), lengkuas (Languas galanga), dan lain-lain yang telah digunakan secara luas di dunia baik sebagai bumbu dapur maupun sebagai obat medis terhadap penyakit-penyakit ringan. Bagian utama yang dimanfaatkan pada tanaman jahe adalah rimpangnya. Dikenal tiga jenis jahe di Indonesia, yaitu jahe putih/jahe gajah, jahe emprit dan jahe merah. Jahe gajah berukuran besar dan berwarna putih (Z. officinale var. roscoe), jahe emprit berukuran kecil dan berwarna putih (Z.
officinale var. amarum), sedangkan jahe merah berukuran kecil dan berwarna merah (Z.
officinale var. rubrum) (Paimin & Murhananto 1991).
Jahe gajah disebut juga jahe putih atau kuning besar atau jahe badak, rimpangnya lebih besar dan gemuk, ruas rimpangnya lebih menggembung dari kedua varietas lainnya. Jahe ini biasa dikonsumsi baik saat berumur muda maupun berumur tua, baik sebagai jahe segar maupun jahe olahan (Koswara 1995). Pemilihan jahe gajah yang digunakan dalam penelitian ini berdasarkan alasan bahwa jahe tersebut adalah jahe lokal yang diproduksi dan dimanfaatkan oleh masyarakat Indonesia serta mudah ditemukan.
Melalui penelitian ini diharapkan dapat menambah informasi dan penjelasan tentang kandungan gingerol jahe sebagai senyawa identitas yang berperan dalam aktivitas anti hiperlipidemia.
Jahe mempunyai komponen aktif antidiabetes dan mampu menurunkan kadar kolesterol (Akhani et al. 2004). Oleoresin jahe banyak mengandung komponen- komponen non volatil (minyak tidak menguap) daripada komponen volatil (minyak mudah menguap). Kandungan oleoresin jahe segar berkisar antara 0,4 – 3,1% (Koswara 1995). Oleoresin jahe merupakan campuran resin dan minyak atsiri yang diperoleh dari ekstraksi serbuk jahe dengan menggunakan pelarut organik. Oleoresin jahe berwarna gelap, hijau-kecoklatan, dan berbentuk semisolid digunakan dalam beberapa minuman dan penggunaan terbatas dalam obat farmasi (Farrell 2012). Resin tersebut terdiri dari komponen-komponen aktif berupa senyawa fenol seperti gingerol, shogaol dan zingerone yang memberikan rasa pedas (Uhl 2000). Komponen fenol dalam oleoresin jahe selain memberikan rasa pedas khas jahe, juga berperan sebagai antioksidan alami (Govindarajan 1983). Melalui penelitian ini diharapkan dapat menambah informasi dan
penjelasan tentang kandungan gingerol sebagai senyawa identitas pada ekstrak rimpang jahe.
B. Masalah Penelitian
Berdasarkan latar belakang tersebut, maka perlu dilakukan Evaluasi Kandungan Gingerol dari ekstrak jahe gajah agar dapat diperoleh aktivitas farmakologi
C. Tujuan Penelitian
Adapun tujuan penelitian ini untuk kandungan gingerol pada ekstrak rimpang jahe putih.
Pemilihan pelarut pengekstraksi, berpengaruh terhadap perolehan metabolit sekunder.
Penentuan senyawa identitas gingerol sebagai upaya kontrol kualitas ekstrak jahe 1. Gingerol dapat larut dalam pelarut etanol dan aseton.
2. Evaluasi gingerol dilakukan dengan metode GC-MS.
3. Penentuan kadar fenolik dilakukan dengan metode spektrofotometri
BAB 2. ROADMAP PENELITIAN
BAB 3. METODE PENELITIAN A. Alur Penelitian
1.
Determinasi tanaman2.
Pengumpulan bahan dan Penyediaan Bahan3.
Pembuatan ekstrak4.
Karakteristik Mutu Ekstrak5.
Penapisan Fitokimia6.
Penentuan kadar total fenolik7.
Analisis kandungan gingerol dari ekstrak jahe putih dengan GC-MS B. Lokasi PenelitianPenelitian dilakukan di Laboratorium Fitokimia, Laboratorium Kimia Terpadu, Laboratorium Teknik Sediaan Solid Fakultas Farmasi dan Sains Universitas Muhammadiyah Prof. Dr. HAMKA dan Laboratorium Kesehatan Daerah Provinsi DKI Jakarta, Laboratorium Instrumen Sucofindo, Cibitung dan Laboratorium Instrumen Universitas Negeri Jakarta.
C. Alat dan Bahan 1. Alat
Alat-alat yang digunakan meliputi : blender, timbangan analitik, ayakan nomor mesh 40, toples kaca, vacuum rotary evaporator, Gas Chromatography - Mass Spectrometer (GC-MS) seri Agilent Technologies 7890A, Spektrofotometri UV-Vis oven, label, krus silikat, krustang, batang pengaduk, corong, lemari asam, botol warna gelap, pipet tetes, lempeng silikat gel, piknometer, kertas saring, deksikator dan Spektroskopi serapan atom flame (SSA), serta alat-alat gelas yang lazim digunakan dalam laboratorium.
2. Bahan
Bahan penelitian simplisia rimpang jahe putih diperoleh dari BALITRO (Balai Penelitian Tanaman Rempah dan Obat), Bogor. Bahan kimia antara lain : asam galat (Merck), natrium karbonat p.a (Merck), Folin-Ciocalteau, etanol 70%, aseton, etanol p.a, logam mg, aqua dest, metanol, HCl pekat, FeCl3, HCl 2N, HNO3 pekat, H2O2, HCl 0,1N, HCl encer, pereaksi Dragendorff, pereaksi Mayer, asetat anhidrat dan H2SO4 pekat.
D. Prosedur kerja
1. Determinasi Tanaman
Jahe putih dideterminasikan di Herbarium Bogoriense, Balitbang Botani Puslitbang Biologi LIPI Cibinong, Bogor.
2. Pengumpulan dan Penyediaan Bahan
Rimpang jahe putih kering diserbuk, setelah itu diayak dengan ayakan bernomor mesh 40 hingga didapatkan serbuk kering jahe putih (Sunaryo dkk. 2017).
3. Pembuatan Ekstrak
Ekstrak rimpang jahe putih dibuat dengan metode maserasi menggunakan dua jenis pelarut yang berbeda yaitu etanol 70% dan aseton dengan perbandingan bahan dan pelarut 1:5 (Sunaryo dkk. 2017). Serbuk direndam sambil sekali-kali diaduk dan didiamkan selama 24 jam. Maserat dipisahkan dan proses diulangi 3 kali dengan jenis dan jumlah pelarut yang sama. Semua filtrat dikumpulkan dan dipekatkan dengan vacuum rotary evaporator pada suhu 45oC hingga diperoleh ekstrak kental. Rendemen yang diperoleh ditimbang dan dicatat.
Rumus perhitungan rendemen ekstrak seperti pada rumus 4
𝑟𝑒𝑛𝑑𝑒𝑚𝑒𝑛(%) = ( )
( )𝑥 100% ……....…..…………...(4)
4. Karakterisasi Mutu Ekstrak a. Pemeriksaan Organoleptis Ekstrak
Ekstrak diidentifikasi berdasarkan warna, rasa, bentuk dan bau dengan panca indra.
b. Penetapan Susut Pengeringan ekstrak
Sebanyak 1 gram bahan uji ditimbang, dimasukkan ke dalam krus silikat yang telah ditara, dikeringkan di dalam oven pada suhu 1050C selama 30 menit, kemudian dimasukan dalam deksikator selama 60 menit, kemudian ditimbang. Setelah itu dimasukan kembali ke dalam oven pada suhu 1050C selama 30 menit, kemudian dimasukan dalam deksikator selama 60 menit, kemudian timbang kembali, sehingga diperoleh bobot tetap.
c. Penetapan kadar air
Penetapan kadar air di lakukan dengan cara destilasi toluen. Toluen yang digunakan dijenuhkan dengan air terlebih dahulu, setelah dikocok didiamkan, kedua lapisan air dan toluen akan terpisah, lapisan air dibuang. Sebanyak 10 g ekstrak yang ditimbang dengan seksama dimasukkan ke dalam labu alas bulat dan ditambahkan toluen yang telah dijenuhkan dengan air. Labu dipanaskan hati-hati selama 100 menit, setelah toluen
mulai mendidih, penyulingan diatur 2 tetes/detik, lalu 4 tetes/detik. Setelah semua toluena mendidih, dilanjutkan pemanasan selama 5 menit. Kemudian dialirkan tabung menerima dingin sampai pada suhu kamar. Setelah lapisan air dan toluena memisah sempurna, volume air dibaca dan dihitung kadar air dalam persen terhadap berat ekstrak semula. Pekerjaan diulangi tiga kali (Khoirani 2013).
d. Penetapan kadar abu total
Ekstrak ditimbang sebanyak 2 gram kemudian dimasukan ke dalam krus silikat yang telah ditara, dipijarkan di dalam tanur dan suhu dinaikkan secara bertahap hingga 6000C (selisih suhu kurang lebih 250C) sampai bebas karbon. Selanjutnya, didinginkan dalam deksikator, kemudian ditimbang. (Anonim 2008 dalam Guntarti dkk 2015).
e. Penetapan Kadar abu tidak larut asam
Abu yang diperoleh dari penetapan kadar abu total, dididihkan dengan 25 ml HCl encer selama 5 menit. Pengumpulan bagian yang tidak larut asam, disaring melalui kertas saring bebas abu, dicuci dengan air panas, kemudian dipijarkan di dalam krus silikat hingga bobot tetap.
f. Bobot Jenis
Piknometer kosong ditimbang. Selanjutnya piknometer diisi penuh dengan air, sehingga berat dapat ditetapkan, kemudian piknometer kosong diisi penuh dengan ekstrak, timbang. Bobot jenis dilakukan pada suhu kamar.
g. Penetapan cemaran Logam Timbal dan Kadmium.
Masing-masing sampel ditimbang seksama sebanyak 5 gram di dalam krus yang telah diketahui massanya. Sampel dimasukkan ke dalam gelas kimia 100 ml untuk dilakukan destruksi basah dengan menggunakan campuran asam HNO3 pekat dan H2O2
pekat. Destruksi dilakukan dengan cara HNO3 pekat, sebanyak 30 ml ditambahkan sedikit demi sedikit hingga sampel larut, untuk melarutkan sampel diaduk dengan menggunakan hot plate, setelah larut kemudian larutan sampel didinginkan selama 15 menit, setelah didinginkan 15 menit lalu ditambahkan sedikit demi sedikit H2O2
sebanyak 10 ml hingga larutan menjadi jernih dan gas keluar sempurna. Campuran tersebut dipanaskan dengan kenaikan suhu secara perlahan-lahan hingga mencapai suhu 100°C. Setelah larutan cuplikan menjadi jernih, kemudian didinginkan. Larutan cuplikan dipindahkan ke dalam labu ukur 50 ml dan diencerkan dengan menggunakan HNO3 1%. Larutan cuplikan disaring dengan menggunakan kertas saring dan filtrat yang dihasilkan digunakan untuk analisis lebih lanjut. Larutan cuplikan siap dianalisis dengan instrumen AAS (Wulandari dan Sukesi 2013).
5. Penapisan fitokimia a. Identifikasi flavonoid
Dimasukkan 500 mg sampel ke dalam tabung reaksi, kemudian ditambahkan metanol, panaskan diatas penangas air pada suhu 100°C , saring dan filtratnya ditambahkan HCl pekat dan logam Mg. Jika terbentuk warna merah menunjukkan adanya senyawa flavonoid (Depkes RI 2000).
b. Identifikasi fenolik
Dimasukkan 500 mg sampel ke dalam tabung reaksi, lalu tambahkan 10 mL air, didihkan selama 5 menit pada suhu 100°C di atas penangas air, dinginkan dan saring.
Tambahkan 1-2 tetes FeCl3 1% ke dalam filtrat, akan terbentuk warna biru tua atau hijau kehitaman yang menunjukkan adanya fenolik (Depkes RI 2000).
c. Identifikasi saponin
Dimasukkan 500 mg sampel ke dalam tabung reaksi, ditambahkan 10 mL air panas, didinginkan dan dikocok selama 10 detik, sehingga terbentuk buih yang mantap selama tidak kurang dari 10 menit setinggi 1 cm sampai 10 cm. Pada penambahan 1 tetes HCl 2N, buih tidak hilang, maka kemungkinan ada saponin (Depkes RI 2000).
d. Identifikasi alkaloid
Dimasukkan 500 mg sampel ke dalam tabung reaksi, tambahnkan 1 mL HCl 2 N dan 9 mL aquadest, panaskan di atas penangas air pada suhu 100°C selama 2 menit, kemudian dinginkan dan saring. Pindahkan hasil saringan dan bagi ke dalam 2 tabung reaksi. Tabung pertama diberi pereaksi Dragendorff, jika ada endapan berwarna merah maka menunjukkan adanya senyawa alkaloid. Pada tabung kedua diberi pereaksi Mayer, jika terdapat endapat putih menunjukkan adanya senyawa alkaloid (Depkes RI 2000).
e. Identifikasi triterpenoid
Dimasukkan 500 mg sampel ke dalam tabung reaksi, ditambahkan 2 mL etanol, dipanaskan kemudian didinginkan dan saring. Filtratnya diuapkan lalu ditambahkan eter, 3 tetes asetat anhidrat dan 1 tetes H2SO4 pekat, jika terbentuk warna merah atau ungu menunjukkan adanya triterpenoid (Depkes RI 2000).
6. Penentuan kadar total fenolik (Alfian dan Susanti 2012) a. Pembuatan larutan induk asam galat
Ditimbang sebanyak 50,0 mg asam galat, dilarutkan dalam 0,5 ml etanol p.a, kemudian volume dicukupkan dengan aqua dest hingga tanda batas labu takar 100 ml.
b. Penentuan panjang gelombang maksimum asam galat
Sebanyak 300 μl larutan asam galat konsentrasi 30 μg/ml ditambah 1,5ml
reagen Folin Ciocalteau (1:10), kemudian digojog dan didiamkan selama 3 menit. Ke dalam larutan tersebut ditambah 1,2 ml larutan Na2CO3 7,5%, digojog homogen dan didiamkan pada suhu kamar. Kemudian absorbansinya diukur pada panjang gelombang 600-850 nm.
c. Penentuan operating time
Sebanyak 300 μl larutan asam galat konsentrasi 30 μg/ml ditambah 1,5ml
reagen Folin Ciocalteau (1:10), kemudian digojog dan didiamkan selama 3 menit. Ke dalam larutan tersebut ditambah 1,2 ml larutan Na2CO3 7,5%, digojog homogen, dan diukur absorbansinya dalam rentang waktu 0-60 menit pada panjang gelombang 764 nm.
d. Pembuatan kurva baku asam galat.
Larutan dibuat dalam berbagai konsentrasi, 20, 30, 40 ,50 ,60 ppm dari larutan induk. Larutan seri konsentrasi (masing-masing 300μl) dimasukkan dalam tabung reaksi, ditambah dengan 1,5 ml reagen Folin Ciocalteau dan digojog. Setelah didiamkan selama 3 menit, masing-masing larutan ditambahkan 1,2 ml natrium karbonat (7,5%
b/v), dicampurkan secara perlahan dan didiamkan 20 menit. Semua larutan diukur absorbansinya pada panjang gelombang 764 nm Persamaan regresi diperoleh dari data konsentrasi dengan absorban sehingga didapat nilai koefisien korelasi (r).
e. Pembuatan larutan uji dan pengukuran kadar fenolik total ekstrak
Sebanyak 100,0 mg masing masing sampel (ekstrak etanol 70% jahe putih dan ekstrak aseton jahe putih) dilarutkan dengan campuran etanol 70% : aqua dest (7:3) dan campuran aseton : aqua dest (7:3) kemudian dimasukkan ke labu ukur 100 ml cukupkan sampai tanda batas. Larutan ekstrak yang diperoleh dipipet 300 μl dan ditambah 1,5 ml reagen Folin-Ciocalteau dan digojog. Didiamkan selama 3 menit, ditambah 1,2ml larutan Na2CO3 7,5% dan didiamkan lagi pada suhu kamar. Absorbansi larutan ekstrak diukur dengan spektrofotometer UV-Vis pada panjang gelombang 764 nm. Dilakukan 5 kali pengulangan.
7. Analisis kandungan gingerol dari ekstrak jahe putih dengan GC-MS
Ekstrak jahe putih dilarutkan dahulu dengan pelarutnya (etanol 70% dan aseton) kemudian dianalisis kualitatif dengan GC-MS di Laboratorium Kesehatan Daerah Provinsi DKI Jakarta. Sebanyak ± 1 µL larutan ekstrak dianalisis dengan GC-MS seri Agilent Technologies 7890A sistem GC dengan Triple Axis Detector. Pemisahan dilakukan dengan menggunakan kolom HP innowax (30 m x 0,25 mm x 0,25 µm).
Sistem pemisahan yang digunkan dengan suhu injektor 250o C, aliran Helium 0,6
mL/menit, suhu awal oven 600C ditahan selama 1 menit, laju kenaikan 30C/menit hingga 1500C, ditahan 2 menit dan akhirnya meningkat 150C/menit hingga 2100C ditahan untuk 10 menit. Data yang diperoleh dari GC-MS kemudian dibandingkan dan ditelaah dengan basis data spektral Wiley.
BAB 4. HASIL DAN PEMBAHASAN A. Determinasi
Hasil determinasi yang dilakukan di Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi LIPI Cibinong – Bogor, menunjukan bahwa simplisia yang digunakan dalam penelitian adalah jahe putih jenis Zingiber officinale Roscoe dari famili Zingiberaceae (Lampiran 2).
B. Pembuatan serbuk jahe putih
Sebelum dilakukan proses maserasi, perlu dilakukan penyerbukan sampai derajat kehalusan tertentu pada jahe gajah untuk memperkecil ukuran partikelnya dengan menggunakan ayakan bernomor mesh 40 yang artinya tiap 1 inchi persegi terdapat 40 lubang yang bisa dilalui serbuk (jika derajat halus suatu serbuk dinyatakan dengan satu nomor, dimaksudkan bahwa semua serbuk dapat melalui pengayak dengan nomor tersebut) (Depkes RI 1995).
Alasan pemilihan pelarut etanol karena lebih efisien dalam dinding sel yang memiliki karakter nonpolar dan menyebabkan senyawa bisa dilepaskan dari sel (Tiwari et al. 2016), sedangkan pemilihan pelarut aseton karena pada umumnya aseton larut dalam berbagai perbandingan dengan air, etanol, dietil eter dan lain-lain (Alfian dan Susanti 2012). Aseton merupakan pelarut polar aprotik yang mana memiliki kepolaran tinggi karena mampu melarutkkan komponen hidrofilik dan lipofilik senyawa pada tanaman (Tiwari et al. 2016). Usman et al. (2013) menyatakan bahwa 6-gingerol dapat ditemukan pada ekstrak rimpang jahe dan biji merica yang diekstraksi dengan pelarut aseton, metanol, metanol-air dan air. Hasil ekstraksi jahe putih dengan metode maserasi menggunakan pelarut etanol 70% dan aseton dapat dilihat pada Tabel 1.
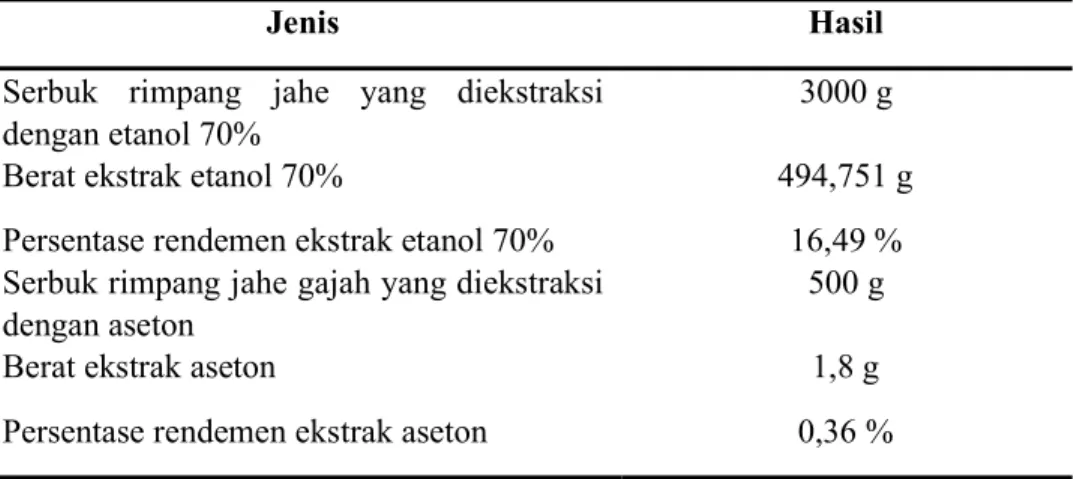
Tabel 1. Hasil Ekstraksi Rimpang Jahe Putih Menggunakan Metode Maserasi dengan Pelarut Etanol 70% dan Aseton
Jenis Hasil
Serbuk rimpang jahe yang diekstraksi dengan etanol 70%
3000 g
Berat ekstrak etanol 70% 494,751 g
Persentase rendemen ekstrak etanol 70%
Serbuk rimpang jahe gajah yang diekstraksi dengan aseton
16,49 % 500 g
Berat ekstrak aseton 1,8 g
Persentase rendemen ekstrak aseton 0,36 %
C. Pemeriksaan Karakteristik Mutu Ekstrak
Untuk mengetahui karakteristik ekstrak jahe putih dapat dilakukan dengan cara pemeriksaan organoleptis, penapisan fitokimia. Bisa dilihat pada tabel berikut.
1. Pemeriksaan Organoleptis
Hasil pemeriksaan organoleptis ekstrak rimpang jahe putih dapat dilihat pada Tabel 2.
Tabel 2. Hasil Pemeriksaan Organoleptis Ekstrak Jahe Putih Parameter Ekstrak Etanol 70% Ekstrak Aseton
Warna Coklat kehitaman Coklat kehitaman
Rasa Pedas Pedas
Bentuk Kental Kental
Bau Bau khas menyengat Bau khas menyengat
2. Susut pengeringan pada ekstrak Penetapan susut pengeringan bertujuan untuk mengetahui penyusutan berat ekstrak setelah dilakukan pengeringan. Pada proses ini, tidak hanya air yang dapat menguap melainkan juga minyak-minyak atsiri serta senyawa-senyawa terpenoid. Hasil yang didapat dari pengujian ekstrak etanol 70%
rimpang jahe gajah adalah 7,16% (b/b).
3. Penetapan kadar air
Tabel 2. Hasil penetapan adar air pada ekstrak
Parameter Hasil Depkes RI,2008
Kadar air 7,92 % Tidak lebih dari 10%
Berbeda halnya dengan penetapan susut pengeringan, pada penetapan kadar air hanya dihitung kadar air yang terkandung dalam ekstrak rimpang jahe gajah yang telah dilakukan pemekatan dengan rotary vacum evaporator.
Pengujian dilakukan di laboratorium Sucofindo Cibitung. Tujuan penetapan kadar air adalah untuk mengetahui persen kadar air yang masih terdapat dalam ekstrak dan hasil yang diperoleh dari penetapan kadar air adalah 7,92%. Berdasarkan hasil tersebut,
ekstrak etanol 70% rimpang jahe gajah telah
memenuhi standar mutu yang ditentukan Farnakope Herbal Indonesia 2008 tidak lebih dari 10 % (Depkes RI 2008).
4. Penetapan kadar abu total
Tabel 3. Hasil penetapan kadar abu total pada ekstrak
Jenis Hasil Depkes RI,2008
Krus silikat kosong
Krus silikat dengan sampel Bobot setelah ditanur kadar abu total
22,891 gram 24,904 gram 22,981 gram 10,52 % (b/b)
Tidak lebih dari 7,6 % Tujuan penetapan kadar abu adalah untuk mengetahui apakah ada unsur mineral dan anorganik yang tertinggal. Penetapan ini memberikan gambaran kandungan mineral internal dan ekstern kadar abu adalah 10,52% dan dari hasil yang didapat diperoleh kadar yang lebih tinggi dari acuan sehingga dapat disimpulkan bahwa ektrak yang didapat terkontaminasi unsur mineral maupun unsur anorganik yang kemungkinan didapat pada saat proses budi daya hingga proses pembuatan ekstrak kental (Depkes RI 2008).
5. Penetapan kadar abu tidak larut asam
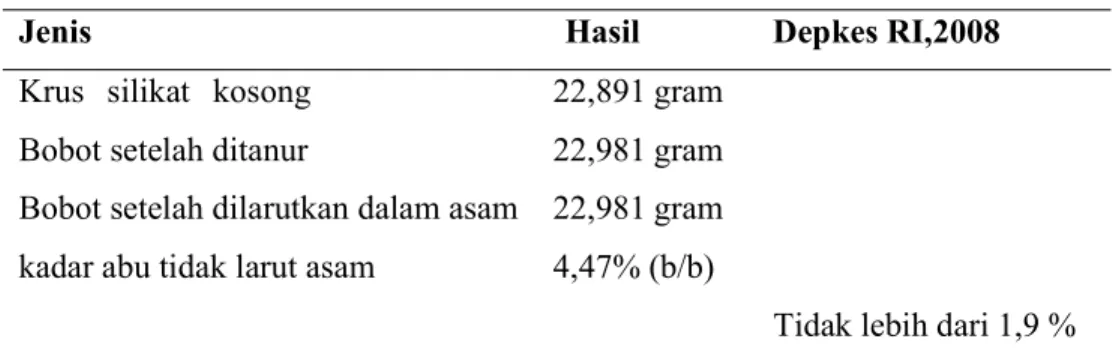
Tabel 4. Hasil penetapan kadar abu tidak larut asam pada ekstrak
Jenis Hasil Depkes RI,2008
Krus silikat kosong Bobot setelah ditanur
Bobot setelah dilarutkan dalam asam kadar abu tidak larut asam
22,891 gram 22,981 gram 22,981 gram 4,47% (b/b)
Tidak lebih dari 1,9 % Tujuan penetapan kadar abu tidak larut asam adalah untuk menentukan tingkat kebersihan dalam proses pengolahan suatu produk. Abu tidak larut asam dicerminkan oleh adanya kontaminasi mineral atau logam yang tidak larut asam dalam suatu produk.
Kadar tidak larut dalam asam biasanya mengandung silikat yang berasal dari tanah liat atau pasir dan unsur logam misalnya Ag, Pb atau Hg (Depkes RI 2008).
Hasil yang diperoleh dari penetapan kadar abu tidak larut asam adalah 4,47%.
Dengan hasil yang tinggi tersebut, ada kemungkinan besar kontaminasi berasal dari tanah yang terbawa pada saat proses panen dan proses pencucian yang kurang bersih (Depkes RI 2008).
6. Berat jenis
Tabel 5. Hasil penetapan bobot jenis pada ekstrak
Jenis Hasil
Berat Piknometer kosong 24,391 gram
Berat Piknometer dengan air 49,807 gram Berat Piknometer dengan sampel 52,165 gram
Berat jenis 1,047 (b/b)
Tujuannya adalah memberikan batasan tentang besarnya masa persatuan volume yang merupakan parameter khusus ekstrak cair sampai ekstrak pekat (kental) yang masih dapat dituang, bobot jenis juga terkait dengan kemurnian dari ekstrak dan kontaminasi.
Hasil bobot jenis yang diperoleh adalah 1,047 b/v.
7. Cemaran logam berat
Tabel 6. Hasil penetapan cemaran logam berat pada ekstrak
Jenis Hasil SNI,2009
Logam Pb (μg/ml) 2,53 ppm < 10.000 ppm
Logam Cd (μg/ml) 0,075 ppm < 10.000 ppm
Penggunaan AAS pada penetapan cemaran logam berat dipilih karena dapat mengetahui tingkat kandungan logam dalam konsentrasi rendah. Prinsip kerja AAS adalah metode analisis untuk menentukan unsur-unsur logam secara kualitatif dan kuantitatif dalam jumlah yang sangat kecil (dalam ppm) berdasarkan serapan atau absorbs radiasi oleh atom bebasnya.
Tujuan penetapan cemaran logam berat adalah untuk mengetahui kandungan logam berat dalam suatu ekstrak, sehingga dapat memberikan jaminan bahwa ekstrak tidak mengandung logam berat tertentu (Pb, Cd) melebihi batas yang telah ditetapkan karena berbahaya bagi kesehatan. Dari hasil penelitian ini dapat disimpulkan untuk cemaran logam berat masih memenuhi syarat standar mutu ekstrak
D. Penapisan Fitokimia
Hasil pemeriksaan penapisan fitokimia esktrak etanol 70% dan aseton positif terbentuknya endapan menggumpal putih pada pereaksi Mayer dan endapan warna
merah pada pereaksi Dragendorff, hal tersebut terjadi karena adanya reaksi penggantian ligan. Alkaloid yang memiliki atom nitrogen yang mempunyai pasangan elektron bebas dapat mengganti ion iodo dalam pereaksi-pereaksi tersebut (Sangi dkk. 2008). Hasil penapisan fitokimia ekstrak rimpang jahe putih dapat dilihat pada Tabel 3.
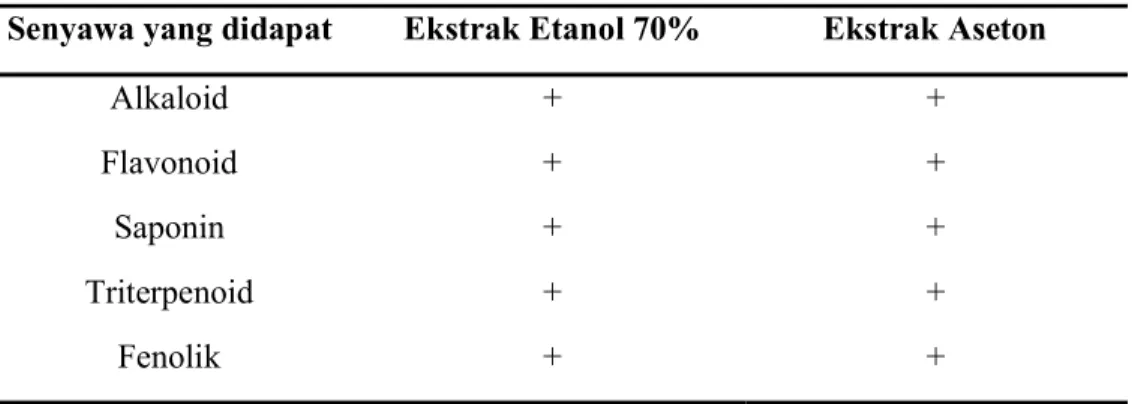
Tabel 3. Hasil Penapisan Fitkomia Ekstrak Rimpang Jahe Putih
Keterangan :
+ : Mengandung senyawa yang diidentifikasi - : tidak mengandung senyawa yang diidentifikasi
Hasil pemeriksaan penapisan fitokimia esktrak etanol 70% dan aseton positif terbentuknya endapan menggumpal putih pada pereaksi Mayer dan endapan warna merah pada pereaksi Dragendorff, hal tersebut terjadi karena adanya reaksi penggantian ligan. Alkaloid yang memiliki atom nitrogen yang mempunyai pasangan elektron bebas dapat mengganti ion iodo dalam pereaksi-pereaksi tersebut (Sangi dkk. 2008).
Flavonoid terutama berupa senyawa yang larut dalam air dan senyawa aktifnya dapat diekstraksi dengan etanol 70% (Harborne 1987). Hasil positif pemeriksaan penapisan ekstrak etanol 70% dan aseton ditunjukkan dengan terbentuknya warna kuning- merah amil alkohol.
Hasil pemeriksaan penapisan saponin menunjukkan positif dengan adanya busa pada sampel. Hal tersebut terjadi karena saponin memiliki gugus polar dan non polar yang akan membentuk misel.
Uji yang banyak digunakan untuk mengetahui kandungan triterpenoid dan steroid ialah reaksi Liberman-Buchard (anhidrat asetat- H2SO4 pekat). Penapisan ekstrak etanol 70% dan aseton rimpang jahe putih menunjukan hasil positif pada uji teriterpenoid dengan adanya cincin ungu sedangkan pada uji steroid tidak menunjukan terbentuknya cincin biru kehijauan (Harborne 1987).
Pemeriksaan fenolik dilakukan dengan penambahan FeCl3. Perubahan warna ini terjadi ketika penambahan FeCI3 yang bereaksi dengan salah satu gugus hidroksil yang
Senyawa yang didapat Ekstrak Etanol 70% Ekstrak Aseton
Alkaloid + +
Flavonoid + +
Saponin + +
Triterpenoid + +
Fenolik + +
ada pada senyawa fenol (Depkes RI 2009). Dari hasil pengujian sampel ekstrak rimpang jahe putih menghasilkan warna biru kehitaman yang menunjukan mengandung senyawa Fenolik
Hasil penapisan fitokimia kedua pelarut menunjukan hasil positif yang sama, hal ini dibenarkan melalui penelitian Sunaryo dkk. (2017) bahwa pengujian fitokimia rimpang jahe putih terdapat alkaloid, flavonoid dan tanin.
E. Penentuan kadar total fenolik
Pada penentuan kadar total fenolik dilakukan dengan menggunakan reagen Folin-Ciocalteau. Reagen Folin-Ciocalteau digunakan karena senyawa fenolik dapat beraksi dengan folin membentuk larutan berwarna yang dapat diukur absorbansinya.
Prinsip metode Folin-Ciocalteau adalah terbentuknya senyawa kompleks yang dapat diukur pada panjang gelombang 765 nm. Pereaksi ini mengoksidasi fenoloat (garam alkali) atau gugus fenolik-hidroksi mereduksi asam heteropoli (fosfomolibdat- fosfotungstat) yang ada pada Folin Ciocalteau menjadi suatu kompleks molibdenum- tungsten, senyawa fenolik bereaksi dengan Folin-Cioacalteau hanya dalam suasana basa agar terjadi disosisi proton pada senyawa fenolik menjadi ion fenolat. Untuk membuat kondisi basa diperlukan Na2CO3 7,5%. Gugus hidroksil yang ada pada senyawa fenolik bereaksi dengan reagen Folin-Ciocalteau membentuk kompleks molibdenum-tungsten berwarna biru yang bisa dideteksi dengan spektrofotometer. Semakin besar konsentrasi senyawa fenolik maka semakin banyak ion fenolat yang akan mereduksi asam heteropoli (fosfomolibdat-fosfotungstat) menjadi kompleks molibdenum-tungsten sehingga warna biru yang dihasilkan akan akan semakin pekat (Alfian dan Susanti 2012).
a. Penentuan Kurva Kalibrasi Asam Galat
Hasil pengukuran absorbansi larutan seri asam galat dapat dilihat pada Tabel 5.
Tabel 5. Hasil Pengukuran Absorbansi Larutan Seri Konsentrasi Asam Galat Konsentrasi (ppm) Absorbansi
20 30 40 50 60
0,333 0,421 0,523 0,616 0,707
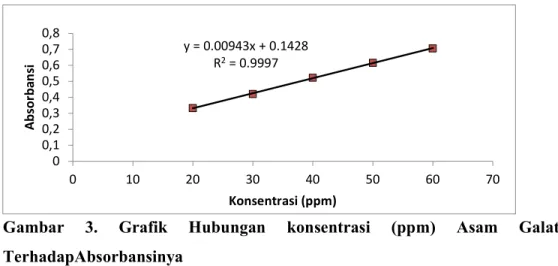
Gambar 3. Grafik Hubungan konsentrasi (ppm) Asam Galat TerhadapAbsorbansinya
Grafik hubungan konsentrasi (ppm) asam galat terhadap absorbansinya dapat dilihat pada Gambar 3. Tujuan adanya grafik tersebut adalah untuk memperoleh persamaan yang membentuk garis lurus sesuai hukum Lambert-Beer.
Berdasarkan Gambar 3 didapatkan persamaan regresi linear y=0,00943x+0,1428 dimana nilai r= 0,9997 yang dibaca menggunakan alat spektrofotometer uv-vis pada panjang gelombang 764,0 nm. Melalui persamaan tersebut selanjutnya dapat digunakan untuk menentukan kadar fenolik total pada ekstrak rimpang jahe putih.
y = 0.00943x + 0.1428 R2= 0.9997
0,10 0,20,3 0,40,5 0,60,7 0,8
0 10 20 30 40 50 60 70
Absorbansi
Konsentrasi (ppm)
b. Penentuan kadar sampel rimpang jahe putih
Gambar 4. Perbandingan Kadar Total Fenolik antara Ekstrak Etanol 70% dengan Ektrak Aseton Rimpang Jahe Putih
Hasil penelitian pada Gambar 4 menunjukkan bahwa ekstrak etanol 70%
rimpang jahe putih memiliki kandungan fenolik total 45,5785 mg GAE/g lebih sedikit dibandingan dengan ekstrak aseton rimpang jahe putih 46,3655 mg GAE/g. Perbedaan kadar fenolik total yang diperoleh dari penelitian ini disebabkan oleh perbedaan polaritas pelarut yang digunakan. Pelarut yang berbeda memiliki polaritas yang berbeda pula. Senyawa fenolik yang terdapat dalam ekstrak seharusnya lebih larut dalam pelarut etanol 70%, dikarenakan pelarut etanol memiliki tingkat kepolaran yang sama dengan senyawa fenolik, sehingga pelarut etanol lebih banyak mengekstrak senyawa fenol dibandingkan pelarut aseton. Selain itu, ekstrak etanol juga lebih efektif dalam melisis dinding sel tumbuhan yang bersifat semipolar yang mengakibatkan senyawa fenolik akan lebih mudah keluar dari sel (Tiwari et al. 2016).
Penentuan kadar fenolik total dilakukan untuk mengetahui jumlah senyawa golongan fenolik yang terdapat dalam sampel. Metode yang digunakan dalam penentuan fenolik total ini adalah metode Folin-Ciocalteau. Prinsip penentuan fenolik total melalui metode ini didasarkan oleh kemampuan senyawa fenolik dalam mereduksi asam fosfomolibdat (H3PMo12O40) atau fosfotungstat (H3PW12O40) yang terdapat pada pereaksi Folin-Ciocalteau dalam kondisi basa, lalu membentuk molibdat yang berwarna biru dan kemudian diukur nilai absorbansinya (Sudjadi 2004). Pembentukan kompleks warna biru menunjukkan jumlah senyawa fenolik yang terdapat dalam sampel. Semakin pekat warna birunya maka semakin banyak pula kandungan senyawa fenolik yang terdapat dalam sampel (Dai dan Mumper 2010). Asam galat digunakan sebagai standar
45,5785 mg
GAE/g 46,3655 mg
GAE/g
0 10 20 30 40 50
Etanol 70% Aseton
Kadar Fenolik Total (mg GAE/g)
Jenis Ekstrak
dalam penentuan fenolik total ini. Hal ini dikarenakan asam galat merupakan senyawa fenolik terbesar yang terdapat dalam daun surian (Chen et al. 2009).
F. Analisis kandungan gingerol dari ekstrak menggunakan GC-MS
Hasil ekstraksi jahe gajah etanol 70% dan aseton dianalisis kandungan gingerolnya menggunakan alat GC-MS. Kromatografi gas merupakan metode analisis, di mana sampel dipisahkan secara fisik menjadi bentuk molekul-molekul yang lebih kecil (hasil pemisahan dapat dilihat berupa kromatogram). Spektrometri massa adalah metode analisis dimana sampel yang ingin dianalisis diubah menjadi ion-ion gasnya.
Massa dari ion-ion tersebut diukur berdasarkan hasil deteksi berupa spektrum massa.
Penggunaan kromatografi gas untuk senyawa-senyawa yang bersifat volatil saja atau senyawa yang harus mengalami derivatisasi terlebih dahulu agar volatil yang bisa dianalisis dengan metode ini (Drozd 1975). Sampel diutamakan harus berbentuk cairan oleh karena itu, pertama senyawa harus diuapkan sehingga membutuhkan pemanasan sebelum masuk kedalam kolom. Oven digunakan untuk memanaskan kolom pada suhu tertentu sehingga mempermudah proses pemisahan komponen sampel. Pada penelitian ini suhu oven dimulai dari 60-210 oC. Proses pemisahan kromatografi gas terjadi didalam kolom melibatkan dua fase yaitu fase gerak dan fase diam. Pada penelitian ini fase geraknya berupa gas helium dan kolom HP Innowax merupakan fase diamnya.
Kolom HP inowax berisi cairan Polyethylene Glycol (PEG). Data disajikan dalam bentuk persen (%) luas area. Hasil kromatogram ekstrak etanol 70% rimpang jahe putih dari 3 replikasi dapat dilihat pada Lampiran 16, Lampiran 17 dan Lampiran 18, sedangkan hasil kromatogram ekstrak aseton rimpang jahe putih dari 3 replikasi dapat dilihat pada Lampiran 19, Lampiran 20 dan Lampiran 21. Hasil analisis senyawa gingerol ekstrak etanol 70% rimpang jahe putih menggunakan GC-MS dapat dilihat pada Tabel 6.
Tabel 6. Hasil Analisis Profil Senyawa Gingerol Ekstrak Etanol 70% Rimpang Jahe Putih
Hasil analisa GC-MS persentase kandungan relatif dari gingerol pada ekstrak etanol 70% rimpang jahe putih dari 3 replikasi adalah 2,60 % ± 1,34, sedangkan hasil analisis senyawa gingerol ekstrak aseton rimpang jahe putih menggunakan GC-MS dapat dilihat pada Tabel 7.
Tabel 7. Hasil Analisis Profil Senyawa Gingerol Ekstrak Aseton Rimpang Jahe Putih
Hasil analisa GC-MS persentase kandungan relatif dari gingerol pada ekstrak rimpang jahe putih dari 3 replikasi adalah 5,94% ± 0,13.
Identifikasi komponen hasil kromatogram GC-MS dilakukan dengan membandingkan pola fragmentasi spektrum massa dari masing-masing puncak kromatogram dengan spektrum massa yang ada pada pustaka Wiley. Dalam suasana asam reaksi berlangsung lambat tapi dengan suhu tinggi reaksi akan berlangsung cepat.
Zingeron merupakan hasil degradasi gingerol akibat suhu tinggi dengan adanya alkali.
Tetapi pada hasil penelitian ini tidak ditemukan adanya senyawa zingeron, hal ini dimungkinkan senyawa gingerol belum berubah menjadi zingeron (Sugiarti et al. 2011).
Analisa spektra massa didasarkan pada nilai Similiarity Indeks (SI), base peak (puncak dasar), dan trend pecahan spektra massa yang dibandingkan dengan spektra dari library yaitu Wiley.
Ekstrak Etanol 70% Rt Kandungan (%) Rata Kandungan Relatif (%) ± SD
Replikasi 1 31,013 4,03
Replikasi 2 31,006 1,36 2,60 ± 1,34
Replikasi 3 30,999 2,42
Ekstrak aseton Rt Kandungan (%) Rata Kandungan relatif (%) ± SD Replikasi 1 32,592 5,84
Replikasi 2 32,599 6,09 5,94 ± 0,13
Replikasi 3 32,606 5,88
Pola fragmentasi gingerol menggunakan teknik ionisasi elektron seperti pada Gambar 5.
Gambar 5. Pola Fragmentasi Gingerol Menggunakan Teknik Ionisasi Elektron (El kareem et al. 2016)
Pola fragmentasi pertama adalah pembentukan ion fragmen [M-H2O-C5H11]+ pada m/z 205. Dengan kehilangan C4H4O maka akan membentuk [M-H2O-C5H11- C4H4O]+ pada m/z 137. Selanjutnya, m/z 91 menunjukkan fragmentasi ion [M-H2O- C5H11-C4H4O-H2O-CO]+ (El kareem et al. 2016). Dengan demikian dapat disimpulkan baik pada ekstrak etanol 70% maupun aseton, gingerol dapat terekstraksi dengan baik.
Berdasarkan persentase kandungan relatifnya, pelarut aseton lebih baik dalam mengekstraksi gingerol dibanding pelarut etanol 70%.
Aseton merupakan pelarut polar aprotik yang mana memiliki kepolaran tinggi karena mampu melarutkkan komponen hidrofilik dan lipofilik senyawa pada tanaman (Tiwari et al. 2016). Tiwari et al. (2016) menyatakan bahwa ekstraksi tanin dan fenolat lebih baik dalam aseton berair daripada di metanol-air. Sedangkan etanol 70% lebih baik dalam menarik senyawa bioaktif seperti flavonoid dibanding etanol murni. Hasil spektrum massa gingerol ekstrak etanol 70% dan ekstrak aseton rimpang jahe putih dapat dilihat pada Tabel 8.
Tabel 8. Identifikasi Spektrum Massa Senyawa Gingerol Dengan Menggunakan GC-MS
Sampel Waktu Retensi
(menit) Bobot Molekul Gingerol (g/mol) Ekstrak etanol 70%
rimpang jahe putih Ekstrak aseton rimpang
jahe putih
31,006
31,040
294,0
294,0
Dari penelitian ini didapatkan hasil identifikasi dengan menggunakan GC-MS pada sample ekstrak etanol 70% rimpang jahe putih menunjukkan massa molekul yang dapat dikategorikan sebagai gingerol, yaitu 294,0 m/e, sedangkan pada sampel ekstrak aseton rimpang jahe putih menunjukan massa molekul sebesar 294,0 m/e. Diagram fragmentasi senyawa gingerol dapat dilihat pada Lampiran 22 dan Lampiran 23.
Garis tegak lurus menunjukkan besarnya arus listrik yang diterima oleh alat pencatat arus yang berarti banyaknya ion datang ke detektor. Tiap garis menunjukkan fragmen atau pecahan berbeda yang dihasilkan ketika ion molekuler (dalam diagram ini pada m/e = 294,0) pecah. Ion-ion molekuler yang tidak stabil akan terpecah menjadi bagian-bagian yang lebih kecil, yakni berupa radikal bebas. Garis paling tinggi pada diagram (dalam diagram ini pada m/e = 137,1) disebut “puncak dasar”.
BAB 5. KESIMPULAN A. Simpulan
Berdasarkan hasil yang diperoleh pada penelitian ini, dapat disimpulkan bahwa ekstrak etanol 70% jahe gajah memenuhi persyaratan dalam pengujian parameter non spesifik, meliputi penetapan kadar air, cemaran logam berat (Pb dan Cd), susut pengeringan, dan bobot jenis. Kandungan gingerol pada ekstrak rimpang jahe putih menggunakan analisis GC-MS menunjukkan bahwa baik ekstrak etanol 70% maupun ekstrak aseton rimpang jahe putih memiliki kandungan gingerol dengan persentase kadar relatifnya masing – masing sebesar 2,60% ± 1,34 dan 5,94% ± 0,13. Kadar fenolik total ekstrak etanol 70% rimpang jahe putih sebesar 45,5788 ± 7,61 mgGAE/g sedangkan ekstrak aseton rimpang jahe putih sebesar 46,3655 ± 8,77 mgGAE/g.
DAFTAR PUSTAKA
Akhani, S. P., Vishwakarma, S. L., & Goyal, R. K. 2004. Anti-diabetic activity of Zingiber officinale in streptozotocin-induced type I diabetic rats. Journal : Pharmacy and Pharmacology. 56(1). Hlm.101–105.
Alfian, R., & Susanti, H. 2012. Penetapan Kadar Fenolik Total Ekstrak Metanol Kelopak Bunga Rosella Merah (Hibiscus sabdariffa Linn) Dengan Variasi Tempat Tumbuh Secara Spektrofotometri. Jurnal Ilmiah Kefarmasian, Yogyakarta. Hlm.
73-80.
Bhandari, U., Kanojia, R., & Pillai, K. K. 2005. Effect of ethanolic extract of Zingiber officinale on dyslipidaemia in diabetic rats. Journal of Ethnopharmacology.
Faculty of Pharmacy, Hamdard University. India. Hlm. 227-230.
Chen, H. M., Wu, Y. C., Chia, Y. C., Chang, F. R., Hsu, H. K., Hsieh, Y. C. Yuan, S. S.
2009. Gallic acid, a major component of Toona sinensis leaf extracts, contains a ROS-mediated anti-cancer activity in human prostate cancer cells. Cancer Letters, Taiwan. Hlm. 161–171.
Chrubasik, S., Pittler, M. H., & Roufogalis, B. D. 2005. Zingiberis rhizoma: A comprehensive review on the ginger effect and efficacy profiles. Phytomedicine.
Hlm. 684-701.
Dachriyanus. 2004. Analisis Struktur Senyawa Organik Secara Spektroskopi. Lembaga Pengembangan Teknologi Informasi dan Komunikasi (LPTIK) Universitas Andalas, Padang. Hlm. 3-13, 41-64.
Dai, J., & Mumper, R. J. 2010. Plant phenolics: Extraction, analysis and their antioxidant and anticancer properties. Molecules, USA. Hlm. 7313-7352.
Departemen Kesehatan RI. 1995. Farmakope Herbal. Edisi I. Direktorat Jendral Pengawasan Obat dan Makanan, Jakarta.
Departemen Kesehatan RI. 2000. Inventaris Tanaman Obat Indonesia. Jilid 1. Badan Penelitian Dan Pengembangan Kesehatan, Departemen Kesehatan &
Kesejahteraan Sosial RI, Jakarta.
Departemen Kesehatan RI. 2009. Farmakope Herbal Indonesia. Edisi 1. Menteri Kesehatan Republik Indonesia, Jakarta. Hlm. 32-35.
Drozd, J. 1975. Chemical derivatization in gas chromatography. Journal of Chromatography A. Hlm. 303-356.
Dwi Oktora, R., & Sudaryanto, Y. 2007. Ekstraksi Oleoresin Dari Jahe. Widya Teknik, Surabaya. Hlm. 131–141.
El Kareem Abd, S. M., Abd El Fattah Rabbih, M., & Taha Mohamed Selim, E. 2016.
Identification of zingiber components by gas chromatograph/mass spectrometer and semi-empirical calculations. International Journal of Physical Research, Egypt. Hlm. 20-26.
Farrell, K. T. 1999. Spices, Condiments and Seasonings. Aspen Publisher, New York.
Hlm. 103.
Gholib, D. 2008. Uji Daya Hambat Ektrak Etanol Jahe Merah (Zingiber officinale var.
Rubrum) Dan Jahe Putih (Zingiber officinale var. Amarum) Terhadap Trichophyton mentagrophytes Dan Cryptococcus neoformans. Seminar Nasional, Teknologi Peternakan Dan Veteriner. Pusat Penelitian dan Pengembangan Peternakan, Bogor. Hlm. 827-830.
Govindarajan, V. S. 1983. Ginger chemistry, technology, and quality evaluation: Part 1.
C R C Press, India. Hlm. 1-87.
Hapsoh, Y. H., & Julianti, E. 2008. Budidaya dan teknologi pascapanen jahe. USU- Press, Medan.
Harborne, J. B. 1987. Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan. Penerbit ITB, Bandung. Hlm. 6-9.
Hargono Pradhita, Fitra Aulia, M. P. 2013. Pemisahan Gingerol Dari Rimpang Jahe Segar Melalui Proses Ekstraksi Secara Batch. Jurnal Momentum UNWAHAS, 9(2).
Fakultas Teknik Universitas Diponegoro, Semarang. Hlm. 16-21.
Koswara, S. 1995. Jahe dan hasil olahannya. Pustaka Sinar Harapan, Jakarta.
Maged, R., Nordin, N., & Abdulla, M. 2013. Anti-inflammatory effects of zingiber officinale roscoe involve suppression of nitric oxide and prostaglandin E2 production. Zanco Journal of Medical Sciences. ISSN 1995-5588. Hlm. 349-356.
Mishra, P. 2009. Isolation, spectroscopic characterization and molecular modeling studies of mixture of Curcuma longa, ginger and seeds of fenugreek. International Journal of PharmTech Research. ISSN 0974-4304. Hlm. 79-95.
Paimin, F. B., & Murhananto. 1991. Budidaya, pengolahan, perdagangan Jahe. Penebar Swadaya, Jakarta.
Pubchem. Gingerol National Center for Biotechnology Information. Diambil dari:
www.pubchem.ncbi.nlm.nih.gov/compound/Gingerol. Diakses 29 Juli 2019.
Purseglove, J. W., Brown, E. G., Green, C. L., & Robbins, S. R. J. 1981. Spices Vol. 2.
Longman Group Ltd, New York.
Ravindran, K., & Babu, N. 2005. Zingiber, The Genus. CRC PRESS, London. Hlm. 1, 87, 181.
Sangi, M., Runtuwene, M. R. J., & Simbala, H. E. I. 2008. Analisis Fitokimia Tumbuhan Obat Di Kabupaten Minahasa Utara. 1(1), Chem. Prog. Vol. 1, Manado.
Hlm 47–53.
Sari, R. P., & Rahayuningsih, H. M. 2014. Pengaruh Pemberian Jahe Merah (Zingiber Officinale Var Rubrum) terhadap Kadar Kolesterol Total Wanita Dislipidemia.
Journal of Nutrition College, Semarang. Hlm. 798-806.
Shahidi, F., & Naczk, M. 1995. Food phenolics : sources, chemistry, effects, applications. Lancaster, Pa.: Technomic Pub. Co. UK. Hlm. 243.
Sudarmadji, Haryono, & Suhardi. 1989. Analisa bahan makanan dan pertanian.
Liberty, Yogyakarta.
Sudjadi. 2004. Analisis obat dan makanan / disusun oleh Dr. Sudjadi, Abdul Rohman (A. Rohman, Ed.). Yayasan Farmasi Indonesia, Pustaka Pelajar, Yogyakarta.
Sugiarti, L., Suwandi, A., & Syawaalz, A. 2011. Gingerol Pada Rimpang Jahe Merah
(Zingiber officinale, Roscoe) Dengan Metode Perkolasi Termodifikasi Basa.
Jurnal Sains Natural, Bogor. Hlm. 156-165.
Sunaryo, H., Rahmania, R. A., Dwitiyanti, D., & Siska, S. 2017. Aktivitas Antioksidan Kombinasi Ekstrak Jahe Gajah (Zingiber officinale Rosc.) dan Zink Berdasarkan Pengukuran MDA, SOD dan Katalase pada Mencit Hiperkolesterolemia dan Hiperglikemia dengan Penginduksi Streptozotosin. Jurnal Ilmu Kefarmasian Indonesia. Universitas Muhammadiyah Prof. DR. Hamka, Jakarta. Hlm. 187-193.
Tiwari, Prashant, Kumar, Bimlesh, Kaur, Mandeep, Kaur, Gurpreet, Kaur, H. 2016.
International Journal of Biological Chemistry Research Article Comparison of Different Solvents for Phytochemical Extraction Potential from Datura metel Plant Leaves Dixon Dhawan and Jeena Gupta. International Journal of Biological Chemistry, India. Hlm. 17–22.
Uhl, S. R. 2000. Handbook of spices, seasonings, and flavorings. Lancaster: Technomic Publishing Company, Inc.
Usman, Y. O., Abechi, S. E., Benedict, O. O., Victor, O., Udiba, U. U., & Ukwuije, N.
O. 2013. Effect of solvents on [ 6 ] -Gingerol Content of Ginger Rhizome and Alligator Pepper Seed. Annals of Biological Research, Kaduna. Hlm. 7–13.
World Health Organization. 1999. WHO monographs on selected medicinal plants.
Essential Medicines and Health Products Information Portal, Geneva. Hlm. 277.