LAPORAN PRAKTIKUM PROSES TEKNIK KIMIA II DISTILASI
Diajukan untuk Memenuhi Laporan Praktikum Proses Teknik Kimia II
Disusun Oleh : Kelompok 6 (A4)
Yayang Nadrakhilla NIM. 200140117 Haqqul Yakinnas NIM. 200140121 Nelly Felania Harahap NIM. 200140126
Fitriani NIM. 200140153
LABORATORIUM TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS MALIKUSSALEH
LHOKSEUMAWE
2022
ABSTRAK
Distilasi merupakan metode operasi pemisahan suatu campuran homogen (cairan- cairan saling melarutkan), berdasarkan perbedaan titik didih atau perbedaan tekanan uap murni (masing-masing komponen yang terdapat dalam campuran) dengan menggunakan sejumlah panas sebagai tenaga pemisah. Pada percobaan distilasi kali ini dilakukan pemisahan pada etanol dan air. Proses pemisahan etanol dengan air dilakukan dengan menggunakan larutan berkonsentrasi 55%, 65%, 75%, 85%, 95%. Untuk setiap konsentrasi proses distilasi dilakukan variasi waktu yang berbeda yaitu 4 menit, 8 menit, dan 12 menit. Berdasarkan pengujian densitas diperoleh densitas etanol 55% yaitu 0.8999 gr/ml, densitas etanol 65%
yaitu 0,8764 gr/ml, densitas etanol 75% yaitu 0,8537, densitas etanol 85% yaitu 0,8231 dan densitas etanol 95% yaitu 0,7939 gr/ml. Pada waktu distilasi selama 4 menit diperoleh refluk seberat 312,6786 gram dan distilat seberat 31,7710 gram.
Pada waktu distilasi selama 8 menit diperoleh refluk seberat 293,1103 gram dan distilat seberat 51,3393 gram. Pada waktu distilasi selama 12 menit diperoleh refluk seberat 276,4250 gram dan distilat seberat 68,0246 gram. Pada percobaan ini didapatkan % konversi untuk run I sebanyak 9,22% pada run II sebanyak 14,90% dan pada run III sebanyak 19,74%. Semakin lama waktu proses distilasi maka semakin sedikit massa refluks dan semakin lama waktu proses distilasi maka volume distilat akan semakin besar.
Kata Kunci: Distilat, Etanol, Homogen, Kondensat, dan Konsentrasi.
BAB I
PENDAHULUAN
1.1 Judul Praktikum : Distilasi
1.2 Tanggal Praktikum : 21 Oktober 2022 1.3 Pelaksana Praktikum : Kelompok VI (A4)
1. Yayang Nadrakhilla NIM. 200140117 2. Haqqul Yaqinnas NIM. 200140121 3. Nelly Felania Harahap NIM. 200140126 4. Fitriani NIM. 200140153 1.4 Tujuan Praktikum : 1. Dapat mengkaji pengaruh perbandingan
refluk (R) terhadap komposisi etanol dalam destilat selama waktu operasi lima menit.
2. Dapat membuat laporan praktikum secara tertulis dengan baik dan benar.
BAB II
TINJAUAN PUSTAKA
2.1 Sejarah Distilasi
Distilasi pertama kali ditemukan oleh kimiawan yunani sekitar abad pertama masehi yang akhirnya perkembangannya dipicu terutama oleh tingginya permintaan akan spiritus Hypathia dan Alexandria dipercaya telah menemukan rangkaian alat untuk distilasi dan zosimus dari Alexandria-lah yang telah berhasil menggambarkan secara akurat tentang proses distilasi pada sekitar abad ke-4.
Bentuk modern distilasi pertama kali ditemukan oleh ahli-ahli kimia islam pada masa kekhalifahan Abbasiyah, terutama oleh Al-Raazi pada pemisahan alkohol menjadi senyawa yang relatif murni melalui alat alembik, bahkan desain ini menjadi semacam inspirasi yang memungkinkan rancangan distilasi skala mikro.
Salah satu penerapan terpenting dan metode distilasi adalah memisahkan minyak mentah menjadi bagian-bagian untuk penggunaan khusus seperti untuk transportasi, pembangkit listrik, pemanas, dan lain-lain. Udara distilasi menjadi komponen-komponen seperti oksigen untuk penggunaan medis dan helium untuk pengisi balon. Distilasi telah digunakan sejak lama untuk pemekatan alkohol dengan penerapan panas terhadap larutan hasil fermentasi untuk menghasilkan minuman suling B.
Beberapa pendapat para ahli mengenai pengertian distilasi adalah sebagai berikut :
Distilasi adalah suatu proses pemisahan dua atau lebih komponen dalam suatu campuran berdasarkan perbedaan titik didih dari masing-masing komponen dengan menggunakan panas sebagai tenaga pemisah (Mc.Cabe, 1999).
Distilasi adalah suatu metode operasi yang digunakan pada proses pemisahan suatu komponen dari campurannya dengan menggunakan panas sebagai tenaga pemisah berdasarkan perbedaan titik didih masing-masing komponennya. Proses pemisahan secara distilasi terdiri dari tiga langkah dasar, yaitu:
a. Proses penguapan atau penambahan panas dalam larutan yang dipisahkan b. Proses pembentukan fase seimbang
c. Proses pemisahan kedua fase seimbang.
(GG.Brown, 1987).
2.2 Distilasi
Distilasi merupakan sebuah proses campuran dua atau lebih zat liquid atau vapor dipisahkan menjadi komponen fraksi yang murni, dengan pengaplikasian dari perpindahan massa dan panas. Metode pemisahan suatu campuran homogen (cairan saling melarutkan), berdasarkan perbedaan titik didih atau perbedaan tekanan uap murni (masing-masing komponen yang terdapat dalam campuran) dengan menggunakan sejumlah panas sebagai tenaga pemisah atau disebut dengan energy separating agent (ESA) (Leily Nurul Komariah, 2009).
Distilasi termasuk proses pemisahan menurut dasar operasi difusi. Secara difusi, proses pemisahan terjadi karena adanya perpindahan massa secara lawan arah, dari fasa uap ke fasa cair atau sebaliknya, sebagai akibat adanya beda potensial diantara dua fasa yang saling kontak. Sehingga pada suatu saat pada suhu dari tekanan tertentu, sistem berada dalam keseimbangan dalam bentuk lain, pengertian distilasi dinyatakan sebagai berikut:
XAD XAWdan
XBD XBW……….(2.1) Keterangan:XA,XB : komposisi komponen A,B
A,B : komponen yang mempunyai tekanan uap tinggi rendah D : hasil puncak,distilat
W : hasil bawah,residu
Pada pemisahan secara distilasi, fasa uap akan segera terbentuk setelah campuran di panaskan. Uap dan sisa cairanya di biarkan saling kontak sedemikian hingga pada saat semua komponen terjadi dalam campuran akan terdistilasi dalam kedua fasa membentuk keseimbangan. Setelah keseimbangan di capai uap segera dipisahkan dari cairanya, kemudian dikondensasikan membentuk distilat Pada beberapa campuran komponen, untuk komposisi, suhu dan tekanan tertentu tidak
memenuhi kecenderungan tersebut, artinya jika campuran tersebut dididihkan maka komposisi fase uapnya akan memiliki komposisi yang sama dengan fase cairnya, keadaan ini disebut kondisi azeotrop, sehingga campuran pada kondisi ini tidak dapat dipisahkan dengan cara distilasi biasa (Abbassato, 2007).
Distilasi air merupakan salah satu cara untuk memisahkan minyak atsiri dari dalam bahan. Pada metode ini, bahan yang didistilasi akan kontak langsung dengan air mendidih Sebelum rimpang jeringau didistilasi, rimpang terlebih dahulu diubah dalam bentuk chips untuk mempermudah dalam proses distilasi.
Permintaan akan minyak jeringau ini sangat luas yaitu dari bidang industri makanan, farmasi, kecantikan maupun industri parfum (Adityo kurniawan, 2008).
Distilasi merupakan metode yang paling populer, digunakan secara luas, dan cost-effective untuk memproduksi minyak esensial di seluruh dunia. Distilasi tanaman aromatik secara sederhana menggunakan penguapan atau membebaskan minyak dari membran sel tanaman dengan adanya kelembaban, dengan menerapkan suhu yang tinggi dan kemudian mendinginkan campuran uap untuk memisahkan minyak dari air berdasarkan ketidak bercampuran dan densitas minyak esensial dengan air (Husnul Khatimah, 2016).
Distilasi sederhana atau destilasi biasa adalah teknik pemisahan kimia untuk memisahkan dua atau lebih komponen yang memiliki perbedaan titik didih yang jauh. Suatu campuran dapat dipisahkan dengan distilasi biasa ini untuk memperoleh senyawa murni. Senyawa yang terdapat dalam campuran akan menguap saat mencapai titik didih masing-masing (Nur Ihda Farikhatin Nisa, 2019).
Untuk memisahkan alkohol dari campuran dan meningkatkan kadar alkohol, alkohol perlu didestilasi. Maksud dan proses distilasi adalah untuk memisahkan etanol dari campuran etanol air. Untuk larutan yang terdiri dari komponen-komponen yang berbeda nyata suhu didihnya, distilasi merupakan cara yang paling mudah dioperasikan dan juga merupakan cara pemisahan yang secara thermal adalah efisien. Pada tekanan atmosfir, air mendidih pada 100ºC dan etanol mendidih pada sekitar 78ºC. Perbedaan dalam titik didih inilah yang memungkinkan pemisahan campuran etanol air. Prinsip: jika larutan campuran
etanol air dipanaskan, maka akan lebih banyak molekul etanol menguap dari pada air. Jika uap-uap ini didinginkan (dikondensasi), maka konsentrasi etanol dalam cairan yang dikondensasikan itu akan lebih tinggi dari pada dalam larutan aslinya.
Jika kondensat ini dipanaskan lagi dan kemudian dikondensasikan, maka konsentrasi etanol akan lebih tinggi lagi. Proses ini bisa diulangi terus, sampai sebagian besar dari etanol dikonsentrasikan dalam suatu fasa. Namun hal ini ada batasnya. Pada larutan 96% etanol, didapatkan suatu campuran dengan titik didih yang sama (azeotrop). Pada keadaan ini, jika larutan 96% alkohol ini dipanaskan, maka rasio molekul air dan etanol dalam kondensat akan tetap konstan sama. Jika dengan cara destilasi ini, alkohol tidak bisa lebih pekat dari 96 %. Pemisahan dan pemurnian senyawa organik dari suatu campuran senyawa dilakukan dengan beberapa cara sesuai dengan karakter sampel. Distilasi sederhana, pemisahan ini dilakukan bedasarkan perbedan titik didih yang besar atau untuk memisahkan zat cair dari campurannya yang yang berwujud padat. Distilasi bertingkat, pemisahan ini dilakukan berdasarkan perbedaan titik didih yang berdekatan. Distilasi uap, dilakukan untuk memisahkan suatu zat yang sukar bercampur dengan air dan memiliki tekanan uap yang relative tinggi atau memiliki Mr yang tinggi (Auliani,2011).
Distilasi merupakan istilah lain dari penyulingan, yakni proses pemanasan suatu bahan pada berbagai temperatur, tanpa kontak dengan udara luar untuk memperoleh hasil tertentu. Hal- hal yang mempengaruhi proses distilasi adalah jenis larutan, volume larutan, suhu, waktu distilasi dan tekanan. Penyulingan adalah perubahan bahan dari bentuk cair ke bentuk gas melalui proses pemanasan cairan tersebut, dan kemudian mendinginkan gas hasil pemanasan, untuk selanjutnya mengumpulkan tetesan cairan yang mengembun. Hasil dari proses distilasi disebut dengan distilat yaitu larutan hasil distilasi yang sudah terkondisi yang berada di penampung yang telah tersedia (Cammack, 2006).
2.3 Macam-Macam Distilasi
Pada distilasi juga memiliki macam-macam jenis distilasi, yakni:
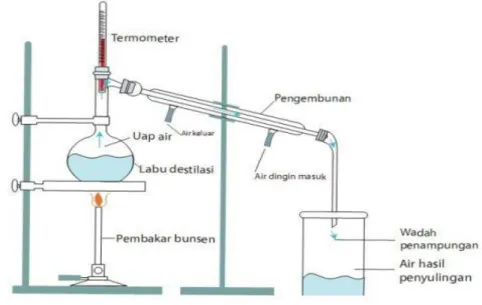
2.3.1 Distilasi Sederhana
Gambar 2.1 Distilasi Sederhana
Jenis distilasi yang pertama adalah destilasi biasa ataupun distilasi sederhana. Jenis distilasi sederhana umumnya dengan cara menaikan suhu, sehingga tekanan uapnya ada diluar cairan ataupun tekanan atmosfer ataupun titik didih normal. Dalam distilasi biasa ini, dasar pemisahannya merupakan perbedaan titik didihnya yang jauh ataupun salah satu komponennya bersifat volatil. Jika campuran dipanaskan, komponen yang mempunyai titik didih yang lebih rendah juga akan menguap lebih dulu. Disamping perbedaan titik didih tersebut, ada pula perbedaan kevolatilan yakni kecendrungan suatu substansi menjadi gas. Proses distilasi ini dapat dilakukan terhadap tekanan atmosfer. Proses distilasi tersebut juga digunakan guna memisahkan antara campuran air dengan alkohol (Nur Ihda Farikhatin Nisa, 2019).
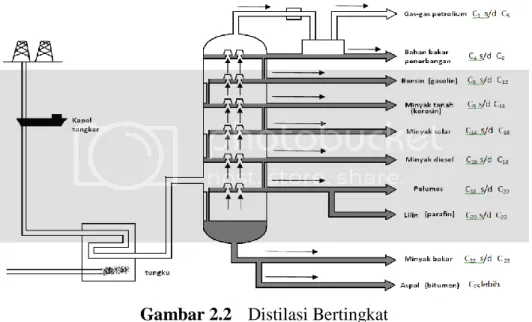
2.3.2 Distilasi Bertingkat
Gambar 2.2 Distilasi Bertingkat
Berikutnya adalah fungsi distilasi fraksionasi ataupun distilasi bertingkat/
distilasi berfraksi. Jenis distilasi ini nantinya akan memisahkan komponen cair, sebanyak dua ataupun lebih dari larutannya menurut perbedaan titik didihnya.
Proses distilasi ini juga sapat digunakan sebagai campuran dengan beda titik didih yang kurang 20°C serta bekerja di tekanan atmosfer ataupun dengan tekanan rendah. Teknis destilasi tersebut dapat di aplikasikan pada industri minyak mentah yakni untuk memisahkan antara komponen yang berada pada minyak mentah.
Beda antara distilasi fraksionasi dengan distilasi biasa ialah ada kolom fraksionasi. Di kolom tersebut akan terjadi pemanasan yang bertahap pada suhu yang beda pula pada setiap platnya. Proses pemanasan yang beda bertujuan memurnikan distilat lebih dari plat yang ada dibawahnya (Leily Nurul Komariah, 2009).
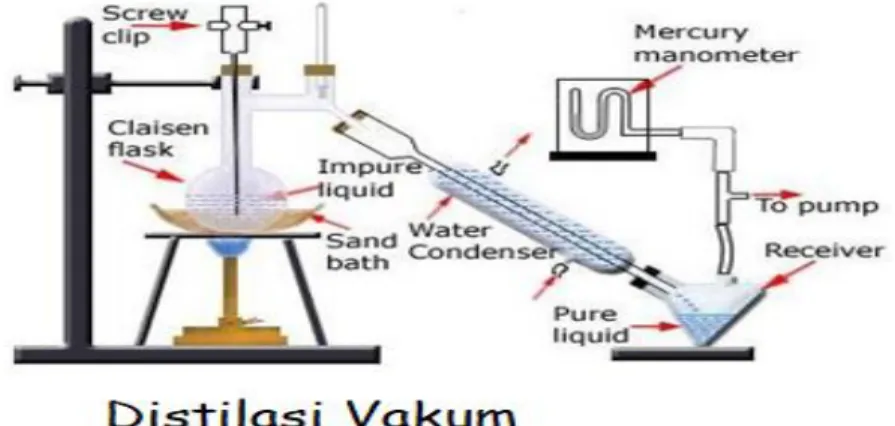
2.3.3 Distilasi Vakum
Berikutnya ada distilasi vakum yang umumnya dipakai jika senyawa yang mau didistilasi tak stabil terhadap pengertian dapat terdekomposisi sebelum atau mendekati titik didihnya maupun campuran bertitik didih melebihi 150°C. Jenis distilasi ini digunakan tak dapat digunakan oleh pelarut pada titik didih yang lebih rendah jika kondensornya memakai air dingin disebabkan komponen yang
menguap tak dapat dikondensasi air. Cara mengurangi tekanan tersebut digunakan oleh pompa vakum ataupun aspirator yang berfungsi penurun tekanan dalam sistem distilasi diatas.
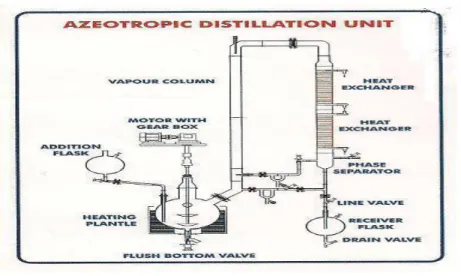
Gambar 2.3 Distilasi Vakum 2.3.4 Distilasi Azeotrop
Gambar 2.4 Distilasi Azeotrop
Azeotrop adalah campuran dari dua atau lebih komponen yang memiliki titik didih yang konstan. Azeotrop dapat menjadi gangguan yang menyebabkan hasil distilasi menjadi tidak maksimal. Komposisi dari azeotrop tetap konstan dalam pemberian atau penambahan tekanan, akan tetapi ketika tekanan total berubah, kedua titik didih dan komposisi dari azeotrop berubah (Leily Nurul Komariah, 2009).
2.4 Hukum Menghitung Distilasi
Berdasarkan Hukum Raoults dan Hukum Dalton, komposisi zat volatile didalam fasa uapnya akan lebih banyak dibandingkan pada fasa cairnya, tergantung pada harga sifat volatilitas relative (αAB) suatu komponen terhadap komponen lain. Hubungan kesetimbangan campuran biner system Etanol (A) –Air (B) pada kondisi tekanan total PT= 101,32 k pada temperatur standar, campuran Etanol-Air (Adityo kurniawan, 2008).
2.5 Etanol
Etanol disebut juga etil alkohol atau alkohol saja, adalah sejenis cairan yang mudah menguap, mudah terbakar, tak berwarna, dan merupakan alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Senyawa ini merupakan obat psikoaktif dan dapat ditemukan pada minuman beralkohol dan termometer modern. Etanol adalah salah satu obat rekreasi yang paling tua. Etanol termasuk ke dalam alkohol rantai tunggal, dengan rumus kimia C2H5OH dan rumus empiris C2H6O. Etanol merupakan isomer konstitusional dari dimetil eter.
Etanol sering disingkat gugus etil (C2H5). Fermentasi gula menjadi etanol merupakan salah satu reaksi organik paling awal yang pernah dilakukan manusia.
Efek dari konsumsi etanol yang memabukkan juga telah diketahui sejak dulu.
Pada zaman modern, etanol yang ditujukan untuk kegunaan industri sering kali dihasilkan dari etilena.
Dalam dunia oil and gas indonesia, etanol dimanfaatkan karena memiliki nilai oktan yang cukup tinggi dan dapat diperoleh dengan mudah melalui fermentasi dengan proses pemurnian menggunakan distilasi. Proses biasanya menggunakan jamur, yeast, dan bakteri kerena memiliki selektivitas yang tinggi (Kunnakorn, 2003).
Etanol banyak digunakan sebagai pelarut berbagai bahan-bahan kimia yang ditujukan untuk konsumsi dan kegunaan manusia. Contohnya adalah pada parfum, perasa, pewarna makanan, dan obat-obatan. Dalam kimia, etanol adalah pelarut yang penting sekaligus sebagai stok umpan untuk sintesis senyawa kimia lainnya. Dalam sejarahnya etanol telah lama digunakan sebagai bahan bakar (Nur Ihda Farikhatin Nisa, 2019).
2.6 Komponen Alat Distilasi 1. Tabung Reaktor
Tabung reaktor berfungsi sebagai wadah atau tempat pemanasan bahan baku (oli bekas). Tabung reaktor berbentuk silinder yang mempunyai tutup yang di cekitkan dengan menggunakan baut sehingga dapat dibuka dan ditutup.
2. Kodensor (pendingin)
Kondensor berfungsi untuk mengubah seluruh gas menjadi fase cair. Air disirkulasikan kedalam tabung kondensor sebagai media pendinginan.
3. Pipa Penyalur
Pipa penyalur yang dibuat berbentuk spiral ini berfungsi untuk menghubungkan dan menyalurkan gas dari tabung reaktor ke kondensor.
4. Thermometer
Termometer digunakan untuk mengamati suhu dalam proses destilasi sehingga suhu dapat dikontrol sesuai dengan suhu yang diinginkan untuk memperoleh destilat murni.
5. Erlenmeyer
Erlenmeyer sebagai wadah untuk menampung destilat yang diperoleh dari proses destilasi.
6. Pemanas
Pemanas berguna untuk memanaskan sampel yang terdapat pada labu alas bulat.
2.7 Faktor-faktor yang Mempengaruhi Operasi Kolom Distilasi Kinerja kolom distilasi ditentukan oleh beberapa faktor, diantaranya : 1. Jenis Bahan
Pemilihan jenis ini didasarkan oleh perbedaan kemudahan menguap relatif antara komponen yang akan dipisahkan dan campuran-campuran cairan yang terdiri dari 2 atau lebih komponen dipanaskan pada titik didihnya, sehingga sebagai cairan menguap.
2. Temperatur
Distilasi juga akan lebih cepat dilakukan pada suhu tinggi, tetapi hal ini dapat mengakibatkan beberapa komponen yang terdapat dalam bahan akan mengalami kerusakan. Suhu tinggi pelarut dapat meningkatkan efisiensi dari proses distilasi karena panas dapat meningkatkan permeabilitas dinding sel, meningkatkan kelarutan dan difusi dari senyawa yang di distilasi dan mengurangi viskositas pelarut, namun suhu tinggi juga dapat mendegradasi senyawa polifenol.
3. Waktu Distilasi
Semakin lama waktu reaksi pada proses distilasi berlangsung maka semakin banyak nilai kondensat yang dihasilkan.
4. Kondisi Feed (q)
Keadaan campuran dan kondisi feed (q) mempengaruhi garis operasi dan jumlah stage dalam pemisahan. Itu juga mempengaruhi lokasi feed tray.
5. Kondisi Refluks
Pemisahan semakin baik jika sedikit tray yang digunakan untuk mendapatkan tingkat pemisahan. Tray minimum dibutuhkan di bawah kondisi total refluks, yakni tidak ada penarikan distilat. Sebaiknya refluks berkurang, garis operasi untuk seksi rektifikasi bergerak terhadap garis kesetimbangan.
6. Kondisi Aliran Uap
Kondisi aliran uap yang merugikan dapat menyebabkan : a. Foaming
Mengacu pada ekspansi liquid melewati uap atau gas. Walaupun menghasilkan kontak antar fase liquid-uap yang tinggi, foaming berlebihan mengarah pada terbentuknya liquid pada tray.
b. Entrainment
Mengacu pada liquid yang terbawa uap menuju tray di atasnya dan di sebabkan laju alir uap yang tinggi menyebabkan efisiensi tray berkurang.
Bahan yang sukar menguap terbawa menuju plate yang menahan liquid dengan bahan yang mudah menguap. Dapat mengganggu kemurnian distilat. Entrainment berlebihan dapat menyebabkan flooding.
c. Weeping/Dumping
Fenomena ini disebabkan aliran uap yang rendah. Tekanan yang dihasilkan uap tidak cukup untuk menahan liquid pada tray. Karena itu liquid mulai merembes melalui perforasi.
d. Flooding
Terjadi karena aliran uap berlebih menyebabkan liquid terjebak pada uap di atas kolom. Peningkatan tekanan dari uap berlebih menyebabkan kenaikan liquid yang tertahan pada plate di atasnya. Flooding ditandai dengan adanya penurunan tekanan diferensial dalam kolom dan penurunan yang signifikan pada efisiensi pemisahan
(Komariah, 2009).
BAB III
METODOLOGI PRAKTIKUM
3.1 Alat dan Bahan
Adapun alat dan bahan yang digunakan dalam percobaan ini adalah:
3.1.1 Alat
Adapun alat yang digunakan pada percobaan ini adalah:
1. Erlenmeyer 125 ml 3 Buah
2. Labu Ukur 50 ml 3 Buah
3. Labu Ukur 500 ml 1 Buah
4. Labu Leher Tiga 500 ml 1 Buah
5. Neraca Digital 1 Buah
6. Corong 1 Buah
7. Picnometer 5 ml 1 Buah
8. Gelas Ukur 100 ml 1 Buah
9. Kondensor 1 Buah
10. Statif dan Klem 2 Buah
11. Stopwatch 1 Buah
12. Termometer 1 Buah
13. Beaker Glass 500 ml 1 Buah
14. Hot Plate 1 Buah
3.1.2 Bahan
Adapun bahan-bahan yang digunakan pada percobaan ini adalah:
1. Etanol 262,96 ml
2. Aquadest Secukupnya
3. Alumunium Foil Secukupnya
3.2 Prosedur Kerja
3.2.1 Membuat Larutan Standar
Adapun prosedur kerja yang dilakukan pada percobaan ini adalah :
1. Membuat larutan etanol 55% dalam air dengan volume total 10 ml kemudian dihitung volume etanol dalam air dengan persamaan :
X1 V1 = X2 V2 ... (3.1) 2. Mengukur volume metanol kemudian ditambahkan aquadest.
3. Menghitung densitas larutan 55% etanol.
4. Membuat larutan 65%, 75%, 85%, 95% dengan cara yang sama.
3.2.2 Membuat etanol 40% sebagai sampel yang akan di distilasi Adapun prosedur kerja yang dilakukan dalam percobaan ini adalah :
1. Membuat larutan etanol 40% dalam air dengan volume total 500 ml kemudian dihitung volume etanol dalam air dengan persamaan :
X1 V1 = X2 V2 ... (3.2) 2. Mengukur volume metanol kemudian ditambahkan aquadest.
3. Ambil etanol yang telah diencerkan sebanyak 400 ml.
4. Kemudian ditimbang dan diukur densitas.
3.2.3 Tahap operasi distilasi
Adapun prosedur kerja yang dilakukan dalam percobaan ini adalah : 1. Mempersiapkan alat hingga siap di operasikan.
2. Umpan sampel yang telah dibuat, dimasukkan kedalam labu leher tiga.
3. Air pemanas diatur sampai suhu 80oC.
4. Air pendingin sebagai kondensat dialirkan.
5. Saat air pemanas sudah mencapai 80oC, alat dijalankan dengan waktu run I 4 menit, run II 8 menit, run III 12 menit.
6. Saat destilat terbentuk, destilat dikeluarkan kemudian ditimbang dan dihitung densitas dan dicatat.
3.2.4 Menentukan densitas distilat.
1. Ditimbang piknometer kosong dan dicatat.
2. Dimasukkan sampel ke dalam piknometer, ditimbang dan dicatat.
3. Hitung densitas sampel menggunakan rumus densitas.
4. Dilakukan penentuan densitas distilat pada waktu 4, 8, dan 12 menit.
5. Hitung densitas sampel menggunakan rumus densitas.
6. Dilakukan penentuan densitas distilat pada waktu 4, 8, dan 12 menit.
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Adapun hasil yang diperoleh pada percobaan ini dapat dilihat pada Tabel 4.1 dan Tabel 4.2.
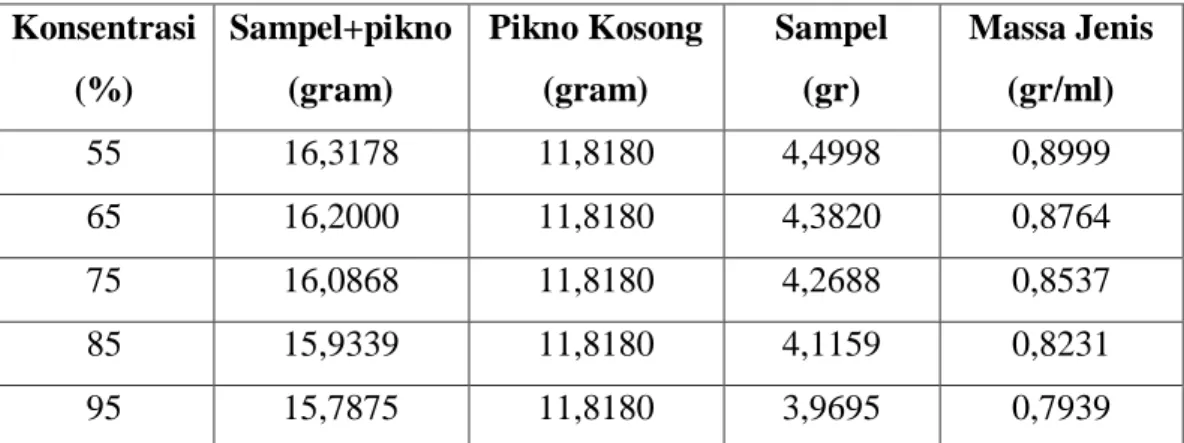
Tabel 4.1 Komposisi Etanol Konsentrasi
(%)
Sampel+pikno (gram)
Pikno Kosong (gram)
Sampel (gr)
Massa Jenis (gr/ml)
55 16,3178 11,8180 4,4998 0,8999
65 16,2000 11,8180 4,3820 0,8764
75 16,0868 11,8180 4,2688 0,8537
85 15,9339 11,8180 4,1159 0,8231
95 15,7875 11,8180 3,9695 0,7939
(Sumber : Praktikum Proses Teknik Kimia II, 2022) Tabel 4.2 Hasil Distilasi
Waktu (menit)
Massa Umpan (gram)
Massa Destilat (gr)
Massa Refluk (gr)
ρ (gr/mol) Distilasi Refluk
4 344,4496 31,7710 312,6786 0,8410 0,9401
8 344,4496 51,3393 293,1103 0,8466 0,9520
12 344,4496 68,0146 276,4250 0,8484 0,9610
(Sumber : Praktikum Proses Teknik Kimia II, 2022) 4.2 Pembahasan
Distilasi sederhana adalah teknik pemisahan untuk memisahkan dua atau lebih komponen zat cair yang memiliki perbedaan titik didih yang jauh. Selain perbedaan titih didih, juga perbedaan kevolatilan, yaitu kecenderungan sebuah zat untuk menjadi gas. Distilasi ini dilakukan pada tekanan atmosfer yang normal.
Aplikasi distilasi sederhana dilakukan untuk memisahkan campuran air dan etanol. Pada percobaan kali ini yang digunakan adalah etanol, dikarenakan etanol
mempunyai titik didih yang lebih rendah dari pada air. Etanol merupakan pelarut polar dan non-polar serta mudah menguap, sifat ini mendasari kenapa etanol lebih mudah menguap dibandingkan dengan air.
Sebelum dilakukan percobaan menggunakan distilasi terlebih dahulu praktikan melakukan uji densitas pada etanol. Uji sampel dilakukan untuk larutan 55%, 65%, 75%, 85% dan 95%, didapatkan hasil berturut-tutut yaitu 0.8999 g/ml, 0.8764 g/ml, 0.8537 g/ml, 0.8231 ml, 0.7939 g/ml. Hasil densitas untuk larutan tersebut mendekati densitas air karena persen air pada sampel diatas lebih banyak.
Percobaan destilasi ini diketahui bahwa destilasi merupakan proses pemisahan yang berdasarkan perbedaan titik didih suatu bahan yang digunakan, bahan yang digunakan didalam percobaan etanol dan aquades. Dimana etanol memilik titik didih sebesar 78,37°C sedangkan air sebesar 100°C.
Adapun suhu yang dipakai pada distilasi ini adalah 85oC. Pada percobaan ini dilakukan proses pemisahan pada etanol dan air dengan massa umpan 344,4496 gram, setelah dipanaskan selama 4 menit sehingga diperoleh refluk seberat 312,6786 gram dan massa distilat seberat 31,7710 gram. Kemudian dilakukan percobaan dengan massa umpan yang sama yaitu 344,4496 gram dengan waktu distilasi selama 8 menit sehingga diperoleh massa refluk seberat 293,1103 gram dan massa distilat seberat 51,3393 gram dan terakhir dilakukan kembali distilasi selama 12 menit dengan massa umpan yang sama dan hasilnya adalah massa refluk seberat 267,4250 gram dan massa distilat seberat 68,0246 gram. Hal ini menunjukkan bahwa semakin lama waktu distilasi maka semakin banyak distilat (etanol) yang menguap karena suhu yang digunakan diatas titik didih etanol (Nur Ihda Farikhatin Nisa, 2019).
Dasar dari penggunaan suhu tersebut karena distilasi sederhana yang digunakan menggunakan sistem terbuka sehingga ada banyak panas yang hilang, selain itu efisiensi alat yang sudah tua sehingga panas didalamnya banyak mengalami kebocoran dan tidak konstan. Massa loss atau massa yang hilang selama proses distilasi berlangsung juga diukur dalam penelitian ini. Massa yang hilang dapat disebabkan oleh minyak yang tertinggal atau menempel pada komponen-komponen alat distilasi fraksinasi (Auliani, 2011).
4.2.1 Hubungan Antara ρ Etanol dengan Xm
Gambar 4.1 Grafik Hubungan Antara ρ Etanol Vs Xm
Dari grafik diatas terlihat bahwa untuk etanol 55% memiliki densitas 0,8999 gr/ml dan nilai Xm 0,3864, untuk etanol 65% memiliki densitas 0,8764 gr/ml dan nilai Xm 0,5284, untuk etanol 75% memiliki densitas 0,8537 gr/ml dan nilai Xm 0,6757 untuk etanol 85% memiliki densitas 0,8231 gr/ml dan nilai Xm 0,8371 dan untuk etanol 95% memiliki densitas 0,7989 gr/ml dan nilai Xe 0,9593.
Xm merupakan fraksi etanol dalam larutan. Hal ini menunjukkan bahwa hasil yang didapat sesuai dengan teoritis yang menyatakan bahwa semakin tinggi konsentrasi maka nilai Xe yang diperoleh juga semakin besar. Perbandingan konsentrasi ini menunjukkan semakin banyaknya etanol didalam larutan tersebut.
Hal ini disebabkan karena banyaknya volume etanol absolut dalam air (Mc. Cabe, 1999).
4.2.2 Hubungan Antara Massa Distilat dengan Waktu.
y = -5.4559x + 5.3116 R² = 0.9933
0 0.2 0.4 0.6 0.8 1 1.2
0.78 0.8 0.82 0.84 0.86 0.88 0.9 0.92
Xm (gram/mol)
ρ (gram/mol)
y = 0,2202x - 3,0935 R² = 0,9979 0
2 4 6 8 10 12 14
20 30 40 50 60 70 80
Massa (gram)
Waktu (menit)
Gambar 4.2 Grafik Hubungan Massa Distilat Vs Waktu
Grafik diatas menunjukkan bahwa pada waktu distilasi selama 4 menit diperoleh massa distilat sebanyak 31,7710 gr pada waktu distilasi selama 8 menit diperoleh massa distilat sebesar 51,3393 gr dan pada waktu distilasi 12 menit diperoleh massa distilat yang semakin besar yaitu 68,0246 gr. Grafik diatas menunjukkan nilai distilat yang bertambah seiring dengan lama waktu pada proses destilasi, hal tersebut disebabkan semakin lama proses distilasi berlangsung maka semakin banyak nilai distilat yang dihasilkan, dan berhubungan dengan proses pemisahan etanol dan air yang akan menghasilkan konsentrasi etanol yang tinggi.
Pada dasarnya waktu operasi dan suhu operasi yang digunakan pada proses distilasi sangat mempengaruhi banyaknya massa distilat yang didapatkan pada proses destilasi ini. Pada percobaan ini didapatkan % konversi untuk run I sebanyak 9,22% pada run II sebanyak 14,90% dan pada run III sebanyak 19,74%.
Dengan lamanya waktu tinggal (waktu operasi) akan membuat konversi produk semakin tinggi yang ditunjukkan dengan semakin banyaknya distilat yang didapat pada proses distilasi ini. Ini menandakan bahwa semakin banyak etanol yang menguap meninggalkan air yang belum menguap di labu distilasi tersebut.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Adapun kesimpulan dari praktikum ini adalah sebagai berikut:
1. Berdasarkan pengujian densitas diperoleh densitas etanol 55% yaitu 0.8999 gr/ml, densitas etanol 65% yaitu 0,8764 gr/ml, densitas etanol 75%
yaitu 0,8537, densitas etanol 85% yaitu 0,8231 dan densitas etanol 95%
yaitu 0,7939 gr/ml.
2. Pada waktu distilasi selama 4 menit diperoleh refluk seberat 312,6786 gram dan distilat seberat 31,7710 gram.
3. Pada waktu distilasi selama 8 menit diperoleh refluk seberat 293,1103 gram dan distilat seberat 51,3393 gram.
4. Pada waktu distilasi selama 12 menit diperoleh refluk seberat 276,4250 gram dan distilat seberat 68,0246 gram.
5. Pada percobaan ini didapatkan % konversi untuk run I sebanyak 9,22%
pada run II sebanyak 14,90% dan pada run III sebanyak 19,74%.
5.2 Saran
Adapun saran untuk praktikum selanjutnya adalah sebagai berikut:
1. Sebaiknya proses distilasi dilakukan dengan waktu proses yang lebih lama agar etanol yang didapat lebih maksimal.
2. Sebaiknya proses distilasi juga dilakukan dengan variasi bahan dan suhu distilasi sehingga diperoleh perbandingannya.
3. Sebaiknya teknik kimia menyediakan alat distilasi yang jauh lebih baik sehingga proses distilasi dapat dilakukan dengan lebih baik.
DAFTAR PUSTAKA
Aan Komariah, Djam’an Satori. 2009. Metode Penelitian Kualitatif. Bandung, Alfabeta.
Abbassato, Tony Irwanto & Eko Aris Budiarto. 2007. Efisiensi Kolom Sieve Tray pada Destilasi yang Mengandung Tiga Komponen (Aceton-Alkohol- Air). Jurnal Nasional. 978-979.
Adityo Kurniawan, Chandra Kurniawan, Nani Indraswati, Mudjijati. 2008.
Ekstraksi Minyak Kulit Jeruk dengan Metode Distilasi, Pengeprasan dan Leaching. Widya Teknik Vol. 7, No. 1
Auliani, 2011. Penuntun Praktikum DDPA. Bandung. Erlangga.
Cammack, R. 2006. Oxford Dictionary of Biochemistry and Molecular Biology.
Oxford University Press. New York. 720
Husnul Khatimah, Hernawati, dan Rahmaniah. 2016. Uji Kualitas Fisis Pengolahan Limbah Oli Bekas Menjadi Bahan Bakar Alternatif dengan Metode Distilasi Sederhana. Jurusan Fisika Fakultas Sains dan Teknologi.
UIN Alauddin. Makassar.
Kunnakorn, D., Rirkosombon T., dkk, 2003, Techno-economic Comparison of Energy Usage Between Azeotropic Distillation and Hybrid System for Etanol-Water Separation, Jurnal Renewable Energy, Vol 51, Hal 310-316.
Leily Nurul Komariah, A. F. Ramdja, Nicky Leonard. 2009. Tinjauan Teoritas Perancangan Kolom Distilasi Untuk Pra-rancangan Pabrik Skala Industri. Jurusan Teknik Kimia Fakultas Teknik. Universitas Sriwijaya.
Palembang.
Mc. Cabe .W.L and Harriot. 1999. Unit Operation of Chemical Engineering 5th edition. Mc. Graw Hill. New York.
Nur Ihda Farikhatin Nisa, Achmad Aminudin. 2019. Pengaruh Waktu Distilasi Etanol-Air Terhadap Konsentrasi Overhead Product dan Bottom Product.
Jurusan Teknik Kimia. Universitas PGRI. Madiun.
Shabrina Iswari Adani, Yunita Ali Pujiastuti. 2017. Pengaruh Suhu dan Waktu Operasi Pada Proses Distilasi Untuk Pengolahan Aquades Di Fakultas Teknik Universitas Mulawarman. Jurusan Teknik Kimia. Universitas Mulawarman. Samarinda.
LAMPIRAN B PERHITUNGAN
B.1 Konsentrasi Etanol 1. 55%, Volume 10 ml
X1 V1 = X2 V2 98% V1 = 55% 10 ml 98 V1 = 55 10 ml 98 V1 = 550 ml
V1 = 550/98 V1 = 5,6 ml 2. 65%, Volume 10 ml
X1 V1 = X2 V2
98% V1 = 65% 10 ml 98 V1 = 65 10 ml 98 V1 = 650 ml
V1 = 650/98 V1 = 6,63 ml 3. 75%, Volume 10 ml
X1 V1 = X2 V2 98% V1 = 75% 10 ml 98 V1 = 75 10 ml 98 V1 = 750 ml
V1 = 750/98 V1 = 7,65 ml 4. 85%, Volume 10 ml
X1 V1 = X2 V2
98% V1 = 85% 10 ml 98 V1 = 85 10 ml
98 V1 = 850 ml V1 = 850/98 V1 = 8,67 ml 5. 95%, Volume 10 ml
X1 V1 = X2 V2
98% V1 = 95% 10 ml 98 V1 = 95 10 ml 98 V1 = 950 ml
V1 = 950/98 V1 = 9,69 ml
4. 40%, Volume 500 ml untuk Umpan X1 V1 = X2 V2
98% V1 = 40% 500 ml 98 V1 = 40 500 ml 98 V1 = 20.000 ml
V1 = 20.000/98 V1 = 224,72 ml B.2 Menghitung Densitas Etanol 1. Etanol 55%
Berat pikno kosong = 11,8180 gr Volume pikno = 5 ml Berat pikno + sampel = 16,3178 gr
Massa sampel = (Berat pikno + sampel) – (Berat pikno kosong)
= 16,3178 – 11,8180
= 4,4998
m
=
4,49985
=
0,8999 gr/ml2. Etanol 65%
Berat pikno kosong = 11,8180 gr Volume pikno = 5 ml Berat pikno + sampel = 16,2000 gr
Massa sampel = (Berat pikno + sampel) – (Berat pikno kosong) = 16,2000 – 11,8180
= 4,3820 m
=
4,38205
=
0,8764 gr/ml 3. Etanol 75%Berat pikno kosong = 11,8180 gr Volume pikno = 5 ml Berat pikno + sampel = 16,0868 gr
Massa sampel = (Berat pikno + sampel) – (Berat pikno kosong) = 16,0868 – 11,8180
= 4,2688 m
=
4,26885
=
0,8537 gr/ml 4. Etanol 85%Berat pikno kosong = 11,8180 gr Volume pikno = 5 ml Berat pikno + sampel = 15,9339 gr
Massa sampel = (Berat pikno + sampel) – (Berat pikno kosong) = 15,9339 – 11,8180
= 4,1159
m
=
4,11595
=
0,8231 gr/ml 5. Etanol 95%Berat pikno kosong = 11,8180 gr Volume pikno = 5 ml Berat pikno + sampel = 15,7875 gr
Massa sampel = (Berat pikno + sampel) – (Berat pikno kosong) = 15,7875 – 11,8180
= 3,9695 m
=
3,96955
=
0,7939 gr/ml B.3 Menghitung XmXm =
(ρ. . ) etanol
(ρ. . ) etanol ( total- etanol) ρ air 1. Etanol 55%
Diketahui : ρ = 0,8999 gr/ml V = 5,6 ml
Xm =
(0.8999 r ml 5,6 ml 0,55)
(0,8999 r ml 5,6 ml 0,55) (10 ml - 5,6 ml)1 r ml
=
2,7716 4,42,7716 = 0,3864 2. Etanol 65%
Diketahui : ρ = 0,8764 gr/ml V = 6,63 ml
Xm =
(0.8764 r ml 6,63 ml 0,65)
(0,8764 r ml 6,63 ml 0,65) (10 ml - 6,63 ml)1 r ml
=
3,7768 3,373,7768 = 0,5284 3. Etanol 75%
Diketahui : ρ = 0,8537 gr/ml V = 7,65 ml
Xm =
(0.8537 r ml 7,65 ml 0,75)
(0,8537 r ml 7,65 ml 0,75) (10 ml - 7,65 ml)1 r ml
=
4,8981 2,354,8981
= 0,6757 4. Etanol 85%
Diketahui : ρ = 0,8231 gr/ml V = 8,76 ml
Xm =
(0.8231 r ml 8,76 ml 0,85)
(0,8231 r ml 8,76 ml 0,85) (10 ml - 8,76 ml)1 r ml
=
6,1288 1,246,1288 = 0,8317 5. Etanol 95%
Diketahui : ρ = 0,7939 gr/ml V = 9,69 ml
Xm =
(0.7939 r ml 9,69 ml 0,95)
(0,7939 r ml 9,69 ml 0,95) (10 ml - 9,69 ml)1 r ml =
7,3082 0,317,3082
= 0,9593
B.4 Massa Distilat dan Refluks 1. Run I (4 Menit)
Massa Umpan = 344,4496 Massa pikno kosong = 11,8180 Massa pikno + Distilat = 16,0231 Massa pikno + reflux = 16,5187
Distilat = m = 16,0231- 11,8180
5 = 0,8410
Refluk =m 16,5187 - 11,8180
5 = 0,9401
2. Run II (8 Menit)
Massa Umpan = 344,4496 Massa pikno kosong = 11,8180 Massa pikno + Distilat = 16,0510 Massa pikno + reflux = 16,5780
Distilat = m = 16,0510 - 11,8180
5 = 0,8466
Refluk = m= 16,5780 - 11,8180
5
=
0,95203. Run III (12 Menit)
Massa Umpan = 344,4496 Massa pikno kosong = 11,8180 Massa pikno + Distilat = 16,0600 Massa pikno + reflux = 16,6232
Distilat
=
m = 16,0600- 11,81805 = 0,8484
Refluk = m = 16,6232 - 11,8180
5
=
0,9610B.5 Menghitung Neraca Massa A = B + C
Keterangan : A = Umpan Masuk B = Refluks
C = Distilat Run I
A = B + C
344,4496 gram = 312,6786 gram + 31,7710 gram 344,4496 gram = 344,4496 gram
Jadi, umpan masuk sama dengan hasil distilasi pada proses distilasi Run I sebesar 344,4496 gram.
Run II
A = B + C
344,4496 gram = 293,1103 gram + 51,3393 gram 344,4496 gram = 344,4496 gram
Jadi, umpan masuk sama dengan hasil distilasi pada proses distilasi Run II sebesar 344,4496 gram.
Run III
A = B + C
344,4496 gram = 276,4250 gram + 68,0246 gram 344,4496 gram = 344,4496 gram
Jadi, umpan masuk sama dengan hasil distilasi pada proses distilasi Run III sebesar 344,4496 gram.
B.6 Menghitung % Konversi
konversi = assa Destilatassa mpan x 100%
1. Run 1 (4 menit)
konversi = assa Destilatassa mpan x 100%
= 31,7710
344,4496 x 100%
= 9,22%
2. Run II (8 menit)
konversi = assa Destilatassa mpan x 100%
= 51,3393
344,4496 x 100%
= 14,90%
3. Run III (12 menit)
konversi = assa Destilatassa mpan x 100%
= 68,0246
344,4496 x 100%
= 19,74%
LAMPIRAN C GAMBAR ALAT
No. Nama dan Gambar Alat Fungsi
1. Labu Leher Tiga Sebagai wadah untuk campuran zat cair yang akan didistilasi
2. Erlenmeyer Sebagai tempat untuk membuat
larutan
3. Gelas Ukur Untuk mengukur volume larutan.
4. Labu Ukur Untuk mengencerkan larutan hingga batas labu ukur.
5. Corong Untuk memasukkan atau
memindahkan larutan dari satu tempat ke tempat lain.
6. Picnometer Untuk mengukur massa jenis atau densitas larutan.
7. Neraca Digital Untuk menimbang massa suatu zat.
8. Kondensor Sebagai tabung pendingin yang digunakan dalam sistem destilasi untu k mengubah uap menjadi air.
9. Statif dan Klem Statif adalah stand sebagai tempat untuk meletakkan klem.
Sedangkan klem sendiri merupakan sebuah alat jepit yang berbuat dari besi dan digunakan untuk menjepit alat gelas kimia.
10. Stopwatch Untuk mengukur lamanya waktu
yang dibutuhkan dalam sebuah kegiatan.
11. Termometer Untuk mengamati suhu dalam proses destilasi sehingga suhu dapat dikontrol sesuai dengan suhu yang diinginkan untuk memperoleh destilat murni.
12. Beaker Glass Sebagai wadah penampung yang digunakan untuk mengaduk, mencampur, dan memanaskan cairan yang biasanya digunakan dalam laboratorium.
13. Hot Plate Hot plate adalah sebuah alat laboratorium yang digunakan untuk memanaskan atau menghangat kan sekaligus mencampurkan atau menghomogenkan larutan kimia.