SKRIPSI
PENGARUH PEREBUSAN KERANG DARAH (Anadara granosa) TERHADAP PENURUNAN KADAR LOGAM KADMIUM (Cd) MENGGUNAKAN AKUADES DAN LARUTAN JERUK NIPIS (Citrus aurantifolia Swingle) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
Oleh:
MERY YULIANDA
NIM 060804028
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENGARUH PEREBUSAN KERANG DARAH (Anadara granosa) TERHADAP PENURUNAN KADAR LOGAM KADMIUM (Cd) MENGGUNAKAN AKUADES DAN LARUTAN JERUK NIPIS (Citrus aurantifolia Swingle) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
Oleh:
MERY YULIANDA NIM 060804028
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal September 2010
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
(Drs. Syafruddin, MS., Apt.) (Prof. Dr. rer. Nat. Effendy De Lux Putra, SU., Apt.) NIP 194811111976031003 NIP 195306191983031001
(Drs. Syafruddin, MS., Apt.) Pembimbing II, NIP 194811111976031003
(Dra. Salbiah, M.Si., Apt.) (Drs. Muchlisyam, M.Si., Apt.) NIP 194810031987012001 NIP 195006221980021001
(Dra. Sudarmi, M.Si., Apt.) NIP 195409101983032001
Dekan,
KATA PENGANTAR Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan
judul:“Pengaruh Perebusan Kerang Darah (Anadara granosa) Terhadap
Penurunan Kadar Logam Kadmium Menggunakan Akuades dan Larutan Jeruk Nipis (Citrus aurantifolia Swingle) Secara Spektrofotometri Serapan Atom”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ayahanda Iswandi dan Ibunda Misnurwati yang telah memberikan cinta dan
kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi
maupun motivasi beserta doa yang tulus yang tidak pernah berhenti.
2. Bapak Drs. Syafruddin, M.Si, Apt dan Dra. Salbiah, M.Si, Apt yang telah
membimbing dan memberikan petunjuk serta saran-saran selama penelitian
hingga selesainya skripsi ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra, Apt selaku Dekan Fakultas Farmasi
USU Medan, yang telah memberikan pengarahan dan bimbingan dalam
4. Ibu Dra. Marline Nainggolan, M.Si, Apt selaku penasihat akademik yang telah
memberikan bimbingan kepada penulis selama masa perkuliahan.
5. Bapak Drs. Fathur Rahman Harun, M.Si, Apt selaku Kepala Laboratorium
Kimia Farmasi Kuantitatif Farmasi USU yang telah memberikan izin dan
fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan
penelitian.
6. Bapak Baharuddin AR selaku penanggung jawab Laboratorium Balai Pusat
Penelitian Kelapa Sawit (BPPKS) Medan dan Bapak Hambali selaku Operator
Laboratorium Pusat Penelitian Kelapa Sawit (PPKS) Medan yang telah
memberikan fasilitas kepada penulis selama melaksanakan penelitian.
7. Adik-adik tercinta ( Zuryandi dan Desy Febriani), serta seluruh keluarga yang
selalu mendoakan dan memberikan semangat.
8. Kakak-kakak Farmasi angkatan 2005, teman-teman Farmasi Reguler angkatan
2006, 2007, 2008, dan 2009, terima kasih untuk perhatian, semangat, doa, dan
kebersamaannya selama ini.
9. Serta seluruh pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Agustus 2010
PENGARUH PEREBUSAN KERANG DARAH (Anadara granosa) TERHADAP PENURUNAN KADAR LOGAM KADMIUM (Cd) MENGGUNAKAN AKUADES DAN LARUTAN JERUK NIPIS (Citrus aurantifolia Swingle) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Kerang darah (Anadara granosa) yang terdapat di perairan belawan telah
tercemar dengan berbagai logam berat diantaranya Kadmium (Cd). Logam ini
sangat berbahaya bagi konsumen kerang darah, jika mengkonsumsi kerang darah
secara terus menerus. Jeruk nipis (Citrus aurantifolia Swingle) mengandung
senyawa organik yang dapat mengikat logam berat seperti Kadmium (Cd). Tujuan
dari penelitian ini adalah untuk melihat pengaruh perebusan kerang darah dalam
akuades dan larutan jeruk nipis selama 1 menit dan 15 menit terhadap penurunan
kadar logam Kadmium (Cd) pada kerang darah.
Pemeriksaan logam Kadmium (Cd) secara kualitatif dilakukan dengan
menggunakan pereaksi dithizon 0,005% b/v pada pH=12, dan pengukuran kadar
logam Kadmium (Cd) dilakukan secara kuantitatif dengan spektrofotometer
serapan atom pada panjang gelombang 228,8 nm.
Hasil penelitian secara kualitatif menunjukkan bahwa kerang darah positif
mengandung logam Kadmium (Cd), dimana dengan reaksi dithizon 0,005% b/v
pada pH=12 menghasilkan warna merah muda, sedangkan secara kuantitatif
menunjukkan kadar logam Kadmium (Cd) sebelum perebusan adalah
2,2432 0,0060 mcg/g. Perebusan dalam akuades selama 1 menit menunjukkan
kadar logam Kadmium (Cd) 2,0594 0,0449 mcg/g dengan penurunan sebesar
8,83%, dan perebusan selama 15 menit adalah 1,4967 0,0083 mcg/g dengan
penurunan sebesar 33,23%, sedangkan kadar logam Kadmium (Cd) setelah
kerang direbus selama 1 menit dalam larutan jeruk nipis adalah 0,9614 0,0143
mcg/g dengan penurunan sebesar 55,95%, dan perebusan selama 15 menit adalah
0,6678 0,0011 mcg/g dengan penurunan sebesar 69,97%. Menurut SNI
7387-2009, batas maksimum cemaran logam berat Kadmium (Cd) pada
kerang-kerangan (bivalvia) sebesar 1,0 mcg/g.
Kata kunci : Kerang darah, logam Kadmium, perairan belawan, jeruk nipis
BOILINGEFFECT OF BLOOD CLAM (Anadara granosa) DECREASE IN CONCENTRATION OF CADMIUM METAL (Cd) USING AQUADEST
and THE LIME SOLUTION (Citrus aurantifolia Swingle) By ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Blood clam (Anadara granosa) was found in belawan waters are polluted
with various heavy metals such as Cadmium (Cd). This metal is very dangerous
for blood clam consumers if consumed continuously. Lime fruit (Citrus
aurantifolia Swingle) contain organic compounds that can bind heavy metals such
as Cadmium (Cd). The purpose of this study was to see the impact of blood clam
boiling in aquadest and lime solution for 1 minute and 15 minutes to decrease the
metal content of Cadmium (Cd) in blood clam.
A qualitative examination of Cadmium (Cd) metal was done by the
dithizon reagent 0.005% w/v at pH = 12, and the quantitative assay of Cadmium
(Cd) metal was done by means atomic absorption spectrophotometer at a
wavelength of 228.8 nm.
The qualitative results showed that blood clam positive contain the
Cadmium (Cd) metal, with the dithizon reagent 0.005% w/v at pH=12 result the
pink colour, while with the quantitative assay showed the content of Cadmium
(Cd) metal before boiling was 2.2432±0.0060 mcg/g. Boiling in aquadest for 1
minute show the content of Cadmium (Cd) metal was 2.0594±0.0449 mcg/g with
decrease of 8.83%, and boiling for 15 minutes was 1.4967±0.0083 mcg/g with
decrease of 33.23%, while the content of Cadmium (Cd) metal after blood clam
boiled for 1 minute in the lime solution was 0.9614±0.0143 mcg/g with decrease
of 55.95%, and boiling for 15 minutes was 0.6678±0.0011 mcg/g with decrease of
69.97%. According to ISO 7387-2009, the limit of heavy metal contamination of
Cadmium (Cd) in blood clam (bivalves) equal to 1.0 mcg/g.
Keywords: Blood clam, Cadmium metal, belawan waters, lime fruit (Citrus
DAFTAR ISI
Halaman
JUDUL………... i
HALAMAN PENGESAHAN………... iii
KATA PENGANTAR... iv
ABSTRAK………... vi
ABSTRACT... vii
DAFTAR ISI………... viii
DAFTAR TABEL………... xi
DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN……….. xiii
BAB I. PENDAHULUAN………. 1
1.1 Latar Belakang………... 1
1.2 Perumusan Masalah………... 3
1.3 Hipotesis……….. 3
1.4 Tujuan Penelitian………... 3
1.5 Manfaat Penelitian………... 3
BAB II. TINJAUAN PUSTAKA... 4
2.1 Uraian Kerang Darah (Anadara granosa)... 4
2.2 Uraian Jeruk Nipis (Citrus aurantifolia Swingle)... 6
2.3 Asam Sitrat... 6
2.4 Pencemaran Laut... 7
2.5 Logam Berat... 8
2.6 Toksisitas Logam Pada Jenis Kerang... 10
2.7 Pengikatan Logam... 11
2.8 Destruksi Basah... 11
2.9 Spektrofotometri Serapan Atom... 12
2.9.1 Instrumen Spektrofotometer Serapan Atom... 13
2.9.2 Bahan Bakar dan Bahan Pengoksidasi... 14
2.9.3 Gangguan-gangguan Pada Spektrofotometri Serapan Atom... 15
2.10 Validasi Metode Analisis... 16
2.10.1 Perolehan Kembali... 16
2.10.2 Batas Deteksi dan Batas Kuantitasi... 16
BAB III. METODOLOGI PENELITIAN………... 17
3.1 Tempat dan Waktu Pelaksanaan Penelitian………... 17
3.2 Bahan-bahan………... 17
3.2.1 Sampel………... 17
3.2.2 Pereaksi………... 17
3.3 Alat………... 17
3.4 Pembuatan Pereaksi………... 18
3.5 Rancangan Penelitian………... 19
3.6 Prosedur penelitian………... 20
3.6.1 Pengambilan Sampel………... 20
3.6.2 Penyiapan Sampel………... 20
3.6.3 Proses Destruksi Basah Untuk Kadmium………... 21
3.6.4 Analisa Kualitatif………... 22
3.6.5.1 Penentuan Panjang Gelombang Maksimum... 22
3.6.5.2 Penentuan Kurva Kalibrasi Logam Kadmium... 22
3.6.5.3 Penentuan Kadar Logam Kadmium dalam Kerang Darah... 23
3.6.5.4 Uji Perolehan kembali... 23
3.6.5.4.1 Pembuatan Larutan Standar... 23
3.6.5.4.2 Prosedur Uji Perolehan Kembali... 23
3.6.5.5 Analisa Data Secara Statistik... 24
3.6.5.6 Penentuan Batas Deteksi dan Batas Kuantitasi... 25
BAB IV. HASIL DAN PEMBAHASAN... 26
4.1 Hasil Uji Kualitatif... 26
4.2 Hasil Uji kuantitatif... 26
4.2.1 Kurva Kalibrasi Logam Kadmium... 26
4.2.2 Analisa Kadar Logam Kadmium... 27
4.2.3 Uji Perolehan Kembali... 31
4.2.4 Batas Deteksi dan Batas Kuantitasi... 31
BAB V. KESIMPULAN DAN SARAN... 32
5.1 Kesimpulan... 32
5.2 Saran... 32
DAFTAR PUSTAKA... 34
DAFTAR TABEL
Halaman
Tabel 1. Jenis-jenis Kerang Yang Bernilai Ekonomis Penting
Yang Ada Di Perairan Indonesia... 4
Tabel 2. Temperatur Nyala dengan Berbagai Konsentrasi Bahan
Bakar dan Bahan Pengoksidasi... 15
Tabel 3. Hasil Uji Kualitatif Logam Kadmium dengan pereaksi
Dithizon 0,005 % b/v ………... 26
Tabel 4. Data Kadar Logam Kadmium (Cd) ………... 28
Tabel 5. Data kadar logam Cd dengan perebusan menggunakan
alat masak berbahan logam ………... 30
Tabel 6. Persen Uji Perolehan Kembali (recovery)
DAFTAR GAMBAR
Halaman
Gambar 1. Sistem Peralatan Spektrofotometer Serapan Atom... 13
Gambar 2. Kurva Kalibrasi Logam Kadmium………... 27
Gambar 3. Hasil Analisa Kualitatif Kerang Tanpa Perebusan... 66
Gambar 4. Hasil Analisa Kualitatif Kerang dengan Perebusan Dalam Akuades... 66
Gambar 5. Hasil Analisa Kualitatif Kerang dengan Perebusan Dalam Larutan Jeruk Nipis... 67
Gambar 6. Alat Spektrofotometer Serapan Atom... 68
Gambar 7. Kerang Darah (Anadara granosa)... 69
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Bagan Proses Penyiapan Sampel………... 37
Lampiran 2. Bagan Proses Destruksi Logam Kadmium………... 38
Lampiran 3. Data Hasil Pengukuran Absorbansi Larutan Standar
Kadmium (Cd)………... 39
Lampiran 4. Contoh Perhitungan Persamaan Regresi Logam
Kadmium………... 40
Lampiran 5. Hasil Analisa Logam Kadmium dalam Kerang Darah (Anadara granosa)………... 42
Lampiran 6. Contoh Perhitungan Kadar Logam Kadmium (Cd)
Dalam Kerang Darah (Anadara granosa)………... 44
Lampiran 7. Perhitungan Statistik Kadar Logam Kadmium dalam
Kerang Darah (Anadara granosa)………... 45
Lampiran 8. Data Hasil Uji Perolehan Kembali Cd dalam Kerang
Darah (Anadara granosa)………... 62
Lampiran 9. Contoh Perhitungan Uji Perolehan Kembali Logam
Kadmium Dalam Kerang Darah………... 63
Lampiran 10. Perhitungan Batas Deteksi dan Batas Kuantitasi
Logam Kadmium (Cd)………... 64
Lampiran 11. Hasil Orientasi Analisa Logam Kadmium dalam Kerang Darah (Anadara granosa) dengan
Perebusan Menggunakan Alat Masak yang
Berbahan Logam... 65
Lampiran 12. Gambar Hasil Analisa Kualitatif Logam Kadmium
(Cd) dengan Pereaksi Dithizon 0,005% b/v………... 66
Lampiran 13. Gambar Alat Spektrofotometer Serapan atom…... 68
Lampiran 14. Gambar Kerang Darah (Anadara granosa) dan Buah Jeruk Nipis (Citrus aurantifolia Swingle)…... 69
PENGARUH PEREBUSAN KERANG DARAH (Anadara granosa) TERHADAP PENURUNAN KADAR LOGAM KADMIUM (Cd) MENGGUNAKAN AKUADES DAN LARUTAN JERUK NIPIS (Citrus aurantifolia Swingle) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Kerang darah (Anadara granosa) yang terdapat di perairan belawan telah
tercemar dengan berbagai logam berat diantaranya Kadmium (Cd). Logam ini
sangat berbahaya bagi konsumen kerang darah, jika mengkonsumsi kerang darah
secara terus menerus. Jeruk nipis (Citrus aurantifolia Swingle) mengandung
senyawa organik yang dapat mengikat logam berat seperti Kadmium (Cd). Tujuan
dari penelitian ini adalah untuk melihat pengaruh perebusan kerang darah dalam
akuades dan larutan jeruk nipis selama 1 menit dan 15 menit terhadap penurunan
kadar logam Kadmium (Cd) pada kerang darah.
Pemeriksaan logam Kadmium (Cd) secara kualitatif dilakukan dengan
menggunakan pereaksi dithizon 0,005% b/v pada pH=12, dan pengukuran kadar
logam Kadmium (Cd) dilakukan secara kuantitatif dengan spektrofotometer
serapan atom pada panjang gelombang 228,8 nm.
Hasil penelitian secara kualitatif menunjukkan bahwa kerang darah positif
mengandung logam Kadmium (Cd), dimana dengan reaksi dithizon 0,005% b/v
pada pH=12 menghasilkan warna merah muda, sedangkan secara kuantitatif
menunjukkan kadar logam Kadmium (Cd) sebelum perebusan adalah
2,2432 0,0060 mcg/g. Perebusan dalam akuades selama 1 menit menunjukkan
kadar logam Kadmium (Cd) 2,0594 0,0449 mcg/g dengan penurunan sebesar
8,83%, dan perebusan selama 15 menit adalah 1,4967 0,0083 mcg/g dengan
penurunan sebesar 33,23%, sedangkan kadar logam Kadmium (Cd) setelah
kerang direbus selama 1 menit dalam larutan jeruk nipis adalah 0,9614 0,0143
mcg/g dengan penurunan sebesar 55,95%, dan perebusan selama 15 menit adalah
0,6678 0,0011 mcg/g dengan penurunan sebesar 69,97%. Menurut SNI
7387-2009, batas maksimum cemaran logam berat Kadmium (Cd) pada
kerang-kerangan (bivalvia) sebesar 1,0 mcg/g.
Kata kunci : Kerang darah, logam Kadmium, perairan belawan, jeruk nipis
BOILINGEFFECT OF BLOOD CLAM (Anadara granosa) DECREASE IN CONCENTRATION OF CADMIUM METAL (Cd) USING AQUADEST
and THE LIME SOLUTION (Citrus aurantifolia Swingle) By ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Blood clam (Anadara granosa) was found in belawan waters are polluted
with various heavy metals such as Cadmium (Cd). This metal is very dangerous
for blood clam consumers if consumed continuously. Lime fruit (Citrus
aurantifolia Swingle) contain organic compounds that can bind heavy metals such
as Cadmium (Cd). The purpose of this study was to see the impact of blood clam
boiling in aquadest and lime solution for 1 minute and 15 minutes to decrease the
metal content of Cadmium (Cd) in blood clam.
A qualitative examination of Cadmium (Cd) metal was done by the
dithizon reagent 0.005% w/v at pH = 12, and the quantitative assay of Cadmium
(Cd) metal was done by means atomic absorption spectrophotometer at a
wavelength of 228.8 nm.
The qualitative results showed that blood clam positive contain the
Cadmium (Cd) metal, with the dithizon reagent 0.005% w/v at pH=12 result the
pink colour, while with the quantitative assay showed the content of Cadmium
(Cd) metal before boiling was 2.2432±0.0060 mcg/g. Boiling in aquadest for 1
minute show the content of Cadmium (Cd) metal was 2.0594±0.0449 mcg/g with
decrease of 8.83%, and boiling for 15 minutes was 1.4967±0.0083 mcg/g with
decrease of 33.23%, while the content of Cadmium (Cd) metal after blood clam
boiled for 1 minute in the lime solution was 0.9614±0.0143 mcg/g with decrease
of 55.95%, and boiling for 15 minutes was 0.6678±0.0011 mcg/g with decrease of
69.97%. According to ISO 7387-2009, the limit of heavy metal contamination of
Cadmium (Cd) in blood clam (bivalves) equal to 1.0 mcg/g.
Keywords: Blood clam, Cadmium metal, belawan waters, lime fruit (Citrus
BAB I PENDAHULUAN 1.1Latar Belakang
Laut merupakan suatu komponen yang berinteraksi dengan lingkungan
daratan, dimana buangan limbah dari daratan akan bermuara ke laut. Limbah
tersebut yang mengandung polutan kemudian masuk kedalam ekosistem perairan,
pantai dan laut. Sebagian larut dalam air, sebagian tenggelam ke dasar laut, dan
sebagian masuk kedalam jaringan tubuh organisme laut (termasuk fitoplankton,
ikan, udang, cumi-cumi, kerang, dan lain-lain) (Purnomo, 2009).
Berdasarkan penelitian lain tentang kadar logam Cd pada kerang yang
terdapat di perairan belawan adalah 0,4310 mcg/g (Nurjanah, 2009). Kadar logam
Kadmium (Cd) ini terus meningkat, karena begitu pesatnya pertumbuhan industri
yang ada di sekitar perairan belawan tersebut dan menyebabkan pembuangan
limbah pabrik ke laut belawan juga akan semakin meningkat dari hari ke hari.
Akibatnya kadar logam Kadmium (Cd) dalam kerang darah (Anadara granosa)
dalam hasil orientasi ini meningkat yaitu menjadi 2,2161 mcg/g, kadarnya lebih
tinggi dibandingkan dengan penelitian-penelitian sebelumnya. Sedangkan
menurut SNI 7387-2009, batas maksimum cemaran logam Kadmium (Cd) pada
kerang-kerangan (bivalvia) sebesar 1,0 mcg/g.
Kerang adalah salah satu makanan laut yang banyak dikonsumsi dan
diminati masyarakat karena mengandung protein, vitamin, mineral, lemak tak
jenuh yang sangat diperlukan untuk pertumbuhan dan kecerdasan. Keberadaannya
pengaruh pencemaran akibat air laut yang tercemar dibandingkan ikan yang
cenderung berpindah-pindah (Anonima, 2005).
Dasar pertimbangan untuk meneliti kadar Kadmium (Cd) dalam kerang
darah adalah karena logam tersebut merupakan logam yang bersifat toksik dan
mengingat kadar logam Kadmium (Cd) dalam perairan belawan telah melewati
baku mutu yang diizinkan. Disamping itu karena banyaknya industri-industri yang
berada di sekitar perairan belawan seperti industri pabrik bahan kimia, industri
cat, baterai, pabrik pipa PVC dan lain-lain (PT. Pelindo I, 2004).
Pada umumnya masyarakat Indonesia menggunakan buah jeruk nipis
(Citrus aurantifolia Swingle) untuk menghilangkan bau amis pada makanan yang
berasal dari laut, namun banyak masyarakat kita yang belum mengetahui bahwa
buah jeruk nipis yang rasanya sangat asam itu mengandung beberapa senyawa
organik seperti asam sitrat, yang berguna sebagai chelator (pengikat logam)
terhadap logam yang terdapat pada hewan laut tersebut (Sarwono, 2001).
Berdasarkan uraian diatas, maka penulis tertarik untuk melakukan
penelitian tentang pengaruh perebusan kerang darah selama 1 menit dan 15 menit
dalam akuades dan larutan jeruk nipis untuk menurunkan logam berat Kadmium
(Cd) pada kerang darah dan menentukan kadarnya dengan Spektrofotometer
Serapan Atom.
Kerang darah dipilih sebagai sampel karena jenis kerang ini merupakan
indikator yang baik dalam memonitor suatu pencemaran lingkungan oleh logam.
Hal tersebut disebabkan oleh sifat kerang yang menetap dalam suatu habitat
tertentu yaitu di dasar laut sehingga proses biokonsentrasi dan bioakumulasi
1.2Perumusan Masalah
Apakah perebusan dalam akuades dan larutan jeruk nipis selama 1 menit dan
15 menit dapat menurunkan kadar logam Kadmium (Cd) pada kerang darah?
1.3Hipotesis
Perebusan dalam akuades dan larutan jeruk nipis selama 1 menit dan 15 menit
dapat menurunkan kadar logam Kadmium (Cd) pada kerang darah.
1.4Tujuan Penelitian
Untuk mengetahui penurunan kadar logam Kadmium (Cd) pada kerang darah
setelah perebusan dalam akuades dan larutan jeruk nipis selama 1 menit dan 15
menit.
1.5 Manfaat Penelitian
Hasill penelitian ini dapat dimanfaatkan oleh masyarakat untuk menurunkan
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Kerang Darah (Anadara granosa)
Menurut data produksi Statistik Perikanan Indonesia (1994), kerang
(bivalvia) tersebar luas di seluruh perairan Indonesia seperti:Bengkulu, Jawa,
Nusa Tenggara Timur, Kalimantan Barat, Kalimantan Selatan, Kalimantan Timur,
Sulawesi Selatan, Maluku dan Irian Jaya (Djamali, 1998).
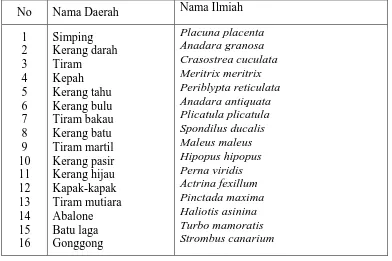
Beberapa jenis kerang-kerangan yang memiliki nilai ekonomis dapat dilihat
pada tabel dibawah ini:
Tabel 1. Jenis-jenis kerang yang bernilai ekonomis penting yang ada di perairan Indonesia.
Jenis-jenis kerang yang sering menjadi konsumsi masyarakat, yaitu kerang
darah (Anadara granosa), kerang bulu (Anadara antiquata), kerang hijau (Mytilus
Kerang Anadara terdapat di pantai laut pada substrat lumpur berpasir dengan
kedalaman 10 m sampai 30 m. Kerang Anadara termasuk kedalam subkelas
Lamellibranchia, dimana filament insang memanjang dan melipat, seperti huruf
W, antar filamen dihubungkan oleh cilia (filiaranchia) atau jaringan
(eulamellibranchia). Anadara juga merupakan ordo Toxodonta, dimana gigi pada
hinge banyak dan sama, kedua otot aduktor berukuran kurang lebih sama,
pertautan antar filament insang tidak ada (Oemarjati, 1990).
Anadara granosa hidup dengan cara membenamkan diri di pantai-pantai
yang berpasir. Anadara granosa umumnya dikenal dengan nama “kerang darah”
(Oemarjati, 1990).
Kerang darah (Anadara granosa) dan kerang bulu (Anadara antiquata)
adalah famili arcidae dan genus anadara. Secara umum kedua kerang ini memiliki
morfologi yang hampir sama. Cangkang memiliki belahan yang sama melekat
satu sama lain pada batas cangkang (Sudrajat, 2008).
Perbedaan dari kedua kerang ini adalah morfologi cangkangnya. Kerang bulu
(Anadara antiquata) memiliki cangkang yang ditutupi oleh rambut-rambut serta
cangkang tersebut lebih tipis daripada kerang darah (Anadara granosa). Kerang
darah memiliki cangkang yang lebih tebal, lebih kasar, lebih bulat dan bergerigi di
bagian puncaknya serta tidak ditumbuhi oleh rambut-rambut (Suwignyo, 2005).
Kerang darah (Anadara granosa) adalah sejenis kerang yang biasa dimakan
oleh warga Asia Timur dan Asia Tenggara. Anggota famili arcidae ini disebut
kerang darah karena menghasilkan hemoglobin dalam cairan merah yang
Budidaya kerang darah sudah dilakukan dan ia memiliki nilai ekonomi yang
baik. Meskipun biasanya direbus atau dikukus, kerang ini dapat pula digoreng
atau dijadikan sate. Ada pula yang memakannya mentah (Anonimb, 2010).
2.2 Uraian Jeruk Nipis (Citrus aurantifolia Swingle) Klasifikasi ilmiah
Kerajaan : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledone
Ordo : Rutales
Famili : Rutacea
Genus : Citrus
Spesies : Citrus aurantifolia Swingle
(Sarwono, 2001)
Jeruk nipis termasuk tipe buah buni. Bentuknya bulat sampai bulat telur.
Diameter buahnya sekitar 3-6 cm. Ketebalan kulit buahnya berkisar 0,2-0,5 mm.
Pohonnya tumbuh sebagai pohon kecil bercabang lebat, tetapi tak beraturan.
Tinggi pohon berkisar antara 1,5-5 m. Ranting-rantingnya berduri pendek, kaku,
dan tajam. Daunnya berselang-seling berbentuk jorong sampai bundar, pinggiran
daunnya bergerigi kecil (Sarwono, 2001).
Jeruk nipis memiliki rasa yang sangat asam, karena kandungan asam sitratnya
tinggi. Rasa jeruk nipis yang sangat asam itu membuat jeruk nipis tidak dapat
2.3Asam Sitrat
Rumus struktur asam sitrat:
Asam sitrat memiliki sifat asam-basa yang dapat dilihat dari nilai pKa nya,
yaitu:
1. pKa1 : 3,13
2. pKa2 : 4,76
3. pKa3 : 6,40 (Karlaganis, 2000)
Asam sitrat merupakan asam organik lemah yang ditemukan pada daun dan
buah tumbuhan genus Citrus (jeruk-jerukan). Senyawa ini merupakan bahan
pengawet yang baik dan alami, selain digunakan sebagai penambah rasa masam
pada makanan dan minuman ringan (Anonimc, 2010).
Asam sitrat terdapat pada berbagai jenis buah dan sayuran, namun paling
banyak ditemukan pada jeruk lemon dan limau (misalnya jeruk nipis dan jeruk
purut) (Anonimc, 2010).
Ion sitrat dapat bereaksi dengan banyak ion logam membentuk garam sitrat.
Selain itu, sitrat dapat mengikat ion-ion logam dengan membentuk kompleks,
sehingga dapat menghilangkan ion-ion logam yang terakumulasi sebagai
kompleks sitrat (Anonimc, 2010).
2.4Pencemaran Laut
Kehidupan manusia di bumi ini sangat bergantung pada lautan, manusia
harus menjaga kebersihan dan kelangsungan kehidupan organisme yang hidup di
asing dan pengendapan barang sisa yang diproduksi oleh manusia. Lautan juga
merupakan tempat bahan-bahan yang terbawa oleh air dari daerah pertanian dan
limbah rumah tangga, sampah dan bahan buangan dari kapal, tumpahan minyak
dari kapal tanker dan pengeboran minyak lepas pantai, dan masih banyak lagi
bahan yang terbuang ke lautan (Darmono, 2001).
Lautan dapat melarutkan dan menyebarkan bahan-bahan tersebut sehingga
konsentrasinya menjadi menurun, terutama di daerah laut dalam. Kehidupan laut
dalam juga terbukti lebih sedikit terpengaruh daripada laut dangkal. Daerah
pantai, terutama daerah muara sungai, sering mengalami pencemaran berat, yang
disebabkan karena proses pencemaran yang berjalan sangat lambat (Darmono,
2001).
2.5Logam Berat
Logam berat masih termasuk golongan logam dengan kriteria-kriteria yang
sama dengan logam-logam lain. Perbedaanya terletak dari pengaruh yang
dihasilkan bila logam berat ini masuk kedalam tubuh organisme hidup. Unsur
logam berat baik itu logam berat beracun seperti Kadmium (Cd), bila masuk
kedalam tubuh dalam jumlah berlebihan akan menimbulkan pengaruh-pengaruh
buruk terhadap fungsi fisiologis tubuh (Palar, 2008).
Berbeda dengan logam biasa, logam berat biasanya menimbulkan efek-efek
khusus pada makhluk hidup. Dapat dikatakan bahwa semua logam berat dapat
menjadi bahan racun yang akan meracuni tubuh makhluk hidup (Palar, 2008).
Di Indonesia, pencemaran logam berat cenderung meningkat sejalan dengan
bisa menimbulkan bahaya bagi kesehatan, baik pada manusia, hewan, tanaman,
maupun lingkungan. Logam berat dibagi dalam 2 jenis, yaitu:
1. Logam berat esensial, yakni logam dalam jumlah tertentu yang sangat
dibutuhkan oleh organisme. Dalam jumlah yang berlebihan logam tersebut bisa
menimbulkan efek toksik. Contohnya adalah Zn, Cu, Fe, Co, Mn dan lain
sebagainya (Widowati, 2008).
2. Logam berat tidak esensial, yakni logam yang keberadaannya dalam tubuh
masih belum diketahui manfatnya, bahkan bersifat toksik, seperti Hg, Cd, Pb,
Cr, dan lain-lain (Widowati, 2008).
2.5.1Kadmium (Cd)
Kadmium (Cd) adalah logam berwarna putih perak, lunak, mengkilap, tidak
larut dalam basa, mudah bereaksi, serta menghasilkan Kadmium oksida bila
dipanaskan. Kadmium (Cd) umumnya terdapat dalam kombinasi dengan klor (Cd
klorida) atau belerang (Cd Sulfit). Kadmium bisa membentuk Cd2+ yang bersifat
tidak stabil. Kadmium (Cd) memiliki nomor atom 48, berat atom 112,4 g/mol,
titik leleh 321oC, dan titik didih 767oC (Widowati, 2008).
Logam Kadmium (Cd) akan mengalami proses biotransformasi dan
bioakumulasi dalam organisme hidup (tumbuhan, hewan, dan manusia). Logam
ini masuk kedalam tumbuhan bersama makanan yang dikonsumsi, tetapi makanan
tersebut telah terkontaminasi oleh logam Kadmium (Cd) dan atau persenyawaan.
Dalam tubuh biota perairan jumlah logam yang terakumulasi akan terus
mengalami peningkatan. Disamping itu, tingkatan biota dalam sistem rantai
makanan turut menentukan jumlah Kadmium (Cd) yang terakumulasi (Darmono,
Sumber pencemaran dan paparan Kadmium (Cd) berasal dari polusi udara,
rokok, air sumur, makanan yang tumbuh di daerah pertanian yang tercemar
Kadmium (Cd), fungisida, pupuk, serta cat. Paparan dan toksisitas Kadmium (Cd)
berasal dari rokok, tembakau, pipa rokok yang mengandung Kadmium (Cd),
perokok pasif, plastik berlapis Kadmium (Cd), serta air minum (Widowati,
20008).
Kadmium (Cd) banyak digunakan sebagai pigmen warna cat, keramik,
plastik, industri baterai, bahan fotografi, pembuatan tabung TV, PVC, dan
percetakan tekstil (Widowati, 2008).
Kasus toksisitas Kadmium (Cd) dilaporkan sejak pertengahan tahun 1980-an
dan kasus tersebut semakin meningkat sejalan dengan perkembangan ilmu kimia
di akhir abad 20-an. Sampai sekarang diketahui bahwa Kadmium (Cd) merupakan
logam berat yang paling banyak menimbulkan toksisitas pada makhluk hidup
(Darmono, 2001).
Logam berat Kadmium (Cd) bisa masuk kedalam tubuh hewan atau manusia
melalui berbagai cara, yaitu:
1. Melalui udara yang tercemar, misalnya asap rokok dan asap pembakaran
batu bara
2. Melalui wadah/tempat berlapis Kadmium (Cd) yang digunakan sebagai
tempat makanan dan minuman
3. Melalui kontaminasi perairan dan hasil pertanian yang tercemar Kadmium
2.6Toksisitas Logam Pada Jenis Kerang
Hewan air jenis kerang-kerangan (bivalvia) atau jenis binatang lunak
(moluska), baik jenis klam (kerang besar) atau oister (kerang kecil),
pergerakannya sangat lambat di dalam air. Mereka biasanya hidup menetap di
suatu lokasi tertentu di dasar air (Darmono, 2001).
Jenis kerang baik yang hidup di air tawar maupun di air laut banyak
digunakan sebagai indikator pencemaran logam. Hal ini disebabkan karena habitat
hidupnya yang menetap atau sifat bioakumulatifnya terhadap logam berat. Karena
kerang banyak dikonsumsi oleh manusia maka sifat bioakumulatif inilah yang
menyebabkan kerang harus diwaspadai bila dikonsumsi terus-menerus (Darmono,
2001).
Logam berat dapat juga terakumulasi pada jaringan kerang. Kerang dapat
mengakumulasi logam lebih besar daripada hewan air lainnya karena sifatnya
yang menetap, lambat untuk dapat menghindarkan diri dari pengaruh polusi, dan
mempunyai toleransi yang tinggi terhadap konsentrasi logam tertentu. Karena itu
jenis kerang ini merupakan indikator yang sangat baik untuk memonitor suatu
pencemaran lingkungan (Darmono, 2001).
2.7Pengikatan Logam
Logam-logam pada umumnya dapat membentuk ikatan dengan bahan-bahan
organik alam maupun bahan-bahan organik buatan. Proses pembentukan ikatan
tersebut dapat terjadi melalui pembentukan garam organik dengan gugus
karboksilat seperti misalnya asam sitrat, tartrat, dan lain-lain. Disamping itu,
logam dapat berikatan dengan atom-atom yang mempunyai elektron bebas dalam
2.8Destruksi Basah
Teknik destruksi basah adalah dengan memanaskan sampel organik dengan
penambahan asam mineral pengoksidasi atau campuran dari asam-asam mineral
tersebut. Penambahan asam mineral pengoksidasi dan pemanasan yang cukup
dalam beberapa menit dapat mengoksidasi sampel secara sempurna, sehingga
menghasilkan ion logam dalam larutan asam sebagai sampel anorganik untuk
dianalisis selanjutnya. Destruksi basah biasanya menggunakan H2SO4, HNO3, dan
HClO4 atau campuran dari ketiga asam mineral tersebut (Anderson, 1987).
2.9 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu metode yang digunakan untuk
mendeteksi atom-atom logam dalam fase gas. Metode ini sering kali
mengandalkan nyala untuk mengubah logam dalam larutan sampel menjadi
atom-atom logam berbentuk gas yang digunakan untuk analisis kuantitatif dari logam
dalam sampel (Bender, 1987).
Spektrofotometri serapan atom digunakan untuka analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace).
Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan
tidak tergantung pada bentuk molekul logam dalam sampel tersebut. Cara ini
cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi
(batas deteksi kurang dari 1 ppm), dan pelaksanaanya relatif sederhana.
Spektrofotometri atom didasarkan pada penyerapan energi sinar oleh atom-atom
netral, dan sinar yang diserap biasanya sinar tampak atau ultraviolet. Dalam garis
spektrofotometri sinar tampak dan ultraviolet. Perbedaan terletak pada bentuk
spektrum, cara pengerjaan sampel dan peralatanya (Rohman, 2007).
Metode spektrofotometri serapan atom berdasarkan pada prinsip absorbsi
cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang
tertentu, tergantung pada sifat unsurnya (Rohman, 2007).
Kelemahan spektrofotometri serapan atom adalah sampel harus dalam
bentuk larutan dan tidak mudah menguap dan satu lampu katoda hanya digunakan
untuk satu unsur saja (Fifield, 1983).
2.9.1 Instrumen Spektrofotometer Serapan atom
a. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari
logam dan dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas
mulia (neon atau argon). Bila antara anoda dan katoda diberi selisih tegangan
yang tinggi (600 volt), maka katoda akan memacarkan berkas-berkas elektron
yang bergerak menuju anoda yang mana kecepatan dan energinya sangat tinggi.
akan bertabrakan dengan gas-gas mulia yang diisikan tadi. Akibat dari
tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan
menjadi bermuatan positif. Ion-ion gas mulia yang bermuatan positif ini
selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi
pula. Pada katoda terdapat unsur-unsur yang sesuai dengan unsur yang akan
dianalisis. Unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat
tabrakan ini, unsur-unsur akan terlempar keluar dari permukaan katoda.
Atom-atom unsur dari katoda ini mungkin akan mengalami eksitasi ke tingkat
energi-energi elektron yang lebih tinggi dan akan memancarkan spektrum pancaran dari
unsur yang sama dengan unsur yang akan dianalisis (Rohman, 2007).
b. Monokromator
Monokromator dimaksudkan untuk memisahkan dan memilih panjang
gelombang yang digunakan dalam analisis. Dalam monokromator terdapat
chopper (pemecah sinar), suatu alat yang berputar dengan frekuensi atau
kecepatan perputaran tertentu (Rohman, 2007).
c. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat
pengatoman. Biasanya digunakan tabung penggandaan foton (photomultiplier
tube) (Rohman, 2007).
d. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang
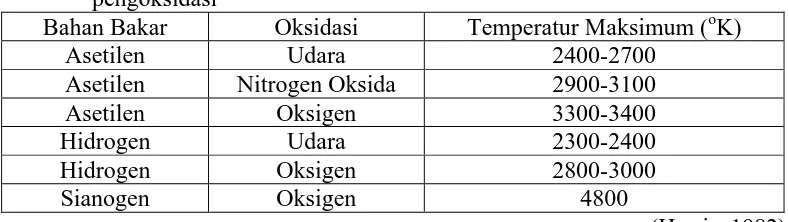
2.9.2 Bahan Bakar dan Bahan Pengoksidasi
Umumnya bahan bakar yang digunakan adalah hidrogen, asetilen, dan
propan, sedangkan oksidatornya adalah udara, oksigen, dan NO2, temperatur dari
berbagai nyala dapat dilihat pada tabel berikut ini:
Tabel 2. Temperatur nyala dengan berbagai kombinasi bahan bakar dan bahan pengoksidasi
Bahan Bakar Oksidasi Temperatur Maksimum (oK)
Asetilen Udara 2400-2700
Asetilen Nitrogen Oksida 2900-3100
Asetilen Oksigen 3300-3400
Hidrogen Udara 2300-2400
Hidrogen Oksigen 2800-3000
Sianogen Oksigen 4800
(Harris, 1982)
2.9.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) yang ada pada AAS adalah
peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis
menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya
dalam sampel (Rohman, 2007).
Gangguan-gangguan yang dapat terjadi dalam AAS adalah sebagai berikut:
1. Gangguan yang berasal dari matriks sampel yang dapat mempengaruhi
banyaknya sampel yang mencapai nyala.
Sifat-sifat tertentu matriks sampel dapat mengganggu analisis yakni
matriks tersebut dapat berpengaruh terhadap laju aliran bahan bakar/gas
pengoksidasi. Sifat-sifat tersebut adalah:viskositas, tegangan permukaan, berat
jenis, dan tekanan unsur (Rohman, 2007).
Gangguan matriks yang lain adalah pengendapan unsur yang dianalisis sehingga
jumlah atom yang mencapai nyala menjadi lebih sedikit dari konsentrasi yang
2. Gangguan kimia yang dapat mempengaruhi jumlah/banyaknya atom yang
terjadi didalam nyala.
Terbentuknya atom-atom netral yang masih dalam keadaan azas di dalam
nyala sering terganggu oleh dua peristiwa kimia, yaitu :
a. Disosiasi senyawa-senyawa yang tidak sempurna (Rohman, 2007).
b. Ionisasi atom-atom di dalam nyala (Rohman, 2007).
3. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang
dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di
dalam nyala (Rohman, 2007).
2.10 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita,
2004).
2.10.1 Uji Perolehan Kembali (Recovery Test)
Persen uji perolehan kembali digunakan untuk menyatakan kecermatan.
Kecermatan merupakan ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit sebenarnya (Harmita, 2004).
Menurut Miller (2005), suatu metode dikatakan teliti jika nilai
recoverynya antara 80-120%. Recovery dapat ditentukan dengan menggunakan
metode standar adisi (Miller, 2005).
Metode standar adisi adalah menambahkan sejumlah tertentu larutan
2.10.2 Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkeci analit dalam sampel yang dapat
dideteksi. Batas deteksi merupakan parameter uji batas (Harmita, 2004).
Batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang
BAB III
METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Pelaksanaan Penelitian
Penelitian ini dilaksanakan di laboratorium Kimia Farmasi Kuantitatif
Fakultas Farmasi Universitas Sumatera Utara dan Pusat Penelitian Kelapa Sawit
(PPKS) Medan.
3.2 Bahan-bahan 3.2.1 Sampel
Sampel yang diperiksa dalam penelitian ini adalah kerang darah (Anadara
granosa) yang berasal dari perairan laut belawan.
3.2.2 Pereaksi
Bahan yang digunakan semua pro analisis keluaran E.Merck, kecuali
disebutkan lain, yaitu asam nitrat 65% b/b, asam sulfat 95% b/b, ammonium
hidroksida 25% b/b, dithizon, kloroform, larutan jeruk nipis (dibuat sendiri),
akuades (Lab. Kimia Farmasi Kuantitatif), akuabides (IKA), dan larutan standar
Cd 1000 ppm.
3.3 Alat
Alat-alat yang digunakan yaitu Spektrofotometer Serapan Atom (GBC
Avanta ∑) dengan nyala udara asetilen, neraca analitik (Boeco Germany), neraca
kasar, blender, spatula, penangas air, kaki tiga, bunsen gas, selang gas, dan
3.4 Pembuatan Pereaksi 1. Larutan HNO3 5N
Larutan HNO3 65% b/b sebanyak 340 ml diencerkan dengan air suling
hingga 1000 ml (Ditjen POM, 1995).
2. Larutan Dithizon 0,005% b/v
Dithizon sebanyak 5 mg dilarutkan dalam 100 ml kloroform (Vogel,
1990).
3. Larutan NH4OH 1N
Ammonium hidroksida 25% b/b sebanyak 7,4 ml diencerkan dalam 100 ml
air suling (Ditjen POM, 1995).
4. Larutan Jeruk Nipis (Citrus aurantifolia Swingle)
Delapan buah jeruk nipis ( 285 gram) diperas, lalu air perasan jeruk nipis
3.5 Rancangan Penelitian
Cara Penelitian dilakukan berdasarkan bagan berikut ini:
Kerang darah dengan kadar Cd tinggi
3.6Prosedur Penelitian 3.6.1 Pengambilan sampel
Metode pengambilan sampel dilakukan secara sampling purposif yang
dikenal juga sebagai sampling pertimbangan dimana pengambilan sampel
dilakukan berdasarkan pertimbangan bahwa semua jenis kerang darah yang dijual
di daerah Pantai Belawan adalah homogen.
3.6.2Penyiapan Sampel
Kerang darah sebanyak 2 kg dicuci bersih, dan dibagi menjadi 5 bagian.
Bagian pertama (400 gram) dikeluarkan daging kerang dari cangkangnya, dicuci
bersih, lalu ditiriskan selama 15 menit. Setelah itu diblender hingga halus. Sampel
yang telah halus ditimbang sebanyak 10 gram (sampel tanpa perebusan).
Bagian Kedua (400 gram) kerang dicuci bersih. Setelah kerang dicuci bersih,
dididihkan akuades terlebih dahulu. Setelah akuades mendidih, dimasukkan
kerang yang telah bersih kedalamnya dan direbus selama 1 menit. Setelah 1 menit,
kerang diangkat dan ditiriskan hingga dingin lalu dikeluarkan daging kerang dari
cangkangnya. Setelah itu diblender hingga halus. Sampel yang telah halus
ditimbang sebanyak 10 gram (sampel dengan perebusan dalam akuades
selama 1 menit).
Bagian ketiga (400 gram) kerang dicuci bersih. Setelah kerang dicuci bersih,
dididihkan akuades terlebih dahulu. Setelah akuades mendidih, dimasukkan
kerang yang telah bersih kedalamnya dan direbus selama 15 menit. Setelah 15
menit, kerang diangkat dan ditiriskan hingga dingin lalu dikeluarkan daging
halus ditimbang sebanyak 10 gram (sampel dengan perebusan dalam akuades
selama 15 menit).
Bagian Keempat (400 gram) kerang dicuci bersih. Setelah kerang dicuci
bersih, dididihkan larutan jeruk nipis terlebih dahulu. Setelah larutan jeruk nipis
mendidih, dimasukkan kerang yang telah bersih kedalamnya dan direbus selama 1
menit. Setelah 1 menit, kerang diangkat dan ditiriskan hingga dingin lalu
dikeluarkan daging kerang dari cangkangnya. Setelah itu diblender hingga halus.
Sampel yang telah halus ditimbang sebanyak 10 gram (sampel dengan
perebusan dalam larutan jeruk nipis selama 1 menit).
Bagian kelima (400 gram) kerang dicuci bersih. Setelah kerang dicuci
bersih, dididihkan larutan jeruk nipis terlebih dahulu. Setelah larutan jeruk nipis
mendidih, dimasukkan kerang yang telah bersih kedalamnya dan direbus selama
15 menit. Setelah 15 menit, kerang diangkat dan ditiriskan hingga dingin lalu
dikeluarkan daging kerang dari cangkangnya. Setelah itu diblender hingga halus.
Sampel yang telah halus ditimbang sebanyak 10 gram (sampel dengan
perebusan dalam larutan jeruk nipis selama 15 menit).
3.6.3Proses Destruksi Basah Untuk Kadmium (Modifikasi dari Haswell, 1991)
Sampel kerang yang telah dihaluskan untuk setiap perlakuan, ditimbang
masing-masing sebanyak 10 gram dalam erlenmeyer. Sampel yang telah diketahui
beratnya selanjutnya ditambahkan H2SO4 (p) sebanyak 5 ml. Lalu ditambahkan
HNO3 (p) sebanyak 20 ml dan diamkan selama 24 jam. Setelah 24 jam, sampel di
destruksi di penangas air hingga larutan sampel berwarna kuning jernih.
Kemudian dipindahkan kedalam labu tentukur 100 ml dan ditepatkan sampai
dengan membuang 10 ml larutan pertama hasil penyaringan. Larutan hasil
destruksi ini digunakan untuk uji kualitatif dan uji kuantitatif logam Kadmium
(Cd).
3.6.4Analisa Kualitatif
Kedalam tabung reaksi dimasukkan 2 ml larutan sampel, diatur pH=12
dengan penambahan ammonium hidroksida 1 N, ditambahkan 2 ml dithizon
0,005% b/v, dikocok kuat, dibiarkan larutan memisah. Terbentuk warna merah
muda berarti sampel mengandung Cd (Fries, 1977).
3.6.5Analisa Kuantitatif
3.6.5.1Penentuan Panjang Gelombang Maksimum
Penentuan panjang gelombang maksimum dilakukan berdasarkan
pengaturan alat spektrofotometer serapan atom yang telah di standardisasi, yaitu
panjang gelombang untuk logam Kadmium (Cd) 228,8 nm.
3.6.5.2Penentuan Kurva Kalibrasi Logam Kadmium (Cd)
Larutan standar Kadmium (Cd) (1000 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan ke dalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3
5N, ditepatkan sampai garis tanda dengan akuabides (konsentrasi 100 mcg/ml).
Larutan standar Kadmium (Cd) (100 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan kedalam labu tentukur 100 ml, kemudian ditambahkan 10 ml HNO3
5N, ditepatkan sampai garis tanda dengan akuabides (konsentrasi 10 mcg/ml).
Larutan kerja Kadmium (Cd) dibuat dengan memipet 0,5; 1; 2; 4; 6 ml
larutan baku 10 mcg/ml, dimasukkan kedalam labu tentukur 100 ml, ditambahkan
(larutan kerja ini mengandung 0,05; 0,1; 0,2; 0,4; dan 0,6 mcg/ml) dan diukur
pada panjang gelombang 228,8 nm.
3.6.5.3 Penentuan Kadar logam Dalam Kerang Darah
Larutan sampel yang telah didestruksi diukur absorbansinya dengan spektrofotometer serapan atom pada panjang gelombang 228,8 nm.
Nilai absorbansi yang diperoleh berada dalam rentang kurva kalibrasi
larutan baku Kadmium (Cd). Konsentrasi Kadmium (Cd) dalam sampel
ditentukan berdasarkan persamaan linier dari kurva kalibrasi. Kadar logam
kadmium (Cd) dalam sampel dapat dihitung dengan cara sebagai berikut:
Kadar logam (mcg/g)
3.6.5.4Uji Perolehan Kembali (Recovery Test) 3.6.5.4.1Pembuatan Larutan Standar
Larutan standar Kadmium (Cd) (1000 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan larutan kedalam labu tentukur 100 ml, kemudian ditambahkan 10 ml
HNO3 5N, ditepatkan sampai garis tanda dengan akuabides (konsentrasi 100
mcg/ml).
Larutan standar Kadmium (Cd) (100 mcg/ml) dipipet sebanyak 10 ml,
dimasukkan larutan kedalam labu tentukur 100 ml, kemudian ditambahkan 10 ml
HNO3 5N, ditepatkan sampai garis tanda dengan akuabides (konsentrasi 10
mcg/ml).
3.6.5.4.2Prosedur Uji Perolehan Kembali (Recovery Test)
Uji perolehan kembali dilakukan dengan cara menentukan kadar logam
dalam sampel, selanjutnya dilakukan penentuan kadar logam dalam sampel
Larutan standar yang ditambahkan yaitu 0,5 ml larutan standar Kadmium (Cd)
(konsentrasi 10 mcg/ml). Uji perolehan kembali dilakukan terhadap sampel yang
sama dan dianalisa dengan cara yang sama dengan pengerjaan sampel awal.
Persen uji perolehan kembali dapat dihitung dengan persamaan berikut:
=
3.6.5.5Analisa Data Secara Statistik
Untuk menentukan kadar logam di dalam sampel dengan interval
kepercayaan 95%, α = 0,05, dk = n-1 , dapat digunakan rumus:
Kadar logam = μ = ( (α/2, dk) x SD / )
Keterangan : = Kadar rata-rata sampel
SD = Standar deviasi
dk = Derajat kebebasan (dk = n-1)
α = interval kepercayaan
n = jumlah pengulangan (Wibisono, 2005)
Untuk menentukan standar deviasi dapat digunakan rumus:
SD =
(Sudjana, 2002)
Untuk menentukan data diterima atau ditolak, dapat digunakan rumus:
t hitung =
Data diterima jika -ttabel thitung ttabel
Keterangan : Xi = Kadar Sampel n = jumlah pengulangan
3.6.5.6 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama.
Batas deteksi dan batas kuantitasi ini dapat diperoleh dari kalibrasi standar
yang diukur sebanyak 6 sampai 10 kali, dan dapat dihitung dengan rumus sebagai
berikut (Harmita, 2004):
Batas deteksi =
Batas kuantitasi =
Keterangan : SB = Simpangan Baku
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Uji Kualitatif
Untuk mengidentifikasi adanya logam berat di dalam kerang darah, maka
dilakukan uji kualitatif dengan menggunakan pereaksi dithizon 0,005% b/v.
Tabel 3. Hasil Uji Kualitatif Logam Kadmium (Cd) dengan Pereaksi Dithizon 0,005% b/v
No Logam pH Reaksi dengan Larutan
Dithizon Sampel Hasil
1 Cd 12 Merah Muda
+ :Mengandung Logam
KTP :Kerang darah tanpa perebusan
KPA :Kerang darah dengan perebusan dalam akuades selama 1 menit KPA 15’ :Kerang darah dengan perebusan dalam akuades selama 15 menit KPJ :Kerang darah dengan perebusan dalam larutan jeruk nipis selama
1 menit
KPJ 15’ :Kerang darah dengan Perebusan dalam larutan jeruk nipis selama 15 menit
Tabel diatas menunjukkan adanya logam berat Kadmium (Cd) yang
terdapat di dalam kerang darah. Dimana dengan reaksi dithizon 0,005% b/v pada
pH 12 menghasilkan warna merah muda. Warna yang terbentuk adalah karena
terbentuknya kompleks logam dithizonat (Fries, 1997).
4.2 Hasil Uji Kuantitatif
4.2.1 Kurva Kalibrasi Logam Kadmium (Cd)
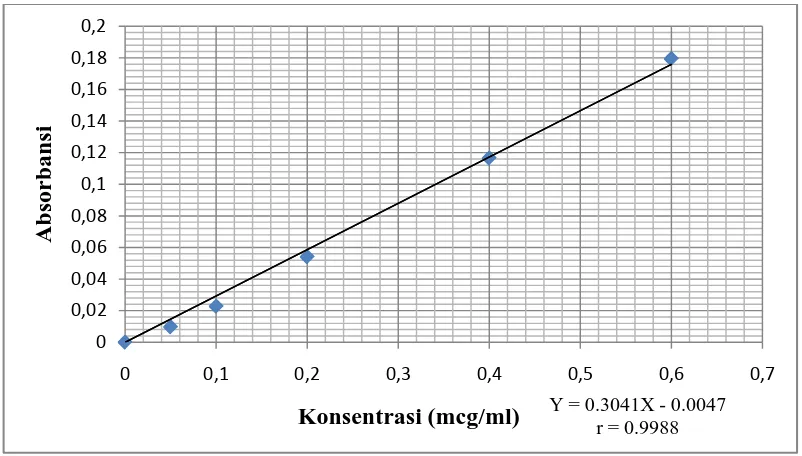
Gambar 2. Kurva Kalibrasi Logam Kadmium (Cd)
Berdasarkan data kalibrasi logam Kadmium (Cd) pada gambar 2 diperoleh
persamaan garis regresi yang linier yaitu: Y = 0,3041X - 0,0047 dengan nilai
koefisien korelasi (r) sebesar 0,9988 (data dapat dilihat pada lampiran 3). Contoh
perhitungan persamaan regresi dapat dilihat pada lampiran 4.
Nilai koefisien korelasi ini menunjukkan hubungan korelasi yang positif
antara konsentrasi dengan absorbansi yang berarti dengan meningkatnya
konsentrasi logam maka absorbansi juga meningkat (Rohman, 2007).
4.2.2 Analisa Kadar Logam Kadmium (Cd) dalam Kerang Darah Sebelum dan Sesudah Perebusan dalam Akuades dan Larutan Jeruk Nipis Selama 1 menit dan 15 menit
Data hasil penetapan kadar logam Kadmium (Cd) dalam sampel, dapat
dilihat pada tabel 4 dibawah ini. Konsentrasi logam Kadmium (Cd) dalam sampel
ditentukan berdasarkan persamaan garis regresi linier kurva kalibrasi larutan
standar Kadmium (Cd). Data dan perhitungan dapat dilihat pada lampiran 5 -
Tabel 4. Data Kadar Logam Kadmium (Cd) Dalam Sampel
Keterangan : Data diatas rata-rata dari 6 kali pengulangan KTP :Kerang darah tanpa perebusan
KPA :Kerang darah dengan perebusan dalam akuades selama 1 menit KPA 15’ :Kerang darah dengan perebusan dalam akuades selama 15 menit KPJ :Kerang darah dengan perebusan dalam larutan jeruk nipis selama
1 menit
KPJ 15’ :Kerang darah dengan perebusan dalam larutan jeruk nipis selama 15 menit
Dari data pada tabel 4 menunjukkan bahwa kadar rata-rata logam
Kadmium (Cd) tanpa perebusan menggunakan akuades dan larutan jeruk nipis
adalah 2,2432 0,0060 mcg/g. Nilai ini lebih besar daripada kadar logam
Kadmium (Cd) setelah perebusan dalam akuades selama 1 menit (2,0594 0,0449
mcg/g) dan 15 menit (1,4967 0,0083 mcg/g). Begitu juga kadar logam Kadmium
(Cd) akan semakin menurun setelah kerang darah direbus dalam larutan jeruk
nipis selama 1 menit (0,9614 0,0143 mcg/g) dan 15 menit (0,6678 0,0011
mcg/g). Menurut SNI 7387-2009, batas maksimum cemaran logam Kadmium
(Cd) pada kerang (bivalvia) sebesar 1,0 mcg/g. Dengan demikian, kadar logam
Kadmium (Cd) pada kerang darah tanpa perebusan telah melebihi ambang batas
maksimum yang diperbolehkan. Dengan adanya perebusan selama 1 menit dan 15
menit dalam akuades, dapat menurunkan kadar logam Kadmium (Cd). Walaupun
penurunan kadar logam Kadmium (Cd) dalam kerang darah tersebut masih belum
efektif karena masih melebihi kadar maksimum yang diperbolehkan untuk
dalam larutan jeruk nipis selama 1 menit dan 15 menit, kadar logam Kadmium
(Cd) menjadi lebih rendah dibawah kadar maksimum yang diperbolehkan.
Sehingga larutan jeruk nipis ini efektif untuk menurunkan kadar logam Kadmium
(Cd).
Terjadinya penurunan kadar logam Kadmium (Cd) dalam kerang darah
(Anadara granosa) setelah perebusan dengan akuades, disebabkan karena
komponen metallothionine yang terdapat dalam daging kerang darah (Anadara
granosa) mengalami degradasi (Nurjanah, dkk; 2005). Degradasi merupakan
suatu pemecahan protein dari ikatan-ikatan yang terdapat di dalamnya. Salah
satunya adalah Metallothionine, yang mempunyai kemampuan mengikat
logam-logam yang dapat bersifat toksik seperti Kadmium (Anonimd, 2010).
Terjadinya penurunan kadar logam Kadmium (Cd) dalam kerang darah
(Anadara granosa) setelah perebusan dalam larutan jeruk nipis disebabkan karena
dalam larutan jeruk nipis tersebut mengandung beberapa senyawa organik (seperti
asam sitrat) yang memiliki kemampuan sebagai chelator (pengikat logam). Kadar
logam Kadmium (Cd) akan terus menurun setelah kerang direbus dalam larutan
jeruk nipis selama 15 menit. Hal ini disebabkan dengan direbus selama 15 menit,
maka logam Kadmium (Cd) yang terdapat dalam kerang darah akan lebih banyak
diikat oleh senyawa organik yang terdapat dalam jeruk nipis. Sehingga dapat
dilihat bahwa kerang darah yang direbus dalam larutan jeruk nipis selama 15
menit kadarnya lebih rendah dibandingkan dengan kerang darah yang direbus
dalam larutan jeruk nipis selama 1 menit.
Dengan demikian, salah satu cara yang dapat dilakukan oleh masyarakat
dengan cara di rebus dalam larutan jeruk nipis. Karena telah terbukti bahwa jeruk
nipis dapat menurunkan kadar logam kadmium (Cd) yang terdapat dalam kerang
darah.
Dalam merebus kerang darah perlu juga diperhatikan alat yang digunakan.
Karena jika alat yang digunakan untuk merebus terbuat dari bahan logam akan
menyebabkan kadar logam Kadmium (Cd) dalam kerang darah akan bertambah
bukan menurun. Alat yang digunakan untuk merebus kerang darah dalam
penelitian ini adalah yang terbuat dari bahan kaca (beaker glass). Karena
berdasarkan hasil orientasi dengan merebus kerang dengan alat yang terbuat dari
logam (seperti panci berbahan logam), menyebabkan kadar logam Kadmium (Cd)
pada kerang darah tersebut lebih besar daripada kadar tanpa perebusan. Hal ini
dapat dilihat pada tabel 5.
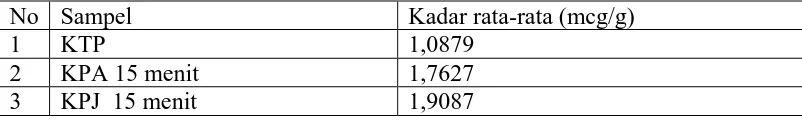
Tabel 5. Data kadar logam Kadmium (Cd) dengan perebusan menggunakan alat masak berbahan logam
No Sampel Kadar rata-rata (mcg/g)
1 KTP 1,0879
2 KPA 15 menit 1,7627
3 KPJ 15 menit 1,9087
Dari tabel 5 tersebut, dapat dilihat bahwa kadar logam Kadmium (Cd) pada
perebusan dalam larutan jeruk nipis lebih tinggi dibandingkan dengan perebusan
dalam akuades dan tanpa perebusan. Hal ini disebabkan karena alat masak yang
terbuat dari logam (panci, dsb) akan bereaksi kimia bila terkena asam cuka, asam
jawa, asam jeruk, dan sebagainya (Silargan, 2009) serta logam Kadmium (Cd)
dapat larut dan masuk kedalam makanan yang direbus menggunakan alat masak
berbahan logam (Sartono, 2001). Sehingga kadar logam Kadmium pada kerang
logam lebih tinggi daripada kerang dengan perebusan dalam akuades dan tanpa
perebusan.
4.2.3 Uji Perolehan Kembali (Recovery Test)
Hasil uji perolehan kembali logam Kadmium (Cd) dalam kerang darah
setelah penambahan larutan standar kadmium (Cd) dapat dilhat pada lampiran 8.
Contoh perhitungan persen uji perolehan kembali logam dalam sampel dapat
dilihat pada lampiran 9. Persen uji perolehan kembali (recovery test) Kadmium
(Cd) dalam kerang darah dapat dilihat pada tabel 6.
Tabel 6. Persen Uji Perolehan Kembali (recovery test) Logam Kadmium (Cd) Dalam Kerang Darah.
No Logam yang dianalisa Recovery rata-rata (%)
1 Cd 117, 11%
Berdasarkan tabel diatas, dapat dilihat bahwa rata-rata hasil uji perolehan
kembali untuk logam Kadmium (Cd) adalah 117,11%. Persen recovery tersebut
menunjukkan ketepatan kerja pada saat pemeriksaan kadar logam dalam sampel.
Menurut Miller (2005), suatu metode dikatakan teliti jika nilai recoverynya antara
80-120%.
4.2.4 Batas Deteksi dan Batas Kuantitasi
Dari hasil perhitungan diperoleh batas deteksi (LOD) untuk Kadmium (Cd)
adalah 0,0306 mcg/ml. Sedangkan batas kuantitasinya (LOQ) sebesar 0,1019
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan hasil penelitian diperoleh kadar logam Kadmium (Cd) dalam
kerang darah (Anadara granosa) tanpa perebusan sebesar 2,2432 0,0060 mcg/g.
Kadar logam Kadmium (Cd) setelah perebusan dalam akuades selama 1 menit
mengalami penurunan dari 2,2432 0,0060 mcg/g menjadi 2,0594 0,0449 mcg/g,
begitu juga dengan yang direbus selama 15 menit mengalami penurunan dari
2,2432 0,0060 mcg/g menjadi 1,4967 0,0083 mcg/g.
Kadar logam Kadmium (Cd) setelah perebusan dalam larutan jeruk nipis
selama 1 menit mengalami penurunan dari 2,2432 0,0060 mcg/g menjadi 0,9614
0,0143 mcg/g dan direbus selama 15 menit mengalami penurunan dari 2,2432
0,0060 mcg/g menjadi 0,6678 0,0011 mcg/g.
Adanya perbedaan waktu perebusan pada kerang darah memberikan
pengaruh yang berbeda terhadap penurunan kadar logam Kadmium (Cd). Setelah
perebusan dalam akuades selama 1 menit dan 15 menit terjadi penurunan
berturut-turut sebesar 8,83% dan 33,23%. Perebusan dalam larutan jeruk nipis selama 1
menit dan 15 menit terjadi penurunan berturut-turut sebesar 55,95% dan 69,97%.
5.2 Saran
Disarankan agar dilakukan penelitian lebih lanjut terhadap penurunan
kadar logam Kadmium (Cd) dengan variasi konsentrasi larutan jeruk nipis dan
Disarankan agar dilakukan penelitian terhadap penurunan kadar logam
Kadmium (Cd) dengan perebusan menggunakan asam-asam lain yang
DAFTAR PUSTAKA
Anderson, R. (1987). Food Analysis. Edisi kedua. New York:Avi Book. Hal.
613-615.
Anonima. (2005). Kerang dan Habitatnya. Tanggal akses 21 Mei 2010.
Anonimb. (2010). Metallothionein dan Detoksifikasi Logam.
Tanggal akses 01 Juni 2010.
Anonimc. (2010). Kerang Darah.
Tanggal akses 21 Juli 2010.
Anonimd. (2010). Asam Sitrat.
Tanggal akses 21 Juli 2010.
Badan Standarisasi Nasional. (2009). Batas Maksimum Cemaran Logam Berat Dalam Pangan. SNI 7387-2009. Hal. 4.
Bender, G.T. (1987). Principal of Chemical Instrumentation. Philadhelphia:W.B. Sounders Company. Page. 98.
Darmono. (2001). Lingkungan Hidup dan Pencemaran. Cetakan I. Jakarta: Universitas Indonesia. Hal. 47, 104-105, 137.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Departemen Kesehatan RI. Jakarta. Hal. 1126, 1213, 1135.
Djamali, A. (1998). Potensi dan Penyebaran sumber Daya Ikan Laut di Perairan Indonesia. Fakultas Perikanan IPB. Institut Pertanian Bogor. Hal. 158.
Fifield, F.W. (1983). Principles and Practice of Analytical Chemistry. Edisi Kedua. London:International Textbook Company Limited. Pages. 10, 277.
Fries, J,.and Getrost, H. (1997). Organic Reagents For Trace Analysis. E. Merck Darmstadt. Pages. 208-209.
Harmita. (2004). Petunjuk Pelaksanaan Validasi, Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. Vol. I. No.3. Hal. 119, 130, 131.
Haswell, S. J., (1991). Atomic Absorption Spectrometry Theory, Design and Application. New York:Elsevier. Page. 219.
Karlaganis, G. (2000). Citric Acid. Switzerland:SIDS Initial Assesment Report. Page. 5.
Miller. (2005). Method Validation in Pharmaceutical Analysis. Weinheim:Wiley-VCH. Page. 171.
Nurjanah, L. (2009). Pengaruh Perebusan Kerang Bulu (Anadara ferruginea) Terhadap Penurunan Kadar Logam Pb dan Cd Menggunakan Akuades dan Asam Gelugur Secara Spektrofotometer Serapan Atom. Skripsi Fakultas Farmasi. Universitas Sumatera Utara. Medan.
Nurjanah, dkk. (2005). Kandungan Mineral dan Proksimat Kerang Darah (Anadara granosa) yang Diambil Dari Kabupaten Boalemo, Gorontalo. Buletin teknologi Hasil Perikanan. Vol. VIII. No. 2. Hal. 21.
Palar. (2008). Pencemaran dan Toksikologi Logam Berat. Cetakan IV. Jakarta:Rineka Cipta. Hal. 23, 25, 53.
Purnomo, D. (2009). Logam Berat Sebagai Penyumbang Pencemaran Laut.
Tanggal akses 13 Mei 2010.
PT. (Persero) Pelabuhan Indonesia I. (2004). Pemantauan Lingkungan Pelabuhan Belawan. Laboratorium Lingkungan BAPEDALDA Propinsi Sumatera Utara. Medan. Hal. 4.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta:Pustaka Pelajar. Hal. 18, 31, 298, 305-311, 319-321.
Sartono, Drs. (2001). Racun dan Keracunan. Jakarta:Widya Medika. Hal. 81, 219.
Sarwono, B. (2001). Khasiat dan Manfaat Jeruk Nipis. Jakarta:Agromedia Pustaka. Hal. 4.
Silargan, S. (2009). Bahaya Di Balik Alat Masak.
Tanggal akses 21 Mei 2010.
Sudjana. (2001). Metode Statistika. Edisi Keenam. Bandung:Tarsito. Hal. 206.
Sudrajat. (2008). Budidaya 23 Komunitas Laut Yang Menguntungkan. Jakarta: Penebar Swadaya. Hal. 41.
Vogel, A.I. (1990). Kimia Analisis Kualitatif Anorganik. Penerjemah:Setiono, L., dkk. Edisi Kelima. Bagian I. Jakarta:PT Kalman Media Pustaka. Hal. 620
Wibisono. (2005). Metode Statistik. Cetakan I. Yogyakarta:Gadjah Mada University Press. Hal. 451-452.
Lampiran 1. Bagan Proses Destruksi Logam Kadmium (Cd)
Ditimbang 10 gram
Dimasukkan kedalam erlenmeyer Ditambahkan 5 ml H2SO4 (p) Ditambahkan 20 ml HNO3 (p) Didiamkan selama 24 jam
Didestruksi sampai larutan berwarna kuning jernih
Didinginkan
Dimasukkan kedalam labu ukur 100 ml
Ditepatkan dengan akuabides sampai garis tanda
Disaring dengan kertas saring whatman no.42 dengan membuang 10 ml larutan pertama hasil penyaringan
Diuji kualitatif
Diuji kuantitatif dengan Spektrofotometri Serapan Atom pada 228,8 nm
Sampel yang sudah halus
Sampel + H2SO4 (p) + HNO3 (p)
100 ml larutan sampel
Larutan sampel
Lampiran 2. Data Hasil Pengukuran Absorbansi Larutan Standar Kadmium (Cd)
No Konsentrasi (mcg/ml) Absorbansi (A)
1 0,000 0,0000
2 0,050 0,0097
3 0,100 0,0227
4 0,200 0,0540
5 0,400 0,1165
Lampiran 3. Contoh Perhitungan Persamaan Regresi Logam Kadmium (Cd)
No X Y XY X2 Y2
1 0,000 0,0000 0,000000 0,0000 0,00000000
2 0,050 0,0097 0,000485 0,0025 0,00009409
3 0,100 0,0227 0,002270 0,0100 0,00051529
4 0,200 0,0540 0,010800 0,0400 0,00291600
5 0,400 0,1165 0,046600 0,1600 0,01357225
6 0,600 0,1793 0,107580 0,3600 0,03214849
∑ 1,35 0,3822 0,1677 0,5725 0,04924612
Rata-rata 0,2250 0,0637 0,0279 0,0954 0,00820769
a
–
a
–
a
a
a = 0,3041
a + b
b = 0,0637 – (0,3041) ( 0,2250)
b = 0,0637 – 0,0684
b = 0,0047
Maka persamaan regresinya adalah : Y= 0,3041 X –
r
r
– –
r
r
r
Keterangan : KTP :Kerang darah tanpa perebusan
KPA :Kerang darah dengan Perebusan dalam Akuades selama 1 menit
KPA 15’ :Kerang darah dengan Perebusan dalam Akuades selama 15 menit
KPJ :Kerang darah dengan Perebusan dalam Larutan Jeruk Nipis selama 1 menit
KPJ 15’ :Kerang darah dengan Perebusan dalam Larutan Jeruk Nipis selama 15 menit
Lampiran 5. Contoh Perhitungan Kadar Logam Kadmium (Cd) dalam Kerang Darah (Anadara granosa)
Berat sampel yang ditimbang = 10,0085 gram
Absorbansi (Y) = 0,0602
Persamaan regresi : Y= 0,3041 X –
X =
X =
X = 0,2134
Konsentrasi logam Cd = 0,2134 mcg/ml
Kadar logam Cd dalam sampel :
=
=
= 2,1322 mcg/g
Selanjutnya dilakukan perhitungan kadar logam kadmium dengan cara
yang sama terhadap sampel KTP2, KTP3, KTP4, KTP5, KTP6, KPA1, KPA2,
KPA3, KPA4, KPA5, KPA6, KPA 15’ 1, KPA15’ 2, KPA15’ 3, KPA15’ 4,
KPA15’ 5, KPA15’ 6, KRJ1, KRJ2, KRJ3 ,KRJ4, KRJ5, KRJ6, KRJ15’ 1,
Lampiran 6. Perhitungan Statistik Kadar Logam Kadmium dalam Kerang Darah
1. Perhitungan statistik kadar logam kadmium (Cd) pada kerang darah tanpa
perebusan
No Sampel Xi
Kadar (mcg/g) (Xi– )
1 KTP 1 2,1322 -0,0838 0,00702244
2 KTP 2 2,1913 -0,0247 0,00061009
3 KTP 3 2,2385 0,0225 0,00050625
4 KTP 4 2,2426 0,0266 0,00070756
5 KTP 5 2,2438 0,0278 0,00077284
6 KTP 6 2,2477 0,0317 0,00100489
13,2961 0,01062407
Rata-rata 2,2160 0,00177068
SD
SD
SD = 0,0460
Pada interval kepercayaan 95% dengan nilai α = 0.05, dk = 5 diperoleh
nilai t tabel = 2,5706.
Data diterima jika t hitung < t tabel
t hitung data 1 = = 4,4574 (Data Ditolak)
t hitung data 2 = = 1,3138
t hitung data 3 = = 1,1968
t hitung data 4 = = 1,4149
t hitung data 5 = = 1,4787
t hitung data 6 = = 1,6862
Untuk itu perhitungan diulangi dengan cara yang sama tanpa
mengikutsertakan data ke-1.
No Sampel Xi
Kadar (mcg/g)
(Xi– )
1 KTP 2 2,1913 -0,0415 0,00172225
2 KTP 3 2,2385 0,0057 0,00003249
3 KTP 4 2,2426 0,0098 0,00009604
4 KTP 5 2,2438 0,0110 0,00012100
5 KTP 6 2,2477 0,0149 0,00022201
∑ 11,1639 0,00219379
Rata-rata 2,2328 0,00043876
SD =
SD = 0,0234
Pada interval kepercayaan 95% dengan nilai α = 0.05, dk = 4 diperoleh
nilai t tabel =2,7765.
Data diterima jika t hitung < t tabel
t hitung data 2 = = 3,9524 (Data Ditolak)
t hitung data 3 = = 0,5429
t hitung data 4 = = 0,9333
t hitung data 5 = = 1,0476
t hitung data 6 = = 1,4190
Untuk itu perhitungan diulangi dengan cara yang sama tanpa
mengikutsertakan data ke-2.
No Sampel Xi
Kadar (mcg/g)
(Xi–
1 KTP 3 2,2385 -0,0047 0,00002209
2 KTP 4 2,2426 -0,0006 0,00000036
3 KTP 5 2,2438 0,0006 0,00000036
4 KTP 6 2,2477 0,0045 0,00002025
∑ 8,9726 0,00004306
Rata-rata 2,2432 0,00001077