SKRIPSI
APLIKASI KOMBINASI BUBUK FULI PALA (Myristica fragrans Houtt) DAN NaCl SEBAGAI PENGAWET ALAMI PADA MI
BASAH MATANG
Oleh: ADI PUTRA
F24103097
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
SKRIPSI
APLIKASI KOMBINASI BUBUK FULI PALA (Myristica fragrans Houtt) DAN NaCl SEBAGAI PENGAWET ALAMI PADA MI
BASAH MATANG
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh: ADI PUTRA
F24103097
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Adi Putra. F24103097. Aplikasi Kombinasi Bubuk Fuli Pala (Myristica fragrans
Houtt) Dan NaCl Sebagai Pengawet Alami Pada Mi Basah Matang. Di bawah bimbingan Prof. Dr. Ir. Betty Sri Laksmi Jenie, MS.
RINGKASAN
Mi basah termasuk bahan pangan yang mudah rusak (High Perishable Food) karena kadar air yang cukup tinggi. Saat ini usaha yang dapat dilakukan oleh produsen untuk menghambat pertumbuhan mikroba dan memperpanjang umur simpan adalah dengan melakukan penambahan bahan pengawet. Akan tetapi seringkali bahan pengawet yang ditambahkan bukan pengawet makanan, seperti penyalahgunaan formalin yang cukup meresahkan masyarakat. Oleh karena itu perlu dilakukan usaha untuk mencari bahan-bahan alami yang aman sebagai pengawet. Fuli pala merupakan bahan alami yang dapat dijadikan alternatif sebagai pengawet alami.
Penelitian ini bertujuan untuk mengawetkan mi basah yang diproduksi dengan bahan pengawet alami yaitu bubuk fuli pala (Myristica fragrans Houtt) yang dikombinasikan dengan NaCl, sehingga lebih aman untuk dikonsumsi. Produk yang dihasilkan diharapkan selain memiliki umur simpan yang lebih panjang juga memiliki karakteristik sensori berupa tekstur, aroma, warna dan rasa yang masih dapat diterima oleh konsumen.
Penelitian ini dibagi dalam dua tahap. Pada penelitian tahap pertama dilakukan pengujian daya simpan mi basah matang, pembuatan bubuk fuli pala, penentuan konsentrasi bubuk fuli pala dan penentuan konsentrasi NaCl secara subyektif. Pada penelitian tahap kedua kombinasi konsentrasi bubuk fuli pala dan NaCl terbaik dianalisis lebih lanjut secara obyektif dan dibandingkan dengan mi basah matang kontrol tanpa penambahan bubuk fuli pala. Analisis yang dilakukan meliputi analisis TPC, total kapang, pH, aw, warna, tekstur, dan organoleptik.
Berdasarkan hasil pengamatan subyektif, diketahui bahwa kerusakan mi basah matang yang disimpan pada suhu ruang terjadi pada jam pengamatan ke-42 ditandai dengan munculnya bau asam sedangkan berdasarkan hasil pengamatan obyektif, secara mikrobiologi telah melewati batas SNI (106 cfu/g) pada jam pengamatan ke-24.
Mi kontrol memiliki nilai aw sebesar 0.97 sedangkan mi yang dibuat dengan penambahan bubuk fuli pala 1% + NaCl 4% memiliki nilai aw sebesar 0.92. Penambahan bubuk fuli pala 1% dan NaCl 4% mampu menurunkan nilai aw.
Mi yang dibuat dengan penambahan bubuk fuli pala 1% + NaCl 4% mempunyai nilai pH awal 9.04 dan pH akhir sebesar 6.97 sedangkan mi kontrol mempunyai nilai pH awal 9.25 dan pH akhir sebesar 5.93. Penambahan bubuk fuli pala 1% dan NaCl 4% mampu menghambat laju penurunan pH.
Perubahan warna pada mi basah matang tidak terlalu berpengaruh selama penyimpanan. Hal itu terlihat pada perubahan ketajaman warna (nilai L) dan golongan warna (ºHue) selama penyimpanan. Kerusakan mi baik secara subyektif maupun obyektif, kurang berpengaruh terhadap warna mi basah matang. Nilai L dan nilai ºHue relatif stabil selama penyimpanan.
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN
APLIKASI KOMBINASI BUBUK FULI PALA (Myristica fragrans Houtt) DAN NaCl SEBAGAI PENGAWET ALAMI PADA MI
BASAH MATANG
Oleh: ADI PUTRA
F24103097
Dilahirkan pada tanggal 13 Maret 1983
di Tangerang
Tanggal lulus : Agustus 2007
Menyetujui,
Bogor, Agustus2007
Prof. Dr. Ir. Betty Sri Laksmi Jenie, MS.
Dosen Pembimbing
Mengetahui,
Dr. Ir. Dahrul Syah, MSc.
RIWAYAT HIDUP
Penulis dilahirkan di Tangerang pada tanggal 13 Maret 1983.
Penulis adalah anak ke-3 dari pasangan Nursin dan Ani.
Penulis menyelesaikan pendidikan dasar pada tahun 1996 di
SDN Parigi 02 Pondok Aren kemudian melanjutkan
pendidikan menengah pertama di Mts. Al – Sa’adah Pondok
Aren Tangerang hingga tahun 1999. Penulis menamatkan
pendidikan menengah atas di SMA Dwiwarna Parung, Bogor pada tahun 2003.
Penulis pernah mengikuti program pertukaran pelajar AFS di Oita Uenogaoka
High School Jepang pada tahun 2001 – 2002. Penulis melanjutkan pendidikan
tinggi di Institut Pertanian Bogor Departemen Ilmu dan Teknologi Pangan,
Fakultas Teknologi Pertanian melalui Sistem Penerimaan Mahasiswa Baru
(SPMB) pada tahun 2003.
Selama menjalani studi di Institut Pertanian Bogor, penulis aktif di
berbagai kegiatan dan organisasi kemahasiswaan, diantaranya menjadi pengurus
Himitepa pada tahun 2005 dan berbagai kepanitiaan lainnya, seperti Kepanitiaan
Lepas Landas Sarjana tahun 2005 dan Lomba Cepat Tepat Ilmu Pangan 2005.
Penulis pernah menjadi Asisten Mata Kuliah Mikrobiologi Pangan dan sebagai
tugas akhir, penulis mengambil penelitian dengan judul Aplikasi Kombinasi
Bubuk Fuli Pala (Myristica fragrans Houtt) Dan NaCl Sebagai Pengawet Alami Pada Mi Basah Matang di bawah bimbingan Prof. Dr. Ir. Betty Sri Laksmi Jenie,
KATA PENGANTAR
Alhamdulillaahirobbil ’alamin, segala puji bagi Allah SWT yang telah
memberikan karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini
sebagai tugas akhir untuk mendapatkan gelar Sarjana Teknologi Pertanian pada
Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Insitut
Pertanian Bogor.
Selama melaksanakan penelitian dan terselesainya skripsi ini penulis telah
mendapatkan banyak bantuan dari berbagai pihak. Oleh karena itu penulis
mengucapkan terima kasih sebesar-besarnya kepada :
1. Prof. Dr. Ir. Betty Sri Laksmi Jenie, MS selaku dosen pembimbing yang
banyak memberikan arahan dan bimbingannya kepada penulis.
2. Dra. Suliantari, MS atas kesediaannya sebagai dosen penguji.
3. Ir. Elvira Syamsir, MSi atas kesediaannya sebagai dosen penguji.
4. Bapak dan ibuku yang tiada henti-hentinya memberikan doa, kasih sayang,
nasehat dan semangat.
5. Kakak-kakakku dan adikku terima kasih atas dukungannya selama ini.
6. Ibu Latifah, Ibu Endang, dan Ibu Nasti terimakasih atas motivasi dan bantuan
yang diberikan selama ini.
7. Pak Koko yang telah banyak membantu dan setia menemani siang dan malam
di laboratorium selama penelitian.
8. Bu Rubiyah, Teh Ida, Bu Antin, Mas Edi, dan Pak Mul terimakasih atas
kerjasamanya.
9. Teman-teman seperjuangan satu bimbingan (Agus, Arie, dan Lita) terimakasih
atas kebersamaan dan kerjasamanya selama ini.
10.Teman-teman penelitianku (Sarwo, Nooy, Hendy, Steph, Mitoel, Wayan,
Jeng-jeng, Rina, Denang, Oneth, Kaninta, Tathan, Martin, dll ) yang telah
banyak membantu selama penelitian.
11.Teman-teman yang pernah membantu menemani lembur di laboratorium (
Tilo, Mardiati, Ekus, Hanifah, Dhani, sinung, udjo ) Terimaksih atas
12.Sinung, Shindu, Gilang, Dito terimakasih atas kedekatan dan persahabatannya
selama ini.
13.Teman-teman ITP 40, 41, dan 42 yang tidak dapat disebutkan satu-persatu.
14.Tak terlupakan sahabat-sahabatku 2 no 8 kumi tokuni Tomomi, Tsubasa, Masami, Moe, Anai. Itsumo hagemashite kurete arigatou.
Penulis menyadari bahwa skripsi ini masih belum sempurna dan
mungkin terdapat kekurangan. Penulis berharap semoga skripsi ini dapat berguna
dan bermanfaat bagi semua pihak yang membutuhkannya.
Bogor, Agustus 2007
Penulis
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... iii
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... ix
I. PENDAHULUAN... 1
A. LATAR BELAKANG ... 1
B. TUJUAN ... 3
C. SASARAN ... 3
D. MANFAAT ... 3
II. TINJAUAN PUSTAKA ... 4
A. FULI PALA ... 4
1. Botani ... 4
2. Komposisi Fisik dan Kimia... 5
B. GARAM... 7
C. MI... 8
1. Jenis Mi ... 8
2. Proses Pembuatan Mi... 10
D. KERUSAKAN MI BASAH... 13
III. METODOLOGI PENELITIAN ... 15
A. BAHAN DAN ALAT ... 15
B. METODE PENELITIAN ... 15
1. Penentuan Konsentrasi Bubuk Fuli Pala dan NaCl... 15
a. Pengujian daya simpan mie basah matang... 15
b. Pembuatan Bubuk Fuli Pala... 16
c. Penentuan Konsentrasi Bubuk Fuli Pala... 17
d. Penentuan Konsentrasi NaCl... 18
3. Prosedur Analisis ... 20
a. Analisis Mikrobiologi ... 20
1). Analisis Total Mikrobiologi ... 20
2). Analisis Total Kapang ... 21
b. Analsisi Fisik... 21
1). Warna... 21
2). Tekstur ... 22
c. Analisis Kimia... 22
1). Nilai pH... 22
2). Nilai aw... 23
d. Uji Organoleptik... 23
IV. HASIL DAN PEMBAHASAN ... 24
A. PENENTUAN KONSENTRASI BUBUK FULI PALA DAN NaCl ... 24
1. Pengujian daya simpan mie basah matang... 24
2. Pembuatan Bubuk Fuli Pala ... 25
3. Penentuan Konsentrasi Bubuk Fuli Pala ... 25
4. Penentuan Konsentrasi NaCl ... 28
B. PENGARUH KOMBINASI BUBUK FULI PALA DAN NaCl PADA MUTU MI BASAH ... 30
1. Total Mikroba Mi Basah Matang Selama Penyimpanan .. 30
2. Total Kapang Mi Basah Matang Selama Penyimpanan.... 36
3. Nilai aw... 37
4. Nilai pH... 39
5. Warna ... 40
a. Nilai L (ketajaman warna)... 40
b. Derajat Hue ... 42
6. Tekstur ... 44
7. Uji Organoleptik... 46
a. Warna ... 46
b. Aroma... 47
SKRIPSI
APLIKASI KOMBINASI BUBUK FULI PALA (Myristica fragrans Houtt) DAN NaCl SEBAGAI PENGAWET ALAMI PADA MI
BASAH MATANG
Oleh: ADI PUTRA
F24103097
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
SKRIPSI
APLIKASI KOMBINASI BUBUK FULI PALA (Myristica fragrans Houtt) DAN NaCl SEBAGAI PENGAWET ALAMI PADA MI
BASAH MATANG
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh: ADI PUTRA
F24103097
2007
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Adi Putra. F24103097. Aplikasi Kombinasi Bubuk Fuli Pala (Myristica fragrans
Houtt) Dan NaCl Sebagai Pengawet Alami Pada Mi Basah Matang. Di bawah bimbingan Prof. Dr. Ir. Betty Sri Laksmi Jenie, MS.
RINGKASAN
Mi basah termasuk bahan pangan yang mudah rusak (High Perishable Food) karena kadar air yang cukup tinggi. Saat ini usaha yang dapat dilakukan oleh produsen untuk menghambat pertumbuhan mikroba dan memperpanjang umur simpan adalah dengan melakukan penambahan bahan pengawet. Akan tetapi seringkali bahan pengawet yang ditambahkan bukan pengawet makanan, seperti penyalahgunaan formalin yang cukup meresahkan masyarakat. Oleh karena itu perlu dilakukan usaha untuk mencari bahan-bahan alami yang aman sebagai pengawet. Fuli pala merupakan bahan alami yang dapat dijadikan alternatif sebagai pengawet alami.
Penelitian ini bertujuan untuk mengawetkan mi basah yang diproduksi dengan bahan pengawet alami yaitu bubuk fuli pala (Myristica fragrans Houtt) yang dikombinasikan dengan NaCl, sehingga lebih aman untuk dikonsumsi. Produk yang dihasilkan diharapkan selain memiliki umur simpan yang lebih panjang juga memiliki karakteristik sensori berupa tekstur, aroma, warna dan rasa yang masih dapat diterima oleh konsumen.
Penelitian ini dibagi dalam dua tahap. Pada penelitian tahap pertama dilakukan pengujian daya simpan mi basah matang, pembuatan bubuk fuli pala, penentuan konsentrasi bubuk fuli pala dan penentuan konsentrasi NaCl secara subyektif. Pada penelitian tahap kedua kombinasi konsentrasi bubuk fuli pala dan NaCl terbaik dianalisis lebih lanjut secara obyektif dan dibandingkan dengan mi basah matang kontrol tanpa penambahan bubuk fuli pala. Analisis yang dilakukan meliputi analisis TPC, total kapang, pH, aw, warna, tekstur, dan organoleptik.
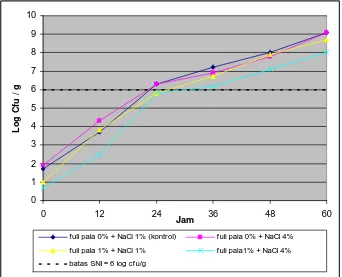
Berdasarkan hasil pengamatan subyektif, diketahui bahwa kerusakan mi basah matang yang disimpan pada suhu ruang terjadi pada jam pengamatan ke-42 ditandai dengan munculnya bau asam sedangkan berdasarkan hasil pengamatan obyektif, secara mikrobiologi telah melewati batas SNI (106 cfu/g) pada jam pengamatan ke-24.
Mi kontrol memiliki nilai aw sebesar 0.97 sedangkan mi yang dibuat dengan penambahan bubuk fuli pala 1% + NaCl 4% memiliki nilai aw sebesar 0.92. Penambahan bubuk fuli pala 1% dan NaCl 4% mampu menurunkan nilai aw.
Mi yang dibuat dengan penambahan bubuk fuli pala 1% + NaCl 4% mempunyai nilai pH awal 9.04 dan pH akhir sebesar 6.97 sedangkan mi kontrol mempunyai nilai pH awal 9.25 dan pH akhir sebesar 5.93. Penambahan bubuk fuli pala 1% dan NaCl 4% mampu menghambat laju penurunan pH.
Perubahan warna pada mi basah matang tidak terlalu berpengaruh selama penyimpanan. Hal itu terlihat pada perubahan ketajaman warna (nilai L) dan golongan warna (ºHue) selama penyimpanan. Kerusakan mi baik secara subyektif maupun obyektif, kurang berpengaruh terhadap warna mi basah matang. Nilai L dan nilai ºHue relatif stabil selama penyimpanan.
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN
APLIKASI KOMBINASI BUBUK FULI PALA (Myristica fragrans Houtt) DAN NaCl SEBAGAI PENGAWET ALAMI PADA MI
BASAH MATANG
Oleh: ADI PUTRA
F24103097
Dilahirkan pada tanggal 13 Maret 1983
di Tangerang
Tanggal lulus : Agustus 2007
Menyetujui,
Bogor, Agustus2007
Prof. Dr. Ir. Betty Sri Laksmi Jenie, MS.
Dosen Pembimbing
Mengetahui,
Dr. Ir. Dahrul Syah, MSc.
RIWAYAT HIDUP
Penulis dilahirkan di Tangerang pada tanggal 13 Maret 1983.
Penulis adalah anak ke-3 dari pasangan Nursin dan Ani.
Penulis menyelesaikan pendidikan dasar pada tahun 1996 di
SDN Parigi 02 Pondok Aren kemudian melanjutkan
pendidikan menengah pertama di Mts. Al – Sa’adah Pondok
Aren Tangerang hingga tahun 1999. Penulis menamatkan
pendidikan menengah atas di SMA Dwiwarna Parung, Bogor pada tahun 2003.
Penulis pernah mengikuti program pertukaran pelajar AFS di Oita Uenogaoka
High School Jepang pada tahun 2001 – 2002. Penulis melanjutkan pendidikan
tinggi di Institut Pertanian Bogor Departemen Ilmu dan Teknologi Pangan,
Fakultas Teknologi Pertanian melalui Sistem Penerimaan Mahasiswa Baru
(SPMB) pada tahun 2003.
Selama menjalani studi di Institut Pertanian Bogor, penulis aktif di
berbagai kegiatan dan organisasi kemahasiswaan, diantaranya menjadi pengurus
Himitepa pada tahun 2005 dan berbagai kepanitiaan lainnya, seperti Kepanitiaan
Lepas Landas Sarjana tahun 2005 dan Lomba Cepat Tepat Ilmu Pangan 2005.
Penulis pernah menjadi Asisten Mata Kuliah Mikrobiologi Pangan dan sebagai
tugas akhir, penulis mengambil penelitian dengan judul Aplikasi Kombinasi
Bubuk Fuli Pala (Myristica fragrans Houtt) Dan NaCl Sebagai Pengawet Alami Pada Mi Basah Matang di bawah bimbingan Prof. Dr. Ir. Betty Sri Laksmi Jenie,
KATA PENGANTAR
Alhamdulillaahirobbil ’alamin, segala puji bagi Allah SWT yang telah
memberikan karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini
sebagai tugas akhir untuk mendapatkan gelar Sarjana Teknologi Pertanian pada
Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Insitut
Pertanian Bogor.
Selama melaksanakan penelitian dan terselesainya skripsi ini penulis telah
mendapatkan banyak bantuan dari berbagai pihak. Oleh karena itu penulis
mengucapkan terima kasih sebesar-besarnya kepada :
1. Prof. Dr. Ir. Betty Sri Laksmi Jenie, MS selaku dosen pembimbing yang
banyak memberikan arahan dan bimbingannya kepada penulis.
2. Dra. Suliantari, MS atas kesediaannya sebagai dosen penguji.
3. Ir. Elvira Syamsir, MSi atas kesediaannya sebagai dosen penguji.
4. Bapak dan ibuku yang tiada henti-hentinya memberikan doa, kasih sayang,
nasehat dan semangat.
5. Kakak-kakakku dan adikku terima kasih atas dukungannya selama ini.
6. Ibu Latifah, Ibu Endang, dan Ibu Nasti terimakasih atas motivasi dan bantuan
yang diberikan selama ini.
7. Pak Koko yang telah banyak membantu dan setia menemani siang dan malam
di laboratorium selama penelitian.
8. Bu Rubiyah, Teh Ida, Bu Antin, Mas Edi, dan Pak Mul terimakasih atas
kerjasamanya.
9. Teman-teman seperjuangan satu bimbingan (Agus, Arie, dan Lita) terimakasih
atas kebersamaan dan kerjasamanya selama ini.
10.Teman-teman penelitianku (Sarwo, Nooy, Hendy, Steph, Mitoel, Wayan,
Jeng-jeng, Rina, Denang, Oneth, Kaninta, Tathan, Martin, dll ) yang telah
banyak membantu selama penelitian.
11.Teman-teman yang pernah membantu menemani lembur di laboratorium (
Tilo, Mardiati, Ekus, Hanifah, Dhani, sinung, udjo ) Terimaksih atas
12.Sinung, Shindu, Gilang, Dito terimakasih atas kedekatan dan persahabatannya
selama ini.
13.Teman-teman ITP 40, 41, dan 42 yang tidak dapat disebutkan satu-persatu.
14.Tak terlupakan sahabat-sahabatku 2 no 8 kumi tokuni Tomomi, Tsubasa, Masami, Moe, Anai. Itsumo hagemashite kurete arigatou.
Penulis menyadari bahwa skripsi ini masih belum sempurna dan
mungkin terdapat kekurangan. Penulis berharap semoga skripsi ini dapat berguna
dan bermanfaat bagi semua pihak yang membutuhkannya.
Bogor, Agustus 2007
Penulis
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
DAFTAR ISI ... iii
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... ix
I. PENDAHULUAN... 1
A. LATAR BELAKANG ... 1
B. TUJUAN ... 3
C. SASARAN ... 3
D. MANFAAT ... 3
II. TINJAUAN PUSTAKA ... 4
A. FULI PALA ... 4
1. Botani ... 4
2. Komposisi Fisik dan Kimia... 5
B. GARAM... 7
C. MI... 8
1. Jenis Mi ... 8
2. Proses Pembuatan Mi... 10
D. KERUSAKAN MI BASAH... 13
III. METODOLOGI PENELITIAN ... 15
A. BAHAN DAN ALAT ... 15
B. METODE PENELITIAN ... 15
1. Penentuan Konsentrasi Bubuk Fuli Pala dan NaCl... 15
a. Pengujian daya simpan mie basah matang... 15
b. Pembuatan Bubuk Fuli Pala... 16
c. Penentuan Konsentrasi Bubuk Fuli Pala... 17
d. Penentuan Konsentrasi NaCl... 18
3. Prosedur Analisis ... 20
a. Analisis Mikrobiologi ... 20
1). Analisis Total Mikrobiologi ... 20
2). Analisis Total Kapang ... 21
b. Analsisi Fisik... 21
1). Warna... 21
2). Tekstur ... 22
c. Analisis Kimia... 22
1). Nilai pH... 22
2). Nilai aw... 23
d. Uji Organoleptik... 23
IV. HASIL DAN PEMBAHASAN ... 24
A. PENENTUAN KONSENTRASI BUBUK FULI PALA DAN NaCl ... 24
1. Pengujian daya simpan mie basah matang... 24
2. Pembuatan Bubuk Fuli Pala ... 25
3. Penentuan Konsentrasi Bubuk Fuli Pala ... 25
4. Penentuan Konsentrasi NaCl ... 28
B. PENGARUH KOMBINASI BUBUK FULI PALA DAN NaCl PADA MUTU MI BASAH ... 30
1. Total Mikroba Mi Basah Matang Selama Penyimpanan .. 30
2. Total Kapang Mi Basah Matang Selama Penyimpanan.... 36
3. Nilai aw... 37
4. Nilai pH... 39
5. Warna ... 40
a. Nilai L (ketajaman warna)... 40
b. Derajat Hue ... 42
6. Tekstur ... 44
7. Uji Organoleptik... 46
a. Warna ... 46
b. Aroma... 47
d. Rasa ... 49
e. Keseluruhan (overall)... 50
V. KESIMPULAN DAN SARAN ... 52
A. KESIMPULAN ... 52
B. SARAN ... 52
DAFTAR PUSTAKA ... 53
DAFTAR TABEL
Halaman
Tabel 1. Persentase berat bagian-bagian buah
pala...
Tabel 2. Komposisi kimia fuli pala berdasarkan analisis proksimat
dalam 100 g edible portion.... Tabel 3. Syarat mutu mi basah (SNI 01-2987-1992)...
Tabel 4. Penggunaan Bubuk Fuli Pala dalam Mie Basah...
Tabel 5. Formulasi Penggunaan NaCl dalam Mi Basah...
Tabel 6. Pengaruh lama penyimpanan terhadap mutu sensori mi basah
matang...
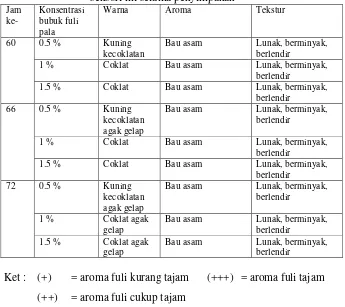
Tabel 7. Pengaruh konsentrasi bubuk fuli pala terhadap mutu sensori
mi selama penyimpanan...
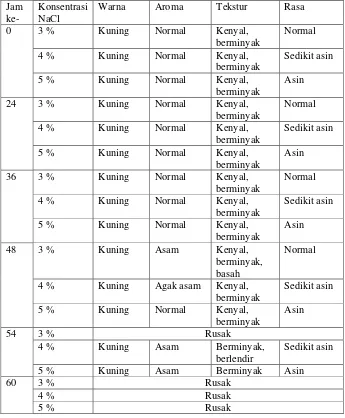
Tabel 8. Pengaruh konsentrasi NaCl terhadap mutu sensori mi
selama penyimpanan...
Tabel 9. Formulasi mi kombinasi bubuk fuli pala dan NaCl...
Tabel 10.Perbandingan umur simpan mi basah matang berdasarkan
pengamatan subyektif dan mikrobiologi...
Tabel 11.Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap nilai
aw mi...
6
6
9
17
18
24
26
29
30
35
DAFTAR GAMBAR
Halaman
Gambar 1. Diagram alir pembuatan mi basah secara umum... 11
Gambar 2. Diagram alir pembuatan mie basah secara umum... 16
Gambar 3. Diagram alir pembuatan bubuk fuli pala... 17
Gambar 4. Diagram alir konsep penelitian... 19
Gambar 5. Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
total mikroba mi selama penyimpanan ... 31
Gambar 6. Grafik persamaan garis lurus nilai total mikroba mi + fuli
Pala 0% dan NaCl 1% (kontrol)... 32
Gambar 7. Grafik persamaan garis lurus nilai total mikroba mi + fuli
Pala 0% dan NaCl 4% ... 33
Gambar 8. Grafik persamaan garis lurus nilai total mikroba mi + fuli
Pala 1% dan NaCl 1% ... 33
Gambar 9. Grafik persamaan garis lurus nilai total mikroba mi + fuli
Pala 1% dan NaCl 4% ... 34
Gambar 10. Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
total kapang mi selama penyimpanan... 36
Gambar 11. Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
nilai pH mi selama penyimpanan... 40
Gambar 12 Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
nilai L mi selama penyimpanan ... 41
Gambar 13 Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
nilai ºHue mi selama penyimpanan... 43
Gambar 14. Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
kekerasan mi selama penyimpanan... 45
Gambar 15. Pengaruh kombinasi bubuk fuli pala dan NaCl terhadap
kelengketan mi selama penyimpanan... 45
Gambar 16. Hasil uji hedonik terhadap warna mi basah matang... 47
Gambar 17. Hasil uji hedonik terhadap aroma mi basah matang... 48
Gambar 19. Hasil uji hedonik terhadap rasa mi basah matang ... 50
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Jumlah total mikroba mi basah matang dengan penambahan
bubuk fuli pala 0 % dan NaCl 1% (kontrol) ... 56
Lampiran 2. Jumlah total mikroba mi basah matang dengan penambahan
bubuk fuli pala 0 % dan NaCl 4 %... 57
Lampiran 3. Jumlah total mikroba mi basah matang dengan penambahan
bubuk fuli pala 1 % dan NaCl 1%... 58
Lampiran 4. Jumlah total mikroba mi basah matang dengan penambahan
bubuk fuli pala 1 % dan NaCl 4 %... 59
Lampiran 5. Jumlah total kapang mi basah matang dengan penambahan
bubuk fuli pala 0 % dan NaCl 1% (kontrol) ... 60
Lampiran 6. Jumlah total kapang mi basah matang dengan penambahan
bubuk fuli pala 0 % dan NaCl 4 %... 61
Lampiran 7. Jumlah total kapang mi basah matang dengan penambahan
bubuk fuli pala 1 % dan NaCl 1%... 62
Lampiran 8. Jumlah total kapang mi basah matang dengan penambahan
bubuk fuli pala 1 % dan NaCl 4 %... 63
Lampiran 9a.Perubahan pH mi basah matang dengan penambahan bubuk
fuli pala 0 % dan NaCl 1 % (kontrol) ... 64
Lampiran 9b.Perubahan pH mi basah matang dengan penambahan bubuk
fuli pala 0 % dan NaCl 4 %... 64
Lampiran 10a.Perubahan pH mi basah matang dengan penambahan bubuk
fuli pala 1 % dan NaCl 1 %... 65
Lampiran 10b. Perubahan pH mi basah matang dengan penambahan bubuk
fuli pala 1 % dan NaCl 4 %... 65
Lampiran 11. Pengamatan analisis warna mi basah matang dengan bubuk
fuli pala 0 % + NaCl 1 % (kontrol) ... 66
Lampiran 12. Pengamatan analisis warna mi basah matang dengan bubuk
fuli pala 0 % + NaCl 4 % ... 68
Lampiran 13. Pengamatan analisis warna mi basah matang dengan bubuk
Lampiran 14. Pengamatan analisis warna mi basah matang dengan bubuk
fuli pala 1 % + NaCl 4 % ... 72
Lampiran 15. Hasil analisis sidik ragam nilai L (Ketajaman warna) .... 74
Lampiran 16. Perubahan tekstur mi basah matang dengan bubuk fuli
pala 0% + NaCl 1% (kontrol)... 75
Lampiran 17. Perubahan tekstur mi basah matang dengan bubuk fuli
pala 0% + NaCl 4%... 76
Lampiran 18. Perubahan tekstur mi basah matang dengan bubuk fuli
pala 1% + NaCl 1%... 77
Lampiran 19. Perubahan tekstur mi basah matang dengan bubuk fuli
pala 1% + NaCl 4%... 78
Lampiran 20. Hasil analisis sidik ragam uji hedonik warna mi basah
matang... 79
Lampiran 21. Hasil analisis sidik ragam uji hedonik aroma mi basah
matang... 80
Lampiran 22. Hasil analisis sidik ragam uji hedonik tekstur mi basah
matang... 81
Lampiran 23. Hasil analisis sidik ragam uji hedonik rasa mi basah
matang... 82
Lampiran 24. Hasil analisis sidik ragam uji hedonik keseluruhan
I. PENDAHULUAN
A. LATAR BELAKANG
Mi merupakan salah satu jenis makanan yang populer di Asia
khususnya di Asia Timur dan Asia Tenggara. Di Indonesia, banyak orang
mengkonsumsi mi karena rasanya yang disukai dan praktis dalam
penyajiannya. Mi sering dijadikan pangan alternatif pengganti nasi sebagai
penghasil energi karena kandungan karbohidratnya yang tinggi.
Produksi mi basah di Indonesia cukup besar. Menurut Badan Pusat
Statistik, data produksi mi basah di Indonesia pada tahun 2002 sebesar
92.492.696 kg, sedangkan data konsumsi mi basah penduduk Indonesia pada
tahun 2004 untuk pengeluaran rata-rata perkapita dalam seminggu adalah
0.003 kg. Artinya konsumsi mi basah setiap penduduk Indonesia dalam
seminggu adalah 3 gram mi basah.
Mi basah yang dikonsumsi umumnya berupa produk olahan dari mi
basah seperti mi ayam yang menggunakan mi basah mentah, soto mi, bakso,
dan taoge goreng yang menggunakan mi basah matang. Produk olahan ini
umumnya dikonsumsi sebagai makanan jajanan, sarapan dan makan siang.
Mi basah mentah biasanya dijual tanpa proses pemasakan terlebih dahulu
dengan kadar air sekitar 35%, sedangkan mi basah matang telah mengalami
proses pemasakan sehingga kadar airnya mencapai 52% (Astawan, 1999).
Kadar air mi basah yang cukup tinggi serta kondisi sanitasi proses
produksi, peralatan dan perilaku pekerja yang kurang terjamin kebersihannya
menyebabkan mi basah cepat mengalami kerusakan akibat pertumbuhan
mikroba seperti kapang, khamir dan bakteri yang cukup tinggi. Pada mi basah
matang kerusakan terjadi setelah 40 jam pada suhu kamar berupa tumbuhnya
kapang (Hoseney, 1998). Saat ini usaha yang dapat dilakukan oleh produsen
untuk menghambat pertumbuhan mikroba dan memperpanjang umur simpan
mi basah adalah dengan melakukan penambahan bahan pengawet. Akan
tetapi seringkali bahan pengawet yang ditambahkan bukanlah pengawet
Produsen mi sering menggunakan bahan yang dilarang seperti
formalin dan boraks sebagai pengawet pada mi basah. Hasil pengujian Badan
POM dari sampling dan pengujian laboratorium secara serentak di Bandar
Lampung, Jakarta, Bandung, Semarang, Yogyakarta, Surabaya, Mataram,
dan Makasar pada Desember 2005 menunjukkan bahwa 64,32% mi basah
tidak memenuhi syarat kesehatan karena mengandung formalin. Selain itu,
Badan POM juga melaporkan, dari 24 sampel yang diuji, lebih dari 80% mi
basah yang dijual di Pasar Bandung mengandung boraks dan formalin
(Anonim, 2005). Alasan produsen menggunakan formalin dan boraks sebagai
bahan pengawet adalah karena harga yang murah, lebih awet, dan mutu mi
basah yang dihasilkan lebih bagus (Astawan, 2006).
Maraknya kasus penggunaan formalin pada mi basah membuat
masyarakat menjadi resah dan lebih selektif dalam memilih bahan pangan.
Hal tersebut mendorong dilakukannya usaha untuk mencari bahan-bahan
alami sebagai pengawet. Fuli pala merupakan bahan alami yang dapat
dijadikan alternaif sebagai pengawet alami.
Fuli pala dihasilkan dari tanaman pala yang merupakan rempah
indigenes Indonesia. Potensi antimikroba fuli pala telah diteliti dengan
mengeskstrak fuli pala dengan etanol. Hasil pengujian menunjukkan bahwa
ekstrak etanol fuli pala memiliki aktivitas antimikroba terhadap Bacillus megaterium, Acinetobacter sp., dan Pseudomonas sp. Ekstrak fuli pala juga
mempunyai sifat antimikroba terhadap Enterobacter aerogenes,
Brevibacterium dan Achromobacter sp., Micrococcus flavus, Bacillus subtilis, Leuconostoc mesenteroides, dan Lactobacillus plantarum (Hirasa dan Takemasa, 1998).
Mengingat proses ekstraksi etanol pada fuli pala membutuhkan waktu
yang cukup lama, biaya yang mahal dan keterampilan khusus, maka perlu
diupayakan cara lain untuk memanfaatkan antimikroba yang terdapat pada
fuli pala. Salah satu caranya yaitu dengan cara membuat bubuk fuli pala.
Bentuk bubuk lebih mudah dibuat dan lebih mudah diaplikasikan ke dalam
sistem pangan karena umumnya rempah-rempah ditambahkan ke dalam
Garam adalah seasoning dan pengawet yang komposisi kimianya adalah natrium klorida, sekitar 40 % natrium dan 60 % klorida (Igoe dan Hui,
1996). Secara umum kristal NaCl tidak berwarna dan berbentuk kubus.
Konsentrasi garam 1-2 % dapat menghambat pertumbuhan beberapa jenis
bakteri. Beberapa mikroba proteolitik dan penyebab kebusukan tidak toleran
pada konsentrasi garam kira-kira 2.5 % (Winarno etal., 1982).
Kombinasi aktivitas antimikroba dari bubuk fuli pala dan garam
diharapkan cukup efektif bila diaplikasikan pada sistem pangan, sehingga
mampu memperpanjang umur simpan mi basah. Bubuk fuli pala diharapkan
dapat digunakan sebagai alternatif pengawet alami oleh produsen mi basah
sehingga menghasilkan produk yang tidak hanya awet tetapi juga aman untuk
dikonsumsi.
B. TUJUAN, SASARAN DAN MANFAAT
1. TUJUAN
Penelitian ini bertujuan untuk mengawetkan mi basah
menggunakan bahan pengawet alami yaitu bubuk fuli pala (Myristica fragrans Houtt) yang dikombinasikan dengan garam, sehingga lebih aman karena tidak mengandung bahan pengawet sintetik.
2. SASARAN
Sasaran dari penelitian ini adalah menghasilkan mi dengan umur
simpan yang lebih panjang dan memiliki karakteristik sensori berupa
tekstur, aroma, warna dan rasa yang masih dapat diterima oleh konsumen.
3. MANFAAT
Penelitian ini diharapkan dapat memberikan manfaat bagi produsen
sehingga dapat memproduksi mi basah dengan umur simpan yang lebih
panjang sekaligus memberikan solusi terhadap masalah penyalahgunaan
formalin sebagai pengawet sehingga memberikan jaminan keamanan bagi
II. TINJAUAN PUSTAKA
A. FULI PALA
1. Botani
Pala (Myristica fragrans Houtt) merupakan salah satu komoditi pertanian yang memiliki nilai ekonomis tinggi. Menurut pendapat para
ahli, pala adalah tanaman asli Indonesia yang berasal dari Malaise
Archipel yaitu gugusan kepulauan Banda dan Maluku. Kemudian
menyebar dan berkembang ke pulau-pulau lain yang berada di
sekitarnya, bahkan sekarang telah mencapai Aceh, Sulawesi Utara dan
Irian Jaya.
Pala termasuk ke dalam famili Myristicaceae yang merupakan tanaman tropis berumah dua dan terdiri dari 18 genera dan 300 spesies.
Genus terbesar adalah Myristica yang terdiri dari 72 spesies. Tinggi tanaman pala antara 4 – 10 meter. Semua bagian tanaman pala bersifat
aromatik (Purseglove et al., 1981).
Tanaman pala memiliki buah berbentuk bulat, berwarna hijau
kekuning-kuningan, buah ini apabila masak terbelah dua. Garis tengah
buah berkisar antara 3 -9 cm, daging buahnya tebal dan asam rasanya.
Biji berbentuk lonjong sampai bulat, panjangnya berkisar antara 1,5 -
4,5 cm dengan lebar 1- 2,5 cm. Kulit biji berwarna coklat dan mengkilat
pada bagian luarnya. Kernel biji berwarna keputih-putihan sedangkan
fulinya berwarna merah gelap dan kadang-kadang putih
kekuning-kuningan dan membungkus biji menyerupai jala.
Menurut Farrell (1985) buah pala terdiri dari tiga bagian utama,
yaitu :
1) Bagian terluar yang disebut daging buah
2) Serabut berwarna merah – oranye yang disebut arillus. Jika arillus
dikeringkan dengan sinar matahari selama 6 – 8 minggu, maka
warnanya berubah menjadi oranye pucat yang disebut fuli (mace).
Bentuk fuli inilah yang diperdagangkan secara komersial sebagai
3) Bagian terdalam dari buah pala yang disebut bjij pala.
Fuli dari buah pala yang belum cukup masak berwarna kuning
pucat. Bila dikeringkan, akan mengalami perubahan warna menjadi
coklat muda. Fuli yang sudah tua berwarna merah api, apabila
dikeringkan akan berwarna merah coklat dan bila disimpan dalam waktu
yang lama akan berubah menjadi kuning tua hingga kuning oranye
seperti warna jerami (Rismunandar, 1988).
Fuli yang berasal dari Indonesia (East India) mempunyai aroma
yang lebih kuat dan warna yang lebih terang dibanding fuli yang berasal
dari Grenada (West India). Hal ini disebabkan karena minyak fuli East India mempunyai kandungan safrole dan myristicin yang lebih tinggi dibandingkan minyak pala West India, disamping itu juga terdapat
perbedaan komponen penyusun monoterpen. Safrole dan myristicin
merupakan senyawa eter aromatis yang menimbulkan flavor yang kuat
pada fuli (Purseglove, 1981).
Dalam bidang makanan, fuli pala sangat baik digunakan sebagai
flavor untuk produk bakery seperti pound cake, doughnuts, fruit cake,
fruit pies, cookies, dan whipped cream toppings. Fuli pala memiliki karakter yang lebih baik dibandingkan biji pala bila digunkan dalam
resep masakan, penggunaanya juga 20 % lebih sedikit. Terkadang fuli
pala juga digunakan sebagai seafood chowders, fish sauces, soups,
chicken casseroles, creamed vegetables, pickles,dan sebagai pengawet (Farrell, 1990).
2. Komposisi Fisik dan Kimia
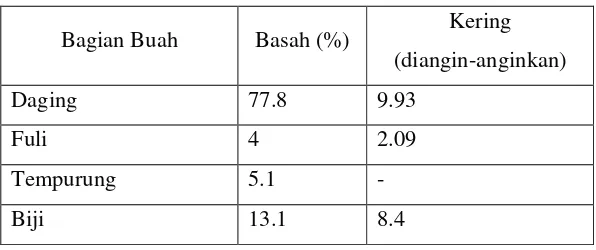
Buah pala terdiri dari 4 bagian yaitu daging, fuli, tempurung
(cangkang) dan biji (Rismunandar, 1988). Perbandingan berat pala
Banda (Myristica fragrans Houtt) dari keempat bagian buah pala dapat dilihat pada Tabel 1.
Purseglove et al. (1981) mengemukakan perbandingan biji pala kering terhadap fuli kering adalah 20 : 3. Pada kenyataannya
pulau lain dari gugusan kepulauan Maluku, berat fulinya agak rendah
(Rismunandar, 1988).
Tabel 1. Persentase berat bagian-bagian buah pala
Bagian Buah Basah (%) Kering
(diangin-anginkan)
Daging 77.8 9.93
Fuli 4 2.09
Tempurung 5.1 -
Biji 13.1 8.4
Rismunandar (1988)
Buah pala segar dapat menghasilkan daging buah sebanyak 83.3
%, fuli 3.22%, tempurung biji 3.94% dan daging biji sebanyak 9.54 %
(Somaatmadja, 1984). Berdasarkan analisis proksimat komposisi kimia
fuli dapat dilihat pada Tabel 2.
Tabel 2. Komposisi kimia fuli pala berdasarkan analisis proksimat dalam 100 g edible portion
Air 8.2 g Magnesium 163 mg
Energi 475 kcal Fosfor 110 mg
Protein 6.7 g Kalium 463 mg
Lemak 32.4 g Natrium 80 mg
Karbohidrat 50.5 g Seng 2 mg
Serat 4.8 g Niasin 1 mg
Abu 2.2 g Vitamin A 800 IU
Kalsium 252 mg Vitamin lainnya insignificant
Zat besi 14 mg
Farrell (1990)
Potensi ekstrak fuli pala sebagai antimikroba telah diketahui
adalah konsentrasi terendah yang dapat menghambat pertumbuhan
mikroba sebanyak 90% dari inokulum asal selama inkubasi 24 jam
(Consentino et al., 1999). Penentuan MIC ekstrak fuli pala dilakukan
pada tujuh jenis mikroba (B. subtilis, S. aureus, E. coli, S. Typhimurium, S. marcescens, P. aeruginosa, P. vulgaris, P. morganii).
Hasil penelitian menunjukkan bahwa ekstrak fuli pala dengan
menggunakan etanol yang ditambahkan pada sosis dapat menghambat
pertumbuhan Bacillus megaterium, Acinetobacter sp., dan
Pseudomonas sp. Ekstrak fuli pala juga mempunyai sifat antimikroba terhadap Enterobacter aerogenes, Brevibacterium dan Achromobacter
sp., Micrococcus flavus, B. subtilis, Leuconostoc mesenteroides, dan
Lactobacillus plantarum (Hirasa dan Takemasa, 1998).
B. GARAM
Bahan pengawet biasanya ditambahkan ke dalam bahan pangan
untuk mencegah pertumbuhan mikroba (antimikroba). Beberapa aditif
makanan yang sering digunakan sebagai senyawa antimikroba adalah
asam-asam organik dan garam-garamnya seperti propionat, benzoat,
sorbat, dan asetat, senyawa nitrit dan nitrat, dan sulfur dioksida dan sulfit,
etilen dan propilen oksida, garam, gula, alkohol, formaldehida,
rempah-rempah dan senyawa lainnya (Frazier dan Westhoff, 1988).
Menurut Igoe dan Hui (1996), garam adalah seasoning dan pengawet yang komposisi kimianya adalah natrium klorida, sekitar 40 %
natrium dan 60 % klorida. Secara umum, kristal NaCl tidak berwarna dan
berbentuk kubus.
Pengaruh garam terhadap pertumbuhan mikroba diantaranya
menyebabkan tekanan osmosis yang tinggi sehingga terjadi lisis pada sel
mikroba dan menyerap air dari sel mikroba sehingga kering (Fardiaz,
1989). Selain itu garam juga dapat terurai menjadi ion Cl- yang berbahaya
bagi mikroba, mengurangi kelarutan O2 dalam air, menyebabkan sel lebih
botulinum dapat dihambat pertumbuhannya pada kadar garam 8 % dan
Pseudomonas pada kadar garam 3 % (Fardiaz et al., 1988).
Menurut Muchtadi (1989), media untuk sebagian bakteri
mengandung garam tidak lebih dari 0.85 % (larutan garam fisiologis).
Konsentrasi garam 1-2 % dapat menghambat pertumbuhan beberapa jenis
bakteri. Beberapa mikroba proteolitik dan penyebab kebusukan tidak
toleran pada konsentrasi garam kira-kira 2.5 % ( Winarno et al., 1980). Penambahan garam sebesar 6 % pada makanan mampu
menghambat pertumbuhan mikroba pembusuk dan mikroba pembentuk
spora, sedangkan mikroba patogen (Clostridium botulinum ) dapat dihambat pertumbuhannya oleh penambahan kadar garam 10-12 %
(Purnomo dan Adiono, 1987). Garam dapat mempengaruhi aktivitas air
(aw) dari bahan sehingga dapat mengendalikan pertumbuhan bakteri
(Buckle et al., 1982). Menurut Fardiaz (1989) garam dapat menurunkan RH (kelembaban) atau aw (aktivitas air).
C. MI
1. Jenis Mi
Mi adalah produk pangan yang terbuat dari terigu dengan atau
tanpa penambahan bahan pangan lain dan bahan tambahan pangan yang
diizinkan, berbentuk khas mi (Dewan Standarisasi Nasional, 1992).
Pagani (1985) menyatakan bahwa mi merupakan produk pasta yang
pertama kali ditemukan oleh bangsa China yang berbahan baku beras
dan tepung kacang-kacangan.
Menurut Pagani (1985) berdasarkan ukuran diameter produk, mi
dibedakan menjadi tiga, yaitu spaghetti (0,11 – 0,27 inci), mi (0,07 –
0,125 inci), dan vermiselli (<0,04 inci). Berdasarkan bahan baku,
terdapat dua macam mi, yaitu mi yang berasal dari tepung terutama
tepung terigu dan mi transparan dari bahan baku pati misalnya soun dan
bihun.
Berdasarkan pembuatan dan cara konsumsi, mi dibedakan
mi kering atau mi bakso). Sedangkan berdasarkan jenis produk yang
dipasarkan, terdapat dua jenis mi yaitu mi basah (mi ayam dan mi
kuning) dan mi kering (mi telor dan mi instant). Pada dasarnya baik
produk mi kering maupun mi basah memiliki komposisi yang hampir
sama, hanya saja kadar air, kadar protein dan tahapan proses
pembuatannya yang berbeda.
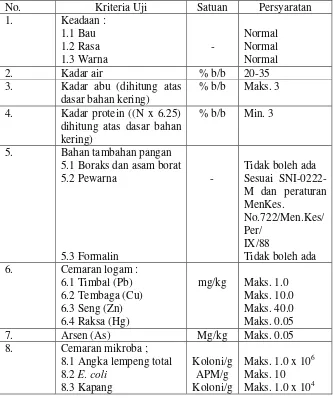
Tabel 3. Syarat mutu mi basah (SNI 01-2987-1992).
Mi basah dapat digolongkan dalam dua kategori berdasarkan
cara pembuatannya, yaitu mi basah mentah (mi ayam) dan mi basah
No. Kriteria Uji Satuan Persyaratan
1. Keadaan :
5. Bahan tambahan pangan
5.1 Boraks dan asam borat 5.2 Pewarna
matang terdapat tahap pemasakan (perebusan/pengukusan) dan
penambahan minyak sawit sehingga kadar airnya meningkat sampai
52%, sedangkan mi basah mentah tidak melewati tahapan tersebut
sehingga kadar airnya sekitar 35% (Astawan, 1999).
Berdasarkan SNI 01–2987–1992, mi basah adalah produk
makanan yang dibuat dari tepung terigu dengan atau tanpa penambahan
bahan makanan lain dan bahan tambahan makanan yang diizinkan,
berbentuk khas mi yang tidak dikeringkan. Syarat mutu mi basah
menurut SNI dapat dilihat pada Tabel 3.
2. Proses Pembuatan Mi
Bahan-bahan yang digunakan pada pembuatan mi basah matang
adalah tepung terigu, garam dapur, air dan garam alkali (Bogasari,
2005). Terigu berfungsi sebagai bahan pembentuk struktur, sumber
karbohidrat dan sumber protein, pelarut garam dan pembentuk sifat
kenyal gluten. Garam berfungsi memberikan rasa, memperkuat tekstur,
membantu reaksi gluten dan karbohidrat, pengikat air serta
meningkatkan elastisitas dan fleksibilitas mi (Astawan, 1999). Air
berfungsi untuk melarutkan garam dapur dan garam alkali, serta
membantu pada pembentukan gluten ( Winarno dan Rahayu, 1994).
Garam alkali yang digunakan dapat terdiri atas natrium karbonat
(Na2CO3), kalium karbonat (K2CO3) atau kalium polifosfat (KH2PO4).
Garam alkali berfungsi meningkatkan pH, menyebabkan warna sedikit
kuning dengan flavor yang lebih baik. Natrium karbonat lebih berperan
untuk kehalusan tekstur, kalium karbonat untuk meningkatkan
kekenyalan sedangkan kalium polifosfat untuk meningkatkan elastisitas
dan fleksibilitas mi. Dapat juga ditambahkan zat warna serta bumbu
untuk memberikan flavor tertentu (Badrudin, 1994).
Proses pembuatan mi basah matang terdiri dari proses
pencampuran, pengadukan, pembentukan lembaran, pengistirahatan/
dan pemberian minyak sawit. Proses pembuatan mi basah dapat dilihat
pada Gambar 1.
pencampuran bahan
pengadukan
pembentukan lembaran
aging
penipisan lembaran
pemotongan lembaran
penaburan mi dengan tapioka
perebusan atau pengukusan
pelumasan
Gambar 1. Diagram alir pembuatan mi basah secara umum.
Tahap pencampuran dalam proses pembuatan mi bertujuan
menghasilkan campuran yang homogen, menghidrasi tepung dengan air
dan membentuk adonan dari jaringan gluten sehingga adonan menjadi
elastis dan halus. Hal-hal yang harus diperhatikan dalam proses
pencampuran adalah jumlah air yang ditambahkan, suhu adonan, dan
waktu pengadukan. Umumnya air yang ditambahkan sekitar 34-40% Bahan-bahan mi
Mi basah matang
dari bobot tepung. Jika air yang ditambahkan kurang dari 34%, adonan
menjadi kalis, rapuh dan sulit dibentuk menjadi lembaran. Sebaliknya
jika air yang ditambahkan lebih dari 40%, adonan menjadi basah dan
lengket. Suhu adonan yang terbaik adalah 25 sampai 40°C. Apabila
suhunya kurang dari 25°C adonan menjadi keras, rapuh dan kasar
sedangkan bila suhunya lebih dari 40°C adonan menjadi lengket dan mi
kurang elastis (Badrudin, 1994).
Pengadukan dilakukan dalam dua tahap. Pengadukan pertama
dilakukan dengan kecepatan lambat selama 1 menit. Selanjutnya
pengadukan dilakukan dengan kecepatan sedang selama 4 menit.
Pengadukan ini berfungsi mendistribusikan air secara merata pada
tepung (Bogasari, 2005).
Setelah pengadukan, dilakukan pembentukan lembaran
(sheeting), proses ini bertujuan menghaluskan serat-serat gluten dan membuat adonan menjadi lembaran (Bahrudin, 1994). Pembentukan
lembaran dilakukan dalam tiga tahap. Tahap pertama adalah
pembentukan lembaran dari adonan dengan jarak roll 3 mm. Tahap
kedua, lembaran yang telah terbentuk dilipat menjadi tiga bagian dan
dilewatkan kembali pada roll yang berjarak 3 mm sebanyak dua kali. Tahap ketiga, lembaran tersebut dilipat menjadi dua bagian dan
dilewatkan kembali di antara dua roll yang berjarak 3 mm. Selanjutnya
lembaran digulung dan diistirahatkan selama 15 menit untuk
menyempurnakan pembentukan gluten.
Setelah diistirahatkan, lembaran ditipiskan sampai terbentuk
lembaran dengan ketebalan 1,5 mm. Lembaran dengan ketebalan 1,5
mm inilah yang siap untuk dipotong menjadi untaian benang-benang mi.
Hasil yang didapatkan setelah tahap pemotongan lembaran adalah
berupa mi basah mentah. Untuk memperoleh produk mi basah matang,
mi dikukus atau direbus. Perebusan dilakukan selama 2 menit,
sedangkan pengukusan dilakukan selama 13 menit. Pemasakan
bertujuan agar terjadi proses gelatinisasi pati dan koagulasi gluten
Gelatinisasi ini membuat pati meleleh dan akan membentuk
lapisan tipis (film) pada permukaan mi yang dapat memberikan kelembutan mi, meningkatkan daya cerna pati dan mempengaruhi daya
rehidrasi mi (Badrudin, 1994). Setelah pemasakan, mi didinginkan
dalam air es selama 1 menit untuk menghentikan reaksi kimia yang
masih terjadi.
Tahap terakhir dalam pembuatan mi basah matang adalah
pemberian minyak sawit. Pelumuran mi dengan minyak sawit dilakukan
agar mi tidak menjadi lengket satu sama lain serta untuk memberikan
citarasa agar mi tampak mengkilap (Mugiarti, 2001 ; Bogasari, 2005).
D. KERUSAKAN MI BASAH
Mi basah digolongkan dalam kelompok bahan pangan yang mudah
rusak (High Perishable Food). Hal inidisebabkan kadar air mi basah yang cukup tinggi serta kondisi sanitasi proses produksi yang kurang terjamin
kebersihannya sehingga mudah ditumbuhi oleh mikroba. Kerusakan yang
terjadi salah satunya disebabkan oleh tumbuhnya kapang. Pertumbuhan
kapang ditandai dengan adanya miselium kapang pada permukaan mi.
Miselium kapang pada mi umumnya berwarna putih atau hitam (Hoseney,
1998).
Kerusakan mi dapat dilihat dari perubahan warna dan diikuti
dengan perubahan aroma mi menjadi asam diikuti dengan pembentukan
lendir. Pembentukan lendir menandakan adanya pertumbuhan bakteri dan
diikuti dengan timbulnya bau asam (Hoseney, 1998).
Mikroba yang terdapat pada mi dapat berasal dari bahan baku mi
yaitu tepung. Menurut Christensen (1974) mikroorganisme yang terdapat
pada tepung adalah kapang, kamir, dan bakteri. Bakteri yang terdapat pada
tepung adalah Pseudomonas, Micrococcus, Lactobacillus serta beberapa spesies Achromobacterium. Kapang yang ditemukan pada tepung antara lain berasal dari genus Aspergillus, Rhizopus, Mucor, Fusarium, dan
Mikroorganisme yang tumbuh pada mi kemungkinan juga berasal
dari air yang digunakan dalam pembuatannya. Mikroorganisme yang
terdapat dalam air yang tidak tercemar adalah khamir, spora Bacillus,
spora Clostridium dan bakteri autotrof (Alcamo, 1983).
Berdasarkan hasil survei yang dilakukan Gracecia dan Priyatna
(2005) terhadap pedagang pasar tradisional dan pedagang produk olahan
mi di daerah Jabotabek, menunjukkan bahwa umur simpan mi basah
mentah dapat mencapai 4 hari, sementara umur simpan mi basah matang
dapat mencapai 14 hari. Padahal menurut Astawan (1999) kerusakan mi
basah matang terjadi pada penyimpanan suhu kamar setelah 40 jam.
Kemungkinan besar telah dilakukan penambahan formalin pada mi
tersebut.
Priyatna (2005) menyatakan bahwa kandungan formalin rata-rata
yang terdapat di dalam mi mentah yang beredar di pasar tradisional
sebesar 106.00 mg/kg bahan, di pedagang produk olahan mi sebesar 72.93
mg/kg bahan, dan mi mentah yang beredar di supermarket sebesar 113.45
mg/kg bahan. Hasil survei yang dilakukan Departemen Ilmu dan
Teknologi Pangan (2005), kandungan formalin yang terdapat pada mi
basah sebesar 2914.36 mg/kg untuk pasar tradisional, 3423.51 mg/kg
untuk produk olahan mi basah, dan 29141.82 mg/kg untuk mi basah yang
terdapat di supermarket.
Secara umum, ciri-ciri kerusakan mi basah mentah dan mi basah
matang hampir sama (Gracecia, 2005 ; dan Priyatna, 2005). Berdasarkan
survei dapat diketahui bahwa kerusakan mi basah mentah ditandai dengan
tumbuhnya kapang (adanya bintik-bintik warna hitam/ merah/ biru),
munculnya bau asam, mi menjadi hancur, patah-patah, atau menjadi
lembek. Begitupula untuk mi basah matang, ciri kerusakan ditandai
dengan adanya bau asam, tekstur menjadi lengket, berlendir, lembek, atau
III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan dalam penelitian ini meliputi bahan
untuk memproduksi mi basah dan bahan untuk analisis. Bahan yang
digunakan untuk produksi mi basah adalah tepung terigu (cakra kembar),
NaCl, soda abu (Na2CO3), air, minyak sawit dan fuli pala dalam bentuk
bubuk. Bahan yang digunakan untuk analisis adalah media PCA (Plate Count Agar), APDA (Acidified Potato Dextrose Agar), larutan pengencer, plastik HDPE, alkohol 70%, dan spiritus.
Alat-alat yang yang digunakan dalam penelitian ini meliputi
alat-alat untuk membuat mi basah dan alat-alat untuk analisis mikrobiologi, fisik
dan sensori. Alat-alat untuk produksi mi basah adalah noodle machine,
mixer, kompor gas, panci, baskom, saringan, sendok, pisau, timbangan, gelas ukur dan gelas piala. Peralatan yang digunakan untuk analisis
mikrobiologi dan fisik adalah cawan petri, stomacher, inkubator, bunsen,
erlenmeyer, tabung reaksi, mikro pipet, otoklaf, oven, hot plate, neraca analitik, pH meter, chromameter minolta dan texture analyzer.
B. METODE PENELITIAN
1.Penentuan Konsentrasi Bubuk Fuli Pala dan NaCl a. Pengujian Daya Simpan Mi Basah Matang
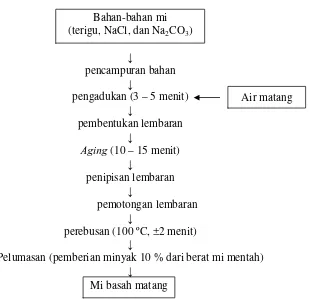
Secara umum proses pembuatan mi basah matang meliputi
formulasi bahan, pencampuran bahan, pembentukan lembaran,
pemotongan, pembentukan mi, perebusan, dan pelumasan
(pemberian minyak). Bahan utama yang digunakan adalah tepung
terigu Cakra Kembar. Bahan-bahan lain yang digunakan adalah
NaCl (1%), natrium karbonat (0.6%), dan air (35%) berdasarkan
pada berat terigu yang digunakan.
Proses pembuatan mi dapat dilihat pada Gambar 2. Mi basah
matang dimasukkan ke dalam plastik HDPE, dibiarkan pada suhu
ruang kemudian dilakukan pengamatan secara subyektif meliputi
adanya tanda-tanda kerusakan berupa bau asam, mi menjadi lunak
dan pembentukan lendir.
↓
pencampuran bahan
↓
pengadukan (3 – 5 menit)
↓
pembentukan lembaran
↓
Aging (10 – 15 menit)
↓
penipisan lembaran
↓
pemotongan lembaran
↓
perebusan (100 ºC, ±2 menit)
↓
Pelumasan (pemberian minyak 10 % dari berat mi mentah)
↓
Gambar 2. Diagram alir pembuatan mi basah.
b. Pembuatan Bubuk Fuli Pala
Fuli pala segar dicuci, ditiriskan, diletakkan dalam cawan,
lalu dikeringkan dalam oven bersuhu 40 - 50°C selama ± 20 jam
hingga kadar airnya mencapai 8-10 % berat kering. Kadar air fuli
pala kering dihitung dengan rumus sebagai berikut :
Keterangan :
a = berat fuli pala segar (g)
b = berat fuli pala setelah dikeringkan dan cawan (g)
c = berat cawan (g)
Setelah kering, fuli pala dihaluskan menggunakan blender Kadar Air (%bk) = ((a-(b-c))/(b-c)) x 100%
Bahan-bahan mi (terigu, NaCl, dan Na2CO3)
Mi basah matang
untuk mendapatkan bubuk fuli pala yang halus dan seragam.
Diagram alir proses pembuatan bubuk fuli pala dapat dilihat pada
Gambar 3.
Cuci dengan air bersih
Tiriskan
Masukkan dalam oven (40-50°C ±20 jam, kadar air mencapai 8-10%)
Blender kering
Ayak (ukuran 60 mesh)
Gambar 3. Diagram alir pembuatan bubuk fuli pala
c. Penentuan Konsentrasi Bubuk Fuli Pala
Bubuk fuli pala ditambahkan ke dalam adonan mi basah
dengan perbandingan tertentu. Formulasi persentase bubuk fuli
pala yang digunakan dapat dilihat pada Tabel 4.
Tabel 4 . Penggunaan bubuk fuli pala dalam mi basah
Bubuk Konsentrasi (b/b)
0.5% dari berat terigu 1% dari berat terigu Fuli pala
1.5% dari berat terigu
Pengaruh konsentrasi bubuk fuli pala terhadap keawetan mi
diamati secara subyektif (warna, aroma, dan tekstur) setelah mi
basah matang selesai dibuat dengan pengamatan setiap 6 jam sekali
sampai terlihat adanya tanda-tanda kerusakan berupa bau asam, mi
menjadi lunak dan pembentukan lendir. Fuli pala segar
Konsentrasi yang dipilih untuk digunakan pada tahap
selanjutnya berdasarkan umur simpan mi terbaik selama
pengamatan subyektif.
d. Penentuan Konsentrasi NaCl
Pengaruh konsentrasi NaCl terhadap keawetan mi basah
matang dilakukan pada beberapa konsentrasi seperti terlihat pada
Tabel 5.
Tabel 5. Formulasi penggunaan NaCl dalam mi basah
Konsentrasi (b/b)
3% dari berat terigu 4% dari berat terigu NaCl
5% dari berat terigu
Pengamatan mi dengan beberapa konsentrasi NaCl di atas
meliputi warna, aroma, dan tekstur secara subyektif setelah mi
basah matang selesai dibuat dengan pengamatan setiap 6 jam sekali
sampai terlihat adanya tanda-tanda kerusakan berupa bau asam, mi
menjadi lunak dan pembentukan lendir. Konsentrasi yang dipilih
untuk digunakan pada tahap selanjutnya berdasarkan umur simpan
mi terbaik selama pengamatan subyektif.
2. Pengaruh Kombinasi Bubuk Fuli Pala dan NaCl Pada Mutu Simpan Mi Basah
Bubuk fuli pala dan NaCl ditambahkan pada tahap
pencampuran adonan dalam pembuatan mi. Konsentrasi bubuk fuli
pala dan NaCl yang digunakan adalah berdasarkan hasil penelitian
sebelumnya. Mi dimasukkan ke dalam plastik HDPE, dibiarkan pada
suhu ruang kemudian dilakukan analisis lebih lanjut setiap 12 jam.
Analisis yang dilakukan meliputi total TPC, total kapang, pH, aw,
organoleptik hanya dilakukan pada saat mi basah matang selesai dibuat
( jam ke-0).
Mi basah matang Mi basah matang
dengan penambahan NaCl dengan penambahan bubuk fuli pala
( 3%, 4%, 5% ) (0.5%, 1%, 1.5% )
Penyimpanan suhu kamar
Analisis setiap 6 jam
(warna, aroma, dan tekstur)
1). Konsentrasi bubuk fuli pala terpilih
2). Konsentrasi NaCl terpilih
Aplikasi pada pembuatan mi basah
(Dibandingkan dengan kontrol tanpa penambahan bubuk fuli pala)
Penyimpanan suhu kamar
Analisis TPC, total kapang, pH, aw, warna, tekstur, dan organoleptik
3. Prosedur Analisis a. Analisis Mikrobiologi
1). Analisis Total Mikroba (BAM-FDA, 2001)
Sebanyak 10 gram sampel mi basah dimasukkan dalam
plastik tahan panas steril yang berisi 90 ml larutan pengencer
steril. Sampel mi basah tersebut kemudian dihancurkan dengan
menggunakan alat stomacher selama 60 detik sehingga dihasilkan sampel mi basah dengan pengenceran 1 : 10. Setelah
itu campuran dikocok, diambil 1 ml dan dimasukkan ke dalam
tabung reaksi berisi 9 ml larutan pengencer steril sehingga
diperoleh tingkat pengenceran 10-2. Dengan cara yang sama
dilakukan pengenceran 10-3 dan 10-4.
Dari masing-masing pengenceran diambil 1 ml suspensi
sampel mi basah secara aseptis dan dimasukkan ke dalam cawan
petri steril secara duplo dan kemudian dituangkan sebanyak 12 –
15 ml media PCA (Plate Count Agar) steril yang bersuhu 45 ±1°C dalam waktu 15 menit dari pengenceran pertama. Setelah
media membeku, cawan petri diinkubasi dengan posisi terbalik
pada suhu 37°C selama dua hari. Perhitungan total mikroba
dilakukan dengan metode BAM-FDA (Bacteriological Analytical Manual), seperti di bawah ini.
Σ C N =
[(1*n1) + (0.1*n2)] * d
Keterangan :
N = jumlah koloni per ml/g produk
Σ C = jumlah seluruh koloni pada cawan yang terhitung n1 = jumlah cawan pada pengenceran pertama
n2 = jumlah cawan pada pengenceran kedua
jumlah koloni pada cawan yang masuk perhitungan
adalah cawan dengan jumlah koloni 25-250 untuk perhitungan
total mikroba. Sementara untuk perhitungan total
kapang-khamir, cawan yang dihitung adalah cawan dengan jumlah
koloni 10-150 (Maturin dan Peeler, 2001).
2). Analisis Total Kapang (SNI-01-2987-1992)
Analisis total kapang sama seperti analisis total mikroba
tetapi media yang digunakan adalah APDA (Acidified Potato Dextrose Agar) dan diinkubasikan pada suhu 25°C atau suhu kamar selama 5 hari. Perhitungan total kapang dilakukan setelah
5 hari. Jumlah kapang dilaporkan per gram atau ml contoh.
b. Analisis Fisik 1). Warna
Analisisis warna dilakukan dengan menggunakan
Chromameter Minolta (tipe CR 200, jepang). Analisis ini dilakukan setiap 12 jam sekali selama 60 jam. Faktor yang
diamati adalah kecerahan (L, a, b). Sampel diletakkan pada
tempat yang tersedia, kemudian ditekan tombol start dan akan diperoleh nilai L, a, dan b dari sampel dengan kisaran nilai 0
sampai 100 (putih). Notasi a menyatakan warna kromatik
campuran merah-hijau dengan nilai +a (positif) dari 0 sampai
+100 untuk warna merah dan nilai –a (negatif) dari 0 sampai
-100 untuk warna hijau. Notasi menyatakan warna kromatik
campuran biru-kuning dengan nilai +b (positif) dari 0 sampai
+70 untuk warna kuning dan nilai –b (negatif) dari 0 sampai -80
untuk warna biru. Sedangkan L menyatakan ketajaman warna.
Semakin tinggi nilai L, maka semakin tinggi tingkat ketajaman
warnanya. Perhitungan nilai a dan b didapatkan nilai h atau
°Hue, dengan rumus sebagai berikut :
Jika hasil yang diperoleh :
18º - 54º maka produk berwarna red (R)
54º - 90º maka produk berwarna yellow red (YR)
90º - 126º maka produk berwarna yellow (Y)
126º - 162º maka produk berwarna yellow green (YG) 162 - 198º maka produk berwarna green (G)
198º - 234º maka produk berwarna blue green (BG) 234º - 270º maka produk berwarna blue (B)
270º - 306º maka produk berwarna blue purple (BP) 306º - 342º maka produk berwarna purple (P) 342º - 378º maka produk berwarna red purple (RP)
2). Tekstur
Pengamatan tekstur dilakukan menggunakan texture analyzer. Faktor yang diamati adalah kekerasan (firmness) dan kelengketan (adhesiveness). Kekerasan dinyatakan dalam satuan
gram force, semakin tinggi nilai gram force semakin tinggi kekerasannya. Kelengketan dinyatakan sebagai luas negative area dengan satuan gram second (gs), semakin luas negative area semakin tinggi kelengketannya. Sampel diletakkan pada tempat yang telah disediakan, kemudian diukur kekerasan dan
kelengketannya.
c. Analisis Kimia
1). Nilai pH (AOAC, 1984)
Mi basah matang terlebih dahulu dilarutkan dalam
akuades dengan perbandingan 1:10. Kemudian mi basah matang
tersebut dihancurkan dengan menggunakan stomacher selama dua menit. Larutan mi basah matang tersebut lalu diukur
menggunakan pH-meter.
Pengukuran nilai pH dilakukan berdasarkan metode
dikalibrasi dengan menggunakan larutan buffer pH 4 dan 7. Kemudian elektroda pH-meter ditempatkan dalam wadah
sampel, ditunggu beberapa saat hingga pH stabil sehingga
terbaca nilai pH yang diukur. Elektroda kemudian diangkat dan
dibilas dengan akuades.
2). Nilai aw
Alat yang digunakan untuk mengukur sampel adalah aw
-meter Shibaura WA-360. Sampel diletakan di dalam cawan
sensor. Kemudian cawan sensor dimasukkan ke dalam sensor
aw-meter dan ditekan tombol start untuk memulai pengukuran. Nilai aw dapat dibaca pada layar setelah ada tulisan complete.
Sebelum digunakan untuk mengukur aw sampel, alat dikalibrasi
dengan NaCl jenuh.
d. Uji Organoleptik (Soekarto, 1985)
Uji organoleptik dilakukan untuk mengetahui tingkat
penerimaan panelis terhadap sampel mi basah matang dengan empat
parameter penilaian, yaitu warna, aroma, tekstur, rasa, dan penilaian
keseluruhan (overall).
Uji yang dilakukan adalah uji hedonik dengan lima
peringkat kesukaan. Uji organoleptik ini menggunakan 30 orang
panelis. Skala yang digunakan pada uji hedonik yaitu : (1) sangat
tidak suka, (2) tidak suka, (3) netral, (4) suka, dan (5) sangat suka.
Data uji hedonik yang didapatkan, dianalisis dengan SPSS 11.5
dengan tipe analisis General Linear Model jenis Univariate. Uji
IV. HASIL DAN PEMBAHASAN
A.PENENTUAN KONSENTRASI BUBUK FULI PALA DAN NaCl 1. Pengujian Daya Simpan Mi Basah Matang
Mi basah matang yang digunakan sebagai kontrol adalah mi basah
dengan formulasi NaCl 1 % dan tanpa penambahan bubuk fuli pala. Mi
basah matang dikemas dalam kantong plastik HDPE dan disimpan pada
suhu ruang kemudian diamati setiap 6 jam sekali sampai terlihat adanya
tanda-tanda kerusakan berupa bau asam, mi menjadi lunak dan
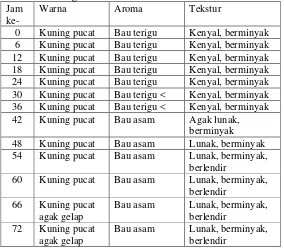
pembentukan lendir. Seperti terlihat pada Tabel 6, mi basah matang telah
mengalami kerusakan pada jam pengamatan ke-42 ditandai dengan adanya
bau asam. Hal ini sesuai dengan apa yang dikemukakan Astawan (1999)
bahwa kerusakan mi basah matang terjadi pada penyimpanan suhu kamar
setelah 40 jam.
Tabel 6. Pengaruh lama penyimpanan terhadap mutu sensori mi basah matang
Jam ke-
Warna Aroma Tekstur
0 Kuning pucat Bau terigu Kenyal, berminyak 6 Kuning pucat Bau terigu Kenyal, berminyak 12 Kuning pucat Bau terigu Kenyal, berminyak 18 Kuning pucat Bau terigu Kenyal, berminyak 24 Kuning pucat Bau terigu Kenyal, berminyak 30 Kuning pucat Bau terigu < Kenyal, berminyak 36 Kuning pucat Bau terigu < Kenyal, berminyak 42 Kuning pucat Bau asam Agak lunak,
berminyak 48 Kuning pucat Bau asam Lunak, berminyak 54 Kuning pucat Bau asam Lunak, berminyak,
berlendir
60 Kuning pucat Bau asam Lunak, berminyak, berlendir
66 Kuning pucat agak gelap
Bau asam Lunak, berminyak, berlendir
72 Kuning pucat agak gelap