DETEKSI DAN IDENTIFIKASI GEN
cry
4 PADA ISOLAT
Bacillus thuringiensis
DAERAH BOGOR DAN SEKITARNYA
NI PUTU AYU SARASWATI
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
NI PUTU AYU SARASWATI. Deteksi dan Identifikasi Gen
cry
4 pada Isolat
Bacillus thuringiensis
Daerah Bogor dan Sekitarnya. Dibimbing oleh LAKSMI
AMBARSARI dan EDDY JUSUF.
ABSTRACT
NI PUTU AYU SARASWATI. Detection and Identification of
cry
4 Genes in
Bacillus thuringiensis
Isolates from Bogor and Its Surrounding Areas. Under the
direction of LAKSMI AMBARSARI and EDDY JUSUF.
DETEKSI DAN IDENTIFIKASI GEN
cry
4 PADA ISOLAT
Bacillus thuringiensis
DAERAH BOGOR DAN SEKITARNYA
NI PUTU AYU SARASWATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Program Studi Biokimia
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Deteksi dan Identifikasi Gen
cry
4 pada Isolat
Bacillus
thuringiensis
Daerah Bogor dan Sekitarnya
Nama
: Ni Putu Ayu Saraswati
NIM :
G44103027
Disetujui
Komisi Pembimbing
Dr. Laksmi Ambarsari, M.Si Drs. Eddy Jusuf, DES
Ketua Anggota
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, M.S.
NIP 131 473 999
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa yang
telah memberikan rahmat dan anugerah-Nya sehingga penulis dapat
menyelesaikan penulisan karya ilmiah ini. Karya ilmiah berjudul Deteksi dan
Identifikasi Gen
cry
4 pada Isolat
Bacillus thuringiensis
Daerah Bogor dan
Sekitarnya merupakan hasil penelitian yang dilakukan penulis mulai dari bulan
Februari hingga Juli 2007 di Laboratorium Rekayasa Mikrob dan Genetika,
Bidang Biologi Molekular dan Mikrob, Pusat Penelitian Bioteknologi LIPI
Cibinong.
Penulis telah melibatkan berbagai pihak, baik dalam proses kegiatan
penelitian maupun penulisan karya ilmiah ini, sehingga pada kesempatan ini
penulis ingin mengucapkan terima kasih kepada Dr. Laksmi Ambarsari, M.Si
serta Drs. Eddy Yusuf, DES selaku komisi pembimbing, Mbak Neneng, Mas
Ridwan, Mbak Yuli, Isra, Andika, Wurian, dan seluruh staf dan peneliti di Pusat
Penelitian Bioteknologi LIPI atas bimbingan dan kerja samanya. Ucapan terima
kasih juga penulis sampaikan kepada Mama, Papa, Nde, serta Wisnu Herlambang
atas kasih sayang, doa, dan dukungannya; serta pihak-pihak lain yang tidak dapat
disebutkan satu per satu.
Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Oktober 2007
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 19 Desember 1985 dari
pasangan I Nyoman Suparta dan Ati Suliyati. Penulis merupakan anak pertama
dari dua bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 2 Bekasi dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis memilih Program Studi Biokimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Penulis pernah menjadi asisten praktikum Biokimia Fisik pada tahun
ajaran 2006/2007. Pada tahun 2006, penulis mengikuti Praktik Kerja Lapang di
Laboratorium Rekayasa Mikrob dan Genetika, Bidang Biologi Molekular dan
Mikrob, Pusat Penelitian Bioteknologi Lembaga Ilmu Pengetahuan Indonesia
(LIPI) Cibinong, Bogor. Penulis juga mendapat beasiswa Peningkatan Prestasi
Akademik (PPA) pada tahun ajaran 2005/2006 dan tahun ajaran 2006/2007.
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 1
Bacillus thuringiensis
...
1
Gen
cry
...
2
Demam Berdarah ... 3
Polymerase Chain Reaction
(PCR) ... 3
BAHAN DAN METODE ... 3
Bahan dan Alat ... 3
Metode ...
4
HASIL DAN PEMBAHASAN ... 5
Plasmid Hasil Induksi dengan Antibiotik ... 5
DNA Genom Hasil Ekstraksi ... 6
Suhu Optimum
Annealing
... 7
Hasil Amplifikasi Gen
cry
4Ba1 ... 8
SIMPULAN DAN SARAN ... 10
DAFTAR PUSTAKA ... 10
DAFTAR TABEL
Halaman
1 Hasil uji antibiotik pada setiap isolat
B. thuringiensis
... 5
2 Konsentrasi dan kemurnian DNA genom hasil ekstraksi ... 6
3 Komposisi pereaksi dalam reaksi ampifikasi ... 7
4 Primer yang digunakan dalam reaksi PCR ... 7
DAFTAR GAMBAR
Halaman
1 Visualisasi
Bacillus thuringiensis
... 2
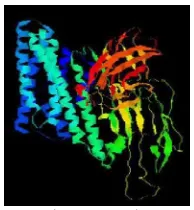
2 Struktur molekul protein Cry ... 2
3 Tahapan reaksi PCR ... 3
4 Elektroforegram fragmen DNA
B. thuringiensis
HD-567 dengan primer
Cry4B4 pada berbagai variasi suhu
annealing
... 8
5 Elektroforegram fragmen DNA
B. thuringiensis
HD-567 dengan primer
Cry4A2 pada berbagai variasi suhu
annealing
... 8
6 Elektroforegram fragmen DNA
B. thuringiensis
HD-567 dengan primer
Dip1A pada berbagai variasi suhu
annealing
... 8
DAFTAR LAMPIRAN
Halaman
1 Strategi penelitian ... 13
2 Tahapan induksi plasmid dengan antibiotik ... 14
3 Tahapan ekstraksi DNA genom ... 14
4 Daftar isolat
B. thuringiensis
yang digunakan beserta asalnya ... 15
DETEKSI DAN IDENTIFIKASI GEN
cry
4 PADA ISOLAT
Bacillus thuringiensis
DAERAH BOGOR DAN SEKITARNYA
NI PUTU AYU SARASWATI
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
NI PUTU AYU SARASWATI. Deteksi dan Identifikasi Gen
cry
4 pada Isolat
Bacillus thuringiensis
Daerah Bogor dan Sekitarnya. Dibimbing oleh LAKSMI
AMBARSARI dan EDDY JUSUF.
ABSTRACT
NI PUTU AYU SARASWATI. Detection and Identification of
cry
4 Genes in
Bacillus thuringiensis
Isolates from Bogor and Its Surrounding Areas. Under the
direction of LAKSMI AMBARSARI and EDDY JUSUF.
DETEKSI DAN IDENTIFIKASI GEN
cry
4 PADA ISOLAT
Bacillus thuringiensis
DAERAH BOGOR DAN SEKITARNYA
NI PUTU AYU SARASWATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Program Studi Biokimia
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Deteksi dan Identifikasi Gen
cry
4 pada Isolat
Bacillus
thuringiensis
Daerah Bogor dan Sekitarnya
Nama
: Ni Putu Ayu Saraswati
NIM :
G44103027
Disetujui
Komisi Pembimbing
Dr. Laksmi Ambarsari, M.Si Drs. Eddy Jusuf, DES
Ketua Anggota
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, M.S.
NIP 131 473 999
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa yang
telah memberikan rahmat dan anugerah-Nya sehingga penulis dapat
menyelesaikan penulisan karya ilmiah ini. Karya ilmiah berjudul Deteksi dan
Identifikasi Gen
cry
4 pada Isolat
Bacillus thuringiensis
Daerah Bogor dan
Sekitarnya merupakan hasil penelitian yang dilakukan penulis mulai dari bulan
Februari hingga Juli 2007 di Laboratorium Rekayasa Mikrob dan Genetika,
Bidang Biologi Molekular dan Mikrob, Pusat Penelitian Bioteknologi LIPI
Cibinong.
Penulis telah melibatkan berbagai pihak, baik dalam proses kegiatan
penelitian maupun penulisan karya ilmiah ini, sehingga pada kesempatan ini
penulis ingin mengucapkan terima kasih kepada Dr. Laksmi Ambarsari, M.Si
serta Drs. Eddy Yusuf, DES selaku komisi pembimbing, Mbak Neneng, Mas
Ridwan, Mbak Yuli, Isra, Andika, Wurian, dan seluruh staf dan peneliti di Pusat
Penelitian Bioteknologi LIPI atas bimbingan dan kerja samanya. Ucapan terima
kasih juga penulis sampaikan kepada Mama, Papa, Nde, serta Wisnu Herlambang
atas kasih sayang, doa, dan dukungannya; serta pihak-pihak lain yang tidak dapat
disebutkan satu per satu.
Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Oktober 2007
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 19 Desember 1985 dari
pasangan I Nyoman Suparta dan Ati Suliyati. Penulis merupakan anak pertama
dari dua bersaudara.
Tahun 2003 penulis lulus dari SMU Negeri 2 Bekasi dan pada tahun yang
sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB
(USMI). Penulis memilih Program Studi Biokimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Penulis pernah menjadi asisten praktikum Biokimia Fisik pada tahun
ajaran 2006/2007. Pada tahun 2006, penulis mengikuti Praktik Kerja Lapang di
Laboratorium Rekayasa Mikrob dan Genetika, Bidang Biologi Molekular dan
Mikrob, Pusat Penelitian Bioteknologi Lembaga Ilmu Pengetahuan Indonesia
(LIPI) Cibinong, Bogor. Penulis juga mendapat beasiswa Peningkatan Prestasi
Akademik (PPA) pada tahun ajaran 2005/2006 dan tahun ajaran 2006/2007.
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 1
Bacillus thuringiensis
...
1
Gen
cry
...
2
Demam Berdarah ... 3
Polymerase Chain Reaction
(PCR) ... 3
BAHAN DAN METODE ... 3
Bahan dan Alat ... 3
Metode ...
4
HASIL DAN PEMBAHASAN ... 5
Plasmid Hasil Induksi dengan Antibiotik ... 5
DNA Genom Hasil Ekstraksi ... 6
Suhu Optimum
Annealing
... 7
Hasil Amplifikasi Gen
cry
4Ba1 ... 8
SIMPULAN DAN SARAN ... 10
DAFTAR PUSTAKA ... 10
DAFTAR TABEL
Halaman
1 Hasil uji antibiotik pada setiap isolat
B. thuringiensis
... 5
2 Konsentrasi dan kemurnian DNA genom hasil ekstraksi ... 6
3 Komposisi pereaksi dalam reaksi ampifikasi ... 7
4 Primer yang digunakan dalam reaksi PCR ... 7
DAFTAR GAMBAR
Halaman
1 Visualisasi
Bacillus thuringiensis
... 2
2 Struktur molekul protein Cry ... 2
3 Tahapan reaksi PCR ... 3
4 Elektroforegram fragmen DNA
B. thuringiensis
HD-567 dengan primer
Cry4B4 pada berbagai variasi suhu
annealing
... 8
5 Elektroforegram fragmen DNA
B. thuringiensis
HD-567 dengan primer
Cry4A2 pada berbagai variasi suhu
annealing
... 8
6 Elektroforegram fragmen DNA
B. thuringiensis
HD-567 dengan primer
Dip1A pada berbagai variasi suhu
annealing
... 8
DAFTAR LAMPIRAN
Halaman
1 Strategi penelitian ... 13
2 Tahapan induksi plasmid dengan antibiotik ... 14
3 Tahapan ekstraksi DNA genom ... 14
4 Daftar isolat
B. thuringiensis
yang digunakan beserta asalnya ... 15
1
PENDAHULUAN
Beberapa jenis serangga dapat menjadi vektor dalam menyebarkan virus atau bakteri penyebab penyakit berbahaya. Aedes aegypti adalah serangga vektor yang membawa virus penyebab penyakit demam berdarah. Sampai saat ini, Indonesia masih belum dapat menanggulangi masalah demam berdarah secara tuntas. Setiap tahun berpuluh-puluh kota di sebagian besar wilayah Indonesia terjangkit oleh penyakit ini, tidak terkecuali Bogor. Kasus demam berdarah bahkan telah ditetapkan sebagai kejadian luar biasa (KLB) di daerah Kabupaten Bogor dan Kota Bogor oleh Gubernur Jawa Barat (Fikri 2007). Penanggulangan demam berdarah dengan melakukan fogging atau pengasapan seringkali kurang efektif. Selain menimbulkan pencemaran lingkungan, pengasapan hanya membunuh nyamuk-nyamuk dewasa. Jentik nyamuk tetap hidup dan akan berkembang menjadi nyamuk dewasa dalam waktu empat hari. Selain itu, pestisida kimiawi juga dapat menimbulkan resistensi pada serangga target. Salah satu alternatif yang dapat dilakukan adalah dengan menggunakan biopestisida yang ramah lingkungan dan dapat membunuh jentik nyamuk.
Bacillus thuringiensis merupakan bakteri yang menghasilkan protein kristal yang bersifat toksik terhadap serangga dan nematoda selama masa sporulasi. Bentuk sediaan kuning bakteri ini, yang terdiri atas spora dan kristal, telah diaplikasikan sebagai pestisida biologis atau biopestisida untuk menghambat perkembangan serangga-serangga hama pertanian maupun nyamuk pembawa penyakit malaria dan demam berdarah (Ben-dovet al. 1997).
Keunggulan dari penggunaan bakteri ini sebagai biopestisida antara lain protein yang dihasilkan oleh B. thuringiensis bersifat antiserangga spesifik dan disebut sebagai protein Cry (dari kata crystal) atau disebut juga dengan nama -endotoksin (Zeigleret al. 1999). Protein Cry hanya bersifat toksik terhadap jenis serangga tertentu dan tidak toksik terhadap serangga yang berguna maupun terhadap organisme lain. Selain itu, reproduksi dari bakteri ini tergolong mudah, yaitu dengan proses fermentasi untuk produksi biomassanya menggunakan bahan-bahan organik buangan atau limbah pertanian dan industri.
Kemajuan teknologi di bidang biologi molekuler telah mendorong para ilmuwan untuk mengisolasi kromosom ataupun plasmid
yang mengandung gen cry. Gen cry merupakan sekuens DNA pembawa sandi pembentukan protein Cry. Kromosom ataupun plasmid yang mengandung gencry ini dapat disisipkan pada alga sebagai pakan nyamuk sehingga alga transgenik tersebut dapat digunakan untuk membunuh jentik nyamuk. Berdasarkan perbedaan dalam untaian asam amino penyusunnya, telah diidentifikasikan lebih dari 300 macam protein kristal -endotoksin hingga tahun ini. Protein Cry yang bersifat toksik terhadap nyamuk adalah protein Cry4. Setiap jenis protein Cry bersifat toksik spesifik terhadap serangga atau nematoda tertentu sehingga diperlukan metode khusus untuk mendeteksi dan mengidentifikasi protein Cry sebelum protein Cry tersebut diaplikasikan. Salah satu cara untuk mengetahui tipe protein Cry pada suatu isolat B. thuringiensis adalah dengan polymerase chain reaction (PCR). Teknik PCR merupakan prosedur yang dapat menentukan keberadaan sekuens DNA target secara cepat. Identifikasi diperoleh dengan menggunakan primer yang spesifik untuk mengamplifikasi DNA yang diinginkan sehingga jenis gencry (penyandi protein Cry) yang terkandung di dalam isolat dapat diketahui dan dapat diperkirakan daya spesifiknya terhadap serangga tertentu.
Penelitian ini bertujuan untuk mengidentifikasi gencry4 pada isolat-isolatB. thuringiensis secara cepat dan akurat dengan metode PCR.
Hipotesis dari penelitian ini adalah isolat-isolat B. thuringiensis yang diuji mengandung gen cry4 yang bersifat toksik terhadap larva nyamukAedes aegypti.
Penelitian ini diharapkan dapat memberikan informasi mengenai isolat-isolat B. thuringiensis yang mengandung gen cry4 sehingga isolat tersebut dapat digunakan lebih lanjut, baik untuk keperluan rekayasa genetik maupun sebagai biopestisida.
TINJAUAN PUSTAKA
Bacillus thuringiensis
2
protein -endotoksin, disebut juga protein Cry, yang bersifat toksik terhadap serangga tertentu. Serangga target harus memakan protein Cry ini agar protein Cry dapat menempel pada protein reseptor yang berada pada permukaan sel epitel usus. Penempelan protein ini akan melumpuhkan sistem pencernaan melalui pembentukan lubang pada usus sehingga sel lisis. Adanya kerusakan pada epitel usus menyebabkan serangga target akan mati karena kelaparan.
Protein Cry yang dihasilkan oleh B. thuringiensis bersifat spesifik terhadap serangga target dan tidak berbahaya bagi serangga yang berguna, misalnya lebah madu. Protein ini bersifat spesifik karena diproduksi dalam bentuk protoksin dan hanya aktif pada kondisi tertentu. Daya spesifik dari toksin ini berdasarkan kelarutannya pada usus serangga kemudian mengaktifkan protoksin menjadi toksin (Broderick et al. 2006). Sifat spesifik dari protein Cry juga dipengaruhi oleh reseptor pada usus serangga target. Protein Cry akan berikatan dengan reseptor khusus pada usus serangga. Perbedaan reseptor di antara berbagai jenis serangga membuat protein Cry memiliki spesifitas yang tinggi. Manusia dan hewan vertebrata lain tidak memiliki reseptor ini dalam tubuhnya sehingga toksin protein Cry tidak membahayakan manusia.
Karakterisasi protein Cry dari setiap isolat B. thuringiensis mutlak diperlukan karena serangga target dari setiap jenis protein Cry berbeda-beda. Identifikasi B. thuringiensis dengan bioassay berlangsung lama dan membutuhkan proses. AnalisisSouthern blot ataupun reaktivitas dengan berbagai antibodi monoklonal banyak menghabiskan waktu dan biaya. Cara terbaru mengidentifikasi protein Cry pada B. thuringiensis melalui metode PCR untuk mengidentifikasi gencry-nya.
Gambar 1 Visualisasi Bacillus thuringiensis. (Sumber:
http://www.dmu.dk/foralle/Bakter ier/Bakterier+i+jordbrugets+tjenes te/Mikrobiologiske+bek%C3%A6 mpelsesmidler.htm)
Gen cry
Gen yang mengendalikan protein cry disebut gencry. Gen cry dapat berada pada plasmid, kromosom, atau keduanya. Klasifikasi terbaru mengenai pembagian jenis gen cry dibuat oleh Dr. D.R. Zeigler dari Departement Biochemistry, The Ohio State University USA. Spesies bakteri ini dibedakan menjadi 68 subspesies dengan istilahserovar yang ditentukan berdasarkan perbedaan sifat antigen flagella-nya. Setiap subspesies ini dibedakan lagi berdasarkan perbedaan sifat protein Cry, toksisitas maupun karakter genetik lainnya dengan istilah strain (galur). Setiap galur memiliki toksisitas yang spesifik dengan serangga target yang spesifik pula (Zeigler et al. 1999). Setiap jenis protein memiliki nama gen sesuai dengan nama proteinnya, misalnya untuk penyandi protein Cry4Aa adalah gen cry4Aa. Gambar 2 menunjukkan salah satu struktur molekul protein Cry.
Ekspresi gen cry dapat tergantung pada sporulasi maupun tidak. Ekspresi gencry yang tergantung pada sporulasi dikontrol oleh succesive activation of sigma factor ( ). Sporulasi dikontrol oleh A yang berikatan dengan RNA polimerase. Contoh gen cry yang berekspresi dengan cara ini adalah cry1Aa, cry1Ba, cry2Aa, cry4Aa, cry4Ba, cry11Aa,cry15Aa, dancry18Aa. Ekspresi gen cry yang tidak bergantung pada sporulasi ditemukan pada gen cry3Aa dari subsp. tenebrionis.
Gen cry4 memiliki daya toksik terhadap larva nyamuk dan lalat hitam. Gen cry4 terbagi menjadi empat tipe, yaitu cry4A, cry4B, cry4C, dan cry4D. Gen cry4A dan cry4B menyandi protein Cry4A dan Cry4B dengan bobot molekul 130 kDa. Protein Cry4A bersifat toksik terhadap Anopheles stephensi, Aedes aegypti, dan Culex pipiens sedangkan protein Cry4B bersifat toksik terhadapAedes aegypti (Bullaet al. 1991).
3
Demam Berdarah
Demam berdarah adalah penyakit akut yang disebabkan infeksi virus yang dibawa oleh nyamuk Aedes aegypti dan Aedes albopictus betina yang umumnya menyerang pada musim panas dan musim hujan. Virus tersebut menyebabkan gangguan pada pembuluh darah kapiler dan sistem pembekuan darah, sehingga mengakibatkan perdarahan.
Penanganan demam berdarah di Indonesia belum memuaskan. Hal ini dapat dilihat dari angka penderita yang signifikan. Setiap tahun, puluhan orang di Indonesia meninggal karena demam berdarah. Bogor dan Jakarta merupakan daerah yang tidak pernah luput dari serangan demam berdarah. Kasus demam berdarah pada kedua daerah ini hampir setiap tahun dinyatakan sebagai kejadian luar biasa (KLB). Kompas (2007) menyebutkan bahwa penderita demam berdarah di Jakarta mencapai 2022 orang sedangkan di daerah Bogor berjumlah 453 orang, dengan 14 orang di antaranya meninggal. Pikiran Rakyat (2006) melaporkan hampir 75% daerah Bogor terjangkit penyakit ini. Tingginya angka penderita demam berdarah di Jakarta dan banyaknya korban yang meninggal akibat penyakit ini di daerah Bogor menunjukkan diperlukannya metode baru untuk mengatasi masalah tersebut.
Polymerase Chain Reaction(PCR)
Reaksi PCR pertama kali diperkenalkan oleh Kary Mullis pada tahun 1983. Teknik ini merupakan teknik penggandaan molekul DNA secarain vitro melibatkan penggunaan primer, yaitu bagian kecil dari pasangan komplementer DNA yang akan disintesis dan DNA polimerase yang tahan panas. Teknik PCR sangat sensitif, dapat menggandakan sampai lebih dari sejuta kali sehingga dapat menghasilkan DNA dalam jumlah yang sangat besar. Oleh karena itu, teknik ini hanya membutuhkan DNA template dalam jumlah kecil (Jones 2003).
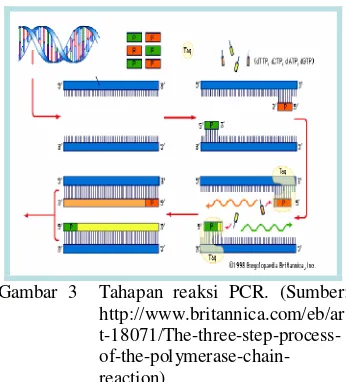
Reaksi PCR berlangsung dalam tiga tahapan, yaitu denaturasi, annealing (penempelan primer), dan elongation (pemanjangan nukleotida). Tahapan tersebut dapat dilihat pada Gambar 3. Teknik PCR membutuhkan komponen-komponen pereaksi, yaitu Taq DNA polimerase, dNTP, DNA template, oligonukleotida primer, dan larutan bufer.TaqDNA polimerase merupakan enzim tahan panas yang diisolasi dari bakteri termofilikThermus aquaticus.
Gambar 3 Tahapan reaksi PCR. (Sumber: http://www.britannica.com/eb/ar t-18071/The-three-step-process- of-the-polymerase-chain-reaction)
Metode PCR digunakan oleh peneliti-peneliti di seluruh dunia untuk mendeteksi gen cry pada isolat-isolatB. thuringiensis di daerah mereka. Carozzi et al. (1991) menggunakan metode PCR untuk memprediksi aktifitas antiseranggga dari isolat-isolat B. thuringiensis yang diisolasi dari tanah dan bangkai serangga di Amerika Serikat sedangkan deteksi gen cry di daerah Spanyol dilakukan oleh Jua´rez-Pe´rez et al. (1997). Daerah Israel, Kazakhstan, dan Usbekistan merupakan daerah yang diteliti oleh Ben-Dov et al. (1997). Bravo et al. (1998) menggunakan PCR untuk melakukan karakterisasi terhadap gen cry pada isolat-isolatB. thuringiensis di Mexico.
BAHAN DAN METODE
Bahan dan Alat
4
tabung mikro, gelas ukur, pipet Pasteur, labu takar, mikropipet, batang pengaduk, sudip, jarum ose, lemari pendingin, autoklaf, inkubator, vorteks, iluminator sinar ultra violet, sentrifus Heraeus Biofuge Fresco dengan rotor tetap #3324 jari-jari 5,5 cm, neraca analitik Sartorius, peralatan elektroforesis Pharmacia, pH meter Thermolyne, masker pelindung radiasi UV, spektrofotometer, mesin termocycler PCR, penangas air, kamera, dan film polaroid.
Metode
Pembuatan Media Luria Bertani (LB) Padat dengan Antibiotik
Media LB dibuat dengan cara mencampurkan 5,00 gyeast extract, 10,00 g bakto tripton, dan 10,00 g NaCl dalam Erlenmeyer kemudian ditambahkan 850 mL air destilata. Larutan diatur pH-nya hingga diperoleh pH 7 dengan menambahkan NaOH 5 N, ditambahkan 12,00 g agar, ditepatkan volumenya hingga 1 L, dan dikocok hingga larut. Media disterilisasi dengan autoklaf selama 15 menit pada suhu 121 °C kemudian dibiarkan hingga mencapai suhu 45 °C, ditambahkan antibiotik, kemudian dituang ke cawan petri steril dan tabung reaksi steril untuk dibuat agar miring. Antibiotik yang digunakan adalah ampisilin 35 µg/mL, kanamisin 50 µg/mL, tetrasiklin 12,5 µg/mL, streptomisin 25 µg/mL, asam nalidiksat 20 µg/mL, dan kloramfenikol 30 µg/mL. Setiap cawan petri masing-masing diisi dengan satu jenis antibiotik. Penggunaan campuran antibiotik dilakukan apabila ada isolat yang memiliki resistensi lebih dari satu antibiotik.
Induksi Plasmid dengan Antibiotik (Sambrook 1989)
Biakan bakteri diambil sebanyak satu ose dari kultur stok, dibiakkan dalam cawan petri berisi media LB dengan metode gores. Biakan ini diinkubasi selama 24 jam, kemudian diamati dan koloni terkecilnya diambil dengan jarum ose untuk digoreskan kembali. Setiap isolat diuji dengan media yang mengandung antibiotik pada suhu 30 °C selama 16 jam, pengujian dilakukan tiga kali untuk setiap isolat. Isolat yang memiliki resistensi terhadap lebih dari satu antibiotik kemudian diujikan kembali dengan menggunakan campuran antibiotik yang dapat ditahan oleh isolat tersebut. Dosis antibiotik yang digunakan pada campuran ini sama dengan uji sebelumnya. Hasil uji antibiotik kemudian
digunakan untuk meremajakan setiap biakan bakteri, baik untuk stock culture maupun untukworking culture.
Pembuatan Media Luria Bertani (LB) Cair dengan Antibiotik
Media LB cair dibuat dengan cara mencampurkan 5,00 gyeast extract, 10,00 g bakto tripton, dan 10,00 g NaCl dalam Erlenmeyer kemudian ditambahkan 850 mL air destilata. Larutan diatur pH-nya hingga mencapai 7, ditepatkan volumenya hingga 1 L, dan dikocok hingga larut. Media kemudian dituang ke dalam tabung reaksi, masing-masing sebanyak 5 mL. Media ini kemudian disterilisasi dengan autoklaf selama 15 menit pada suhu 121 °C, dibiarkan hingga mencapai suhu 45 °C, kemudian ditambahkan antibiotik.
Ekstraksi DNA
Prosedur ekstraksi DNA secara cepat diadaptasi dari berbagai teknik (Juarez-Perez et al. 1997, Frederiksenet al. 2006). Sebanyak 5 ml kultur B. thuringiensis ditumbuhkan selama 16 jam pada suhu 30 °C, dengan pengocokan 200 rpm, untuk dijadikanstarter. Sebanyak 0,1 mL dari starter diinkubasi dalam 5 mL media LB selama 4 jam pada suhu 30 °C dengan pengocokan 200 rpm. Kultur tersebut kemudian disentrifugasi selama 5 menit pada kecepatan 10000 rpm. Pelet yang diperoleh dicuci dengan akuabides, kemudian diresuspensi dengan 100 µ L akuabides steril. Pemecahan sel dilakukan dengan cara melakukan inkubasi sebanyak dua siklus pada suhu 100 °C dan -5 °C masing-masing selama 10 menit. Selanjutnya dilakukan sentrifugasi selama 5 menit pada kecepatan 12000 rpm dan supernatan yang diperoleh digunakan sebagai DNA template pada reaksi PCR.
Optimasi SuhuAnnealing
5
sebanyak 35 siklus. Amplikon hasil PCR dielektroforesis dengan 1% gel agarosa dalam bufer TBE, diwarnai dengan EtBr, kemudian divisualisasi. Suhu annealing yang dapat menghasilkan amplikon digunakan dalam reaksi selanjutnya.
Identifikasi Gencry4Ba1
Identifikasi dilakukan dengan teknik PCR. Setiap tabung mikro PCR diisi dengan 2,5 µL bufer reaksi PCR 10x, 2 U enzimTaq DNA polimerase, 200 nM untuk masing-masing dNTP, 0,4 µM untuk masing-masing primer, dan 1 µL DNA hasil isolasi. Larutan ini kemudian ditambah aquabides sampai volume reaksi menjadi 25 µL. Reaksi PCR dilakukan sesuai dengan kondisi yang sesuai menurut optimasi suhu annealing pada tahap sebelumnya. Amplikon hasil PCR di-elektroforesis dengan 1% gel agarosa dalam bufer TBE, diwarnai dengan EtBr, kemudian divisualisasi.
HASIL DAN PEMBAHASAN
Plasmid Hasil Induksi dengan Antibiotik
Bakteri yang terus-menerus diremajakan dalam media yang kaya nutrisi berpotensi untuk kehilangan plasmidnya. Plasmid, elemen ekstrakromosom dan menyandi metabolit sekunder, tidak diproduksi oleh bakteri karena bakteri tersebut berada dalam keadaan aman dan tidak memerlukan plasmid untuk bertahan hidup. Oleh karena itu, B. thuringiensis ditumbuhkan dalam media yang ditambahkan antibiotik untuk menginduksi B. thuringiensis agar tetap mempertahankan plasmidnya. Keberadaan plasmid pada isolat-isolat B. thuringiensis sangat diperlukan karena sebagian besar gen cry yang akan dianalisis terdapat dalam plasmid walaupun ada beberapa galur yang terbukti memiliki gencryyang terdapat dalam kromosomnya (Kronstadet al. 1983).
Penambahan antibiotik dalam media akan membuat B. thuringiensis dalam keadaan tercekam sehingga bakteri tersebut akan membutuhkan suatu bentuk pertahanan untuk tetap hidup dan berkembang. Cara pertahanan tersebut adalah dengan memproduksi plasmid yang mengandung gen-gen yang resisten terhadap antibiotik. Diharapkan plasmid hasil induksi ini adalah plasmid-plasmid yang membawa gencry sehingga gen cry tersebut dapat dianalisis lebih lanjut dengan teknik PCR.
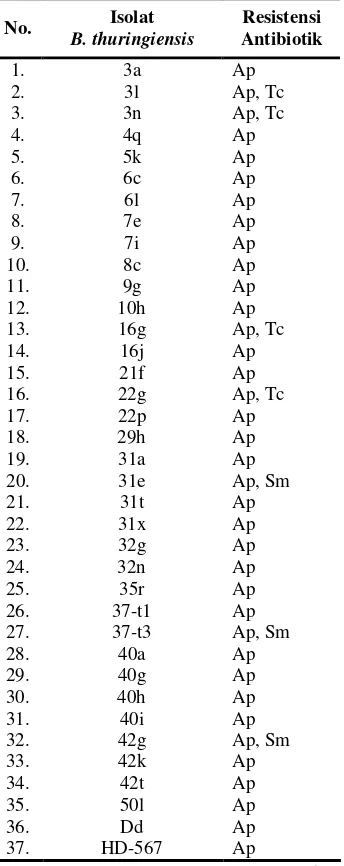
Tabel 1 menunjukkan hasil induksi antibiotik terhadap isolat-isolat B. thuringiensis. Semua isolat dan galur pembanding HD-567 memiliki resistensi terhadap ampisilin. Hanya ada empat isolat yang memiliki resistensi terhadap ampisilin dan tetrasiklin, yaitu 3l, 3n, 16g, dan 22g. Isolat 31e, 37-t3, dan 42g memiliki resistensi terhadap ampisilin dan streptomisin. Tidak ada isolat yang memiliki resistensi terhadap kloramfenikol, asam nalidiksat, dan kanamisin.
Tabel 1 Hasil uji antibiotikB. thuringiensis (Herlambang W, 9 Mei 2007, komunikasi pribadi)
No. Isolat
B. thuringiensis
Resistensi Antibiotik
1. 3a Ap
2. 3l Ap, Tc
3. 3n Ap, Tc
4. 4q Ap
5. 5k Ap
6. 6c Ap
7. 6l Ap
8. 7e Ap
9. 7i Ap
10. 8c Ap
11. 9g Ap
12. 10h Ap
13. 16g Ap, Tc
14. 16j Ap
15. 21f Ap
16. 22g Ap, Tc
17. 22p Ap
18. 29h Ap
19. 31a Ap
20. 31e Ap, Sm
21. 31t Ap
22. 31x Ap
23. 32g Ap
24. 32n Ap
25. 35r Ap
26. 37-t1 Ap
27. 37-t3 Ap, Sm
28. 40a Ap
29. 40g Ap
30. 40h Ap
31. 40i Ap
32. 42g Ap, Sm
33. 42k Ap
34. 42t Ap
35. 50l Ap
36. Dd Ap
37. HD-567 Ap
6
Adanya resistensi antibiotik pada isolat-isolat B. thuringiensis dan galur pembanding HD-567 menunjukkan bahwa bakteri-bakteri tersebut mengandung gen resisten terhadap antibiotik. Jusuf (2001) menyebutkan bahwa gen-gen resistensi terhadap antibiotik terdapat pada transposon yang sebagian besar terdapat pada plasmid. Gen-gen tersebut membuat isolat-isolat B. thuringiensis tidak terhambat pertumbuhannya pada media yang mengandung antibiotik. Cara kerja gen resisten terhadap antibiotik ini disebabkan karena satu dari tiga mekanisme berikut, yaitu dengan mengubah daerah target interaksi antibiotik, mencegah masuknya antibiotik ke dalam sel, atau menghasilkan enzim yang memodifikasi atau menginaktifkan antibiotik (Rodriguez & Tait 1983).
DNA Genom Hasil Ekstraksi
Gencry yang akan dianalisis dengan PCR dapat berada pada plasmid ataupun pada kromosom sehingga DNAtemplate yang akan digunakan pada reaksi PCR harus mengandung keduanya, baik DNA plasmid maupun DNA kromosom. Oleh karena itu, ekstraksi yang dilakukan adalah ekstraksi DNA genom atau DNA total sehingga DNA plasmid dan DNA kromosom dapat terekstrak dan dapat digunakan sebagai DNA template pada reaksi PCR.
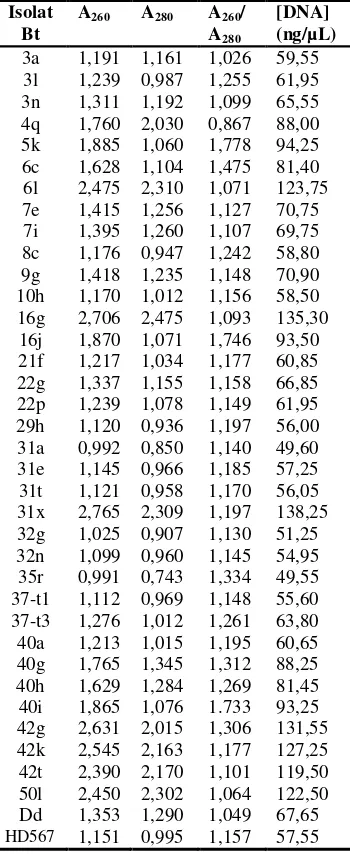
Ekstraksi DNA genom dilakukan dengan menggunakan metode cepat yang diadaptasi dari Juarez-Perez et al. (1997) dan Frederiksen et al. (2006). Perlakuan fisik dengan suhu panas dan dingin secara berulang akan menyebabkan sel bakteri lisis dan komponen protein terdenaturasi sehingga DNA akan terlarut dalam supernatan ketika dilakukan sentrifugasi. Tabel 2 menunjukkan DNA genom hasil ekstraksi memiliki konsentrasi yang bervariasi, mulai dari 49,55 sampai dengan 138,25 ng/µL. Konsentrasi DNA genom yang diperoleh tersebut cukup memadai untuk digunakan sebagai DNA template pada reaksi PCR. Jumlah DNA template yang dibutuhkan dalam reaksi PCR hanya 10 ng per reaksi (Sambrook & Russel 2001). Oleh karena itu, 1 µL DNA genom hasil ekstraksi sudah memadai untuk digunakan dalam reaksi PCR.
Kemurnian DNA dinilai dari perbandingan absorbansinya pada panjang gelombang 260 (mewakili konsentrasi DNA) dan panjang gelombang 280 (mewakili konsentrasi protein). DNA yang murni akan memiliki nilai perbandingan A260/ A280 sebesar 1,8-2,0
(Sambrook & Russel 2001). Kemurnian DNA genom hasil ekstraksi bervariasi mulai dari 0,867 sampai dengan 1,778. DNA genom hasil ekstraksi dari isolat 5k, 16j, dan 40i memiliki nilai kemurnian yang cukup tinggi, namun sebagian besar DNA genom hasil ekstraksi justru tidak memberikan hasil yang memuaskan (Tabel 2). Kemurnian DNA bukanlah hal yang paling penting dalam reaksi PCR. Reaksi PCR dapat tetap berlangsung walaupun DNA yang digunakan sebagai template tidak memiliki kemurnian yang tinggi. Yuwono (2006) bahkan menyebutkan bahwa reaksi PCR dapat tetap berlangsung dengan menggunakan sel bakteri utuh sebagai template.
Tabel 2 Konsentrasi ekstrak DNA genom
Isolat Bt
A260 A280 A260/
A280
[DNA] (ng/µL)
7
Suhu OptimumAnnealing
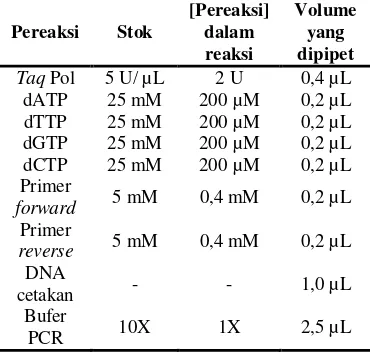
Pereaksi-pereaksi PCR yang digunakan pada tahap optimasi suhu annealing beserta komposisinya dapat dilihat pada Tabel 3. Volume total per reaksi adalah 25 µL. Ketepatan suhu yang digunakan dalam reaksi, terutama suhu annealing, merupakan salah satu faktor penentu keberhasilan reaksi PCR. Suhuannealing sangat tergantung pada primer yang digunakan. Tabel 4 menunjukkan primer-primer yang digunakan dalam reaksi PCR beserta spesifikasinya.
Secara teoritis, suhu annealing dapat ditentukan dengan menghitung Tm (temperature of melting) primer terlebih dahulu.
Tm (°C) = 2(A+T) + 4(G+C)
(A+T) adalah jumlah nukleotida adenin dan timin sedangkan (G+C) adalah jumlah nukleotida guanin dan sitosin dalam primer. Suhu annealing yang digunakan biasanya 2-10 °C di bawah Tm (Sambrook & Russel 2001).
Penentuan suhu annealing tidak dapat berdasarkan perhitungan teoritis saja. Reaksi PCR sebaiknya dicoba pada berbagai suhu annealing sehingga akan diperoleh hasil yang optimal. Oleh karena itu, setiap primer Cry diuji pada berbagai suhu annealing untuk menentukan suhu annealing yang optimum pada setiap reaksi PCR. Suhuannealing yang optimum ditentukan dengan mengamplifikasi DNA genom galur pembanding HD-567 pada suhu 45 °C, 47 °C, 49 °C, 51 °C, dan 53 °C dengan berbagai primer Cry, seperti yang tertera pada Tabel 4 mulai dari primer nomor 1 sampai dengan primer nomor 3. Suhu annealing yang dapat menghasilkan amplikon digunakan sebagai suhuannealing pada reaksi PCR untuk mendeteksi gen cry pada isolat-isolat B. thuringiensis.
Tabel 3 Komposisi pereaksi dalam reaksi ampifikasi Pereaksi Stok [Pereaksi] dalam reaksi Volume yang dipipet
TaqPol 5 U/ µL 2 U 0,4 µL dATP 25 mM 200 µM 0,2 µL dTTP 25 mM 200 µM 0,2 µL dGTP 25 mM 200 µM 0,2 µL dCTP 25 mM 200 µM 0,2 µL Primer
forward 5 mM 0,4 mM 0,2 µL Primer
reverse 5 mM 0,4 mM 0,2 µL DNA
cetakan - - 1,0 µL
Bufer
PCR 10X 1X 2,5 µL
B. thuringiensis subsp.israelensis HD-567 digunakan sebagai galur pembanding karena galur komersil ini telah diketahui memiliki gen cry4 seperti yang telah dilaporkan oleh Carozzi et al. (1991). Sekuensing terhadap bakteri ini juga pernah dilakukan oleh Berryet al. (2002) dan bakteri ini diketahui memiliki gen cry4Aa, gen cry4Ba, gen cry11Aa, dan gen cyt. Gen-gen inilah yang berfungsi menyandi protein Cry yang bersifat toksik terhadap nyamuk. Oleh karena itu, galur ini seharusnya memberikan hasil yang positif ketika diuji dengan primer-primer yang tertera pada Tabel 4.
Kontrol positif diujikan pada setiap reaksi untuk menandai bahwa suatu reaksi berlangsung dengan baik. Konsentrasi dari setiap pereaksi dan kondisi suhu PCR diperlakukan sama dengan sampel. Perbedaannya, DNAtemplate yang digunakan pada kontrol positif adalah DNA lambda dan menggunakan kontrol primer. Spesifikasi kontrol primer dapat dilihat pada Tabel 4. Tabel 4 Primer yang digunakan dalam reaksi PCR
No. Nama primer
Gencry
target Sekuens (5’ 3’) %GC
Tm (°C)
Amplikon (bp)
Cry 4B4 (F) GAGAACAGACCTAATCAACCAACT 41,67 68
1
Cry 4B4 (R)
cry4Ba1
GCGTGACATACCCATTTCCAGGTCC 56,00 78 1951
Cry 4A2 (F) GGGTATGGCACTCAACCCCACTT 56,52 72
2
Cry 4A2 (R) cry4Aa1 GCGTGACATACCCATTTCCAGGTCC 56,00 78 1529
Dip1A (F) CAAGCCGCAAATCTTGTGGA 50,00 60
3
Dip1A (R) cry4 ATGGCTTGTTTCGCTACATC 45,00 58 796
Kontrol (F) GGTTATCGAAATCAGCCACAGCGCC 56,00 78
8
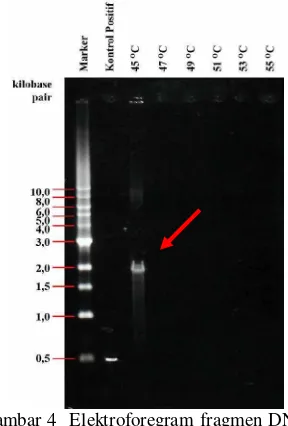
Berdasarkan hasil percobaan, seperti terlihat pada Gambar 4, optimasi suhu annealing pada reaksi PCR dengan primer Cry4B4 dicapai pada suhu annealing 45 °C sedangkan pada suhu yang lainnya reaksi PCR tidak berlangsung. Hal ini ditandai dengan adanya amplikon sebesar 1951 bp (panah merah) pada suhuannealing 45 °C sedangkan pada suhuannealinglainnya tidak dihasilkan amplikon.
Hasil optimasi suhuannealing pada primer Cry4A2, seperti terlihat pada Gambar 5, menunjukkan bahwa tidak ada amplikon yang dihasilkan. Demikian pula dengan optimasi suhuannealing pada primer Dip1A, yang juga tidak menghasilkan amplikon (Gambar 6). Walaupun suhu annealing yang digunakan masih di bawah Tm, masih terdapat kemungkinan suhuannealing yang digunakan kurang tepat sehingga tidak diperoleh amplikon pada kedua reaksi tersebut. Oleh karena itu, diperlukan penelitian lebih lanjut mengenai suhu annealing optimum untuk kedua primer tersebut.
Tidak dihasilkannya amplikon PCR juga dapat disebabkan galur tersebut telah mengalami mutasi pada sebagian daerahnya. Berryet al. (2002) menyebutkan bahwa lebih dari 23% gen dalam plasmidB. thuringiensis subsp.israelensis diapit oleh transposon, salah satu gen tersebut adalah gen cry4Aa1. Transposon merupakan elemen loncat yang dapat menyebabkan terjadinya mutasi pada bakteri tersebut (Jusuf 2001).
Gambar 4 Elektroforegram fragmen DNAB. thuringiensis HD-567 dengan primer Cry4B4 pada berbagai variasi suhuannealing.
Gambar 5 Elektroforegram fragmen DNAB. thuringiensis HD-567 dengan primer Cry4A2 pada berbagai variasi suhuannealing.
Gambar 6 Elektroforegram fragmen DNAB. thuringiensis HD-567 dengan primer Dip1A pada berbagai variasi suhuannealing.
Hasil Amplifikasi Gencry4Ba1
9
terhadapAedes aegypti. Semua sampel DNA genom dari isolat-isolat B. thuringiensis diamplifikasi dengan menggunakan primer Cry4B4 untuk mendeteksi keberadaan gen cry4Ba1 pada isolat-isolat tersebut. Isolat-isolat tersebut adalah Isolat-isolat-Isolat-isolat yang diduga memiliki gencry4. Pemilihan isolat dilakukan berdasarkan ukuran protein Cry yang dihasilkan pada masa sporulasi (Handayani 2006). Protein Cry4 memiliki ukuran sebesar 134 kDa. Ukuran protein Cry4 tersebut hampir sama dengan ukuran protein Cry1, yaitu sebesar 130-135 kDa. Oleh karena itu, isolat yang digunakan adalah isolat-isolat yang memiliki protein berukuran 130-135 kDa.
Suhu annealing yang digunakan pada reaksi PCR tersebut adalah suhu annealing yang menghasilkan amplikon pada optimasi suhuannealing tahap sebelumnya, yaitu suhu 45 °C. Sampel DNA genomB. thuringiensis tidak diuji dengan menggunakan primer Dip1A dan primer Cry4A2. Hal ini tidak dilakukan karena pada tahap sebelumnya, yaitu optimasi suhu annealing, tidak didapatkan kondisi optimum yang dapat menyebabkan pembentukan amplikon pada reaksi dengan primer Dip1A dan primer Cry4A2.
Prinsip dasar pendeteksian gen cry4Ba1 adalah sebagai berikut, sampel yang memiliki gen cry4Ba1 akan teramplifikasi dengan reaksi PCR dan terdeteksi sebagai pita amplikon ketika di-running dengan elektroforesis gel agarosa. Hal ini dapat terjadi karena primer Cry4B4 yang digunakan akan menempel pada gen target, yaitu gencry4Ba1. EnzimTaq DNA polimerase kemudian akan mengkatalisis reaksi polimerasi, secara terus-menerus, sehingga akan didapatkan sejumlah besar DNA hasil amplifikasi pada tahap akhir reaksi. DNA dalam jumlah besar ini akan menumpuk pada satu tempat pada saat dilakukan elektroforesis dan ketika divisualisasi dengan UV akan terlihat sebagai pita amplikon. Panjang amplikon yang terbentuk adalah sejumlah nukleotida yamg terdapat di antara primer Cry 4B4forward dan primer Cry 4B4 reverse, yaitu sebesar 1951 bp.
Berdasarkan hasil percobaan, seperti yang terlihat pada Gambar 7, amplifikasi isolat-isolatB. thuringiensis dengan primer Cry4B4 menunjukkan bahwa tidak ada isolat B. thuringiensis yang menghasilkan amplikon. Tidak terdapatnya amplikon PCR pada 36 isolat yang diuji menunjukkan bahwa kemungkinan tidak ada isolatB. thuringiensis
di daerah Bogor dan sekitarnya yang mengandung gencry4Ba1. Tidak adanya gen cry4Ba1 menyebabkan isolat-isolat B. thuringiensis tersebut tidak dapat memproduksi protein Cry4Ba1 yang toksik terhadap Aedes aegypti. Dengan kata lain, isolat-isolat B. thuringiensis tersebut tidak dapat digunakan sebagai biopestisida untuk membasmi nyamuk Aedes aegypti penyebab demam berdarah.
(a)
(b)
(c)
10
SIMPULAN DAN SARAN
Metode ekstraksi DNA genom yang diadaptasi dari Juarez-Perezet al. (1997) dan Frederiksen et al. (2006) dapat digunakan untuk memperoleh DNA genom galur pambanding sebagai DNA template pada reaksi PCR. Tidak ada amplikon yang dihasilkan ketika dilakukan PCR dengan primer Cry4B4.
Penelitian lebih lanjut mengenai gen cry yang terkandung dari setiap isolat dapat dilakukan agar isolat tersebut dapat dimanfaatkan dengan optimal. Ekstraksi DNA dengan metode lain dapat dilakukan untuk memperoleh DNAtemplate. Selain itu, dapat dilakukan isolasi kembali dari tanah dan bangkai serangga yang memiliki kemungkinan lebih besar mengandung gen cry4.
DAFTAR PUSTAKA
Ben-Dov Eet al. 1997. Extended screening by PCR for sevencry-group genes from field-collected strains of Bacillus thuringiensis. Aem Asm 63:4883-4890.
Berry et al. 2002. Complete sequence and organization of pBtoxis, the toxin-coding plasmid of Bacillus thuringiensis subsp. israelensis.Aem Asm 68:5082-5095. Bravo et al. 1998. Characterization of cry
genes in Mexican Bacillus thuringiensis strain collection.Aem Asm 64:4965-4972. Broderick NA, Raffa KF, Handelsman J.
2006. Midgut bacteria required forBacillus thuringiensis insecticidal activity. PNAS 103: 15196-15199.
Brown TA. 2003. Pengantar Kloning Gen. Soemiati AHP, editor. Yogyakarta: Essentia Medica. Terjemahan dari: Gene Cloning an Introduction.
Bulla LA, Raymond KC, Faust RM. 1991. Mosquitocidal toxin gene of Bacillus thuringiensis subsp. israelensis. Di dalam: Karl Maramorosch, editor. Biotechnology for Biologycal Control of Pests and Vectors. New Jersey: CRC Pr. hlm 25-34. Carozzi NB et al. 1991. Prediction of
insectisidal activity of Bacillus
thuringiensis strains by Polymerase Chain Reaction product profiles. Aem Asm 57:3057-3061.
Debabov VG et al. 1984. Genetic and biochemical study of Bacillus thuringiensis. Di dalam: Ganesan AT dan James AH, editor. Genetics and Biotechnology of Bacilli. Orlando: Academic Pr. hlm 345-358.
[Encyclopaedia Britannica]. 1998. Polymerase chain reaction: three-step process.
http://www.britannica.com/eb/art- 18071/The-three-step-process-of-the-polymerase-chain-reaction [26 September 2006].
Fikri A. 2007. April-Maret puncak demam berdarah. http://www.tempointeraktif.com/ hg/nusa/jawamadura/2007/01/31/brk,20070 131-92267,id.html [20 Maret 2007]. Frederiksen K, Rosenquist H, Jørgensen K,
Wilcks A. 2006. Occurrence of natural Bacillus thuringiensis contaminants and residues of Bacillus thuringiensis-based insecticides on fresh fruits and vegetables. Aem Asm 72:3435-3440.
Handayani ES. 2006. Penyebaran protein Cry dan tipe gen penyandinya di wilayah Jabodetabek dan Sukabumi. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Jones NL. 2003. PCR: Principles, procedures, and parameters. Di dalam: Theophilus BDM, Ralpley R, editor. Methods in Molecular Biology: PCR Mutation Detection Protocols. Vol. 187. New Jersey: Humana Pr. hlm 37-46.
Jua´rez-Pe´rez VM, Ferrandis MD, Frutos R. 1997. PCR-based approach for detection of novelBacillus thuringiensis cry genes. Aem Asm 63:2997 3002.
Jusuf M. 2001.Genetika I Struktur & Ekspresi Gen. Jakarta: Sagung Seto.
11
[Kompas]. 2007. Bogor KLB DBD korban meninggal di seluruh Indonesia 98 orang. http://www.kompas.com/kompas-cetak/0701/31/utama/3276891.htm [20 Maret 2007].
Kronstad JW, Schnepf HE, Whiteley HR. 1983. Diversity of location for Bacillus thuringiensis crystal protein genes. J Bacteriol. 160:95-102.
Muladno. 2002. Seputar Teknologi Rekayasa Genetika. Bogor: Pustaka Wirausaha Muda.
[Pikiran Rakyat]. 2006. 75% wilayah Bogor terancam DBD. http://www.pikiran-rakyat.com/cetak/2006/032006/27/0320.ht m [20 Maret 2007].
Rodriguez RL, Tait RC. 1983. Recombinant DNA Techniques: An Introduction. Massachusetts: Addison-Wesley Publishing Company.
Rosso ML, Delecluse A. 1997. Contribution of the 65-Kilodalton protein encoded by the cloned gene cry19A to the mosquitocidal activity of Bacillus thuringiensis subsp.jegathesan.Aem Asm 63:4449-4455.
Sambrook J, Russell DW. 2001. Molecular Cloning: A Laboratory Manual, Ed ke-3. New York: Cold-Spring Harbor Laboratory Pr.
Schnepf et al. 1998. Bacillus thuringiensis and its pestisidal crystal protein. Microbiol. Moleculer Biol. 62:775-806. Suharsono S. 2000. Prinsip Amplifikasi DNA
dengan PCR. Bogor: Pusat Antar Universitas Bioteknologi IPB.
[University of California]. 1999. Bacillus thuringiensis. http://www.bt.ucsd.edu/ what_is_crystal.html [13 Desember 2006]. Widiastuti H, Santoso D. 2001. Isolasi gencry dari isolat lokal Bacillus thuringiensis toksik pengerek buah kakao dengan teknik PCR.J Mikrobiol Indon6:50-53.
Winding A, Hansen BM. 2001. Mikrobiologiske bekæmpelsesmidler. http://www.dmu.dk/foralle/Bakterier/Bakte
rier+i+jordbrugets+tjeneste/Mikrobiologisk e+bek%C3%A6mpelsesmidler.htm [25 Februari 2007].
Yuwono T. 2006. Teori dan Aplikasi Polymerase Chain Reaction. Yogyakarta: ANDI OFFSET.
13
Elektroforesis Gel Agarosa Ekstraksi DNA
Induksi antibiotik
Amplifikasi DNA spesifik dengan PCR
Lampiran 1 Strategi penelitian
DNA Genom
Isolat
B. thuringiensis
daerah Bogor dan
sekitarnya
Pita
amplikon
PCR
berukuran spesifik
Gen Cry
Isolat dengan plasmid
14
Lampiran 2 Tahapan induksi plasmid dengan antibiotik
Lampiran 3 Tahapan ekstraksi DNA genom
Agar miring berisi isolat Bt
Agar pet ri LB dengan ant ibiotik
I solat Bt berplasmid resisten antibiotik Agar petri
LB dengan antibiotik
Agar pet ri LB dengan ant ibiot ik
o/ n o/ n o/ n
5 m L LB cair
5 mL LB cair Working
culture
1 ose 0,1 mL
o/ n
10000 rpm
4 jam
100µL ddH2O
Pelet biomassa
100 ° C 10
- 5 ° C 10 12000 rpm
15
Lampiran 4 Daftar isolat
B. thuringiensis
yang digunakan beserta asalnya
No.
Isolat
B. thuringiensis
Asal
1
3a
Tanah rerumputan-Cibining, Bogor
2
3l
Tanah rerumputan-Cibinong, Bogor
3
3n
Tanah rerumputan-Cibinong, Bogor
4
4q
Tanah di bawah pohon jambu-Cibinong, Bogor
5
5k
Tanah di bawah pohon jambu-Cibinong, Bogor
6
6c
Lumpur air selokan-Cibinong, Bogor
7
6l
Lumpur air selokan-Cibinong, Bogor
8
7e
Bangkai larva-Cibinong, Bogor
9
7i
Bangkai ulat-Cibinong, Bogor
10
8c
Tanah di bawah pohon-Muara Tawar, Bekasi
11
9g
Tanah sawah-Muara Tawar, Bekasi
12
10h
Tanah kering-Muara Tawar, Bekasi
13
16j
Tanah di sekitar Monas, Jakarta Pusat
14
16g
Tanah di sekitar Monas, Jakarta Pusat
15
21f
Tanah di bawah pohon-Lapangan Banteng, Jakarta
16
22g
Tanah di taman SMPN 5 Pasar Baru, Jakarta
17
22p
Tanah di halaman SMPN 5 Pasar Baru, Jakarta
18
29h
Tanah di halaman SMPN 5 Pasar Baru, Jakarta
19
31a
Tanah area perkemahan-Cisarua, Bogor
20
31e
Tanah area perkemahan-Cisarua, Bogor
21
31t
Tanah area perkemahan-Cisarua, Bogor
22
31x
Tanah area perkemahan-Cisarua, Bogor
23
32g
Tanah hutan lindung- Cisarua, Bogor
24
32n
Tanah hutan lindung- Cisarua, Bogor
25
35r
Tanah di bawah pohon-Bojong, Bekasi
26
37-t
1Daun
Morinda citrifolia
-Bojong, Bekasi
27
37-t
3Daun
Morinda citrifolia
-Bojong, Bekasi
28
40a
Tanah peternakan ayam-Bojong, Bekasi
16
Lanjutan lampiran 4...
30
40i
Tanah peternakan ayam-Bojong, Bekasi
31
40g
Tanah peternakan ayam-Bojong, Bekasi
32
42g
Tanah kosong-Cipayung, Jakarta
33
42k
Tanah kosong-Cipayung, Jakarta
34
42t
Tanah kosong-Cipayung, Jakarta
35
50l
Tanah perkampungan-Situgunung, Sukabumi
17
Lampiran 5 Pembagian jenis protein Cry (Zeigler 1999)
Jenis protein Cry
Toksisitas spesifik
Cry1
Lepidoptera,Coleoptera
Cry2
Lepidoptera, Diptera
Cry3
Coleoptera
Cry4
Diptera
Cry5
Nematoda
Cry6
Nematoda
Cry7
Coleoptera
Cry8
Coleoptera
Cry9
Lepidoptera
Cry10
Diptera
Cry11
Diptera
Cry12
Nematoda
Cry13
Nematoda
Cry14
Nematoda, Coleoptera
Cry15
Lepidoptera
Cry16
Diptera
Cry19
Diptera
Cry20
Diptera
Cry21
Diptera
Cry22
Coleoptera